Alimento geneticamente modificado
| Parte de uma série sobre |
| Engenharia genética |
|---|
 |
| Organismos Geneticamente Modificados |
|
Bactérias · Vírus Animais (Mamíferos · Peixes · Insetos) Plantas (Milho · Soja · Arroz · Trigo · Algodão · Feijão · Cana-de-açúcar · Eucalipto) |
| História e regulamentação |
| História · Regulamentação (Equivalência substancial · Protocolo de Cartagena sobre Biossegurança) |
| Biossegurança |
| Comissão Técnica Nacional de Biossegurança (CTNBio) · Conselho Nacional de Biossegurança (CNBS) · |
| Processo |
| Técnicas · Clonagem molecular (ADN recombinante) · Transgênese · (Transformação · Transfecção · Transdução) · Edição de genoma (TALEN · CRISPR) |
| Aplicações |
| Culturas geneticamente modificadas (Alimentos) · Terapia genética · Bebê projetado |
| Controvérsias |
| Controvérsia sobre alimentos geneticamente modificados · Teorias da conspiração sobre OGMs · Caso Pusztai · Caso Séralini · Caso He Jiankui |

Alimentos geneticamente modificados (alimentos GMs), às vezes chamados de alimentos bioengenheirados, são alimentos produzidos com base em organismos que, através das técnicas da engenharia genética, sofreram alterações específicas no seu material genético. Se esses alimentos provêm de organismos que receberam genes de outras espécies, são conhecidos como alimentos transgênicos (português brasileiro) ou alimentos transgénicos (português europeu).[1] Essa técnica tem permitido a introdução de culturas agrícolas de traços diferenciados, assim como um controle sobre a estrutura genética bastante superior em relação ao que proporciona o melhoramento por mutação e a seleção artificial.[2]
A descoberta do DNA e a melhoria da tecnologia genética no século XX desempenharam um papel crucial no desenvolvimento da tecnologia transgênica.[3] Em 1988, enzimas microbianas geneticamente modificadas foram aprovadas pela primeira vez para uso na fabricação de alimentos nos Estados Unidos. A quimosina recombinante foi usada em alguns países na década de 1990, substituindo o coalho na fabricação de queijo.[4] A venda comercial de alimentos geneticamente modificados começou em 1994, quando a Calgene comercializou pela primeira vez seu malsucedido tomate de maturação retardada Flavr Savr.[5] Em 1998, foi aprovado para cultivo comercial na União Europeia o uso de milho geneticamente modificado para conferir resistência à broca europeia do milho, sendo a primeira variedade transgênica plantada em Portugal em 1999.[6] Em 2000, com a criação do arroz dourado, os cientistas obtiveram êxito em modificar geneticamente um alimento para aumentar seu valor nutritivo.[7] A soja transgênica foi aprovada provisoriamente para cultivo no Rio Grande do Sul em 2003. Já em 2005, foi liberada em todo o país, juntamente com o algodão geneticamente modificado resistente a insetos.[8] Internacionalmente, o salmão AquAdvantage foi o primeiro animal geneticamente modificado aprovado para consumo humano, tendo sido autorizado pela FDA nos Estados Unidos em 2015.[9] Em 2021, a FDA aprovou uma modificação genética em suínos.[9][10]
A maior parte das modificações genéticas aplicadas a alimentos concentrou-se em culturas comerciais de alta demanda entre os agricultores. No Brasil, exemplos de culturas geneticamente modificadas incluem algodão, cana-de-açúcar, feijão, milho, soja e trigo, além do eucalipto, usado na indústria madeireira.[11] Culturas geneticamente modificadas têm sido projetadas para oferecer resistência a patógenos e herbicidas, tolerância à seca,[11] e para obter melhores perfis nutricionais.[12]
Genes que codificam características desejadas, como níveis nutricionais aprimorados, tolerância à seca, resistências a pesticidas e herbicidas e a capacidade de produzir substâncias terapêuticas, são frequentemente extraídos e transferidos para os organismos-alvo, conferindo a eles maior capacidade de sobrevivência e produção.[13][14][15][16][17][18][19] O valor de utilização aprimorado geralmente proporciona benefícios aos consumidores em aspectos específicos, como sabor, aparência ou tamanho.[13][14][18]
Existe um consenso científico[20][21][22][23][24] de que os alimentos atualmente disponíveis derivados de culturas geneticamente modificadas não representam um risco maior para a saúde humana do que os alimentos convencionais,[25][26][27][28][29][30][31] mas que cada alimento geneticamente modificado precisa ser testado caso a caso antes da introdução.[32][33][34] No entanto, os membros do público são muito menos propensos do que os cientistas a perceber os alimentos geneticamente modificados como seguros.[35][36][37][38] O status legal e regulatório dos alimentos geneticamente modificados varia de país para país, com algumas nações proibindo-os ou restringindo-os, e outras permitindo-os com graus de regulamentação amplamente diferentes,[39][40][41][42][43] que variam devido a fatores geográficos, religiosos, sociais e outros.[13][44][45][46][47]
Definição
Alimentos geneticamente modificados são alimentos produzidos a partir de organismos que tiveram alterações introduzidas em seu material genético usando métodos de engenharia genética, em oposição ao cruzamento tradicional.[48][49] De acordo com a Organização Mundial da Saúde, “os alimentos produzidos a partir de ou utilizando organismos geneticamente modificados são frequentemente chamados de alimentos geneticamente modificados”.[48] OGM é, segundo o artigo 3º, inciso V, da Lei Federal brasileira nº 11.105, de 24 de março de 2005, "o organismo cujo material genético (DNA/RNA) tenha sido modificado por qualquer técnica de engenharia genética". A lei exclui da categoria de OGM (pelo §1º do mesmo artigo) o organismo "resultante de técnicas que impliquem a introdução direta, num organismo, de material hereditário, desde que não envolvam a utilização de moléculas de DNA/RNA recombinante ou OGM, tais como: fecundação in vitro, conjugação, transdução, transformação, indução poliplóide e qualquer outro processo natural.[50]
O que constitui um organismo geneticamente modificado (OGM) não é claro e varia muito entre países, organismos internacionais e outras comunidades, mudou significativamente ao longo do tempo e foi sujeito a inúmeras exceções baseadas em "convenção", como a exclusão do melhoramento por mutação da definição da União Europeia.[51]
Inconsistência e confusão ainda maiores estão associadas a vários esquemas de rotulagem "Não OGM/Transgênico" "Livre de OGMs/Transgênicos" no marketing de alimentos, onde até mesmo produtos como água ou sal, que não contêm nenhuma substância orgânica e material genético (e, portanto, não podem ser geneticamente modificados por definição) estão sendo rotulados para criar uma impressão de serem "mais saudáveis".[52][53]
Tipos de modificações
Transgênico
Na maioria das vezes, quando se fala em alimentos geneticamente modificados, está-se referindo a produtos obtidos de organismos transgênicos. No entanto, OGM e transgênico não são sinônimos: todo transgênico é um OGM, mas nem todo OGM é transgênico. Um OGM é qualquer organismo cujo material genético foi alterado, através das técnicas da engenharia genética, sem que isso implique necessariamente na inserção de genes de outra espécie.[1][54] Os organismos transgênicos têm genes inseridos neles que são derivados de outra espécie. Os genes inseridos podem vir de espécies dentro do mesmo reino (planta para planta, animal para animal), ou entre reinos (por exemplo, bactéria para planta). Em muitos casos, o material genético inserido tem que ser modificado ligeiramente para ser expresso de forma correta e eficiente no organismo hospedeiro.[1][54] Alimentos produzidos a partir de ou utilizando organismos transgênicos são frequentemente chamados de alimentos transgênicos.[55]
Cisgênico
Os organismos cisgênicos são produzidos usando genes encontrados na mesma espécie ou em uma espécie sexualmente compatível e intimamente relacionada, onde o melhoramento convencional de plantas pode ocorrer.[56][54] Alguns criadores e cientistas argumentam que a modificação cisgênica é útil para plantas que são difíceis de cruzar por meios convencionais (como batatas), e que as plantas na categoria cisgênica não devem exigir o mesmo escrutínio regulatório que os transgênicos.[57]
Subgênico
Organismos geneticamente modificados também podem ser desenvolvidos usando knockdown ou knockout de genes para alterar sua composição genética sem incorporar genes de outros organismos. Em 2014, o pesquisador chinês Gao Caixia registrou patentes sobre a criação de uma variedade de trigo resistente ao oídio. A variedade não possui genes que codificam proteínas que reprimem as defesas contra o oídio. Os pesquisadores excluíram todas as três cópias dos genes do genoma hexaplóide do trigo. Gao usou as ferramentas de edição de genes TALEN e CRISPR sem adicionar ou alterar quaisquer outros genes. Nenhum teste de campo foi planejado imediatamente.[58][59] A técnica CRISPR também foi usada pelo pesquisador Yinong Yang da Universidade Estadual da Pensilvânia para modificar cogumelos Champignon para não escurecerem,[60] e pela DuPont Pioneer para fazer uma nova variedade de milho.[61]
História
A manipulação genética de alimentos dirigida pelos seres humanos começou com a domesticação de plantas e animais por meio da seleção artificial, por volta de 13.000–11.000 a.C.[62][63][64] O processo de reprodução seletiva, no qual organismos com características desejadas (e, portanto, com os genes desejados) são usados para gerar a próxima geração, enquanto os organismos sem essas características não são reproduzidos, é um precursor do conceito moderno de modificação genética.[64][65] Com a descoberta do DNA no início do século XX e, posteriormente, com a constatação em 1946 de que ele pode ser transferido entre organismos,[66] abriu-se caminho para que, a partir dos avanços em técnicas genéticas alcançados até a década de 1970,[3] se tornasse possível alterar diretamente o DNA e os genes presentes nos alimentos.
As enzimas microbianas geneticamente modificadas foram a primeira aplicação de organismos geneticamente modificados na produção de alimentos e foram aprovadas em 1988 pela Food and Drug Administration (FDA) dos Estados Unidos.[4] No início da década de 1990, a quimosina recombinante foi aprovada para uso em diversos países.[4][67] Tradicionalmente, o queijo era produzido utilizando o complexo enzimático coalho, extraído do revestimento do estômago de vacas. Cientistas modificaram bactérias para produzir quimosina, que também consegue coagular o leite, formando a coalhada usada na produção de queijo.[68]
A China foi o primeiro país a comercializar uma cultura transgênica em 1993, com a introdução do tabaco resistente a vírus.[5] O primeiro alimento geneticamente modificado aprovado para lançamento foi o tomate Flavr Savr em 1994.[5] Desenvolvido pela Calgene, o tomate foi projetado para ter maior durabilidade por meio da inserção de um gene antissentido, que retardava o amadurecimento. Esse gene bloqueava parcialmente a produção da enzima poligalacturonase, responsável por degradar a pectina da parede celular e acelerar o amolecimento do fruto.[69] Em 1995, a batata Bacillus thuringiensis (Bt) foi aprovada para cultivo, tornando-se a primeira cultura produtora de inseticidas a ser aprovada nos EUA.[70] Outras culturas geneticamente modificadas que receberam aprovação de comercialização nos Estados Unidos em 1995 foram: canola com composição de óleo modificada, milho Bt, algodão resistente ao herbicida Bromoxinil, algodão Bt, soja tolerante ao glifosato, abóbora resistente a vírus e outro tomate de amadurecimento retardado.[5]
No Brasil, através da lei nº 8.974, de 5 de janeiro de 1995, foi criada a CTNBio (Comissão Técnica Nacional de Biossegurança), órgão vinculado ao Ministério da Ciência e Tecnologia e Inovação, com finalidade de prestar apoio técnico consultivo e assessoramento ao Governo Federal na formulação, atualização e implementação da Política Nacional de Biossegurança relativa a organismos geneticamente modificados (OGMs), bem como no estabelecimento de normas técnicas de segurança e pareceres técnicos referentes à proteção da saúde humana, dos organismos vivos e do meio ambiente, para atividades que envolvam a construção, experimentação, cultivo, manipulação, transporte, comercialização, consumo, armazenamento, liberação e descarte de OGM e derivados.[71]
Em 1998, o cultivo experimental de organismos geneticamente modificados começou nos estados de São Paulo, Minas Gerais, Paraná e Rio Grande do Sul.[72] No mesmo ano, a Monsanto obteve autorização para o plantio comercial da soja Roundup Ready resistente ao glifosato. Contudo, uma liminar da Justiça Federal impediu a liberação do produto para consumo até a regulamentação da comercialização de OGMs e a realização de estudos sobre seus impactos ambientais.[72][73] Também em 1998, foi aprovado para cultivo comercial na União Europeia o uso de milho geneticamente modificado para conferir resistência à broca europeia do milho, sendo a primeira variedade transgênica plantada em Portugal em 1999.[6] Pouco tempo depois, a UE decretou uma moratória de facto sobre novas aprovações de OGM que durou até 2003.[6]
Em 2000, com a criação do arroz dourado, os cientistas obtiveram êxito em modificar geneticamente um alimento para aumentar seu valor nutritivo.[7] Essa variedade de arroz foi desenvolvida para produzir betacaroteno, precursor da vitamina A, com o objetivo de ser utilizada como alimento biofortificado para combater a deficiência dessa vitamina em países em desenvolvimento da África, América Latina e, sobretudo, da Ásia.[7][74][75][76][77]
A soja transgênica Roundup Ready, que já era cultivada de forma clandestina, recebeu aprovação provisória para cultivo no Rio Grande do Sul em 2003.[73] As regulamentações dos transgênicos no Brasil vão voltar a ser elaboradas em 2005, com a lei nº 11.105, de 24 de março de 2005, a atual Lei de Biossegurança.[43] Esta reestruturou o CTNBio, criou Conselho Nacional de Biossegurança (CNBS), órgão superior à CTNBio,[78] e revogou a disposição anterior. No mesmo ano, a soja transgênica foi liberada em todo o país, juntamente com o algodão geneticamente modificado resistente a insetos.[8]
Em 2010, 29 países tinham plantado culturas transgênicas e outros 31 países tinham concedido aprovação regulamentar para a importação de culturas geneticamente modificadas.[79] Os EUA foram o país líder na produção de alimentos geneticamente modificados em 2011, com vinte e cinco culturas geneticamente modificadas a receberem aprovação regulamentar.[79] Em 2015, 92% do milho, 94% da soja e 94% do algodão produzidos nos EUA eram variedades geneticamente modificadas.[80]
Na safra de 2014, o Brasil cultivou aproximadamente 42,2 milhões de hectares com culturas transgênicas de soja, milho e algodão, o que representou um aumento de 4,6% em relação ao ano anterior e correspondeu a 23% da área global. A soja transgênica foi a principal cultura, com um crescimento de 7,9% em relação a 2013. O milho transgênico foi a segunda cultura mais importante, com uma redução de 2,9% devido à diminuição da área total cultivada com milho. O algodão transgênico registrou um aumento de 25,1% em relação ao ano anterior. Com esses números, o Brasil manteve-se como o segundo maior produtor mundial de transgênicos, atrás apenas dos Estados Unidos, que cultivaram 73,1 milhões de hectares, correspondendo a 40% da área global.[81]
O salmão AquAdvantage foi o primeiro animal geneticamente modificado aprovado para consumo humano, tendo sido autorizado pela FDA nos Estados Unidos em 2015.[9] Esse salmão recebeu um gene regulador do hormônio do crescimento proveniente do salmão-rei e um promotor extraído do peixe-carneiro americano, o que lhe permitiu crescer durante todo o ano, em vez de apenas na primavera e no verão.[82] A comercialização do salmão modificado foi também aprovada no Canadá em 2016[83] e no Brasil em 2021.[84] Ainda em 2021, a FDA aprovou uma modificação genética em suínos que remove um alérgeno.[9][10]
Um cogumelo champignon geneticamente modificado é aprovado nos Estados Unidos desde 2016.[85]
Os organismos geneticamente modificados mais cultivados foram desenvolvidos para tolerar herbicidas. O uso de herbicidas exerce uma forte pressão seletiva sobre as plantas daninhas tratadas, favorecendo a aquisição de resistência ao produto. O plantio em larga escala de culturas transgênicas resistentes ao glifosato levou ao uso intensivo desse pesticida para o controle de ervas daninhas, varias espécies desenvolveram resistência ao herbicida.[86][87][88]
Em 2021, o primeiro alimento editado com CRISPR foi colocado à venda no Japão. Tomates foram geneticamente modificados para conter cerca de cinco vezes a quantidade normal de GABA,[89] que pode ter efeito calmante.[90] O CRISPR foi aplicado pela primeira vez em tomates em 2014.[91] Pouco depois, os primeiros animais marinhos editados com CRISPR e o segundo conjunto de alimentos editados com CRISPR foram colocados à venda ao público no Japão: dois peixes, dos quais uma espécie cresce até o dobro do tamanho dos espécimes naturais devido à interrupção do gene da leptina, que controla o apetite, e a outra cresce até 1,2 vezes o tamanho médio natural com a mesma quantidade de alimento devido à inativação da miostatina, que inibe o crescimento muscular.[92][93][94]
Métodos
A criação de alimentos geneticamente modificados é um processo de múltiplas etapas. O primeiro passo é identificar um gene útil de outro organismo que se deseja inserir. O gene pode ser obtido a partir de uma célula[95] ou sintetizado artificialmente,[96] sendo então combinado com outros elementos genéticos, incluindo uma região promotora e terminadora e um marcador selecionável.[97] Em seguida, os elementos genéticos são inseridos no genoma do organismo-alvo. O DNA geralmente é inserido em células animais por microinjeção, podendo ser injetado diretamente no núcleo através da membrana nuclear da célula, ou por meio do uso de vetores virais.[98] Nas plantas, o DNA é frequentemente inserido usando recombinação mediada por agrobactérias,[99][100] biolística[101] ou eletroporação.[102] A eletroporação aplica um campo elétrico nas células, de modo a aumentar a permeabilidade da membrana celular, permitindo que produtos químicos, medicamentos ou DNA possam ser introduzidos.[102] Biolística consiste na propulsão dos genes de interesse no interior das células com a ajuda de um canhão de DNA, com o qual se modifica o DNA da célula.[103] As agrobactérias são parasitas de plantas que possuem a capacidade de transferir naturalmente seus genes para as plantas parasitadas, num processo conhecido como transferência horizontal de genes, elas são modificadas para receber genes escolhidos, e os transferem para as células-alvo.[100][104]
Como apenas uma única célula é transformada com o material genético, o organismo precisa ser regenerado a partir dessa célula única. Nas plantas, isso é feito por meio de cultura de tecidos.[105][106] Nos animais, é necessário garantir que o DNA inserido esteja presente nas células-tronco embrionárias.[99] Testes adicionais, como RCP, Southern blot e sequenciamento de DNA, são realizados para confirmar que o organismo contém o novo gene.[107]
Tradicionalmente, o novo material genético era inserido aleatoriamente no genoma hospedeiro. Técnicas de gene targeting, que criam quebras de fita dupla e aproveitam os sistemas naturais de reparo por recombinação homóloga das células, foram desenvolvidas para direcionar a inserção a locais específicos. A edição genômica utiliza nucleases artificialmente projetadas que geram quebras em pontos específicos. Existem quatro famílias de nucleases projetadas: meganucleases,[108][109] nucleases de dedo de zinco,[110][111] nucleases TALEN[112][113] e o sistema Cas9-guia RNA (adaptado do CRISPR).[114][115] TALEN e CRISPR são os dois métodos mais usados, cada um com suas vantagens.[116] As TALENs apresentam maior especificidade de alvo, enquanto o CRISPR é mais fácil de projetar e mais eficiente.[116]
Por organismo
Culturas agrícolas
Culturas geneticamente modificadas são plantas geneticamente modificadas utilizadas na agricultura. As primeiras culturas desenvolvidas tinham como destino a alimentação animal ou humana e forneciam resistência a certas pragas, doenças, condições ambientais, deterioração ou tratamentos químicos (por exemplo, resistência a um herbicida). A segunda geração de culturas buscou melhorar a qualidade, muitas vezes alterando o perfil nutricional. As culturas geneticamente modificadas de terceira geração poderiam ser usadas para fins não alimentares, incluindo a produção de agentes farmacêuticos, biocombustíveis e outros produtos de utilidade industrial, bem como para biorremediação.[117] As culturas geneticamente modificadas têm sido produzidas para melhorar as colheitas por meio da redução da pressão de insetos, aumento do valor nutricional e tolerância a diferentes estresses abióticos. Até 2018, as culturas comercializadas globalmente limitavam-se principalmente a culturas de alto valor comercial, como algodão, soja, milho e canola, e a vasta maioria dos caracteres introduzidos proporcionava tolerância a herbicidas ou resistência a insetos.[117]
A maioria das culturas transgênicas foi modificada para ser resistente a herbicidas específicos, geralmente à base de glifosato ou glufosinato. As culturas geneticamente modificadas desenvolvidas para resistir a herbicidas são atualmente mais comuns do que as variedades resistentes obtidas por melhoramento convencional.[118] A maioria dos genes atualmente disponíveis e utilizados para desenvolver resistência a insetos provém da bactéria Bacillus thuringiensis (Bt) e codifica delta-endotoxinas. Alguns utilizam genes que codificam proteínas inseticidas vegetais.[119] O único gene comercialmente utilizado para fornecer proteção contra insetos que não se origina do B. thuringiensis é o inibidor de tripsina do feijão-frade (CpTI). O CpTI foi aprovado pela primeira vez para uso no algodão em 1999 e atualmente está em fase de testes em arroz.[120][121] Em 2014, menos de 1% das culturas geneticamente modificadas apresentaram outros caracteres, incluindo resistência a vírus, tolerância a seca, atraso da senescência e alteração na composição das plantas.[81]
A adoção por parte dos agricultores foi rápida: entre 1996 e 2013, a área total de terras cultivadas com culturas transgênicas aumentou em um fator de 100.[122] Geograficamente, porém, a expansão foi desigual, com forte crescimento nas Américas e em partes da Ásia e pouco na Europa e na África,[117] em 2013, apenas 10% das terras agrícolas mundiais eram geneticamente modificadas, com Estados Unidos, Canadá, Brasil e Argentina representando 90% desse total.[23] Sua distribuição socioeconômica foi mais equilibrada, com aproximadamente 54% das culturas transgênicas mundiais cultivadas em países em desenvolvimento em 2013.[122] Embora tenham sido levantadas dúvidas, a maioria dos estudos constatou que o cultivo de culturas transgênicas tem sido benéfico para os agricultores, tanto pela redução do uso de pesticidas quanto pelo aumento do rendimento das colheitas e do lucro agrícola.[6][123][124][125]
Frutas e vegetais
Muito antes de os seres humanos começarem a utilizar transgênicos, a batata-doce surgiu naturalmente há cerca de 8.000 anos, incorporando genes de bactérias que aumentaram seu teor de açúcar. Kyndt et al. (2015) identificaram que o DNA de Agrobacterium tumefaciens, proveniente desse evento transgênico natural, ainda está presente no genoma da cultura atualmente.[126][127][128][129][130]

O mamão foi geneticamente modificado para resistir ao vírus da mancha anelar (PRSV). O “SunUp” é uma variedade transgênica de polpa vermelha derivada da variedade de mamão "Sunset", homozigótica para o gene da proteína do capsídeo do PRSV, já o “Rainbow” é um híbrido F1 de polpa amarela, desenvolvido pelo cruzamento entre o “SunUp” e o “Kapoho” não transgênico.[132] Essa variedade transgênica foi aprovada em 1998[133] e, em 2010, 80% do mamão cultivado no Havaí já era geneticamente modificado.[134] O New York Times declarou que, sem ela, a indústria havaiana de mamão teria colapsado.[134] Na China, um mamão transgênico resistente ao PRSV foi desenvolvido pela Universidade Agrícola do Sul da China e aprovado para cultivo comercial em 2006, em 2012, 95% do mamão cultivado na província de Guangdong e 40% do mamão em Hainan eram transgênicos.[135] Em Hong Kong, onde existe uma isenção para o cultivo e liberação de variedades de mamão transgênico, mais de 80% dos mamões cultivados e importados eram transgênicos.[136][137]
A batata New Leaf, um alimento transgênico desenvolvido com o uso de Bacillus thuringiensis (Bt), foi criada para fornecer proteção contra o escaravelho-da-batata, que reduz a produtividade.[13] Comercializada pela Monsanto no fim da década de 1990, foi destinada ao mercado de fast food, mas retirada em 2001 após rejeição de varejistas e problemas de exportação enfrentados por processadores. Em 2011, a BASF solicitou à Autoridade Europeia para a Segurança Alimentar (EFSA) a aprovação de sua batata Fortuna como ração e alimento. A batata foi tornada resistente à requeima pela adição dos genes resistentes blb1 e blb2, originários da batata selvagem mexicana Solanum bulbocastanum.[138][139] No entanto, em fevereiro de 2013, a empresa retirou o pedido. Em 2014, o Departamento de Agricultura dos Estados Unidos (USDA) aprovou uma batata geneticamente modificada desenvolvida pela J. R. Simplot Company com dez modificações genéticas que reduzem o escurecimento por impacto e diminuem a formação de acrilamida quando frita. Nesse caso, a técnica utilizada foi a interferência por RNA, que elimina proteínas específicas ao invés de introduzir novas.[140][141]

Em 2005, cerca de 13% da abobrinha cultivada nos Estados Unidos era geneticamente modificada para resistir a três vírus, variedade também plantada no Canadá.[142][143]
Em 2013, o USDA aprovou a importação de um abacaxi transgênico de coloração rosa, que "superexpressa" um gene derivado da tangerina e suprime outros, aumentando a produção de licopeno. O ciclo de floração da planta foi alterado para proporcionar maior uniformidade de crescimento e qualidade. Segundo o USDA APHIS, esse abacaxi “não tem a capacidade de se propagar e persistir no ambiente após a colheita”. A Del Monte declarou que a produção ocorre em regime de monocultura, impedindo a formação de sementes, já que as flores não entram em contato com pólen compatível. A importação para o Havaí foi proibida por razões de “sanidade vegetal”.[144] Em outubro de 2020, a Del Monte lançou a venda comercial desses frutos sob a marca "Pinkglow".[145]
Em fevereiro de 2015, a maçã Arctic foi aprovada pelo USDA,[146] tornando-se a primeira maçã geneticamente modificada liberada para consumo nos Estados Unidos.[147] Essa variedade utiliza silenciamento genético para reduzir a expressão da polifenol oxidase (PPO), prevenindo assim o escurecimento da fruta.[148]
Tomate
Após a retirada do tomate Flavr Savr do mercado em 1999, os tomates geneticamente modificados não foram vendidos nos Estados Unidos durante décadas.[149]
Em fevereiro de 2024, o Tomate Roxo, criado pela Norfolk Plant Sciences, sediada no Reino Unido, foi lançado ao público. Ele se distingue por sua marcante cor roxa, proveniente do antioxidante antocianina. Esses tomates podem oferecer uma série de benefícios potenciais à saúde devido ao seu alto teor de antioxidantes. Cathie Martin, a criadora desses tomates, observou em um estudo que camundongos que receberam esses tomates viveram 30% mais do que aqueles que não os consumiram.[150]
Também em desenvolvimento no Reino Unido estão os tomates enriquecidos com vitamina D. Este tomate tem mais provitamina D3 que, quando exposta à luz UVB, se converte em vitamina D3.[151]
Milho
O milho, empregado tanto na alimentação quanto na produção de etanol, foi geneticamente modificado para tolerar diversos herbicidas, expressar a proteína derivada de Bacillus thuringiensis (Bt), capaz de eliminar certos insetos, além de apresentar tolerância à seca e ao calor, bem como restauração de fertilidade para produção de sementes em híbridos.[152][153] Em 2008, quando os cultivares transgênicos de milho foram liberados para comercialização no Brasil, apenas 6% do milho cultivado era transgênico. Na safra de 2014/2015 esse número superou 59%, chegando a atingir 89% na safra 2018/2019.[153] O milho pode ser processado em grãos, sêmola e farinha, sendo utilizado como ingrediente em panquecas, muffins, rosquinhas, empanados, massas, além de papinhas infantis, produtos cárneos, cereais e alguns produtos fermentados. A farinha de milho é usada na produção de bolos, pães, farofa, cuscuz, polenta e chips de milho.
Soja
A soja foi responsável por metade de todas as culturas geneticamente modificadas plantadas globalmente em 2014.[81] Essa cultura foi modificada para apresentar tolerância a herbicidas, resistência a insetos, tolerância à seca e produção de óleos com perfil nutricional mais saudável.[154][155] No Brasil, a soja transgênica é amplamente adotada, representando 98% da safra em 2019, o que consolida o país entre os principais produtores globais.[156]
Arroz

O arroz vem sendo modificado para características como valor nutricional,[7] fotossíntese melhorada,[157] resistência a pragas,[158] tolerância a herbicidas, aumento do tamanho dos grãos e sabores.[159]
O arroz dourado é a cultura transgênica mais conhecida voltada para o aumento do valor nutricional. Ele foi desenvolvido com três genes capazes de biossintetizar betacaroteno, precursor da vitamina A, nas partes comestíveis do arroz.[7] O objetivo é produzir um alimento biofortificado para cultivo e consumo em regiões com deficiência de vitamina A,[74][75][76][77] condição que, a cada ano, é estimada como responsável pela morte de cerca de 670 mil crianças menores de cinco anos[160] e por mais 500 mil casos de cegueira infantil irreversível.[161] A versão original do arroz dourado produzia 1,6 μg/g de carotenoides, valor que foi posteriormente ampliado em 23 vezes com novos desenvolvimentos.[162] Em 2018, o arroz dourado recebeu suas primeiras aprovações para uso alimentar.[163]
Trigo
Trigo geneticamente modificado tem sido desenvolvido para características como tolerância a seca e herbicidas. O trigo HB4, desenvolvido para tolerar a seca e resistir ao herbicida glufosinato, recebeu aprovação inicial na Argentina em 2020 e, em 2023, foi autorizado para cultivo no Brasil e no Paraguai.[164][165]
Algodão
O algodão geneticamente modificado é alterado para características como resistência a insetos e herbicidas.[166] Uma variedade de algodão foi geneticamente modificada para remover de suas sementes a toxina gossipol, de modo que seria seguro para os humanos comerem. A toxina permanece presente em outras partes da planta para proteger contra pragas.[167][168] O algodão livre da toxina é visto como uma forte fonte de proteína.[169]
Cana-de-açúcar
O Brasil se tornou o primeiro país a aprovar para comercialização o cultivo de cana-de-açúcar geneticamente modificada em 2017, a cana recebeu genes que conferem a habilidade de resistir a broca-da-cana.[170]
Feijão
Um feijão geneticamente modificado desenvolvido pela Embrapa para resistir ao vírus do mosaico dourado (BGMV) é aprovado para cultivo no Brasil desde 2011.[171] Várias variedades de feijão-caupi (Vigna unguiculata) geneticamente modificado foram desenvolvidas e aprovadas para cultivo em países africanos, como a Nigéria e Gana. A principal característica dessas variedades é a resistência a insetos, especialmente à broca da vagem (Maruca vitrata), uma praga que pode causar perdas de até 80% na produção.[172][173]
Cogumelo
Em abril de 2016, um cogumelo champignon modificado pela técnica CRISPR recebeu aprovação de facto nos Estados Unidos, após o USDA afirmar que não precisaria passar pelo processo regulatório da agência. A agência considera o cogumelo isento porque o processo de edição não envolveu a introdução de DNA estranho, em vez disso, vários pares de bases foram deletados de um gene duplicado que codifica uma enzima que causa o escurecimento, resultando em uma redução de 30% no nível dessa enzima.[85]
Pecuária
Um gado geneticamente modificado é um organismo do grupo de bovinos, ovinos, suínos, caprinos, aves, equinos e peixes, criados para consumo humano, cujo material genético (DNA) foi alterado por meio de técnicas de engenharia genética. Em alguns casos, o objetivo é introduzir uma nova característica nos animais que não ocorre naturalmente na espécie.
Uma revisão de 2003, publicada em nome da Food Standards Australia and New Zealand, examinou a experimentação transgênica em espécies de animais terrestres, bem como em espécies aquáticas, como peixes e crustáceos. A revisão examinou as técnicas moleculares utilizadas para a experimentação, bem como as técnicas de rastreamento dos transgenes em animais e produtos, bem como questões relacionadas à estabilidade dos transgenes.[174]
Alguns mamíferos normalmente usados para produção de alimentos foram modificados para produzir produtos não alimentícios, uma prática às vezes chamada de Pharming.
Salmão
O salmão AquAdvantage foi o primeiro animal geneticamente modificado aprovado para consumo humano, tendo sido autorizado pela FDA nos Estados Unidos em 2015.[9] Esse salmão recebeu um gene regulador do hormônio do crescimento proveniente do salmão-rei e um promotor extraído do peixe-carneiro americano, o que lhe permitiu crescer durante todo o ano, em vez de apenas na primavera e no verão.[82] A comercialização do salmão modificado foi também aprovada no Canadá em 2016[83] e no Brasil em 2021.[84] No entanto, o produtor deste salmão, AquaBounty Technologies, fechou suas instalações de salmão em dezembro de 2024 devido à perda de fundos.[175]
Suíno
Em 2021, a FDA norte-americana aprovou uma modificação genética em suínos que elimina quantidades detectáveis de alfa-gal, um gatilho para uma alergia rara.[9][10]
Microorganismos
Os bacteriófagos são uma causa economicamente significativa de falha de cultura na produção de queijo. Diversos microrganismos de cultura – especialmente Lactococcus lactis e Streptococcus thermophilus – têm sido estudados para análise genética e modificação visando aumentar a resistência a fagos. Isso tem se concentrado especialmente em modificações plasmidiais e cromossômicas recombinantes.[176][177]
Microorganismos geneticamente modificados também estão sendo utilizados na agricultura e na saúde do solo. O Proven, um produto geneticamente modificado criado pela empresa de biotecnologia Pivot Bio, utiliza micróbios fixadores de nitrogênio em vez de nitrogênio sintético no solo para culturas como o milho.[178][179]
Produtos derivados
Lecitina
A lecitina é um lipídio de ocorrência natural, encontrado na gema de ovo e em plantas produtoras de óleo. Atua como emulsificante e, por isso, é utilizada em diversos alimentos. Óleo de milho, soja e cártamo são fontes de lecitina, embora a maior parte da lecitina disponível comercialmente seja derivada da soja.[180][181][182] Quando suficientemente processada, a lecitina muitas vezes se torna indetectável pelos métodos padrão de análise.[183] Segundo a FDA, não há evidências que indiquem riscos à saúde pública quando a lecitina é utilizada em níveis comuns. A quantidade adicionada aos alimentos representa apenas de 2 a 10% dos 1 a 5 g de fosfoglicerídeos consumidos diariamente, em média.[180][181] Ainda assim, preocupações de consumidores em relação a alimentos transgênicos também se estendem a produtos como a lecitina.[184] Essas preocupações levaram a mudanças de políticas e regulamentações na Europa em 2000, quando foi aprovada a Regulamentação (CE) 50/2000,[185] que passou a exigir rotulagem de alimentos contendo aditivos derivados de organismos geneticamente modificados, incluindo a lecitina. Devido à dificuldade de identificar a origem de derivados como a lecitina com os métodos atuais de análise, as regulamentações europeias exigem que aqueles que desejam comercializar lecitina no continente utilizem um sistema abrangente de preservação de identidade.[186][187]
Açúcar
Os Estados Unidos importam 10% do seu açúcar, enquanto os 90% restantes são extraídos da beterraba-sacarina e da cana-de-açúcar. Após a desregulamentação em 2005, a beterraba resistente ao glifosato foi amplamente adotada no país, de modo que, em 2011, 95% da área cultivada com beterraba utilizava sementes resistentes ao herbicida.[188] As beterrabas transgênicas são aprovadas para cultivo nos Estados Unidos, Canadá e Japão, sendo a grande maioria produzida nos EUA. Elas também são aprovadas para importação e consumo na Austrália, Canadá, Colômbia, União Europeia, Japão, Coreia, México, Nova Zelândia, Filipinas, Federação Russa e Singapura.[189] A polpa resultante do processo de refino é utilizada como ração animal. O açúcar produzido a partir de beterrabas transgênicas não contém DNA nem proteínas — trata-se apenas de sacarose, quimicamente indistinguível do açúcar obtido de beterrabas não transgênicas.[190][191] Análises independentes, conduzidas por laboratórios internacionalmente reconhecidos, confirmaram que o açúcar proveniente da beterraba Roundup Ready é idêntico ao açúcar derivado de beterrabas convencionais cultivadas em condições comparáveis.[192]
Em 2017, o Brasil se tornou o primeiro país a aprovar para comercialização o cultivo de cana-de-açúcar geneticamente modificada resistente a insetos.[193] Alguns outros países também aprovam a importação de açúcar refinado derivado dessas culturas geneticamente modificadas, o produto refinado é considerado indistinguível do açúcar convencional.[194]
Óleo vegetal
A maior parte do óleo vegetal usado no Brasil é produzido a partir de culturas transgênicas como milho, algodão e soja.[195] O óleo vegetal é vendido diretamente aos consumidores como óleo de cozinha, gordura vegetal e margarina e é usado em alimentos preparados. Há uma quantidade extremamente pequena de proteína ou DNA da cultura original no óleo vegetal.[183][196] O óleo vegetal é feito de triglicerídeos extraídos de plantas ou sementes e, em seguida, refinados, podendo ser posteriormente processados por hidrogenação para transformar óleos líquidos em sólidos. O processo de refino remove todos ou quase todos os ingredientes não triglicerídeos.[197]
Outros usos
Ração animal
Gado e aves são criados com ração animal, grande parte da qual é composta por sobras de processamento de safras, incluindo safras transgênicas. Por exemplo, aproximadamente 43% de uma semente de canola é óleo. O que resta após a extração do óleo é uma farinha que se torna um ingrediente na ração animal e contém proteína de canola.[198] Da mesma forma, a maior parte da safra de soja é cultivada para óleo e farelo. O farelo de soja desengordurado e torrado com alto teor de proteína se torna ração para gado e ração para cães. 98% da safra de soja dos EUA é destinada à ração para gado.[199][200] Em 2011, 49% da colheita de milho dos EUA foi usada para ração para gado (incluindo a porcentagem de resíduos de dreche).[201] Apesar dos métodos se tornarem cada vez mais sensíveis, os testes ainda não conseguiram estabelecer diferenças na carne, no leite ou nos ovos dos animais, dependendo do tipo de ração com que são alimentados. É impossível dizer se um animal foi alimentado com soja transgênica apenas observando a carne, os laticínios ou os ovos resultantes. A única maneira de verificar a presença de OGM na ração animal é analisar a origem da própria ração.[202]
Enzimas produzidas por microrganismos geneticamente modificados também são integradas à ração animal para aumentar a disponibilidade de nutrientes e a digestão geral. Essas enzimas também podem trazer benefícios ao microbioma intestinal de um animal, bem como hidrolisar fatores antinutricionais presentes na ração.[203]
Proteínas
A base da engenharia genética é o DNA, que direciona a produção de proteínas. As proteínas também são a fonte comum de alérgenos humanos.[204] Quando novas proteínas são introduzidas, elas devem ser avaliadas quanto à potencial alergenicidade.[205]
O coalho é uma mistura de enzimas usada para coagular o leite na produção de queijos. Originalmente, estava disponível apenas no quarto estômago de bezerros, sendo, portanto, escasso e caro, ou proveniente de fontes microbianas, que muitas vezes resultavam em sabores indesejáveis. A engenharia genética tornou possível extrair genes produtores de coalho do estômago de animais e inseri-los em bactérias, fungos ou leveduras, fazendo com que esses microrganismos passassem a produzir quimosina, a principal enzima envolvida nesse processo.[206][207] Após a fermentação, o microrganismo modificado é eliminado. A quimosina é então isolada do meio de fermentação, de modo que a quimosina produzida por fermentação (FPC) utilizada na indústria queijeira possui uma sequência de aminoácidos idêntica à do coalho bovino.[208] A maior parte da quimosina aplicada permanece no soro, mas pequenas quantidades podem permanecer no queijo.[208]
A FPC foi a primeira enzima produzida artificialmente a ser aprovada pela Food and Drug Administration (FDA) dos Estados Unidos.[4] Os produtos derivados dessa técnica estão no mercado desde 1990 e, até 2015, não haviam sido superados comercialmente.[209] Em 1999, cerca de 60% dos queijos duros produzidos nos Estados Unidos eram feitos com FPC, participação que chegava a aproximadamente 80% no mercado global.[210] Já em 2008, entre 80% e 90% dos queijos comerciais produzidos nos EUA e no Reino Unido utilizavam FPC.[208]
Em alguns países, a somatotropina bovina recombinante (rBST, também chamada de hormônio de crescimento bovino ou BGH) é aprovada para administração com o objetivo de aumentar a produção de leite. A rBST pode estar presente no leite de vacas tratadas, mas é destruída no sistema digestivo e, mesmo que fosse injetada diretamente na corrente sanguínea humana, não teria efeito observável.[211] A FDA, a Organização Mundial da Saúde, a Associação Médica Americana, a Associação Dietética Americana e os Institutos Nacionais de Saúde dos Estados Unidos (NHI) já declararam, de forma independente, que os produtos lácteos e a carne de vacas tratadas com rBST são seguros para o consumo humano.[212] No entanto, em 30 de setembro de 2010, a Corte de Apelações do Sexto Circuito dos Estados Unidos, ao analisar evidências apresentadas, identificou uma “diferença composicional” entre o leite de vacas tratadas com rBGH e o de vacas não tratadas.[213][214] O tribunal afirmou que o leite de vacas tratadas apresenta níveis aumentados do hormônio fator de crescimento semelhante à insulina 1 (IGF-1), maior teor de gordura e menor teor de proteínas em determinados períodos do ciclo de lactação da vaca, além de contagem mais elevada de células somáticas, o que pode “fazer com que o leite azede mais rapidamente”.[214]
Benefícios
Alimentos geneticamente modificados são geralmente editados para apresentar algumas características desejadas, incluindo certos benefícios para a sobrevivência em ambientes extremos, um nível nutricional aprimorado, acesso a substâncias terapêuticas, desintoxicação e genes de resistência a pesticidas e herbicidas. Essas características podem ser benéficas para os humanos e o meio ambiente de determinadas maneiras.
Uma meta-análise de 2014 concluiu que a adopção da tecnologia transgênica reduziu a utilização de pesticidas químicos em 37%, aumentou o rendimento das colheitas em 22% e aumentou os lucros dos agricultores em 68%.[215] Essa redução no uso de pesticidas tem sido ecologicamente benéfica, mas os benefícios podem ser reduzidos pelo uso excessivo.[216] Os ganhos de produtividade e as reduções de pesticidas são maiores para culturas resistentes a insetos do que para culturas tolerantes a herbicidas.[217] Os ganhos de rendimento e lucro são maiores nos países em desenvolvimento do que nos países desenvolvidos.[215] Os envenenamentos por pesticidas foram reduzidos em 2,4 a 9 milhões de casos por ano somente na Índia.[218] As características combinadas de aumento da produtividade, redução do uso da terra, redução do uso de fertilizantes e redução do uso de máquinas agrícolas criam um ciclo de retroalimentação que reduz as emissões de carbono relacionadas à agricultura. Essas reduções foram estimadas em 7,5% do total de emissões agrícolas na União Europeia,[219] ou 33 milhões de toneladas de CO2, e em cerca de 8,76 milhões de toneladas de CO2 na Colômbia.[220]
Preparo para condições climáticas extremas
Plantas geneticamente modificadas podem apresentar maior resistência a condições climáticas extremas.[11][13] Alimentos geneticamente modificados podem, ocasionalmente, ser cultivados em locais com condições climáticas desfavoráveis.[14] A qualidade e o rendimento dos alimentos geneticamente modificados costumam ser aprimorados.[13] Esses alimentos tendem a crescer mais rapidamente do que os cultivados de forma convencional. Além disso, o uso de alimentos geneticamente modificados pode ser benéfico na tolerância à seca e a solos pobres.[14][221] Essas cultivares ganham destaque no contexto das mudanças climáticas e da desertificação, que impactam especialmente a agricultura no Brasil.[221]
Melhoria nutricional
O aumento dos níveis de nutrientes específicos em culturas alimentares pode ser alcançado por meio da engenharia genética. O estudo dessa técnica, às vezes chamada de melhoria nutricional, já está bastante avançado.[13] Os alimentos são cuidadosamente monitorados para adquirir qualidades específicas que se tornaram viáveis, como altos níveis de nutracêuticos e compostos benéficos à saúde, tornando-os um componente desejável de uma dieta variada.[222] Entre os avanços mais notáveis da modificação genética está o arroz dourado, cujo genoma foi alterado pela inserção de um gene de vitamina A proveniente do narciso, possibilitando a produção de pró-vitamina A.[13] Isso aumenta a atividade da fitoeno sintase, que, por sua vez, sintetiza maior quantidade de betacaroteno, além de permitir a modificação e o aprimoramento dos níveis de ferro e de sua biodisponibilidade.[16][18] Essa alteração afeta a cor e o teor de vitaminas do arroz, o que é benéfico em locais onde a deficiência de vitamina A é comum.[13] Além disso, o aumento nos teores de minerais, vitamina A e proteínas tem desempenhado um papel fundamental na prevenção da cegueira infantil e da anemia por deficiência de ferro.[16]
A composição lipídica também pode ser manipulada para produzir características desejáveis e nutrientes essenciais.[18] Evidências científicas mostram que o consumo inadequado de ácidos graxos poli-insaturados ômega-3 está ligada ao desenvolvimento de doenças crônicas e problemas de crescimento.[15][17] Por meio da engenharia genética, é possível introduzir genes que estimulam a produção desses ácidos graxos, elevando seus níveis nos alimentos.[18] O consumo de ômega-3 está associado à redução do colesterol LDL, dos triglicerídeos e do risco de doenças cardiovasculares.[15][17][18]
Produção de substâncias terapêuticas
Os organismos geneticamente modificados, incluindo batata, tomate e espinafre, podem ser utilizados na produção de substâncias que estimulam o sistema imunológico a responder a patógenos específicos.[18] Com o auxílio de técnicas de DNA recombinante, genes que codificam antígenos virais ou bacterianos podem ser transcritos e traduzidos em células vegetais.[18][19] Anticorpos são frequentemente produzidos em resposta à introdução de antígenos, permitindo que a microflora patológica gere uma resposta imune direcionada a esses antígenos. Os organismos transgênicos podem ser usados como vacinas orais, permitindo que as substâncias ativas entrem no sistema digestivo humano e estimulem uma resposta imune mucosal no trato alimentar. Essa técnica tem sido amplamente aplicada na produção de vacinas, incluindo em arroz, milho e soja.[18] Além disso, plantas transgênicas são amplamente usadas como biorreatores na produção de proteínas e peptídeos farmacêuticos, incluindo vacinas, hormônios, albumina sérica humana (HSA), entre outros. A utilização de plantas transgênicas ajuda a atender à demanda pelo rápido crescimento na produção de anticorpos terapêuticos.[17][18][19]
Desintoxicação
Uma variedade de algodão foi geneticamente modificada para remover de suas sementes a toxina gossipol, de modo que seria seguro para os humanos comerem. A toxina permanece presente em outras partes da planta para proteger contra pragas.[167][168]
Saúde e segurança
Existe um consenso científico[20][21][22][23][24] de que os alimentos atualmente disponíveis derivados de culturas geneticamente modificadas não representam um risco maior para a saúde humana do que os alimentos convencionais,[25][26][27][28][29][30][31] mas que cada alimento geneticamente modificado precisa ser testado caso a caso antes da introdução.[32][33][34] No entanto, os membros do público são muito menos propensos do que os cientistas a perceber os alimentos geneticamente modificados como seguros.[35][36][37][38] O status legal e regulatório dos alimentos geneticamente modificados varia de país para país, com algumas nações proibindo-os ou restringindo-os, e outras permitindo-os com graus de regulamentação amplamente diferentes,[39][40][41][42][43] que variam devido a fatores geográficos, religiosos, sociais e outros.[13][44][45][46][47]
"Os alimentos geneticamente modificados atualmente disponíveis no mercado internacional passaram por avaliações de segurança e não é provável que representem riscos para a saúde humana. Além disso, não foram demonstrados efeitos para a saúde resultantes do consumo desses alimentos na população em geral dos países em que foram aprovados."
A OMS enfatiza que os alimentos convencionais são geralmente considerados seguros com base em seu longo histórico de consumo, e novas variedades desenvolvidas por meio de técnicas tradicionais de melhoramento genético são frequentemente comercializadas sem avaliações de segurança obrigatórias, mesmo que tais processos possam levar a alterações em certas características, sejam elas benéficas ou potencialmente adversas. Em contrapartida, na maioria dos sistemas regulatórios, os alimentos geneticamente modificados devem passar por avaliações de segurança específicas, caso a caso, antes da comercialização, incluindo avaliações dos possíveis efeitos sobre a saúde humana e o meio ambiente.[48]
Os críticos alegam que os riscos para a saúde a longo prazo não foram adequadamente avaliados e propõem várias combinações de testes adicionais, rotulagem ou remoção do mercado.[13][223][224][225][226][227][228] Apesar dessas preocupações, estudos de longo prazo em seres humanos são limitados por restrições éticas e práticas.[229][230] No entanto, estudos em animais não humanos,[231][232][233][234][235][236][237] especialmente em gado,[238][239][240][241][242] não identificaram efeitos adversos à saúde após o uso contínuo de rações transgênicas. Uma revisão bibliográfica de 2012 sobre estudos que avaliaram o efeito da ração transgênica na saúde dos animais não encontrou evidências de que os animais tenham sido afetados negativamente, embora pequenas diferenças biológicas tenham sido ocasionalmente encontradas. Os estudos incluídos na revisão variaram de 90 dias a dois anos, com vários dos estudos mais longos considerando efeitos reprodutivos e intergeracionais.[237] Um estudo que analisou a microbiota intestinal e os perfis de metabólitos em duas gerações de macacos-cinomolgos que foram alimentados com milho transgênico não encontrou diferenças significativas na maioria dos indicadores biológicos, e as pequenas variações observadas não afetaram as funções fisiológicas durante o período de alimentação.[243] Além disso, os dados epidemiológicos disponíveis não demonstram associações entre o consumo de alimentos geneticamente modificados e o surgimento de doenças ou condições crônicas.[31] Até o momento, nenhum efeito nocivo à saúde humana foi comprovado com a introdução de alimentos transgênicos.[48]
Alguns estudos que pretendiam demonstrar danos foram desacreditados, levando em alguns casos à condenação acadêmica dos pesquisadores, como o caso Pusztai e o caso Séralini.[23]
Não existem certificações para alimentos que tenham sido verificados como geneticamente modificados — especialmente de uma forma que seja bem compreendida, segura e ambientalmente amigável — e que, ao mesmo tempo, sejam orgânicos (ou seja, produzidos sem o uso de pesticidas químicos) no Brasil,[244] na União Europeia,[245] nos Estados Unidos e possivelmente no mundo, oferecendo aos consumidores a escolha binária entre alimentos geneticamente modificados ou alimentos orgânicos.[246][247][248]
Equivalência substancial
O status legal e regulatório dos alimentos geneticamente modificados varia de país para país, com algumas nações proibindo-os ou restringindo-os, e outras permitindo-os com graus de regulamentação amplamente diferentes[39][40][41][42][43]
Os governos gerenciam a comercialização e a liberação de alimentos transgênicos caso a caso. Os países diferem em suas avaliações de risco e regulamentações. Diferenças marcantes distinguem os EUA da Europa.[41] Culturas que não se destinam a alimentos geralmente não são revisadas quanto à segurança alimentar.[249] Alimentos transgênicos não são testados em humanos antes da comercialização porque não são um único produto químico, nem se destinam a ser ingeridos em doses e intervalos específicos, o que complica o desenho de estudos clínicos.[250] Os reguladores examinam a modificação genética, os produtos proteicos relacionados e quaisquer alterações que essas proteínas façam no alimento.[251]
Os reguladores verificam se os alimentos geneticamente modificados são "substancialmente equivalentes" aos seus equivalentes convencionais, para detectar quaisquer consequências negativas não intencionais.[250][252][253][254] Para determinar essa equivalência, o fabricante conduz testes destinados a identificar possíveis alterações inesperadas em componentes específicos — como toxinas, nutrientes ou alérgenos — e geralmente avaliando também os efeitos do processamento e da transformação do alimento in natura, comparando o produto geneticamente modificado ao seu equivalente convencional não modificado. Esses dados são posteriormente analisados por uma agência reguladora. Se os reguladores concluírem que não há diferenças significativas entre os produtos modificados e os convencionais, geralmente não são necessários testes adicionais de segurança alimentar. Contudo, caso o produto não tenha equivalente natural, apresente diferenças relevantes em relação ao alimento não modificado ou envolva outros fatores de risco — por exemplo, a expressão de uma proteína que não existia anteriormente na composição —, testes de segurança suplementares podem ser exigidos. Proteínas novas ou anomalias detectadas na análise de equivalência substancial passam por avaliações toxicológicas adicionais, resultando em uma análise final de segurança.[250][254][255] Testes adicionais podem ser recomendados para avaliar impactos ambientais.[256]
A equivalência substancial é o princípio subjacente na avaliação da segurança alimentar dos alimentos geneticamente modificados para uma série de agências nacionais e internacionais, incluindo a Comissão Técnica Nacional de Biossegurança (CTNBio),[257] a Agência Canadense de Inspeção de Alimentos (CFIA), o Ministério da Saúde, Trabalho e Bem-Estar do Japão (MHLW), a Food and Drug Administration dos EUA (FDA) e a Organização das Nações Unidas para Alimentação e Agricultura (FAO) e a Organização Mundial da Saúde (OMS).[258]
"A Organização Mundial da Saúde, a Associação Médica Americana, a Academia Nacional de Ciências dos EUA, a Sociedade Real Britânica e todas as outras organizações respeitadas que examinaram as evidências chegaram à mesma conclusão: consumir alimentos que contenham ingredientes derivados de culturas geneticamente modificadas não é mais arriscado do que consumir os mesmos alimentos que contenham ingredientes de plantas cultivadas modificadas por técnicas convencionais de melhoramento de plantas."
O conceito de comparar alimentos geneticamente modificados com alimentos tradicionais como base para avaliação de segurança foi introduzido pela primeira vez como uma recomendação durante a consulta conjunta de de especialistas FAO/OMS sobre biotecnologia e segurança alimentar de 1990 (uma conferência científica de autoridades e da indústria), embora o termo "equivalência substancial" não tenha sido usado.[260] A equivalência substancial foi definida pela primeira vez em 1993 pela Organização para a Cooperação e Desenvolvimento Econômico (OCDE).[227][261][253] O conceito foi reforçado por uma consulta conjunta de especialistas da FAO/OMS em 1996. Essa reunião destacou que a equivalência substancial não constitui, em si, uma avaliação de segurança, mas fornece uma estrutura para organizar a análise dos alimentos derivados de plantas com DNA recombinante, considerando suas características e composição. Quando um novo produto é considerado equivalente a um alimento convencional com histórico de consumo seguro, entende-se que ele será tão seguro quanto o alimento tradicional, desde que utilizado sob padrões semelhantes de consumo e processamento. A FAO reforça que uma das principais vantagens do conceito é sua flexibilidade, útil na avaliação de segurança de alimentos oriundos da biotecnologia moderna. Ele permite identificar diferenças que possam demandar investigação mais aprofundada. Por se basear em uma comparação, pode ser aplicado em diferentes etapas da cadeia alimentar, como no produto colhido, em frações processadas ou no alimento final, direcionando a análise ao nível mais adequado conforme a natureza do produto.[255]
Em 2000, uma nova consulta conjunta da FAO/OMS sobre alimentos derivados da biotecnologia revisitou o conceito. O grupo concluiu que a avaliação de segurança deve seguir uma abordagem integrada, gradual e caso a caso, apoiada por um conjunto estruturado de questões. Reafirmou-se que a equivalência substancial, ao comparar alimentos derivados de plantas transgênicas com seus equivalentes convencionais, é a estratégia mais apropriada para identificar possíveis questões de segurança e nutrição. Ressaltou-se também que a equivalência substancial não substitui a análise de risco — já que não caracteriza perigos diretamente —, mas deve orientar o processo comparativo em relação ao alimento convencional utilizado como referência. Os especialistas consideraram satisfatória a metodologia empregada na avaliação de segurança dos alimentos transgênicos aprovados comercialmente até então e concluíram que a aplicação da equivalência substancial fortalece o quadro de avaliação existente. Segundo a consulta, não havia, à época, estratégias alternativas que oferecessem maior garantia de segurança.[255]
Algumas organizações médicas, incluindo a Associação Médica Britânica, defendem mais cautela na regulação de OGMs com base no princípio da precaução.[34] Ele recomenda que, diante de riscos potenciais ou incerteza científica relevante, sejam tomadas medidas preventivas ou que a ação proposta seja suspensa ou reavaliada, em vez de aguardar prova conclusiva de dano.[262] Na sua formulação rigorosa, o princípio só pode ser relaxado quando for conseguida prova robusta de que nenhum mal será produzido.[262] O princípio da precaução foi incorporado ao Protocolo de Cartagena sobre Biossegurança, desenvolvido no âmbito da Convenção sobre Diversidade Biológica.[263]
No ano de 1997, a União Europeia estabeleceu um procedimento de avaliação de novos alimentos pelo qual, uma vez que o produtor tenha confirmado a equivalência substancial com um alimento existente, a notificação governamental, com evidências científicas que a acompanham, é o único requisito para a liberação comercial. No entanto, alimentos que contêm organismos geneticamente modificados são excluídos e exigem autorização obrigatória.[261] Na UE, aplica-se o princípio da precaução, segundo o qual os riscos potenciais dos OGM ainda não são plenamente conhecidos. Por isso, exige-se uma demonstração rigorosa de segurança antes da aprovação, bem como autorização prévia para a comercialização e monitoramento ambiental após a entrada no mercado.[262][264]
Regulamentações
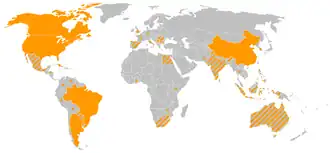
_Food_labeling_laws_map_4.png)
Amarelo: regulamentação de rotulagem obrigatória e negativa para alimentos transgênicos (ou seja, que não contêm OGMs).
A regulamentação governamental sobre o desenvolvimento e a liberação de OGMs varia amplamente entre os países. Diferenças marcantes separam a regulamentação de OGMs nos EUA e na União Europeia.[41] A regulamentação também varia de acordo com o uso pretendido do produto. Por exemplo, uma cultura não destinada ao uso alimentar geralmente não é analisada pelas autoridades responsáveis pela segurança alimentar.[249] A regulamentação europeia e da UE tem sido muito mais restritiva do que em qualquer outro lugar do mundo: em 2013, apenas 1 cultivar de milho e 1 cultivar de batata foram aprovadas, e oito Estados-membros da UE não permitiram nem mesmo essas.[23]
Regulamentações do Brasil
A Lei de Biossegurança (Lei nº 11.105), sancionada em 2005 e regulamentada pelo Decreto nº 5.591/2005, estabeleceu normas de segurança e fiscalização para atividades com organismos geneticamente modificados (OGMs) e seus derivados. Ela atualizou a legislação anterior (Lei nº 8.974/1995), criada principalmente para regulamentar o plantio comercial da soja transgênica resistente ao glifosato em 1998.[43][73] A lei define regras gerais para pesquisa, produção, transporte, importação, exportação, armazenamento, liberação ambiental e comercialização de OGMs. Seu objetivo é garantir a biossegurança, proteger a saúde humana, animal, vegetal e o meio ambiente, observando o princípio da precaução.[43][78]
A Lei criou quatro instâncias principais:
- Conselho Nacional de Biossegurança (CNBS) – formado por Ministros de Estado, assessora o Presidente na formulação da Política Nacional de Biossegurança e pode vetar liberações comerciais por razões socioeconômicas ou estratégicas.[265]
- Comissão Técnica Nacional de Biossegurança (CTNBio) – vinculada ao Ministério da Ciência, Tecnologia e Inovação, sua finalidade é prestar apoio técnico consultivo e assessoramento ao Governo Federal na formulação, atualização e implementação da Política Nacional de Biossegurança relativa a organismos geneticamente modificados (OGMs), bem como no estabelecimento de normas técnicas de segurança e pareceres técnicos referentes à proteção da saúde humana, dos organismos vivos e do meio ambiente, para atividades que envolvam a construção, experimentação, cultivo, manipulação, transporte, comercialização, consumo, armazenamento, liberação e descarte de OGM e derivados.[43][265]
- Comissão Interna de Biossegurança (CIBio) – obrigatória em cada instituição que utilize OGMs; garante condições de biossegurança nas instalações e envia relatórios anuais à CTNBio.[265]
- Órgãos e Entidades de Registro e Fiscalização (OERF) – como Ministério da Agricultura e Pecuária, Ministério da Saúde, Ministério do Meio Ambiente e Mudança do Clima e Ministério de Pesca e Aquicultura; fiscalizam pesquisas e atividades comerciais, aplicando sanções quando necessário.[265]
Um Certificado de Qualidade em Biossegurança (CQB), é uma autorização emitida pela CTNBio para instituições que desejam desenvolver atividades com OGMs e seus derivados. Para obtê-lo, a instituição precisa ter uma CIBio e cumprir requisitos de infraestrutura, pessoal técnico e segurança para manipular um OGM.[266]
A CTNBio estabeleceu em 2018 normas para a avaliação das Técnicas Inovadoras de Melhoramento de Precisão (TIMPs), também chamadas de New Breeding Technologies (NBTs), incluindo, por exemplo, CRISPR e TALEN. Segundo a resolução, produtos resultantes de TIMPs podem não ser considerados organismos geneticamente modificados (OGMs) caso atendam a critérios como: ausência comprovada de DNA/RNA recombinante, uso de moléculas que não se multiplicam em células vivas ou mutagênese sítio-dirigida sem inserção de transgenes. Nesses casos, cabe às instituições interessadas solicitar consulta à CTNBio, em uma análise caso a caso, apresentando dados técnicos sobre o organismo parental, a técnica empregada e o produto final.[267]
Regulamentações africanas
Nações como África do Sul, Nigéria, Gana, Etiópia, Sudão, Malawi, Essuatíni, Burkina Faso e Quênia já aprovaram ou cultivam comercialmente algumas culturas geneticamente modificadas, como algodão, feijão-caupi, soja e milho.[268][269] Muitos outros países africanos ainda se encontram em fases de ensaios de campo, discussão legislativa ou mesmo em impasse político e regulatório.[269][270] Os principais obstáculos para a expansão dos OGMs na África incluem a fragilidade das estruturas regulatórias, a escassez de recursos financeiros e técnicos, a falta de capacidade para monitoramento e avaliação de risco, além de um forte componente político e social.[269]
Até 2024, nenhum país da África Lusófona aprova ou cultiva legalmente culturas geneticamente modificadas para comercialização.[268]
Angola
Em Angola, a legislação, estabelecida pelo Decreto Presidencial nº 14/192 de 2004, proíbe a importação de sementes geneticamente modificadas, embora permita sua entrada para fins de pesquisa mediante autorização do Ministro da Agricultura. Apesar da proibição formal, Angola depende fortemente de importações de alimentos e não possui mecanismos eficazes para rastrear a origem de produtos adquiridos de países que produzem organismos geneticamente modificados (OGMs) em larga escala, o que gera contradições práticas na política adotada. O país está desenvolvendo uma estrutura institucional para avaliação de segurança de alimentos geneticamente modificados, rotulagem ou monitoramento de situações de presença adventícia de OGMs.[270] Em 2024, foi criado um Comité de Sementes Geneticamente Modificadas (CSGM) para estabelecer um sistema de biossegurança no país.[271] Atualmente, Angola está em processo de desenvolver diretrizes nacionais de biossegurança mas nunca realizou avaliações próprias de segurança alimentar com produtos transgênicos.[270]
Cabo Verde
Em Cabo Verde, a regulamentação sobre organismos geneticamente modificados ainda está em desenvolvimento. O Quadro Nacional de Biossegurança (QNB) de Cabo Verde foi elaborado em 2007.[272] Até o momento não existe uma estrutura formal para a avaliação de segurança alimentar de OGMs, e nunca foram conduzidas avaliações nacionais desse tipo. O país está em processo de elaboração de regulamentos e políticas para identificar produtos que contenham ingredientes geneticamente modificados.[270]
Guiné-Bissau
Na Guiné-Bissau, a regulamentação sobre organismos geneticamente modificados ainda está em desenvolvimento. A Guiné-Bissau nunca realizou avaliações de segurança de alimentos transgênicos. O país não produz nem importa alimentos ou rações geneticamente modificados, tendo proibido a sua entrada. Da mesma forma, não possui sistema de monitoramento de situações de presença adventícia de OGMs e não conta com regulamentação sobre rotulagem desses produtos.[270]
Moçambique
Moçambique possui um regulamento de biossegurança (Decreto n.º 71/2014) que estabelece normas e mecanismos para a pesquisa e o uso de OGMs, com o objetivo de proteger a saúde humana e o ambiente.[273] A Autoridade Nacional de Biossegurança, sob responsabilidade do Ministério da Ciência e Tecnologia, coordena o processo com apoio do Grupo Inter-Institucional de Bio-Segurança (GIIBS).[273] Em 2025, o Instituto de Investigação Agrária de Moçambique (IIAM) realizou testes de campo com milho geneticamente modificado e, diante dos resultados positivos, submeteu os dados à autoridade reguladora competente para obter autorização de uso comercial dessas sementes no país.[274]
Regulamentações dos Estados Unidos
Nos EUA, três organizações governamentais regulamentam os OGMs. A FDA (Food and Drug Administration) verifica a composição química dos organismos em busca de potenciais alérgenos. O Departamento de Agricultura dos Estados Unidos (USDA) supervisiona os testes de campo e monitora a distribuição de sementes geneticamente modificadas. A Agência de Proteção Ambiental dos Estados Unidos (EPA) é responsável por monitorar o uso de pesticidas, incluindo plantas modificadas para conter proteínas tóxicas para insetos. Assim como o USDA, a EPA também supervisiona os testes de campo e a distribuição de culturas que tiveram contato com pesticidas para garantir a segurança ambiental.[275]
Regulamentações da União Europeia
Tanto a Autoridade Europeia para a Segurança Alimentar (EFSA) quanto os Estados-membros elaboram uma avaliação de risco. Essa avaliação deve demonstrar que o alimento é seguro para a saúde humana e para o meio ambiente "nas condições de uso pretendidas".[262][264]
O controle da União Europeia sobre organismos geneticamente modificados é uma parte específica de uma imagem da promessa e das limitações do debate como uma estrutura para regulamentação supranacional.[46] As questões levantadas pela regulamentação de OGMs da UE causaram grandes problemas na agricultura, na política, nas sociedades, no status e em outros campos.[45][46] A legislação da UE regula o desenvolvimento e o uso de OGMs atribuindo responsabilidades a diferentes autoridades, públicas e privadas, acompanhadas pelo reconhecimento limitado dos direitos públicos de informação, consulta e participação.[46] A Convenção Europeia dos Direitos Humanos (CEDH) garantiu certos direitos e proteção para a biotecnologia OGM na UE. No entanto, o valor da dignidade humana, da liberdade, da igualdade e da solidariedade, bem como o status da democracia e do direito, conforme enfatizado na Carta dos Direitos Fundamentais da União Europeia, são considerados a estrutura ética que rege o emprego da pesquisa e do desenvolvimento científico e tecnológico.[45]
Devido às diferenças políticas, religiosas e sociais entre os países da UE, a posição da UE sobre os alimentos transgênicos tem sido dividida geograficamente, incluindo mais de 100 regiões "livres de transgênicos". As diferentes atitudes regionais em relação aos alimentos transgênicos tornam quase impossível chegar a um acordo comum sobre esses alimentos.[46] Nos últimos anos, porém, a sensação de crise que isso gerou para a União Europeia se intensificou.[47] Alguns Estados-membros, incluindo Alemanha, França, Áustria, Itália e Luxemburgo, até proibiram o plantio de certos alimentos geneticamente modificados em seus países em resposta à resistência pública aos alimentos geneticamente modificados.[46][47] Tudo isso acontece em um cenário em que consumidores defendem a ideia de que alimentos geneticamente modificados são prejudiciais ao meio ambiente e à saúde humana, revoltando-se contra eles em uma coalizão antibiotecnologia.[44] O atual impasse político sobre alimentos geneticamente modificados também é uma consequência da proibição e ainda precisa ser resolvido por métodos e processos científicos.[47] A opinião pública tende a politizar a questão dos OGM, que constitui o principal obstáculo a um acordo na UE.[46]
Rotulagem

Em 2015, 64 países exigiam a rotulagem de produtos OGM no mercado.[276] Outras jurisdições tornam essa rotulagem voluntária ou têm planos para exigir a rotulagem.[270] Alguns exportadores de alimentos geneticamente modificados, como os Estados Unidos (até 2018), Argentina e Canadá, adotaram abordagens de rotulagem voluntária.[277]
No Brasil, a rotulagem de produtos com OGMs é regulada pelo Decreto nº 4.680/2003, que determina que alimentos contendo ou derivados de OGMs, acima de 1% da composição, devem informar o consumidor sobre a natureza transgênica do produto. Os alimentos e ingredientes produzidos a partir de animais alimentados com ração contendo ingredientes transgênicos devem trazer a seguinte expressão: "(nome do animal) alimentado com ração contendo ingrediente transgênico" ou "(nome do ingrediente) produzido a partir de animal alimentado com ração contendo ingrediente transgênico". Aos alimentos e ingredientes alimentares que não contenham nem sejam produzidos a partir de organismos geneticamente modificados é facultativa a rotulagem "(nome do produto ou ingrediente) livre de transgênicos", desde que tenham similares transgênicos no mercado brasileiro.[278]
Na União Europeia, todos os alimentos (incluindo alimentos processados) ou rações que contenham mais de 0,9% de OGMs devem ser rotulados.[279] Ao mesmo tempo, devido à falta de uma definição única e clara do que caracteriza um OGM, vários alimentos criados usando técnicas de engenharia genética (como melhoramento por mutação) são excluídos da rotulagem e regulamentação com base em "convenções" e uso tradicional.[51]
Nos Estados Unidos, em julho de 2016, a Lei Pública 114-214 foi promulgada para regulamentar a rotulagem de alimentos transgênicos em nível nacional.[280]
Os esforços em todo o mundo que estão sendo feitos para ajudar a restringir e rotular os OGMs nos alimentos envolvem campanhas anti-engenharia genética.[281]
Detecção
Testes para detecção de OGMs em alimentos e rações são feitos rotineiramente usando técnicas moleculares como RCP e bioinformática.[282]
Em um artigo de janeiro de 2010, foi descrita a extração e detecção de DNA ao longo de toda a cadeia de processamento industrial do óleo de soja, com o objetivo de monitorar a presença da soja Roundup Ready (RR):
“A amplificação do gene da lectina da soja por reação em cadeia da polimerase (RCP) em ponto final foi obtida com sucesso em todas as etapas dos processos de extração e refino, até o óleo de soja totalmente refinado. A amplificação da soja RR por ensaios de PCR usando primers específicos para o evento também foi obtida em todas as etapas de extração e refino, exceto nas etapas intermediárias de refino (neutralização, lavagem e branqueamento), possivelmente devido à instabilidade da amostra. Os ensaios de PCR em tempo real, utilizando sondas específicas, confirmaram todos os resultados e demonstraram que é possível detectar e quantificar organismos geneticamente modificados no óleo de soja totalmente refinado. Até onde sabemos, isso nunca havia sido relatado antes e representa uma conquista importante em relação à rastreabilidade de organismos geneticamente modificados em óleos refinados.”[283]
Comércio
O Protocolo de Cartagena estabelece os requisitos para o comércio internacional de OGMs entre os países signatários. Quaisquer remessas que contenham organismos geneticamente modificados destinados à alimentação animal, animal ou industrialização devem ser identificadas e uma lista dos eventos transgênicos deve estar disponível.[284] Alguns países restrigem a importação de alimentos produzidos com OGMs.[270]
Desenho da metodologia de regulamentação
Os cientistas têm argumentado ou elaborado a necessidade de uma reforma baseada em evidências da regulamentação de culturas agrícolas geneticamente modificadas que a mova da regulamentação baseada nas características do processo de desenvolvimento (regulamentação baseada no processo) para as características do produto (regulamentação baseada no produto).[285]
Controvérsias
A controvérsia sobre alimentos geneticamente modificados consiste em um conjunto de disputas sobre o uso de alimentos feitos a partir de culturas geneticamente modificadas. As disputas envolvem consumidores, agricultores, empresas de biotecnologia, reguladores governamentais, organizações não governamentais, ativistas ambientais e políticos e cientistas. As principais divergências incluem se os alimentos geneticamente modificados podem ser consumidos com segurança, prejudicam o corpo humano e o meio ambiente e/ou são adequadamente testados e regulamentados.[13][223][224][225][226][227][228][286] A objetividade da pesquisa científica e das publicações tem sido contestada. Muitos estudos sobre a segurança dos alimentos geneticamente modificados foram questionados como falhos, insuficientes, artificiosos e/ou apresentando conflito de interesses.[287][288][289][290][291][292][293] As disputas relacionadas à agricultura incluem o uso e o impacto de pesticidas, a produção e o uso de sementes, os efeitos colaterais em culturas/fazendas não transgênicas, e o potencial controle do fornecimento de alimentos transgênicos por empresas de sementes.[294][295][296][297][298][299][300][301] Discussões éticas sobre o patenteamento de vidas também são abordadas.[302]

Os conflitos perduram desde a invenção dos alimentos geneticamente modificados. Ocuparam a mídia, os tribunais, os governos locais, regionais, nacionais e organizações internacionais. Protestos populares contra os alimentos transgênicos têm sido organizados em vários países.[303][304][305] Em 2012 a Monsanto, uma das principais empresas de biotecnologia, hoje detida pela Bayer, foi condenada no Brasil a pagar 500 mil reais por danos morais causados aos consumidores e por propaganda enganosa e abusiva.[306]
Os esquemas de rotulagem "livre de OGMs" ou "livre de transgênicos" estão causando controvérsias na comunidade agrícola devido à falta de definição clara, à inconsistência de sua aplicação e são descritos como "enganosos".[307]
Alergenicidade
Novas alergias podem ser introduzidas inadvertidamente, de acordo com cientistas, grupos comunitários e membros do público preocupados com a variação genética dos alimentos.[13] Um exemplo envolve a produção de soja rica em metionina.[18] A metionina é um aminoácido obtido pela síntese de substâncias derivadas da castanha-do-pará, que pode ser um alérgeno.[18][308] O gene da castanha-do-pará foi inserido na soja durante testes de laboratório.[14] Como foi descoberto que pessoas alérgicas à castanha-do-pará também poderiam ser alérgicas à soja geneticamente modificada, o experimento foi interrompido.[13][309] Ensaios in vitro, como RAST ou soro de pessoas alérgicas à cultura original, podem ser aplicados para testar a alergenicidade de produtos geneticamente modificados com fonte conhecida do gene.[13] Isso foi estabelecido em soja transgênica que expressou proteínas 2S de castanha-do-pará e batatas transgênicas que expressaram genes de proteína de bacalhau.[14] A expressão e a síntese de novas proteínas, antes indisponíveis nas células parentais, foram alcançadas pela transferência de genes das células de um organismo para o núcleo de outro. Os riscos potenciais de alergia que podem se desenvolver com a ingestão de alimentos transgênicos advêm da sequência de aminoácidos na formação das proteínas.[222] No entanto, não houve relatos de reações alérgicas a alimentos geneticamente modificados atualmente aprovados para consumo humano, e os experimentos não mostraram nenhuma diferença mensurável na alergenicidade entre a soja geneticamente modificada e a não geneticamente modificada.[13][222][310][311]
Genes de resistência
Cientistas sugerem que os consumidores também devem prestar atenção aos problemas de saúde associados ao uso de plantas resistentes a pesticidas e herbicidas.[14] Os genes ‘Bt’ causam resistência a insetos nas culturas geneticamente modificadas atuais, no entanto, outros métodos para conferir resistência a insetos estão em desenvolvimento.[312] Os genes Bt são geralmente obtidos da bactéria do solo Bacillus thuringiensis e podem gerar uma proteína que se decompõe no intestino do inseto, liberando uma toxina chamada delta-endotoxina, que causa paralisia e morte.[47] Preocupações sobre a resistência e os efeitos não desejados de culturas que expressam toxinas Bt, consequências de plantas transgênicas tolerantes a herbicidas causadas pelo uso de herbicidas e a transferência de expressão genética de culturas geneticamente modificadas por meio de transferência genética vertical e horizontal estão todas relacionadas à expressão de material transgênico.[45]
Transferência horizontal de genes
A transferência horizontal de genes é o movimento de genes de um organismo para outro de uma maneira diferente da reprodução.
O risco de transferência horizontal de genes entre plantas geneticamente modificadas e animais é muito baixo e, na maioria dos casos, espera-se que seja menor do que as taxas de ocorrência natural de fundo.[313] Dois estudos sobre os possíveis efeitos da alimentação de animais com alimentos geneticamente modificados não encontraram resíduos de DNA recombinante ou novas proteínas em nenhuma amostra de órgão ou tecido.[314][315] Estudos encontraram DNA do vírus M13, proteína fluorescente verde e genes RuBisCO no sangue e tecido de animais,[316][317] e em 2012, um artigo sugeriu que um microRNA específico do arroz poderia ser encontrado em quantidades muito baixas no soro humano e animal. Outros estudos[318][319] no entanto, não encontraram nenhuma ou insignificante transferência de microRNAs vegetais para o sangue de humanos ou de qualquer um dos três organismos modelo.
Outra preocupação é que o gene de resistência a antibióticos comumente usado como marcador genético em culturas transgênicas pode ser transferido para bactérias, no solo ou no trato digestivo, podendo criar superbactérias resistentes.[320][321] A transferência de genes de plantas para bactérias é extremamente rara devido às condições necessárias e aos mecanismos específicos necessários para a transferência, incorporação e transmissão dos genes nas bactérias.[322][323][324][325][326][327] Um estudo de 2004 envolvendo voluntários humanos examinou se o transgene da soja modificada seria transferido para bactérias que vivem no intestino humano. Em 2012, este foi o único estudo de alimentação humana conduzido com alimentos transgênicos. O transgene foi detectado em três voluntários de um grupo de sete que tiveram seus intestinos grossos removidos por razões médicas. Como essa transferência genética não aumentou após o consumo da soja modificada, os pesquisadores concluíram que a transferência genética não ocorreu. Em voluntários com tratos digestivos intactos, o transgene não sobreviveu.[328] Os genes de resistência a antibióticos usados na engenharia genética são encontrados naturalmente em muitos patógenos[329] e os antibióticos aos quais esses genes conferem resistência não são amplamente prescritos.[324][330]
Não há evidências de que os marcadores atualmente usados representem um risco à saúde humana.[255][322][323][324][325][326][327] No entanto, a OMS aconselha a indústria a evitar genes marcadores que conferem resistência a antibióticos.[48]
Impactos ambientais
Outra preocupação levantada pelos ecologistas é a possível disseminação dos genes resistentes a pragas para a vida selvagem.[13][47] Este é um exemplo de poluição genética, que frequentemente está associada à diminuição da biodiversidade, à proliferação de ervas daninhas resistentes e à formação de novas pragas e patógenos.[312][331]
O fluxo gênico entre culturas geneticamente modificados e plantas compatíveis, junto com o aumento do uso de herbicidas de amplo espectro,[332] pode aumentar o risco de populações de ervas daninhas resistentes a herbicidas.[333] O debate sobre a extensão e as consequências do fluxo gênico se intensificou em 2001, quando um artigo foi publicado mostrando que transgenes haviam sido encontrados no milho tradicional no México, o centro de diversidade da cultura.[334][335] Verificou-se que o fluxo gênico das safras geneticamente modificadas para outros organismos geralmente é menor do que o que ocorreria naturalmente.[336] A fim de abordar algumas dessas preocupações, alguns OGMs foram desenvolvidos com características para ajudar a controlar sua disseminação. Para evitar que o salmão geneticamente modificado se reproduza inadvertidamente com salmão selvagem, todos os peixes criados para alimentação são fêmeas, triplóides, 99% são reprodutivamente estéreis e criados em áreas onde o salmão fugitivo não poderia sobreviver.[337][338] As bactérias também foram modificadas para depender de nutrientes que não podem ser encontrados na natureza,[339] e a tecnologia de restrição de uso genético foi desenvolvida, embora ainda não comercializada, que faz com que a segunda geração de plantas transgênicas seja estéril.[340]
Estudos comprovam que o pólen resistente a herbicidas da colza transgênica pode se espalhar por até 3 km, enquanto a dispersão média de genes de culturas transgênicas é de 2 km e pode chegar a um máximo de 21 quilômetros.[331] A alta agressividade dessas culturas geneticamente modificadas pode causar certos desastres ao competir com as culturas tradicionais por água, luz e nutrientes.[308] O cruzamento de pólens espalhados com organismos circundantes levou à introdução de genes resistentes modificados.[14] Um banco de dados internacional que demonstrou contaminações genéticas com sementes indesejadas tem sido um grande problema devido à expansão dos testes de campo e do cultivo comercialmente viável de culturas geneticamente modificadas em todo o mundo.[308][331] Mesmo uma diminuição no número de uma praga sob o impacto de uma erva daninha resistente a pragas pode aumentar a população de outras pragas que competem com ela.[14] Os insetos benéficos, assim chamados porque se alimentam de pragas nas colheitas, também podem ser expostos a doses perigosas de toxina Bt.[13]
Outras preocupações ambientais e agronômicas incluem a diminuição da biodiversidade, o aumento de pragas secundárias (pragas não direcionadas) e a evolução de insetos resistentes.[341][342][343] Nas áreas da China e dos EUA com culturas Bt, a biodiversidade geral de insetos aumentou e o impacto de pragas secundárias foi mínimo. Descobriu-se que a resistência demorava a evoluir quando as estratégias de melhores práticas eram seguidas.[344] O impacto das safras Bt em organismos benéficos não-alvo tornou-se uma questão pública depois que um artigo de 1999 sugeriu que elas poderiam ser tóxicas para borboletas monarca . Estudos de acompanhamento mostraram que os níveis de toxicidade encontrados no campo não eram altos o suficiente para prejudicar as larvas.[345]
Outras preocupações
A introdução de culturas geneticamente modificadas no lugar de variedades mais adaptadas localmente pode levar a efeitos negativos de longo prazo em todo o sistema agrícola.[19] Grande parte da preocupação com a tecnologia transgênica envolve a inserção de genes que aumentam ou reduzem determinados compostos bioquímicos. Alternativamente, a nova enzima programada pode consumir o substrato, levando à formação e ao acúmulo dos produtos resultantes.[13]
Do ponto de vista socioeconômico, as culturas transgênicas geralmente dependem de altos níveis de insumos externos, como pesticidas e herbicidas, o que as restringe à agricultura de alta intensidade e monocultura. Somado a isso, a ampla rede de patentes sobre essas culturas limita o direito dos agricultores de comercializar as sementes colhidas sem o pagamento de royalties. Outros argumentos levantados por opositores dos transgênicos baseiam-se nos altos custos de isolamento e distribuição das culturas transgênicas em relação às não transgênicas.[19] As culturas transgênicas também vêm sendo criticadas por representarem potenciais riscos à segurança e à soberania alimentar, devido ao controle dos cultivos por empresas estrangeiras e à concentração do abastecimento de alimentos em companhias que produzem e comercializam organismos geneticamente modificados.[297]
Os consumidores podem ser categorizados com base em suas atitudes em relação aos alimentos geneticamente modificados.[44] O setor ‘atitudinal’ dos consumidores nos EUA pode ser explicado em parte por características cognitivas que nem sempre são observáveis. Características e valores individuais, por exemplo, podem influenciar a aceitação da biotecnologia pelos consumidores. A ideia de transplantar DNA animal em plantas é perturbadora para muitas pessoas.[14] Estudos mostraram que as atitudes dos consumidores em relação à tecnologia transgênica estão positivamente correlacionadas ao nível de conhecimento sobre o tema.[346] Constatou-se que uma maior aceitação da modificação genética geralmente está associada a níveis mais altos de escolaridade, enquanto níveis elevados de percepção de risco tendem a estar associados ao oposto.[44][346] As pessoas tendem a se preocupar com perigos imprevisíveis devido à falta de conhecimento suficiente para prever ou evitar impactos negativos.[346]
Outro fator crucial na mudança das atitudes dos consumidores em relação aos alimentos geneticamente modificados mostrou-se estar intimamente ligado à sua interação com características socioeconômicas e demográficas, como idade, etnia, local de residência e nível de consumo.[44][308] A oposição aos alimentos geneticamente modificados também pode incluir grupos religiosos e culturais, pois a natureza desses alimentos contraria o que acreditam serem produtos naturais.[14][308][347] Acusações de que os cientistas estão "brincando de Deus" e outras questões religiosas foram atribuídas à tecnologia desde o início.[348] Por um lado, verificou-se que os consumidores na maioria dos países europeus, especialmente no norte da Europa, no Reino Unido e na Alemanha, acreditam que os benefícios dos alimentos transgênicos não superam os riscos potenciais. Por outro lado, consumidores nos Estados Unidos e em outros países europeus geralmente consideram que os riscos dos alimentos transgênicos podem ser muito menores do que os benefícios que eles proporcionam.[222] Assim, espera-se que os alimentos transgênicos recebam apoio por meio de políticas mais adequadas e de regulamentações mais claras.[308]
Ver também
- Organismos geneticamente modificados
- Controvérsia sobre alimentos geneticamente modificados
- Transgênese
- Melhoramento por mutação
Referências
- ↑ a b c «OGMs e Transgênicos». Convivium Gastronomia UFRJ. 8 de julho de 2021. Consultado em 21 de agosto de 2025
- ↑ GM Science Review First Report Arquivado em 16 de outubro de 2013, no Wayback Machine., Prepared by the UK GM Science Review panel (julho de 2003) (em inglês) Chairman Professor Sir David King, Chief Scientific Advisor to the UK Government, p. 9
- ↑ a b Jackson, David A.; Symons, Robert H.; Berg, Paul (outubro de 1972). «Biochemical Method for Inserting New Genetic Information into DNA of Simian Virus 40: Circular SV40 DNA Molecules Containing Lambda Phage Genes and the Galactose Operon of Escherichia coli». Proceedings of the National Academy of Sciences (em inglês) (10): 2904–2909. ISSN 0027-8424. PMC 389671
 . PMID 4342968. doi:10.1073/pnas.69.10.2904. Consultado em 21 de agosto de 2025
. PMID 4342968. doi:10.1073/pnas.69.10.2904. Consultado em 21 de agosto de 2025
- ↑ a b c d Archives, L. A. Times (24 de março de 1990). «FDA Approves 1st Genetically Engineered Product for Food». Los Angeles Times (em inglês). Consultado em 21 de agosto de 2025
- ↑ a b c d Clive, James; F. Krattiger, Anatole (1996). «Global Review of the Field Testing and Commercialization of Transgenic Plants: 1986 to 1995» (PDF). ISAAA Briefs (em inglês). Consultado em 23 de agosto de 2025
- ↑ a b c d Brookes, Graham (3 de abril de 2019). «Twenty-one years of using insect resistant (GM) maize in Spain and Portugal: farm-level economic and environmental contributions». GM Crops & Food (2): 90–101. ISSN 2164-5698. PMC 6615534
 . PMID 31072184. doi:10.1080/21645698.2019.1614393. Consultado em 21 de agosto de 2025
. PMID 31072184. doi:10.1080/21645698.2019.1614393. Consultado em 21 de agosto de 2025
- ↑ a b c d e Ye, Xudong; Al-Babili, Salim; Klöti, Andreas; Zhang, Jing; Lucca, Paola; Beyer, Peter; Potrykus, Ingo (14 de janeiro de 2000). «Engineering the Provitamin A (β-Carotene) Biosynthetic Pathway into (Carotenoid-Free) Rice Endosperm». Science (em inglês) (5451): 303–305. ISSN 0036-8075. doi:10.1126/science.287.5451.303. Consultado em 21 de agosto de 2025
- ↑ a b Orenstein, José (5 de agosto de 2017). «Transgênicos: uma tecnologia em constante disputa». Nexo Jornal. Consultado em 21 de agosto de 2025
- ↑ a b c d e f «GMO Crops, Animal Food, and Beyond». US Food and Drug Administration (em inglês). Consultado em 21 de agosto de 2025
- ↑ a b c Cima, Greg (21 de janeiro de 2021). «FDA approves genetic alteration in pigs». American Veterinary Medical Foundation (em inglês). Consultado em 21 de agosto de 2025
- ↑ a b c «Descubra quais são as plantas transgênicas aprovadas no Brasil». CropLife. 11 de outubro de 2022. Consultado em 21 de agosto de 2025
- ↑ Ye, Xudong; Al-Babili, Salim; Klöti, Andreas; Zhang, Jing; Lucca, Paola; Beyer, Peter; Potrykus, Ingo (14 de janeiro de 2000). «Engineering the Provitamin A (β-Carotene) Biosynthetic Pathway into (Carotenoid-Free) Rice Endosperm». Science (em inglês) (5451): 303–305. ISSN 0036-8075. doi:10.1126/science.287.5451.303. Consultado em 21 de agosto de 2025
- ↑ a b c d e f g h i j k l m n o p q r s Bawa, A. S.; Anilakumar, K. R. (dezembro de 2013). «Genetically modified foods: safety, risks and public concerns-a review». Journal of Food Science and Technology (em inglês) (6): 1035–1046. ISSN 0022-1155. PMC 3791249
 . PMID 24426015. doi:10.1007/s13197-012-0899-1. Consultado em 21 de agosto de 2025
. PMID 24426015. doi:10.1007/s13197-012-0899-1. Consultado em 21 de agosto de 2025
- ↑ a b c d e f g h i j k Healey, Justin, ed. (2016). Organic and genetically modified food. Col: Issues in society. Thirroul, N.S.W: The Spinney Press
- ↑ a b c Mahgoub, Salah E. O.; Nollet, Leo M. L., eds. (2019). Testing and analysis of GMO-containing foods and feed. Col: Food analysis & properties series. Boca Raton London New York: CRC Press
- ↑ a b c Dizon, Francis; Costa, Sarah; Rock, Cheryl; Harris, Amanda; Husk, Cierra; Mei, Jenny (fevereiro de 2016). «Genetically Modified (GM) Foods and Ethical Eating». Journal of Food Science (em inglês) (2). ISSN 0022-1147. doi:10.1111/1750-3841.13191. Consultado em 21 de agosto de 2025
- ↑ a b c d Huang, Kunlun (2017). Safety Assessment of Genetically Modified Foods (em inglês). Singapore: Springer Singapore. Consultado em 21 de agosto de 2025
- ↑ a b c d e f g h i j k l Kramkowska, Marta; Grzelak, Teresa; Czyżewska, Krystyna (2013). «Benefits and risks associated with genetically modified food products». OCLC 922412861
- ↑ a b c d e Spreng, S; Viret, J (18 de março de 2005). «Plasmid maintenance systems suitable for GMO-based bacterial vaccines». Vaccine (em inglês) (17-18): 2060–2065. doi:10.1016/j.vaccine.2005.01.009. Consultado em 21 de agosto de 2025
- ↑ a b Nicolia, Alessandro; Manzo, Alberto; Veronesi, Fabio; Rosellini, Daniele (1 de março de 2014). «An overview of the last 10 years of genetically engineered crop safety research». Critical Reviews in Biotechnology (em inglês) (1): 77–88. ISSN 0738-8551. PMID 24041244. doi:10.3109/07388551.2013.823595. Consultado em 21 de agosto de 2025.
Revisamos a literatura científica sobre a segurança de cultivos transgênicos dos últimos 10 anos, que reflete o consenso científico amadurecido desde que as plantas transgênicas passaram a ser amplamente cultivadas em todo o mundo, e podemos concluir que a pesquisa científica conduzida até o momento não detectou nenhum risco significativo diretamente relacionado ao uso de cultivos transgênicos. A literatura sobre biodiversidade e o consumo de alimentos/rações transgênicos tem, por vezes, resultado em debates acalorados sobre a adequação dos delineamentos experimentais, a escolha dos métodos estatísticos ou a acessibilidade pública dos dados. Tal debate, mesmo que positivo e parte do processo natural de revisão pela comunidade científica, tem sido frequentemente distorcido pela mídia e frequentemente utilizado de forma política e inadequada em campanhas anti-cultivos transgênicos.
- ↑ a b «State of Food and Agriculture 2003–2004. Agricultural Biotechnology: Meeting the Needs of the Poor. Health and environmental impacts of transgenic crops». FAO (em inglês). Consultado em 21 de agosto de 2025.
As culturas transgênicas atualmente disponíveis e os alimentos derivados delas foram considerados seguros para consumo, e os métodos utilizados para testar sua segurança foram considerados apropriados. Essas conclusões representam o consenso das evidências científicas levantadas pelo ICSU (2003) e são consistentes com as opiniões da Organização Mundial da Saúde (OMS, 2002). Esses alimentos foram avaliados quanto ao aumento dos riscos à saúde humana por diversas autoridades regulatórias nacionais (entre outras, Argentina, Brasil, Canadá, China, Reino Unido e Estados Unidos), utilizando seus procedimentos nacionais de segurança alimentar (ICSU). Até o momento, nenhum efeito tóxico ou nutricionalmente deletério verificável, resultante do consumo de alimentos derivados de culturas geneticamente modificadas, foi descoberto em qualquer lugar do mundo (GM Science Review Panel). Milhões de pessoas consumiram alimentos derivados de plantas geneticamente modificadas — principalmente milho, soja e colza — sem quaisquer efeitos adversos observados (ICSU).
- ↑ a b Ronald, Pamela (1 de maio de 2011). «Plant Genetics, Sustainable Agriculture and Global Food Security». Genetics (em inglês) (1): 11–20. ISSN 1943-2631. PMC 3120150
 . PMID 21546547. doi:10.1534/genetics.111.128553. Consultado em 21 de agosto de 2025.
. PMID 21546547. doi:10.1534/genetics.111.128553. Consultado em 21 de agosto de 2025. Há amplo consenso científico de que as culturas geneticamente modificadas atualmente no mercado são seguras para consumo. Após 14 anos de cultivo e um total acumulado de 2 bilhões de acres plantados, nenhum efeito adverso à saúde ou ao meio ambiente resultou da comercialização de culturas geneticamente modificadas (Board on Agriculture and Natural Resources, Committee on Environmental Impacts Associated with Commercialization of Transgenic Plants, National Research Council and Division on Earth and Life Studies 2002) Tanto o Conselho Nacional de Pesquisa dos EUA quanto o Centro Conjunto de Pesquisa (laboratório de pesquisa científica e técnica da União Europeia e parte integrante da Comissão Europeia) concluíram que existe um conjunto abrangente de conhecimentos que aborda adequadamente a questão da segurança alimentar das culturas geneticamente modificadas (Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human Health and National Research Council 2004; European Commission Joint Research Centre 2008). Esses e outros relatórios recentes concluem que os processos de engenharia genética e melhoramento convencional não são diferentes em termos de consequências não intencionais para a saúde humana e o meio ambiente (European Commission Directorate-General for Research and Innovation 2010).
- ↑ a b c d e Freedman, David H. (setembro de 2013). «Are engineered foods evil?». Scientific American (em inglês) (3): 80–85. ISSN 0036-8733. PMID 24003560. doi:10.1038/scientificamerican0913-80. Consultado em 21 de agosto de 2025
- ↑ a b Mas também veja:
Domingo, José L.; Giné Bordonaba, Jordi (1 de maio de 2011). «A literature review on the safety assessment of genetically modified plants». Environment International (4): 734–742. ISSN 0160-4120. doi:10.1016/j.envint.2011.01.003. Consultado em 21 de agosto de 2025 "Apesar disso, o número de estudos especificamente focados na avaliação de segurança de plantas GM ainda é limitado. No entanto, é importante observar que, pela primeira vez, foi observado um certo equilíbrio no número de grupos de pesquisa que sugerem, com base em seus estudos, que diversas variedades de produtos GM (principalmente milho e soja) são tão seguras e nutritivas quanto as respectivas plantas convencionais não-GM, e aqueles que ainda levantam sérias preocupações. Além disso, vale mencionar que a maioria dos estudos que demonstram que os alimentos GM são tão nutritivos e seguros quanto aqueles obtidos por melhoramento convencional foram realizados por empresas de biotecnologia ou associadas, que também são responsáveis pela comercialização dessas plantas GM. De qualquer forma, isso representa um avanço notável em comparação com a falta de estudos publicados nos últimos anos em periódicos científicos por essas empresas."
Krimsky, Sheldon (1 de novembro de 2015). «An Illusory Consensus behind GMO Health Assessment». Science, Technology, & Human Values (em inglês) (6): 883–914. ISSN 0162-2439. doi:10.1177/0162243915598381. Consultado em 22 de agosto de 2025 "Comecei este artigo com depoimentos de cientistas respeitados de que não há literalmente nenhuma controvérsia científica sobre os efeitos dos OGMs na saúde. Minha investigação na literatura científica conta outra história."
Hilbeck, Angelika; Binimelis, Rosa; Defarge, Nicolas; Steinbrecher, Ricarda; Székács, András; Wickson, Fern; Antoniou, Michael; Bereano, Philip L; Clark, Ethel Ann (dezembro de 2015). «No scientific consensus on GMO safety». Environmental Sciences Europe (em inglês) (1). ISSN 2190-4707. doi:10.1186/s12302-014-0034-1. Consultado em 22 de agosto de 2025 "Na declaração conjunta a seguir, o consenso alegado é demonstrado como uma construção artificial que tem sido falsamente perpetuada por diversos fóruns. Independentemente das evidências contraditórias na literatura arbitrada, conforme documentado abaixo, a alegação de que agora existe um consenso sobre a segurança dos OGM continua a ser amplamente e frequentemente divulgada de forma acrítica."
E contraste:
Panchin, Alexander Y.; Tuzhikov, Alexander I. (17 de fevereiro de 2017). «Published GMO studies find no evidence of harm when corrected for multiple comparisons». Critical Reviews in Biotechnology (2): 213–217. ISSN 0738-8551. PMID 26767435. doi:10.3109/07388551.2015.1130684. Consultado em 22 de agosto de 2025 "Aqui, demonstramos que diversos artigos, alguns dos quais influenciaram forte e negativamente a opinião pública sobre os cultivos transgênicos e até mesmo provocaram ações políticas, como o embargo aos transgênicos, compartilham falhas comuns na avaliação estatística dos dados. Considerando essas falhas, concluímos que os dados apresentados nesses artigos não fornecem nenhuma evidência substancial de danos causados pelos transgênicos.Os artigos apresentados, sugerindo possíveis danos causados pelos transgênicos, receberam grande atenção pública. No entanto, apesar de suas alegações, eles, na verdade, enfraquecem as evidências dos danos e a falta de equivalência substancial dos transgênicos estudados. Ressaltamos que, com mais de 1.783 artigos publicados sobre transgênicos nos últimos 10 anos, espera-se que alguns deles tenham relatado diferenças indesejadas entre transgênicos e cultivos convencionais, mesmo que tais diferenças não existam na realidade."
Yang, Y. Tony; Chen, Brian (abril de 2016). «Governing GMOs in the USA: science, law and public health». Journal of the Science of Food and Agriculture (em inglês) (6): 1851–1855. ISSN 0022-5142. doi:10.1002/jsfa.7523. Consultado em 22 de agosto de 2025 "Portanto, não é surpreendente que os esforços para exigir rotulagem e proibir OGMs tenham sido uma questão política crescente nos EUA (citando Domingo e Bordonaba, 2011). De modo geral, um amplo consenso científico sustenta que os alimentos transgênicos atualmente comercializados não apresentam riscos maiores do que os alimentos convencionais... As principais associações científicas e médicas nacionais e internacionais declararam que nenhum efeito adverso à saúde humana relacionado a alimentos transgênicos foi relatado ou comprovado na literatura revisada por pares até o momento.Apesar de várias preocupações, hoje, a Associação Americana para o Avanço da Ciência, a Organização Mundial da Saúde e muitas organizações científicas internacionais independentes concordam que os OGMs são tão seguros quanto outros alimentos. Comparada às técnicas convencionais de melhoramento genético, a engenharia genética é muito mais precisa e, na maioria dos casos, menos propensa a gerar um resultado inesperado." - ↑ a b «Statement by the AAAS Board of Directors On Labeling of Genetically Modified Foods» (PDF). American Association for the Advancement of Science (em inglês). 20 de outubro de 2012.
A UE, por exemplo, investiu mais de € 300 milhões em pesquisas sobre a biossegurança de OGM. Seu relatório recente afirma: "A principal conclusão a ser tirada dos esforços de mais de 130 projetos de pesquisa, abrangendo um período de mais de 25 anos de pesquisa e envolvendo mais de 500 grupos de pesquisa independentes, é que a biotecnologia, e em particular os OGM, não são, por si só, mais arriscados do que, por exemplo, as tecnologias convencionais de melhoramento genético de plantas." A Organização Mundial da Saúde, a Associação Médica Americana, a Academia Nacional de Ciências dos EUA, a Sociedade Real Britânica e todas as outras organizações respeitadas que examinaram as evidências chegaram à mesma conclusão: consumir alimentos que contêm ingredientes derivados de culturas geneticamente modificadas não é mais arriscado do que consumir os mesmos alimentos que contêm ingredientes de plantas cultivadas modificadas por técnicas convencionais de melhoramento genético.
- ↑ a b Pinholster, Ginger (25 de outubro de 2012). «AAAS Board of Directors: Legally Mandating GM Food Labels Could "Mislead and Falsely Alarm Consumers» (PDF). American Association for the Advancement of Science (em inglês)
- ↑ a b European Commission. Directorate-General for Research (2010). A decade of EU-funded GMO research (2001-2010) (em inglês). LU: Publications Office. Consultado em 22 de agosto de 2025
- ↑ a b «ISAAA Summary of AMA Report on Genetically Modified Crops and Foods». The International Service for the Acquisition of Agri-biotech Applications (ISAAA) (em inglês). 2001. Consultado em 22 de agosto de 2025.
Um relatório emitido pelo conselho científico da Associação Médica Americana (AMA) diz que nenhum efeito de longo prazo na saúde foi detectado pelo uso de culturas transgênicas e alimentos geneticamente modificados, e que esses alimentos são substancialmente equivalentes aos seus equivalentes convencionais.
- ↑ a b «Featured CSA Report: Genetically Modified Crops and Foods (I-00) Full Text». American Medical Association (em inglês). Consultado em 22 de agosto de 2025. Cópia arquivada em 10 de junho de 2001.
Culturas e alimentos produzidos com técnicas de DNA recombinante estão disponíveis há menos de 10 anos e nenhum efeito a longo prazo foi detectado até o momento. Esses alimentos são substancialmente equivalentes aos seus equivalentes convencionais.
- ↑ a b «Report 2 of the Council on Science and Public Health (A-12): Labeling of Bioengineered Foods» (PDF). American Medical Association. 2012. Consultado em 25 de agosto de 2025. Cópia arquivada (PDF) em 7 de setembro de 2012.
Alimentos bioengenheirados são consumidos há quase 20 anos e, durante esse tempo, nenhuma consequência evidente à saúde humana foi relatada e/ou comprovada na literatura revisada por pares.
- ↑ a b c Committee on Genetically Engineered Crops: Past Experience and Future Prospects; Board on Agriculture and Natural Resources; Division on Earth and Life Studies; National Academies of Sciences, Engineering, and Medicine (28 de dezembro de 2016). Genetically Engineered Crops: Experiences and Prospects (em inglês). Washington, D.C.: National Academies Press. p. 149. ISBN 978-0-309-43738-7. PMID 28230933. doi:10.17226/23395. Consultado em 22 de agosto de 2025.
Conclusão geral sobre os supostos efeitos adversos à saúde humana de alimentos derivados de culturas geneticamente modificadas: Com base no exame detalhado de comparações de alimentos geneticamente modificados atualmente comercializados com alimentos não geneticamente modificados em análises composicionais, testes de toxicidade aguda e crônica em animais, dados de longo prazo sobre a saúde de animais alimentados com alimentos geneticamente modificados e dados epidemiológicos humanos, o comitê não encontrou diferenças que impliquem em um risco maior à saúde humana dos alimentos geneticamente modificados do que de seus equivalentes não geneticamente modificados.
- ↑ a b «Food, genetically modified». World Health Organization (em inglês). Consultado em 22 de agosto de 2025.
Diferentes organismos geneticamente modificados incluem diferentes genes inseridos de diferentes maneiras. Isso significa que cada alimento geneticamente modificado e sua segurança devem ser avaliados caso a caso, e que não é possível fazer afirmações gerais sobre a segurança de todos os alimentos geneticamente modificados. Os alimentos geneticamente modificados atualmente disponíveis no mercado internacional foram aprovados em avaliações de segurança e provavelmente não apresentam riscos para a saúde humana. Além disso, não foram demonstrados efeitos sobre a saúde humana em decorrência do consumo desses alimentos pela população em geral nos países onde foram aprovados. A aplicação contínua de avaliações de segurança baseadas nos princípios do Codex Alimentarius e, quando apropriado, o monitoramento pós-comercialização adequado devem constituir a base para garantir a segurança dos alimentos geneticamente modificados.
- ↑ a b Haslberger, Alexander G. (julho de 2003). «Codex guidelines for GM foods include the analysis of unintended effects». Nature Biotechnology (em inglês) (7): 739–741. ISSN 1087-0156. PMID 12833088. doi:10.1038/nbt0703-739. Consultado em 22 de agosto de 2025.
Esses princípios determinam uma avaliação pré-comercialização caso a caso, que inclui uma avaliação dos efeitos diretos e não intencionais.
- ↑ a b c Algumas organizações médicas, incluindo a Associação Médica Britânica, defendem maior cautela com base no princípio da precaução:
«Genetically modified foods and health: a second interim statement» (PDF). British Medical Association (em inglês). Março de 2004. Consultado em 20 de novembro de 2025 "Em nossa visão, o potencial de que alimentos transgênicos causem efeitos nocivos à saúde é muito pequeno, e muitas das preocupações expressas se aplicam com igual força aos alimentos obtidos por meios convencionais. No entanto, preocupações com segurança não podem, até o momento, ser completamente descartadas com base nas informações atualmente disponíveis.
Ao buscar otimizar o equilíbrio entre benefícios e riscos, é prudente adotar uma postura cautelosa e, acima de tudo, aprender com o conhecimento e a experiência acumulados. Qualquer nova tecnologia, como a modificação genética, deve ser examinada quanto a possíveis benefícios e riscos para a saúde humana e o meio ambiente. Como ocorre com todos os alimentos novos, as avaliações de segurança relacionadas a alimentos transgênicos devem ser feitas caso a caso.
Os membros do projeto GM jury foram informados sobre vários aspectos da modificação genética por um grupo diverso de especialistas reconhecidos nos respectivos temas. O júri sobre transgênicos concluiu que a venda dos alimentos transgênicos atualmente disponíveis deve ser interrompida e que o moratório sobre o cultivo comercial de plantas transgênicas deve ser mantido. Essas conclusões basearam-se no princípio da precaução e na ausência de evidências de qualquer benefício. O júri expressou preocupação com o impacto das culturas transgênicas na agricultura, no meio ambiente, na segurança alimentar e em outros potenciais efeitos sobre a saúde.
A revisão da Royal Society (2002) concluiu que os riscos à saúde humana associados ao uso de sequências específicas de DNA viral em plantas transgênicas são insignificantes e, embora tenha recomendado cautela na introdução de potenciais alérgenos em culturas alimentares, destacou a ausência de evidências de que alimentos transgênicos comercialmente disponíveis causem manifestações clínicas de alergia. A BMA compartilha a visão de que não há evidências robustas de que alimentos transgênicos sejam inseguros, mas apoia o apelo por mais pesquisas e monitoramento para fornecer evidências convincentes de segurança e benefício." - ↑ a b Funk, Cary; Rainie, Lee (29 de janeiro de 2015). «Public and Scientists' Views on Science and Society». Pew Research Center (em inglês). Consultado em 23 de agosto de 2025. Cópia arquivada em 9 de janeiro de 2019.
As maiores diferenças entre o público e os cientistas da AAAS estão nas crenças sobre a segurança do consumo de alimentos geneticamente modificados (GM). Quase nove em cada dez cientistas (88%) afirmam que é geralmente seguro consumir alimentos geneticamente modificados, em comparação com 37% do público em geral, uma diferença de 51 pontos percentuais.
- ↑ a b Marris, Claire (julho de 2001). «Public views on GMOs: deconstructing the myths: Stakeholders in the GMO debate often describe public opinion as irrational. But do they really understand the public?». EMBO reports (em inglês) (7): 545–548. ISSN 1469-221X. doi:10.1093/embo-reports/kve142. Consultado em 23 de agosto de 2025
- ↑ a b «Public Perceptions of Agricultural Biotechnologies in Europe». Commission of European Communities (em inglês). Dezembro de 2001. Consultado em 22 de agosto de 2025. Cópia arquivada em 17 de maio de 2025
- ↑ a b Scott, Sydney E.; Inbar, Yoel; Rozin, Paul (maio de 2016). «Evidence for Absolute Moral Opposition to Genetically Modified Food in the United States». Perspectives on Psychological Science (em inglês) (3): 315–324. ISSN 1745-6916. doi:10.1177/1745691615621275. Consultado em 23 de agosto de 2025
- ↑ a b c Bashshur, Ramona (fevereiro de 2013). «FDA and Regulation of GMOs». American Bar Association (em inglês). Consultado em 23 de agosto de 2025. Cópia arquivada em 21 de junho de 2018
- ↑ a b c Sifferlin, Alexandra (3 de agosto de 2015). «Over Half of E.U. Countries Are Opting Out of GMOs». Time (em inglês). Consultado em 23 de agosto de 2025
- ↑ a b c d e Diahanna, Lynch; David, Vogel (5 de abril de 2001). «The Regulation of GMOs in Europe and the United States: A Case-Study of Contemporary European Regulatory Politics». Council on Foreign Relations. Consultado em 23 de agosto de 2025. Cópia arquivada em 29 de setembro de 2016
- ↑ a b c Committee on Genetically Engineered Crops: Past Experience and Future Prospects; Board on Agriculture and Natural Resources; Division on Earth and Life Studies; National Academies of Sciences, Engineering, and Medicine (28 de dezembro de 2016). Genetically Engineered Crops: Experiences and Prospects. Regulation of Current and Future Genetically Engineered Crops (em inglês). Washington, D.C.: National Academies Press. ISBN 978-0-309-43738-7. PMID 28230933. doi:10.17226/23395. Consultado em 23 de agosto de 2025
- ↑ a b c d e f g «Lei nº 11.105». Planalto Brasileiro. Consultado em 23 de agosto de 2025
- ↑ a b c d e f Skogstad, Grace (julho de 2011). «Contested Accountability Claims and GMO Regulation in the European Union». JCMS: Journal of Common Market Studies (em inglês) (4): 895–915. doi:10.1111/j.1468-5965.2010.02166.x. Consultado em 23 de agosto de 2025
- ↑ a b c d e Thayyil, Naveen (2014). Biotechnology regulation and GMOs: law, technology and public contestations in Europe. Col: Biotechnology regulation. Cheltenham, UK ; Northampton, MA, USA: Edward Elgar
- ↑ a b c d e f g h Weimer, Maria (setembro de 2015). «Risk Regulation and Deliberation in EU Administrative Governance— GMO Regulation and Its Reform». European Law Journal (em inglês) (5): 622–640. ISSN 1351-5993. doi:10.1111/eulj.12140. Consultado em 23 de agosto de 2025
- ↑ a b c d e f g Wickson, Fern (dezembro de 2014). «Environmental protection goals, policy & publics in the European regulation of GMOs». Ecological Economics (em inglês): 269–273. doi:10.1016/j.ecolecon.2014.09.025. Consultado em 23 de agosto de 2025
- ↑ a b c d e f «Food, genetically modified». World Health Organization (em inglês)
- ↑ «Genetically engineered foods». University of Maryland Medical Center (em inglês). Consultado em 26 de agosto de 2025. Cópia arquivada em 14 de fevereiro de 2016
- ↑ Lei nº 11.105, de 24 de março de 2005. Regulamenta os incisos II, IV e V do § 1o do art. 225 da Constituição Federal, estabelece normas de segurança e mecanismos de fiscalização de atividades que envolvam organismos geneticamente modificados – OGM e seus derivados, cria o Conselho Nacional de Biossegurança – CNBS, reestrutura a Comissão Técnica Nacional de Biossegurança – CTNBio, dispõe sobre a Política Nacional de Biossegurança – PNB, revoga a Lei no 8.974, de 5 de janeiro de 1995, e a Medida Provisória no 2.191-9, de 23 de agosto de 2001, e os artigos. 5º, 6º, 7º, 8º, 9º, 10 e 16 da Lei n° 10.814, de 15 de dezembro de 2003, e dá outras providências.
- ↑ a b «Organisms obtained by mutagenesis are GMOs and are, in principle, subject to the obligations laid down by the GMO Directive» (PDF). curia.europa.eu. Consultado em 26 de agosto de 2025
- ↑ Knutson, Jonathan (28 de maio de 2018). «A sad day for our society when salt is labeled non-GMO». Agweek (em inglês). Consultado em 26 de agosto de 2025
- ↑ «Non GMO salt? Water? Food companies exploit GMO free labels, misleading customers, promoting misinformation». Genetic Literacy Project (em inglês). 24 de agosto de 2015. Consultado em 26 de agosto de 2025
- ↑ a b c «Qual a diferença entre OGMs, Transgênicos e Cisgênicos?». CropLife. Consultado em 26 de agosto de 2025
- ↑ «Alimentos transgênicos». Secretaria de Meio Ambiente, Infraestrutura e Logística. São Paulo (Estado). Consultado em 29 de outubro de 2025
- ↑ Schouten, Henk J; Krens, Frans A; Jacobsen, Evert (agosto de 2006). «Cisgenic plants are similar to traditionally bred plants: International regulations for genetically modified organisms should be altered to exempt cisgenesis». EMBO reports (em inglês) (8): 750–753. ISSN 1469-221X. PMC 1525145
 . PMID 16880817. doi:10.1038/sj.embor.7400769. Consultado em 9 de outubro de 2025
. PMID 16880817. doi:10.1038/sj.embor.7400769. Consultado em 9 de outubro de 2025
- ↑ «How the humble potato could feed the world». New Scientist (em inglês). Consultado em 9 de outubro de 2025
- ↑ «Beijing Researchers Use Gene Editing to Create Disease-Resistant Wheat | MIT Technology Review». MIT Technology Review (em inglês). 21 de julho de 2014. Consultado em 9 de outubro de 2025
- ↑ Wang, Yanpeng; Cheng, Xi; Shan, Qiwei; Zhang, Yi; Liu, Jinxing; Gao, Caixia; Qiu, Jin-Long (setembro de 2014). «Simultaneous editing of three homoeoalleles in hexaploid bread wheat confers heritable resistance to powdery mildew». Nature Biotechnology (em inglês) (9): 947–951. ISSN 1087-0156. doi:10.1038/nbt.2969. Consultado em 9 de outubro de 2025
- ↑ Waltz, Emily (21 de abril de 2016). «Gene-edited CRISPR mushroom escapes US regulation». Nature (em inglês) (7599): 293–293. ISSN 0028-0836. doi:10.1038/nature.2016.19754. Consultado em 9 de outubro de 2025
- ↑ Brodwin, Erin. «The next generation of GMO food is here, and it's technically not a GMO». Business Insider (em inglês). Consultado em 9 de outubro de 2025
- ↑ Diamond, Jared (agosto de 2002). «Evolution, consequences and future of plant and animal domestication». Nature (em inglês) (6898): 700–707. ISSN 1476-4687. doi:10.1038/nature01019. Consultado em 23 de agosto de 2025
- ↑ Meyer, Rachel S.; Purugganan, Michael D. (dezembro de 2013). «Evolution of crop species: genetics of domestication and diversification». Nature Reviews Genetics (em inglês) (12): 840–852. ISSN 1471-0064. doi:10.1038/nrg3605. Consultado em 23 de agosto de 2025
- ↑ a b Zohary, Daniel; Hopf, Maria; Weiss, Ehud (março de 2012). Domestication of Plants in the Old World: The Origin and Spread of Domesticated Plants in Southwest Asia, Europe, and the Mediterranean Basin (em inglês). [S.l.]: OUP Oxford. Consultado em 23 de agosto de 2025
- ↑ Roots, Clive (30 de julho de 2007). Domestication (em inglês). [S.l.]: Bloomsbury Publishing. Consultado em 24 de agosto de 2025
- ↑ Lederberg, Joshua; Tatum, E. L. (outubro de 1946). «Gene Recombination in Escherichia Coli». Nature (em inglês) (4016): 558–558. ISSN 1476-4687. doi:10.1038/158558a0. Consultado em 24 de agosto de 2025
- ↑ «Chymosin». www.ncbe.reading.ac.uk. Consultado em 24 de agosto de 2025. Cópia arquivada em 22 de maio de 2016
- ↑ Campbell-Platt, Geoffrey (26 de agosto de 2011). Food Science and Technology (em inglês). [S.l.]: John Wiley & Sons. Consultado em 24 de agosto de 2025
- ↑ Martineau, Belinda (2001). First fruit: the creation of the Flavr Savr tomato and the birth of genetically engineered food. New York: McGraw-Hill. ISBN 0071360565
- ↑ «Genetically Altered Potato Ok'd For Crops». Lawrence Journal-World. 6 de maio de 1995. Consultado em 24 de agosto de 2025
- ↑ «Lei nº 8.974». Planalto Brasileiro. 5 de janeiro de 1995. Consultado em 23 de agosto de 2025
- ↑ a b «Cronologia dos Transgênicos». www1.folha.uol.com.br. Consultado em 21 de agosto de 2025
- ↑ a b c «Cronologia do embargo judicial» (PDF). Embrapa. 2003
- ↑ a b Kettenburg, Annika J.; Hanspach, Jan; Abson, David J.; Fischer, Joern (1 de setembro de 2018). «From disagreements to dialogue: unpacking the Golden Rice debate». Sustainability Science (em inglês) (5): 1469–1482. ISSN 1862-4057. PMC 6132390
 . PMID 30220919. doi:10.1007/s11625-018-0577-y. Consultado em 19 de julho de 2022
. PMID 30220919. doi:10.1007/s11625-018-0577-y. Consultado em 19 de julho de 2022
- ↑ a b Mallikarjuna Swamy, B. P.; Marundan, Severino; Samia, Mercy; Ordonio, Reynante L.; Rebong, Democrito B.; Miranda, Ronalyn; Alibuyog, Anielyn; Rebong, Anna Theresa; Tabil, Ma. Angela (28 de janeiro de 2021). «Development and characterization of GR2E Golden rice introgression lines». Scientific Reports (em inglês) (1). ISSN 2045-2322. PMC 7843986
 . PMID 33510272. doi:10.1038/s41598-021-82001-0. Consultado em 24 de agosto de 2025
. PMID 33510272. doi:10.1038/s41598-021-82001-0. Consultado em 24 de agosto de 2025
- ↑ a b Tang, Guangwen; Qin, Jian; Dolnikowski, Gregory G; Russell, Robert M; Grusak, Michael A (junho de 2009). «Golden Rice is an effective source of vitamin A». The American Journal of Clinical Nutrition (em inglês) (6): 1776–1783. doi:10.3945/ajcn.2008.27119. Consultado em 24 de agosto de 2025
- ↑ a b Wu, Felicia; Wesseler, Justus; Zilberman, David; Russell, Robert M.; Chen, Chen; Dubock, Adrian C. (21 de dezembro de 2021). «Allow Golden Rice to save lives». Proceedings of the National Academy of Sciences (em inglês) (51). ISSN 0027-8424. PMC 8713968
 . PMID 34911769. doi:10.1073/pnas.2120901118. Consultado em 24 de agosto de 2025
. PMID 34911769. doi:10.1073/pnas.2120901118. Consultado em 24 de agosto de 2025
- ↑ a b Bosetti, Cleber José (13 de dezembro de 2012). «Ciência e política nas decisões da CTNBio». Plural - Revista de Ciências Sociais. 19 (2): 29–50. ISSN 2176-8099. doi:10.11606/issn.2176-8099.pcso.2012.74434
- ↑ a b James, Clive (2011). «Global tatus of Commercialized iotech/GM Crops: 2011» (PDF). ISAAA Briefs (em inglês). Consultado em 25 de agosto de 2025
- ↑ «Adoption of Genetically Engineered Crops in the United States». Economic Research Service, USDA. Consultado em 25 de agosto de 2025
- ↑ a b c James, Clive (2014). «Global Status of Commercialized Biotech/GM Crops: 2014» (PDF). ISAAA Brief. Consultado em 5 de setembro de 2025
- ↑ a b Yaskowiak, Edward S.; Shears, Margaret A.; Agarwal-Mawal, Alka; Fletcher, Garth L. (agosto de 2006). «Characterization and multi-generational stability of the growth hormone transgene (EO-1α) responsible for enhanced growth rates in Atlantic Salmon». Transgenic Research (em inglês) (4): 465–480. ISSN 0962-8819. doi:10.1007/s11248-006-0020-5. Consultado em 25 de agosto de 2025
- ↑ a b «Canada Approves Sale of Genetically Modified Salmon». Democracy Now! (em inglês). Consultado em 21 de agosto de 2025
- ↑ a b Outram, Robert (3 de junho de 2021). «AquaBounty's GM salmon approved for Brazil». Fish Farmer (em inglês). Consultado em 21 de agosto de 2025
- ↑ a b Waltz, Emily (21 de abril de 2016). «Gene-edited CRISPR mushroom escapes US regulation». Nature (em inglês) (7599): 293–293. ISSN 0028-0836. doi:10.1038/nature.2016.19754. Consultado em 25 de agosto de 2025
- ↑ Culpepper, A. Stanley; Grey, Timothy L.; Vencill, William K.; Kichler, Jeremy M.; Webster, Theodore M.; Brown, Steve M.; York, Alan C.; Davis, Jerry W.; Hanna, Wayne W. (agosto de 2006). «Glyphosate-resistant Palmer amaranth ( Amaranthus palmeri ) confirmed in Georgia». Weed Science (em inglês) (4): 620–626. ISSN 0043-1745. doi:10.1614/WS-06-001R.1. Consultado em 25 de agosto de 2025
- ↑ Lopez Ovejero, R. F.; Fonseca, L. B.; Galli, A. J. B.; Christoffoleti, Pedro Jacob (2009). «Resistência de plantas daninhas ao herbicida glifosato no Brasil: situação atual e mitigação». Herbologia e Biodiversidade numa agricultura sustentável. Consultado em 25 de agosto de 2025
- ↑ «Brasil registra pela primeira vez picão-preto resistente ao glifosato». IHARA. 18 de outubro de 2023. Consultado em 25 de agosto de 2025
- ↑ «Tomato In Japan Is First CRISPR-Edited Food In The World To Go On Sale». IFLScience (em inglês). 30 de setembro de 2021. Consultado em 25 de agosto de 2025
- ↑ Boonstra, Evert; de Kleijn, Roy; Colzato, Lorenza S.; Alkemade, Anneke; Forstmann, Birte U.; Nieuwenhuis, Sander (6 de outubro de 2015). «Neurotransmitters as food supplements: the effects of GABA on brain and behavior». Frontiers in Psychology. ISSN 1664-1078. PMC 4594160
 . PMID 26500584. doi:10.3389/fpsyg.2015.01520. Consultado em 25 de agosto de 2025
. PMID 26500584. doi:10.3389/fpsyg.2015.01520. Consultado em 25 de agosto de 2025
- ↑ Wang, Tian; Zhang, Hongyan; Zhu, Hongliang (dezembro de 2019). «CRISPR technology is revolutionizing the improvement of tomato and other fruit crops». Horticulture Research (em inglês) (1). ISSN 2052-7276. PMC 6570646
 . PMID 31240102. doi:10.1038/s41438-019-0159-x. Consultado em 25 de agosto de 2025
. PMID 31240102. doi:10.1038/s41438-019-0159-x. Consultado em 25 de agosto de 2025
- ↑ «Japan embraces CRISPR-edited fish». Nature Biotechnology (em inglês) (1): 10–10. Janeiro de 2022. ISSN 1087-0156. doi:10.1038/s41587-021-01197-8. Consultado em 25 de agosto de 2025
- ↑ «Startup hopes genome-edited pufferfish will be a hit in 2022». The Japan Times (em inglês). 5 de janeiro de 2022. Consultado em 25 de agosto de 2025. Cópia arquivada em 17 de janeiro de 2022
- ↑ «Gene-edited sea bream set for sale in Japan». The Fish Site (em inglês). 22 de setembro de 2021. Consultado em 25 de agosto de 2025
- ↑ Nicholl, Desmond S. T. (29 de maio de 2008). An Introduction to Genetic Engineering. [S.l.]: Cambridge University Press. Consultado em 26 de agosto de 2025
- ↑ Liang, Jing; Luo, Yunzi; Zhao, Huimin (janeiro de 2011). «Synthetic biology: putting synthesis into biology». WIREs Systems Biology and Medicine (em inglês) (1): 7–20. ISSN 1939-5094. doi:10.1002/wsbm.104. Consultado em 26 de agosto de 2025
- ↑ Berg, Paul; Mertz, Janet E (1 de janeiro de 2010). «Personal Reflections on the Origins and Emergence of Recombinant DNA Technology». Genetics (em inglês) (1): 9–17. ISSN 1943-2631. doi:10.1534/genetics.109.112144. Consultado em 26 de agosto de 2025
- ↑ Chen, Inês; Dubnau, David (1 de março de 2004). «DNA uptake during bacterial transformation». Nature Reviews Microbiology (em inglês) (3): 241–249. ISSN 1740-1526. doi:10.1038/nrmicro844. Consultado em 26 de agosto de 2025
- ↑ a b Health, National Research Council (US) Committee on Identifying and Assessing Unintended Effects of Genetically Engineered Foods on Human (2004). «Methods and Mechanisms for Genetic Manipulation of Plants, Animals, and Microorganisms». National Academies Press (US) (em inglês). Consultado em 26 de agosto de 2025
- ↑ a b Gelvin, Stanton B. (março de 2003). «Agrobacterium -Mediated Plant Transformation: the Biology behind the "Gene-Jockeying" Tool». Microbiology and Molecular Biology Reviews (em inglês) (1): 16–37. ISSN 1092-2172. doi:10.1128/MMBR.67.1.16-37.2003. Consultado em 26 de agosto de 2025
- ↑ Tzotzos, George T.; Head, Graham; Hull, Roger (2009). Genetically modified plants: assessing safety and managing risk 1st ed. Amsterdam Boston: Academic Press/Elsevier
- ↑ a b Neumann, E.; Schaefer-Ridder, M.; Wang, Y.; Hofschneider, P. H. (1982). «Gene transfer into mouse lyoma cells by electroporation in high electric fields». The EMBO journal (7): 841–845. ISSN 0261-4189. PMC 553119
 . PMID 6329708. doi:10.1002/j.1460-2075.1982.tb01257.x. Consultado em 26 de agosto de 2025
. PMID 6329708. doi:10.1002/j.1460-2075.1982.tb01257.x. Consultado em 26 de agosto de 2025
- ↑ SANFORD, JOHN C.; KLEIN, THEODORE M.; WOLF, EDWARD D.; ALLEN, NELSON (1 de janeiro de 1987). «Delivery of Substances into Cells and Tissues Using a Particle Bombardment Process». Particulate Science and Technology (1): 27–37. ISSN 0272-6351. doi:10.1080/02726358708904533. Consultado em 26 de agosto de 2025
- ↑ Schell, J.; Van Montagu, M. (1977). «The Ti-plasmid of Agrobacterium tumefaciens, a natural vector for the introduction of nif genes in plants?». Basic Life Sciences: 159–179. ISSN 0090-5542. PMID 336023. doi:10.1007/978-1-4684-0880-5_12. Consultado em 26 de agosto de 2025
- ↑ Tuomela, M; Stanescu, I; Krohn, K (1 de outubro de 2005). «Validation overview of bio-analytical methods». Gene Therapy (em inglês) (S1): S131–S138. ISSN 0969-7128. doi:10.1038/sj.gt.3302627. Consultado em 26 de agosto de 2025
- ↑ Constabel, Friedrich; Shyluk, Jerry P. (1994). «Initiation, Nutrition, and Maintenance of Plant Cell and Tissue Cultures». Dordrecht: Springer Netherlands: 3–15. ISBN 978-90-481-4327-6. Consultado em 26 de agosto de 2025
- ↑ Setlow, Jane K., ed. (2002). «Genetic Engineering: Principles and Methods». Genetic Engineering. doi:10.1007/b113582. Consultado em 26 de agosto de 2025
- ↑ Grizot, Sylvestre; Smith, Julianne; Daboussi, Fayza; Prieto, Jesús; Redondo, Pilar; Merino, Nekane; Villate, Maider; Thomas, Séverine; Lemaire, Laetitia (setembro de 2009). «Efficient targeting of a SCID gene by an engineered single-chain homing endonuclease». Nucleic Acids Research (em inglês) (16): 5405–5419. ISSN 1362-4962. doi:10.1093/nar/gkp548. Consultado em 26 de agosto de 2025
- ↑ Gao, Huirong; Smith, Jeff; Yang, Meizhu; Jones, Spencer; Djukanovic, Vesna; Nicholson, Michael G.; West, Ande; Bidney, Dennis; Falco, S. Carl (janeiro de 2010). «Heritable targeted mutagenesis in maize using a designed endonuclease». The Plant Journal (em inglês) (1): 176–187. doi:10.1111/j.1365-313X.2009.04041.x. Consultado em 26 de agosto de 2025
- ↑ Townsend, Jeffrey A.; Wright, David A.; Winfrey, Ronnie J.; Fu, Fengli; Maeder, Morgan L.; Joung, J. Keith; Voytas, Daniel F. (maio de 2009). «High-frequency modification of plant genes using engineered zinc-finger nucleases». Nature (em inglês) (7245): 442–445. ISSN 0028-0836. PMC 2743854
 . PMID 19404258. doi:10.1038/nature07845. Consultado em 26 de agosto de 2025
. PMID 19404258. doi:10.1038/nature07845. Consultado em 26 de agosto de 2025
- ↑ Shukla, Vipula K.; Doyon, Yannick; Miller, Jeffrey C.; DeKelver, Russell C.; Moehle, Erica A.; Worden, Sarah E.; Mitchell, Jon C.; Arnold, Nicole L.; Gopalan, Sunita (maio de 2009). «Precise genome modification in the crop species Zea mays using zinc-finger nucleases». Nature (em inglês) (7245): 437–441. ISSN 0028-0836. doi:10.1038/nature07992. Consultado em 26 de agosto de 2025
- ↑ Christian, Michelle; Cermak, Tomas; Doyle, Erin L; Schmidt, Clarice; Zhang, Feng; Hummel, Aaron; Bogdanove, Adam J; Voytas, Daniel F (1 de outubro de 2010). «Targeting DNA Double-Strand Breaks with TAL Effector Nucleases». Genetics (em inglês) (2): 757–761. ISSN 1943-2631. PMC 2942870
 . PMID 20660643. doi:10.1534/genetics.110.120717. Consultado em 26 de agosto de 2025
. PMID 20660643. doi:10.1534/genetics.110.120717. Consultado em 26 de agosto de 2025
- ↑ Li, Ting; Huang, Sheng; Jiang, Wen Zhi; Wright, David; Spalding, Martin H.; Weeks, Donald P.; Yang, Bing (janeiro de 2011). «TAL nucleases (TALNs): hybrid proteins composed of TAL effectors and FokI DNA-cleavage domain». Nucleic Acids Research (em inglês) (1): 359–372. ISSN 1362-4962. PMC 3017587
 . PMID 20699274. doi:10.1093/nar/gkq704. Consultado em 26 de agosto de 2025
. PMID 20699274. doi:10.1093/nar/gkq704. Consultado em 26 de agosto de 2025
- ↑ Esvelt, Kevin M; Wang, Harris H (janeiro de 2013). «Genome‐scale engineering for systems and synthetic biology». Molecular Systems Biology (em inglês) (1). ISSN 1744-4292. PMC 3564264
 . PMID 23340847. doi:10.1038/msb.2012.66. Consultado em 26 de agosto de 2025
. PMID 23340847. doi:10.1038/msb.2012.66. Consultado em 26 de agosto de 2025
- ↑ Tan, Wenfang (Spring); Carlson, Daniel F.; Walton, Mark W.; Fahrenkrug, Scott C.; Hackett, Perry B. (2012). «Precision Editing of Large Animal Genomes». Elsevier (em inglês): 37–97. ISBN 978-0-12-404742-6. doi:10.1016/b978-0-12-404742-6.00002-8. Consultado em 26 de agosto de 2025
- ↑ a b Malzahn, Aimee; Lowder, Levi; Qi, Yiping (dezembro de 2017). «Plant genome editing with TALEN and CRISPR». Cell & Bioscience (em inglês) (1). ISSN 2045-3701. PMC 5404292
 . PMID 28451378. doi:10.1186/s13578-017-0148-4. Consultado em 26 de agosto de 2025
. PMID 28451378. doi:10.1186/s13578-017-0148-4. Consultado em 26 de agosto de 2025
- ↑ a b c Qaim, Matin (2016). Genetically Modified Crops and Agricultural Development. Col: Palgrave Studies in Agricultural Economics and Food Policy. New York: Palgrave Macmillan. ISBN 9781137405722
- ↑ Darmency, Henri (agosto de 2013). «Pleiotropic effects of herbicide-resistance genes on crop yield: a review: Yield of herbicide-resistant varieties». Pest Management Science (em inglês) (8): 897–904. doi:10.1002/ps.3522. Consultado em 5 de setembro de 2025
- ↑ Fleischer, Shelby J.; Hutchison, William D.; Naranjo, Steven E. (2014). Ricroch, Agnès; Chopra, Surinder; Fleischer, Shelby J., eds. «Sustainable Management of Insect-Resistant Crops». Cham: Springer International Publishing (em inglês): 115–127. ISBN 978-3-319-06891-6. doi:10.1007/978-3-319-06892-3_10. Consultado em 5 de setembro de 2025
- ↑ «SGK321». GM Approval Database. ISAAA.org. Consultado em 5 de setembro de 2025
- ↑ Qiu, Jane (outubro de 2008). «Agriculture: Is China ready for GM rice?». Nature (em inglês) (7215): 850–852. ISSN 0028-0836. doi:10.1038/455850a. Consultado em 5 de setembro de 2025
- ↑ a b James, Clive (2013). «Global tatus of commercialized biotech/GM crops: 2013» (PDF). ISAAA Brief. Consultado em 5 de setembro de 2025
- ↑ Areal, F. J.; Riesgo, L.; RodríGuez-Cerezo, E. (fevereiro de 2013). «Economic and agronomic impact of commercialized GM crops: a meta-analysis». The Journal of Agricultural Science (em inglês) (1): 7–33. ISSN 0021-8596. doi:10.1017/S0021859612000111. Consultado em 5 de setembro de 2025
- ↑ Finger, Robert; El Benni, Nadja; Kaphengst, Timo; Evans, Clive; Herbert, Sophie; Lehmann, Bernard; Morse, Stephen; Stupak, Nataliya (10 de maio de 2011). «A Meta Analysis on Farm-Level Costs and Benefits of GM Crops». Sustainability (em inglês) (5): 743–762. ISSN 2071-1050. doi:10.3390/su3050743. Consultado em 5 de setembro de 2025
- ↑ Klümper, Wilhelm; Qaim, Matin (3 de novembro de 2014). albertini, emidio, ed. «A Meta-Analysis of the Impacts of Genetically Modified Crops». PLoS ONE (em inglês) (11): e111629. ISSN 1932-6203. PMC 4218791
 . PMID 25365303. doi:10.1371/journal.pone.0111629. Consultado em 5 de setembro de 2025
. PMID 25365303. doi:10.1371/journal.pone.0111629. Consultado em 5 de setembro de 2025
- ↑ Kyndt, Tina; Quispe, Dora; Zhai, Hong; Jarret, Robert; Ghislain, Marc; Liu, Qingchang; Gheysen, Godelieve; Kreuze, Jan F. (5 de maio de 2015). «The genome of cultivated sweet potato contains Agrobacterium T-DNAs with expressed genes: An example of a naturally transgenic food crop». Proceedings of the National Academy of Sciences (em inglês) (18): 5844–5849. ISSN 0027-8424. PMC 4426443
 . PMID 25902487. doi:10.1073/pnas.1419685112. Consultado em 5 de setembro de 2025
. PMID 25902487. doi:10.1073/pnas.1419685112. Consultado em 5 de setembro de 2025
- ↑ Doucleff, Michaeleen (5 de maio de 2015). «Natural GMO? Sweet Potato Genetically Modified 8,000 Years Ago». NPR (em inglês). Consultado em 5 de setembro de 2025
- ↑ Lebot, Vincent (2020). Tropical root and tuber crops: cassava, sweet potato, yams and aroids. Col: Crop production science in horticulture 2nd ed. Wallingford: CABl
- ↑ Soucy, Shannon M.; Huang, Jinling; Gogarten, Johann Peter (agosto de 2015). «Horizontal gene transfer: building the web of life». Nature Reviews Genetics (em inglês) (8): 472–482. ISSN 1471-0056. doi:10.1038/nrg3962. Consultado em 5 de setembro de 2025
- ↑ Andersen, Martin Marchman; Landes, Xavier; Xiang, Wen; Anyshchenko, Artem; Falhof, Janus; Østerberg, Jeppe Thulin; Olsen, Lene Irene; Edenbrandt, Anna Kristina; Vedel, Suzanne Elizabeth (julho de 2015). «Feasibility of new breeding techniques for organic farming». Trends in Plant Science (em inglês) (7): 426–434. doi:10.1016/j.tplants.2015.04.011. Consultado em 5 de setembro de 2025
- ↑ Gonsalves, Dennis (28 de outubro de 2004). «Transgenic Papaya in Hawaii and Beyond». www.agbioforum.org. Consultado em 5 de setembro de 2025. Cópia arquivada em 6 de julho de 2010
- ↑ Gonsalves, Dennis (28 de outubro de 2004). «Transgenic Papaya in Hawaii and Beyond». www.agbioforum.org. Consultado em 5 de setembro de 2025. Cópia arquivada em 6 de julho de 2010
- ↑ «Hawaii Papaya Industry Association in Hawaii - Rainbow Papaya Story». www.hawaiipapaya.com. Consultado em 5 de setembro de 2025. Cópia arquivada em 7 de janeiro de 2015
- ↑ a b Ronald, Pamela; McWilliams, James (14 de maio de 2010). «Genetically Engineered Distortions». The New York Times. Consultado em 5 de setembro de 2025
- ↑ Li, Yunhe; Peng, Yufa; Hallerman, Eric M.; Wu, Kongming (abril de 2014). «Biosafety management and commercial use of genetically modified crops in China». Plant Cell Reports (em inglês) (4): 565–573. ISSN 0721-7714. doi:10.1007/s00299-014-1567-x. Consultado em 5 de setembro de 2025
- ↑ Loo, Jacky; But, Grace Wing-Chiu; Kwok, Ho-Chin; Lau, Pui-Man; Kong, Siu-Kai; Ho, Ho-Pui; Shaw, Pang-Chui (fevereiro de 2019). «A rapid sample-to-answer analytical detection of genetically modified papaya using loop-mediated isothermal amplification assay on lab-on-a-disc for field use». Food Chemistry (em inglês): 822–830. doi:10.1016/j.foodchem.2018.09.049. Consultado em 5 de setembro de 2025
- ↑ «Genetically Modified Organisms (Control of Release) Ordinance Cap. 607: Review of the Exemption of Genetically Modified Papayas in Hong Kong» (PDF). afcd.gov.hk. Abril de 2015. Consultado em 5 de setembro de 2025
- ↑ «Business BASF applies for approval for another biotech potato». Research in Germany (em inglês). 17 de novembro de 2011. Consultado em 5 de setembro de 2025. Cópia arquivada em 2 de junho de 2013
- ↑ «BASF applies for EU approval for Fortuna GM potato». Reuters (em inglês). 31 de outubro de 2011. Consultado em 5 de setembro de 2025
- ↑ «U.S.D.A. Approves Modified Potato. Next Up: French Fry Fans. (Published 2014)» (em inglês). 7 de novembro de 2014. Consultado em 5 de setembro de 2025
- ↑ «Availability of Petition for Determination of Nonregulated Status of Potato Genetically Engineered for Low Acrylamide Potential and Reduced Black Spot Bruise». Federal Register (em inglês). 3 de maio de 2013. Consultado em 5 de setembro de 2025
- ↑ Johnson, Stanley R. (fevereiro de 2008). «Quantification of the Impacts on US Agriculture of Biotechnology-Derived Crops Planted in 2006» (PDF). National Center for Food and Agricultural Policy. Consultado em 5 de setembro de 2025
- ↑ «GMO Database: Zucchini (courgette)». GMO Compass. 7 de novembro de 2007. Consultado em 5 de setembro de 2025. Cópia arquivada em 25 de fevereiro de 2017
- ↑ «Del Monte Gets Approval to Import GMO Pineapple». www.fooddemocracynow.org. Consultado em 5 de setembro de 2025. Cópia arquivada em 22 de abril de 2013
- ↑ Bradley, Diana (27 de outubro de 2020). «Inside the sweet and successful launch of the world's first pink pineapple». PRWeek. Consultado em 5 de setembro de 2025
- ↑ Pollack, A (13 de fevereiro de 2015). «First Genetically Modified Apple Approved for Sale in U.S.». The New York Times. Consultado em 5 de setembro de 2025
- ↑ Tracy, Tennille (13 de fevereiro de 2015). «First Genetically Modified Apple Approved for Sale in U.S.». Wall Street Journal (em inglês). Consultado em 5 de setembro de 2025
- ↑ «How'd we 'make' a nonbrowning apple?». Okanagan Specialty Fruits. 7 de dezembro de 2011. Consultado em 5 de setembro de 2025. Cópia arquivada em 12 de agosto de 2019
- ↑ «20 years ago today ... What have we learned since the GMO Flavr Savr tomato?». theecologist.org (em inglês). 5 de fevereiro de 2015. Consultado em 17 de outubro de 2025
- ↑ Woodruff, Sasa (6 de fevereiro de 2024). «Gardeners can now grow a genetically modified purple tomato made with snapdragon DNA». NPR (em inglês). Consultado em 17 de outubro de 2025
- ↑ Staff, Non-GMO Project (10 de julho de 2025). «New GMO Alert: GMO Tomatoes Are Back in Fashion! - The Non-GMO Project» (em inglês). Consultado em 17 de outubro de 2025
- ↑ «Know Before You Grow». National Corn Growers Association. Consultado em 5 de setembro de 2025. Cópia arquivada em 23 de outubro de 2011
- ↑ a b «Desmistificando o milho transgênico». CropLife. 16 de setembro de 2020. Consultado em 5 de setembro de 2025
- ↑ Padgette, SR; et al. (1995). «Development, identification, and characterization of a glyphosate-tolerant soybean line». Crop Sci. Consultado em 5 de setembro de 2025
- ↑ «Desmistificando a soja transgênica». CropLife. 1 de outubro de 2020. Consultado em 5 de setembro de 2025
- ↑ «O cultivo de plantas transgênicas no Brasil». CropLife. 18 de janeiro de 2021. Consultado em 5 de setembro de 2025
- ↑ Ermakova, Maria; Danila, Florence R.; Furbank, Robert T.; von Caemmerer, Susanne (fevereiro de 2020). «On the road to C4 rice: advances and perspectives». The Plant Journal: For Cell and Molecular Biology (4): 940–950. ISSN 1365-313X. PMC 7065233
 . PMID 31596523. doi:10.1111/tpj.14562. Consultado em 5 de setembro de 2025
. PMID 31596523. doi:10.1111/tpj.14562. Consultado em 5 de setembro de 2025
- ↑ Fujimoto, Hideya; Itoh, Kimiko; Yamamoto, Mikihiro; Kyozuka, Junko; Shimamoto, Ko (outubro de 1993). «Insect Resistant Rice Generated by Introduction of a Modified δ-endotoxin Gene of Bacillus thuringiensis». Nature Biotechnology (em inglês) (10): 1151–1155. ISSN 1087-0156. doi:10.1038/nbt1093-1151. Consultado em 5 de setembro de 2025
- ↑ Sharma, Arun K.; Sharma, Manoj K. (2009). «Plants as bioreactors: Recent developments and emerging opportunities». Biotechnology Advances (6): 811–832. ISSN 1873-1899. PMC 7125752
 . PMID 19576278. doi:10.1016/j.biotechadv.2009.06.004. Consultado em 5 de setembro de 2025
. PMID 19576278. doi:10.1016/j.biotechadv.2009.06.004. Consultado em 5 de setembro de 2025
- ↑ Black, Robert E.; Allen, Lindsay H.; Bhutta, Zulfiqar A.; Caulfield, Laura E.; de Onis, Mercedes; Ezzati, Majid; Mathers, Colin; Rivera, Juan; Maternal and Child Undernutrition Study Group (19 de janeiro de 2008). «Maternal and child undernutrition: global and regional exposures and health consequences». Lancet (London, England) (9608): 243–260. ISSN 1474-547X. PMID 18207566. doi:10.1016/S0140-6736(07)61690-0. Consultado em 5 de setembro de 2025
- ↑ Humphrey, J. H.; West, K. P.; Sommer, A. (1992). «Vitamin A deficiency and attributable mortality among under-5-year-olds». Bulletin of the World Health Organization (2): 225–232. ISSN 0042-9686. PMC 2393289
 . PMID 1600583. Consultado em 5 de setembro de 2025
. PMID 1600583. Consultado em 5 de setembro de 2025
- ↑ Paine, Jacqueline A; Shipton, Catherine A; Chaggar, Sunandha; Howells, Rhian M; Kennedy, Mike J; Vernon, Gareth; Wright, Susan Y; Hinchliffe, Edward; Adams, Jessica L (abril de 2005). «Improving the nutritional value of Golden Rice through increased pro-vitamin A content». Nature Biotechnology (em inglês) (4): 482–487. ISSN 1087-0156. doi:10.1038/nbt1082. Consultado em 5 de setembro de 2025
- ↑ Entine, Jon (29 de maio de 2018). «US FDA approves GMO Golden Rice as safe to eat». Genetic Literacy Project (em inglês). Consultado em 5 de setembro de 2025
- ↑ Catucci, Anaísa; Salati, Paula (11 de maio de 2023). «Trigo transgênico no Brasil: o que muda com a liberação do plantio e quais as críticas à medida». G1. Consultado em 5 de setembro de 2025
- ↑ «HB4 Wheat». GM Approval Database: ISAAA. Consultado em 23 de setembro de 2025
- ↑ «Desmistificando o algodão transgênico». CropLife. 30 de setembro de 2020. Consultado em 5 de setembro de 2025
- ↑ a b Charles, Dan (17 de outubro de 2018). «Not Just For Cows Anymore: New Cottonseed Is Safe For People To Eat». NPR (em inglês). Consultado em 28 de agosto de 2025
- ↑ a b Waltz, Emily (dezembro de 2018). «First edible cottonseed go-ahead». Nature Biotechnology (em inglês) (12): 1126–1126. ISSN 1087-0156. doi:10.1038/nbt1218-1126. Consultado em 28 de agosto de 2025
- ↑ «Os diversos usos da semente de algodão». eCycle. 14 de abril de 2021. Consultado em 5 de setembro de 2025
- ↑ «Genetically modified sugarcane developed by CTC in Brazil is approved at CTNBio». CTC - Centro de Tecnologia Canavieira (em inglês). 8 de junho de 2017. Consultado em 14 de setembro de 2025
- ↑ «CTNBio aprova feijão transgênico desenvolvido pela Embrapa - Portal Embrapa». www.embrapa.br. Consultado em 5 de setembro de 2025
- ↑ Gottems, Leonardo (2019). «Nigéria comercializa primeiro feijão caupi OGM». Portal Agrolink. Consultado em 14 de setembro de 2025
- ↑ «Ghana Releases GM Cowpea for Commercial Cultivation». ISAAA: Crop Biotech Update (em inglês). Consultado em 14 de setembro de 2025
- ↑ «Global progress toward transgenic food animals: A survey of publicly available information» (PDF). Food Standards Australia and New Zealand. 2003. Consultado em 5 de setembro de 2025. Cópia arquivada (PDF) em 13 de fevereiro de 2020
- ↑ «The rise and fall of genetically engineered salmon». www.nationalfisherman.com (em inglês). Consultado em 17 de outubro de 2025
- ↑ Coffey, Aidan; Ross, R. Paul (agosto de 2002). «Bacteriophage-resistance systems in dairy starter strains: molecular analysis to application». Antonie van Leeuwenhoek (em inglês) (1-4): 303–321. ISSN 0003-6072. doi:10.1023/A:1020639717181. Consultado em 5 de setembro de 2025
- ↑ O'Sullivan, Lisa; Bolton, Declan; McAuliffe, Olivia; Coffey, Aidan (25 de março de 2019). «Bacteriophages in Food Applications: From Foe to Friend». Annual Review of Food Science and Technology (em inglês) (1): 151–172. ISSN 1941-1413. doi:10.1146/annurev-food-032818-121747. Consultado em 5 de setembro de 2025
- ↑ Marston, Jennifer (19 de abril de 2023). «Pivot Bio pilot replaces synthetic nitrogen on nearly 1m acres of farmland». AgFunderNews (em inglês). Consultado em 17 de outubro de 2025
- ↑ «Publication : USDA ARS». www.ars.usda.gov. Consultado em 17 de outubro de 2025
- ↑ a b «Lecithin». GMO Compass. Outubro de 2015. Consultado em 5 de setembro de 2025. Cópia arquivada em 1 de novembro de 2015
- ↑ a b «GRAS Substances (SCOGS) Database - Select Committee on GRAS Substances (SCOGS) Opinion: Lecithin». www.fda.gov (em inglês). Consultado em 5 de setembro de 2025. Cópia arquivada em 26 de fevereiro de 2014
- ↑ «Corn Oil, 5th Edition» (PDF). Corn Refiners Association. 2006. Consultado em 5 de setembro de 2025
- ↑ a b Jaffe, Greg (7 de fevereiro de 2013). «What You Need to Know About Genetically Engineered Food». The Atlantic (em inglês). Consultado em 5 de setembro de 2025
- ↑ «Danisco emulsifier to subsitute non-GM soy lecithin as demand outstrips supply». FoodNavigator.com (em inglês). 30 de junho de 2005. Consultado em 5 de setembro de 2025
- ↑ Commission Regulation (EC) No 50/2000 of 10 January 2000 on the labelling of foodstuffs and food ingredients containing additives and flavourings that have been genetically modified or have been produced from genetically modified organisms (em inglês), 10 de janeiro de 2000, consultado em 5 de setembro de 2025
- ↑ Marx, Gertruida M (dezembro de 2010). «Monitoring of Genetically Modified Food Products in South Africa» (PDF). Consultado em 5 de setembro de 2025. Cópia arquivada (PDF) em 1 de setembro de 2015
- ↑ Davison, J.; Bertheau, Y. (9 de abril de 2008). «EU regulations on the traceability and detection of GMOs: difficulties in interpretation, implementation and compliance.». CABI Reviews (em inglês). ISSN 1749-8848. doi:10.1079/PAVSNNR20072077. Consultado em 5 de setembro de 2025
- ↑ James, Clive (2011). «Global Status of Commercialized Biotech/GM Crops: 2011». ISAAA Brief. Consultado em 5 de setembro de 2025
- ↑ «Sugar beet». GMO Compass. Consultado em 5 de setembro de 2025. Cópia arquivada em 1 de março de 2016
- ↑ Jaffe, Greg (7 de fevereiro de 2013). «What You Need to Know About Genetically Engineered Food». The Atlantic (em inglês). Consultado em 5 de setembro de 2025
- ↑ «Sugar Beet: White Sugar» (PDF). Food and Agriculture Organization of the United Nations. 2009. Consultado em 5 de setembro de 2025. Cópia arquivada (PDF) em 5 de setembro de 2015
- ↑ Klein, Joachim; Altenbuchner, Josef; Mattes, Ralf (fevereiro de 1998). «Nucleic acid and protein elimination during the sugar manufacturing process of conventional and transgenic sugar beets». Journal of Biotechnology (em inglês) (3): 145–153. doi:10.1016/S0168-1656(98)00006-6. Consultado em 5 de setembro de 2025
- ↑ «Aprovada primeira cana-de-açúcar transgênica do mundo». Confederação da Agricultura e Pecuária do Brasil (CNA). Consultado em 5 de setembro de 2025
- ↑ Lajolo, Franco Maria; Yokoyama, Silvia Mine; Cheavegatti Gianotto, Adriana (março de 2021). «Sugar derived from genetically modified sugarcane». Food Science and Technology (1): 1–7. ISSN 1678-457X. doi:10.1590/fst.30619. Consultado em 14 de setembro de 2025
- ↑ «Oilseeds and Products Annual». United States Department of Agriculture Foreign Agricultural Service. 22 de março de 2024. Consultado em 13 de novembro de 2025
- ↑ «USDA Protein(g) in Fats and Oils». ndb.nal.usda.gov (em inglês). Consultado em 5 de setembro de 2025. Cópia arquivada em 5 de outubro de 2018
- ↑ Crevel, R.W.R; Kerkhoff, M.A.T; Koning, M.M.G (abril de 2000). «Allergenicity of refined vegetable oils». Food and Chemical Toxicology (em inglês) (4): 385–393. doi:10.1016/S0278-6915(99)00158-1. Consultado em 5 de setembro de 2025
- ↑ «What is Canola Oil?». Canola Info (em inglês). 23 de outubro de 2024. Consultado em 5 de setembro de 2025
- ↑ «World soybean consumption quickens». southeastfarmpress.com. Consultado em 5 de setembro de 2025. Cópia arquivada em 5 de junho de 2006
- ↑ «Soybean». Encyclopædia Britannica Online (em inglês). 4 de setembro de 2025. Consultado em 5 de setembro de 2025
- ↑ «2012 World of Corn, National Corn Growers Association» (PDF). www.ncga.com. Consultado em 5 de setembro de 2025. Cópia arquivada (PDF) em 7 de fevereiro de 2020
- ↑ «Genetic Engineering: Feeding the EU's Livestock». GMO Compass. 7 de dezembro de 2006. Consultado em 5 de setembro de 2025. Cópia arquivada em 12 de janeiro de 2017
- ↑ Fellows, Peter (2009). Food processing technology: principles and practice. Col: Woodhead Publishing in food science, technology and nutrition 3rd ed. Boca Raton, Fla: CRC Press
- ↑ Gerdes, Louise I., ed. (2004). Genetic engineering: opposing viewpoints. Col: Opposing viewpoints series. Farmington Hills, MI: Greenhaven Press
- ↑ Taylor, Steve L.; Hefle, Susan L. (maio de 2001). «Will genetically modified foods be allergenic?». Journal of Allergy and Clinical Immunology (em inglês) (5): 765–771. doi:10.1067/mai.2001.114241. Consultado em 6 de setembro de 2025
- ↑ Emtage, J S; Angal, S; Doel, M T; Harris, T J; Jenkins, B; Lilley, G; Lowe, P A (junho de 1983). «Synthesis of calf prochymosin (prorennin) in Escherichia coli.». Proceedings of the National Academy of Sciences (em inglês) (12): 3671–3675. ISSN 0027-8424. PMC 394112
 . PMID 6304731. doi:10.1073/pnas.80.12.3671. Consultado em 6 de setembro de 2025
. PMID 6304731. doi:10.1073/pnas.80.12.3671. Consultado em 6 de setembro de 2025
- ↑ Harris, T.J.R.; Lowe, P.A.; Lyons, A.; Thomas, P.G.; Eaton, M.A.W.; Millican, T.A.; Patel, T.P.; Bose, C.C.; Carey, N.H. (1982). «Molecular cloning and nucleotide sequence of cDNA coding for calf preprochymosin». Nucleic Acids Research (em inglês) (7): 2177–2187. ISSN 0305-1048. PMC 320601
 . PMID 6283469. doi:10.1093/nar/10.7.2177. Consultado em 6 de setembro de 2025
. PMID 6283469. doi:10.1093/nar/10.7.2177. Consultado em 6 de setembro de 2025
- ↑ a b c «Chymosin». GMO Compass. Consultado em 6 de setembro de 2025. Cópia arquivada em 26 de março de 2015
- ↑ Law, Barry A (2010). «Technology of Cheesemaking». UK: Wiley-Blackwell (em inglês). ISBN 978-1-4051-8298-0. Consultado em 6 de setembro de 2025. Cópia arquivada em 26 de dezembro de 2023
- ↑ Johnson, M.E.; Lucey, J.A. (abril de 2006). «Major Technological Advances and Trends in Cheese». Journal of Dairy Science (em inglês) (4): 1174–1178. doi:10.3168/jds.S0022-0302(06)72186-5. Consultado em 6 de setembro de 2025
- ↑ «Use of Bovine Somatotropin in Dairy Production» (PDF). www.agribiotech.info. Consultado em 6 de setembro de 2025. Cópia arquivada (PDF) em 13 de maio de 2013
- ↑ Brennand, Charlotte P. «Bovine Somatotropin in Milk» (PDF). Consultado em 5 de setembro de 2025
- ↑ Cima, Greg (18 de novembro de 2010). «Appellate court gives mixed ruling on Ohio rBST labeling rules». JAVMA News. Consultado em 6 de setembro de 2025
- ↑ a b «International Dairy Foods Ass'n v. Boggs – Argued: June 10, 2010». Leagle (em inglês). Consultado em 6 de setembro de 2025
- ↑ a b Klümper, Wilhelm; Qaim, Matin (3 de novembro de 2014). albertini, emidio, ed. «A Meta-Analysis of the Impacts of Genetically Modified Crops». PLoS ONE (em inglês) (11): e111629. ISSN 1932-6203. PMC 4218791
 . PMID 25365303. doi:10.1371/journal.pone.0111629. Consultado em 6 de setembro de 2025
. PMID 25365303. doi:10.1371/journal.pone.0111629. Consultado em 6 de setembro de 2025
- ↑ Pollack, A (13 de abril de 2010). «Study Says Overuse Threatens Gains From Modified Crops». The New York Times (em inglês). Consultado em 6 de setembro de 2025
- ↑ Perry, Edward D.; Ciliberto, Federico; Hennessy, David A.; Moschini, GianCarlo (5 de agosto de 2016). «Genetically engineered crops and pesticide use in U.S. maize and soybeans». Science Advances (em inglês) (8). ISSN 2375-2548. PMC 5020710
 . PMID 27652335. doi:10.1126/sciadv.1600850. Consultado em 6 de setembro de 2025
. PMID 27652335. doi:10.1126/sciadv.1600850. Consultado em 6 de setembro de 2025
- ↑ Smyth, Stuart J. (abril de 2020). «The human health benefits from GM crops». Plant Biotechnology Journal (em inglês) (4): 887–888. ISSN 1467-7644. PMC 7061863
 . PMID 31544299. doi:10.1111/pbi.13261. Consultado em 6 de setembro de 2025
. PMID 31544299. doi:10.1111/pbi.13261. Consultado em 6 de setembro de 2025
- ↑ Kovak, Emma; Blaustein-Rejto, Dan; Qaim, Matin (julho de 2022). «Genetically modified crops support climate change mitigation». Trends in Plant Science (em inglês) (7): 627–629. doi:10.1016/j.tplants.2022.01.004. Consultado em 6 de setembro de 2025
- ↑ Brookes, Graham (2 de julho de 2020). «Genetically modified (GM) crop use in Colombia: farm level economic and environmental contributions». GM Crops & Food (em inglês) (3): 140–153. ISSN 2164-5698. PMC 7518743
 . PMID 32008444. doi:10.1080/21645698.2020.1715156. Consultado em 6 de setembro de 2025
. PMID 32008444. doi:10.1080/21645698.2020.1715156. Consultado em 6 de setembro de 2025
- ↑ a b Drago, Carolina (5 de janeiro de 2011). «Biotecnologia contra a seca». Ciência Hoje. Consultado em 27 de agosto de 2025
- ↑ a b c d Costa-Font, Montserrat; Gil, José M.; Traill, W. Bruce (abril de 2008). «Consumer acceptance, valuation of and attitudes towards genetically modified food: Review and implications for food policy». Food Policy (em inglês) (2): 99–111. doi:10.1016/j.foodpol.2007.07.002. Consultado em 26 de agosto de 2025
- ↑ a b Costa, Thadeu Estevam Moreira Maramaldo; Dias, Aline Peçanha Muzy; Scheidegger, Érica Miranda Damasio; Marin, Victor Augustus (janeiro de 2011). «Avaliação de risco dos organismos geneticamente modificados». Ciência & Saúde Coletiva (1): 327–336. ISSN 1413-8123. doi:10.1590/S1413-81232011000100035. Consultado em 25 de agosto de 2025
- ↑ a b Lenzi, Cristiano Luis (2010). «A rotulagem como precaução: a liberação da soja RR e a regulação dos transgênicos no Brasil». Estudos Sociedade e Agricultura (1): 220–255. Consultado em 25 de agosto de 2025
- ↑ a b Giuliani, Gian Mario (2000). «O dilema dos transgênicos». Estudos Sociedade e Agricultura. ISSN 2526-7752. Consultado em 25 de agosto de 2025
- ↑ a b Pouteau, Sylvie (1 de setembro de 2000). «Beyond Substantial Equivalence: Ethical Equivalence». Journal of Agricultural and Environmental Ethics (em inglês) (3): 273–291. ISSN 1573-322X. doi:10.1023/A:1009546031890. Consultado em 25 de agosto de 2025
- ↑ a b c «Elements of Precaution: Recommendations for the Regulation of Food Biotechnology in Canada» (PDF). The Royal Society of Canada (em inglês). 2001. Cópia arquivada (PDF) em 19 de maio de 2017
- ↑ a b «Saiba o que são os alimentos transgênicos e quais os seus riscos». Instituto de Defesa do Consumidor. Consultado em 25 de agosto de 2025
- ↑ «Why are there no long-term GMO safety studies or studies on humans?». Genetic Literacy Project (em inglês). Consultado em 5 de novembro de 2025
- ↑ Katiraee, Layla (20 de julho de 2016). «Why aren't GMOs tested on humans?». Biofortified (em inglês). Consultado em 5 de novembro de 2025
- ↑ Seek Rhee, Gyu; Hyun Cho, Dae; Hyuck Won, Yong; Hyun Seok, Ji; Sun Kim, Soon; Jun Kwack, Seung; Da Lee, Rhee; Yeong Chae, Soo; Woo Kim, Jae (dezembro de 2005). «Multigeneration Reproductive and Developmental Toxicity Study of bar Gene Inserted into Genetically Modified Potato on Rats». Journal of Toxicology and Environmental Health, Part A (em inglês) (23-24): 2263–2276. ISSN 1528-7394. doi:10.1080/15287390500182446. Consultado em 5 de novembro de 2025
- ↑ Zhang, Min; Zhuo, Qin; Tian, Yuan; Piao, Jianhua; Yang, Xiaoguang (janeiro de 2014). «Long-term toxicity study on transgenic rice with Cry1Ac and sck genes». Food and Chemical Toxicology (em inglês): 76–83. doi:10.1016/j.fct.2013.10.035. Consultado em 5 de novembro de 2025
- ↑ Kılıç, Aysun; Akay, M. Turan (março de 2008). «A three generation study with genetically modified Bt corn in rats: Biochemical and histopathological investigation». Food and Chemical Toxicology (em inglês) (3): 1164–1170. doi:10.1016/j.fct.2007.11.016. Consultado em 5 de novembro de 2025
- ↑ Flachowsky, Gerhard; Halle, Ingrid; Aulrich, Karen (dezembro de 2005). «Long term feeding of Bt-corn – a ten-generation study with quails». Archives of Animal Nutrition (em inglês) (6): 449–451. ISSN 1745-039X. doi:10.1080/17450390500353549. Consultado em 5 de novembro de 2025
- ↑ Sissener, N.H.; Sanden, M.; Bakke, A.M.; Krogdahl, å.; Hemre, G.-I. (setembro de 2009). «A long term trial with Atlantic salmon (Salmo salar L.) fed genetically modified soy; focusing general health and performance before, during and after the parr–smolt transformation». Aquaculture (em inglês) (1-2): 108–117. doi:10.1016/j.aquaculture.2009.05.002. Consultado em 5 de novembro de 2025
- ↑ Ricroch, Agnès E.; Boisron, Audrey; Kuntz, Marcel (2014). «Looking back at safety assessment of GM food/feed: an exhaustive review of 90-day animal feeding studies». International Journal of Biotechnology (em inglês) (4). 230 páginas. ISSN 0963-6048. doi:10.1504/IJBT.2014.068940. Consultado em 5 de novembro de 2025
- ↑ a b Snell, Chelsea; Bernheim, Aude; Bergé, Jean-Baptiste; Kuntz, Marcel; Pascal, Gérard; Paris, Alain; Ricroch, Agnès E. (março de 2012). «Assessment of the health impact of GM plant diets in long-term and multigenerational animal feeding trials: A literature review». Food and Chemical Toxicology (em inglês) (3-4): 1134–1148. doi:10.1016/j.fct.2011.11.048. Consultado em 5 de setembro de 2025.
Os resultados de todos os 24 estudos não sugerem quaisquer riscos para a saúde e, em geral, não foram observadas diferenças estatisticamente significativas nos parâmetros analisados. No entanto, foram observadas algumas pequenas diferenças, embora estas se enquadrassem na variação normal do parâmetro considerado e, por isso, não tivessem qualquer significado biológico ou toxicológico. Se necessário, um estudo de alimentação de 90 dias realizado em roedores, de acordo com a Diretriz de Teste da OCDE, é geralmente considerado suficiente para avaliar os efeitos na saúde dos alimentos geneticamente modificados. Os estudos analisados apresentam evidências que mostram que as plantas geneticamente modificadas são nutricionalmente equivalentes às suas contrapartes não geneticamente modificadas e podem ser utilizadas com segurança em alimentos e rações.
- ↑ Steinke, K.; Guertler, P.; Paul, V.; Wiedemann, S.; Ettle, T.; Albrecht, C.; Meyer, H. H. D.; Spiekers, H.; Schwarz, F. J. (outubro de 2010). «Effects of long-term feeding of genetically modified corn (event MON810) on the performance of lactating dairy cows: Long-term feeding of genetically modified corn in dairy cows». Journal of Animal Physiology and Animal Nutrition (em inglês) (5): e185–e193. doi:10.1111/j.1439-0396.2010.01003.x. Consultado em 5 de novembro de 2025
- ↑ Van Eenennaam, A. L.; Young, A. E. (1 de outubro de 2014). «Prevalence and impacts of genetically engineered feedstuffs on livestock populations». Journal of Animal Science (em inglês) (10): 4255–4278. ISSN 0021-8812. doi:10.2527/jas.2014-8124. Consultado em 5 de novembro de 2025
- ↑ Walsh, Maria C.; Buzoianu, Stefan G.; Rea, Mary C.; O’Donovan, Orla; Gelencsér, Eva; Ujhelyi, Gabriella; Ross, R. Paul; Gardiner, Gillian E.; Lawlor, Peadar G. (4 de maio de 2012). Gilbert, Jack Anthony, ed. «Effects of Feeding Bt MON810 Maize to Pigs for 110 Days on Peripheral Immune Response and Digestive Fate of the cry1Ab Gene and Truncated Bt Toxin». PLoS ONE (em inglês) (5): e36141. ISSN 1932-6203. PMC 3345032
 . PMID 22574138. doi:10.1371/journal.pone.0036141. Consultado em 5 de novembro de 2025
. PMID 22574138. doi:10.1371/journal.pone.0036141. Consultado em 5 de novembro de 2025
- ↑ Trabalza-Marinucci, Massimo; Brandi, Giorgio; Rondini, Cristina; Avellini, Luca; Giammarini, Camilla; Costarelli, Silva; Acuti, Gabriele; Orlandi, Chiara; Filippini, Giovanni (fevereiro de 2008). «A three-year longitudinal study on the effects of a diet containing genetically modified Bt176 maize on the health status and performance of sheep». Livestock Science (em inglês) (2-3): 178–190. doi:10.1016/j.livsci.2007.03.009. Consultado em 5 de novembro de 2025
- ↑ Buzoianu, S. G.; Walsh, M. C.; Rea, M. C.; Cassidy, J. P.; Ryan, T. P.; Ross, R. P.; Gardiner, G. E.; Lawlor, P. G. (1 de janeiro de 2013). «Transgenerational effects of feeding genetically modified maize to nulliparous sows and offspring on offspring growth and health1». Journal of Animal Science (em inglês) (1): 318–330. ISSN 0021-8812. doi:10.2527/jas.2012-5360. Consultado em 5 de novembro de 2025
- ↑ Wang, Chenyun; Fan, Shengtao; Li, Minghao; Ye, Yousong; Li, Zheli; Long, Weihu; Li, Yongjie; Huang, Zhangqiong; Jiang, Qinfang (junho de 2025). «A 7-year feed study on the long-term effects of genetically modified maize containing cry1Ab/cry2Aj and EPSPS genes on gut microbiota and metabolite profiles across two generations of cynomolgus macaques». Food and Chemical Toxicology (em inglês). 115419 páginas. doi:10.1016/j.fct.2025.115419
 . Consultado em 5 de novembro de 2025.
. Consultado em 5 de novembro de 2025. Em conclusão, este estudo investigou a microbiota intestinal e os perfis metabólicos de duas gerações de macacos-cinomolgos alimentados com uma dieta de milho geneticamente modificado e não encontrou diferenças significativas na maioria dos indicadores. Embora tenham sido observadas algumas diferenças estatisticamente significativas entre os grupos alimentados com milho geneticamente modificado e os alimentados com milho não geneticamente modificado, essas diferenças não afetaram as funções biológicas durante o período de alimentação.
- ↑ «Lei nº 10.831». Planalto Brasileiro. Consultado em 25 de agosto de 2025
- ↑ Regulation (EU) 2018/848 of the European Parliament and of the Council of 30 May 2018 on organic production and labelling of organic products and repealing Council Regulation (EC) No 834/2007 (em inglês), 25 de março de 2025, consultado em 25 de agosto de 2025
- ↑ Department of Agricultural Economics and Extension, School of Agriculture, University of Cape Coast, Ghana; Owusu, Rebecca; Dadzie, Samuel; Department of Agricultural Economics and Extension, School of Agriculture, University of Cape Coast, Ghana (30 de junho de 2021). «Heterogeneity in consumer preferences for organic and genetically modified food products in Ghana». African Journal of Agricultural and Resource Economics (2): 112–125. doi:10.53936/afjare.2021.16(2).08. Consultado em 25 de agosto de 2025
- ↑ «Can GMOs Be Used in Organic Products?». www.ams.usda.gov (em inglês). Consultado em 25 de agosto de 2025
- ↑ Ashaolu, Tolulope J.; Ashaolu, Joseph O. (dezembro de 2020). «Perspectives on the trends, challenges and benefits of green, smart and organic (GSO) foods». International Journal of Gastronomy and Food Science (em inglês). 100273 páginas. PMC 7574864
 . PMID 33101552. doi:10.1016/j.ijgfs.2020.100273. Consultado em 25 de agosto de 2025
. PMID 33101552. doi:10.1016/j.ijgfs.2020.100273. Consultado em 25 de agosto de 2025
- ↑ a b «The History and Future of GM Potatoes». www.potatopro.com. Consultado em 26 de agosto de 2025. Cópia arquivada em 12 de outubro de 2013
- ↑ a b c Winter, CK; Gallegos, LK. «Safety of Genetically Engineered Food» (PDF). University of California Agricultural and Natural Resource Service. ANR Publication 8180. (em inglês). Consultado em 25 de agosto de 2025
- ↑ EFSA Panel on Genetically Modified Organisms (GMO) (maio de 2011). «Guidance for risk assessment of food and feed from genetically modified plants». EFSA Journal (5). doi:10.2903/j.efsa.2011.2150. Consultado em 25 de agosto de 2025
- ↑ «The Safety of Genetically Modified Foods Produced through Biotechnology». Toxicological Sciences (em inglês) (1): 2–8. 1 de janeiro de 2003. doi:10.1093/toxsci/71.1.2. Consultado em 25 de agosto de 2025
- ↑ a b «Substantial Equivalence in Food Safety Assessment» (PDF). Council for Biotechnology Information (em inglês). 11 de abril de 2001. Consultado em 26 de agosto de 2025. Cópia arquivada (PDF) em 6 de fevereiro de 2009
- ↑ a b Kok, Esther J; Kuiper, Harry A (outubro de 2003). «Comparative safety assessment for biotech crops». Trends in Biotechnology (em inglês) (10): 439–444. doi:10.1016/j.tibtech.2003.08.003. Consultado em 25 de agosto de 2025
- ↑ a b c d FAO, ed. (2009). Gm food safety assessment: tools for trainers. Rome: Food and Agriculture Organization of the United Nations
- ↑ «EPA's Regulation of Biotechnology for Use in Pest Management». www.epa.gov (em inglês). 9 de setembro de 2015. Consultado em 25 de agosto de 2025
- ↑ Resolução Normativa Nº 32, de 15 de Junho de 2021 - CTNBio Dispõe sobre as normas para liberação comercial e monitoramento de animais e vegetais Geneticamente Modificados - OGM e seus derivados de origem vegetal e animal.
- ↑ «Substantial Equivalence in Food Safety Assessment» (PDF). Council for Biotechnology Information (em inglês). 11 de abril de 2001. Consultado em 26 de agosto de 2025. Cópia arquivada (PDF) em 6 de fevereiro de 2009
- ↑ American Association for the Advancement of Science (AAAS), Board of Directors (2012). «Statement by the AAAS Board of Directors On Labeling of Genetically Modified Foods» (PDF). Consultado em 7 de novembro de 2025
- ↑ «Joint FAO/WHO Expert Consultation on Biotechnology and Food Safety» (PDF). FAO/WHO. Outubro de 1990. Consultado em 25 de agosto de 2025. Cópia arquivada (PDF) em 18 de maio de 2017
- ↑ a b Schauzu, Marianna (abril de 2000). «The concept of substantial equivalence in safety assessment of foods derived from genetically modified organisms» (PDF). AgBiotechNet. Consultado em 25 de agosto de 2025
- ↑ a b c d Guida, Alessandra (2021). «The precautionary principle and genetically modified organisms: A bone of contention between European institutions and member states». Journal of Law and the Biosciences (1): lsab012. ISSN 2053-9711. PMC 8132481
 . PMID 34040782. doi:10.1093/jlb/lsab012. Consultado em 26 de agosto de 2025
. PMID 34040782. doi:10.1093/jlb/lsab012. Consultado em 26 de agosto de 2025
- ↑ «The Cartagena Protocol on Biosafety». The Biosafety Clearing-House (BCH) (em inglês). 31 de outubro de 2025. Consultado em 7 de novembro de 2025
- ↑ a b «Fact Sheet: Questions and Answers on EU\'s policies on GMOs». European Commission. Consultado em 26 de agosto de 2025
- ↑ a b c d Vieira, Letícia Rios; Freitas, Natália Chagas; Justen, Fernanda; Miranda, Vívian de Jesus; Garcia, Bruno de Oliveira; Nepomuceno, Alexandre Lima; Fuganti-Pagliarini, Renata; Felipe, Maria Sueli Soares; Molinari, Hugo Bruno Correa; Velini, Edivaldo Domingues; Pinto, Eduardo Romano de Campos; Dagli, Maria Lucia Zaidan; Andrade, Galdino; Fernandes, Patricia Machado Bueno; Mertz-Henning, Liliane Marcia; Kobayashi, Adilson Kenji (2021). «Regulatory framework of genome editing in Brazil and worldwide.» (PDF). alice.cnptia.embrapa.br. Consultado em 8 de setembro de 2025
- ↑ «Certificado de Qualidade em Biossegurança». Comissão Interna de Biossegurança – CIBio, Faculdade de Medicina Veterinária e Zootecnia da USP. Consultado em 8 de setembro de 2025
- ↑ Resolução Normativa CTNBio nº 16, de 15.01.2018 Estabelece os requisitos técnicos para apresentação de consulta à CTNBio sobre as Técnicas Inovadoras de Melhoramento de Precisão.
- ↑ a b Tome, Kristine Grace; Dionglay, Clement; Escasura, Janine Cyren. «Countries Approving GM Crop Cultivation». Science Speaks: ISAAA (em inglês). Consultado em 21 de setembro de 2025
- ↑ a b c Gbadegesin, Lanre Anthony; Ayeni, Emmanuel Ayodeji; Tettey, Carlos Kwesi; Uyanga, Victoria Anthony; Aluko, Oluwaseun Olayemi; Ahiakpa, John Kojo; Okoye, Charles Obinwanne; Mbadianya, Jane Ifunanya; Adekoya, Modinat Adejoke (novembro de 2022). «GMOs in Africa: Status, adoption and public acceptance». Food Control (em inglês). doi:10.1016/j.foodcont.2022.109193. Consultado em 21 de setembro de 2025
- ↑ a b c d e f g «FAO GM Foods Platform». Food and Agriculture Organization. Consultado em 13 de setembro de 2025
- ↑ «SEMENTES GENETICAMENTE MODIFICADAS». Portal Oficial do Governo de Angola. Consultado em 21 de setembro de 2025
- ↑ «O QUADRO NACIONAL DE BIOSEGURANÇA PARA CABO VERDE». MINISTÉRIO DO AMBIENTE E AGRICULTURA. Novembro de 2007
- ↑ a b «Boletim da República» (PDF). Publicação Oficial da República de Moçambique. 28 de novembro de 2014
- ↑ Sixpense, Nário (28 de maio de 2025). «Instituto de Investigação Agrária Recomenda Uso de Milho Geneticamente Modificado Após Resultados Positivos no País». Diário Económico. Consultado em 21 de setembro de 2025
- ↑ «Commonly Asked Questions about the Food Safety of GMOs». www.monsanto.com. Consultado em 8 de setembro de 2025. Cópia arquivada em 18 de junho de 2017
- ↑ «International Labeling Laws». Center for Food Safety (em inglês). Consultado em 13 de setembro de 2025
- ↑ Guillaume P. Gruère and S.R. Rao (11 de maio de 2007). «A Review of International Labeling Policies of Genetically Modified Food to Evaluate India's Proposed Rule». agbioforum.org. Consultado em 13 de setembro de 2025. Cópia arquivada em 3 de março de 2016
- ↑ «D4680». www.planalto.gov.br. Consultado em 13 de setembro de 2025
- ↑ Davison, John (fevereiro de 2010). «GM plants: Science, politics and EC regulations». Plant Science (em inglês) (2): 94–98. doi:10.1016/j.plantsci.2009.12.005. Consultado em 13 de setembro de 2025
- ↑ Waddell, Melissa (24 de março de 2022). «U.S. Becomes 65th Country to Label GMOs». The Non-GMO Project (em inglês). Consultado em 13 de setembro de 2025
- ↑ Wunderlich, Shahla; Gatto, Kelsey A. (novembro de 2015). «Consumer perception of genetically modified organisms and sources of information». Advances in Nutrition (Bethesda, Md.) (6): 842–851. ISSN 2156-5376. PMC 4642419
 . PMID 26567205. doi:10.3945/an.115.008870. Consultado em 13 de setembro de 2025
. PMID 26567205. doi:10.3945/an.115.008870. Consultado em 13 de setembro de 2025
- ↑ «EU GMO testing homepage». European Commission Join Research Centre (em inglês). Consultado em 13 de setembro de 2025
- ↑ Costa, Joana; Mafra, Isabel; Amaral, Joana S.; Oliveira, M.B.P.P. (janeiro de 2010). «Monitoring genetically modified soybean along the industrial soybean oil extraction and refining processes by polymerase chain reaction techniques». Food Research International (em inglês) (1): 301–306. doi:10.1016/j.foodres.2009.10.003. Consultado em 13 de setembro de 2025
- ↑ Falkner, Robert (abril de 2000). «Regulating Biotech Trade: the Cartegena Protocol on Biosafety». International Affairs (em inglês) (2): 299–313. ISSN 0020-5850. doi:10.1111/1468-2346.00135. Consultado em 13 de setembro de 2025
- ↑ Gould, Fred; Amasino, Richard M.; Brossard, Dominique; Buell, C. Robin; Dixon, Richard A.; Falck-Zepeda, Jose B.; Gallo, Michael A.; Giller, Ken E.; Glenna, Leland L. (2 de setembro de 2022). «Toward product-based regulation of crops». Science (em inglês) (6610): 1051–1053. ISSN 0036-8075. doi:10.1126/science.abo3034. Consultado em 13 de setembro de 2025
- ↑ «IDEA Position on Genetically Modified Foods». IDEA Ireland (em inglês). Consultado em 26 de agosto de 2025. Cópia arquivada em 26 de março de 2014
- ↑ Noisette, Christophe. "OGM: as empresas colhem os dividendos da fome". In: Zanoni, Magda & Ferment, Gilles (orgs.). Transgênicos para quem? Agricultura, Ciência e Sociedade. Ministério do Desenvolvimento Agrário, 2011, pp. 394-398
- ↑ Almeida Jr, Antonio Ribeiro de; Mattos, Zilda Paes de Barros (2005). «Ilusórias sementes». Ambiente & Sociedade: 101–120. ISSN 1414-753X. doi:10.1590/S1414-753X2005000100007. Consultado em 26 de agosto de 2025
- ↑ de Vendômois, Joël Spiroux; Cellier, Dominique; Vélot, Christian; Clair, Emilie; Mesnage, Robin; Séralini, Gilles-Eric (5 de outubro de 2010). «Debate on GMOs health risks after statistical findings in regulatory tests». International Journal of Biological Sciences (6): 590–598. ISSN 1449-2288. PMC 2952409
 . PMID 20941377. doi:10.7150/ijbs.6.590. Consultado em 26 de agosto de 2025
. PMID 20941377. doi:10.7150/ijbs.6.590. Consultado em 26 de agosto de 2025
- ↑ Hams, Marcia; Wilkinson, Wells G.; Zentner, Lynn; Schmidt, Cory; Dweik, Raed A.; Karafa, Matthew; Rose, Susannah L. (15 de mar. de 2017). «A new survey to evaluate conflict of interest policies at academic medical centers». PLOS ONE (em inglês) (3): e0172472. ISSN 1932-6203. PMC 5351836
 . PMID 28296898. doi:10.1371/journal.pone.0172472. Consultado em 26 de agosto de 2025
. PMID 28296898. doi:10.1371/journal.pone.0172472. Consultado em 26 de agosto de 2025
- ↑ Diels, Johan; Cunha, Mario; Manaia, Célia; Sabugosa-Madeira, Bernardo; Silva, Margarida (1 de abril de 2011). «Association of financial or professional conflict of interest to research outcomes on health risks or nutritional assessment studies of genetically modified products». Food Policy (2): 197–203. ISSN 0306-9192. doi:10.1016/j.foodpol.2010.11.016. Consultado em 26 de agosto de 2025
- ↑ Deepa Arya. Genetically Modified Foods: Benefits and Risks. Massachusetts Medical Society, 2015, p. 1
- ↑ Hauter, Wenonah. "GM crops: Follow the money". Euractiv, 10/02/2012
- ↑ Fernandes, Gabriel B. (org.). Mesa de Controvérsias sobre Transgênicos — Relatório Final. Conselho Nacional de Segurança Alimentar e Nutricional, 2013
- ↑ Deepa Arya. Genetically Modified Foods: Benefits and Risks. Massachusetts Medical Society, 2015
- ↑ Carta de Salvador – Carta Política Final do Encontro de Diálogos e Convergências. Fórum Brasileiro de Economia Solidária, 2011
- ↑ a b Conselho Nacional de Segurança Alimentar e Nutricional. Mesa de Controvérsias sobre Transgênicos: Relatório Final, 2014.
- ↑ Londres, Flavia. "Transgênicos no Brasil: as verdadeiras conseqüências". In: XVII Congresso Brasileiro de Ciência e Tecnologia de Alimentos — A Sustentabilidade na Produção de Alimentos e a Agenda 21 do Brasil. Fortaleza, 09/08/2000
- ↑ Weissheimer, Marco. "Esse brócolis tem dono! É da Monsanto!" Sul 21, 17/07/2013
- ↑ Dufumier, Marc. "Os organismos geneticamente modificados (OMGs) poderiam alimentar o terceiro mundo?" In: Zanoni, Magda & Ferment, Gilles (orgs.). Transgênicos para quem? Agricultura, Ciência e Sociedade. Ministério do Desenvolvimento Agrário, 2011, pp. 368-393
- ↑ "Milho transgênico: uma morte lenta e silenciosa. Entrevista especial com Antônio Inácio Andrioli". Revista do Instituto Humanitas — Unisinos, 09/03/2009
- ↑ Brown, Carolyn (3 de outubro de 2000). «Patenting life: genetically altered mice an invention, court declares». CMAJ: Canadian Medical Association Journal (em inglês). 163 (7). 867 páginas. PMID 11033718. Consultado em 14 de janeiro de 2022
- ↑ "Possível liberação de transgênicos já motiva protestos". O Estado de São Paulo, 23/09/2003
- ↑ "Produtora de transgênicos Monsanto enfrenta onda de protestos pelo mundo". Carta Capital, 29/05/2013
- ↑ Allain, Juliana Mezzomo; Nascimento-Schulze, Clélia Maria; Camargo, Brígido Vizeu. "As representações sociais de transgênicos nos jornais brasileiros". In: Estudos de Psicologia (Natal), 2009; 14 (1)
- ↑ "Justiça condena Monsanto por propaganda enganosa sobre transgênico". Conselho Nacional de Segurança Alimentar e Nutricional, 22/08/2012
- ↑ Knutson, Jonathan (22 de maio de 2018). «Dairy farmers fight back against deceptive advertising». Agweek (em inglês). Consultado em 26 de agosto de 2025
- ↑ a b c d e f Paparini, Andrea; Romano-Spica, Vincenzo (2004). «Public health issues related with the consumption of food obtained from genetically modified organisms». Elsevier (em inglês): 85–122. ISBN 978-0-444-51749-4. doi:10.1016/s1387-2656(04)10004-5. Consultado em 26 de agosto de 2025
- ↑ Prescott, Vanessa E.; Hogan, Simon P. (agosto de 2006). «Genetically modified plants and food hypersensitivity diseases: Usage and implications of experimental models for risk assessment». Pharmacology & Therapeutics (em inglês) (2): 374–383. doi:10.1016/j.pharmthera.2005.10.005. Consultado em 26 de agosto de 2025
- ↑ Ahmed, Farid E. (novembro de 2003). «Genetically modified probiotics in foods». Trends in Biotechnology (em inglês) (11): 491–497. doi:10.1016/j.tibtech.2003.09.006. Consultado em 26 de agosto de 2025
- ↑ D'Agnolo, G. (agosto de 2005). «GMO: Human Health Risk Assessment». Veterinary Research Communications (em inglês) (S2): 7–11. ISSN 0165-7380. doi:10.1007/s11259-005-0003-7. Consultado em 26 de agosto de 2025
- ↑ a b Watson, Ronald Ross; Preedy, Victor R. (2016). Genetically modified organisms in food: production, safety, regulation, and public health. Amsterdam Boston Heidelberg: Elsevier, Academic Press
- ↑ Keese, Paul (julho de 2008). «Risks from GMOs due to Horizontal Gene Transfer». Environmental Biosafety Research (3): 123–149. ISSN 1635-7922. doi:10.1051/ebr:2008014. Consultado em 26 de agosto de 2025
- ↑ Flachowsky, Gerhard; Chesson, Andrew; Aulrich, Karen (fevereiro de 2005). «Animal nutrition with feeds from genetically modified plants». Archives of Animal Nutrition (em inglês) (1): 1–40. ISSN 1745-039X. doi:10.1080/17450390512331342368. Consultado em 26 de agosto de 2025
- ↑ Beagle, J. M.; Apgar, G. A.; Jones, K. L.; Griswold, K. E.; Radcliffe, J. S.; Qiu, X.; Lightfoot, D. A.; Iqbal, M. J. (1 de abril de 2006). «The digestive fate of Escherichia coli glutamate dehydrogenase deoxyribonucleic acid from transgenic corn in diets fed to weanling pigs1». Journal of Animal Science (em inglês) (3): 597–607. ISSN 0021-8812. doi:10.2527/2006.843597x. Consultado em 26 de agosto de 2025
- ↑ Brigulla, Matthias; Wackernagel, Wilfried (abril de 2010). «Molecular aspects of gene transfer and foreign DNA acquisition in prokaryotes with regard to safety issues». Applied Microbiology and Biotechnology (em inglês) (4): 1027–1041. ISSN 0175-7598. doi:10.1007/s00253-010-2489-3. Consultado em 26 de agosto de 2025
- ↑ Guertler, Patrick; Paul, Vijay; Albrecht, Christiane; Meyer, Heinrich H. D. (março de 2009). «Sensitive and highly specific quantitative real-time PCR and ELISA for recording a potential transfer of novel DNA and Cry1Ab protein from feed into bovine milk». Analytical and Bioanalytical Chemistry (em inglês) (6-7): 1629–1638. ISSN 1618-2642. doi:10.1007/s00216-009-2667-2. Consultado em 26 de agosto de 2025
- ↑ Snow, Jonathan W.; Hale, Andrew E.; Isaacs, Stephanie K.; Baggish, Aaron L.; Chan, Stephen Y. (julho de 2013). «Ineffective delivery of diet-derived microRNAs to recipient animal organisms». RNA Biology (em inglês) (7): 1107–1116. ISSN 1547-6286. PMC 3849158
 . PMID 23669076. doi:10.4161/rna.24909. Consultado em 26 de agosto de 2025
. PMID 23669076. doi:10.4161/rna.24909. Consultado em 26 de agosto de 2025
- ↑ Witwer, Kenneth W.; McAlexander, Melissa A.; Queen, Suzanne E.; Adams, Robert J. (julho de 2013). «Real-time quantitative PCR and droplet digital PCR for plant miRNAs in mammalian blood provide little evidence for general uptake of dietary miRNAs: Limited evidence for general uptake of dietary plant xenomiRs». RNA Biology (em inglês) (7): 1080–1086. ISSN 1547-6286. PMC 3849155
 . PMID 23770773. doi:10.4161/rna.25246. Consultado em 26 de agosto de 2025
. PMID 23770773. doi:10.4161/rna.25246. Consultado em 26 de agosto de 2025
- ↑ Uzogara, Stella G. (maio de 2000). «The impact of genetic modification of human foods in the 21st century». Biotechnology Advances (em inglês) (3): 179–206. doi:10.1016/S0734-9750(00)00033-1. Consultado em 26 de agosto de 2025
- ↑ Nelson, Gerald C. (2001). Genetically Modified Organisms in Agriculture: Economics and Politics 1st ed. San Diego: Elsevier Science & Technology
- ↑ a b Bennett, P. M. (12 de fevereiro de 2004). «An assessment of the risks associated with the use of antibiotic resistance genes in genetically modified plants: report of the Working Party of the British Society for Antimicrobial Chemotherapy». Journal of Antimicrobial Chemotherapy (em inglês) (3): 418–431. ISSN 1460-2091. doi:10.1093/jac/dkh087. Consultado em 26 de agosto de 2025
- ↑ a b Gay, Philippe B.; Gillespie, Stephen H. (1 de outubro de 2005). «Antibiotic resistance markers in genetically modified plants: a risk to human health?». The Lancet Infectious Diseases (em inglês) (10): 637–646. ISSN 1473-3099. PMID 16183518. doi:10.1016/S1473-3099(05)70241-3. Consultado em 26 de agosto de 2025
- ↑ a b c «Consolidated presentation of the joint Scientific Opinion of the GMO and BIOHAZ Panels on the "Use of Antibiotic Resistance Genes as Marker Genes in Genetically Modified Plants" and the Scientific Opinion of the GMO Panel on "Consequences of the Opinion | EFSA». www.efsa.europa.eu (em inglês). 11 de junho de 2009. Consultado em 26 de agosto de 2025
- ↑ a b Ramessar, Koreen; Peremarti, Ariadna; Gómez-Galera, Sonia; Naqvi, Shaista; Moralejo, Marian; Muñoz, Pilar; Capell, Teresa; Christou, Paul (junho de 2007). «Biosafety and risk assessment framework for selectable marker genes in transgenic crop plants: a case of the science not supporting the politics». Transgenic Research (em inglês) (3): 261–280. ISSN 0962-8819. doi:10.1007/s11248-007-9083-1. Consultado em 26 de agosto de 2025
- ↑ a b Bodnar, Anastasia (19 de março de 2010). «GMOs could render important antibiotics worthless». Biofortified (em inglês). Consultado em 26 de agosto de 2025
- ↑ a b Halford, N. G; Shewry, P. R (1 de janeiro de 2000). «Genetically modified crops: methodology, benefits, regulation and public concerns». British Medical Bulletin (em inglês) (1): 62–73. ISSN 0007-1420. doi:10.1258/0007142001902978. Consultado em 26 de agosto de 2025.
…a transferência horizontal de um gene de material vegetal ingerido para bactérias nunca foi demonstrada, e não há indícios de que tenha ocorrido durante a evolução. A probabilidade de que isso possa ocorrer é, portanto, considerada tão baixa que não é relevante quando comparada com a ocorrência natural de genes de resistência a antibióticos.
- ↑ Netherwood, Trudy; Martín-Orúe, Susana M; O'Donnell, Anthony G; Gockling, Sally; Graham, Julia; Mathers, John C; Gilbert, Harry J (fevereiro de 2004). «Assessing the survival of transgenic plant DNA in the human gastrointestinal tract». Nature Biotechnology (em inglês) (2): 204–209. ISSN 1087-0156. doi:10.1038/nbt934. Consultado em 26 de agosto de 2025
- ↑ Käppeli, O (1 de julho de 1998). «How safe is safe enough in plant genetic engineering?». Trends in Plant Science (7): 276–281. doi:10.1016/S1360-1385(98)01251-5. Consultado em 26 de agosto de 2025
- ↑ Bakshi, Anita (janeiro de 2003). «Potential Adverse Health Effects of Genetically Modified Crops». Journal of Toxicology and Environmental Health, Part B (em inglês) (3): 211–225. ISSN 1093-7404. doi:10.1080/10937400306469. Consultado em 26 de agosto de 2025
- ↑ a b c Walters, Reece (2011). Eco crime and genetically modified food. Abingdon [England]: Routledge
- ↑ Gilbert, Natasha (1 de maio de 2013). «Case studies: A hard look at GM crops». Nature. 497: 24–26. Bibcode:2013Natur.497...24G. PMID 23636378. doi:10.1038/497024a

- ↑ Schütte, Gesine; Eckerstorfer, Michael; Rastelli, Valentina; Reichenbecher, Wolfram; Restrepo-Vassalli, Sara; Ruohonen-Lehto, Marja; Saucy, Anne-Gabrielle Wuest; Mertens, Martha (21 de janeiro de 2017). «Herbicide resistance and biodiversity: agronomic and environmental aspects of genetically modified herbicide-resistant plants». Environmental Sciences Europe. 29. PMC 5250645
 . PMID 28163993. doi:10.1186/s12302-016-0100-y
. PMID 28163993. doi:10.1186/s12302-016-0100-y
- ↑ Dalton, Rex (1 de novembro de 2008). «Modified genes spread to local maize». Nature (em inglês) (7219): 149–149. ISSN 1476-4687. doi:10.1038/456149a. Consultado em 14 de janeiro de 2022
- ↑ Agapito-Tenfen, Sarah; Lopez, Flor R.; Mallah, Narmeen; Abou-Slemayne, Gretta; Trtikova, Miluse; Nodari, Rubens O.; Wickson, Fern (2017). «Transgene flow in Mexican maize revisited: Socio-biological analysis across two contrasting farmer communities and seed management systems». Ecology and Evolution (em inglês) (22): 9461–9472. ISSN 2045-7758. PMC 5696427
 . PMID 29187982. doi:10.1002/ece3.3415. Consultado em 14 de janeiro de 2022
. PMID 29187982. doi:10.1002/ece3.3415. Consultado em 14 de janeiro de 2022
- ↑ Keese, Paul (20 de setembro de 2008). «Risks from GMOs due to Horizontal Gene Transfer». Environmental Biosafety Research. 7: 123–149. PMID 18801324. doi:10.1051/ebr:2008014

- ↑ «FDA: Genetically engineered fish would not harm nature». USA Today. 2012. Consultado em 28 de novembro de 2015
- ↑ Medicine, Center for Veterinary. «Animals with Intentional Genomic Alterations - AquAdvantage Salmon Fact Sheet». www.fda.gov. Consultado em 6 de fevereiro de 2019
- ↑ «Containing Genetically Modified Bacteria». National Institutes of Health (NIH). 9 de novembro de 2015. Consultado em 12 de setembro de 2018
- ↑ Lombardo, Luca (2014). «Genetic use restriction technologies: a review». Plant Biotechnology Journal (em inglês) (8): 995–1005. ISSN 1467-7652. doi:10.1111/pbi.12242. Consultado em 14 de janeiro de 2022
- ↑ Carpenter, Janet E. (1 de janeiro de 2011). «Impact of GM crops on biodiversity». GM Crops. 2: 7–23. PMID 21844695. doi:10.4161/gmcr.2.1.15086
- ↑ Tabashnik, Bruce E.; Brévault, Thierry; Carrière, Yves (junho de 2013). «Insect resistance to Bt crops: lessons from the first billion acres». Nature Biotechnology (em inglês) (6): 510–521. ISSN 1546-1696. doi:10.1038/nbt.2597. Consultado em 14 de janeiro de 2022
- ↑ Qiu, Jane (13 de maio de 2010). «GM crop use makes minor pests major problem». Nature (em inglês). ISSN 1476-4687. doi:10.1038/news.2010.242. Consultado em 14 de janeiro de 2022
- ↑ National Academies of Sciences, Engineering, and Medicine (2016). Genetically Engineered Crops: Experiences and Prospects. Agronomic and Environmental Effects of Genetically Engineered Crops (em inglês). Washington, DC: The National Academies Press
- ↑ Waltz, Emily (1 de setembro de 2009). «GM crops: Battlefield». Nature (em inglês) (7260): 27–32. ISSN 1476-4687. doi:10.1038/461027a. Consultado em 14 de janeiro de 2022
- ↑ a b c Hwang, Hyesun; Nam, Su-Jung (2 de janeiro de 2021). «The influence of consumers' knowledge on their responses to genetically modified foods». GM Crops & Food (em inglês) (1): 146–157. ISSN 2164-5698. PMC 7644159
 . PMID 33138666. doi:10.1080/21645698.2020.1840911. Consultado em 26 de agosto de 2025
. PMID 33138666. doi:10.1080/21645698.2020.1840911. Consultado em 26 de agosto de 2025
- ↑ Lucht, Jan (30 de julho de 2015). «Public Acceptance of Plant Biotechnology and GM Crops». Viruses (em inglês) (8): 4254–4281. ISSN 1999-4915. PMC 4576180
 . PMID 26264020. doi:10.3390/v7082819. Consultado em 26 de agosto de 2025
. PMID 26264020. doi:10.3390/v7082819. Consultado em 26 de agosto de 2025
- ↑ Dabrock P (dezembro de 2009). «Playing God? Synthetic biology as a theological and ethical challenge». Systems and Synthetic Biology. 3: 47–54. PMC 2759421
 . PMID 19816799. doi:10.1007/s11693-009-9028-5
. PMID 19816799. doi:10.1007/s11693-009-9028-5
