Peptídeo
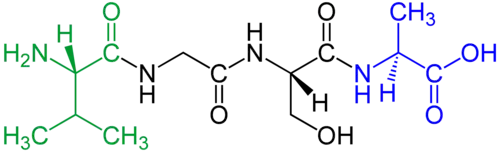
Os peptídios, peptídeos ou péptidos são biomoléculas formadas pela ligação de dois ou mais aminoácidos atrávés de ligações peptídicas, estabelecidas entre um grupo amina de um aminoácido, e um grupo carboxilo do outro aminoácido. Os peptídios são resultantes do processamento de proteínas e podem possuir na sua constituição 2 ou mais aminoácidos.
Os péptidos, do mesmo modo que as proteínas, estão presentes na natureza e são responsáveis por um grande número de funções, muitas das quais ainda não são conhecidas. A união de um baixo número de aminoácidos dá origem a um péptido. Uma classificação tradicional das cadeias peptídicas pelo seu tamanho é a seguinte:
- Oligopéptido: menos de 10 aminoácidos. Podem ser dipéptidos, tripéptidos, tetrapéptidos... consoante tenham dois, três, quatro aminoácidos, respetivamente.
- Polipéptido: mais de 10 aminoácidos.
- Proteína: mais de 100 aminoácidos.
As proteínas com uma só cadeia polipeptídica denominam-se proteínas monoméricas, enquanto as compostas por mais de uma cadeia polipeptídica são conhecidas como proteínas multiméricas. Os péptidos diferenciam-se das proteínas por serem mais pequenos (têm menos de dez mil ou doze mil daltons) e pelo facto de as proteínas poderem ser formadas pela união de vários polipéptidos e, por vezes, grupos prostéticos. No entanto, a distinção entre polipéptidos e proteínas é um tanto arbitrária e variável na literatura científica, dado que alguns autores colocam outros limites no número de aminoácidos (menos de 100), e o critério estrutural também não é definitivo. Não é claro o limite entre os polipéptidos grandes e as proteínas pequenas. Alguns autores usam os termos cadeia polipeptídica e até mesmo "polipéptido" com o significado de cadeia simples de aminoácidos independentemente do seu tamanho. Um exemplo de polipéptido é a insulina, composta por 55 aminoácidos e conhecida como uma hormona de acordo com a função que tem no organismo dos seres humanos. Entre os péptidos pequenos são exemplos o tripéptido glutatião e a hormona oxitocina, de nove aminoácidos. As peptonas são derivados do leite ou de carne digerida por proteólise.[1] Além de conterem pequenos péptidos, o material resultante inclui gorduras, metais, sais, vitaminas e muitos outros compostos biológicos. As peptonas são utilizadas como meios nutrientes para o crescimento de bactérias e fungos.[2]
Comportamento ácido/base dos péptidos
Uma vez que têm um grupo amina terminal e um carboxilo terminal; e podem ter grupos R ionizáveis, os péptidos têm um comportamento ácido/básico similar ao dos aminoácidos. Os péptidos, do mesmo modo que aminoácidos e proteínas são biomoléculas com um carácter anfótero que permitem a regulação homeostática dos organismos. É de destacar este comportamento nas enzimas, péptidos que funcionam como catalisadores biológicos das reações metabólicas, já que têm uma valência de atuação dentro de certos níveis de pH. Caso se ultrapassem, produz-se uma descompensação de cargas na superfície da enzima, que perde a sua estrutura e a sua função.
Reações químicas dos péptidos
São as mesmas que para os aminoácidos; isto é, as que dão o seu grupo amino, carboxilo e R. Estas reações (sobretudo as dos grupos amino e carboxilo) foram empregues para sequenciar péptidos.
Reações do grupo amino
Relativamente às reações do grupo amino, é muito interessante a reação com o reagente de Sanger para sequenciar, já que se tivermos o 2,4-dinitrofenil-péptido e o hidrolizarmos por hidrólise ácida, hidrolizar-se-ão todas as ligações peptídicas e obteremos o dinitrofenil do primeiro aminoácido da sequência, o NH2 terminal, mais o resto dos aminoácidos desagregados no meio. Com esta reação Sanger conseguiu sequenciar a insulina. Nesta reação, o núcleo colorido de dinitrobenzeno liga-se ao átomo de nitrogénio do aminoácido para produzir um derivado amarelo, o derivado 2,4-dinitrofenil ou DNP-aminoácido. O composto DNFB reage com o grupo amino livre da extremidade amino de um polipéptido, bem como com os grupos amino dos aminoácidos livres. A ligação C – N que se forma é geralmente muito mais estável do que uma ligação peptídica. Desta forma, fazendo reagir uma proteína nativa ou um polipéptido intacto com o DNFB, hidrolisando a proteína em ácido e isolando os DNP-aminoácidos coloridos, pode identificar-se o grupo amino terminal do aminoácido numa cadeia polipeptídica. O grupo amino terminal da lisina e alguns outros grupos funcionais das cadeias laterais também reagem com o DNFB. Contudo, depois da hidrólise, apenas o derivado do grupo amino terminal do aminoácido original terá o seu grupo α-amino bloqueado; assim mesmo, tais DNP-α-aminoácidos podem ser separados de outros derivados DNP por meio de procedimentos de extração simples. Com qualquer dos variados métodos cromatográficos poder-se-á identificar os DNP-α-aminoácidos.
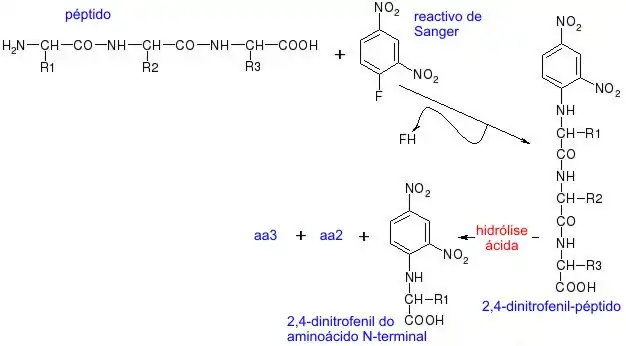
Mas este processo consome muita energia, já que, tendo o primeiro aminoácido, é necessário obter os demais rompendo por outras zonas. Isto evita-se com o procedimento de Edman (também é uma reação de aminoácidos): Como a ciclização se dá em condições ácidas suaves, forma-se inicialmente um péptido feniltiocarbamilado, as ligações não se rompem, e origina-se a feniltio-hidantoína do aminoácido NH2-terminal + o resto do péptido intacto.
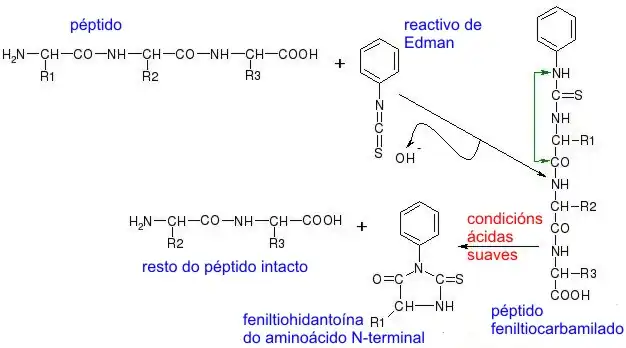
Separam-se ambos os compostos e deteta-se por cromatografia. Com o resto do péptido segue-se com o mesmo procedimento até se ter a sequência completa. Este método é conhecido como Degradação de Edman, e é a reação que usam os sequenciadores automáticos de proteínas. Mas estes sequenciadores só podem sequenciar os primeiros 20-30 aminoácidos, pelo que teremos de hidrolisar e seguir depois. Isto deve-se a o rendimento não ser de 100% e perdermos péptido aos poucos, e no final não nos restar. Apenas as enzimas conseguem um rendimento de 100%.
Reações do grupo carboxilo
Também podemos sequenciar começando pela extremidade carboxilo terminal, para o que se usam enzimas como a carboxipeptidase. É uma protease que hidrolisa as ligações peptídicas. Esta em concreto é uma exoprotease (ataca a proteína por uma extremidade) que ataca a extremidade carboxilo terminal. Empregam-se 2 tipos, a carboxipeptidase A e B. Catalisam a mesma reação, mas têm especificidade distinta. A A só rompe a ligação peptídica se o aminoácido carboxilo terminal é hidrofóbico. A B rompe-a se for básico. É necessário controlar muito bem o tempo de reação, já que quando se liberta um carboxilo terminal, o seguinte aminoácido converte-se no carboxilo terminal.
Reações dos grupos R
Relativamente às reações dos grupos R, existem muitos reagentes que reagem de forma específica com determinados grupos R (OH da serina, tiol da cisteína...). Isto é usado para ver qual o aminoácido essencial para o funcionamento da proteína. Dentro das reações dos grupos R, uma interessante sob o ponto de vista de isolamento e purificação de proteínas é a do grupo tiólico (SH) da cisteína, que é fortemente redutor. Na presença de O2 tem muita tendência a oxidar-se. Se há duas moléculas de cisteína; na presença de oxigénio, oxidam-se para originar uma molécula de cistina:
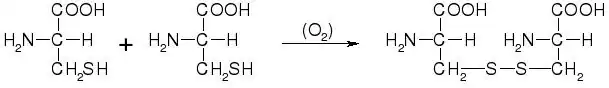
Isto ocorre frequentemente numa proteína, quando se dobra e duas moléculas de cisteína ficam próximas no espaço, gerando uma ponte dissulfureto. A ponte dissulfureto ocorre de forma natural, e deve formar-se para estabilizar a estrutura tridimensional da proteína. Contudo, pode ser que não deva ocorrer de forma natural, por exemplo, se há cisteínas essenciais expostas (necessárias para a funcionalidade). Quando isolamos uma proteína do seu ambiente natural, pomos a proteína na presença de oxigénio, com o qual esses grupos tiólicos podem oxidar-se, e a proteína perder a sua funcionalidade. Para evitar isto, nos meios de isolamento e purificação de proteínas adicionamos β-mercapto-etanol, cujo grupo tiólico é mais redutor do que o da própria cisteína; tem mais tendência a oxidar-se.
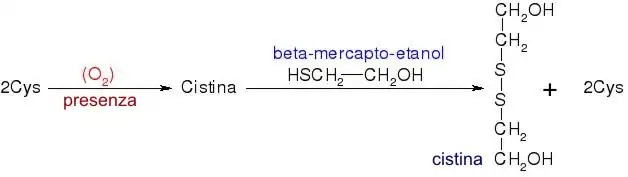
De modo que ao adicionar β-mercapto-etanol, este oxida-se e protege assim os grupos tiólicos da cisteína. Quando queremos estudar a composição de aminoácidos de uma proteína, temos de hidrolisá-la completamente, obtendo uma mistura de todo o conjunto de aminoácidos livres que constituem essa proteína. Para evitar, em toda esta manipulação, que as Cys que tivermos no meio se oxidem, temos de proteger o seu grupo tiólico adicionando como reagente iodoacetato:
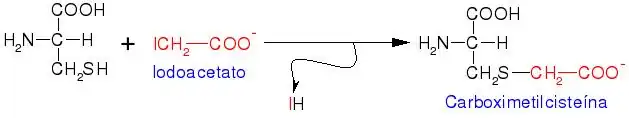
Assim transformamos a cisteína em carboximetilcisteína.
Péptidos não ribossómicos
A maioria dos péptidos sintetiza-se nos ribossomas ou são resultado da quebra de cadeias polipeptídicas maiores (péptidos do leite, peptonas), mas existem também péptidos que se originam enzimaticamente sem intervenção dos ribossomas, que se chamam péptidos não ribossómico. Os péptidos não ribossómicos são montados por enzimas que são específicas para cada péptido. O péptido não ribossómico mais comum é o glutatião, que faz parte dos mecanismos de defesa contra a oxidação da maioria dos organismos aeróbicos.[3] Outros péptidos não ribossómicos são muito mais frequentes em organismos unicelulares, plantas, e fungos e são sintetizados por complexos enzimáticos modulares chamados péptido não ribossómico sintetases, que são independentes dos ribossomas e dos ARNm.[4] Estes complexos podem conter muitos módulos diferentes para poder realizar um conjunto diverso de manipulações químicas sobre o produto que estão a formar, e cada módulo introduz um aminoácido.[5] Os péptidos não ribossómicos são frequentemente cíclicos ou ramificados e podem ter estruturas cíclicas muito complexas, mas são muito comuns também os péptidos não ribossómicos lineares. Este sistema tem similaridades com a maquinaria biossintética para produzir ácidos gordos e policétidos, e podem originar-se moléculas híbridas de péptido-policétido. A presença de um oxazol ou tiazol costuma indicar que o composto foi sintetizado desta maneira.[6]
Referências
- ↑ «UsvPeptides- USVPeptides is a leading pharmaceutical company in India». USVPeptides
- ↑ Payne JW (1976). «Peptides and micro-organisms». Advances in Microbial Physiology Volume 13. Col: Advances in Microbial Physiology. 13. [S.l.: s.n.] pp. 55–113. ISBN 9780120277131. PMID 775944. doi:10.1016/S0065-2911(08)60038-7
- ↑ Meister A, Anderson ME (1983). «Glutathione». Annual Review of Biochemistry. 52 (1): 711–60. PMID 6137189. doi:10.1146/annurev.bi.52.070183.003431
- ↑ Hahn M, Stachelhaus T (2004). «Selective interaction between nonribosomal peptide synthetases is facilitated by short communication-mediating domains». Proceedings of the National Academy of Sciences of the United States of America. 101 (44): 15585–90. PMC 524835
 . PMID 15498872. doi:10.1073/pnas.0404932101
. PMID 15498872. doi:10.1073/pnas.0404932101
- ↑ Finking R, Marahiel MA (2004). «Biosynthesis of nonribosomal peptides1». Annual Review of Microbiology. 58 (1): 453–88. PMID 15487945. doi:10.1146/annurev.micro.58.030603.123615
- ↑ Du L, Shen B (2001). «Biosynthesis of hybrid peptide-polyketide natural products». Current Opinion in Drug Discovery & Development. 4 (2): 215–28. PMID 11378961