Recombinação homóloga
A recombinação homóloga (HR - homologous recombination) é um tipo de recombinação genética, assim como a Recombinação Sítio-Específica e a Transposição, das quais se distingue pois é um fenômeno de troca de material genético a nível molecular que ocorre entre sequências precisamente correspondentes, de modo que nenhum par de bases é adicionado ou perdido durante o processo, ou seja, que carregam informações homólogas sem perdas ou ganhos de informação. [1] [2] [3] [4]
Acontece em eucariotos, durante a prófase I da meiose que forma os gametas, a troca física do material dos cromossomos parentais gera cromossomos recombinantes com uma nova sequência de informações, esse evento também é conhecido como crossing-over. Esse processo é fundamental para a evolução, diversidade genética, reparo de danos no DNA (deoxyribonucleic acid) e segregação cromossômica adequada durante a meiose. [1] [2] [3] [4] [5]
História
..png)
Em 1856, o monge Gregor Johann Mendel iniciou experimentos de cruzamento seletivo em plantas de ervilhas, Pisum sativum, para observar a hereditariedade de seus caracteres de geração em geração, como: a textura (lisa ou rugosa), a cor (verde ou amarela), a altura e a coloração das flores, em seu trabalho essas características são citadas como “fatores discretos”, e posteriormente foram denominadas por Wilhelm Johannsen em 1909 como “genes”.[6] Mendel não foi o único botânico de sua época a realizar experimentos quanto a da reprodução de plantas, muitos outros também foram instigados a realizar o mesmo a partir da afirmativa do botânico Nehemiah Grew de que através do pólen que determinados vegetais se reproduzem sexualmente. [4]
Após diversos cruzamentos, a anotação e triagem de seus resultados, Mendel foi capaz de descrever certos fenômenos, conhecidos como as “Leis da Hereditariedade”, como: dominância e recessividade, homozigoto e heterozigoto, segregação independente, e casos específicos, como as formas híbridas peculiares.[7] [6] Assim, Gregor Mendel formulou os princípios da hereditariedade, se consagrando em 1900 como “pai da genética moderna” após ter seus estudos redescobertos por três estudiosos europeus da época, Carl F. J. E Correns, Hugo M. de Vries e Erich von Tschermak-Seysenegg, tornando-se base para os estudos dos mesmos. [8]
A partir da redescoberta dos estudos de Gregor Mendel, a mais nova área de conhecimento denominada por William Bateson como “genética” em 1906, passou a receber muita atenção da comunidade científica e crescer exponencialmente com o tempo, com os estudiosos abrangendo a metodologia de Mendel a outros organismos, testando suas afirmativas, confirmando algumas e refutando outras.[6]
Ano |
Pesquisa |
|---|---|
| 1859 | Evolução pela seleção natural: Charles Robert Darwin |
| 1865 | Genética Mendeliana: Gregor Mendel |
| 1869-1900 | Descoberta dos ácidos nucleicos, nome e composição:
Johannes Friedrich Miescher, Richard Altmann e Ludwig Karl Martin Leonhard Albrecht Kossel |
| 1900 | Redescoberta dos estudos de Mendel: Carl Franz Joseph |
| 1902-1903 | Estrutura e comportamento dos cromossomos: Walter
Stanborough Sutton |
| 1905 | Descoberta dos cromossomos sexuais: Nettie Maria
Stevens e Edmund Beecher Wilson |
| 1909 | Herança citoplasmática em M. jalapa: Carl Franz Joseph |
| 1909 | Descoberta da ribose : Phoebus Aaron Theodore Levene |
| 1910-1935 | Bases da genética: Thomas Hunt Morgan , Alfred Henry |
| 1911 | Cromossomos carregam genes: Thomas Hunt Morgan |
| 1928 | Princípio transformante em bactérias: Frederick Griffith |
| 1929 | Descoberta da desoxirribose: Phoebus Aaron Theodore Levene |
| 1940 | Os estudos do material genético em vírus: Max Delbrück,
Salvador Edward Luria e Alfred Hershey |
| 1940-1945 | Quantificação de nucleotídeos e bases do DNA: Archer John
Porter Martin, Richard Laurence Millington Synge e Erwin Chargaff |
| 1943-1944 | DNA é o fator transformante: Oswald Theodore Avery Jr., |
| 1944 | Descoberta dos genes saltadores ou transposões: |
| 1944 | 1º Fago mutante é isolado: Salvador Edward Luria |
| 1949 | Mapeamento de genes em fagos: Alfred Day Hershey e
Raquel Rotman |
| 1952 | Genes são feitos de DNA: Alfred Day Hershey e Martha
Cowles Chase |
| 1953 | A estrutura do DNA é de uma dupla hélice: Rosalind Franklin |
| 1958 | Replicação semiconservativa do DNA: Matthew Stanley
Meselson e Franklin William Stahl |
| 1959 | Descoberta de anomalias nos cromossomos pela 1ª vez:
Jérôme Jean Louis Marie Lejeune |
| 1972 | 1º DNA Recombinante |
| 1973 | 1º Clone animal |
Em 1902 e 1903, Walter Stanborough Sutton foi capaz de descrever a estrutura e o comportamento dos cromossomos, tendo como objeto de estudo a espécie de gafanhoto Brachystola magna. [61] Ele afirmou que cada cromossomo apresenta duas cópias, ou seja, são cromossomos homólogos, que a quantidade de cromossomos nas células sexuais era metade do visto em células somáticas, e as células-filhas apresentavam o número completo de cromossomos das células parentais somadas, com duas bases (alelos) de informação para cada característica, um comportamento já levantado por Mendel no passado, porém Sutton comprovou esses comportamentos de maneira detalhada. [9] [10]

Em 1905, Nettie Maria Stevens e Edmund Beecher Wilson publicaram seus estudos, respectivamente, na Carnegie Institution of Washington e na Science, eles buscavam estudar os chamados “cromossomos acessórios” e uma possível relação entre eles e o determinante sexual, uma questão levantada por Clarence Erwin McClung em 1902, com isso a descoberta dos cromossomos sexuais foi atribuída à eles.[6] Nettie Stevens, utilizou sete espécies de insetos e descreveu a espermatogênese de cada um deles, o que tornou possível ela observar na espécie Tenebrio molitor a presença de 20 cromossomos nas células somáticas e germinativas tanto no macho quanto na fêmea, onde nas células do macho haviam 19 cromossomos grande e 1 pequeno enquanto na fêmea havia 20 cromossomos grandes, logo para Stevens, o cromossomo doado pelo macho seria o determinante sexual. [11] Edmund Wilson por sua vez, teve como objeto de estudo espécies de hemípteros, assim como Nettie Stevens ele observou diferentes números de cromossomos por espécie, e a diferença nos cromossomos acessórios em machos e fêmeas.[12] A partir da descoberta das bases da hereditariedade, da estrutura, comportamento dos cromossomos e do determinante sexual, novas pesquisas passaram a explorar os mecanismos e as possibilidades de descobertas a partir dessa base. Em 1909, Thomas Hunt Morgan, Alfred Henry Sturtevant e Calvin Blackman Bridges dão início a uma série de estudos com moscas (Drosophila melanogaster). Morgan iniciou uma investigação da presença de olhos brancos em alguns machos, algo incomum nas moscas, e acabou por descobrir que esse fenótipo está associado ao cromossomo sexual, ou seja, os genes estão localizados nos cromossomos. Calvin passou a estudar o aparecimento de fêmeas com olhos brancos descrevendo assim uma não disjunção dos cromossomos, sexuais onde os dois cromossomos X da fêmea não se separaram na anáfase I, conferindo um genótipo XXY à prole. Sturtevant foi capaz de mapear os genes das Drosophilas após determinar as taxas de
recombinação dos genes no cromossomo X, demonstrando que as taxas de recombinação estão associadas à distância física entre os genes. As inferências descritas por Morgan, Sturtevant e Bridges tornaram-se os princípios físicos da hereditariedade e, consequentemente, foram essenciais para o entendimento da recombinação genética, da mutação genética e da evolução dos organismos. [13] [2] [4] [6]

Em 1952, Alfred Day Hershey, com Martha Cowles Chase descreveu que genes são feitos de DNA, reforçando as afirmações dos estudos de Oswald Theodore Avery Jr., Colin Munro MacLeod e Maclyn McCarty de 1943-1944, onde concluíram a partir da pesquisa de Frederick Griffith de 1928, que o DNA é o material transformante das células bacterianas de Streptococcus pneumoniae que ele havia estudado.
Em 1953, com base no trabalho de Rosalind Franklin, os pesquisadores James D. Watson e Francis Crick conseguiram descrever a estrutura dupla hélice do DNA, abrindo portas para um maior aprofundamento dos estudos voltados às características genéticas, à hereditariedade, à recombinação, à evolução, à mutação genética, processos e problemas associados ao DNA. [2] [6]
Mecanismo Molecular
Mecanismo molecular é a base, ao nível molecular, de todo o processo que irá acontecer em algo biológico. A recombinação homóloga (HR — homologous recombination), em síntese, é um processo fundamental da genética que envolve a troca de genes de moléculas que compartilham sequências semelhantes (homólogas). Sendo o mecanismo molecular quem cuida e organiza tudo o que deve ser feito para que a recombinação homóloga seja realizada com êxito no final.
No decorrer do texto, há um destaque maior no caminho, isso é, nas etapas, proteínas e enzimas chaves. Ou seja, é possível dividir em cinco etapas essenciais, sendo elas a iniciação pela Quebra do Filamento Duplo (DSB — Double-Strand Break), erosão das extremidades, invasão do filamento e busca homóloga, síntese de DNA (deoxyribonucleic acid) e formação de heteroduplex e resolução do crossover, onde para que o seu funcionamento seja eficaz, são necessárias algumas proteínas e enzimas em específico, como: Spo11, RAD51, Dmc1, DNA Polimerase e DNA Ligase. [1] [14] [2] [15] [16] [5]
Etapas do Processo
O modelo mais aceito para explicar a recombinação homóloga é o Modelo de Reparo por Quebra de Dupla Fita (DSBR — Double-Strand Break Repair).[17] O processo é iniciado por uma quebra em uma das moléculas de DNA e prossegue com a troca de fitas, conforme ilustrado nas figuras originais.

Quebra da Dupla Fita e Processamento
- O processo inicia-se com um rompimento de dupla fita (DSBs) em uma das moléculas de DNA (o "receptor") e, em seguida, enzimas como a Spo11 (em eucariotos) catalisam essa quebra.[18]
- As extremidades da quebra são então "lixadas" por exonucleases, que digerem as fitas 5' para gerar extremidades 3' de fita simples, um passo conhecido como ressecamento (resection).
Invasão de Fita e Formação da Junção de Holliday
- Uma das extremidades 3' de fita simples "invade" a molécula de DNA homóloga intacta (o "doador"). Esta etapa é mediada por proteínas como RAD51 (RecA em bactérias), que formam um filamento que procura e pareia com a sequência complementar no DNA doador.[19]
- Esta invasão forma uma estrutura intermediária crucial denominada Junção de Holliday, uma junção ramificada de quatro braços onde as fitas de DNA são trocadas entre as duas moléculas.
Resolução da Junção
- As junções de Holliday devem ser clivadas ("resolvidas") para separar as duas moléculas de DNA. Esta determinação é realizada especificamente por enzimas chamadas resolvases (como a RuvC em E. coli). [20]
- Procedendo da orientação em que a fragmentação ocorre, o resultado pode ser:
- Produtos de Crossover: Onde há troca física de segmentos de DNA entre os cromossomos homólogos. Esse evento, visível ao microscópio, é responsável pela recombinação genética que mistura alelos maternos e paternos.
- Produtos de Não-Crossover: Onde preserva-se a estrutura original dos cromossomos, sem troca de segmento aparente. Todavia, ainda assim é possível ocorrer uma transferência de informação em pequena escala, conhecida como conversão gênica. [20] [21] [22] [16] [23] [8] [24]
Proteínas e Enzimas Chave
A recombinação homóloga (HR) começa com uma quebra de dupla fita (DSBs). O primeiro passo é processar essa quebra para criar as extremidades de fita simples (ssDNA) necessárias para buscar por homologia.
- O complexo MRN (Mre11- RAD50 - Nbs1) é o primeiro a se ligar à quebra de dupla fita. Caso a atividade se quebre (por conta da proteína RAD50). O Mre11 atua como uma nucleotidase, dando início ao processo de recessão - a degradação de uma das fitas para expor uma cauda de DNA (deoxyribonucleic acid) de fita simples no sentido 3’ que é elemento muito importante para a próxima fase.
- As proteínas de recessão (Exo1, Sgsl, BLM, Dna2) continuam a recessão do DNA que é iniciada pelo complexo MRN, gerando caudas 3’ de ssDNA mais prolongadas. Este processo é regulado, com essa recessão podendo gerar um grande trecho de ssDNA (que é o molde principal) que é coberto pelas proteínas, protegendo a degradação e preparam para a fase de busca homóloga.
- A homologia e invasão da fita (coração do HR) são as principais características, onde se encontra a fita simples do DNA recém-formada que acaba “invadindo” a molécula de DNA homóloga buscando sequência complementar. RecA (em procariontes)/ RAD51 (em eucariotos) é uma proteína central da HR que liga ao ssDNA 3’ coberto pelas proteínas de ligação a fita simples, formando um filamento nucleoproteico. O filamento RAD51 é ativo buscando por homologia na dupla fita de DNA intacta, depois de encontrado na região homóloga, é catalisada a invasão de fita, deslocando apenas uma das fitas do molde, formando um intermediário de 3 fitas chamado de alça D (D-loop). É o momento em que a informação genética é “copiada” do molde intacto para a fita danificada.
- O Rad 54 é uma helicase que coopera com a RAD51. A RAD54 usa energia do ATP para facilitar a formação da alça D, ajudando a remover a RAD51 do DNA depois da invasão de fita, permitindo começar a síntese de DNA.
- A DNA polimerase usa a cauda 3’ quando é invadida primeiro, começando a síntese de DNA, copiando informações perdidas da fita molde intacta, restaurando o DNA que foi degradado durante a recessão. Já a DNA ligase é uma enzima fundamental que fecha as “quebras” no esqueleto de açúcar-fosfato do DNA, selando fitas recém-sintetizadas que conectam a molécula original.
- RuABC (em procariotos) / Resolvases (com GEN1 em eucariotos) são enzimas de resolução do intermediário de recombinações, depois da síntese de DNA, formando estruturas em formas X, chamadas de Junção De Holliday. As Resolvases (gene GEN1) atuam como endonuclease, clivando, determinando se haverá ou não uma troca de marcadores genéticos, se o complexo RuvABC/GEN1 não for clicado, o complexo Sgs1/BLM pode “dissolver” estas junções de Holliday através da atividade helicase. Ela transforma a fita simples, que é vulnerável, em uma ferramenta de busca e pareamento, sem ela a etapa crucial de invasão de fita não ocorreria, com isto a célula ficaria vulnerável a mutações e rearranjos cromossômicos, podendo levar a doenças graves, inclusive o câncer. [25]
Funções e Importância Biológica
A recombinação homóloga (HR - homologous recombination) é um mecanismo refinado fundamental para manutenção dos organismos para além de sua função principal, que é a troca de material genético entre sequências homólogas. A evolução, mutação, e replicação, reparo e manutenção do DNA (deoxyribonucleic acid), etc, se relacionam à recombinação homóloga em algum ponto de seus processos, porém a recombinação homóloga também está relacionada a eventos de instabilidade no genoma, ocasionando repercussões negativas à saúde do organismo, como o câncer.
A recombinação homóloga (HR) atua no reparo de quebras de cadeia dupla de DNA (DSBs - DNA double-strand breaks), ligações cruzadas entre fitas (ICLs - interstrand crosslink) e lacunas de DNA, na geração de diversidade genética na meiose (via segregação independente e crossing-over), na segurança da segregação cromossômica (descarte de recombinações desfavoráveis), restaurando forquilhas de replicação de DNA (manutenção da replicação), e entre outras funções. Entretanto, a mutação do gene BRCA2, gene associado a supressão de cânceres, pode causar a deficiência da recombinação homóloga (HRD - homologous recombination deficiency) que leva ao desequilíbrio do mecanismo de replicação do DNA levando ao aumento de mutações. O comprometimento das vias de reparo do DNA por recombinação homóloga (HR) pode levar aos cânceres de próstata, ovário, mama e pâncreas. [26] [27] [5] [28] [29] [30]
Reparo de Quebras de DNA de Dupla Fita

Quebras de dupla fita de DNA — causadas por problemas de forquilha, recombinação ou químicos e radiação iônica — são consideradas como fonte de estresse no processo de duplicação, sendo barreiras físicas que atrapalham o funcionamento da forquilha de replicação, as induzindo ao colapso, aumentando as chances de mutações e o acúmulo de ssDNA — DNA que foi solto porém não copiado.[31] Duas das soluções primárias para lidar com o estresse é o método de ligação de extremidades não homólogas (NHEJ), modo rápido e propenso a erros onde a união é feita diretamente das quebras, e a recombinação homóloga, uma forma segura usando o cromossomo homólogo como molde, com a associação de componentes como proteínas de RAD51, BRCA1 e BRCA2, que são de extrema importância para o bom funcionamento da recuperação da fita e suas deficiências são frequentemente associadas a doenças. [1] [32]
O modelo atualmente aceito de explicação do processo é o de Szostak et al. (1983), que propõe que a reparação da dupla fita é realizada iniciando na detecção da quebra pelo complexo MRN, que detecta as extremidades danificadas e faz o recrutamento de proteínas como o ATM, que, por sua vez, faz a ativação de outras proteínas para lidar com o dano, entre elas a BRCA1. Uma das partes do MRN, a Mre11, também realiza “cortes” nas pontas, deixando-as livres de empecilhos para um melhor reparo.
Para finalizar a preparação, uma exonuclease, Exo1, ou uma endonuclease, DNA2, realizam a degradação da fita 5’, deixando apenas uma cauda de fita simples 3’, que é coberta com proteína, a RPA, para evitar degradação, que é posteriormente substituída pela RAD51, com o auxílio da BRCA2 e RAD52. Essa parte livre é, posteriormente, utilizada como primer para a síntese.
A enzima RAD51 é a peça central da recombinação, formando um nucleofilamento ativo — uma estrutura em forma de hélice — ao redor da fita, que busca por estruturas intactas com um bom pareamento. Esses requerimentos, quando cumpridos, desencadeiam a formação da junção de D-loop, que acontece com a invasão de uma dupla fita pela cauda 3’, onde a original forma uma “alça”, o loop, e permite o primeiro contato estável entre a fita invasora e a complementar e, logo, seu uso como molde.
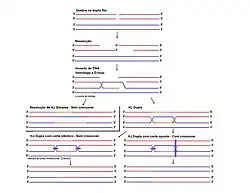
O resultado é a junção simples de Holliday, o ponto de encontro e conexão entre as duas fitas, que usam a ponta quebrada 3’ como ‘prime’ e estendem a fita danificada para recuperar o que se perdeu na quebra, por conta disso a junção é chamada de móvel, pois o local de conexão migra conforme a complementar é formada pela DNA polimerase e, depois de terminar a formação, a conexão se dissolve e essa fita restaurada se conecta novamente com seu par original, onde agora essa nova parte será usada como molde. Caso a outra extremidade quebrada também invada a dupla homóloga, a situação é denominada de dupla junção de Holliday, e, nesse caso, a cópia da fita não invasora é feita usando a fita deslocada como molde e sua resolução é feita por meio também de dissolução por meio de helicases ou por dois possíveis tipos de corte: os cortes em planos idênticos, onde não há crossing over, e em planos opostos, onde o crossing over acontece.
Esses pontos são importantes para um bom alinhamento e correção das fitas e, para resolver as junções, são usados dois métodos: corte ou dissolução, onde, no primeiro, as resolvases realizam cortes que podem gerar trocas de segmentos (crossovers) ou não dependendo do sentido do corte, e, no segundo, na junção dupla dois pontos se chocam um com o outro e são dissolvidos. Por fim, o fim do processo de reparo consegue restaurar o funcionamento de forquilhas, promover a estabilidade cromossômica e a proteção de telômeros. [1] [33] [34]
Geração de Diversidade Genética na Meiose
A geração de diversidade genética na meiose é um processo ligado a recombinação meiótica, no qual fornece uma evolução e sobrevivência de espécies que fazem reprodução assexuada. À princípio tal recombinação origina um produto
meiótico através de novas combinações dos alelos que foram levados pelos genótipos haploides e que se uniram para formar o meiócito (a célula diploide
que sofre meiose). Tanto a recombinação quanto a diversidade genética dependem de duas fases importantes: segregação independente de cromossomos e o crossing over.
Segregação independente (segundo Mendel):
Mendel tentou explicar um mecanismo biológico, o que veio a se tornar a Segregação Independente ou 2º Lei de Mendel, através de testes com cruzamento de ervilhas. Ele concluiu que diferentes pares de genes se distribuem independentemente durante a formação dos gametas. [8]
| AA | aa | |
|---|---|---|
| BB | AABB | aaBB |
| bb | AAbb | aabb |
A segregação independente de pares de genes localizados em diferentes cromossomos é totalmente explicada pelo comportamento dos cromossomos durante a meiose.

Todo o processo começa com a organização das moléculas de DNA, onde o cromossomo é criado. O ponto-chave da atuação dos cromossomos está na fase Metáfase I — em que os cromossomos homólogos se alinham na placa metafásica e estabelecem a base física para a segregação independente — e na fase Anáfase I — onde os pares de cromossomos homólogos se separam (evento chamado disjunção dos homólogos) e se movem em direção aos polos opostos da célula, contribuindo para a variação genética dentro da segregação.
Crossing over:
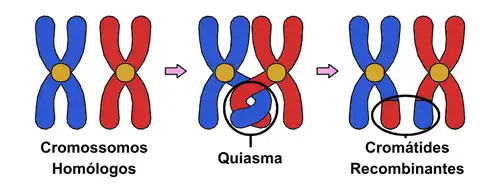
O crossing over é uma característica fundamental na meiose, pois gera a recombinação de genes ligados ao mesmo cromossomo, essencial para a garantia e melhoria da variação genética.
Nele ocorrem alguns processos como a Quebra do Filamento Duplo (DSBs) (primeiro evento tanto para o reparo de DNA quanto para o crossover meiótico), Erosão das Extremidades (depois da quebra a célula erodi/destrói as extremidades 5’ do DNA, deixando ambas as extremidades 3’ expostas em filamentos simples), Invasão do Filamento e Reconhecimento Homólogo (um filamento exposto se liga a um cromossomo homólogo vizinho que o complete), Síntese de DNA e Formação de Heteroduplex (a ponta 3' livre do filamento exposto utiliza o DNA invadido como molde para iniciar a síntese de um novo DNA, porém pode ocorrer o que chamamos de heteroduplex — quando uma molécula de DNA tem um par de nucleotídeos incorretamente pareados) e Resolução e Crossover Final (a síntese de DNA preenche os espaços, e os filamentos são selados, resultando em uma estrutura peculiar com duas junções de filamento simples, chamadas junções de Holliday). A formação final desse processo é o quiasma (estrutura em formato de cruz), crucial para manter os cromossomos homólogos conectados e estabilizados. [1] [17] [35] [2] [36] [37] [38]
Outras Funções
Segurança na segregação cromossômica:
A segurança na segregação cromossômica é crucial a partir do momento em que a sua falha leva a anomalias no número ou na estrutura dos cromossomos, resultando em distúrbios/doenças. A segurança é garantida por mecanismos celulares da divisão das células somáticas (mitose) e da formação dos gametas (meiose).
A importância desse processo para o crescimento celular normal é ilustrada pela observação de que muitos tumores são caracterizados por um estado de desequilíbrio genético resultante de erros mitóticos na distribuição dos cromossomos para as células-filhas.
No crossing over, como mostrado, os segmentos homólogos de DNA são trocados entre as cromátides não irmãs (não idênticas) de um par de cromossomos homólogos, garantindo assim que nenhum dos gametas produzidos pela meiose seja idêntico ao outro. A aneuploidia, por exemplo, é uma não disjunção cromossômica (na qual dois cromossomos ou duas cromátides vão para um polo e não para outro) que pode ocasionar um distúrbio cromossômico no autossomo inteiro: trissomia do 21 (Síndrome de Down), além de outros. Por isso, o crossover é importante para a manutenção do pareamento, evitando esses erros nas ligações gênicas.
Geração de diversidade em células B:
A diversidade dos linfócitos B é gerada pela recombinação V(D)J, um tipo específico de recombinação somática que utiliza enzimas especializadas denominadas recombinase V(D)J, que reconhece as sequências sinal de recombinação no DNA que ataca cada segmento gênico que deve ser unido. (ALBERTS, 2017, p.1320). A perda e o ganho de nucleotídeos aleatórios, que ocorre na V(D)J, nos locais de união, são denominados diversificação juncional, e em muitos casos, isso desloca a fase de leitura, produzindo genes não funcionais e, nesse caso, a célula B falha na produção de uma molécula de imunoglobulina funcional e, como consequência, morre na medula óssea. [1] [39] [40] [2] [41] [42] [43] [44]
Regulação do Processo
A recombinação homóloga (HR - homologous recombination) é rigidamente controlada para assegurar que ocorra no momento e local certos, prevenindo rearranjos genômicos nocivos ao indivíduo. A regulação do ciclo celular ocorre em sua atividade máxima nas fases S e G2, quando uma cópia irmã do DNA (deoxyribonucleic acid) está disponível como molde para realizar um reparo de alta fidelidade. Essa via é reprimida na fase G1. Os checkpoints de DNA ocorrem quando o DNA evidencia pontos de verificação que congelam o ciclo celular e convocam as maquinarias de reparo, incluindo a recombinação homóloga. A BRCA1 e BRCA2, são proteínas supressoras de tumor e reguladoras essenciais do processo de segurança do genoma, atuam convocando a RAD51 aos sítios de dano. As mutações nesses genes levam à perda da estabilidade genômica e aumentam o risco de cânceres, como de próstata, mama, ovário e pâncreas. [45] [46] [29] [47] [48] [5]
Evolução e Conservação
A primeira função é conservada da recombinação homóloga é o reparo de quebras de fitas duplas (DSBR - Double-Strand Break Repair). As DSBs (Double-Strand Breaks) são eventos catastróficos para uma célula, que ocorrem por conta da radiação, estresse oxidativo ou até mesmo falhas de replicação. Caso não sejam reparados corretamente, pode acontecer o rearranjo cromossômico, instabilidade genômica, morte celular ou chegar em casos extremos como o câncer em eucariotos.
A recombinação homóloga (HR - homologous recombination) usufrui de uma sequência homóloga (geralmente a cromátide irmã assim que acontece a replicação) como molde para o DNA (deoxyribonucleic acid) ser refeito, isso só ocorre quando o DNA é quebrado ou danificado. Isto faz com que seja um reparo eficiente e sem chance de cometer erros. Por isso, o modelo mais aceito para o reparo é SDSA (Synthesis-Dependent Strand Annealing), principalmente em reparo mitótico.
A maquinaria central da HR, como proteínas da família RocA (em procariotos) / RAD51 (em eucariotos), é conservada através dos domínios da vida. Desta forma, sugere-se que a capacidade para reparar o DNA com precisão é uma característica fundamental que surgiu há muitos anos, dentro da história evolutiva, e foi mantida sob forte pressão seletiva. A perda nestas vias (como proteínas) está diretamente ligada a síndromes de instabilidade e predisposição ao câncer.
A HR é importante para resolver problemas que surgem na forquilha de replicação. Quando a polimerase encontra um dano, que pode fazer com que a forquilha entre em colapso, a HR ajuda a reconstruir esta forquilha de replicação de forma correta e mantendo a replicação do genoma.
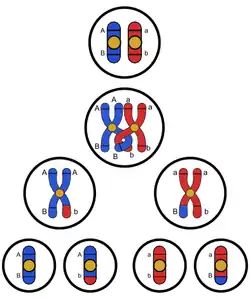
O aumento da diversidade genética é uma permuta de segmentos de DNA entre os cromossomos homólogos (um de origem paterna e outro de origem materna) que cria novas combinações de alelos que não existiam em nenhum lugar. Este é o motor da variabilidade genética.
- Exemplo: Se um cromossomo paterno tem alelos “A” e “b”, e o materno tem “a” e “B”, a recombinação pode gerar cromossomos “AB” e “ab”.
A garantia da segregação são os sítios de crossing-over que são essenciais para manter os cromossomos homólogos pareados até a Anáfase I. Sem a HR, pode causar aneuploidia e gametas inviáveis, caso os homólogos separem incorretamente. Sendo assim, a HR garante a fertilidade e a transmissão correta do material genético.
A nova mistura de alelos que HR proporciona possibilita que a seleção natural atue em combinações genéticas mais favoráveis, que influenciam na aceleração da capacidade de uma população se adaptar a qualquer mudança ambiental. Ou seja, a HR permite que mutações benéficas que surgiram de formas diferentes individuais sejam reunidas em apenas um genoma de forma rápida.
Seleção contra o reparo “perigoso” ocorre caso a recombinação homóloga seja desregulada, podendo causar recombinações entre sequências não homólogas (quando sequências repetitivas dispersas, ou recombinação ilegítima), levando a duplicações, deleções e translocações cromossômicas. Com a evolução, criaram-se mecanismos que limitam a HR a sequências homólogas, dando prioridade à integridade genômica.
A melhor seleção, para obter uma maior frequência de variação, é a seleção sexual, que favorece organismos que podem gerar uma proteína genética mais diversificada, conferindo maior capacidade de sobrevivência da espécie. O avanço evolutivo fez com que exista uma estabilidade meiótica e o aumento da variabilidade, acelerando desta forma a capacidade das espécies em se adaptarem e sobreviverem ao longo dos anos, comprovado com a estabilidade de curto prazo (reparo) e adaptatividade de longo prazo (evolução). [25]
Aplicações em Biotecnologia e Pesquisa
Esse mecanismo é fundamental para variabilidade genética, reparo de DNA (deoxyribonucleic acid) e manutenção da estabilidade genômica. A recombinação homóloga vem sendo muito usada nas pesquisas científicas e biotecnologias para precisão em manipulações genéticas.
Pesquisas biomoleculares possibilitam a remoção ou inativação de genes específicos para analisar suas funções fisiológicas (knockout gênico), o que é extremamente útil no estudo de doenças humanas. Ademais, a análise das conversões gênicas e recombinações intracromossômicas permite a compreensão dos processos de recombinação natural, reparo do DNA e evoluções geneticamente programadas. Em resumo, organismos modificados por (HR - homologous recombination) auxiliam na reprodução de doenças hereditárias ou tipos específicos de câncer, o que facilita a identificação de novos alvos para tratamento.
Já na engenharia genética e na biotecnologia, temos a possibilidade de inserção controlada de genes em locais específicos do genoma de plantas, animais ou microrganismos, concedendo novas características como resistência a pragas ou herbicidas em plantas e a produção de proteínas terapêuticas ou hormônios em bactérias ou células eucarióticas. Ademais, tendo a recombinação homóloga como base, é possível alterar nucleotídeos específicos no DNA, viabilizando modificações precisas como o silenciamento gênico, a alteração de sequência de aminoácidos em proteínas e a modificação de elementos regulatórios. Por fim, na terapia gênica é possível corrigir mutações genéticas em células humanas, oferecendo um jeito meticuloso de consertar o genoma, reduzindo efeitos off-target.
É importante notar também que estudos em microrganismos e transferências genéticas também avançaram, afinal, a troca de DNA entre células receptoras e doadoras tornou-se mais oportuna, o que contribuiu para a evolução adaptativa, geração de resistência antibiótica e produção de metabólitos bioativos.
Em outras palavras, é possível afirmar que a recombinação homóloga é uma ferramenta essencial para a biotecnologia e pesquisas de maneira geral, pois permite intervenções genéticas precisas e seguras. Podendo ser aplicada tanto em estudos básicos de biologia molecular, quanto em desenvolvimento de terapias genéticas, vacinas, plantas e animais transgênicos, sendo indispensável para o avanço da ciência e da medicina moderna. [39] [20] [21] [49] [16] [50]
Implicações na Saúde Humana
O que causa a implicação à saúde é principalmente a deficiência de reparo por recombinação homóloga (HRD - homologous recombination deficiency). Isto acontece quando as proteínas essenciais para a recombinação homóloga (HR - homologous recombination) (como BRCA2, RAD51, entre outras) estão misturadas ou não funcionam da maneira certa. Sem a HR, as células precisam usar outras vias de reparo e têm mais chances de cometer erros, como a ligação de extremidades não homólogas (NHES). Como resultado, a instabilidade genômica, se manifesta como um aumento da taxa de mutações, rearranjos e alterações estruturais do DNA (deoxyribonucleic acid). [51]
Esta instabilidade genômica é uma característica marcante do câncer, que se dá pelo acúmulo descontrolado de danos e mutações que podem silenciar os genes do tumor ou ativar os oncogenes, levando a uma proliferação celular desregulada que se dá no processo da carcinogênese.
- Os genes BRCA1 e BRCA2 são exemplos clássicos, as mutações herdadas (germinativas) conferem um risco a mais para o câncer de mama, próstata, ovário e pâncreas. Isto se dá porque ambos são proteínas cruciais ao coração do maquinário de HR. Quando o alelo é herdado mutado, a célula precisará de um segundo evento (mutação somática) para perder totalmente a função de HR.
- A enzima PARP (Poli-ADP Ribose Polimerase) é essencial para o reparo de quebras de fita simples. Em uma célula normal, caso a PARP seja inibida, o dano na fita simples acaba se transformando em quebra de fita dupla, que é automaticamente reparada pela HR. No entanto, o efeito letal ocorre em uma célula tumoral que já tem HRD (não consegue fazer HR), a inibição da PARP leva ao acúmulo de quebras de fita dupla. Como o tumor não tem nenhuma das duas vias de reparo funcionando, o dano ao DNA é maior que a célula tumoral, levando à morte celular. Dessa forma, a identificação da HRD acontece por meio da análise de mutações em BRCA e de "cicatrizes genômicas" que se tornaram um biomarcador crucial para selecionar pacientes com câncer de ovário, mama e próstata que terão resultados positivos com o tratamento com inibidores de PARP (como o olaparib e o rucaparibe). [25]

Doenças Associadas a Defeitos em Recombinação Homóloga
A recombinação homóloga (HR) é um método para a resolução de erros e quebras na sequência de DNA e diversas partes do seu processo podem sofrer mutações e ocasionar a falta desse processo — e logo a não manutenção das fitas danificadas —, podendo causar mutações e erros, levando a situações como a predisposição de doenças oncológicas ou a Síndrome de Down.[52]
Câncer.
O câncer é uma doença originada do excesso de mutações celulares, causadas por instabilidade genômica, que afetam seu funcionamento, divisão e outros, onde a célula afetada adquire vantagem em proliferação e se espalha rapidamente pelos tecidos do corpo. Essa instabilidade se origina por defeitos genéticos em, principalmente, BRCA1 e BRCA2, já que, sem recrutamento ou posicionamento de proteínas essenciais para o reparo de quebras, os métodos de reparo principal passam a ser a junção de extremidades não homóloga, o que acumula sequências errôneas ao longo das divisões. [1]
O p53 é um supressor tumoral que protege o genoma, induzindo o reparo celular ou apoptose caso o dano ao DNA aconteça. [36] Essa proteína é de extrema importância no processo imune antitumoral e está ligada ao funcionamento da BRCA1, pois a BRCA1 serve como um sensor de dano, que ativa e estabiliza p53 e seu funcionamento. Quando há ausência desse sensor de dano, o p53 não tem fosforilação e não realiza o controle do reparo, causando danos letais à instabilidade genômica. Outro ponto é que os BRCA são associados a casos de câncer com base hereditária de heterozigose, a manutenção de telômeros e a diversidade genética presente nos tumores, o que adiciona ainda mais aos perigos da mutação do grupo BRCA. [1]
A RAD51 também é parte essencial no câncer, mas de forma negativa, pois ajuda na adaptação metabólica das células cancerígenas e sua melhor locomoção, promovendo a transição epitélio-mesenquimal, além de conferir resistência a tratamentos quimioterápicos por estarem muito presentes nessas células. [53] Além disso, outros genes que participam da recombinação homóloga também têm capacidades cancerígenas caso haja deficiência, podendo se comportar de forma quase idêntica aos BRCA, usando como base para uma escala do quão “BRCAness” um gene é — ou seja, o nível de semelhança. Um dos casos é o do gene ATM, que causa mutações hereditárias que aumentam em até quatro vezes o risco de câncer. [54] [53]
Trissomia 21
A Síndrome de Down é uma condição onde há a presença de um cromossomo extra nas células do corpo, totalizando 47 no total. Através de uma pesquisa realizada em 2023, que buscava entender a pré-disposição precoce de leucemia por pessoas com trissomia 21, mostrou que as células sanguíneas do grupo são naturalmente mais instáveis. Essa instabilidade celular foi associada ao gene DYRK1A, do cromossomo 21 — logo, super expressa em T21 —, que diminui a recombinação homóloga e, igualmente, forçando o corpo a seguir por caminhos como a ligação não homóloga para reparos. [55] Outro trabalho também mostra que, conforme o tempo, a capacidade de separação cromossômica diminui, prejudicando a recombinação genética homóloga, ocasionando em más recombinações e em não disjunção, a principal causa da T21. [56]

Estratégias terapêuticas
O uso de recombinação homóloga no tratamento de doenças é de extrema importância e relevância, pois se utiliza de uma parte já proveniente do paciente, sendo ela modificada de modo que o necessário se muta, o restante se mantém igual, sem riscos, e a recuperação da modificação é feita sem altas chances de dano mutagênico e garantindo a eficácia do tratamento.
Terapia gênica.
A recombinação homóloga é usada de forma terapêutica em tratamentos por terapia gênica de diversas doenças, sendo alternativas essenciais para condições como anemia falciforme, uma doença causada por mutação de hemoglobina. Nesse caso, seu tratamento é comumente feito por terapia gênica por lentivírus, porém, pesquisas em que foi testado o método por recombinação homóloga com células-tronco embrionárias se mostraram muito mais eficazes e sem riscos de mutagênese.[57]
A escolha dos componentes do tratamento são sempre semelhante e acontece pois, além de evitar mutagênicos devido ao lentivirus, a recombinação homóloga permite a correção do que é necessário, mas preservando o controle natural do gene, enquanto as células-tronco podem ser manipuladas e depois inseridas novamente. Por isso, mesmo a ação da recombinação em alguns casos, como em células hematopoiéticas, não sendo tão funcional, ainda são pesquisados e utilizados métodos que melhorem sua eficácia para seu uso regular. [58] [59]
Edição gênica.
A edição gênica é uma tecnologia onde se pode alterar o DNA de um indivíduo, seja para retirar, adicionar ou mudar a expressão de genes, com o uso principal focado em medicina. Seu principal sistema de edição atual é o CRISPR-Cas9, que utiliza um RNA (ribonucleic acid) guia, que serve para encaminhar a enzima editora, a Cas9, até o gene desejado. Um dos principais problemas apresentados no sistema é uma boa probabilidade de que, após os cortes, as fitas se juntem por junção de extremidades não homólogas, criando mutações e impedindo que o gene drive — mecanismo que força a propagação de um gene específico — siga para as próximas gerações e, logo, que a edição seja eficaz. [60]
Como esperado, é necessário o acontecimento da recombinação homóloga para o bom funcionamento e eficácia do sistema de edição, assim, Tran et al., (2019) descobriram que o sistema mais simples e eficaz possível para aumentar as chances desse acontecimento é deixar os componentes necessários para o início da recombinação junto ao Cas9, fundidos diretamente nele, na gRNA, forçando essa proximidade.[61] Posteriormente, foi descoberto a TREX1, uma enzima que tem a capacidade de degradar a fita molde, atrapalhando o processo inicial da HR. Naturalmente, ela é essencial para o controle de recombinações, porém, durante o processo de edição, ela atrapalha a recuperação da fita editada, assim sua retirada, por knockout, ou a proteção das pontas da fita molde demonstrou um grande aumento de taxa de recombinação homóloga. [62] [63] [64] [33] [61] [65]
Referências
- ↑ a b c d e f g h i ALBERTS, Bruce. Biologia molecular da célula. 6. ed. Porto Alegre: ArtMed, 2017. ISBN 9788582714232.
- ↑ a b c d e f g Griffiths, Anthony J. F. (11 de outubro de 2022). Introdução a Genética. Catherine Peichel, David A. Wassarman, John Doebley, Claudia Gallo, Karina Carvalho, Heliosa Wheels, Vilma Varga 12 ed. RIO DE JANEIRO, RJ: Editora Guanabara Koogan Ltda
- ↑ a b Lewin, Benjamin (2008). Genes IX 9th ed ed. Sudbury, Mass: Jones and Bartlett Publishers
- ↑ a b c d Pierce, Benjamin A. (2017). Genetics: a conceptual approach Sixth edition ed. New York, NY: W. H. Freeman, Macmillan Learning
- ↑ a b c d Sun, Yueru; McCorvie, Thomas J.; Yates, Luke A.; Zhang, Xiaodong (janeiro de 2020). «Structural basis of homologous recombination». Cellular and Molecular Life Sciences (em inglês) (1): 3–18. ISSN 1420-682X. doi:10.1007/s00018-019-03365-1. Consultado em 21 de novembro de 2025
- ↑ a b c d e f Dna Recombinante: Genes E Genomas. [S.l.]: Artmed. 10 de novembro de 2021
- ↑ Castle, W. E. (25 de setembro de 1903). «Mendel's Law of Heredity». Science (em inglês) (456): 396–406. ISSN 0036-8075. doi:10.1126/science.18.456.396. Consultado em 21 de novembro de 2025
- ↑ a b c Mendel, G. “Experiments on Plant Hybridization.” Verhandlungen des naturforschenden Vereines in Brünn, 4: 3–47.4, 1866.
- ↑ SUTTON, Walter S. On the morphology of the chromosome group in Brachystola Magna. The biological bulletin, v. 4, n. 1, p. 24–39, 1902.
- ↑ SUTTON, Walter S. THE CHROMOSOMES IN HEREDITY. The biological bulletin, v. 4, n. 5, p. 231–250, 1903.
- ↑ STEVENS, Nettie M. Studies in Spermatogenesis...: With Special reference to the" accessory chromosome". Carnegie Institution of Washington, 1905.
- ↑ Wilson, Edmund B. (20 de outubro de 1905). «The Chromosomes in Relation to the Determination of Sex in Insects». Science (em inglês) (564): 500–502. ISSN 0036-8075. doi:10.1126/science.22.564.500. Consultado em 21 de novembro de 2025
- ↑ CREAGER, Angela N. H. Hershey heaven. Nature structural biology, v. 8, n. 1, p. 18–19, 2001.
- ↑ Ribeiro, Maria Cecília (23 de janeiro de 2009). Genética Molecular. [S.l.]: Biologia - Ead - Ufsc
- ↑ Hunter, Neil (28 de outubro de 2015). «Meiotic Recombination: The Essence of Heredity». Cold Spring Harbor Perspectives in Biology (em inglês): a016618. ISSN 1943-0264. PMC 4665078
 . PMID 26511629. doi:10.1101/cshperspect.a016618. Consultado em 21 de novembro de 2025
. PMID 26511629. doi:10.1101/cshperspect.a016618. Consultado em 21 de novembro de 2025
- ↑ a b c Jinek, Martin; Chylinski, Krzysztof; Fonfara, Ines; Hauer, Michael; Doudna, Jennifer A.; Charpentier, Emmanuelle (17 de agosto de 2012). «A Programmable Dual-RNA–Guided DNA Endonuclease in Adaptive Bacterial Immunity». Science (em inglês) (6096): 816–821. ISSN 0036-8075. doi:10.1126/science.1225829. Consultado em 21 de novembro de 2025
- ↑ a b Argueso, Juan Lucas; Westmoreland, James; Mieczkowski, Piotr A.; Gawel, Malgorzata; Petes, Thomas D.; Resnick, Michael A. (19 de agosto de 2008). «Double-strand breaks associated with repetitive DNA can reshape the genome». Proceedings of the National Academy of Sciences (em inglês) (33): 11845–11850. ISSN 0027-8424. PMC 2515620
 . PMID 18701715. doi:10.1073/pnas.0804529105. Consultado em 21 de novembro de 2025
. PMID 18701715. doi:10.1073/pnas.0804529105. Consultado em 21 de novembro de 2025
- ↑ Baumann, Peter; West, Stephen C (julho de 1998). «Role of the human RAD51 protein in homologous recombination and double-stranded-break repair». Trends in Biochemical Sciences (em inglês) (7): 247–251. doi:10.1016/S0968-0004(98)01232-8. Consultado em 21 de novembro de 2025
- ↑ Bonilla, Braulio; Hengel, Sarah R.; Grundy, McKenzie K.; Bernstein, Kara A. (23 de novembro de 2020). «RAD51 Gene Family Structure and Function». Annual Review of Genetics (em inglês) (1): 25–46. ISSN 0066-4197. PMC 7703940
 . PMID 32663049. doi:10.1146/annurev-genet-021920-092410. Consultado em 21 de novembro de 2025
. PMID 32663049. doi:10.1146/annurev-genet-021920-092410. Consultado em 21 de novembro de 2025
- ↑ a b c Brown, Terence A. (2021). Gene cloning and DNA analysis: an introduction Eighth edition ed. Hoboken, NJ: Wiley Blackwell
- ↑ a b Cohen, Stanley N.; Chang, Annie C. Y.; Boyer, Herbert W.; Helling, Robert B. (novembro de 1973). «Construction of Biologically Functional Bacterial Plasmids In Vitro». Proceedings of the National Academy of Sciences (em inglês) (11): 3240–3244. ISSN 0027-8424. PMC 427208
 . PMID 4594039. doi:10.1073/pnas.70.11.3240. Consultado em 21 de novembro de 2025
. PMID 4594039. doi:10.1073/pnas.70.11.3240. Consultado em 21 de novembro de 2025
- ↑ Harrison, Jacob C.; Haber, James E. (1 de dezembro de 2006). «Surviving the Breakup: The DNA Damage Checkpoint». Annual Review of Genetics (em inglês) (1): 209–235. ISSN 0066-4197. doi:10.1146/annurev.genet.40.051206.105231. Consultado em 21 de novembro de 2025
- ↑ International Human Genome Sequencing Consortium; Whitehead Institute for Biomedical Research, Center for Genome Research:; Lander, Eric S.; Linton, Lauren M.; Birren, Bruce; Nusbaum, Chad; Zody, Michael C.; Baldwin, Jennifer; Devon, Keri (15 de fevereiro de 2001). «Initial sequencing and analysis of the human genome». Nature (em inglês) (6822): 860–921. ISSN 0028-0836. doi:10.1038/35057062. Consultado em 21 de novembro de 2025
- ↑ Mullis, Kary B.; Faloona, Fred A. (1987). «[21] Specific synthesis of DNA in vitro via a polymerase-catalyzed chain reaction». Elsevier (em inglês): 335–350. ISBN 978-0-12-182056-5. doi:10.1016/0076-6879(87)55023-6. Verifique
|doi=(ajuda). Consultado em 21 de novembro de 2025 - ↑ a b c Slatkin, Montgomery (junho de 2008). «Linkage disequilibrium — understanding the evolutionary past and mapping the medical future». Nature Reviews Genetics (em inglês) (6): 477–485. ISSN 1471-0056. doi:10.1038/nrg2361. Consultado em 21 de novembro de 2025
- ↑ Collins, Francis S. (7 de fevereiro de 2001). «Implications of the Human Genome Project for Medical Science». JAMA (em inglês) (5). 540 páginas. ISSN 0098-7484. doi:10.1001/jama.285.5.540. Consultado em 21 de novembro de 2025
- ↑ Stewart, Mark D; Merino Vega, Diana; Arend, Rebecca C; Baden, Jonathan F; Barbash, Olena; Beaubier, Nike; Collins, Grace; French, Tim; Ghahramani, Negar (11 de março de 2022). «Homologous Recombination Deficiency: Concepts, Definitions, and Assays». The Oncologist (em inglês) (3): 167–174. ISSN 1083-7159. doi:10.1093/oncolo/oyab053. Consultado em 21 de novembro de 2025
- ↑ West, Stephen C. (dezembro de 1997). «PROCESSING OF RECOMBINATION INTERMEDIATES BY THE R uv ABC PROTEINS». Annual Review of Genetics (em inglês) (1): 213–244. ISSN 0066-4197. doi:10.1146/annurev.genet.31.1.213. Consultado em 21 de novembro de 2025
- ↑ a b Li, Xuan; Heyer, Wolf-Dietrich (janeiro de 2008). «Homologous recombination in DNA repair and DNA damage tolerance». Cell Research (em inglês) (1): 99–113. ISSN 1001-0602. doi:10.1038/cr.2008.1. Consultado em 21 de novembro de 2025
- ↑ Zickler, Denise; Kleckner, Nancy (27 de novembro de 2023). «Meiosis: Dances Between Homologs». Annual Review of Genetics (em inglês) (1): 1–63. ISSN 0066-4197. doi:10.1146/annurev-genet-061323-044915. Consultado em 21 de novembro de 2025
- ↑ Saxena, Sneha; Zou, Lee (junho de 2022). «Hallmarks of DNA replication stress». Molecular Cell (em inglês) (12): 2298–2314. PMC 9219557
 . PMID 35714587. doi:10.1016/j.molcel.2022.05.004. Consultado em 21 de novembro de 2025
. PMID 35714587. doi:10.1016/j.molcel.2022.05.004. Consultado em 21 de novembro de 2025
- ↑ Szostak, Jack W.; Orr-Weaver, Terry L.; Rothstein, Rodney J.; Stahl, Franklin W. (maio de 1983). «The double-strand-break repair model for recombination». Cell (em inglês) (1): 25–35. doi:10.1016/0092-8674(83)90331-8. Consultado em 21 de novembro de 2025
- ↑ a b Karasu, Mehmet E.; Toufektchan, Eléonore; Chen, Yanyang; Albertelli, Alessandra; Cullot, Grégoire; Maciejowski, John; Corn, Jacob E. (julho de 2025). «Removal of TREX1 activity enhances CRISPR–Cas9-mediated homologous recombination». Nature Biotechnology (em inglês) (7): 1168–1176. ISSN 1087-0156. PMC 12263433
 . PMID 39134754. doi:10.1038/s41587-024-02356-3. Consultado em 21 de novembro de 2025
. PMID 39134754. doi:10.1038/s41587-024-02356-3. Consultado em 21 de novembro de 2025
- ↑ Watson, J. D.; Crick, F. H. C. (25 de abril de 1953). «Molecular Structure of Nucleic Acids: A Structure for Deoxyribose Nucleic Acid». Nature (em inglês) (4356): 737–738. ISSN 0028-0836. doi:10.1038/171737a0. Consultado em 21 de novembro de 2025
- ↑ Ciccia, Alberto; Elledge, Stephen J. (outubro de 2010). «The DNA Damage Response: Making It Safe to Play with Knives». Molecular Cell (em inglês) (2): 179–204. PMC 2988877
 . PMID 20965415. doi:10.1016/j.molcel.2010.09.019. Consultado em 21 de novembro de 2025
. PMID 20965415. doi:10.1016/j.molcel.2010.09.019. Consultado em 21 de novembro de 2025
- ↑ a b Hassin, Ori; Oren, Moshe (fevereiro de 2023). «Drugging p53 in cancer: one protein, many targets». Nature Reviews Drug Discovery (em inglês) (2): 127–144. ISSN 1474-1776. PMC 9549847
 . PMID 36216888. doi:10.1038/s41573-022-00571-8. Consultado em 21 de novembro de 2025
. PMID 36216888. doi:10.1038/s41573-022-00571-8. Consultado em 21 de novembro de 2025
- ↑ Kimble, Michael T.; Sane, Aakanksha; Reid, Robert J.D.; Johnson, Matthew J.; Rothstein, Rodney; Symington, Lorraine S. (janeiro de 2025). «Repair of replication-dependent double-strand breaks differs between the leading and lagging strands». Molecular Cell (em inglês) (1): 61–77.e6. doi:10.1016/j.molcel.2024.10.032. Consultado em 21 de novembro de 2025
- ↑ Liu, Pengfei; Carvalho, Claudia MB; Hastings, Pj; Lupski, James R (junho de 2012). «Mechanisms for recurrent and complex human genomic rearrangements». Current Opinion in Genetics & Development (em inglês) (3): 211–220. doi:10.1016/j.gde.2012.02.012. Consultado em 21 de novembro de 2025
- ↑ a b Almeida, Daniel Manzoni de (22 de setembro de 2021). Imunologia na sala de aula | Immunology in the classroom: sequências de ensino | teaching sequences. Caio Cotta Natale, Paula Seixas Mello, Valdir Lamim Guedes Junior. São Paulo, SP: Editora Na Raiz
- ↑ Capecchi, Mario R. (junho de 2005). «Gene targeting in mice: functional analysis of the mammalian genome for the twenty-first century». Nature Reviews Genetics (em inglês) (6): 507–512. ISSN 1471-0056. doi:10.1038/nrg1619. Consultado em 21 de novembro de 2025
- ↑ Lyttle, Terrence W. (dezembro de 1991). «SEGREGATION DISTORTERS». Annual Review of Genetics (em inglês) (1): 511–581. ISSN 0066-4197. doi:10.1146/annurev.ge.25.120191.002455. Consultado em 21 de novembro de 2025
- ↑ Thompson & Thompson: Genetica Medica. [S.l.]: Editora Guanabara Koogan Ltda. 14 de julho de 2023
- ↑ Pardo-Manuel de Villena, Fernando; Sapienza, Carmen (1 de maio de 2001). «Nonrandom segregation during meiosis: the unfairness of females». Mammalian Genome (5): 331–339. ISSN 0938-8990. doi:10.1007/s003350040003. Consultado em 21 de novembro de 2025
- ↑ Searle, Jeremy B.; de Villena, Fernando Pardo-Manuel (julho de 2022). «The evolutionary significance of meiotic drive». Heredity (em inglês) (1): 44–47. ISSN 0018-067X. doi:10.1038/s41437-022-00534-0. Consultado em 21 de novembro de 2025
- ↑ Devlin, Thomas M., ed. (2011). Textbook of biochemistry: with clinical correlations 7th ed ed. Hoboken, NJ: John Wiley & Sons
- ↑ Jasin, M.; Rothstein, R. (1 de novembro de 2013). «Repair of Strand Breaks by Homologous Recombination». Cold Spring Harbor Perspectives in Biology (em inglês) (11): a012740–a012740. ISSN 1943-0264. doi:10.1101/cshperspect.a012740. Consultado em 21 de novembro de 2025
- ↑ Murray, Patrick (19 de abril de 2023). Microbiologia Médica. Ken Rosenthal, Michael Pfaller, Angela Satie Nishikaku 9 ed. Rio de Janeiro, RJ: Grupo Gen
- ↑ Prakash, Rohit; Zhang, Yu; Feng, Weiran; Jasin, Maria (abril de 2015). «Homologous Recombination and Human Health: The Roles of BRCA1, BRCA2, and Associated Proteins». Cold Spring Harbor Perspectives in Biology (em inglês) (4): a016600. ISSN 1943-0264. PMC 4382744
 . PMID 25833843. doi:10.1101/cshperspect.a016600. Consultado em 21 de novembro de 2025
. PMID 25833843. doi:10.1101/cshperspect.a016600. Consultado em 21 de novembro de 2025
- ↑ Collins, Francis S. (7 de fevereiro de 2001). «Implications of the Human Genome Project for Medical Science». JAMA (em inglês) (5). 540 páginas. ISSN 0098-7484. doi:10.1001/jama.285.5.540. Consultado em 21 de novembro de 2025
- ↑ Sanger, F.; Nicklen, S.; Coulson, A. R. (dezembro de 1977). «DNA sequencing with chain-terminating inhibitors». Proceedings of the National Academy of Sciences (em inglês) (12): 5463–5467. ISSN 0027-8424. PMC 431765
 . PMID 271968. doi:10.1073/pnas.74.12.5463. Consultado em 21 de novembro de 2025
. PMID 271968. doi:10.1073/pnas.74.12.5463. Consultado em 21 de novembro de 2025
- ↑ Jasin, M.; Rothstein, R. (1 de novembro de 2013). «Repair of Strand Breaks by Homologous Recombination». Cold Spring Harbor Perspectives in Biology (em inglês) (11): a012740–a012740. ISSN 1943-0264. doi:10.1101/cshperspect.a012740. Consultado em 21 de novembro de 2025
- ↑ Biologia molecular do gene. [S.l.]: Artmed. 10 de novembro de 2021
- ↑ a b Wang, Ziyi; Jia, Renxiang; Wang, Linlin; Yang, Qiwei; Hu, Xiaohai; Fu, Qiang; Zhang, Xinyu; Li, Wenya; Ren, Yi (7 de julho de 2022). «The Emerging Roles of Rad51 in Cancer and Its Potential as a Therapeutic Target». Frontiers in Oncology. ISSN 2234-943X. doi:10.3389/fonc.2022.935593. Consultado em 21 de novembro de 2025
- ↑ Tran, Ngoc-Tung; Bashir, Sanum; Li, Xun; Rossius, Jana; Chu, Van Trung; Rajewsky, Klaus; Kühn, Ralf (30 de abril de 2019). «Enhancement of Precise Gene Editing by the Association of Cas9 With Homologous Recombination Factors». Frontiers in Genetics. ISSN 1664-8021. doi:10.3389/fgene.2019.00365. Consultado em 21 de novembro de 2025
- ↑ Chen, Chun-Chin; Amon, Angelika; Hemann, Michael; Rowe, Robert Grant (2 de novembro de 2023). «Inherent Genome Instability Underlies Trisomy 21-Associated Myeloid Malignancies». Blood (em inglês) (Supplement 1): 1388–1388. ISSN 0006-4971. doi:10.1182/blood-2023-181931. Consultado em 21 de novembro de 2025
- ↑ Lamb, Neil E.; Yu, Kai; Shaffer, John; Feingold, Eleanor; Sherman, Stephanie L. (janeiro de 2005). «Association between Maternal Age and Meiotic Recombination for Trisomy 21». The American Journal of Human Genetics (em inglês) (1): 91–99. PMC 1196437
 . PMID 15551222. doi:10.1086/427266. Consultado em 21 de novembro de 2025
. PMID 15551222. doi:10.1086/427266. Consultado em 21 de novembro de 2025
- ↑ Wu, Li-Chen; Sun, Chiao-Wang; Ryan, Thomas M.; Pawlik, Kevin M.; Ren, Jinxiang; Townes, Tim M. (15 de agosto de 2006). «Correction of sickle cell disease by homologous recombination in embryonic stem cells». Blood (em inglês) (4): 1183–1188. ISSN 0006-4971. PMC 1895869
 . PMID 16638928. doi:10.1182/blood-2006-02-004812. Consultado em 21 de novembro de 2025
. PMID 16638928. doi:10.1182/blood-2006-02-004812. Consultado em 21 de novembro de 2025
- ↑ Allen, Daniel; Kalter, Nechama; Rosenberg, Michael; Hendel, Ayal (24 de abril de 2023). «Homology-Directed-Repair-Based Genome Editing in HSPCs for the Treatment of Inborn Errors of Immunity and Blood Disorders». Pharmaceutics (em inglês) (5). 1329 páginas. ISSN 1999-4923. PMC 10220672
 . PMID 37242571. doi:10.3390/pharmaceutics15051329. Consultado em 21 de novembro de 2025
. PMID 37242571. doi:10.3390/pharmaceutics15051329. Consultado em 21 de novembro de 2025
- ↑ Farmer, Hannah; McCabe, Nuala; Lord, Christopher J.; Tutt, Andrew N. J.; Johnson, Damian A.; Richardson, Tobias B.; Santarosa, Manuela; Dillon, Krystyna J.; Hickson, Ian (abril de 2005). «Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy». Nature (em inglês) (7035): 917–921. ISSN 0028-0836. doi:10.1038/nature03445. Consultado em 21 de novembro de 2025
- ↑ Verkuijl, Sebald A. N.; Ang, Joshua X. D.; Alphey, Luke; Bonsall, Michael B.; Anderson, Michelle A. E. (28 de março de 2022). «The Challenges in Developing Efficient and Robust Synthetic Homing Endonuclease Gene Drives». Frontiers in Bioengineering and Biotechnology. ISSN 2296-4185. PMC 8996256
 . PMID 35419354. doi:10.3389/fbioe.2022.856981. Consultado em 21 de novembro de 2025
. PMID 35419354. doi:10.3389/fbioe.2022.856981. Consultado em 21 de novembro de 2025
- ↑ a b Keeney, Scott; Giroux, Craig N; Kleckner, Nancy (fevereiro de 1997). «Meiosis-Specific DNA Double-Strand Breaks Are Catalyzed by Spo11, a Member of a Widely Conserved Protein Family». Cell (em inglês) (3): 375–384. doi:10.1016/S0092-8674(00)81876-0. Consultado em 21 de novembro de 2025
- ↑ Doudna, Jennifer A.; Charpentier, Emmanuelle (28 de novembro de 2014). «The new frontier of genome engineering with CRISPR-Cas9». Science (em inglês) (6213). ISSN 0036-8075. doi:10.1126/science.1258096. Consultado em 21 de novembro de 2025
- ↑ Hastings, P. J.; Ira, Grzegorz; Lupski, James R. (30 de janeiro de 2009). Matic, Ivan, ed. «A Microhomology-Mediated Break-Induced Replication Model for the Origin of Human Copy Number Variation». PLoS Genetics (em inglês) (1): e1000327. ISSN 1553-7404. PMC 2621351
 . PMID 19180184. doi:10.1371/journal.pgen.1000327. Consultado em 21 de novembro de 2025
. PMID 19180184. doi:10.1371/journal.pgen.1000327. Consultado em 21 de novembro de 2025
- ↑ Heyer, Wolf-Dietrich; Ehmsen, Kirk T.; Liu, Jie (1 de dezembro de 2010). «Regulation of Homologous Recombination in Eukaryotes». Annual Review of Genetics (em inglês) (1): 113–139. ISSN 0066-4197. PMC 4114321
 . PMID 20690856. doi:10.1146/annurev-genet-051710-150955. Consultado em 21 de novembro de 2025
. PMID 20690856. doi:10.1146/annurev-genet-051710-150955. Consultado em 21 de novembro de 2025
- ↑ Tran, Ngoc-Tung; Bashir, Sanum; Li, Xun; Rossius, Jana; Chu, Van Trung; Rajewsky, Klaus; Kühn, Ralf (30 de abril de 2019). «Enhancement of Precise Gene Editing by the Association of Cas9 With Homologous Recombination Factors». Frontiers in Genetics. ISSN 1664-8021. doi:10.3389/fgene.2019.00365. Consultado em 21 de novembro de 2025
Ver também
- Recombinação genética
- Recombinação
- Reparo de ADN
- Gene targeting
- Quebra de Dupla Fita
- Desvio de segregação
Ligações Externas
Portal Biologia
Portal Genética
Portal Medicina