Medicamentos para fertilidade
Medicamentos para fertilidade, também conhecidos como fármacos de fertilidade, são medicamentos que aumentam a fertilidade reprodutiva. Para mulheres, esses medicamentos são usados para estimular o desenvolvimento do folículo no ovário.[1] Existem muito poucas opções de medicamentos de fertilidade disponíveis para homens.[2]
Agentes que aumentam a atividade ovariana podem ser classificados como hormônio liberador de gonadotrofina, estrogênio antagonistas ou gonadotrofinas.
A tomada de decisão no tratamento envolve quatro fatores principais: eficácia, carga do tratamento (como frequência de injeções e visitas médicas), segurança e custos financeiros.[3]
Mulheres
Principais técnicas
As principais técnicas envolvendo medicamentos para fertilidade em mulheres são:
- Indução da ovulação, com o objetivo de produzir um ou dois folículos ovulatórios para fertilização por relação sexual ou inseminação artificial
- Hiperestimulação ovariana controlada, que geralmente faz parte da fertilização in vitro, e cujo objetivo é desenvolver múltiplos folículos (idealmente entre 12 e 14 folículos antrais medindo 2–8 mm de diâmetro),[4] seguida por punção folicular transvaginal, co-incubação e, posteriormente, transferência de embriões de no máximo dois embriões por vez.[5]
- Indução da maturação final dos folículos, também desencadeando um momento previsível da ovulação.
Hormônio liberador de gonadotrofina
Tanto o hormônio liberador de gonadotrofina (GnRH) quanto qualquer agonista do hormônio liberador de gonadotrofina (como Lupron) podem ser usados em combinação com hormônio luteinizante (LH) através de uma bomba de infusão para simular a produção endógena de hormônios. O GnRH estimula a liberação de gonadotrofinas (LH e FSH) pela hipófise anterior. Esse conjunto de terapias é reservado para um subconjunto de mulheres inférteis e produziu taxas de ovulação de 90% e taxas de gravidez de 80% ou mais.
Antiestrogênios
Os antiestrogênios inibem os efeitos do estrogênio, que incluem os moduladores seletivos do receptor de estrogênio (SERM) e os inibidores da aromatase.
Moduladores seletivos do receptor de estrogênio
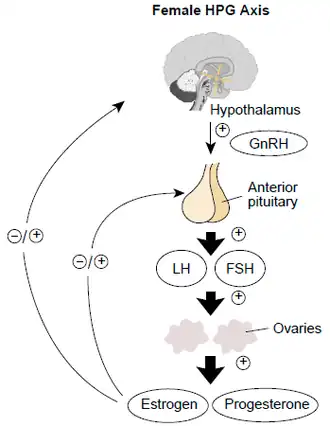
O clomifeno é um modulador seletivo do receptor de estrogênio (SERM).[6] Ele é o medicamento para fertilidade mais amplamente utilizado.[7] Outros medicamentos dessa classe incluem tamoxifeno e raloxifeno, embora ambos não sejam tão eficazes quanto o clomifeno e, portanto, sejam menos utilizados para fins de fertilidade.[8] São usados na indução da ovulação por meio da inibição do feedback negativo do estrogênio no hipotálamo. Com essa inibição, o hipotálamo secreta GnRH, que por sua vez estimula a hipófise anterior a liberar LH e FSH, os quais auxiliam na ovulação. Entre 60 e 85% das mulheres, principalmente com síndrome dos ovários policísticos (SOP), ovulam com sucesso em resposta ao clomifeno, com uma taxa cumulativa de gravidez de 30 a 40%.[9][10][11]
Inibidores da aromatase
Embora usados principalmente no tratamento do câncer de mama, os inibidores da aromatase (particularmente o letrozol genérico) também são usados na indução da ovulação. Inibidores da aromatase são um tratamento comum de fertilidade para mulheres com SOP. Uma meta-análise analisando as taxas de nascimento com vida em mulheres com SOP tratadas com clomifeno em comparação ao letrozol concluiu que o letrozol resultou em maiores taxas de nascidos vivos.[12] No entanto, a indução da ovulação permanece uma indicação off-label, o que impacta seu uso.
Gonadotrofinas
As gonadotrofinas são hormônios proteicos que estimulam as gônadas (testículos e ovários). Para uso medicamentoso, podem ser extraídas da urina de mulheres pós-menopausa ou obtidas por modificação genética e recombinação bacteriana. Exemplos de FSH recombinante são Follistim e Gonal F, enquanto o Luveris é um LH recombinante. FSH e análogos de FSH recombinante são usados principalmente na hiperestimulação ovariana controlada bem como na indução da ovulação.[13] Houve alguma controvérsia sobre a eficácia entre FSH extraído e recombinante na indução da ovulação; entretanto, uma meta-análise de 14 ensaios com 1726 mulheres concluiu que não havia diferenças nos resultados de gravidez clínica ou nascimento com vida.[14]
O tratamento com quimioterapia em mulheres pré-menopáusicas pode comprometer a reserva e a função ovariana, com efeitos gonadotóxicos que variam de infertilidade temporária a permanente e falência ovariana prematura (FOP). Os mecanismos propostos para o dano ovariano induzido por quimioterapia incluem apoptose de folículos em crescimento, fibrose das células estromais e lesão nos vasos sanguíneos resultando em isquemia. As opções de primeira linha para preservação da fertilidade incluem a preservação de embriões e oócitos antes do início da quimioterapia, embora esses métodos não contribuam para a preservação da função gonadal. As terapias com agonista de GnRH têm sido associadas a risco, tempo e custo relativamente baixos.[15] Há evidências de que o tratamento conjunto da quimioterapia com hormônio liberador de gonadotrofina (GnRH) pode aumentar a probabilidade de retorno da menstruação espontânea e da ovulação. No entanto, esse cotratamento não demonstrou melhora nas taxas de gravidez.[16]
Gonadotrofina coriônica humana
A gonadotrofina coriônica humana (hCG), também conhecida como “hormônio da gravidez”, é um hormônio normalmente produzido durante a gestação e que desempenha papel essencial em toda a reprodução.[17] É fundamental para a manutenção da gestação, desde as fases de placentação até o desenvolvimento inicial do embrião.[17] Também é usada em técnicas de reprodução assistida, podendo substituir o LH na indução da maturação final.[17]
Outros medicamentos
Embora a metformina tenha sido usada off-label para tratar oligomenorreia e a síndrome de hiperestimulação ovariana (SHO) em mulheres com SOP, a metformina deixou de ser recomendada como tratamento de infertilidade pela American Society for Reproductive Medicine (ASRM) em 2017. Seu uso para tratar infertilidade anovulatória baseava-se na associação da resistência insulínica em mulheres não obesas com SOP. Embora a metformina possa aumentar a ovulação em mulheres com SOP, não há evidências de aumento nas taxas de gravidez ou de nascidos vivos, e a terapia combinada de metformina com citrato de clomifeno não mostrou benefício significativo em comparação ao uso isolado do citrato de clomifeno. A terapia de primeira linha para indução da ovulação em mulheres com SOP continua sendo o antiestrogênio citrato de clomifeno ou o inibidor da aromatase letrozol.[18]
Homens
O tratamento para oligozoospermia é centrado nas causas subjacentes, como distúrbios endócrinos e sistêmicos que podem causar hipogonadismo.[19]
Normalmente, outras tecnologias de reprodução assistida são utilizadas. Embora não haja indicação da FDA para o uso de inibidores da aromatase na melhora da espermatogênese, o testolactona demonstrou eficácia em comparação ao placebo.[20]
Embora não haja indicação da FDA para o uso de clomifeno na infertilidade masculina, ele tem sido prescrito desde a década de 1960.[21] Em 2013, não havia evidências substanciais de que o clomifeno pudesse tratar a infertilidade masculina.[21]
Combinações de vitaminas e minerais, incluindo selênio, coenzima Q10, L-carnitina, ácido fólico, zinco, ácido eicosapentaenoico (EPA) e ácido docosa-hexaenoico (DHA), mostraram melhorar a infertilidade masculina, mas devido ao baixo número de estudos e participantes, são necessários mais ensaios clínicos.[22] A suplementação de folato em combinação com zinco mostrou efeito estatisticamente significativo na concentração e morfologia dos espermatozoides em comparação ao placebo.[23] Há evidências sugerindo associação significativa entre concentrações séricas de vitamina D e a qualidade do esperma em homens, caracterizada pela motilidade e progressão dos espermatozoides.[24] Como a qualidade do esperma masculino é influenciada pela genética, os resultados devem ser interpretados com cautela. Há poucas evidências de que a suplementação com antioxidantes, como a pentoxifilina, aumente a fertilidade masculina.[25][26]
Em setembro de 2017, a terapia com células-tronco mesenquimais para infertilidade havia sido estudada em animais, mas ainda não havia entrado em ensaios clínicos.[27] Células-tronco coletadas da medula óssea e do cordão umbilical mostraram maior potencial para reabilitar a fertilidade em animais, mas mais estudos são necessários para determinar a eficácia.[27]
Efeitos adversos
Câncer
Como a infertilidade aumenta o risco de câncer de ovário, medicamentos para fertilidade têm sido utilizados nesse contexto, mas os riscos de câncer ainda não são totalmente conhecidos.[28] Desde 2019 alguns estudos mostraram que o risco de desenvolver câncer de ovário é maior com o uso desses medicamentos. No entanto, devido ao baixo número de estudos, à falta de tempo de acompanhamento e a outros fatores de contribuição, o risco permanece incerto.[28] A maioria dos estudos conduzidos mostrou que medicamentos para fertilidade não aumentam o risco de outros cânceres ginecológicos (colo do útero e endométrio) ou de outros cânceres malignos (tireoide, cólon, melanoma, mama).[29] A validade desses dados pode ser afetada por vieses de relato dos pacientes, baixo número de sujeitos e outras variáveis de confusão.[29]
Crianças nascidas de mães que usaram medicamentos para fertilidade a fim de induzir a ovulação têm mais que o dobro de chances de desenvolver leucemia na infância em comparação com outras crianças.[30]
Síndrome de hiperestimulação ovariana
Antagonistas de estrogênio e gonadotrofinas podem estimular múltiplos folículos e outros hormônios ovarianos, levando a gravidez múltipla e possível síndrome de hiperestimulação ovariana (SHO).[31] O desenvolvimento da SHO depende da administração de hCG e é mediado pelo fator de crescimento endotelial vascular (VEGF). A SHO é caracterizada pelo aumento do volume dos ovários.[32]
A gravidez múltipla é especialmente prejudicial devido aos riscos adicionais, incluindo parto prematuro e baixo peso ao nascer, pré-eclâmpsia e maior risco de mortalidade neonatal.[33] Embora os nascimentos de trigêmeos tenham diminuído nas TRA, em 2022 as gestações múltiplas ainda representavam mais de 45% dos nascimentos por FIV nos Estados Unidos.[34] No entanto, há limitações nas medições, já que de 4% a 8% das clínicas de FIV não reportam seus dados ao CDC.
Em 2020, estatísticas do Reino Unido mostraram que 11% das gestações por FIV resultaram em partos múltiplos, em comparação com 1–2% das gestações naturais.[35] Números da Austrália em 2024 indicaram que os partos múltiplos após TRA haviam reduzido pela metade nos últimos dez anos, com apenas 2,7% dos nascimentos resultando em gêmeos ou trigêmeos.[36]
Descontinuação
As principais razões para a descontinuação em todos os tipos de tratamento de fertilidade e em qualquer estágio do tratamento são: "adiamento do tratamento, carga física e psicológica e problemas relacionais e pessoais".[37]
Ver também
Referências
- ↑ Crowley F, Martin KA (2020). «Patient Education: Infertility in Women». In: Post TW. UpToDate. Waltham, MA: UpToDate
- ↑ Drobnis EZ, Nangia AK (2017). Impacts of Medications on Male Fertility. Cham, Switzerland: Palgrave Macmillan. ISBN 978-3-319-69535-8. Consultado em 23 de fevereiro de 2019
- ↑ Dancet EA, Fleur Dancet EA, D'Hooghe TM, d'Hooghe TM, van der Veen F, Bossuyt P, et al. (2014-04-). «"Patient-centered fertility treatment": what is required?». Fertility and Sterility. 101 (4): 924–6. PMID 24502889. doi:10.1016/j.fertnstert.2013.12.045
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ De Vos, Michel (7 de abril de 2025). «Randomized controlled trial to evaluate the impact of follicle priming on IVM outcomes in women with polycystic ovaries: CFA versus FSH-B». Stanford University Magazine. Human Reproduction, Volume 40, Issue 6, page 1127. Consultado em 4 de junho de 2025
- ↑ «Fertility problems: assessment and treatment». NICE clinical guideline CG156. U.K. National Institute for Health and Care Excellence (NICE). 2013-02- Verifique data em:
|data=(ajuda) - ↑ Stute P, Birkhauser M (2015). «Selective estrogen receptor modulators (SERM)/Selektive Ostrogenrezeptormodulatoren (SERM).» (PDF). Gynakologische Endokrinologie. 13 (2): 126. doi:10.1007/s10304-015-0003-9
- ↑ Fauser BC (2014-12-). «Reproductive endocrinology: revisiting ovulation induction in PCOS». Nature Reviews. Endocrinology. 10 (12): 704–5. PMID 25178733. doi:10.1038/nrendo.2014.156 Verifique data em:
|data=(ajuda) - ↑ Goldstein SR, Siddhanti S, Ciaccia AV, Plouffe L (2000). «A pharmacological review of selective oestrogen receptor modulators». Human Reproduction Update. 6 (3): 212–24. PMID 10874566. doi:10.1093/humupd/6.3.212

- ↑ Dickey RP, Holtkamp DE (1996). «Development, pharmacology and clinical experience with clomiphene citrate». Human Reproduction Update. 2 (6): 483–506. PMID 9111183. doi:10.1093/humupd/2.6.483

- ↑ Gorlitsky GA, Kase NG, Speroff L (1978-03-). «Ovulation and pregnancy rates with clomiphene citrate». Obstetrics and Gynecology. 51 (3): 265–9. PMID 628527. doi:10.1097/00006250-197803000-00002 Verifique data em:
|data=(ajuda) - ↑ Gysler M, March CM, Mishell DR, Bailey EJ (1982-02-). «A decade's experience with an individualized clomiphene treatment regimen including its effect on the postcoital test». Fertility and Sterility. 37 (2): 161–7. PMID 7060766. doi:10.1016/s0015-0282(16)46033-4
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Franik, Sebastian; Le, Quang-Khoi; Kremer, Jan Am; Kiesel, Ludwig; Farquhar, Cindy (27 de setembro de 2022). «Aromatase inhibitors (letrozole) for ovulation induction in infertile women with polycystic ovary syndrome». The Cochrane Database of Systematic Reviews. 2022 (9): CD010287. ISSN 1469-493X. PMC 9514207
 . PMID 36165742. doi:10.1002/14651858.CD010287.pub4
. PMID 36165742. doi:10.1002/14651858.CD010287.pub4
- ↑ Conforti A, Esteves SC, Di Rella F, Strina I, De Rosa P, Fiorenza A, et al. (2019-02-). «The role of recombinant LH in women with hypo-response to controlled ovarian stimulation: a systematic review and meta-analysis». Reproductive Biology and Endocrinology. 17 (1). PMC 6366097
 . PMID 30728019. doi:10.1186/s12958-019-0460-4
. PMID 30728019. doi:10.1186/s12958-019-0460-4 Parâmetro desconhecido
Parâmetro desconhecido |article-number=ignorado (ajuda); Verifique data em:|data=(ajuda) - ↑ Weiss NS, Kostova E, Nahuis M, Mol BW, van der Veen F, van Wely M (2019-01-). «Gonadotrophins for ovulation induction in women with polycystic ovary syndrome». The Cochrane Database of Systematic Reviews. 1 (1): CD010290. PMC 6353048
 . PMID 30648738. doi:10.1002/14651858.CD010290.pub3 Verifique data em:
. PMID 30648738. doi:10.1002/14651858.CD010290.pub3 Verifique data em: |data=(ajuda) - ↑ Hickman LC, Llarena NC, Valentine LN, Liu X, Falcone T (2018-04-). «Preservation of gonadal function in women undergoing chemotherapy: a systematic review and meta-analysis of the potential role for gonadotropin-releasing hormone agonists». Journal of Assisted Reproduction and Genetics. 35 (4): 571–581. PMC 5949114
 . PMID 29470701. doi:10.1007/s10815-018-1128-2 Verifique data em:
. PMID 29470701. doi:10.1007/s10815-018-1128-2 Verifique data em: |data=(ajuda) - ↑ Bedaiwy MA, Abou-Setta AM, Desai N, Hurd W, Starks D, El-Nashar SA, et al. (2011-03-). «Gonadotropin-releasing hormone analog cotreatment for preservation of ovarian function during gonadotoxic chemotherapy: a systematic review and meta-analysis». Fertility and Sterility. 95 (3): 906–14.e1–4. PMID 21145541. doi:10.1016/j.fertnstert.2010.11.017
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b c Leão R, Esteves SC (2014). «Gonadotropin therapy in assisted reproduction: an evolutionary perspective from biologics to biotech». Clinics (Review). 69 (4): 279–93. PMC 3971356
 . PMID 24714837. doi:10.6061/clinics/2014(04)10
. PMID 24714837. doi:10.6061/clinics/2014(04)10
- ↑ Penzias A, Bendikson K, Butts S, Coutifaris C, Falcone T, Fossum G, et al. (2017-09-). «Role of metformin for ovulation induction in infertile patients with polycystic ovary syndrome (PCOS): a guideline». Fertility and Sterility. 108 (3): 426–441. PMID 28865539. doi:10.1016/j.fertnstert.2017.06.026
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ de Kretser DM (1997-03-). «Male infertility». Lancet (Review). 349 (9054): 787–90. PMID 9074589. doi:10.1016/s0140-6736(96)08341-9 Verifique data em:
|data=(ajuda) - ↑ Ribeiro MA, Gameiro LF, Scarano WR, Briton-Jones C, Kapoor A, Rosa MB, El Dib R (2016-05-). «Aromatase inhibitors in the treatment of oligozoospermic or azoospermic men: a systematic review of randomized controlled trials». JBRA Assisted Reproduction (Review). 20 (2): 82–8. PMID 27244767. doi:10.5935/1518-0557.20160019
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b Willets AE, Corbo JM, Brown JN (2013-07-). «Clomiphene for the treatment of male infertility». Reproductive Sciences (Review). 20 (7): 739–44. PMID 23202725. doi:10.1177/1933719112466304 Verifique data em:
|data=(ajuda) - ↑ Buhling K, Schumacher A, Eulenburg CZ, Laakmann E (2019-08-). «Influence of oral vitamin and mineral supplementation on male infertility: a meta-analysis and systematic review». Reproductive Biomedicine Online. 39 (2): 269–279. PMID 31160241. doi:10.1016/j.rbmo.2019.03.099
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Irani M, Amirian M, Sadeghi R, Lez JL, Latifnejad Roudsari R (2017-08-). «The Effect of Folate and Folate Plus Zinc Supplementation on Endocrine Parameters and Sperm Characteristics in Sub-Fertile Men: A Systematic Review and Meta-Analysis». Urology Journal. 14 (5): 4069–4078. PMID 28853101 Verifique data em:
|data=(ajuda) - ↑ Arab A, Hadi A, Moosavian SP, Askari G, Nasirian M (2019-11-). «The association between serum vitamin D, fertility and semen quality: A systematic review and meta-analysis». International Journal of Surgery. 71: 101–109. PMID 31561004. doi:10.1016/j.ijsu.2019.09.025
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Smits RM, Mackenzie-Proctor R, Fleischer K, Showell MG (2018-09-). «Antioxidants in fertility: impact on male and female reproductive outcomes». Fertility and Sterility. 110 (4): 578–580. PMID 30196940. doi:10.1016/j.fertnstert.2018.05.028
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Chehab M, Madala A, Trussell JC (2015-03-). «On-label and off-label drugs used in the treatment of male infertility». Fertility and Sterility (Review). 103 (3): 595–604. PMID 25660648. doi:10.1016/j.fertnstert.2014.12.122
 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b Fazeli Z, Abedindo A, Omrani MD, Ghaderian SM (2018-02-). «Mesenchymal Stem Cells (MSCs) Therapy for Recovery of Fertility: a Systematic Review». Stem Cell Reviews and Reports. 14 (1): 1–12. PMID 28884412. doi:10.1007/s12015-017-9765-x Verifique data em:
|data=(ajuda) - ↑ a b Rizzuto I, Behrens RF, Smith LA (-06-). «Risk of ovarian cancer in women treated with ovarian stimulating drugs for infertility». The Cochrane Database of Systematic Reviews. 2019 (6): CD008215. PMC 6579663
 . PMID 31207666. doi:10.1002/14651858.cd008215.pub3 Verifique data em:
. PMID 31207666. doi:10.1002/14651858.cd008215.pub3 Verifique data em: |data=(ajuda) - ↑ a b Kroener L, Dumesic D, Al-Safi Z (2017-08-). «Use of fertility medications and cancer risk: a review and update». Current Opinion in Obstetrics & Gynecology. 29 (4): 195–201. PMC 5551049
 . PMID 28538003. doi:10.1097/GCO.0000000000000370 Verifique data em:
. PMID 28538003. doi:10.1097/GCO.0000000000000370 Verifique data em: |data=(ajuda) - ↑ Rudant J, Amigou A, Orsi L, Althaus T, Leverger G, Baruchel A, et al. (2013-02-). «Fertility treatments, congenital malformations, fetal loss, and childhood acute leukemia: the ESCALE study (SFCE)». Pediatric Blood & Cancer. 60 (2): 301–308. PMID 22610722. doi:10.1002/pbc.24192 Verifique data em:
|data=(ajuda) - ↑ Banker M, Garcia-Velasco JA (2015). «Revisiting ovarian hyper stimulation syndrome: Towards OHSS free clinic». J Hum Reprod Sci. 8 (1): 13–7. PMC 4381376
 . PMID 25838743. doi:10.4103/0974-1208.153120
. PMID 25838743. doi:10.4103/0974-1208.153120
- ↑ «Clinical Practice Guideline: Ovarian Hyperstimulation Syndrome (OHSS) Diagnosis and Management» (PDF). Institute of Obstetricians and Gynaecologists, Royal College of Physicians of Ireland. 7 de abril de 2012. Consultado em 4 de junho de 2025
- ↑ «Medications for Inducing Ovulation: A Guide for Parents». American Society for Reproductive Science. 2016. Consultado em 27 de maio de 2025
- ↑ «Understanding The Risks Of IVF Twins And Multiples». The Fertility Institute Los Angeles. 22 de março de 2020. Consultado em 27 de maio de 2025
- ↑ «Key statistics on multiple births» (PDF). Twin Trust UK. Consultado em 27 de maio de 2025
- ↑ «Rates of IVF twins and triplets hit record low: new report». University of New South Wales. 13 de setembro de 2024. Consultado em 27 de maio de 2025
- ↑ Gameiro S, Boivin J, Peronace L, Verhaak CM (2012-08-). «Why do patients discontinue fertility treatment? A systematic review of reasons and predictors of discontinuation in fertility treatment». Human Reproduction Update. 18 (6): 652–69. PMC 3461967
 . PMID 22869759. doi:10.1093/humupd/dms031 Verifique data em:
. PMID 22869759. doi:10.1093/humupd/dms031 Verifique data em: |data=(ajuda)