Medicamentos na gravidez
Drogas, incluindo medicamentos e drogas recreativas, podem ter efeitos durante a gravidez sobre a gestante e o feto que variam em relação aos efeitos da droga em pessoas que não estão grávidas. A Administração de Alimentos e Medicamentos (FDA) nos Estados Unidos relata que há seis milhões de gestações, com pelo menos 50% das mulheres tomando ao menos um medicamento.[1] Além disso, entre 5–10% das mulheres em idade fértil relatam o uso de álcool ou outras substâncias aditivas.[2] Para aquelas que levam a gestação adiante, o uso de drogas recreativas pode ter sérias consequências à saúde não apenas da mãe, mas também do feto, já que muitos medicamentos podem atravessar a placenta e alcançar o bebê. Algumas das consequências nos bebês incluem anomalias físicas e mentais, maior risco de natimorto, Síndrome de abstinência neonatal (NAS), Síndrome da morte súbita infantil (SIDS), baixo peso ao nascer, entre outras.[3]
Drogas tomadas durante a gravidez, incluindo medicamentos de venda livre, medicamentos sob prescrição, suplementos nutricionais, drogas recreativas e ilícitas, podem causar danos à mãe ou ao feto. O consumo de tabaco, álcool, maconha e drogas ilícitas durante a gravidez pode ser perigoso para o bebê em desenvolvimento e levar a graves problemas de saúde e/ou defeitos congênitos.[4] Mesmo pequenas quantidades de álcool, tabaco e maconha não foram comprovadamente seguras quando consumidas durante a gravidez.[5] Em alguns casos, por exemplo, quando a mãe tem epilepsia ou diabetes, o risco de interromper um medicamento pode ser maior do que os riscos associados ao seu uso durante a gravidez. O profissional de saúde da mãe ajudará a tomar essas decisões sobre a forma mais segura de proteger a saúde tanto da mãe quanto do bebê.[6] Além de medicamentos e substâncias recreativas, alguns suplementos alimentares são importantes para uma gravidez saudável; no entanto, outros podem causar danos ao bebê.[7]
Categorias na gravidez
As classificações de medicamentos com base na segurança durante a gravidez variam de país para país.
Até 2014, o Código de Regulamentos Federais dos Estados Unidos exigia que certos medicamentos e produtos biológicos fossem rotulados especificamente em relação aos seus efeitos sobre gestantes, incluindo a definição de uma "categoria de gravidez". Essas regras eram aplicadas pela FDA, e os medicamentos que foram estudados quanto aos seus efeitos na gravidez eram enquadrados nas seguintes categorias: A, B, C, D ou X, dependendo de como foram estudados e quais resultados foram encontrados.[8][9][10] Em 2014, no entanto, a FDA desenvolveu a "Regra de Rotulagem para Gravidez e Lactação (PLLR)", que exige que os rótulos dos produtos incluam informações específicas relacionadas à segurança e eficácia de medicamentos para gestantes e lactantes. Essa regra eliminou a exigência de categorias de gravidez nos rótulos de medicamentos sob prescrição.[11]
O sistema de categorização da Austrália leva em consideração defeitos congênitos, os efeitos no momento do nascimento ou próximo dele e problemas que podem surgir mais tarde na vida da criança em decorrência do uso da droga. O sistema os coloca em uma categoria com base na gravidade das consequências que o medicamento pode ter sobre o bebê ao atravessar a placenta.[12]
Medicamentos
Medicamentos durante a gravidez devem ser considerados com cautela. Muitos fármacos, medicamentos e suplementos nutricionais podem afetar o desenvolvimento fetal ou causar complicações. Para medicamentos de venda livre e sob prescrição, profissionais de saúde podem ajudar a avaliar os potenciais riscos e benefícios do uso durante a gestação. Alguns medicamentos podem ser necessários para a saúde e bem-estar da mãe e do bebê, e outros podem trazer risco de danos, mas em alguns casos os benefícios podem superar os riscos.
Medicamentos para dor
O uso de curto prazo de acetaminofeno, conforme indicado, é um dos poucos medicamentos recomendados para o tratamento de dor e febre em gestantes.[13] Não há associação estabelecida com teratogenicidade ou aumento na ocorrência de defeitos congênitos pelo uso de acetaminofeno em qualquer momento da gestação.[13] Existe, no entanto, potencial para toxicidade hepática fetal em casos de overdose materna, quando a mãe consome mais do que a dose diária recomendada.[14]
Ibuprofeno e naproxeno não foram frequentemente estudados durante a gravidez, mas estudos recentes não mostram risco aumentado de aborto espontâneo nas primeiras seis semanas.[15][13] Entretanto, todos os AINEs mostraram associação com defeitos cardíacos estruturais quando usados nas primeiras semanas da gravidez. Quando ibuprofeno e naproxeno são usados no terceiro trimestre, há aumento significativo do risco de fechamento prematuro do ducto arterioso com hipertensão pulmonar primária no recém-nascido.[13] Diante da escassez de estudos sobre os efeitos de ibuprofeno e naproxeno na gravidez, recomenda-se que gestantes evitem esses medicamentos ou os usem com cautela, conforme recomendação médica.[15]
O uso de aspirina para alívio da dor durante a gravidez não é recomendado. O uso de aspirina na gestação não demonstrou aumento de risco de aborto espontâneo nas primeiras semanas, mas seu consumo durante a organogênese e no terceiro trimestre pode levar ao aumento do risco de Restrição de crescimento intrauterino e hemorragia materna.[16]
Embora a aspirina deva ser evitada para o tratamento de dor, a aspirina em baixa dose é utilizada na prevenção da pré-eclâmpsia e da restrição de crescimento fetal (RCF) em pacientes com fatores de risco (ex.: pré-eclâmpsia prévia, gestações múltiplas, hipertensão e diabetes).[17]
Analgésicos contendo opioides
Gestantes que usam medicamentos prescritos contendo opioides durante a gravidez podem causar danos graves à mãe ou ao bebê.[18] Para algumas pessoas, o risco de interromper o uso de opioides prescritos pode ser mais grave do que o risco de mantê-los.[18]
Anticonvulsivantes
Muitos anticonvulsivantes comumente prescritos estão associados a um risco aumentado de defeitos congênitos, como defeitos do tubo neural; no entanto, a maioria das mulheres com epilepsia tem bebês saudáveis e uma gravidez segura.[19] Mulheres com epilepsia frequentemente ainda necessitam de tratamento para controlar ou prevenir convulsões e, portanto, precisam de orientação médica precoce (idealmente antes da concepção) para determinar a forma mais segura de proteger mãe e bebê.[19]
O Ácido valpróico e seus derivados, como o valproato de sódio e o divalproato de sódio, usados para prevenir convulsões e tratar transtornos do humor, aumentam o risco de malformações congênitas, incluindo defeitos do tubo neural, se tomados durante a gravidez.[20] Há evidências de que doses elevadas ou maior exposição in utero estão associadas a menores escores em testes de desenvolvimento neurocognitivo.[21]
Antiácidos
Azia é um sintoma comum no final da gestação, durante o qual até 80% das mulheres grávidas apresentam o problema até o fim do terceiro trimestre.[13] A azia geralmente indica o desenvolvimento da doença do refluxo gastroesofágico (DRGE), em que o esfíncter esofágico inferior relaxa devido ao aumento dos níveis de progesterona, causando maior frequência e intensidade do refluxo gástrico ou azia. Se a azia aparecer após 20 semanas de gestação ou for grave e persistente, isso pode indicar outras condições, incluindo Síndrome HELLP e pré-eclâmpsia.[22]
Antiácidos comuns incluem hidróxido de alumínio/hidróxido de magnésio (Maalox) e carbonato de cálcio (Tums). Bloqueadores dos receptores H2 de histamina e inibidores da bomba de prótons, como famotidina (Pepcid) e omeprazol (Prilosec), respectivamente, também podem ser usados para aliviar a azia, sem efeitos teratogênicos conhecidos ou malformações congênitas.[13] O hidróxido de alumínio/hidróxido de magnésio e o carbonato de cálcio, quando consumidos, não atravessam a placenta e são considerados opções farmacológicas seguras para tratar a azia, já que não há associação significativa com malformações ou danos ao feto.[15]
Gengibre e acupressão são opções não farmacológicas usadas com frequência para tratar náuseas e vômitos como alternativas aos antiácidos, bloqueadores H2 e inibidores da bomba de prótons.[23] Modificações no estilo de vida também são recomendadas. As mudanças podem incluir evitar alimentos gordurosos, reduzir o tamanho e a frequência das refeições e diminuir a ingestão de cafeína.[24]
Antiacne
A acne vulgar (acne) pode ocorrer na gravidez possivelmente devido às mudanças hormonais que influenciam a produção de sebo.[25][26] Existem poucos medicamentos antiacne seguros na gravidez. Aplicações externas de ácido azelaico, ácido glicólico ou peróxido de benzoíla (isoladamente ou combinados com clindamicina ou eritromicina) são as opções mais seguras para tratar acne leve a moderada.[26][27][28]
A eritromicina é o antibiótico de escolha para acne grave, exceto no uso do sal estolato, que pode causar hepatotoxicidade materna.[29] Nicotinamida tópica e zinco tópico são seguros; no entanto, não há classificações de categoria de gravidez da FDA.[29][30]
O ácido salicílico tópico e a dapsona tópica são classificados como categoria C pela FDA.[25][30] Medicamentos contra acne a serem evitados na gravidez incluem isotretinoína oral e tazaroteno tópico, pois há relatos de defeitos congênitos.[25][31][32]
Devido à falta de dados de segurança, o uso de retinoides tópicos, como adapaleno e tretinoína, não é recomendado.[27][33] Fármacos antiandrogênicos, incluindo espironolactona e acetato de ciproterona, devem ser evitados.[25][32]
Se houver planejamento de gravidez durante o uso de medicamentos contraindicados, recomenda-se um período de depuração antes da concepção.[26] Um fitoterápico, o vitex agnus-castus, não deve ser usado durante a gestação devido a efeitos hormonais indesejáveis.[34]
Dados de segurança apoiam o uso de terapia com luz azul e vermelha como tratamentos não farmacológicos a serem considerados.[25][26] Higiene pessoal e estilo de vida saudável também ajudam, embora restrições alimentares e agentes abrasivos em produtos de limpeza facial não sejam benéficos.[27] Como existem poucas opções seguras para tratar a acne na gravidez, recomenda-se a tomada de decisão conjunta entre o profissional de saúde e a paciente.[25][27]
Anticoagulantes
Anticoagulantes são medicamentos que evitam a formação de coágulos sanguíneos, também conhecidos como afinadores do sangue.[35] Esses medicamentos são usados tanto para prevenção quanto para tratamento em pessoas com risco ou histórico de infarto, derrame ou tromboembolismo venoso.[35]
A gravidez aumenta o risco de formação de coágulos devido à elevação de certos fatores de coagulação e compostos no corpo, risco que se intensifica logo após o parto e permanece elevado por até três meses.[36][37]
Anticoagulantes devem ser prescritos com cautela, pois podem trazer riscos ao feto em desenvolvimento, exigindo atenção à dosagem e ao manejo medicamentoso.[38]
A Varfarina (nome comercial Coumadin) é um anticoagulante amplamente prescrito em ambiente hospitalar. Em gestantes, a varfarina é contraindicada e deve ser evitada, pois atravessa a placenta. Além disso, está listada como categoria D de gravidez, indicando risco de danos ao feto.[39] Entretanto, doses diárias de até 5 mg podem ser benéficas em gestantes com maior risco de tromboembolismo.[40]
Um exemplo comum de heparina de baixo peso molecular é a enoxaparina (nome comercial Lovenox). A enoxaparina é listada como categoria B de gravidez, significando que estudos em animais não mostraram efeitos nocivos ao feto, sendo considerada segura para uso em gestantes.[39][41]
Contudo, mulheres grávidas em uso de HBPM podem não experimentar o efeito anticoagulante pleno devido à natureza do fármaco em comparação com outros anticoagulantes (como a varfarina) e pode ser menos favorável por ser administrada por injeção.[42]
A heparina não fracionada é outro tipo amplamente utilizado. Ela é classificada como categoria C, significando que estudos em animais apontaram potenciais efeitos adversos ao feto; porém, são necessárias mais pesquisas para confirmar esse risco. Pode ser usada em gestantes desde que os benefícios superem os riscos.[39]
Os Anticoagulantes orais diretos (DOACs) são tipos mais recentes de anticoagulantes disponíveis em formulação oral, amplamente usados em não gestantes. Como muitos estudos excluem gestantes, não há evidências suficientes para comprovar sua segurança e eficácia nesse grupo.[42] Atualmente, rivaroxabana (Xarelto), dabigatrana (Pradaxa) e edoxabana (Savaysa) estão listados como categoria C de gravidez, enquanto apixabana (Eliquis) está listada como categoria B.[43]
Antidepressivos
Antidiabéticos
Mulheres que têm diabetes melito podem necessitar de terapia intensiva com insulina para prevenir complicações para a mãe e o bebê. O diabetes gestacional é uma forma de diabetes diagnosticada pela primeira vez durante a gravidez e pode causar níveis elevados de glicose no sangue que afetam a mulher e o bebê.[44] Em 10–20% das mulheres cuja dieta e exercício não são suficientes para controlar a glicemia, pode ser necessário o uso de injeções de insulina.[44] Medicamentos que podem ser usados no tratamento do diabetes durante a gravidez incluem insulina, gliburida e metformina.[45]
Antidiarreicos
A diarreia não é um sintoma comum da gravidez; entretanto, pode ocorrer como resultado da redução da acidez gástrica e da motilidade intestinal lenta.[46] Subsalicilato de bismuto (Pepto-Bismol), loperamida (Imodium) e atropina/difenoxilato (Lomotil) são agentes antidiarreicos usados no tratamento da diarreia. Contudo, nem todos são seguros durante a gravidez. Um dos componentes do subsalicilato de bismuto é o salicilato, que atravessa a placenta. Por isso, há risco aumentado de restrição de crescimento intrauterino, hemorragia fetal e hemorragia materna durante a organogênese e no segundo/terceiro trimestre.[13] A loperamida possui poucos dados sobre impacto na gravidez, mas há associação com malformações cardiovasculares no primeiro trimestre.[15][13] A combinação atropina/difenoxilato não possui evidências suficientes de teratogenicidade em humanos, mas estudos com animais mostraram efeitos teratogênicos.[15]
Anti-histamínicos
Anti-histamínicos podem ser prescritos no início da gravidez para o tratamento de náusea e vômito, assim como sintomas de asma e alergia.[47] Anti-histamínicos de primeira geração incluem difenidramina (Benadryl), clorfeniramina (Diabetic Tussin), hidroxizina (Atarax) e doxepina (Sinequan).[48] Anti-histamínicos de segunda geração incluem loratadina (Claritin), cetirizina (Zyrtec) e fexofenadina (Allegra).[13] Os de primeira geração atravessam a barreira hematoencefálica, podendo causar efeitos sedativos e anticolinérgicos, embora sejam eficazes no tratamento de reações alérgicas e náusea e vômito relacionados à gravidez. Já os de segunda geração não atravessam essa barreira, evitando efeitos sedativos. Atualmente, não há associação entre uso pré-natal de anti-histamínicos e defeitos congênitos.[47]
O uso de anti-histamínicos na gravidez não foi associado a defeitos congênitos; no entanto, mais pesquisas são necessárias para alguns medicamentos a fim de confirmar a segurança.[49] É recomendado que mulheres consultem profissionais de saúde antes de tomar qualquer medicamento de venda livre ou prescrito durante a gestação, para evitar riscos à saúde.[50]
Anti-hipertensivos
Distúrbios hipertensivos são os problemas cardiovasculares mais comuns durante a gravidez, ocorrendo em 5 a 10% das gestantes.[51] Anti-hipertensivos são medicamentos usados para tratar hipertensão arterial em gestantes.[40] Essa classe de fármacos também é usada em condições como insuficiência cardíaca, infarto agudo do miocárdio e insuficiência renal.[40] Deve-se ter cautela no uso de diferentes agentes anti-hipertensivos.[51] Inibidores da Enzima Conversora da Angiotensina (ECA), Bloqueadores dos Receptores da Angiotensina II (BRA) e inibidores da neprilisina associados a bloqueadores dos receptores da angiotensina não são recomendados durante a gravidez.[51] ECA e BRA possuem efeitos fetotóxicos conhecidos quando usados no segundo ou terceiro trimestre.[52] Sinais e sintomas associados incluem lesão renal, oligoidrâmnio, anúria, contraturas articulares e hipoplasia do crânio.[52] Agentes alternativos comuns para hipertensão na gravidez incluem antiadrenérgicos e betabloqueadores, como metildopa ou metoprolol.[52]
Descongestionantes
Descongestionantes são usados junto a medicamentos para resfriado ou para combater rinite gestacional. Os mais comuns são pseudoefedrina e fenilefrina.[15] A pseudoefedrina é um agonista alfa-adrenérgico que promove vasoconstrição, reduzindo a resistência ao fluxo de ar na cavidade nasal e facilitando a respiração. Há evidências limitadas de associação entre pseudoefedrina no início da gestação e defeitos congênitos, mas é difícil isolar seu efeito devido à presença em medicamentos combinados.[18] Como ativa receptores alfa-adrenérgicos, pode aumentar a pressão arterial e causar vasoconstrição nas artérias uterinas, reduzindo o fluxo sanguíneo para o feto.[15] Pelo número reduzido de estudos, recomenda-se uso cauteloso de descongestionantes isolados ou combinados durante a gravidez. Sprays nasais salinos e outros tratamentos não farmacológicos são alternativas seguras.[13]
Suplementos alimentares
Suplemento alimentares como ácido fólico e ferro são importantes para uma gravidez saudável.[7] Alguns suplementos podem causar efeitos adversos à mãe ou ao feto.[7] Mulheres grávidas devem discutir com profissionais de saúde o uso de suplementos, a dosagem e a segurança durante a gestação.[7]
Deve-se ter cautela antes do consumo, já que suplementos são classificados como "alimentos" e não como medicamentos, não sendo regulamentados pela FDA quanto à segurança e eficácia.[53][54]
Ácido fólico
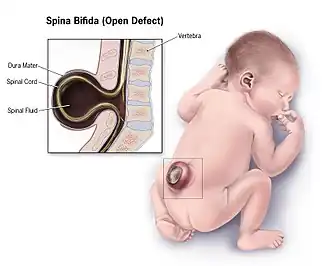
Diversos países como EUA, Canadá, Chile e Costa Rica fortificaram alimentos com ácido fólico e observaram redução na incidência de defeitos do tubo neural (DTN).[55]
O Centers for Disease Control and Prevention (CDC) recomenda que todas as mulheres em idade fértil recebam 400 μg de ácido fólico por dia, mesmo sem planejamento de gravidez. Mulheres que já tiveram gestação com DTN e desejam engravidar novamente devem receber 4000 μg diários um mês antes e durante os três primeiros meses de gestação.[56] A recomendação se baseou em um estudo do Medical Research Council (MRC) entre 1983 e 1991 em 33 centros (17 no Reino Unido e 16 em outros seis países), comparando resultados de gravidez com ácido fólico, vitaminas ou placebo. O estudo mostrou redução de 71% no risco de recorrência de DTN em gestações com ácido fólico em comparação ao placebo. Foram quatro grupos: A recebeu 4 mg de ácido fólico; B um multivitamínico com ácido fólico; C placebo; D multivitamínico sem ácido fólico. Nos grupos com ácido fólico, 6 de 593 (1%) fetos tiveram DTN, contra 21 de 602 (3,5%) sem suplementação.[57] Não foram observados benefícios significativos nos grupos com multivitamínicos sem ácido fólico.[55]
Ferro
A deficiência de ferro é comum na gravidez, sendo mais prevalente no terceiro trimestre devido ao aumento da demanda para a placenta, desenvolvimento fetal e reservas do recém-nascido. Níveis baixos de ferro podem causar fadiga, menor capacidade de trabalho, estresse cardiovascular, menor resistência a infecções e anemia ferropriva. Durante a gravidez, a anemia ferropriva pode aumentar o risco de parto prematuro, baixo peso ao nascer e mortalidade perinatal.[58]
A Ingestão Dietética Recomendada (IDR) sugere 27 mg de ferro por dia para compensar perdas, uso fetal e alterações maternas na massa de hemoglobina.[58] A OMS recomenda suplementação de 30–60 mg de ferro elementar por dia ao longo da gravidez. A necessidade varia conforme fatores individuais; para doses específicas, deve-se consultar um médico.[59]
Fontes alimentares incluem carnes, aves, peixes, ovos, leguminosas, verduras, frutas, cereais, nozes e produtos enriquecidos com ferro. Recomenda-se consumir uma fonte de Vitamina C em cada refeição, pois aumenta a absorção de ferro. Exemplos incluem brócolis, melão, frutas cítricas e sucos, kiwis, mangas, batatas, morangos, pimentões, tomates e molho de tomate. Já cafeína, suplementos de cálcio e antiácidos devem ser consumidos com intervalo de 1–2 horas das refeições ou suplementos de ferro, pois reduzem a absorção.[58]
Drogas ilícitas e recreativas
De acordo com a Organização Mundial da Saúde, o abuso de substâncias refere-se ao consumo prejudicial ou arriscado de substâncias psicoativas, o que inclui álcool e drogas ilegais.[60][61] Quando mulheres grávidas usam substâncias psicotrópicas, sejam elas prescritas ou não, isso pode ter efeitos adversos no feto em desenvolvimento.[60] Esses efeitos podem incluir causar defeitos congênitos, atraso no desenvolvimento e restrição de crescimento intrauterino.[60] Além disso, aumenta a probabilidade de várias complicações da gravidez, incluindo aborto espontâneo, parto prematuro, e expõe a mãe a um risco maior de problemas médicos, como hemorragia pós-parto e descolamento prematuro da placenta.[60]
Álcool
O álcool não deve ser consumido durante a gravidez. Mesmo uma pequena quantidade de álcool não é considerada segura para o bebê.[62] O álcool passa facilmente da corrente sanguínea da mãe através da placenta para a corrente sanguínea do feto. Como o feto é menor e não possui fígado totalmente desenvolvido, a concentração de álcool em seu sangue dura mais tempo, aumentando as chances de efeitos prejudiciais.[63] A gravidade dos efeitos do álcool em um feto em desenvolvimento depende da quantidade e da frequência do consumo, bem como da fase da gravidez. As taxas de consumo de álcool podem ser categorizadas de três formas: consumo pesado (mais de 48-60 gramas de etanol/dia), consumo moderadamente alto (24-48 gramas de etanol/dia) e consumo em excesso (4-5 doses/90 gramas de etanol de uma vez).[64]
Transtorno do espectro alcoólico fetal
O consumo excessivo e o consumo em excesso estão intimamente associados a um risco maior de transtornos do espectro alcoólico fetal (TEAF). A forma mais grave de TEAF é a síndrome alcoólica fetal (SAF). Esta costumava ser a única forma de diagnóstico para distúrbios fetais devido ao consumo de álcool, mas o termo foi ampliado para um "espectro" devido à variedade de anomalias observadas em recém-nascidos. Isso provavelmente se deve às diferentes quantidades de álcool ingeridas durante a gravidez, indicando que não existe uma dose específica que determine se o feto será afetado ou não. A SAF é caracterizada por crescimento físico mais lento, anomalias faciais distintas como filtro nasal liso, vermelhão fino e fissuras palpebrais curtas, déficit neurológico ou circunferência craniana menor. Outros problemas associados ao TEAF incluem atraso ou falta de coordenação nas habilidades motoras, problemas de audição ou visão, dificuldade de aprendizagem, transtorno de comportamento e habilidades sociais inadequadas em comparação com pares da mesma idade. Os afetados têm maior probabilidade de ter dificuldades na escola, problemas legais, comportamentos de risco e desenvolver transtorno por uso de substâncias.
Aborto espontâneo
O consumo de álcool é um fator de risco para aborto espontâneo.[65]
Abstinência neonatal
Bebês expostos ao álcool, benzodiazepínicos, barbitúricos e alguns antidepressivos (ISRSs) durante a gravidez podem apresentar abstinência neonatal.[66]
O início da apresentação clínica geralmente ocorre entre 48 e 72 horas após o nascimento, mas pode levar até 8 dias.[67][68]
Síndrome da morte súbita infantil
O consumo de álcool pelos pais está associado à síndrome da morte súbita infantil (SMSI).[69] Um estudo encontrou correlação positiva entre os dois durante as celebrações de Ano Novo e fins de semana.[70] Outro estudo descobriu que o transtorno por uso de álcool estava associado a mais que o dobro do risco.[71]
Cafeína
A cafeína é uma droga amplamente consumida por adultos devido aos seus efeitos comportamentais e estimulantes. Segundo o Colégio Americano de Obstetras e Ginecologistas, uma ingestão aceitável de cafeína para gestantes é de até 200 mg por dia.[72] O consumo de cafeína não está associado a efeitos adversos reprodutivos e de desenvolvimento.[73] A meia-vida da cafeína é maior na gravidez, de 8 a 16 horas a mais, o que significa que a substância permanece mais tempo no organismo, aumenta a exposição fetal e é eliminada mais lentamente.[72] Outras revisões abrangentes relataram que a ingestão de cafeína superior a 300 mg por dia tem sido associada a abortos espontâneos e baixo peso ao nascer, mas mais pesquisas são necessárias para estabelecer essa relação causal.[72]
Cannabis
O uso de cannabis durante a gravidez deve ser evitado.[74] Não existe uma dose segura conhecida de cannabis durante a gestação, e seu uso pode levar a defeitos congênitos, parto prematuro ou baixo peso ao nascer.[74] O tetraidrocanabinol (THC), um dos principais componentes ativos da cannabis, pode atravessar a placenta e acumular-se em altas concentrações no leite materno.[75] O consumo de cannabis durante a gravidez pode estar associado a restrições no crescimento fetal, aborto espontâneo e déficits cognitivos.[75] Recém-nascidos expostos à cannabis de forma pré-natal podem apresentar sinais de tremores aumentados e padrões de sono alterados.[76] A cannabis é a droga ilícita mais frequentemente usada entre mulheres grávidas.[77] Existem limitações significativas nas pesquisas atuais disponíveis. Uma delas é que muitos estudos foram realizados nos anos 1980.[78] Além disso, muitos estudos que avaliam a segurança da cannabis frequentemente não consideram fatores de confusão, variáveis que também podem afetar os resultados além da substância em análise. Por exemplo, o uso de tabaco e diferenças sociodemográficas muitas vezes não são devidamente ajustados.[79]
Cocaína
O uso de cocaína por gestantes é perigoso e pode levar a complicações cardiovasculares como hipertensão, infarto agudo do miocárdio e isquemia, insuficiência renal, ruptura hepática, isquemia cerebral, enfarte cerebral e até morte materna.[80] O músculo cardíaco torna-se mais sensível à cocaína durante a gravidez, devido ao aumento das concentrações de progesterona.[80] O uso de cocaína está associado ao aumento do risco de desfechos perinatais: parto prematuro, baixo peso ao nascer (menos de 2500 gramas), menor taxa de crescimento, menor tamanho e menor idade gestacional no parto.[81]
A Exposição pré-natal à cocaína (PCE) está associada a parto prematuro, defeitos congênitos, transtorno do déficit de atenção e hiperatividade (TDAH) e outras condições.[82]
Metanfetamina
O uso de metanfetamina é perigoso para gestantes e para o feto.[83] As metanfetaminas constituem uma classe de drogas com efeitos estimulantes, incluindo euforia e aumento do estado de alerta. A substância atravessa a placenta e afeta o feto durante a fase gestacional da gravidez.[83] O uso de metanfetamina durante a gestação pode resultar em bebês com menor idade gestacional ao nascer (pré-termo), baixo peso ao nascer e menor circunferência craniana.[83] O uso de metanfetamina na gravidez também impacta negativamente o desenvolvimento cerebral e o funcionamento comportamental, aumentando o risco de TDAH e redução na velocidade de processamento mental.[83]
Opioides
Opioides como heroína, fentanil, oxicodona e metadona não devem ser consumidos durante a gravidez. O uso de opioides nesse período pode causar desfechos adversos para a mãe e o feto.[18] Mulheres que utilizam opioides de forma não médica durante a gravidez apresentam maior risco de parto prematuro, baixo peso ao nascer, natimorto, defeitos congênitos específicos e síndrome de abstinência neonatal.[18]
Os opioides podem atravessar a placenta e a barreira hematoencefálica até o feto.[84] O uso de opioides é a principal causa da síndrome de abstinência neonatal, condição na qual o bebê experimenta sintomas de abstinência devido à exposição a opioides durante a gravidez. Os sintomas típicos incluem tremores, convulsões, espasmos, choro excessivo, dificuldade de sucção, ganho de peso lento, problemas respiratórios, febre, diarreia e vômito.[85] Não há consenso sobre os efeitos nas habilidades cognitivas.[86] Mais pesquisas são necessárias para determinar os efeitos a longo prazo da exposição in utero a opioides em crianças.[18]
Tabaco
Fumar durante a gravidez é perigoso para o bebê e pode causar parto prematuro, malformações congênitas como fissura labial ou palato fendido, além de aborto espontâneo.[87][74] O tabaco é a substância mais utilizada entre gestantes, chegando a 25%.[81][88] A nicotina atravessa a placenta e acumula-se nos tecidos fetais. Filhos de mulheres que fumaram intensamente apresentam maior suscetibilidade a problemas comportamentais como TDAH, baixo controle de impulsos e comportamento agressivo.[81] O tabaco contém monóxido de carbono, que pode impedir que o feto receba oxigênio suficiente. Outros riscos incluem parto prematuro, baixo peso ao nascer e maior risco de síndrome da morte súbita infantil (SMSI), até três vezes maior em comparação a bebês não expostos.[87] O tabagismo na gravidez duplica o risco de ruptura prematura de membranas, descolamento prematuro da placenta e placenta prévia. Além disso, mulheres que fumam intensamente apresentam menor probabilidade de engravidar.[89]
Referências
- ↑ Office of the Commissioner (4 de setembro de 2019). «Medicine and Pregnancy». FDA (em inglês). Consultado em 5 de agosto de 2020. Arquivado do original em 10 de agosto de 2020
- ↑ Morse B, Gehshan S, Hutchins E (1997). «Screening for Substance Abuse During Pregnancy» (PDF). National Center for Education in Maternal and Child Health. Consultado em 22 de março de 2019. Cópia arquivada (PDF) em 7 de dezembro de 2021
- ↑ National Institute on Drug Abuse (2020). «Substance Use While Pregnant and Breastfeeding». National Institute on Drug Abuse (em inglês). Consultado em 28 de julho de 2020. Cópia arquivada em 23 de junho de 2020
- ↑ NIH (abril de 2020). «Substance Use While Pregnant and Breastfeeding». National Institute on Drug Abuse (em inglês). Consultado em 13 de agosto de 2020. Cópia arquivada em 23 de junho de 2020
- ↑ «Tobacco, Alcohol, Drugs, and Pregnancy». www.acog.org (em inglês). Consultado em 13 de agosto de 2020. Cópia arquivada em 20 de outubro de 2020
- ↑ Tao, Qiuji; Shen, Yajun; Li, Yang; Luo, Huan; Yuan, Meng; Gan, Jing (2022). «Prenatal exposure to antibiotics and risk of neurodevelopmental disorders in offspring: A systematic review and meta-analysis». Frontiers in Neurology. 13. 1045865 páginas. ISSN 1664-2295. PMC 9732381
 . PMID 36504646. doi:10.3389/fneur.2022.1045865
. PMID 36504646. doi:10.3389/fneur.2022.1045865
- ↑ a b c d US Food and Drug Administration (23 de agosto de 2019). «Dietary Supplements: Tips for Women». FDA (em inglês). Consultado em 4 de agosto de 2020. Arquivado do original em 8 de agosto de 2020
- ↑ «FDA Pregnancy Categories - CHEMM». chemm.nlm.nih.gov. Consultado em 6 de agosto de 2020. Arquivado do original em 27 de agosto de 2021
- ↑ FDA (1 de abril de 2015), CFR – Code of Federal Regulations Title 21, 4, Food and Drug Administration, consultado em 9 de março de 2020, cópia arquivada em 26 de abril de 2020
- ↑ FDA (3 de dezembro de 2014), Pregnancy and Lactation Labeling (Drugs) Final Rule, Food and Drug Administration, consultado em 16 de dezembro de 2019, arquivado do original em 23 de abril de 2019
- ↑ Center for Drug Evaluation and Research (2 de março de 2020). «Pregnancy and Lactation Labeling (Drugs) Final Rule». FDA (em inglês). Consultado em 6 de agosto de 2020. Arquivado do original em 23 de abril de 2019
- ↑ «Australian categorisation system for prescription medicines in pregnancy». Australian Government. 2014. Consultado em 18 de maio de 2016. Cópia arquivada em 10 de junho de 2016
- ↑ a b c d e f g h i j Servey J, Chang J (2014-10-). «Over-the-Counter Medications in Pregnancy». American Family Physician. 90 (8): 548–55. PMID 25369643. Consultado em 31 de julho de 2020. Cópia arquivada em 8 de agosto de 2020 Verifique data em:
|data=(ajuda) - ↑ Chambers C (novembro de 2015). «Over-the-counter medications: Risk and safety in pregnancy»
 . Seminars in Perinatology. Medications in Pregnancy and Lactation. 39 (7): 541–4. PMID 26452317. doi:10.1053/j.semperi.2015.08.009
. Seminars in Perinatology. Medications in Pregnancy and Lactation. 39 (7): 541–4. PMID 26452317. doi:10.1053/j.semperi.2015.08.009
- ↑ a b c d e f g Black RA, Hill DA (-06-). «Over-the-counter medications in pregnancy». American Family Physician. 67 (12): 2517–24. PMID 12825840. Consultado em 31 de julho de 2020. Cópia arquivada em 30 de julho de 2020 Verifique data em:
|data=(ajuda) - ↑ Servey J, Chang J (outubro de 2014). «Over-the-Counter Medications in Pregnancy». American Family Physician. 90 (8): 548–55. PMID 25369643. Consultado em 31 de julho de 2020. Cópia arquivada em 8 de agosto de 2020
- ↑ Di Girolamo, Raffaella; Alameddine, Sara; Khalil, Asma; Santilli, Francesca; Rizzo, Giuseppe; Maruotti, Giuseppe Maria; Liberati, Marco; D'Antonio, Francesco (31 de dezembro de 2022). «Clinical practice guidelines on the use of aspirin in pregnancy: Systematic review»
 . European Journal of Obstetrics & Gynecology and Reproductive Biology (em inglês). 282: 64–71. PMID 36652835. doi:10.1016/j.ejogrb.2022.12.032. Consultado em 3 de maio de 2023. Cópia arquivada em 23 de maio de 2023
. European Journal of Obstetrics & Gynecology and Reproductive Biology (em inglês). 282: 64–71. PMID 36652835. doi:10.1016/j.ejogrb.2022.12.032. Consultado em 3 de maio de 2023. Cópia arquivada em 23 de maio de 2023
- ↑ a b c d e f CDC (30 de abril de 2020). «Basics About Opioid Use During Pregnancy | CDC». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 24 de julho de 2020
- ↑ a b «Epilepsy and pregnancy». nhs.uk (em inglês). 21 de dezembro de 2017. Consultado em 13 de agosto de 2020. Cópia arquivada em 12 de agosto de 2020
- ↑ Macfarlane A, Greenhalgh T (junho de 2018). «Sodium valproate in pregnancy: what are the risks and should we use a shared decision-making approach?». BMC Pregnancy and Childbirth. 18 (1). PMC 5984824
 . PMID 29859057. doi:10.1186/s12884-018-1842-x
. PMID 29859057. doi:10.1186/s12884-018-1842-x Parâmetro desconhecido
Parâmetro desconhecido |article-number=ignorado (ajuda) - ↑ Bromley R, Weston J, Adab N, Greenhalgh J, Sanniti A, McKay AJ, et al. (outubro de 2014). «Treatment for epilepsy in pregnancy: neurodevelopmental outcomes in the child». The Cochrane Database of Systematic Reviews. 2020 (10): CD010236. PMC 7390020
 . PMID 25354543. doi:10.1002/14651858.CD010236.pub2
. PMID 25354543. doi:10.1002/14651858.CD010236.pub2
- ↑ Gregory DS, Wu V, Tuladhar P (2018-11-). «The Pregnant Patient: Managing Common Acute Medical Problems». American Family Physician. 98 (9): 595–602. PMID 30325641. Consultado em 5 de agosto de 2020. Cópia arquivada em 17 de julho de 2020 Verifique data em:
|data=(ajuda) - ↑ Festin M (2014-03-). «Nausea and vomiting in early pregnancy». BMJ Clinical Evidence. 2014. PMC 3959188
 . PMID 24646807 Verifique data em:
. PMID 24646807 Verifique data em: |data=(ajuda) - ↑ Vazquez JC (2010-08-). «Constipation, haemorrhoids, and heartburn in pregnancy». BMJ Clinical Evidence. 2010. PMC 3217736
 . PMID 21418682 Verifique data em:
. PMID 21418682 Verifique data em: |data=(ajuda) - ↑ a b c d e f Kong, Y. L.; Tey, H. L. (junho de 2013). «Treatment of Acne Vulgaris During Pregnancy and Lactation»
 . Drugs (em inglês). 73 (8): 779–787. ISSN 0012-6667. PMID 23657872. doi:10.1007/s40265-013-0060-0
. Drugs (em inglês). 73 (8): 779–787. ISSN 0012-6667. PMID 23657872. doi:10.1007/s40265-013-0060-0
- ↑ a b c d Pugashetti, Rupa; Shinkai, Kanade (julho de 2013). «Treatment of acne vulgaris in pregnant patients: Treatment of acne vulgaris in pregnant patients». Dermatologic Therapy (em inglês). 26 (4): 302–311. PMID 23914887. doi:10.1111/dth.12077

- ↑ a b c d Meredith, Fiona M.; Ormerod, Anthony D. (outubro de 2013). «The Management of Acne Vulgaris in Pregnancy»
 . American Journal of Clinical Dermatology (em inglês). 14 (5): 351–358. ISSN 1175-0561. PMID 23996075. doi:10.1007/s40257-013-0041-9
. American Journal of Clinical Dermatology (em inglês). 14 (5): 351–358. ISSN 1175-0561. PMID 23996075. doi:10.1007/s40257-013-0041-9
- ↑ Worret, Wolf-Ingo; Fluhr, Joachim W. (abril de 2006). «Acne therapy with topical benzoyl peroxide, antibiotics and azelaic acid»
 . JDDG (em inglês). 4 (4): 293–300. ISSN 1610-0379. PMID 16638058. doi:10.1111/j.1610-0387.2006.05931.x. Consultado em 13 de junho de 2022. Cópia arquivada em 18 de maio de 2022
. JDDG (em inglês). 4 (4): 293–300. ISSN 1610-0379. PMID 16638058. doi:10.1111/j.1610-0387.2006.05931.x. Consultado em 13 de junho de 2022. Cópia arquivada em 18 de maio de 2022
- ↑ a b Chien, A. L.; Qi, J.; Rainer, B.; Sachs, D. L.; Helfrich, Y. R. (1 de março de 2016). «Treatment of Acne in Pregnancy». The Journal of the American Board of Family Medicine (em inglês). 29 (2): 254–262. ISSN 1557-2625. PMID 26957383. doi:10.3122/jabfm.2016.02.150165

- ↑ a b Liu, Haibo; Yu, Haiyan; Xia, Jun; Liu, Ling; Liu, Guan J.; Sang, Hong; Peinemann, Frank (1 de maio de 2020). «Topical azelaic acid, salicylic acid, nicotinamide, sulphur, zinc and fruit acid (alpha-hydroxy acid) for acne». The Cochrane Database of Systematic Reviews. 5 (5): CD011368. ISSN 1469-493X. PMC 7193765
 . PMID 32356369. doi:10.1002/14651858.CD011368.pub2
. PMID 32356369. doi:10.1002/14651858.CD011368.pub2
- ↑ Costa, Caroline S; Bagatin, Ediléia; Martimbianco, Ana Luiza C; da Silva, Edina MK; Lúcio, Marília M; Magin, Parker; Riera, Rachel (24 de novembro de 2018). Cochrane Skin Group, ed. «Oral isotretinoin for acne». Cochrane Database of Systematic Reviews (em inglês). 2019 (2): CD009435. PMC 6383843
 . PMID 30484286. doi:10.1002/14651858.CD009435.pub2
. PMID 30484286. doi:10.1002/14651858.CD009435.pub2
- ↑ a b Murase, Jenny E.; Heller, Misha M.; Butler, Daniel C. (março de 2014). «Safety of dermatologic medications in pregnancy and lactation»
 . Journal of the American Academy of Dermatology (em inglês). 70 (3): 401.e1–401.e14. PMID 24528911. doi:10.1016/j.jaad.2013.09.010. Consultado em 28 de abril de 2022. Cópia arquivada em 20 de março de 2022
. Journal of the American Academy of Dermatology (em inglês). 70 (3): 401.e1–401.e14. PMID 24528911. doi:10.1016/j.jaad.2013.09.010. Consultado em 28 de abril de 2022. Cópia arquivada em 20 de março de 2022
- ↑ Leachman, Sancy A.; Reed, Barbara R. (abril de 2006). «The Use of Dermatologic Drugs in Pregnancy and Lactation»
 . Dermatologic Clinics (em inglês). 24 (2): 167–197. PMID 16677965. doi:10.1016/j.det.2006.01.001. Consultado em 28 de abril de 2022. Cópia arquivada em 15 de junho de 2022
. Dermatologic Clinics (em inglês). 24 (2): 167–197. PMID 16677965. doi:10.1016/j.det.2006.01.001. Consultado em 28 de abril de 2022. Cópia arquivada em 15 de junho de 2022
- ↑ Daniele, Claudia; Thompson Coon, Joanna; Pittler, Max H.; Ernst, Edzard (2005). «Vitex agnus castus: a systematic review of adverse events». Drug Safety. 28 (4): 319–332. ISSN 0114-5916. PMID 15783241. doi:10.2165/00002018-200528040-00004
- ↑ a b «Anticoagulant medicines». nhs.uk (em inglês). 6 de fevereiro de 2018. Consultado em 30 de julho de 2020. Cópia arquivada em 13 de abril de 2020
- ↑ Alshawabkeh L, Economy KE, Valente AM (outubro de 2016). «Anticoagulation During Pregnancy: Evolving Strategies With a Focus on Mechanical Valves». Journal of the American College of Cardiology. 68 (16): 1804–1813. PMID 27737747. doi:10.1016/j.jacc.2016.06.076
 . Consultado em 31 de julho de 2020. Cópia arquivada em 24 de fevereiro de 2020
. Consultado em 31 de julho de 2020. Cópia arquivada em 24 de fevereiro de 2020
- ↑ CDC (12 de fevereiro de 2020). «Pregnant? Don't Overlook Blood Clots | CDC». Centers for Disease Control and Prevention (em inglês). Consultado em 31 de julho de 2020. Cópia arquivada em 24 de julho de 2020
- ↑ «UpToDate». www.uptodate.com. Consultado em 31 de julho de 2020. Cópia arquivada em 3 de dezembro de 2021
- ↑ a b c Toyoda K (2013). «Antithrombotic therapy for pregnant women». Neurologia Medico-Chirurgica. 53 (8): 526–30. PMID 23979047. doi:10.2176/nmc.53.526

- ↑ a b c Xu Z, Fan J, Luo X, Zhang WB, Ma J, Lin YB, et al. (outubro de 2016). «Anticoagulation Regimens During Pregnancy in Patients With Mechanical Heart Valves: A Systematic Review and Meta-analysis»
 . The Canadian Journal of Cardiology. 32 (10): 1248.e1–1248.e9. PMID 26927861. doi:10.1016/j.cjca.2015.11.005
. The Canadian Journal of Cardiology. 32 (10): 1248.e1–1248.e9. PMID 26927861. doi:10.1016/j.cjca.2015.11.005
- ↑ Deruelle P, Coulon C (dezembro de 2007). «The use of low-molecular-weight heparins in pregnancy--how safe are they?». Current Opinion in Obstetrics & Gynecology. 19 (6): 573–7. PMID 18007136. doi:10.1097/GCO.0b013e3282f10e33
- ↑ a b Lameijer H, Aalberts JJ, van Veldhuisen DJ, Meijer K, Pieper PG (setembro de 2018). «Efficacy and safety of direct oral anticoagulants during pregnancy; a systematic literature review». Thrombosis Research. 169: 123–127. PMID 30036784. doi:10.1016/j.thromres.2018.07.022
- ↑ Myers B, Neal R, Myers O, Ruparelia M (março de 2016). «Unplanned pregnancy on a direct oral anticoagulant (Rivaroxaban): A warning». Obstetric Medicine. 9 (1): 40–2. PMC 4950440
 . PMID 27512489. doi:10.1177/1753495X15621814
. PMID 27512489. doi:10.1177/1753495X15621814
- ↑ a b «Gestational diabetes - Diagnosis and treatment - Mayo Clinic». www.mayoclinic.org (em inglês). Consultado em 5 de agosto de 2020. Cópia arquivada em 7 de agosto de 2020
- ↑ Buchanan TA, Xiang AH, Page KA (novembro de 2012). «Gestational diabetes mellitus: risks and management during and after pregnancy». Nature Reviews. Endocrinology. 8 (11): 639–49. PMC 4404707
 . PMID 22751341. doi:10.1038/nrendo.2012.96
. PMID 22751341. doi:10.1038/nrendo.2012.96
- ↑ Giddings SL, Stevens AM, Leung DT (2016-03-). «Traveler's Diarrhea». The Medical Clinics of North America. 100 (2): 317–30. PMC 4764790
 . PMID 26900116. doi:10.1016/j.mcna.2015.08.017 Verifique data em:
. PMID 26900116. doi:10.1016/j.mcna.2015.08.017 Verifique data em: |data=(ajuda) - ↑ a b Gilboa SM, Ailes EC, Rai RP, Anderson JA, Honein MA (2014-12-). «Antihistamines and birth defects: a systematic review of the literature». Expert Opinion on Drug Safety. 13 (12): 1667–98. PMC 4474179
 . PMID 25307228. doi:10.1517/14740338.2014.970164 Verifique data em:
. PMID 25307228. doi:10.1517/14740338.2014.970164 Verifique data em: |data=(ajuda) - ↑ Fein MN, Fischer DA, O'Keefe AW, Sussman GL (2019). «1-antihistamines and should be the first-line antihistamines for the treatment of allergic rhinitis and urticaria». Allergy, Asthma, and Clinical Immunology. 15. 61 páginas. PMC 6771107
 . PMID 31582993. doi:10.1186/s13223-019-0375-9
. PMID 31582993. doi:10.1186/s13223-019-0375-9
- ↑ CDC (4 de abril de 2018). «Key Findings: Antihistamines and Birth Defects | NCBDDD | CDC». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 14 de julho de 2020
- ↑ CDC (31 de julho de 2020). «Pregnant or thinking of getting pregnant? | CDC». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 28 de julho de 2020
- ↑ a b c Regitz-Zagrosek V, Roos-Hesselink JW, Bauersachs J, Blomström-Lundqvist C, Cífková R, De Bonis M, et al. (2018-09-). «2018 ESC Guidelines for the management of cardiovascular diseases during pregnancy». European Heart Journal. 39 (34): 3165–3241. PMID 30165544. doi:10.1093/eurheartj/ehy340
 . hdl:10044/1/72032
. hdl:10044/1/72032 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b c Dathe K, Schaefer C (2019-11-). «The Use of Medication in Pregnancy». Deutsches Ärzteblatt International. 116 (46): 783–790. PMC 6935972
 . PMID 31920194. doi:10.3238/arztebl.2019.0783 Verifique data em:
. PMID 31920194. doi:10.3238/arztebl.2019.0783 Verifique data em: |data=(ajuda) - ↑ Office of the Commissioner (9 de fevereiro de 2019). «FDA 101: Dietary Supplements». FDA (em inglês). Consultado em 4 de agosto de 2020. Arquivado do original em 7 de março de 2023
- ↑ Dwyer JT, Coates PM, Smith MJ (2018-01-). «Dietary Supplements: Regulatory Challenges and Research Resources». Nutrients. 10 (1): 41. PMC 5793269
 . PMID 29300341. doi:10.3390/nu10010041
. PMID 29300341. doi:10.3390/nu10010041 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b Ramakrishnan, Usha; Grant, Frederick; Goldenberg, Tamar; Zongrone, Amanda; Martorell, Reynaldo (28 de junho de 2012). «Effect of Women's Nutrition before and during Early Pregnancy on Maternal and Infant Outcomes: A Systematic Review: Periconceptual nutrition and maternal and infant outcomes». Paediatric and Perinatal Epidemiology (em inglês). 26: 285–301. PMID 22742616. doi:10.1111/j.1365-3016.2012.01281.x

- ↑ CDC (28 de junho de 2022). «Folic Acid Recommendations». Centers for Disease Control and Prevention (em inglês). Consultado em 3 de maio de 2023. Cópia arquivada em 25 de agosto de 2017
- ↑ «Effectiveness in Disease and Injury Prevention Use of Folic Acid for Prevention of Spina Bifida and Other Neural Tube Defects -- 1983-1991». www.cdc.gov. Consultado em 3 de maio de 2023. Cópia arquivada em 8 de maio de 2023
- ↑ a b c Health Canada (2009). Prenatal Nutrition Guidelines for Health Professionals (PDF). [S.l.]: Health Canada. ISBN 978-1-100-12207-6. Consultado em 5 de maio de 2023. Cópia arquivada (PDF) em 4 de maio de 2023
- ↑ WHO (2012). Guideline: Daily iron and folic acid supplementation in pregnant women (PDF). [S.l.]: World Health Organization. ISBN 978-92-4-150199-6. Consultado em 5 de maio de 2023. Cópia arquivada (PDF) em 4 de maio de 2023
- ↑ a b c d Cohen, Abigail; Osorio, Ruby; Page, Louise M. (2017). «Substance misuse in pregnancy». Elsevier BV. Obstetrics, Gynaecology & Reproductive Medicine. 27 (10): 316–321. ISSN 1751-7214. doi:10.1016/j.ogrm.2017.07.003
- ↑ «Substance Abuse». OMS. 7 de dezembro de 2019. Consultado em 18 de setembro de 2023. Cópia arquivada em 21 de junho de 2023
- ↑ CDC (1 de julho de 2020). «Alcohol Use in Pregnancy». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 28 de junho de 2015
- ↑ «Pregnancy and Alcohol: Safety, Effects & Addiction». American Pregnancy Association. 27 de abril de 2012. Consultado em 21 de março de 2019. Cópia arquivada em 15 de fevereiro de 2020
- ↑ Ornoy A, Ergaz Z (2010-02-). «Alcohol abuse in pregnant women: effects on the fetus and newborn, mode of action and maternal treatment». International Journal of Environmental Research and Public Health. 7 (2): 364–79. PMC 2872283
 . PMID 20616979. doi:10.3390/ijerph7020364
. PMID 20616979. doi:10.3390/ijerph7020364 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Oliver A, Overton C (maio de 2014). «Diagnosis and management of miscarriage». The Practitioner. 258 (1771): 25–8, 3. PMID 25055407
- ↑ «Neonatal abstinence Syndrome». MedlinePlus. US Library of Medicine. 2017. Consultado em 27 de julho de 2017. Cópia arquivada em 28 de julho de 2017
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ Ghazanfarpour M, Najafi MN, Roozbeh N, Mashhadi ME, Keramat-Roudi A, Mégarbane B, Tsatsakis A, Moghaddam MM, Rezaee R (-06-). «Therapeutic approaches for neonatal abstinence syndrome: a systematic review of randomized clinical trials». Daru: Journal of Faculty of Pharmacy, Tehran University of Medical Sciences. 27 (1): 423–431. PMC 6593026
 . PMID 31093953. doi:10.1007/s40199-019-00266-3 Verifique data em:
. PMID 31093953. doi:10.1007/s40199-019-00266-3 Verifique data em: |data=(ajuda) - ↑ Ko JY, Wolicki S, Barfield WD, Patrick SW, Broussard CS, Yonkers KA, Naimon R, Iskander J (2017). «CDC Grand Rounds: Public Health Strategies to Prevent Neonatal Abstinence Syndrome». MMWR. Morbidity and Mortality Weekly Report. 66 (9): 242–245. PMC 5687191
 . PMID 28278146. doi:10.15585/mmwr.mm6609a2
. PMID 28278146. doi:10.15585/mmwr.mm6609a2
- ↑ Van Nguyen JM, Abenhaim HA (2013-10-). «Sudden infant death syndrome: review for the obstetric care provider». American Journal of Perinatology. 30 (9): 703–714. PMID 23292938. doi:10.1055/s-0032-1331035 Verifique data em:
|data=(ajuda) - ↑ Phillips DP, Brewer KM, Wadensweiler P (2011-03-). «Alcohol as a risk factor for sudden infant death syndrome (SIDS)». Addiction. 106 (3): 516–525. PMID 21059188. doi:10.1111/j.1360-0443.2010.03199.x. Consultado em 6 de setembro de 2017. Cópia arquivada em 6 de setembro de 2017 Verifique data em:
|data=(ajuda) - ↑ O'Leary CM, Jacoby PJ, Bartu A, D'Antoine H, Bower C (2013-03-). «Maternal alcohol use and sudden infant death syndrome and infant mortality excluding SIDS». Pediatrics. 131 (3): e770–e778. PMID 23439895. doi:10.1542/peds.2012-1907 Verifique data em:
|data=(ajuda) - ↑ a b c Temple JL, Bernard C, Lipshultz SE, Czachor JD, Westphal JA, Mestre MA (2017). «The Safety of Ingested Caffeine: A Comprehensive Review». Frontiers in Psychiatry. 8. 80 páginas. PMC 5445139
 . PMID 28603504. doi:10.3389/fpsyt.2017.00080
. PMID 28603504. doi:10.3389/fpsyt.2017.00080
- ↑ Wikoff D, Welsh BT, Henderson R, Brorby GP, Britt J, Myers E, et al. (novembro de 2017). «Systematic review of the potential adverse effects of caffeine consumption in healthy adults, pregnant women, adolescents, and children». Food and Chemical Toxicology. 109 (Pt 1): 585–648. PMID 28438661. doi:10.1016/j.fct.2017.04.002

- ↑ a b c CDC (3 de junho de 2020). «Commit to Healthy Choices to Help Prevent Birth Defects | CDC». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 4 de março de 2021
- ↑ a b Fonseca BM, Correia-da-Silva G, Almada M, Costa MA, Teixeira NA (2013). «The Endocannabinoid System in the Postimplantation Period: A Role during Decidualization and Placentation». International Journal of Endocrinology (Review). 2013. 510540 páginas. PMC 3818851
 . PMID 24228028. doi:10.1155/2013/510540
. PMID 24228028. doi:10.1155/2013/510540
- ↑ El Marroun H, Brown QL, Lund IO, Coleman-Cowger VH, Loree AM, Chawla D, Washio Y (2018-11-). «An epidemiological, developmental and clinical overview of cannabis use during pregnancy». Preventive Medicine. 116: 1–5. PMID 30171964. doi:10.1016/j.ypmed.2018.08.036
 . hdl:1765/110103
. hdl:1765/110103 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ Committee on the Health Effects of Marijuana: An Evidence Review and Research Agenda; Board on Population Health and Public Health Practice; Health and Medicine Division; National Academies of Sciences Engineering (12 de janeiro de 2017). Prenatal, Perinatal, and Neonatal Exposure to Cannabis. [S.l.]: National Academies Press (US). Consultado em 22 de março de 2019. Cópia arquivada em 11 de agosto de 2020
- ↑ Grant KS, Petroff R, Isoherranen N, Stella N, Burbacher TM (2018-02-). «Cannabis use during pregnancy: Pharmacokinetics and effects on child development». Pharmacology & Therapeutics. 182: 133–151. PMC 6211194
 . PMID 28847562. doi:10.1016/j.pharmthera.2017.08.014 Verifique data em:
. PMID 28847562. doi:10.1016/j.pharmthera.2017.08.014 Verifique data em: |data=(ajuda) - ↑ Metz TD, Borgelt LM (2018-11-). «Marijuana Use in Pregnancy and While Breastfeeding». Obstetrics and Gynecology. 132 (5): 1198–1210. PMC 6370295
 . PMID 30234728. doi:10.1097/AOG.0000000000002878 Verifique data em:
. PMID 30234728. doi:10.1097/AOG.0000000000002878 Verifique data em: |data=(ajuda) - ↑ a b Smid MC, Metz TD, Gordon AJ (2019-03-). «Stimulant Use in Pregnancy: An Under-recognized Epidemic Among Pregnant Women». Clinical Obstetrics and Gynecology. 62 (1): 168–184. PMC 6438363
 . PMID 30601144. doi:10.1097/GRF.0000000000000418 Verifique data em:
. PMID 30601144. doi:10.1097/GRF.0000000000000418 Verifique data em: |data=(ajuda) - ↑ a b c Cornelius MD, Day NL (abril de 2009). «Developmental consequences of prenatal tobacco exposure». Current Opinion in Neurology. 22 (2): 121–5. PMC 2745235
 . PMID 19532034. doi:10.1097/WCO.0b013e328326f6dc
. PMID 19532034. doi:10.1097/WCO.0b013e328326f6dc
- ↑ Ackerman JP, Riggins T, Black MM (2010-03-). «A review of the effects of prenatal cocaine exposure among school-aged children». Pediatrics. 125 (3): 554–65. PMC 3150504
 . PMID 20142293. doi:10.1542/peds.2009-0637 Verifique data em:
. PMID 20142293. doi:10.1542/peds.2009-0637 Verifique data em: |data=(ajuda) - ↑ a b c d Freye E (2009). «Treatment Options in Methamphetamine Addiction and Withdrawal». Pharmacology and Abuse of Cocaine, Amphetamines, Ecstasy and Related Designer Drugs. Dordrecht: Springer Netherlands. pp. 131–133. ISBN 978-90-481-2447-3. doi:10.1007/978-90-481-2448-0_20
- ↑ Lind JN, Interrante JD, Ailes EC, Gilboa SM, Khan S, Frey MT, et al. (-06-). «Maternal Use of Opioids During Pregnancy and Congenital Malformations: A Systematic Review». Pediatrics. 139 (6): e20164131. PMC 5561453
 . PMID 28562278. doi:10.1542/peds.2016-4131 Verifique data em:
. PMID 28562278. doi:10.1542/peds.2016-4131 Verifique data em: |data=(ajuda) - ↑ https://docs.google.com/document/d/1p0fwjFSlsgWkT643vw04_HNl4NKe9rBIu9vbbOD5uf8/edit [ligação inativa]
- ↑ Nygaard E, Slinning K, Moe V, Walhovd KB (2017-02-). «Cognitive function of youths born to mothers with opioid and poly-substance abuse problems during pregnancy». Child Neuropsychology. 23 (2): 159–187. PMID 26471942. doi:10.1080/09297049.2015.1092509
 . hdl:10852/55276
. hdl:10852/55276 Verifique data em:
Verifique data em: |data=(ajuda) - ↑ a b CDCTobaccoFree (6 de fevereiro de 2018). «Smoking During Pregnancy». Centers for Disease Control and Prevention. Consultado em 21 de março de 2019. Cópia arquivada em 20 de setembro de 2020
- ↑ Tawfeek, Karam T; Zuhair, Ghufran Z.; Al-hussaniy, Hany A.; naji, Meena (2022). «Neurodevelopmental Abnormalities in Children Associated with Maternal Use of Psychoactive Medication». Medical and Pharmaceutical Journal (em inglês). 1 (2): 24–33. ISSN 2957-6067. doi:10.55940/medphar202210

- ↑ CDCTobaccoFree (29 de maio de 2019). «Smoking During Pregnancy». Centers for Disease Control and Prevention (em inglês). Consultado em 4 de agosto de 2020. Cópia arquivada em 20 de setembro de 2020
Leituras adicionais
- Briggs GG, Freeman RK, Towers CV, Forinash A (2016). Drugs in pregnancy and lactation: a reference guide to fetal and neonatal risk 11th ed. [S.l.]: Lippincott Williams & Wilkins. ISBN 978-1-4963-5037-4
- Lee A, Inch S, Finegan D (2019). Therapeutics in Pregnancy and Lactation. [S.l.]: Routledge. ISBN 978-1-315-34863-6
- Lowinson JH, Ruiz P, Millman RB, Langrod JG, eds. (2005). «Capítulo 53. Efeitos maternos e neonatais do álcool e drogas por Loretta B. Finnegan e Stephen R. Kandall». Substance abuse: a comprehensive textbook. [S.l.]: Lippincott Williams & Wilkins. pp. 805–839. ISBN 9780781734745
- Schaefer C, ed. (2001). Drugs during pregnancy and lactation: handbook of prescription drugs and comparative risk assessment. [S.l.]: Elsevier. ISBN 978-0-444-50763-1
- Schaefer C, Peters PW, Miller RK, eds. (2011). Drugs during pregnancy and lactation: treatment options and risk assessment 2nd ed. [S.l.]: Elsevier. ISBN 978-0-08-054977-4. Consultado em 4 de agosto de 2020. Cópia arquivada em 9 de novembro de 2023