Desordens do espectro alcoólico fetal
| Transtornos do espectro alcoólico fetal | |
|---|---|
| Sinónimos | Transtornos do espectro alcoólico fetal, TEAF, SAF, EAP, Exposição pré-natal a substâncias, EPS |
 | |
| Apenas 10% dos indivíduos com TEAF apresentam características faciais associadas. | |
| Especialidade | Embriologia, Toxicologia, Psiquiatria, Neurologia, Ginecologia, Obstetrícia, Neonatologia, Pediatria |
| Sintomas | Anomalias craniofaciais, baixa estatura, baixo peso corporal, microcefalia, má coordenação, problemas de comportamento semelhantes ao TDAH, dificuldades de aprendizagem e de fala, deficiência intelectual[1][2] |
| Complicações | Bebês: aborto espontâneo, natimorto, parto prematuro Adultos: alcoolismo, abuso de substâncias |
| Início habitual | Pré-natal |
| Duração | Vitalícia[1][3] |
| Tipos | Síndrome alcoólica fetal, síndrome alcoólica fetal parcial, transtorno do neurodesenvolvimento relacionado ao álcool, encefalopatia estática, defeitos congênitos relacionados ao álcool[1] |
| Causas | Consumo de álcool durante a gravidez[1] |
| Método de diagnóstico | Baseado nos sintomas e na exposição pré-natal ao álcool[1] |
| Condições semelhantes | TDAH, autismo, transtorno bipolar, transtorno de conduta, dificuldade de aprendizagem, transtorno desafiador de oposição |
| Prevenção | Evitar o consumo de álcool durante a gravidez[4] |
| Tratamento | Terapia de interação pai-filho, intervenções comportamentais, eventualmente medicamentos[5] |
| Prognóstico | Varia conforme a gravidade; na SAF a expectativa de vida é de cerca de 34 anos sem intervenções.[6] Não confirmado (outros tipos) |
| Frequência | Estimativas entre 1 em 20 (~390 milhões)[7] e 1 em 13 (~600 milhões) (todos os tipos)[8] 0,2 a 9 por 1.000 (SAF) |
| Classificação e recursos externos | |
| CID-10 | Q86.0 |
| CID-9 | 760.71 |
| DiseasesDB | 32957 |
| MedlinePlus | 000911 |
| eMedicine | ped/767 |
| MeSH | D005310 |
As desordens do espectro alcoólico fetal são um grupo de condições que podem ocorrer numa pessoa cuja mãe tenha consumido álcool durante a gravidez.[9][10] Entre os problemas que ocorrem estão anomalias estruturais, comportamentais e neurocognitivas, déficit intelectual e de crescimento, baixo peso ao nascer, microcefalia e perda de audição ou visão.[10][11] Indivíduos afetados tem geralmente maior propensão a dificuldades de aprendizado e experiências escolares problemáticas, conflitos com a lei, comportamento sexual inadequado e problemas com o álcool ou outras drogas.[10][12] O mais grave destes distúrbios denomina-se síndrome alcoólica fetal.[9][13] Entre outros tipos estão a síndrome alcoólica fetal parcial, encefalopatia alcoólica e as desordens neurocomportamentais da exposição ao álcool.[9][14]
Levantamentos feitos nos Estados Unidos detectaram que cerca de 10% das mulheres grávidas consomem álcool no último mês de gestação e que 20% a 30% consumiram em algum momento da gravidez.[15] Cerca de 4,7% das gestantes norte-americanas são alcoólatras.[16] O risco de complicações depende da quantidade de álcool consumida, a frequência de consumo e em que momento da gestação ele ocorre. Outros fatores de risco podem incluir idade avançada, tabagismo e má alimentação.[15] O consumo de pequenas doses de álcool neste período também é deletério e, embora não cause anomalias faciais, pode causar problemas de comportamento, pois a substância atravessa a barreira hematoencefálica e afeta direta e indiretamente o desenvolvimento do feto.[16][17] O diagnóstico é baseado em sinais e sintomas.[9]
A condição dos indivíduos afetados é permanente, mas o tratamento de suporte pode melhorar os sintomas, visando promover melhor adaptação do sujeito ao seu meio, levando em conta suas dificuldades específicas, prevenção e abordagem de consequências relacionadas ao quadro.[9][18] Terapia medicamentosa também pode ser utilizada em casos específicos.[19]
Estima-se que as desordens do espectro alcoólico fetal afetem entre 2% e 5% de pessoas nos Estados Unidos (0,2 a 9 afetados por 1000 nascidos vivos) e na Europa Ocidental.[20] Na África do Sul, algumas populações chegam a ter taxas de prevalência de até 9%.[14] O termo "síndrome alcoólica fetal" foi utilizado pela primeira vez em 1973.[14]
Sinais e sintomas

Os principais sinais da síndrome alcoólica fetal (SAF) necessários para o diagnóstico incluem:
- Deficiência de crescimento ou falha em prosperar: crescimento fetal lento, baixo peso ao nascer ou altura, perímetro cefálico reduzido (microcefalia)[21][a]
- Malformações congênitas dos lábios: pequenas fendas palpebrais, filtro labial liso e lábio superior fino.[22][b]
- Danos no sistema nervoso: comprometimento neurológico estrutural ou funcional clinicamente significativo[c]
Popova et al. identificaram 428 condições da CID-10 como coexistentes em indivíduos com SAF. Excluindo as condições usadas no diagnóstico de SAF, condições coexistentes com prevalência de 50% ou mais incluem:[23]
- Transtorno de conduta, problemas de comportamento, comportamento disruptivo ou impulsividade[d]
- Transtorno do desenvolvimento da linguagem[e]
- Perda auditiva[f]
- Deficiência visual, incluindo cegueira ou astigmatismo[g]
- Atraso do desenvolvimento, transtorno cognitivo ou deficiência mental[h]
- Nascimento prematuro[i]
- Dependência de substâncias[j]
- Malformação congênita da retina[k]
- Fusão congênita de vértebras cervicais ou fusão da coluna cervical[l]
- Transtorno do déficit de atenção com hiperatividade ou atenção prejudicada[m]
- Pequenas aberturas oculares (blefarofimose),[n] ou aumento anormal da distância entre os olhos, ou ambos (hipertelorismo)[o]
Outras condições do TEAF são expressões parciais da SAF, em que o sistema nervoso central apresenta déficits clínicos. Nessas outras condições, o indivíduo pode estar em maior risco de desfechos adversos porque há dano cerebral sem sinais visuais associados de crescimento deficiente ou a "face da SAF", que normalmente desencadearia uma avaliação. Esses indivíduos podem ser diagnosticados incorretamente com transtornos mentais primários como TDAH ou Transtorno desafiador opositivo sem considerar que o dano cerebral é a causa subjacente, exigindo um tratamento diferente dos transtornos mentais típicos. Embora outras condições do TEAF ainda não estejam incluídas como diagnósticos na CID ou no DSM-IV-TR, elas representam comprometimentos significativos no comportamento funcional devido ao dano cerebral subjacente.[24] Muitas manifestações dos transtornos do espectro alcoólico fetal são de desenvolvimento. Assim, embora uma criança possa parecer "normal" ao nascer, deficiências intelectuais causadas pelo álcool antes do nascimento podem não se manifestar até o início da vida escolar.[25]
De forma mais ampla, o consumo de álcool durante a gravidez também está associado a:[1][26]
- Deficiência intelectual, tanto em medidas globais de QI quanto em muitos testes funcionais[27]
- Mortalidade fetal, como aborto espontâneo (aborto), natimorto,[28] e síndrome da morte súbita infantil[29]
- Violência doméstica e potencial dano ao bebê[28]
- Problemas de sono e sucção no bebê[30]
- Coração: sopro cardíaco que frequentemente desaparece até o primeiro ano de vida. Comunicação interventricular, comunicação interatrial, tetralogia de Fallot, coarctação da aorta ou disfunção do ritmo cardíaco.
- Ossos: anomalias nas articulações, incluindo posição e função anormais, alterações nos padrões das linhas palmares, falanges distais pequenas e unhas mínimas no quinto dedo.
- Rins: em ferradura, aplásicos, displásicos ou hipoplásicos.
- Olhos: estrabismo, hipoplasia do nervo óptico[31] (que pode causar fotofobia, diminuição da acuidade visual ou movimentos oculares involuntários).
- Fissura labial com ou sem fissura palatina: o álcool é conhecido como antagonista do ácido fólico, e o palato e o lábio do bebê se desenvolvem durante o primeiro trimestre da gravidez (primeiras 12 semanas). O consumo excessivo de álcool e a embriaguez episódica nesse período têm sido associados a fissuras orofaciais.[32]
- Problemas ocasionais: ptose da pálpebra, microftalmia, pescoço alado, pescoço curto, sinostose radioulnar, espinha bífida e hidrocefalia.
O álcool também pode prejudicar a fertilidade de mulheres que planejam engravidar. Os efeitos adversos do álcool podem levar à desnutrição, convulsões, vômitos e desidratação. A mãe pode sofrer de ansiedade e depressão, o que pode resultar em abuso/negligência da criança. Também foi observado que, quando a mãe grávida interrompe o consumo de álcool, seus efeitos são visíveis no bebê. O bebê pode apresentar irritabilidade, choro frequente, distúrbios de sono, fraqueza na sucção e aumento da fome.[33]
Em 2019, um estudo descobriu que indivíduos com TEAF têm maior risco de hipertensão, independentemente de raça/etnia e obesidade.[34]
Causas
Os transtornos do espectro alcoólico fetal são causados pela exposição ao álcool durante o desenvolvimento gestacional.[1] Se um indivíduo não foi exposto ao álcool antes do nascimento, ele não terá TEAF.[35] No entanto, nem todos os bebês expostos ao álcool in utero terão SAF, TEAF ou complicações na gestação detectáveis.[36]
Limite de exposição
Não foi estabelecido um nível seguro de exposição fetal ao álcool.[37] Como o álcool é um conhecido teratógeno, é considerado antiético realizar ensaios clínicos randomizados em mulheres grávidas para determinar os efeitos tóxicos precisos do álcool.[38] Entre as mulheres que consomem qualquer quantidade de álcool durante a gravidez, o risco de dar à luz uma criança com TEAF é de cerca de 15%, e de uma criança com SAF é de aproximadamente 1,5%. Beber 2 dose padrãos por dia, ou 6 doses padrão em um curto período, acarreta um risco de 4,3% de nascimento com SAF (ou seja, uma em cada 23 gestantes que consomem muito álcool dará à luz uma criança com SAF). Além disso, anomalias congênitas relacionadas ao álcool ocorrem com uma incidência de aproximadamente uma em cada 67 mulheres que bebem durante a gestação.[36] Entre as mães que possuem transtorno por uso de álcool, estima-se que um terço de seus filhos tenham SAF.[39] A variação observada nos desfechos do consumo de álcool durante a gestação é pouco compreendida. Fatores agravantes podem incluir idade materna avançada, tabagismo, má alimentação,[40][41] genética e fatores de risco sociais.[42]
O risco de TEAF aumenta com a quantidade consumida, a frequência do consumo e a maior duração da ingestão de álcool durante a gestação.[42][41][43] A concentração de álcool no sangue foi identificada como um fator relevante.[44] Todas as formas de álcool, como cerveja, vinho e destilados, apresentam risco semelhante.[45] O consumo excessivo de álcool aumenta as chances e a gravidade dos TEAF a tal ponto que Svetlana Popova afirmou que "o consumo excessivo de álcool é a causa direta da SAF ou TEAF".[46] Pequenas quantidades de álcool podem não causar uma aparência anormal, contudo, pequenas quantidades de consumo durante a gestação podem gerar problemas comportamentais e também aumentar o risco de aborto espontâneo.[47][39][48][49] Estudos quase-experimentais fornecem evidência moderadamente forte de que a exposição pré-natal ao álcool causa efeitos cognitivos prejudiciais, e algumas evidências de redução do peso ao nascer, embora nenhum estudo tenha sido totalmente avaliado como de baixo risco de viés e a quantidade de estudos tenha sido limitada.[50]
As evidências são inconsistentes e contraditórias quanto aos efeitos do consumo baixo a moderado, por exemplo, menos de 12 gramas de etanol por dia.[51] Muitos estudos não encontram efeito significativo, mas alguns encontram associações benéficas, e outros associações prejudiciais, até mesmo sobre os mesmos desfechos. A síntese dos estudos por país mostra alguma similaridade nos resultados, devido ao uso das mesmas fontes de dados. A definição de baixo consumo de álcool varia significativamente entre os estudos e muitas vezes não incorpora todos os aspectos de tempo, dose e duração. O viés de recordação e fatores socioeconômicos e psicossociais foram controlados na maioria dos estudos, mas é provável que ainda exista confundimento residual devido a fatores ausentes e variação nos métodos, maior do que quaisquer efeitos observados.[52][53][39][54][30][26]
Consumo paterno de álcool
Pais que consomem álcool antes da concepção podem contribuir para o TEAF por meio de modificações epigenéticas de longo prazo no esperma paterno,[55] mas isso tem sido questionado; as evidências de que isso pode causar SAF completo são inconclusivas.[39]
Prevenção e estigma

Quase todos os especialistas recomendam que a mãe se abstenha do uso de álcool durante a gravidez para prevenir os TEAFs.[4][56][57] Uma mulher grávida pode não estar ciente de que engravidou até várias semanas de gestação, portanto também é recomendado abster-se do álcool ao tentar engravidar.[58] As recomendações de abstinência de álcool durante a gravidez e durante a tentativa de engravidar foram feitas pelo Cirurgião-geral dos Estados Unidos,[59][58] pelos Centros de Controle e Prevenção de Doenças,[30] pelo Colégio Americano de Obstetras e Ginecologistas, pela Academia Americana de Pediatria,[45] pela Organização Mundial da Saúde,[60] pelo Instituto Nacional para a Saúde e Excelência Clínica do Reino Unido,[61] entre outros.[45] Nos Estados Unidos, a legislação federal exige desde 1988 que rótulos de advertência sejam colocados em todos os recipientes de bebidas alcoólicas, conforme a Lei de Rotulagem de Bebidas Alcoólicas.[62]
Estigma
As perspectivas atuais de defesa incentivam que pessoas e sistemas abordem o TEAF com intervenções e apoio a indivíduos que já vivem com a condição. Focar apenas na prevenção frequentemente estigmatiza ainda mais as pessoas com TEAF e seus pais biológicos. Defensores afirmam que, se alguém apoia pessoas que já vivem com TEAF, essa pessoa está promovendo a conscientização necessária para esforços preventivos bem-sucedidos; “Intervenção é Prevenção”. Muitos determinantes sociais da saúde afetam os efeitos da exposição pré-natal ao álcool:[63]
- Genética
- Pobreza/Acesso a alimentos nutritivos
- Desnutrição
- Redes de apoio social precárias
- Falta de autonomia pessoal
- Acesso a cuidados de saúde
- Traumas geracionais e socioculturais
- Acesso a cuidados de saúde mental e tratamento
Medicação
Mulheres podem apresentar sintomas graves decorrentes da abstinência de álcool durante a gravidez. Segundo a Organização Mundial da Saúde, esses sintomas podem ser tratados durante a gestação com o uso breve de benzodiazepínicos tranquilizantes.[28] Atualmente, a FDA aprovou três medicamentos — naltrexona, acamprosato e dissulfiram — para o tratamento do Transtorno por uso de álcool (TUA). No entanto, há poucos dados sobre a segurança desses medicamentos para mulheres grávidas.[64]
- Naltrexona é um antagonista opioide não seletivo usado no tratamento do TUA e do transtorno por uso de opioides.[65] Os efeitos de longo prazo da naltrexona sobre o feto ainda são desconhecidos.[66] Estudos em animais mostram que a naltrexona administrada durante a gestação aumenta a incidência de perdas fetais precoces; no entanto, não há dados suficientes para determinar até que ponto isso representa um risco em mulheres grávidas.[67]
- Acamprosato atua como antagonista de NMDA e de glutamato e como agonista em receptores GABAA, embora seu mecanismo molecular não seja totalmente compreendido. O acamprosato é eficaz na prevenção da recaída alcoólica durante a abstinência.[65] Dados em animais, contudo, sugerem que o acamprosato pode ter possíveis efeitos teratogênicos nos fetos.[64]
- Dissulfiram previne recaídas ao bloquear o metabolismo do acetaldeído após o consumo de álcool, o que leva a dores de cabeça, náusea e vômito.[65] Algumas evidências sugerem que o uso de dissulfiram durante o primeiro trimestre está associado a um risco aumentado de malformações congênitas, como defeitos de redução e fenda palatina.[66] Além disso, os efeitos do dissulfiram podem envolver hipertensão, o que pode ser prejudicial tanto para a gestante quanto para o feto.[64]
As diretrizes da Associação Psiquiátrica Americana recomendam que medicamentos não sejam usados no tratamento do transtorno por uso de álcool em gestantes, exceto em casos de abstinência alcoólica aguda ou outras condições coexistentes.[68] Em vez disso, intervenções comportamentais são geralmente preferidas como tratamento para gestantes com TUA. Medicamentos devem ser usados em mulheres grávidas apenas após cuidadosa consideração dos riscos e danos potenciais em comparação com os benefícios da cessação do álcool.[64]
Mecanismo
Após uma mulher grávida consumir álcool, a substância atravessa a placenta e o cordão umbilical até o feto em desenvolvimento. O álcool é metabolizado lentamente no feto e permanece por mais tempo em comparação com um adulto.[69][44] Um feto humano parece estar em risco triplicado com o consumo materno de álcool:[70][71]
- A placenta permite a livre entrada de etanol e metabólitos tóxicos, como o acetaldeído, no compartimento fetal. A chamada barreira placentária é praticamente ausente em relação ao etanol.
- O sistema nervoso fetal em desenvolvimento parece particularmente sensível à toxicidade do etanol. Este interfere na proliferação, diferenciação, migração neuronal, crescimento axonal, integração e ajuste fino da rede sináptica. Em resumo, todos os principais processos do sistema nervoso central em desenvolvimento parecem comprometidos.
- Os tecidos fetais são bastante diferentes dos tecidos adultos em função e propósito. Por exemplo, o principal órgão de desintoxicação em adultos é o fígado, enquanto o fígado fetal é incapaz de desintoxicar o etanol, já que as enzimas ADH e ALDH ainda não foram expressas nesta fase inicial. Até o termo, os tecidos fetais não possuem capacidade significativa para a desintoxicação do etanol, e o feto permanece exposto ao álcool no líquido amniótico por períodos muito mais longos do que o tempo de eliminação materno. A ausência de quantidades significativas de ADH e ALDH significa que os tecidos fetais possuem menores níveis de enzimas antioxidantes, como SOD, transferases de glutationa e glutationa peroxidases, resultando em uma proteção antioxidante muito menos eficaz.
Embora o álcool seja reconhecido como um teratógeno (causador de defeitos congênitos), os mecanismos biológicos exatos para o desenvolvimento da SAF ou TEAF ainda são desconhecidos. Contudo, estudos clínicos e em animais identificaram um amplo espectro de vias pelas quais o álcool materno pode afetar negativamente o resultado de uma gestação. Conclusões universais são difíceis de estabelecer, pois diferentes grupos étnicos apresentam considerável polimorfismo genético nas enzimas hepáticas responsáveis pela desintoxicação do etanol.[72] Exames genéticos revelaram um contínuo de efeitos moleculares de longa duração que não são apenas específicos do momento da exposição, mas também da dose; mesmo quantidades moderadas podem causar alterações.[73] Além disso, o etanol pode alterar o desenvolvimento fetal ao interferir na sinalização do ácido retinoico, já que o acetaldeído pode competir com o retinaldeído e impedir sua oxidação em ácido retinoico.[74]
Estágios do desenvolvimento
Diferentes sistemas do corpo do bebê crescem, amadurecem e se desenvolvem em momentos específicos da gestação. O efeito do consumo de álcool varia em cada um desses estágios de desenvolvimento:[25]
- Da concepção até a terceira semana, os sistemas e órgãos mais suscetíveis são o cérebro, a medula espinhal e o coração. Os efeitos do consumo de álcool no início da gravidez podem resultar em defeitos nesses sistemas e órgãos.[25]
- Durante a terceira semana, o álcool também pode danificar o sistema nervoso central do feto.[75]
- Na quarta semana de gestação, os membros estão sendo formados, e é nesse ponto que o álcool pode afetar o desenvolvimento de braços, pernas, dedos das mãos e dos pés. Os olhos e ouvidos também se formam nesta fase e são mais suscetíveis aos efeitos do álcool.[25]
- Na sexta semana de gestação, os dentes e o palato estão em formação, e o consumo de álcool neste período afetará essas estruturas. O uso de álcool nesta janela é responsável por muitas das características faciais da síndrome alcoólica fetal.[25]
- Durante a décima segunda semana, a exposição frequente ao álcool pode impactar negativamente o desenvolvimento cerebral, afetando habilidades cognitivas, de aprendizagem e comportamentais antes do nascimento.[75]
- Na 20ª semana de gestação, a formação dos órgãos e sistemas já está bem desenvolvida. O bebê ainda é suscetível aos efeitos nocivos do álcool.[25]
- A exposição ao etanol no segundo trimestre reduz os níveis nutricionais e pode afetar o funcionamento do sistema endócrino tanto do feto quanto da mãe. Isso ocorre porque o fluxo sanguíneo pela artéria umbilical para o cérebro fetal é reduzido.[76]
Diagnóstico
Os transtornos do espectro alcoólico fetal englobam uma variedade de problemas físicos e neurodesenvolvimentais que podem resultar da exposição pré-natal ao álcool. O diagnóstico é baseado nos sinais e sintomas apresentados pela pessoa e em evidências de uso de álcool.[1] Atualmente, são reconhecidos os seguintes diagnósticos dentro do espectro alcoólico fetal:
- Síndrome alcoólica fetal (SAF)[1]
- Síndrome alcoólica fetal parcial (SAFp), que se refere a indivíduos com histórico conhecido, ou altamente suspeito, de exposição pré-natal ao álcool e que apresentam déficits físicos e neurodesenvolvimentais relacionados ao álcool, mas que não preenchem todos os critérios para SAF.[29]
- Transtorno do neurodesenvolvimento relacionado ao álcool (ARND, do inglês Alcohol-related neurodevelopmental disorder)[29][1]
- Transtorno neurocomportamental associado à exposição pré-natal ao álcool (ND-PAE, do inglês Neurobehavioral disorder associated with prenatal alcohol exposure)[1]
A partir de 2016, a Agência Sueca de Avaliação de Tecnologias em Saúde e de Avaliação dos Serviços Sociais aceita apenas a SAF como diagnóstico, considerando inconclusivas as evidências para os demais tipos. A agência considera incerto se identificar uma condição relacionada ao espectro alcoólico fetal traz benefícios ao indivíduo diagnosticado.[77]
Classificação
Atualmente, quatro sistemas diagnósticos para SAF e outras condições do espectro alcoólico fetal foram desenvolvidos na América do Norte:
- As diretrizes do Instituto de Medicina para SAF, o primeiro sistema a padronizar diagnósticos de indivíduos com exposição pré-natal ao álcool;[26]
- O código diagnóstico de quatro dígitos da Universidade de Washington (The 4-Digit Diagnostic Code), que classifica as quatro características principais do espectro alcoólico fetal em uma Escala Likert de um a quatro, gerando 256 códigos descritivos que podem ser categorizados em 22 categorias clínicas distintas, variando de SAF a ausência de achados;[78]
- As diretrizes do Centro de Controle e Prevenção de Doenças dos Estados Unidos (CDC), intituladas "Fetal Alcohol Syndrome: Guidelines for Referral and Diagnosis", que estabeleceram consenso sobre o diagnóstico da SAF nos EUA, mas não abordaram outras condições do espectro;[79]
- As diretrizes canadenses para diagnósticos do espectro alcoólico fetal, que estabeleceram critérios para diagnóstico no Canadá e harmonizaram a maioria das diferenças entre os sistemas do IOM e da Universidade de Washington.[2]
Cada sistema diagnóstico exige a avaliação de quatro características principais: crescimento, características faciais, sistema nervoso central e exposição ao álcool. Para determinar qualquer condição dentro do espectro alcoólico fetal, é necessária uma avaliação interdisciplinar que considere cada uma dessas quatro características. Geralmente, um médico treinado determina a deficiência de crescimento e as características faciais típicas da SAF. Embora médicos qualificados possam também avaliar anormalidades estruturais ou neurológicas do sistema nervoso central, em geral o comprometimento é determinado por meio de testes psicológicos, avaliações fonoaudiológicas e terapia ocupacional para verificar prejuízos clinicamente significativos em três ou mais dos Dez Domínios Cerebrais.[80] O risco de exposição pré-natal ao álcool pode ser avaliado por um médico, psicólogo, assistente social ou conselheiro especializado em dependência química. Esses profissionais trabalham em equipe para avaliar e interpretar os dados de cada característica e elaborar um relatório interdisciplinar integrado para diagnosticar a SAF (ou outras condições do espectro) em um indivíduo.[81]
(Um achado positivo em todas as quatro características é necessário para o diagnóstico de SAF, e os quatro sistemas diagnósticos essencialmente concordam nos critérios para a síndrome alcoólica fetal (SAF). No entanto, há diferenças entre os sistemas quando os critérios completos para SAF não são atendidos. A exposição pré-natal ao álcool e o dano ao sistema nervoso central são os elementos principais do espectro, e um achado positivo nessas duas características já é suficiente para um diagnóstico de transtorno do espectro alcoólico fetal em todos os sistemas.[82] Contudo, diferentes pesquisadores e sistemas podem usar uma ampla variedade de terminologias para descrever a condição de um indivíduo, já que a nomenclatura ainda está em evolução. A maioria dos indivíduos com déficits resultantes da exposição pré-natal ao álcool não apresenta todas as características da SAF e se enquadra em outras condições do espectro.[26] As diretrizes canadenses recomendam a avaliação e abordagem descritiva do "Código Diagnóstico de 4 Dígitos" para cada característica, bem como a terminologia do IOM nas categorias diagnósticas, com exceção do ARBD.[2]
Síndrome alcoólica fetal
A condição mais grave é chamada de Síndrome Alcoólica Fetal (SAF),[1] que se refere a indivíduos que apresentam um conjunto específico de malformações congênitas e transtornos do neurodesenvolvimento característicos do diagnóstico.[29] Os seguintes critérios devem ser totalmente atendidos para o diagnóstico de SAF:[2][26][78][79]
- Altura ou peso (pré-natal ou pós-natal, ou ambos) no 10º percentil ou abaixo[21]
- Presença das três características faciais típicas da SAF[22]
- Prejuízo estrutural, neurológico ou funcional clinicamente significativo do sistema nervoso central
- Exposição pré-natal ao álcool confirmada ou desconhecida
A SAF é a única manifestação do espectro que obteve consenso entre especialistas para se tornar um diagnóstico oficial no CID-9 e CID-10.
SAF parcial
A SAF parcial (SAFp) era anteriormente conhecida como SAF atípica na edição de 1997 do "Código Diagnóstico de 4 Dígitos". Pessoas com SAFp possuem histórico confirmado de exposição pré-natal ao álcool, mas podem não apresentar deficiência de crescimento ou todas as características faciais típicas. O dano ao sistema nervoso central está presente no mesmo nível que na SAF. Esses indivíduos possuem as mesmas incapacidades funcionais, mas "se parecem menos" com casos clássicos de SAF.[83]
Os seguintes critérios devem ser totalmente atendidos para o diagnóstico de SAF parcial:[2][26][78]
- Presença de duas ou três características faciais da SAF[22]
- Prejuízo estrutural, neurológico ou funcional clinicamente significativo em três ou mais dos Dez Domínios Cerebrais[80]
- Exposição pré-natal ao álcool confirmada
O crescimento ou a estatura podem variar de normal a deficiente.[21]
Transtorno do neurodesenvolvimento relacionado ao álcool
O Transtorno do Neurodesenvolvimento Relacionado ao Álcool (ARND) é o diagnóstico específico do tipo não dismórfico do espectro, onde a maioria dos sintomas é observada.[84] A designação foi inicialmente sugerida pelo Instituto de Medicina para substituir os termos EAF (efeitos do álcool fetal). O foco está nos danos ao sistema nervoso central, em vez da deficiência de crescimento ou das características faciais da SAF. As diretrizes canadenses também utilizam este diagnóstico com os mesmos critérios. Embora o "Código Diagnóstico de 4 Dígitos" inclua esses critérios em três de suas categorias diagnósticas, refere-se a essa condição como encefalopatia estática. Os efeitos comportamentais do ARND não são necessariamente exclusivos do álcool, portanto o uso do termo deve estar sempre vinculado a um histórico confirmado de exposição pré-natal ao álcool.[56] O ARND pode estar ganhando aceitação em substituição aos termos EAF e ARBD para descrever condições do espectro com anormalidades do sistema nervoso central ou anormalidades comportamentais ou cognitivas, ou ambas, devido à exposição pré-natal ao álcool, independentemente de deficiência de crescimento ou características faciais da SAF.[56][85]
Os seguintes critérios devem ser totalmente atendidos para o diagnóstico de ARND ou encefalopatia estática:[2][26][78]
- Presença mínima ou ausência de características faciais da SAF[22]
- Prejuízo estrutural, neurológico ou funcional clinicamente significativo em três ou mais dos Dez Domínios Cerebrais[80]
- Exposição pré-natal ao álcool confirmada
O crescimento ou a estatura podem variar de normal a minimamente deficientes.[21]
Transtorno neurocomportamental associado à exposição pré-natal ao álcool
O Transtorno Neurocomportamental Associado à Exposição Pré-natal ao Álcool (ND-PAE) é o termo abrangente para os sintomas psiquiátricos, comportamentais e neurológicos presentes em todo o espectro. Foi introduzido no DSM-5 como uma "condição para estudos adicionais" e também como uma condição especificada dentro da categoria "outros transtornos do neurodesenvolvimento especificados", como forma de estudar melhor os aspectos comportamentais de todos os transtornos do espectro alcoólico fetal.[84]
Critérios específicos
Crescimento
No contexto do espectro alcoólico fetal, a deficiência de crescimento é definida como altura, peso ou ambos significativamente abaixo da média devido à exposição pré-natal ao álcool, podendo ser avaliada em qualquer momento do ciclo de vida. As medidas de crescimento devem ser ajustadas de acordo com a altura dos pais, idade gestacional (em caso de prematuridade) e outros fatores pós-natais (como desnutrição), embora a altura e o peso ao nascimento sejam as medidas preferenciais.[78] Deficiências são documentadas quando altura ou peso estão no 10º percentil ou abaixo em gráficos de crescimento padronizados e apropriados para a população.[21] As deficiências podem aparecer tanto no período pré-natal quanto pós-natal, mas são mais frequentes após o nascimento.[86]
Os critérios de crescimento são menos específicos no sistema do Instituto de Medicina ("baixo peso ao nascer..., desaceleração do peso não atribuída à nutrição..., [ou] peso desproporcionalmente baixo em relação à altura", p. 4 do resumo executivo),[26] enquanto o CDC utiliza o 10º percentil como ponto de corte para definir deficiência de crescimento.[79] O "Código Diagnóstico de 4 Dígitos" permite gradações intermediárias (entre o 3º e o 10º percentil) e deficiência grave quando no 3º percentil ou abaixo.[78] A deficiência de crescimento (em níveis grave, moderado ou leve) contribui para os diagnósticos de SAF e SAF parcial, mas não para ARND ou encefalopatia estática.[carece de fontes]
O "Código Diagnóstico de 4 Dígitos" (2004) classifica a deficiência de crescimento da seguinte forma:[78]
- Grave: altura e peso no 3º percentil ou abaixo.
- Moderada: altura ou peso no 3º percentil ou abaixo, mas não ambos.
- Leve: altura ou peso (ou ambos) entre o 3º e o 10º percentil.
- Ausente: altura e peso acima do 10º percentil.
Nos estudos iniciais que descreveram a SAF, a deficiência de crescimento era critério obrigatório de inclusão; assim, todas as pessoas inicialmente diagnosticadas apresentavam essa condição como um artefato das características de amostragem utilizadas.[26] A deficiência de crescimento pode ser menos relevante para compreender as incapacidades do espectro do que as sequelas neurocomportamentais decorrentes das lesões cerebrais.[26] As diretrizes canadenses atualizadas em 2016 removeram o crescimento como critério diagnóstico.[87]
Características faciais
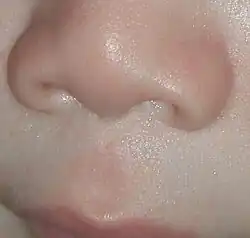
Diversas anomalias craniofaciais características são frequentemente visíveis em indivíduos com SAF.[88] A presença dessas características indica lesão cerebral, embora ela também possa ocorrer na ausência delas. Acredita-se que as características faciais da SAF (e a maioria das demais deformidades visíveis, mas não diagnósticas) sejam causadas principalmente entre a 10ª e a 20ª semana de gestação.[89]
O refinamento dos critérios diagnósticos desde 1975 levou à definição de três características faciais distintivas e significativas para diferenciar a SAF de outros transtornos com sintomas parcialmente sobrepostos.[90][91] As três características são:
- Filtro nasal liso: o sulco entre o nariz e o lábio superior se achata com o aumento da exposição ao álcool.
- Vermelhão fino: o lábio superior se afina com maior exposição ao álcool.
- Fenda palpebral pequena: a largura do olho diminui com maior exposição ao álcool.
A medição dessas características utiliza critérios desenvolvidos pela Universidade de Washington. O lábio e o filtro nasal são avaliados por um médico treinado com o Lip-Philtrum Guide,[92] uma escala Likert de cinco pontos com fotografias representativas de combinações de lábio e filtro nasal, variando do normal (grau 1) ao grave (grau 5). O comprimento da fenda palpebral (PFL) é medido em milímetros com paquímetros ou régua transparente e comparado a gráficos de crescimento desenvolvidos também pela Universidade de Washington.[22]
A classificação é complexa porque as três características podem ser afetadas de forma independente pela exposição ao álcool. Resumidamente:[78][93]
- Grave: todas as três características faciais classificadas como graves (lábio 4 ou 5, filtro nasal 4 ou 5 e PFL duas ou mais desvios-padrão abaixo da média).
- Moderada: duas características graves e uma moderada (lábio ou filtro nasal grau 3, ou PFL entre um e dois desvios-padrão abaixo da média).
- Leve: combinações variadas, como:
- duas características graves e uma dentro da normalidade,
- uma característica grave e duas moderadas, ou
- uma grave, uma moderada e uma normal.
- Ausente: todas as três características dentro da normalidade.
Sistema nervoso central
O sistema nervoso central (SNC) é a principal área afetada em qualquer diagnóstico do espectro alcoólico fetal. A exposição pré-natal ao álcool, classificada como teratógeno, pode lesar o cérebro em diferentes níveis, do grave ao sutil, dependendo da quantidade, do momento e da frequência da exposição, além da predisposição genética do feto e da mãe.[26][94] Embora as anomalias funcionais sejam a expressão comportamental e cognitiva da deficiência, o dano ao SNC pode ser avaliado em três áreas: estrutural, neurológica e funcional.
Os quatro sistemas diagnósticos permitem avaliação nessas três áreas, mas os critérios variam. O sistema do IOM exige prejuízo estrutural ou neurológico para diagnóstico de SAF, mas também aceita um "padrão complexo" de anomalias funcionais para SAF parcial e ARND.[26] O "Código Diagnóstico de 4 Dígitos" e as diretrizes do CDC permitem que um achado positivo no SNC em qualquer uma das três áreas seja suficiente, mas exigem anomalias funcionais de dois desvios-padrão ou mais em três ou mais domínios funcionais para diagnóstico de SAF, SAFp e ARND.[78][79] O "Código Diagnóstico de 4 Dígitos" também aceita diagnóstico quando apenas dois domínios funcionais apresentam esse nível de comprometimento.[78] Esse sistema ainda classifica o grau de dano em quatro níveis:
- Definido: anomalias estruturais ou neurológicas para SAF ou encefalopatia estática.
- Provável: disfunção significativa (≥ 2 desvios-padrão) em três ou mais domínios funcionais.
- Possível: disfunção leve a moderada em um ou dois domínios funcionais ou julgamento da equipe clínica de que não se pode descartar dano ao SNC.
- Improvável: nenhuma evidência de dano.
Estrutural
Anormalidades estruturais do cérebro são observáveis e decorrem de danos físicos ao cérebro ou às suas estruturas causados pela exposição pré-natal ao álcool. Os comprometimentos estruturais podem incluir microcefalia (tamanho reduzido da cabeça) de duas ou mais desvios-padrão abaixo da média, ou outras anormalidades na estrutura cerebral (por exemplo, agênese do corpo caloso, hipoplasia cerebelar).[26]
A microcefalia é determinada comparando a circunferência craniana (frequentemente chamada de circunferência occipitofrontal, ou COF) com gráficos de crescimento de COF apropriados.[21] Outros comprometimentos estruturais devem ser observados por meio de técnicas de imagem médica realizadas por um médico treinado. Como os procedimentos de imagem são caros e relativamente inacessíveis para a maioria das pessoas, o diagnóstico da SAF raramente é feito por comprometimentos estruturais, exceto no caso da microcefalia.[carece de fontes]
Evidências de comprometimento estrutural do SNC devido à exposição pré-natal ao álcool resultarão em um diagnóstico de SAF, sendo altamente prováveis os comprometimentos neurológicos e funcionais.[2][26][78][79]
Durante o primeiro trimestre da gestação, o álcool interfere na migração e organização das células cerebrais, o que pode gerar deformidades ou déficits estruturais no cérebro.[95] Durante o terceiro trimestre, podem ocorrer danos no hipocampo, estrutura responsável pela memória, aprendizado, emoção e codificação de informações visuais e auditivas, o que também pode gerar comprometimentos neurológicos e funcionais do SNC.[96]
Em 2002, havia 25 relatos de autópsias de bebês com diagnóstico de SAF. A primeira ocorreu em 1973, em um bebê que morreu logo após o nascimento.[97] O exame revelou extensos danos cerebrais, incluindo microcefalia, anomalias de migração, disgenesia do corpo caloso e uma extensa neuroglia, leptomeninge heterotopia cobrindo o hemisfério esquerdo.[98]
Em 1977, Clarren descreveu um segundo bebê cuja mãe praticava consumo excessivo episódico de álcool. O bebê morreu dez dias após o nascimento. A autópsia revelou grave hidrocefalia, migração neuronal anormal e corpo caloso reduzido.[98] A SAF também foi associada a alterações no tronco encefálico e no cerebelo, agênese do corpo caloso e da comissura anterior, erros de migração neuronal, ausência de bulbos olfatórios, meningomielocele e porencefalia.[98]
Defeitos estruturais adicionais foram identificados em diversas autópsias desde então, incluindo: ulegiria, microgiria, lesões hipóxico-isquêmicas e/ou hemorrágicas devido a acidente vascular cerebral perinatal, ventriculomegalia e atrofia cerebelar.[99]
Neurológico
Quando os comprometimentos estruturais não são observáveis ou não existem, avaliam-se os comprometimentos neurológicos. No contexto do TEAF, os transtornos neurológicos são causados pela exposição pré-natal ao álcool, que provoca danos neurológicos gerais ao sistema nervoso central (SNC), ao sistema nervoso periférico ou ao sistema nervoso autônomo. A determinação de um problema neurológico deve ser feita por um médico treinado, e não pode ser decorrente de uma agressão pós-natal, como meningite, concussão, traumatismo cranioencefálico etc.[carece de fontes]
Os quatro sistemas diagnósticos apresentam concordância praticamente total quanto aos critérios para identificar danos ao SNC em nível neurológico, e a evidência de comprometimento neurológico do SNC devido à exposição pré-natal ao álcool resultará em um diagnóstico de SAF ou SAF parcial, sendo altamente prováveis os comprometimentos funcionais.[2][26][78][79]
Os problemas neurológicos podem se manifestar como sinais duros, ou distúrbios diagnosticáveis, como epilepsia ou outros transtornos convulsivos, ou como sinais brandos. Os sinais brandos são comprometimentos neurológicos mais amplos e inespecíficos, ou sintomas como prejuízo de habilidade motora fina, perda auditiva neurossensorial, marcha deficiente, desajeitamento e baixa coordenação olho-mão. Muitos sinais brandos têm critérios normativos, enquanto outros são determinados pelo julgamento clínico. O "julgamento clínico" só é tão bom quanto o profissional, e esses sinais devem ser avaliados por um neurologista pediátrico, um neuropsicólogo pediátrico ou ambos.[carece de fontes]
Funcional
Quando não são observados comprometimentos estruturais ou neurológicos, os quatro sistemas diagnósticos permitem que os danos ao SNC devido à exposição pré-natal ao álcool sejam avaliados em termos de comprometimentos funcionais.[2][26][78][79] Os comprometimentos funcionais são déficits, problemas, atrasos ou anormalidades decorrentes da exposição pré-natal ao álcool (e não de causas hereditárias ou agressões pós-natais) em domínios observáveis e mensuráveis relacionados ao funcionamento diário, frequentemente referidos como deficiências do desenvolvimento. Não há consenso sobre um padrão específico de comprometimentos funcionais causados pela exposição pré-natal ao álcool[26] e apenas as diretrizes do CDC classificam atrasos no desenvolvimento dessa forma,[79] de modo que os critérios (e os diagnósticos de TEAF) variam entre os sistemas diagnósticos.
Os quatro sistemas diagnósticos listam diversos domínios do SNC que podem qualificar para comprometimento funcional, os quais podem determinar um diagnóstico de TEAF:
- Evidência de um padrão complexo de comportamento ou anormalidades cognitivas inconsistente com o nível de desenvolvimento nos seguintes domínios do SNC – Suficiente para um diagnóstico de SAF parcial ou ARND pelas diretrizes do IOM[26]
- dificuldades de aprendizagem, desempenho acadêmico, controle de impulso, percepção social, comunicação, abstração, habilidades matemáticas, memória, atenção, julgamento
- Desempenho de dois ou mais desvios-padrão em testes padronizados em três ou mais dos seguintes domínios do SNC – Suficiente para um diagnóstico de SAF, SAF parcial ou encefalopatia estática pelo Código Diagnóstico 4-Dígitos[78]
- Funções executivas, memória, cognição, habilidades sociais/adaptativas, desempenho acadêmico, comunicação, habilidades motoras, atenção, nível de atividade
- Déficits cognitivos gerais (por exemplo, QI) no 3º percentil ou abaixo em testes padronizados – Suficiente para um diagnóstico de SAF pelas diretrizes do CDC[79]
- Desempenho no 16º percentil ou abaixo em testes padronizados em três ou mais dos seguintes domínios do SNC – Suficiente para um diagnóstico de SAF pelas diretrizes do CDC[79]
- Cognição, funções executivas, funcionamento motor, problemas de atenção e hiperatividade, habilidades sociais, transtorno do processamento sensorial, comunicação social, memória, dificuldades em responder a práticas comuns de paternidade
- Desempenho de dois ou mais desvios-padrão em testes padronizados em três ou mais dos seguintes domínios do SNC – Suficiente para um diagnóstico de SAF pelas diretrizes canadenses
- Cognição, comunicação, desempenho acadêmico, memória, funções executivas, comportamento adaptativo, habilidades motoras, habilidades sociais, comunicação social
Dez domínios cerebrais
Um esforço para padronizar a avaliação de danos funcionais do SNC foi sugerido por uma equipe de diagnóstico de SAF no Minnesota. O quadro proposto tenta harmonizar o IOM, o Código Diagnóstico de 4 Dígitos, os critérios do CDC e as diretrizes canadenses para medir os danos ao SNC em avaliações e diagnósticos de SAF. A abordagem padronizada é chamada de Dez Domínios Cerebrais e abrange aspectos das recomendações dos quatro sistemas diagnósticos para avaliar os danos ao SNC devido à exposição pré-natal ao álcool. O quadro fornece definições claras de disfunção cerebral, especifica os dados empíricos necessários para um diagnóstico preciso e define considerações de intervenção que abordam a natureza complexa do SAF, com a intenção de evitar deficiências secundárias comuns.[80]
Os Dez Domínios Cerebrais propostos incluem:[80]
- Realização
- Comportamento adaptativo
- Atenção
- Cognição
- Funções executivas
- Linguagem
- Memória
- Habilidades motoras
- Integração multissensorial ou problemas neurológicos leves
- Comunicação social[80]
O Programa Diagnóstico de Álcool Fetal (FADP) usa critérios não publicados do estado de Minnesota de desempenho em 1,5 ou mais desvio padrão em testes padronizados em três ou mais dos Dez Domínios Cerebrais para determinar danos ao SNC. No entanto, os Dez Domínios Cerebrais são facilmente incorporados em qualquer um dos quatro sistemas diagnósticos para critérios de danos ao SNC, já que o quadro apenas propõe os domínios, em vez dos critérios de corte para SAF.[100]
Exposição ao álcool
A exposição pré-natal ao álcool é determinada por entrevista com a mãe biológica ou outros membros da família com conhecimento sobre o uso de álcool da mãe durante a gravidez (se disponível), registros de saúde pré-natal (se disponíveis), revisão dos registros de nascimento, registros judiciais (se aplicável), registros de tratamento da dependência química (se aplicável), biomarcadores químicos,[101] ou outras fontes confiáveis.
O nível de exposição é avaliado como exposição confirmada, exposição desconhecida e ausência confirmada de exposição pelos sistemas diagnósticos do IOM, CDC e canadenses. O "Código Diagnóstico de 4 Dígitos" distingue ainda a exposição confirmada como Alto Risco e Algum Risco:[carece de fontes]
- Exposição confirmada: As diretrizes do CDC são omissas quanto ao uso de informações sobre a quantidade, frequência e tempo do consumo pré-natal de álcool para fins de diagnóstico. O IOM e as diretrizes canadenses exploram isso mais profundamente, reconhecendo a importância da exposição significativa ao álcool pelo consumo regular ou episódico pesado de álcool na determinação, mas não oferecem um padrão para diagnóstico. As diretrizes canadenses discutem essa falta de clareza e apontam, entre parênteses, que o "uso pesado de álcool" é definido pelo Instituto Nacional sobre Abuso de Álcool e Alcoolismo como cinco ou mais doses por episódio em cinco ou mais dias durante 30 dias.[102] O sistema de classificação do "Código Diagnóstico de 4 Dígitos" distingue entre níveis de exposição pré-natal ao álcool como alto risco e algum risco. Ele operacionaliza a exposição de alto risco como uma concentração de álcool no sangue (BAC) superior a 100 mg/dL administrada pelo menos semanalmente no início da gravidez. Esse nível de BAC é tipicamente atingido por uma mulher de 55 kg bebendo seis a oito cervejas em uma única ocasião.[78]
- Alto Risco: Uso confirmado de álcool durante a gravidez conhecido por estar em altos níveis de álcool no sangue (100 mg/dL ou mais) administrado pelo menos semanalmente no início da gravidez.
- Algum Risco: Uso confirmado de álcool durante a gravidez com uso inferior ao de Alto Risco ou padrões de uso desconhecidos.
- Risco Desconhecido: Uso desconhecido de álcool durante a gravidez. Para muitos adultos adotados e crianças em lares adotivos, registros ou outras fontes confiáveis podem não estar disponíveis para revisão. Relatar o uso de álcool durante a gravidez também pode ser estigmatizante para as mães biológicas, especialmente se o uso de álcool estiver em andamento. Muitas relutam em admitir que beberam ou fornecer um relato preciso da quantidade ingerida.[79] Nesses casos, todos os sistemas diagnósticos usam uma designação de exposição pré-natal ao álcool desconhecida. Um diagnóstico de SAF ainda é possível com um nível de exposição desconhecido se outras características-chave do espectro do SAF estiverem presentes em níveis clínicos.[carece de fontes]
- Sem Risco: Ausência confirmada de exposição pré-natal ao álcool. A ausência confirmada de exposição se aplicaria a gestações planejadas nas quais não foi usado álcool ou gestações de mulheres que não usam álcool ou relatam não ter usado durante a gravidez. Essa designação é relativamente rara, já que a maioria das pessoas apresentando-se para uma avaliação de SAF é pelo menos suspeita de ter tido exposição pré-natal ao álcool devido à presença de outras características-chave do SAF.[78][79]
Biomarcadores
As evidências são insuficientes para o uso de biomarcadores químicos para detectar a exposição pré-natal ao álcool.[103] Biomarcadores em estudo incluem ésteres etílicos de ácidos graxos (FAEE) detectados no mecônio (primeiras fezes de um recém-nascido) e no cabelo. FAEE pode estar presente se a exposição crônica ao álcool ocorrer durante o segundo e o terceiro trimestres, já que é quando o mecônio começa a se formar. No entanto, as concentrações de FAEE podem ser influenciadas pelo uso de medicamentos, dieta e variações genéticas individuais no metabolismo de FAEE.[101][104]
Diagnóstico diferencial
O CDC revisou nove síndromes que têm características sobrepostas com SAF; no entanto, nenhuma dessas síndromes inclui todas as três características faciais do SAF, e nenhuma é resultado de exposição pré-natal ao álcool:[79]
- Síndrome de Aarskog
- Síndrome de Williams
- Síndrome de Noonan
- Síndrome de Dubowitz
- Síndrome de Brachman-DeLange
- Síndrome do tolueno
- Síndrome da hidantoína fetal
- Síndrome fetal por valproato
- Efeitos fetais da PKU materna
Outros distúrbios que apresentam sintomas comportamentais sobrepostos que podem ser comórbidos ao transtorno do espectro alcoólico fetal incluem:[105]
- Transtorno do déficit de atenção e hiperatividade
- Transtorno do espectro autista
- Transtorno de apego reativo
- Transtorno desafiador opositivo
- Disfunção de integração sensorial
- Transtorno bipolar
- Depressão
A maioria das pessoas com SAF foi muitas vezes diagnosticada erroneamente com TDAH devido à grande sobreposição entre seus déficits comportamentais.
Tratamento
Embora a condição não tenha cura disponível, o tratamento pode melhorar os resultados.[1][3] Como os danos ao SNC, sintomas, deficiências secundárias e necessidades variam amplamente por indivíduo, não existe um único tipo de tratamento que funcione para todos.[40]
Entre 2017 e 2019, pesquisadores fizeram uma descoberta ao identificar uma possível cura usando células-tronco neurais (NSCs); eles propõem que, se aplicadas a um recém-nascido, os danos podem ser revertidos e prevenidos quaisquer efeitos duradouros no futuro.[106]
Medicamentos
Psicotrópicos são frequentemente testados, já que muitos sintomas do SAF são confundidos com ou se sobrepõem a outros transtornos, mais notavelmente o TDAH. Os medicamentos são usados para tratar especificamente sintomas dos SAFs e não o SAF como um todo. Alguns dos medicamentos utilizados são antidepressivos, estimulantes, neurolépticos e ansiolíticos.[107]
Intervenções comportamentais
Intervenção precoce desde o nascimento até os 3 anos de idade demonstrou melhorar o desenvolvimento de uma criança nascida com SAFD.[104] As intervenções podem incluir terapia de interação pais-filho, esforços para modificar o comportamento da criança e uso de medicamentos.[5] Intervenções comportamentais são baseadas na Teoria da aprendizagem, que é a base de muitas estratégias e intervenções parentais e profissionais.[85] Junto com os estilos parentais comuns, essas estratégias são frequentemente usadas como padrão no tratamento daqueles com SAF, já que os diagnósticos de transtorno desafiador de oposição (TDO), transtorno de conduta, transtorno reativo de apego (TRA) frequentemente se sobrepõem ao SAF (assim como o TDAH), e às vezes acredita-se que esses diagnósticos se beneficiem de intervenções comportamentais. Frequentemente, o baixo desempenho acadêmico resulta em serviços de educação especial, que também utilizam princípios da Teoria da aprendizagem, modificação de comportamento e educação baseada em resultados.[carece de fontes]
Crianças com SAF se beneficiam de treinamento comportamental e funcional, treinamento de habilidades sociais e reforço escolar. Grupos de apoio e terapia da fala não apenas ajudam as crianças afetadas pelo SAF, mas também auxiliam os pais e irmãos dessas crianças.[carece de fontes]
Estrutura de desenvolvimento
Muitos livros e folhetos sobre SAF recomendam uma abordagem desenvolvimentista, baseada na psicologia do desenvolvimento, embora a maioria não especifique isso explicitamente nem forneça muito embasamento teórico. O desenvolvimento humano ideal geralmente ocorre em estágios identificáveis (por exemplo, a teoria do desenvolvimento cognitivo de Jean Piaget, os estágios do desenvolvimento psicossocial de Erik Erikson, a teoria do apego de John Bowlby e outras teorias de estágios do desenvolvimento). O SAF interfere no desenvolvimento normal,[108] o que pode fazer com que estágios sejam atrasados, pulados ou desenvolvidos de forma imatura. Com o tempo, uma criança não afetada pode lidar com as crescentes demandas da vida ao progredir normalmente pelos estágios do desenvolvimento, mas isso não ocorre com uma criança com SAF.[108]
Conhecer quais estágios e tarefas do desenvolvimento as crianças seguem permite que tratamentos e intervenções para o SAF sejam adaptados para ajudar a pessoa a cumprir com sucesso as tarefas e demandas do desenvolvimento.[108] Se uma pessoa apresenta atraso no domínio do comportamento adaptativo, por exemplo, intervenções seriam recomendadas para direcionar atrasos específicos por meio de educação e prática adicionais (por exemplo, instrução prática em como amarrar os cadarços), fornecendo lembretes ou fazendo acomodações (por exemplo, usar sapatos sem cadarço) para apoiar o nível de funcionamento desejado. Essa abordagem representa um avanço em relação às intervenções comportamentais, pois leva em conta o contexto desenvolvimentista da pessoa ao elaborar intervenções.[carece de fontes]
Modelo de advocacia
O modelo de advocacia adota o ponto de vista de que alguém é necessário para mediar ativamente entre o ambiente e a pessoa com SAF.[56] As atividades de advocacia são conduzidas por um defensor (por exemplo, um membro da família, amigo ou gerente de caso) e se enquadram em três categorias básicas. Um defensor para o SAF: (1) interpreta o SAF e as deficiências que dele surgem e explica ao ambiente em que a pessoa vive, (2) promove mudanças ou acomodações em nome da pessoa e (3) auxilia a pessoa a desenvolver e alcançar metas possíveis.[56]
O modelo de advocacia é frequentemente recomendado, por exemplo, ao desenvolver um programa educacional individualizado (PEI) para o progresso da pessoa na escola.[107]
Uma compreensão da estrutura de desenvolvimento presumivelmente informaria e reforçaria o modelo de advocacia, mas a advocacia também implica intervenções em nível de sistemas, como educar escolas, assistentes sociais e assim por diante sobre as melhores práticas para o SAF. Entretanto, várias organizações dedicadas ao SAF também utilizam o modelo de advocacia em nível de prática comunitária.[109]
Tratar o SAF nos níveis de saúde pública e política pública promove a prevenção do SAF e a destinação de serviços públicos para apoiar aqueles com SAF.[56] Está relacionado ao modelo de advocacia, mas promovido em nível de sistemas (em vez de com o indivíduo ou a família), como o desenvolvimento de educação e apoio comunitários, esforços de prevenção em nível estadual ou provincial (por exemplo, triagem do consumo de álcool materno durante consultas de obstetrícia ou pré-natal) ou programas de conscientização nacional. Várias organizações e agências estaduais nos EUA se dedicam a esse tipo de intervenção.[109]
Prognóstico
O prognóstico do SAFD é variável, dependendo do tipo, gravidade e se há tratamento adequado.[carece de fontes] As deficiências prognósticas são divididas em primárias e secundárias.
Deficiências primárias
As deficiências primárias do SAF são as dificuldades funcionais com as quais a criança já nasce como resultado dos danos ao SNC devido à exposição pré-natal ao álcool.[110]
Frequentemente, deficiências primárias são confundidas como problemas de comportamento, mas o dano subjacente ao SNC é a origem da dificuldade funcional,[111] e não uma condição de saúde mental, que é considerada uma deficiência secundária. Os mecanismos exatos para os problemas funcionais das deficiências primárias nem sempre são totalmente compreendidos, mas estudos com animais começaram a lançar luz sobre algumas correlações entre problemas funcionais e estruturas cerebrais danificadas pela exposição pré-natal ao álcool.[56] Exemplos representativos incluem:
- Prejuízos de aprendizagem estão associados a dendritos prejudicados do hipocampo[112]
- Desenvolvimento e funcionamento motor prejudicados estão associados à redução do tamanho do cerebelo[113]
- Hiperatividade está associada à diminuição do tamanho do corpo caloso[114]
Dificuldades funcionais podem resultar de danos ao SNC em mais de um domínio, mas as dificuldades funcionais comuns por domínio incluem:[56][85][108][111] Nota: esta não é uma lista exaustiva de dificuldades.
- Realização: Dificuldades de aprendizagem
- Comportamento adaptativo: Fraco controle de impulso, limites pessoais frágeis, fraca regulação da raiva, teimosia, comportamento intrusivo, excessivamente amigável com estranhos, fracas habilidades de vida diária, atrasos no desenvolvimento
- Atenção: Transtorno do déficit de atenção e hiperatividade (TDAH), pouca atenção ou concentração, distração fácil
- Cognição: Deficiência intelectual, confusão sob pressão, fracas habilidades de abstração, dificuldade em distinguir entre fantasia e realidade, processamento cognitivo mais lento
- Funções executivas: Fraco julgamento, transtorno do processamento sensorial, dificuldade em perceber padrões, fraco raciocínio de causa e efeito, inconsistência em vincular palavras a ações, baixa capacidade de generalização
- Linguagem: Transtornos de linguagem expressiva ou receptiva, compreensão parcial mas não de conceitos completos, falta de entendimento de metáforas, expressões idiomáticas ou sarcasmo
- Memória: Fraca memória de curto prazo, memória e base de conhecimentos inconsistentes
- Habilidades motoras: Má caligrafia, fracas habilidades motoras finas, fracas habilidades motoras grossas, atraso no desenvolvimento motor (ex.: aprender a andar de bicicleta em idade adequada)
- Processamento sensorial e problemas neurológicos leves: transtorno do processamento sensorial, defensividade sensorial, baixa sensibilidade à estimulação
- Comunicação social: Interrupção em conversas, incapacidade de ler sinais não verbais ou sociais, "falante" mas sem conteúdo
Deficiências secundárias
As deficiências secundárias do SAF são aquelas que surgem mais tarde na vida, em decorrência dos danos ao SNC. Essas deficiências geralmente emergem ao longo do tempo devido a um descompasso entre as deficiências primárias e as expectativas do ambiente; deficiências secundárias podem ser atenuadas com intervenções precoces e serviços de apoio adequados.[110]
Seis principais deficiências secundárias foram identificadas em um estudo da Universidade de Washington com 473 sujeitos diagnosticados com SAF, SAFP (síndrome alcoólica fetal parcial) e TNDÁ (transtorno do neurodesenvolvimento relacionado ao álcool):[56][110]
- Problemas de saúde mental: Diagnóstico de TDAH, depressão clínica ou outra doença mental, presente em mais de 90% dos sujeitos
- Experiência escolar interrompida: Suspensão ou expulsão da escola, ou abandono escolar, presente em 60% dos sujeitos (com 12 anos ou mais)
- Problemas com a lei: Acusação ou condenação por crime, presente em 60% dos sujeitos (com 12 anos ou mais)
- Confinamento: Internação psiquiátrica, tratamento de dependência química ou encarceramento por crime, presente em cerca de 50% dos sujeitos (com 12 anos ou mais)
- Comportamento sexual inadequado: Avanços sexuais, toques sexuais ou promiscuidade, presente em cerca de 50% dos sujeitos (com 12 anos ou mais)
- Problemas com álcool e drogas: Abuso ou dependência, presente em 35% dos sujeitos (com 12 anos ou mais)
Duas deficiências secundárias adicionais foram identificadas em adultos:[56][110]
- Vida dependente: Moradia coletiva, viver com família ou amigos ou algum tipo de residência assistida, presente em 80% dos sujeitos (com 21 anos ou mais)
- Problemas com emprego: Necessidade de treinamento ou orientação contínuos, incapacidade de manter um emprego, desemprego, presente em 80% dos sujeitos (com 21 anos ou mais)
Fatores de proteção e pontos fortes
O mesmo estudo identificou oito fatores universais de proteção que reduziram a taxa de incidência das deficiências secundárias:[56][110]
- Viver em um lar estável e acolhedor por mais de 73% da vida
- Receber diagnóstico de SAF antes dos seis anos de idade
- Nunca ter experienciado violência
- Permanecer em cada situação de moradia por pelo menos 2,8 anos
- Ter vivido em um "lar de boa qualidade" (com 10 ou mais qualidades definidas) entre os 8 e 12 anos de idade
- Ter sido considerado elegível para serviços de deficiência do desenvolvimento (DD)
- Ter as necessidades básicas atendidas por pelo menos 13% da vida
- Ter diagnóstico de SAF (em vez de outra condição do espectro FASD)
Malbin (2002) identificou as seguintes áreas de interesse e talentos como pontos fortes que frequentemente se destacam em pessoas com FASD e que devem ser utilizados, como qualquer ponto forte, no planejamento do tratamento:[85]
- Música, tocar instrumentos, composição, canto, arte, soletração, leitura, informática, mecânica, marcenaria, profissões qualificadas (soldagem, eletricista etc.), escrita, poesia
- Participação em esportes sem impacto ou atividades de condicionamento físico
Expectativa de vida
Um estudo constatou que pessoas com SAF têm uma expectativa de vida significativamente mais curta.[6] Com uma média de 34 anos, verificou-se que 44% das mortes tiveram "causa externa", sendo 15% delas suicídios.
Epidemiologia
Globalmente, uma em cada dez mulheres consome álcool durante a gravidez. Dentro dessa população, 20% praticam consumo excessivo episódico de álcool e ingerem quatro ou mais doses alcoólicas em uma única ocasião.[46] O uso de álcool durante a gravidez ocorre em diferentes taxas ao redor do mundo, possivelmente devido a diferenças culturais e legislações. Os cinco países com maior prevalência de uso de álcool durante a gravidez são Irlanda (60%), Bielorrússia (47%), Dinamarca (46%), Reino Unido (41%) e Federação Russa (37%).[36]
Em uma contagem recente, a prevalência de algum transtorno do espectro FASD foi de 1 em cada 20 pessoas, mas alguns estimam que possa ser tão alto quanto 1 em cada 7.[7] As taxas de SAF e FASD provavelmente são subestimadas, devido à dificuldade de diagnóstico e à relutância de clínicos em rotular crianças e mães.[115]
Austrália
O FASD entre jovens australianos é mais comum entre os indígenas australianos.[116] Os únicos estados que registraram defeitos congênitos em jovens australianos foram Austrália Ocidental, Nova Gales do Sul, Vitória e Austrália Meridional.[117] Na Austrália, apenas 12% dos profissionais de saúde conhecem os diagnósticos e sintomas do FASD.[116] Na Austrália Ocidental, a taxa de nascimentos resultando em FASD é de 0,02 por 1.000 nascimentos entre não indígenas, enquanto entre indígenas a taxa é de 2,76 por 1.000.[117] Em Vitória, não houve registros de nascimentos relacionados ao FASD entre indígenas, mas a taxa para a população geral é de 0,01–0,03 por 1.000 nascimentos.[117] Não há clínicas dedicadas ao FASD na Austrália Ocidental, mas também não existem critérios diagnósticos apoiados nacionalmente em todo o país.[118] A vigilância passiva é uma técnica de prevenção usada no país para auxiliar no monitoramento e na identificação de defeitos detectáveis durante a gravidez e a infância.[117]
Canadá
Um artigo de revisão de 2015 estimou os custos totais do FASD no Canadá em 9,7 bilhões de dólares (incluindo custos relacionados ao crime, saúde, educação etc.).[119]
África do Sul
Na África do Sul, algumas populações apresentam taxas de até 9%.[120]
Estados Unidos
Nos Estados Unidos, o uso de álcool em algum momento durante a gravidez é comum e parece estar aumentando em prevalência.[121][122][123][42] Entre 2006 e 2010, estimou-se que 7,6% das gestantes consumiram álcool, enquanto 1,4% relataram consumo excessivo episódico durante a gestação. As maiores prevalências foram entre mulheres de 35–44 anos (14,3%), brancas (8,3%), com ensino superior (10,0%) ou empregadas (9,6%).[124] Em 2015, cerca de 10% das gestantes consumiram álcool no último mês, e entre 20% a 30% em algum momento da gravidez.[41] Em um estudo epidemiológico de 2001, 3,6% das gestantes americanas preencheram critérios para transtorno por uso de álcool.[47] Em 2016, os Centros de Controle e Prevenção de Doenças dos EUA estimaram que 3 milhões de mulheres no país estavam em risco de ter um bebê com FASD.[125]
Estima-se que o FASD afete entre 1–2% e 5% da população nos Estados Unidos e na Europa Ocidental.[126] A SAF ocorre entre 0,2 e 9 a cada 1.000 nascidos vivos nos EUA.[126] Usando registros médicos e outros, estudos do CDC identificaram entre 0,2 e 1,5 bebês com SAF a cada 1.000 nascidos vivos em certas regiões do país.[127] Um estudo mais recente do CDC, com dados de 2010, analisou registros médicos e encontrou SAF em 0,3 a cada 1.000 crianças entre 7 e 9 anos de idade.[128]
O custo vitalício por criança com SAF nos EUA foi estimado em 2 milhões de dólares (com custo total superior a 4 bilhões de dólares no país) pelo CDC em 2002.[126]
Histórico
Antes da designação
Alguns sustentam que fontes antigas descrevem os efeitos negativos do álcool durante a gravidez,[120] identificando advertências da Grécia Antiga, Roma, do Talmude e da Bíblia.[129] Por exemplo, Platão escreve em seu Leis do século IV a.C. (6.775): "Beber em excesso é uma prática que em lugar algum é decente... nem tampouco segura... Convém que tanto a noiva quanto o noivo estejam sóbrios... a fim de garantir, tanto quanto possível, em todos os casos, que a criança concebida seja originada dos lombos de pais sóbrios." O Talmude do século VI d.C. (Kethuboth 60b) adverte: "Aquele que bebe bebida inebriante terá filhos desajeitados." Contudo, fontes antigas raramente, se é que alguma vez, distinguem o consumo materno de álcool do paterno, estando mais preocupadas com a concepção do que com a gravidez. Muitas vezes, as fontes podem ser vistas como expressando ideias de hereditariedade, ou seja, que as crianças provavelmente se pareceriam com seus pais (alcoólatras), em vez de apresentar a visão moderna de que o álcool em si tem impacto.[130][97]

Em 1725, no auge da Febre do Gin, médicos britânicos peticionaram à Câmara dos Comuns sobre os efeitos das bebidas fortes quando consumidas por mulheres grávidas, afirmando que tal prática era "muitas vezes a causa de crianças fracas, débeis e doentias, que, em vez de uma vantagem e força, seriam um encargo para o seu país".[131] Há muitas outras referências históricas semelhantes durante esse período.[132] O gin foi especificamente implicado como prejudicial à saúde das crianças e como causa de natimortos e mortalidade infantil, como retratado em Gin Lane, de William Hogarth. Em contraste, Beer Street, de Hogarth, mostra comércio e felicidade, sugerindo que o álcool da cerveja não era conhecido por ter efeitos nocivos nessa época.[130]
No século XIX, Benjamin Rush e Thomas Trotter fizeram campanha contra o consumo de álcool durante a gravidez para evitar dependência e deficiência mental em crianças.[130] O movimento abstêmio e os movimentos de temperança popularizaram essas e outras alegações,[133][134] incluindo os efeitos teratogênicos do álcool em embriões animais,[130] mas frequentemente de forma sensacionalista, a ponto de que qualquer achado de que o álcool era prejudicial fosse amplamente denunciado como propaganda.[132] Uma observação relevante sobre possíveis ligações entre o uso materno de álcool e danos fetais foi feita em 1899 pelo Dr. William Sullivan, médico prisional de Liverpool, que notou taxas mais altas de natimorto entre 120 prisioneiras alcoólatras do que entre suas parentes sóbrias. Ele sugeriu que o agente causal fosse o consumo de álcool.[135] Isso contradizia a crença predominante da época de que a hereditariedade causava deficiência intelectual, pobreza e comportamento criminoso, conclusão comum nos estudos da época.[56] Um estudo de caso de Henry H. Goddard sobre a Família Kallikak — popular no início do século XX — representa essa perspectiva anterior,[136] embora pesquisadores posteriores tenham sugerido que os Kallikaks quase certamente apresentavam SAF.[137] Estudos gerais e discussões sobre alcoolismo ao longo da metade do século XX eram tipicamente baseados em argumentos hereditários.[138] Pesquisadores eram frequentemente defensores da temperança e financiados por organizações como a Anti-Saloon League, de modo que clínicos encaravam essas pesquisas com grande ceticismo. O movimento de temperança efetivamente paralisou a pesquisa séria sobre o assunto por quase 50 anos após a Lei Seca.[130] Na década de 1940, era geralmente descartado como superstição.[39]
Entre as décadas de 1960 e 1980, o álcool foi comumente usado como tocolítico, um método para interromper o trabalho de parto prematuro (nascimentos com menos de 37 semanas de gestação). O método foi introduzido pelo Dr. Fritz Fuchs, chefe do departamento de obstetrícia e ginecologia da Cornell University Medical College.[139][140] Médicos recomendavam uma pequena quantidade de álcool para acalmar o útero durante contrações no início da gravidez ou contrações de Braxton Hicks. Nos estágios posteriores, o álcool era administrado por via intravenosa e frequentemente em grandes quantidades. "As mulheres experimentavam efeitos semelhantes aos da ingestão oral, incluindo intoxicação, náuseas e vômitos, e potencial intoxicação alcoólica, seguidos de ressaca quando o álcool era interrompido."[141] O vômito colocava a mãe em alto risco de aspiração e era "um procedimento brutal para todos os envolvidos".[139] Como o álcool era administrado por via intravenosa, o médico podia continuar o tratamento mesmo após a paciente ter desmaiado, resultando em intoxicação muito maior do que seria possível por ingestão oral. Tal intoxicação intensa era altamente propensa a contribuir para SAFD.[139] Em uma revisão de 2015, concluiu-se que o etanol não era melhor que placebo (água com açúcar) na prevenção do parto prematuro e da mortalidade neonatal. Além de ser menos eficaz que outros fármacos beta-miméticos (agentes tocolíticos) para adiar o parto, o etanol também levou a uma maior taxa de bebês com baixo peso, problemas respiratórios ao nascer e morte neonatal.[142]
Reconhecimento como síndrome
Na França, em 1957, Jacqueline Rouquette descreveu em sua tese (não publicada) 100 crianças cujos pais eram alcoólatras. "Ela forneceu uma boa descrição em certos casos do facies", segundo seu orientador, Paul Lemoine.[143] Em 1968, Paul Lemoine, de Nantes, publicou um estudo em uma revista médica francesa sobre crianças com características distintas cujas mães eram alcoólatras.[144]
Independentemente, nos Estados Unidos, Christy Ulleland, da Universidade de Washington, conduziu um estudo de 18 meses entre 1968–1969 documentando o risco do consumo materno de álcool entre os filhos de 11 mães alcoólatras.[145] Este estudo é, provavelmente, a verdadeira origem da compreensão moderna.[132] Os bebês foram estudados pelos disformologistas Kenneth Lyons Jones e David Weyhe Smith, colegas de Ulleland na Universidade de Washington,[132] que identificaram um padrão de "defeitos craniofaciais, de membros e cardiovasculares associados a deficiência de crescimento pré-natal e atraso no desenvolvimento" em oito crianças. O padrão de malformações indicava que o dano era pré-natal. Eles nomearam esses defeitos como "síndrome alcoólica fetal".[146] A notícia da descoberta surpreendeu alguns, enquanto outros foram céticos em relação aos resultados.[147] Enquanto muitas síndromes são epônimas, isto é, nomeadas em homenagem ao médico que primeiro relatou a associação dos sintomas, Smith nomeou a SAF pelo agente causal dos sintomas.[148] Ele argumentou que isso incentivaria a prevenção, acreditando que se as pessoas soubessem que o consumo materno de álcool causava a síndrome, a abstinência durante a gravidez se seguiria a partir da educação do paciente e da conscientização pública.[148] Na época, ninguém conhecia toda a gama de possíveis defeitos congênitos da SAF nem sua taxa de prevalência.[148]
Em 1978, dentro de nove anos após a descoberta em Washington, estudos com animais, incluindo primatas não humanos realizados no Primate Center da Universidade de Washington por Sterling Clarren, confirmaram que o álcool era um teratógeno. Em 1978, 245 casos de SAF já haviam sido relatados por pesquisadores médicos, e a síndrome começou a ser descrita como a causa mais frequente conhecida de deficiência intelectual.[carece de fontes] Em 1979, as descobertas de Washington e Nantes foram confirmadas por um grupo de pesquisa em Gotemburgo, Suécia.[149]
“Espectro” em vez de Síndrome
Com o tempo, pesquisas subsequentes e a experiência clínica sugeriram que uma variedade de efeitos poderia surgir da exposição pré-natal ao álcool. O termo efeitos do álcool fetal (FAE) foi usado para transtorno do neurodesenvolvimento relacionado ao álcool e defeitos congênitos relacionados ao álcool.[1] Foi inicialmente usado em estudos de pesquisa para descrever humanos e animais em que efeitos teratogênicos foram observados após exposição pré-natal confirmada ao álcool (ou exposição desconhecida no caso de humanos), mas sem anomalias físicas óbvias.[150] Smith (1981) descreveu o FAE como um "conceito extremamente importante" para destacar os efeitos debilitantes da lesão cerebral, independentemente do crescimento ou das características faciais.[151] Esse termo caiu em desuso entre os clínicos na década de 1990 porque muitas vezes era considerado pelo público como uma deficiência menos grave do que a SAF, quando, na verdade, seus efeitos podiam ser igualmente prejudiciais.[152] Em 1996, os termos substitutos ARBD e ARND foram introduzidos. Em 2002, o Congresso dos Estados Unidos determinou que o CDC desenvolvesse diretrizes diagnósticas para SAF e, em 2004, foi adotada uma definição de um termo que já havia sido usado por alguns nos anos 1990, o Transtorno do Espectro Alcoólico Fetal (TEAF),[45]> para incluir a SAF, bem como outras condições resultantes da exposição pré-natal ao álcool.[148]
Atualmente, a SAF[26][150][146] é a única expressão da exposição pré-natal ao álcool definida pela Classificação Estatística Internacional de Doenças e Problemas Relacionados com a Saúde e associada a códigos de CID-9 e diagnósticos.[carece de fontes]
Defeitos congênitos relacionados ao álcool (ARBD), anteriormente conhecidos como possível efeito do álcool fetal (PFAE),[150] foi um termo proposto como alternativa a FAE e PFAE.[153] O IOM apresenta ARBD como uma lista de anomalias congênitas que estão ligadas ao uso materno de álcool, mas não possuem características-chave de TEAF.[26] PFAE e ARBD caíram em desuso porque essas anomalias não são necessariamente específicas ao consumo materno de álcool e não são critérios para diagnóstico de TEAF.[56]
Em 2013, a Associação Americana de Psiquiatria introduziu o transtorno do neurocomportamento associado à exposição pré-natal ao álcool (ND-PAE).[84]
Sociedade e cultura
Criminalização
A criminalização do uso de substâncias durante a gravidez devido a danos ao feto ou à criança é fortemente debatida.[154][155] Elizabeth Armstrong questionou a abordagem de tolerância zero em relação ao consumo de álcool durante a gravidez, descrevendo-a como um pânico moral.[156][157] Embora o consumo excessivo de álcool durante a gravidez seja reconhecido como prejudicial ao feto, os efeitos de ingestões baixas permanecem debatidos, particularmente na ausência de ensaios clínicos randomizados (cf. § Causas).[51][49] A recomendação de abstinência do Reino Unido não foi escolhida com base em evidências científicas, mas sim por ser um conselho simples que garantiria que ninguém subestimasse o risco.[158] A lei de agressão fetal de 2014 do Tennessee (que expirou em 2016) foi criticada por não abordar o uso de álcool.[159][160] A lei criminalizou o uso de opioides durante a gravidez e resultou em mulheres evitando atendimento médico profissional por medo de processo judicial.[161] Uma ampla variedade de organizações profissionais se opõe à criminalização.[162][163] Minnesota, Dakota do Norte, Oklahoma, Dakota do Sul e Wisconsin têm autorização legal para a internação civil involuntária de mulheres que abusam do álcool durante a gravidez.[164]
Controvérsia do CDC em 2016
Em 2016, um comunicado de imprensa e um infográfico do CDC intitulado "Mais de 3 milhões de mulheres nos EUA em risco de gravidez exposta ao álcool" causaram controvérsia.[165] O comunicado do CDC continha a mensagem "O risco é real. Por que arriscar?".[166][167] Darlena Cunha, da revista Time, interpretou o infográfico como dizendo que todas as mulheres em idade fértil não deveriam beber de forma alguma, caso engravidassem acidentalmente, e chamou-o de "táticas de medo" e "recomendações de vergonha".[168] Julie Beck disse que o infográfico insinuava que "seu útero é uma caixa de Schrödinger e você não deveria despejar álcool nele a menos que tenha verificado se o caminho está 100% livre".[169] O CDC posteriormente esclareceu que o infográfico não tinha a intenção de criar novas diretrizes ou recomendações para mulheres em idade pré-gravídica, mas sim de incentivar conversas sobre álcool com profissionais de saúde.[170] Mesmo assim, metade das gestações em países desenvolvidos e mais de 80% em países em desenvolvimento são não planejadas. Muitas mulheres não percebem que estão grávidas nos estágios iniciais e continuam bebendo durante a gestação.[46]
Na ficção
No romance Admirável Mundo Novo (1932), de Aldous Huxley, (em que todos os fetos são gestados in vitro em uma fábrica), fetos de castas inferiores são criados recebendo transfusões de álcool (Processo Bokanovsky) para reduzir a inteligência e a altura, condicionando-os assim a tarefas simples e manuais. Conexões entre álcool e embriões incubados são feitas várias vezes no romance.[171]
Notas e referências
Notas
- ↑ Códigos CID no estudo de Popova: R62.8††, R62.8¶¶, P05.9, P07.1, R62.8§§, R62.8‡‡, Q02
- ↑ Q10.3†, Q38.0*, Q38.0†
- ↑ R94.1
- ↑ F91
- ↑ F80, F80.1, F80.2, F80.9
- ↑ H65.2,H90.2,H90.5,H65.0
- ↑ H54,H52.2,H52.6,H54.2/54.4/54.5
- ↑ F89
- ↑ P07.3
- ↑ F10.2/F19.2
- ↑ Fóvea coccígea (Q14.1‡). Tortuosidade da retina (Q14.1§)
- ↑ Q76.4
- ↑ F90.0
- ↑ Q10.0¶
- ↑ Q75.2
Referências
- ↑ a b c d e f g h i j k l m n «Facts about FASDs». 16 de abril de 2015. Consultado em 10 de junho de 2015. Cópia arquivada em 23 de maio de 2015
- ↑ a b c d e f g h i Chudley AE, Conry J, Cook JL, Loock C, Rosales T, LeBlanc N (março 2005). «Fetal alcohol spectrum disorder: Canadian guidelines for diagnosis». Canadian Medical Association Journal. 172 (5 Suppl): S1–S21. PMC 557121
 . PMID 15738468. doi:10.1503/cmaj.1040302
. PMID 15738468. doi:10.1503/cmaj.1040302
- ↑ a b Rasmussen C, Andrew G, Zwaigenbaum L, Tough S (março de 2008). «Neurobehavioural outcomes of children with fetal alcohol spectrum disorders: A Canadian perspective». Paediatrics & Child Health. 13 (3): 185–191. PMC 2529423
 . PMID 19252695
. PMID 19252695
- ↑ a b «Alcohol Use in Pregnancy». 17 de abril de 2014. Consultado em 10 de junho de 2015. Cópia arquivada em 28 de junho de 2015
- ↑ a b Roszel EL (abril 2015). «Central nervous system deficits in fetal alcohol spectrum disorder». The Nurse Practitioner. 40 (4): 24–33. PMID 25774812. doi:10.1097/01.NPR.0000444650.10142.4f
- ↑ a b Thanh NX, Jonsson E (2016). «Life Expectancy of People with Fetal Alcohol Syndrome». Journal of Population Therapeutics and Clinical Pharmacology. 23 (1): e53–e59. PMID 26962962
- ↑ a b May PA, Chambers CD, Kalberg WO, Zellner J, Feldman H, Buckley D, et al. (fevereiro de 2018). «Prevalence of Fetal Alcohol Spectrum Disorders in 4 US Communities». JAMA. 319 (5): 474–482. PMC 5839298
 . PMID 29411031. doi:10.1001/jama.2017.21896
. PMID 29411031. doi:10.1001/jama.2017.21896
- ↑ Oh SS, Kim YJ, Jang SI, Park S, Nam CM, Park EC (novembro de 2020). «Hospitalizations and mortality among patients with fetal alcohol spectrum disorders: a prospective study». Scientific Reports. 10 (1). 19512 páginas. PMC 7658994
 . PMID 33177533. doi:10.1038/s41598-020-76406-6
. PMID 33177533. doi:10.1038/s41598-020-76406-6
- ↑ a b c d e «Facts about FASDs». Centers for Disease Control and Prevention (em inglês). Division of Birth Defects and Developmental Disabilities - U.S. Department of Health and Human Services. 2015. Consultado em 28 de Agosto de 2016
- ↑ a b c Coriale et al 2013, p. 359-369.
- ↑ Lamônica et al 2010, p. 129-133.
- ↑ Momino et al 2008, p. S76-S79.
- ↑ «Síndrome Alcoólica Fetal». Álcool e Drogas sem Distorção. NEAD - Núcleo Einstein de Álcool e Drogas do Hospital Israelita Albert Einstein. 2009. Consultado em 28 de Agosto de 2016. Arquivado do original em 14 de setembro de 2016
- ↑ a b c Riley et al 2011, p. 73-80.
- ↑ a b «Fetal Alcohol Exposure». National Institute on Alcohol Abuse and Alcoholism (em inglês). U.S. Department of Health and Human Services - National Institutes of Health. 2015. Consultado em 28 de Agosto de 2016
- ↑ a b McHugh et al 2014, p. 177-189.
- ↑ Uban et al 2011, p. 73-75.
- ↑ Lima, M.G.A.; Palhares, H.M. (19 de abril de 2016). «Sobre a Síndrome Alcoólica Fetal - Consulta nº 17.791/16». Pareceres. Conselho Regional de Medicina do Estado de São Paulo. Consultado em 28 de Agosto de 2016
- ↑ Roszel 2015, p. 24-33.
- ↑ «Prevalence of FASDs». Centers for Disease Control and Prevention (em inglês). Division of Birth Defects and Developmental Disabilities - U.S. Department of Health and Human Services. 2016. Consultado em 28 de Agosto de 2016
- ↑ a b c d e f Clinical growth charts. Arquivado em 2010-12-03 no Wayback Machine National Center for Growth Statistics. Consultado em 10 de abril de 2007
- ↑ a b c d e FAS facial features Arquivado em 2007-10-27 no Wayback Machine. FAS Diagnostic and Prevention Network, University of Washington. Consultado em 10 de abril de 2007
- ↑ Popova, Svetlana; Lange, Shannon; Shield, Kevin; Mihic, Alanna; Chudley, Albert E.; Mukherjee, Raja A. S.; Bekmuradov, Dennis; Rehm, Jürgen (5 de março de 2016). «Comorbidity of fetal alcohol spectrum disorder: a systematic review and meta-analysis»
 . The Lancet (em inglês). 387 (10022): 978–987. ISSN 0140-6736. PMID 26777270. doi:10.1016/S0140-6736(15)01345-8
. The Lancet (em inglês). 387 (10022): 978–987. ISSN 0140-6736. PMID 26777270. doi:10.1016/S0140-6736(15)01345-8
- ↑ Brown, Jasmine M.; Bland, Roger; Jonsson, Egon; Greenshaw, Andrew J. (3 de março de 2019). «The Standardization of Diagnostic Criteria for Fetal Alcohol Spectrum Disorder (FASD): Implications for Research, Clinical Practice and Population Health». Canadian Journal of Psychiatry. Revue Canadienne de Psychiatrie. 64 (3): 169–176. ISSN 0706-7437. PMC 6405816
 . PMID 29788774. doi:10.1177/0706743718777398
. PMID 29788774. doi:10.1177/0706743718777398
- ↑ a b c d e f «An Alcohol-free pregnancy is the best choice for your baby» (PDF). Centers for Disease Control and Prevention. Consultado em 10 de agosto de 2017. Arquivado do original (PDF) em 20 de dezembro de 2023
 Este artigo incorpora texto desta fonte, que está no domínio público.
Este artigo incorpora texto desta fonte, que está no domínio público.
- ↑ a b c d e f g h i j k l m n o p q r s t Institute of Medicine Committee to Study Fetal Alcohol Syndrome (1995). Stratton K, Howe C, Battaglia FC, eds. Fetal alcohol syndrome: diagnosis, epidemiology, prevention, and treatment. Washington, D.C.: National Academy Press. ISBN 978-0-309-05292-4. Cópia arquivada em 11 de março de 2016
- ↑ Coriale, G; Fiorentino, D; Di Lauro, F; Marchitelli, R; Scalese, B; Fiore, M; Maviglia, M; Ceccanti, M (2013). «Fetal Alcohol Spectrum Disorder (FASD): neurobehavioral profile, indications for diagnosis and treatment.». Rivista di Psichiatria. 48 (5): 359–369. PMID 24326748. doi:10.1708/1356.15062
- ↑ a b c «Guidelines for the identification and management of substance use and substance use disorders in pregnancy» (PDF). World Health Organization. 2014. Consultado em 11 de agosto de 2017
- ↑ a b c d Kingdon D, Cardoso C, McGrath JJ (fevereiro de 2016). «Research Review: Executive function deficits in fetal alcohol spectrum disorders and attention-deficit/hyperactivity disorder - a meta-analysis». Journal of Child Psychology and Psychiatry, and Allied Disciplines. 57 (2): 116–131. PMC 5760222
 . PMID 26251262. doi:10.1111/jcpp.12451
. PMID 26251262. doi:10.1111/jcpp.12451
- ↑ a b c CDC (24 de maio de 2021). «Alcohol Use in Pregnancy». Centers for Disease Control and Prevention (em inglês). Consultado em 13 de setembro de 2021
- ↑ Strömland K, Pinazo-Durán MD (2002). «Ophthalmic involvement in the fetal alcohol syndrome: clinical and animal model studies». Alcohol and Alcoholism. 37 (1): 2–8. PMID 11825849. doi:10.1093/alcalc/37.1.2

- ↑ Yin, X.; Li, J.; Li, Y.; Zou, S. (novembro de 2019). «Maternal alcohol consumption and oral clefts: a meta-analysis»
 . British Journal of Oral and Maxillofacial Surgery (em inglês). 57 (9): 839–846. PMID 31473040. doi:10.1016/j.bjoms.2019.08.013
. British Journal of Oral and Maxillofacial Surgery (em inglês). 57 (9): 839–846. PMID 31473040. doi:10.1016/j.bjoms.2019.08.013
- ↑ «Dangers of Drinking While Pregnant - DrugAbuse.com». drugabuse.com (em inglês). 27 de julho de 2016. Consultado em 17 de novembro de 2018
- ↑ Cook, Jonathan C.; Lynch, Mary Ellen; Coles, Claire D. (5 de junho de 2019). «Association Analysis: Fetal Alcohol Spectrum Disorder and Hypertension Status in Children and Adolescents»
 . Alcoholism: Clinical and Experimental Research. 43 (8): 1727–1733. PMID 31166027. doi:10.1111/acer.14121. Consultado em 30 de março de 2023
. Alcoholism: Clinical and Experimental Research. 43 (8): 1727–1733. PMID 31166027. doi:10.1111/acer.14121. Consultado em 30 de março de 2023
- ↑ «Understanding Fetal Alcohol Spectrum Disorders». National Institute on Alcohol Abuse and Alcoholism (NIAAA). Consultado em 18 de março de 2024
- ↑ a b c Popova S, Lange S, Probst C, Gmel G, Rehm J (março 2017). «Estimation of national, regional, and global prevalence of alcohol use during pregnancy and fetal alcohol syndrome: a systematic review and meta-analysis». The Lancet. Global Health. 5 (3): e290–e299. PMID 28089487. doi:10.1016/S2214-109X(17)30021-9

- ↑ «Alcohol during pregnancy». www.marchofdimes.org (em inglês). Consultado em 17 de julho de 2024
- ↑ Welch, Ashley (4 de fevereiro de 2016). «CDC to younger women: Better take your birth control before you drink that glass of wine». Los Angeles Times
- ↑ a b c d e Yaffe SJ (2011). Drugs in pregnancy and lactation: a reference guide to fetal and neonatal risk 9 ed. Philadelphia: Wolters Kluwer Health/Lippincott Williams & Wilkins. p. 527. ISBN 978-1-60831-708-0. Cópia arquivada em 10 de setembro de 2017
- ↑ a b Gupta KK, Gupta VK, Shirasaka T (agosto 2016). «An Update on Fetal Alcohol Syndrome-Pathogenesis, Risks, and Treatment». Alcoholism: Clinical and Experimental Research. 40 (8): 1594–1602. PMID 27375266. doi:10.1111/acer.13135
- ↑ a b c «Fetal Alcohol Exposure». Abril de 2015. Consultado em 10 de junho de 2015. Cópia arquivada em 10 de junho de 2015
- ↑ a b c Chang. «UpToDate: Alcohol intake and pregnancy». www.uptodate.com. Consultado em 11 de setembro de 2021
- ↑ «Committee opinion no. 496: At-risk drinking and alcohol dependence: obstetric and gynecologic implications». Obstetrics and Gynecology. 118 (2 Pt 1): 383–388. Agosto de 2011. ISSN 1873-233X. PMID 21775870. doi:10.1097/AOG.0b013e31822c9906
- ↑ a b Burd, L; Blair, J; Dropps, K (17 de maio de 2012). «Prenatal alcohol exposure, blood alcohol concentrations and alcohol elimination rates for the mother, fetus and newborn». Journal of Perinatology (em inglês). 32 (9): 652–659. ISSN 0743-8346. PMID 22595965. doi:10.1038/jp.2012.57
- ↑ a b c d Williams JF, Smith VC (2015). «Fetal Alcohol Spectrum Disorders». Pediatrics. 136 (5): e1395–e1406. PMID 26482673. doi:10.1542/peds.2015-3113

- ↑ a b c «Counting the costs of drinking alcohol during pregnancy». Bulletin of the World Health Organization. 95 (5): 320–321. 2017. PMC 5418824
 . PMID 28479632. doi:10.2471/BLT.17.030517. Consultado em 11 de agosto de 2017
. PMID 28479632. doi:10.2471/BLT.17.030517. Consultado em 11 de agosto de 2017
- ↑ a b McHugh RK, Wigderson S, Greenfield SF (junho de 2014). «Epidemiology of substance use in reproductive-age women». Obstetrics and Gynecology Clinics of North America. 41 (2): 177–189. PMC 4068964
 . PMID 24845483. doi:10.1016/j.ogc.2014.02.001
. PMID 24845483. doi:10.1016/j.ogc.2014.02.001
- ↑ Sundermann AC, Zhao S, Young CL, Lam L, Jones SH, Velez Edwards DR, Hartmann KE (agosto 2019). «Alcohol Use in Pregnancy and Miscarriage: A Systematic Review and Meta-Analysis». Alcoholism: Clinical and Experimental Research. 43 (8): 1606–1616. PMC 6677630
 . PMID 31194258. doi:10.1111/acer.14124
. PMID 31194258. doi:10.1111/acer.14124
- ↑ a b Mamluk L, Edwards HB, Savović J, Leach V, Jones T, Moore TH, et al. (agosto 2017). «Low alcohol consumption and pregnancy and childhood outcomes: time to change guidelines indicating apparently 'safe' levels of alcohol during pregnancy? A systematic review and meta-analyses». BMJ Open. 7 (7): e015410. PMC 5642770
 . PMID 28775124. doi:10.1136/bmjopen-2016-015410
. PMID 28775124. doi:10.1136/bmjopen-2016-015410
- ↑ Mamluk, Loubaba; Jones, Timothy; Ijaz, Sharea; Edwards, Hannah B; Savović, Jelena; Leach, Verity; Moore, Theresa H M; von Hinke, Stephanie; Lewis, Sarah J; Donovan, Jenny L; Lawlor, Deborah A; Davey Smith, George; Fraser, Abigail; Zuccolo, Luisa (23 de janeiro de 2021). «Evidence of detrimental effects of prenatal alcohol exposure on offspring birthweight and neurodevelopment from a systematic review of quasi-experimental studies». International Journal of Epidemiology. 49 (6): 1972–1995. PMC 7825937
 . PMID 31993631. doi:10.1093/ije/dyz272
. PMID 31993631. doi:10.1093/ije/dyz272
- ↑ a b Flak, Audrey L.; Su, Su; Bertrand, Jacquelyn; Denny, Clark H.; Kesmodel, Ulrik S.; Cogswell, Mary E. (2014). «The association of mild, moderate, and binge prenatal alcohol exposure and child neuropsychological outcomes: a meta-analysis». Alcoholism: Clinical and Experimental Research. 38 (1): 214–226. ISSN 1530-0277. PMID 23905882. doi:10.1111/acer.12214

- ↑ Bandoli, G; Hayes, S; Delker, E (2023). «Low to Moderate Prenatal Alcohol Exposure and Neurodevelopmental Outcomes: A Narrative Review and Methodological Considerations.». Alcohol Research: Current Reviews. 43 (1). 01 páginas. PMC 10027299
 . PMID 36950180. doi:10.35946/arcr.v43.1.01
. PMID 36950180. doi:10.35946/arcr.v43.1.01
- ↑ Mamluk L, Edwards HB, Savović J, Leach V, Jones T, Moore TH, et al. (agosto 2017). «Low alcohol consumption and pregnancy and childhood outcomes: time to change guidelines indicating apparently 'safe' levels of alcohol during pregnancy? A systematic review and meta-analyses». BMJ Open. 7 (7): e015410. PMC 5642770
 . PMID 28775124. doi:10.1136/bmjopen-2016-015410
. PMID 28775124. doi:10.1136/bmjopen-2016-015410
- ↑ «Pregnancy and alcohol: occasional, light drinking may be safe». Prescrire International. 21 (124): 44–50. Fevereiro de 2012. PMID 22413723
- ↑ Liyanage-Zachariah V, Harding K (2019), Genetic and Epigenetic Perspectives on the Role of Fathers in Fetal Alcohol Spectrum Disorder (PDF), Canada FASD Research Network
- ↑ a b c d e f g h i j k l m Streissguth, A. (1997). Fetal Alcohol Syndrome: A Guide for Families and Communities. Baltimore: Brookes Publishing. ISBN 1-55766-283-5.
- ↑ «Alcohol and Pregnancy Questions and Answers | FASD | NCBDDD | CDC». www.cdc.gov. 4 de agosto de 2017. Consultado em 25 de setembro de 2017
- ↑ a b Carmona RH (2005). «A 2005 Message to Women from the U.S. Surgeon General» (PDF). Consultado em 12 de junho de 2015. Cópia arquivada (PDF) em 24 de setembro de 2015
- ↑ Rankin, Lissa (23 de agosto de 2011). Fertility, Pregnancy, and Childbirth. [S.l.]: St. Martin's Press. p. 14. ISBN 978-1-4299-5932-2.
In 1981, the surgeon general put out the now-ubiquitous warning about alcohol and pregnancy.
- ↑ «Framework for alcohol policy in the WHO European Region» (PDF). World Health Organisation. Consultado em 15 de março de 2024. Arquivado do original (PDF) em 3 de maio de 2010
- ↑ «Drinking alcohol while pregnant». NHS. 2 de dezembro de 2020. Consultado em 31 de dezembro de 2020. Cópia arquivada em 31 de dezembro de 2020
- ↑ Deaver EL (1 de janeiro de 1997). «History and implications of the Alcoholic Beverage Labeling Act of 1988»
 . Journal of Substance Misuse. 2 (4): 234–237. ISSN 1357-5007. doi:10.3109/14659899709081975
. Journal of Substance Misuse. 2 (4): 234–237. ISSN 1357-5007. doi:10.3109/14659899709081975
- ↑ Jonsson, Egon; Salmon, Amy; Warren, Kenneth R (março de 2014). «The international charter on prevention of fetal alcohol spectrum disorder». The Lancet Global Health. 2 (3): e135–e137. PMID 25102841. doi:10.1016/S2214-109X(13)70173-6

- ↑ a b c d DeVido, Jeffrey; Bogunovic, Olivera; Weiss, Roger D. (2015). «Alcohol Use Disorders in Pregnancy». Harvard Review of Psychiatry. 23 (2): 112–121. ISSN 1067-3229. PMC 4530607
 . PMID 25747924. doi:10.1097/HRP.0000000000000070
. PMID 25747924. doi:10.1097/HRP.0000000000000070
- ↑ a b c Fairbanks, Jeremiah; Umbreit, Audrey; Kolla, Bhanu Prakash; Karpyak, Victor M.; Schneekloth, Terry D.; Loukianova, Larissa L.; Sinha, Shirshendu (1 de setembro de 2020). «Evidence-Based Pharmacotherapies for Alcohol Use Disorder: Clinical Pearls». Mayo Clinic Proceedings (em inglês). 95 (9): 1964–1977. ISSN 0025-6196. PMID 32446635. doi:10.1016/j.mayocp.2020.01.030

- ↑ a b Thibaut, Florence; Chagraoui, Abdeslam; Buckley, Leslie; Gressier, Florence; Labad, Javier; Lamy, Sandrine; Potenza, Marc N.; Kornstein, Susan G.; Rondon, Marta; Riecher-Rössler, Anita; Soyka, Michael (2 de janeiro de 2019). «WFSBP and IAWMH Guidelines for the treatment of alcohol use disorders in pregnant women»
 . The World Journal of Biological Psychiatry. 20 (1): 17–50. ISSN 1562-2975. PMID 30632868. doi:10.1080/15622975.2018.1510185
. The World Journal of Biological Psychiatry. 20 (1): 17–50. ISSN 1562-2975. PMID 30632868. doi:10.1080/15622975.2018.1510185
- ↑ Alkermes. VIVITROL (naltrexone for extended-release injectable suspension) U.S. Food and Drug Administration website. [1]. Revised March 2021. Accessed September 12, 2021.
- ↑ Reus, Victor I.; Fochtmann, Laura J.; Bukstein, Oscar; Eyler, A. Evan; Hilty, Donald M.; Horvitz-Lennon, Marcela; Mahoney, Jane; Pasic, Jagoda; Weaver, Michael; Wills, Cheryl D.; McIntyre, Jack (1 de janeiro de 2018). «The American Psychiatric Association Practice Guideline for the Pharmacological Treatment of Patients With Alcohol Use Disorder»
 . American Journal of Psychiatry. 175 (1): 86–90. ISSN 0002-953X. PMID 29301420. doi:10.1176/appi.ajp.2017.1750101
. American Journal of Psychiatry. 175 (1): 86–90. ISSN 0002-953X. PMID 29301420. doi:10.1176/appi.ajp.2017.1750101
- ↑ Bhuvaneswar, Chaya G.; Chang, Grace; Epstein, Lucy A.; Stern, Theodore A. (2007). «Alcohol Use During Pregnancy: Prevalence and Impact». Primary Care Companion to the Journal of Clinical Psychiatry. 9 (6): 455–460. ISSN 1523-5998. PMC 2139915
 . PMID 18185825. doi:10.4088/PCC.v09n0608
. PMID 18185825. doi:10.4088/PCC.v09n0608
- ↑ Brien JF, Loomis CW, Tranmer J, McGrath M (maio 1983). «Disposition of ethanol in human maternal venous blood and amniotic fluid». American Journal of Obstetrics and Gynecology. 146 (2): 181–186. PMID 6846436. doi:10.1016/0002-9378(83)91050-5
- ↑ Nava-Ocampo AA, Velázquez-Armenta Y, Brien JF, Koren G (junho de 2004). «Elimination kinetics of ethanol in pregnant women». Reproductive Toxicology. 18 (4): 613–617. Bibcode:2004RepTx..18..613N. PMID 15135856. doi:10.1016/j.reprotox.2004.02.012
- ↑ Warren KR, Li TK (abril 2005). «Genetic polymorphisms: impact on the risk of fetal alcohol spectrum disorders». Birth Defects Research. Part A, Clinical and Molecular Teratology. 73 (4): 195–203. PMID 15786496. doi:10.1002/bdra.20125

- ↑ Laufer BI, Mantha K, Kleiber ML, Diehl EJ, Addison SM, Singh SM (julho 2013). «Long-lasting alterations to DNA methylation and ncRNAs could underlie the effects of fetal alcohol exposure in mice». Disease Models & Mechanisms. 6 (4): 977–992. PMC 3701217
 . PMID 23580197. doi:10.1242/dmm.010975
. PMID 23580197. doi:10.1242/dmm.010975
- ↑ Shabtai Y, Fainsod A (abril 2018). «Competition between ethanol clearance and retinoic acid biosynthesis in the induction of fetal alcohol syndrome». Biochemistry and Cell Biology. 96 (2): 148–160. PMID 28982012. doi:10.1139/bcb-2017-0132
- ↑ a b «Drinking and Your Pregnancy». pubs.niaaa.nih.gov (em inglês). Consultado em 16 de novembro de 2018
- ↑ Bake, Shameena; Tingling, Joseph D.; Miranda, Rajesh C. (5 de dezembro de 2011). «Ethanol exposure during pregnancy persistently attenuates cranially-directed blood flow in the developing fetus: Evidence from ultrasound imaging in a murine second trimester equivalent model». Alcoholism: Clinical and Experimental Research. 36 (5): 748–758. ISSN 0145-6008. PMC 3297711
 . PMID 22141380. doi:10.1111/j.1530-0277.2011.01676.x
. PMID 22141380. doi:10.1111/j.1530-0277.2011.01676.x
- ↑ «Fetal Alcohol Syndrome (FAS) and Fetal Alcohol Spectrum Disorders (FASD) – conditions and interventions». www.sbu.se. Swedish Agency for Health Technology Assessment and Assessment of Social Services (SBU). 14 de dezembro de 2016. Consultado em 8 de junho de 2017. Cópia arquivada em 6 de junho de 2017
- ↑ a b c d e f g h i j k l m n o p Astley, S.J. (2004). Diagnostic Guide for Fetal Alcohol Spectrum Disorders: The 4-Digit Diagnostic Code. Seattle: University of Washington. PDF disponível em FAS Diagnostic and Prevention Network Arquivado em 2006-12-16 no Wayback Machine. Consultado em 11 de abril de 2007.
- ↑ a b c d e f g h i j k l m Fetal Alcohol Syndrome: Guidelines for Referral and Diagnosis (PDF). CDC (julho de 2004). Consultado em 19 de outubro de 2019
- ↑ a b c d e f Lang J (2006). «Ten Brain Domains: A Proposal for Functional Central Nervous System Parameters for Fetal Alcohol Spectrum Disorder Diagnosis and Follow-up» (PDF). Journal of the FAS Institute. 4: 1–11. Consultado em 4 de fevereiro de 2007. Arquivado do original (PDF) em 26 de setembro de 2006
- ↑ Chudley, Albert E.; Conry, Julianne; Cook, Jocelynn L.; Loock, Christine; Rosales, Ted; LeBlanc, Nicole (1 de março de 2005). «Fetal alcohol spectrum disorder: Canadian guidelines for diagnosis». Canadian Medical Association Journal. 172 (5 Suppl): S1–S21. ISSN 0820-3946. PMC 557121
 . PMID 15738468. doi:10.1503/cmaj.1040302
. PMID 15738468. doi:10.1503/cmaj.1040302
- ↑ Okulicz-Kozaryn K, Maryniak A, Borkowska M, Śmigiel R, Dylag KA (15 de julho de 2021). «Diagnosis of Fetal Alcohol Spectrum Disorders (FASDs): Guidelines of Interdisciplinary Group of Polish Professionals». International Journal of Environmental Research and Public Health. 18 (14). 7526 páginas. ISSN 1661-7827. PMC 8304012
 . PMID 34299977. doi:10.3390/ijerph18147526
. PMID 34299977. doi:10.3390/ijerph18147526
- ↑ Moore, Eileen M.; Riley, Edward P. (3 de setembro de 2015). «What Happens When Children with Fetal Alcohol Spectrum Disorders Become Adults?». Current Developmental Disorders Reports. 2 (3): 219–227. ISSN 2196-2987. PMC 4629517
 . PMID 26543794. doi:10.1007/s40474-015-0053-7
. PMID 26543794. doi:10.1007/s40474-015-0053-7
- ↑ a b c Hagan JF, Balachova T, Bertrand J, Chasnoff I, Dang E, Fernandez-Baca D, et al. (outubro 2016). «Neurobehavioral Disorder Associated With Prenatal Alcohol Exposure». Pediatrics. 138 (4): e20151553. PMC 5477054
 . PMID 27677572. doi:10.1542/peds.2015-1553
. PMID 27677572. doi:10.1542/peds.2015-1553
- ↑ a b c d Malbin, D. (2002). Fetal Alcohol Spectrum Disorders: Trying Differently Rather Than Harder. Portland, Oregon: FASCETS, Inc. ISBN 0-9729532-0-5.
- ↑ Del Campo M, Jones KL (janeiro 2017). «A review of the physical features of the fetal alcohol spectrum disorders». European Journal of Medical Genetics. 60 (1): 55–64. PMID 27729236. doi:10.1016/j.ejmg.2016.10.004
- ↑ Cook JL, Green CR, Lilley CM, Anderson SM, Baldwin ME, Chudley AE, et al. (fevereiro de 2016). «Fetal alcohol spectrum disorder: a guideline for diagnosis across the lifespan». Canadian Medical Association Journal. 188 (3): 191–197. PMC 4754181
 . PMID 26668194. doi:10.1503/cmaj.141593
. PMID 26668194. doi:10.1503/cmaj.141593
- ↑ Jones KL, Smith DW (agosto 1975). «The fetal alcohol syndrome». Teratology. 12 (1): 1–10. PMID 1162620. doi:10.1002/tera.1420120102
- ↑ Renwick JH, Asker RL (julho 1983). «Ethanol-sensitive times for the human conceptus». Early Human Development. 8 (2): 99–111. PMID 6884260. doi:10.1016/0378-3782(83)90065-8
- ↑ Astley SJ, Clarren SK (julho 1996). «A case definition and photographic screening tool for the facial phenotype of fetal alcohol syndrome». The Journal of Pediatrics. 129 (1): 33–41. PMID 8757560. doi:10.1016/s0022-3476(96)70187-7
- ↑ Astley SJ, Stachowiak J, Clarren SK, Clausen C (novembro 2002). «Application of the fetal alcohol syndrome facial photographic screening tool in a foster care population». The Journal of Pediatrics. 141 (5): 712–717. PMID 12410204. doi:10.1067/mpd.2002.129030
- ↑ Lip-philtrum guides Arquivado em 2007-02-08 no Wayback Machine. FAS Diagnostic and Prevention Network, University of Washington. Consultado em 10 de abril de 2007.
- ↑ Astley, Susan. Backside of Lip-Philtrum Guides (2004) (PDF) Arquivado em 2007-06-19 no Wayback Machine. University of Washington, Fetal Alcohol Syndrome Diagnostic and Prevention Network. Consultado em 11 de abril de 2007
- ↑ West, J.R. (Ed.) (1986). Alcohol and Brain Development. New York: Oxford University Press.
- ↑ Clarren SK, Alvord EC, Sumi SM, Streissguth AP, Smith DW (janeiro 1978). «Brain malformations related to prenatal exposure to ethanol». The Journal of Pediatrics. 92 (1): 64–67. PMID 619080. doi:10.1016/S0022-3476(78)80072-9
- ↑ Coles CD, Brown RT, Smith IE, Platzman KA, Erickson S, Falek A (1991). «Effects of prenatal alcohol exposure at school age. I. Physical and cognitive development». Neurotoxicology and Teratology. 13 (4): 357–367. Bibcode:1991NTxT...13..357C. PMID 1921915. doi:10.1016/0892-0362(91)90084-A
- ↑ a b Jones KL, Smith DW (novembro 1973). «Recognition of the fetal alcohol syndrome in early infancy». Lancet. 302 (7836): 999–1001. PMID 4127281. doi:10.1016/s0140-6736(73)91092-1
- ↑ a b c Mattson, S.N., & Riley, E.P. (2002). "Neurobehavioral and Neuroanatomical Effects of Heavy Prenatal Exposure to Alcohol," in Streissguth and Kantor. (2002). p. 10.
- ↑ Jarmasz JS, Basalah DA, Chudley AE, Del Bigio MR. Human Brain Abnormalities Associated With Prenatal Alcohol Exposure and Fetal Alcohol Spectrum Disorder. J Neuropathol Exp Neurol. 2017 Sep 1;76(9):813-833. doi: 10.1093/jnen/nlx064. PMID: 28859338; PMCID: PMC5901082.
- ↑ «fadpmn.org, Nisan 2022». fadpmn.org. Arquivado do original em 23 de fevereiro de 2007
- ↑ a b Bager H, Christensen LP, Husby S, Bjerregaard L (fevereiro de 2017). «Biomarkers for the Detection of Prenatal Alcohol Exposure: A Review». Alcoholism: Clinical and Experimental Research. 41 (2): 251–261. PMID 28098942. doi:10.1111/acer.13309
- ↑ U.S. Department of Health and Human Services. (2000). National Institute on Alcohol Abuse and Alcoholism. Tenth special report to the U.S Congress on alcohol and health: Highlights from current research. Washington, DC: The Institute.
- ↑ McQuire C, Paranjothy S, Hurt L, Mann M, Farewell D, Kemp A (setembro 2016). «Objective Measures of Prenatal Alcohol Exposure: A Systematic Review» (PDF). Pediatrics. 138 (3): e20160517. PMID 27577579. doi:10.1542/peds.2016-0517
- ↑ a b Dejong K, Olyaei A, Lo JO (março 2019). «Alcohol Use in Pregnancy». Clinical Obstetrics and Gynecology. 62 (1): 142–155. PMC 7061927
 . PMID 30575614. doi:10.1097/GRF.0000000000000414
. PMID 30575614. doi:10.1097/GRF.0000000000000414
- ↑ «Overlapping Behavioral Characteristics of FASD's & Related Mental Health Diagnosis». www.fasdfamilies.com. Cathy Bruer-Thompson. Consultado em 28 de julho de 2019
- ↑ Lippert T, Gelineau L, Napoli E, Borlongan CV (janeiro 2018). «Harnessing neural stem cells for treating psychiatric symptoms associated with fetal alcohol spectrum disorder and epilepsy». Progress in Neuro-Psychopharmacology & Biological Psychiatry. 80 (Pt A): 10–22. PMID 28365374. doi:10.1016/j.pnpbp.2017.03.021
- ↑ a b Buxton, B. (2005). Damaged Angels: An Adoptive Mother Discovers the Tragic Toll of Alcohol in Pregnancy. New York: Carroll & Graf. ISBN 0-7867-1550-2.
- ↑ a b c d McCreight, B. (1997). Recognizing and Managing Children with Fetal Alcohol Syndrome/Fetal Alcohol Effects: A Guidebook. Washington, DC: CWLA. ISBN 0-87868-607-X.
- ↑ a b National Organization on Fetal Alcohol Syndrome, Arquivado em 2007-04-05 no Wayback Machine Minnesota Organization on Fetal Alcohol Syndrome. Arquivado em 2007-04-05 no Wayback Machine Retrieved on 2007-04-11
- ↑ a b c d e Streissguth, A.P., Barr, H.M., Kogan, J., & Bookstein, F.L. (1996). Understanding the occurrence of secondary disabilities in clients with fetal alcohol syndrome (FAS) and fetal alcohol effects (FAE): Final report to the Centers for Disease Control and Prevention on Grant No. RO4/CCR008515 (Tech. Report No. 96-06). Seattle: University of Washington, Fetal Alcohol and Drug Unit.
- ↑ a b Malbin, D. (1993). Fetal Alcohol Syndrome, Fetal Alcohol Effects: Strategies for Professionals. Center City, MN: Hazelden. ISBN 0-89486-951-5
- ↑ Abel EL, Jacobson S, Sherwin BT (1983). «In utero alcohol exposure: functional and structural brain damage». Neurobehavioral Toxicology and Teratology. 5 (3): 363–366. PMID 6877477
- ↑ Meyer LS, Kotch LE, Riley EP (1990). «Neonatal ethanol exposure: functional alterations associated with cerebellar growth retardation». Neurotoxicology and Teratology. 12 (1): 15–22. Bibcode:1990NTxT...12...15M. PMID 2314357. doi:10.1016/0892-0362(90)90107-N
- ↑ Zimmerberg B, Mickus LA (dezembro 1990). «Sex differences in corpus callosum: influence of prenatal alcohol exposure and maternal undernutrition». Brain Research. 537 (1–2): 115–122. PMID 2085766. doi:10.1016/0006-8993(90)90347-e
- ↑ Larkby, C.; Day, N. (1997). «The effects of prenatal alcohol exposure». Alcohol Health and Research World. 21 (3): 192–198. ISSN 0090-838X. PMC 6826810
 . PMID 15706768
. PMID 15706768
- ↑ a b Elliott EJ, Payne J, Haan E, Bower C (novembro 2006). «Diagnosis of foetal alcohol syndrome and alcohol use in pregnancy: a survey of paediatricians' knowledge, attitudes and practice». Journal of Paediatrics and Child Health. 42 (11): 698–703. PMID 17044897. doi:10.1111/j.1440-1754.2006.00954.x
- ↑ a b c d Burns L, Breen C, Bower C, O' Leary C, Elliott EJ (setembro 2013). «Counting fetal alcohol spectrum disorder in Australia: the evidence and the challenges». Drug and Alcohol Review. 32 (5): 461–467. PMID 23617437. doi:10.1111/dar.12047
- ↑ Mutch RC, Watkins R, Bower C (abril 2015). «Fetal alcohol spectrum disorders: notifications to the Western Australian Register of Developmental Anomalies». Journal of Paediatrics and Child Health. 51 (4): 433–436. PMID 25412883. doi:10.1111/jpc.12746

- ↑ Thanh, Nguyen Xuan; Jonsson, Egon (2015). «Costs of Fetal Alcohol Spectrum Disorder in the Canadian Criminal Justice System». Journal of Population Therapeutics and Clinical Pharmacology. 22 (1): e125-31. PMID 26072470. Consultado em 14 de novembro de 2022
- ↑ a b Riley EP, Infante MA, Warren KR (junho de 2011). «Fetal alcohol spectrum disorders: an overview». Neuropsychology Review. 21 (2): 73–80. PMC 3779274
 . PMID 21499711. doi:10.1007/s11065-011-9166-x
. PMID 21499711. doi:10.1007/s11065-011-9166-x
- ↑ Denny, Clark H.; Acero, Cristian S.; Naimi, Timothy S.; Kim, Shin Y. (26 de abril de 2019). «Consumption of Alcohol Beverages and Binge Drinking Among Pregnant Women Aged 18-44 Years - United States, 2015-2017». MMWR. Morbidity and Mortality Weekly Report. 68 (16): 365–368. ISSN 1545-861X. PMC 6483284
 . PMID 31022164. doi:10.15585/mmwr.mm6816a1
. PMID 31022164. doi:10.15585/mmwr.mm6816a1
- ↑ Centers for Disease Control and Prevention (CDC) (20 de julho de 2012). «Alcohol use and binge drinking among women of childbearing age--United States, 2006-2010». MMWR. Morbidity and Mortality Weekly Report. 61 (28): 534–538. ISSN 1545-861X. PMID 22810267
- ↑ Tan, Cheryl H.; Denny, Clark H.; Cheal, Nancy E.; Sniezek, Joseph E.; Kanny, Dafna (25 de setembro de 2015). «Alcohol use and binge drinking among women of childbearing age - United States, 2011-2013». MMWR. Morbidity and Mortality Weekly Report. 64 (37): 1042–1046. ISSN 1545-861X. PMID 26401713. doi:10.15585/mmwr.mm6437a3

- ↑ Centers for Disease Control and Prevention (CDC) (20 de julho de 2012). «Alcohol use and binge drinking among women of childbearing age--United States, 2006-2010». MMWR. Morbidity and Mortality Weekly Report. 61 (28): 534–538. ISSN 1545-861X. PMID 22810267
- ↑ «More than 3 million US women at risk for alcohol-exposed pregnancy | CDC Online Newsroom | CDC». www.cdc.gov. 2 de fevereiro de 2016. Consultado em 20 de novembro de 2016. Cópia arquivada em 21 de novembro de 2016
- ↑ a b c «Data & Statistics Prevalence of FASDs». Center for Disease Control and Prevention. 16 de abril de 2015. Consultado em 10 de junho de 2015. Cópia arquivada em 29 de junho de 2015
- ↑ «Fetal Alcohol Syndrome --- Alaska, Arizona, Colorado, and New York, 1995--1997». www.cdc.gov. Consultado em 13 de setembro de 2021
- ↑ «Fetal Alcohol Syndrome Among Children Aged 7–9 Years — Arizona, Colorado, and New York, 2010». www.cdc.gov. Consultado em 13 de setembro de 2021
- ↑ Oba PS (2007). «History of FASD». FAS Aware UK. Consultado em 20 de novembro de 2016. Arquivado do original em 4 de janeiro de 2017
- ↑ a b c d e Sanders, JL (2009). «Were our forebears aware of prenatal alcohol exposure and its effects? A review of the history of fetal alcohol spectrum disorder.». The Canadian Journal of Clinical Pharmacology. 16 (2): e288-95. PMID 19439773
- ↑ Jackson R (24 de abril de 1828). Valpy AJ, ed. «Considerations on the Increase of Crime, and the Degree of its Extent». Londres: John Hatchard and Son ... and T. and G. Underwood ... The Pamphleteer. 29 (57): 325. OCLC 1761801.
[Alcohol consumption is] too often the cause of weak, feeble, and distempered children, who must be, instead of an advantage and strength, a charge to their country
. Biografia do autor Randle Jackson - ↑ a b c d Price, Alan D. (2021). «Overview of FASD: How Our Understanding of FASD Has Progressed». Prevention, Recognition and Management of Fetal Alcohol Spectrum Disorders. [S.l.: s.n.] pp. 9–22. ISBN 978-3-030-73965-2. doi:10.1007/978-3-030-73966-9_2
- ↑ Jonathan Townley Crane, Arts of Intoxication: The Aim and the Results (Nova Iorque: Carlton & Lanahan, 1870), 173–175
- ↑ Jennifer L. Tait, The Poisoned Chalice (Tuscaloosa, Alabama: University of Alabama Press, 2010), 27,28.
- ↑ Sullivan WC (1899). «A note on the influence of maternal inebriety on the offspring». Journal of Mental Science. 45 (190): 489–503. doi:10.1192/bjp.45.190.489
- ↑ Goddard, H. H. (1912). The Kallikak Family: A Study in the Heredity of Feeble-Mindedness. Nova Iorque: Macmillan.
- ↑ Karp RJ, Qazi QH, Moller KA, Angelo WA, Davis JM (janeiro 1995). «Fetal alcohol syndrome at the turn of the 20th century: An unexpected explanation of the Kallikak family». Archives of Pediatrics & Adolescent Medicine. 149 (1): 45–48. PMID 7827659. doi:10.1001/archpedi.1995.02170130047010
- ↑ Haggard, H. W., & Jellinek, E. M. (1942). Alcohol Explored. Nova Iorque: Doubleday.
- ↑ a b c Armstrong, E. M. (2003). Conceiving risk, bearing responsibility: Fetal alcohol syndrome & the diagnosis of moral disorder. Baltimore: The Johns Hopkins University Press.
- ↑ Saxon W (4 de março de 1995). «Dr. Fritz Fuchs, 76, Who Advanced Obstetrics». The New York Times. Consultado em 16 de fevereiro de 2017. Cópia arquivada em 27 de junho de 2017
- ↑ King, T. L., & Brucker, M. C. (2011). Pharmacology for women's health. Sudbury, MA: Jones and Bartlett.
- ↑ Haas, David M; Morgan, Amanda M; Deans, Samantha J; Schubert, Frank P (5 de novembro de 2015). «Ethanol for preventing preterm birth in threatened preterm labor». Cochrane Database of Systematic Reviews. 2015 (11): CD011445. PMC 8944412
 . PMID 26544539. doi:10.1002/14651858.CD011445.pub2
. PMID 26544539. doi:10.1002/14651858.CD011445.pub2
- ↑ Lemoine, Paul (agosto de 1994). «The letter from Professor Lemoine»
 . Addiction (em inglês). 89 (8): 1021–1023. ISSN 0965-2140. doi:10.1111/j.1360-0443.1994.tb03364.x
. Addiction (em inglês). 89 (8): 1021–1023. ISSN 0965-2140. doi:10.1111/j.1360-0443.1994.tb03364.x
- ↑ Lemoine P.; Harousseau H.; Borteyru J.B.; Menuet J.C. (1968). «Les enfants de parents alcooliques. Anomalies observées, à propos de 127 cas». Quest Medical. 21: 476–482 Reprinted in Lemoine P, Harousseau H, Borteyru JP, Menuet JC (abril 2003). «Children of alcoholic parents--observed anomalies: discussion of 127 cases». Therapeutic Drug Monitoring. 25 (2): 132–136. PMID 12657907. doi:10.1097/00007691-200304000-00002
- ↑ Ulleland CN (maio 1972). «The offspring of alcoholic mothers». Annals of the New York Academy of Sciences. 197 (1): 167–169. Bibcode:1972NYASA.197..167U. PMID 4504588. doi:10.1111/j.1749-6632.1972.tb28142.x
- ↑ a b Jones KL, Smith DW, Ulleland CN, Streissguth P (junho de 1973). «Pattern of malformation in offspring of chronic alcoholic mothers». Lancet. 1 (7815): 1267–1271. PMID 4126070. doi:10.1016/S0140-6736(73)91291-9
- ↑ Streissguth, A.P. (2002). In A. Streissguth, & J. Kanter (Eds.), The Challenge in Fetal Alcohol Syndrome: Overcoming Secondary Disabilities. Seattle: University of WA Press. ISBN 0-295-97650-0.
- ↑ a b c d Clarren, S.K. (2005). A thirty year journey from tragedy to hope. Foreword to Buxton, B. (2005). Damaged Angels: An Adoptive Mother Discovers the Tragic Toll of Alcohol in Pregnancy. New York: Carroll & Graf. ISBN 0-7867-1550-2.
- ↑ Olegård R, Sabel KG, Aronsson M, Sandin B, Johansson PR, Carlsson C, et al. (1979). «Effects on the child of alcohol abuse during pregnancy. Retrospective and prospective studies». Acta Paediatrica Scandinavica. Supplement. 275: 112–121. PMID 291283. doi:10.1111/j.1651-2227.1979.tb06170.x
- ↑ a b c Clarren SK, Smith DW (maio 1978). «The fetal alcohol syndrome». The New England Journal of Medicine. 298 (19): 1063–1067. PMID 347295. doi:10.1056/NEJM197805112981906
- ↑ Smith DW (1981). «Fetal alcohol syndrome and fetal alcohol effects». Neurobehavioral Toxicology and Teratology. 3 (2). 127 páginas. PMID 7254460
- ↑ Aase JM, Jones KL, Clarren SK (março 1995). «Do we need the term "FAE"?». Pediatrics. 95 (3): 428–430. PMID 7862486
- ↑ Sokol RJ, Clarren SK (agosto 1989). «Guidelines for use of terminology describing the impact of prenatal alcohol on the offspring». Alcoholism: Clinical and Experimental Research. 13 (4): 597–598. PMID 2679217. doi:10.1111/j.1530-0277.1989.tb00384.x
- ↑ Angelotta, C; Appelbaum, PS (junho de 2017). «Criminal Charges for Child Harm from Substance Use in Pregnancy.». The Journal of the American Academy of Psychiatry and the Law. 45 (2): 193–203. PMID 28619859
- ↑ Hackler, C (novembro de 2011). «Ethical, legal and policy issues in management of fetal alcohol spectrum disorder.». The Journal of the Arkansas Medical Society. 108 (6): 123–4. PMC 4049518
 . PMID 23252025
. PMID 23252025
- ↑ Armstrong, Elizabeth M.; Abel, Ernest L. (2000). «Fetal alcohol syndrome: the origins of a moral panic». Alcohol and Alcoholism (em inglês). 35 (3): 276–282. ISSN 0735-0414. PMID 10869248. doi:10.1093/alcalc/35.3.276

- ↑ Armstrong, EM (2017). «Making Sense of Advice About Drinking During Pregnancy: Does Evidence Even Matter?». The Journal of Perinatal Education. 26 (2): 65–69. PMC 6353268
 . PMID 30723369. doi:10.1891/1058-1243.26.2.65
. PMID 30723369. doi:10.1891/1058-1243.26.2.65
- ↑ «'No alcohol in pregnancy' advised». 25 de maio de 2007
- ↑ Humphrey, Tom (20 de março de 2016). «Legislators clash with doctors, judges over renewing fetal assault law». Knoxville News Sentinel (em inglês)
- ↑ Bassett, Laura (30 de abril de 2014). «State Enacts Law To Incarcerate Pregnant Women Who Use Drugs». HuffPost (em inglês)
- ↑ Darlington, Caroline K.; Compton, Peggy A.; Hutson, Sadie P. (maio de 2021). «Revisiting the Fetal Assault Law in Tennessee: Implications and the Way Forward». Policy, Politics, & Nursing Practice. 22 (2): 93–104. PMID 33567969. doi:10.1177/1527154421989994
- ↑ Picciuto, Elizabeth (9 de dezembro de 2014). «Court Says Fetal Alcohol Syndrome Isn't a Crime». The Daily Beast (em inglês)
- ↑ «Medical and Public Health Groups Oppose Punishment of Pregnant People». Pregnancy Justice. 2023. Consultado em 15 de março de 2024
- ↑ «Civil Commitment: About This Policy». Alcohol Policy Information System (em inglês). NIAAA. Consultado em 15 de março de 2024
- ↑ «CDC faces backlash over alcohol warning to women» (em inglês). Consultado em 6 de abril de 2018
- ↑ «More than 3 million US women at risk for alcohol-exposed pregnancy». Centers for Disease Control and Prevention (em inglês). 2 de fevereiro de 2016
- ↑ «Alcohol and Pregnancy | VitalSigns | CDC». www.cdc.gov (em inglês). 20 de março de 2017. Consultado em 6 de abril de 2018. Cópia arquivada em 26 de setembro de 2016
- ↑ «The CDC's Alcohol and Pregnancy Warning Shames Women». Time. 5 de fevereiro de 2016. Consultado em 6 de abril de 2018
- ↑ Khazan, Olga; Beck, Julie (3 de fevereiro de 2016). «CDC to Women: Don't Drink Unless You're On Birth Control». The Atlantic (em inglês). Consultado em 15 de março de 2024
- ↑ Schumaker, Erin (4 de fevereiro de 2016). «No, The Government Did Not Just Tell Women To Stop Drinking». HuffPost (em inglês). Consultado em 15 de março de 2024
- ↑ Brown JM, Bland R, Jonsson E, Greenshaw AJ (março 2019). «A Brief History of Awareness of the Link Between Alcohol and Fetal Alcohol Spectrum Disorder». Canadian Journal of Psychiatry. 64 (3): 164–168. PMC 6405809
 . PMID 29807454. doi:10.1177/0706743718777403
. PMID 29807454. doi:10.1177/0706743718777403
Bibliografia
- Coriale, G.; Fiorentino, D.; Di Lauro, F.; Marchitelli, R.; Scalese, B.; Fiore, M.; Maviglia, M.; Ceccanti, M (setembro–outubro de 2013). «Fetal Alcohol Spectrum Disorder (FASD): neurobehavioral profile, indications for diagnosis and treatment» (PDF). Rivista di Psichiatria (em inglês). 48 (5): 359-369. ISSN 2038-2502. Consultado em 28 de agosto de 2016
- Lamônica, D.A.C.; Gejão, M.G.; Aguiar, S.N.R.; Silva, G.K.; Lopes, A.C.; Richieri-Costa, A (setembro–outubro de 2010). «Desordens do espectro alcoólico fetal e habilidades de comunicação: relato de caso familiar» (PDF). Revista da Sociedade Brasileira de Fonoaudiologia. 15 (1): 129-133. ISSN 1982-0232. Consultado em 28 de agosto de 2016
- McHugh, R.K.; Wigderson, S.; Greenfield, S.F (junho de 2014). «Epidemiology of Substance Use in Reproductive-Age Women». Obstetrics and Gynecology Clinics of North America (em inglês). 41 (2): 177-189. ISSN 0889-8545. Consultado em 28 de agosto de 2016
- Momino, W.; Sanseverino, M.T.V.; Schüler-Faccini, L (agosto de 2008). «A exposição pré–natal ao álcool como fator de risco para comportamentos disfuncionais: o papel do pediatra» (PDF). Jornal de Pediatria. 84 (4): S76-S79. ISSN 1678-4782. Consultado em 28 de agosto de 2016
- Riley, E.P.; Infante, M.A.; Warren, K.R (abril de 2011). «Fetal Alcohol Spectrum Disorders: An Overview». Neuropsychology Review (em inglês). 21 (2): 73-80. ISSN 1573-6660. Consultado em 28 de agosto de 2016
- Roszel, E.L. (abril de 2015). «Central nervous system deficits in fetal alcohol spectrum disorder». The Nurse Practitioner (em inglês). 40 (4): 24-33. ISSN 0361-1817. Consultado em 28 de agosto de 2016
- Uban, K.A.; Bodnar, T.; Butts, K.; Sliwowska, J.H.; Comeau, W.; Weinberg, J. (2014). «Capítulo 5: Direct and indirect mechanisms of alcohol teratogenesis: implications for understanding alterations in brain and behavior in FASD». In: Riley, E.P.; Clarren, S.; Weinberg, J.; Jonsson, E. Fetal Alcohol Spectrum Disorder: Management and Policy Perspectives of FASD (em inglês) 1ª ed. Weinheim: Wiley-Blackwell. pp. 73–75. ISBN 978-3-527-32839-0. Consultado em 28 de agosto de 2016