Adenocarcinoma de glândula salivar
Os adenocarcinomas de glândula salivar são um grupo de neoplasias malignas (cânceres) que afetam as glândulas salivares.[1]
Classificação
Podem ser classificados em:[1]
- Adenocarcinoma de células basais
- Adenocarcinoma microcístico esclerosante
- Adenocarcinoma microsecretório
- Adenocarcinoma mucinoso
- Adenocarcinoma polimórfico
- Adenocarcinoma sebáceo
- Carcinoma adenoide cístico
- Carcinoma de células acinares
- Carcinoma de células claras hialinizante
- Carcinoma do ducto salivar
- Carcinoma epitelial-mioepitelial
- Carcinoma ex-adenoma pleomórfico
- Carcinoma intraductal
Adenocarcinoma de células basais
O adenocarcinoma de células basais é uma neoplasia bifásica de baixo grau que afeta principalmente a parótida, sendo raro nas outras glândulas salivares maiores e menores: ele é raro, representando entre 1 e 2% dos tumores malignos de glândula salivar, afetando adultos a partir dos 40 anos e com ligeira predileção por mulheres (1,2:1).[2] Ele surge a partir de células ductais e mioepiteliais, e a maior parte dos casos é de novo, embora 25% surjam a partir de um adenoma de células basais; pode estar relacionado à síndrome de Brooke-Spiegler.[2][3][4]
Clinicamente, apresenta-se como uma massa de crescimento lento e assintomático por muitos anos, e é raramente associado a cilindromas dermais.[2] Não possui características radiográficas marcantes, e histologicamente é semelhante ao adenoma de células basais, mas com evidências de um padrão de crescimento invasivo, apresentando um parênquima tumoral de células ductais ao centro e organização em paliçada, com possível diferenciação escamosa ou sebácea e áreas de necrose.[2]
O tratamento inclui a ressecção cirúrgica com margens livres, mas possui risco de recidiva local de 50%, e risco de metástase local para linfonodos de 15%.[2] A radioterapia adjuvante pode ser utilizada.[2][5]
Adenocarcinoma microcístico esclerosante
O adenocarcinoma microcístico esclerosante (AME) é uma neoplasia maligna extremamente rara, afetando principalmente pacientes acima dos 50 anos, com predileção por mulheres (4:1).[6] Afeta principalmente as glândulas salivares menores, e está relacionado à imunossupressão.[7][8]
Clinicamente se apresenta como uma massa de crescimento lento e assintomática a princípio, mas seu perfil de crescimento infiltrativo e comportamento localmente agressivo, com invasão perineural, frequentemente levam à parestesia.[6] Em uma tomografia por emissão de pósitrons (PET) com FDG, pode se mostrar como uma lesão infiltrativa amorfa que é fortemente corada por FDG.[6] Histologicamente, o AME se assemelha ao carcinoma adnexo cutâneo microcístico, sendo composto por ductos, túbulos e ilhotas de células mioepiteliais e células cuboides em um estroma tumoral densamente esclerótico.[6]
Apesar do seu aspecto agressivo, o prognóstico do AME não é desfavorável, com recidiva ou metástases sendo raras.[6][9] O tratamento consiste na ressecção cirúrgica com margens amplas, e para os casos onde há margens positivas ou invasão perineural recomenda-se a radioterapia adjuvante.[6][10][11]
Adenocarcinoma microsecretório
O adenocarcinoma microsecretório é uma neoplasia de glândula salivar recentemente descrita, com ligeira predileção feminina e que afeta principalmente as glândulas salivares menores.[12] Ela é caracterizada pela fusão dos genes MEF2C e SS18.[12]
Clinicamente é uma massa intraoral pequena e indolor, tendo um comportamento indolente, com bordas bem delimitadas e comportamento minimamente invasivo.[12][13] Histologicamente é caracterizada por microcistos de células atenuadas, de citoplasma eosinofílico e núcleo arredondado, com produção de secreção intraluminal basofílica.[12][14]
Por ser uma nova entidade, pouco se sabe sobre seu tratamento, mas a cirurgia parece ser efetiva na cura.[12]
Adenocarcinoma mucinoso
O adenocarcinoma mucinoso é uma nova entidade na classificação de lesões de glândula salivar da OMS, sendo extremamente raro e representando menos de 0,1% das neoplasias de glândulas salivares.[15] Clinicamente é caracterizado como uma massa exofítica, que afeta principalmente o palato e a região sublingual.[15] O adenocarcinoma mucinoso é caracterizado histologicamente por possuir ilhotas de células epiteliais em um mar de mucina.[15] Possui alta taxa de recidiva e metástase, e baixa sobrevida global.[15]
Adenocarcinoma polimórfico
O adenocarcinoma polimórfico é uma neoplasia maligna indolente, que afeta principalmente as glândulas salivares menores no palato (60% dos casos), sendo o segundo carcinoma mais comum de palato.[16] Afeta mais pacientes entre 50 e 60 anos, com predileção por mulheres (2:1).[16] É caracterizado por mutações do gene PRKD, especialmente a mutação PRKD1 E710D.[16]
Clinicamente apresenta-se como uma massa tumoral, e não possui achados radiológicos específicos.[16] Histologicamente, possui citologia uniforme (células de núcleo pálido, semelhantes ao carcinoma papilar de tireoide) e diversidade arquitetural.[16] Possui excelente prognóstico, com alta sobrevida (94 a 99% em 10 anos) e sobrevida livre de recidiva (83 a 88% em 10 anos), mas a presença de arquitetura papilar ou cribiforme podem apresentar um prognóstico menos favorável, com risco de metástase linfonodal.[16]
Adenocarcinoma sebáceo
O adenocarcinoma sebáceo é uma neoplasia maligna extremamente rara quando ocorre em glândulas salivares, com menos de 50 casos relatados no mundo.[17] É caracterizado pela presença de ilhotas epiteliais de células poliédricas com citoplasma claro e presença de secreção sebácea intracelular, e ao redor delas, células basaloides.[17] Possui um prognóstico bastante desfavorável, sendo um tumor com alta taxa de recidiva e metástase.[17]
Carcinoma adenoide cístico
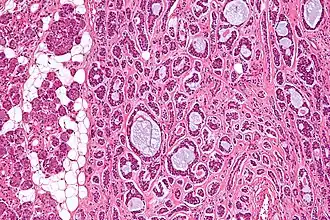
O carcinoma adenoide cístico (CAC) é um tipo de adenocarcinoma que afeta glândulas salivares maiores (especialmente a parótida) e menores, com incidência semelhante entre homens e mulheres e maior incidência na faixa dos 50 anos; é o mais comum da glândula submandibular (28%) e o terceiro tumor maligno mais comum de glândulas salivares.[18] Entre 60 a 90% dos CAC possuem a mutação de MYB-NFIB ou a fusão de MYBL1-NFIB.[18]
Histologicamente, o CAC é caracterizado pelo parênquima bifásico de células ductais e mioepiteilais, com arquitetura tubular, cribiforme ou sólida, frequentemente com invasão perineural.[18] A arquitetura sólida é um fator de risco para mau prognóstico.[18] De forma geral, o CAC possui um prognóstico desfavorável: a sobrevida em 5 anos varia entre 55 e 89%, caindo para 20 a 40% em 10 anos, e ele possui alta taxa de recidiva local (16 a 67%) e de metástase (8 a 46%).[18]
Carcinoma de células acinares
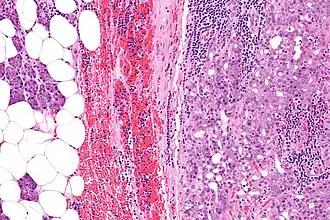
O carcinoma de células acinares é um tumor de glândulas salivares que afeta principalmente a parótida (91%), sendo o segundo tumor maligno de glândulas salivares mais comum em crianças (atrás do carcinoma mucoepidermoide) e o terceiro mais comum em adultos (atrás do carcinoma mucoepidermoide e CAC)[19]. Afeta mais mulheres do que homens (1,6:1) e mais comum nas pessoas brancas.[19] Está ligado a predisposição familiar e exposição à radiação.[19][20][21]
Clinicamente, tende a se apresentar como uma massa de crescimento lento, podendo causar dor e disfunção do nervo facial.[19][22] Achados radiológicos podem não ser específicos, com uma lesão sólida ou cística em TC, e aspecto lobular bem delimitado e hipoecoico, heterogêneo e pouco vascularizado na ultrassonografia.[19] Histologicamente, é caracterizado pela diferenciação de células acinares serosas de núcleo excêntrico, com arquitetura tecidual sólida, microcística, cística papilar ou folicular.[19]
De forma geral, o prognóstico é bem favorável, com sobrevida em 5 anos de 97%.[19] O tratamento de escolha é a cirurgia de ressecção, e em casos de margens positivas ou fatores de risco para metástase, pode-se utilizar radioterapia ou quimioterapia.[19][23]
Carcinoma de células claras hialinizante
O carcinoma de células claras hialinizante é uma neoplasia maligna rara que afeta majoritariamente as glândulas salivares menores (>80%), com ligeira predominância feminina e por pacientes idosos.[24][25] É caracterizada pela presença da fusão do oncogene EWSR1 com outro gene, frequentemente o ATF1.[24]
Clinicamente tende a se apresentar como um edema na submucosa que pode estar ulcerado, mas a maior parte dos achados são incidentais.[24] Na ressonância magnética seus achados são inespecíficos, apresentando-se como uma lesão bem delimitada e isointensa em T1 e hiperintensa em T2.[24] Histologicamente, é caracterizado por possuir um estroma de tecido hipocelular hialinizado denso, com células claras em ilhotas, cordões e trabéculas, justaposto a um estroma desmoplásico. Teoriza-se que seja um tipo especial de carcinoma adenoescamoso pela presença ocasional de glândulas e mucina.[24][26]
É um carcinoma de baixo grau, com baixo risco de metástase ou recidiva, mas a presença de necrose, margens positivas após ressecção ou disseminação linfonodal estão associadas à recidiva.[24][27][28][29]
Carcinoma do ducto salivar
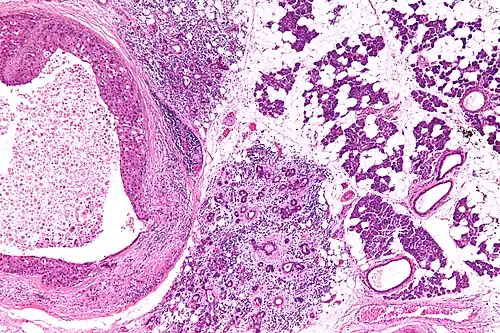
O carcinoma do ducto salivar é uma neoplasia maligna agressiva de alto grau, que representa ~10% dos cânceres de glândula salivar, afetando mais idosos e homens (2,4:1).[30] Afeta frequentemente a parótida e está associado a diversas mutações de oncogenes conhecidos, como TP53, HRAS, PIK3CA, PTEN e BRAF.[30][31] Cerca de 60% surgem de novo, mas 40% são originários de um adenoma pleomórfico.[30][32]
Clinicamente, apresenta-se como uma massa de rápido crescimento associada a dor, parestesia ou paralisia da face.[30][31] Na TC, pode se apresentar como uma massa heterogênea com focos de calcificação, e na ressonância magnética se observa o caráter invasivo de aspecto hipointenso comparado ao tecido glandular normal em T1 e hiperintenso em T2.[30][33][34] Histologicamente, é caracterizado por ser semelhante ao carcinoma ductal de mama, com células oncocíticas em cordões e ilhotas em um estroma desmoplásico, com alto grau de pleomorfismo e necrose; pode ser rico em mucina, de aspecto micropapilar, sarcomatoide, rabdoide ou basaloide; normalmente é positivo para receptor andrógeno.[30][35]
O prognóstico é desfavorável, com sobrevida de ~35%, estando em média em 3,1 anos.[30] A ressecção radical com dissecção de linfonodos cervicais é o tratamento de escolha e a radioterapia adjuvante deve ser considerada.[30][36] Em alguns casos, para doença avançada, a quimioterapia com antiandrógenos, trastuzumabe, anti-BRAF e anti-PIK3CA pode ser indicada.[30]
Carcinoma epitelial-mioepitelial
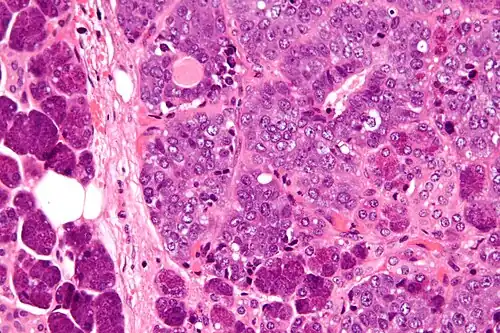
O carcinoma epitelial-mioepitelial é uma neoplasia maligna bifásica, que representa 1 a 2% dos tumores salivares malignos, mais comum em mulheres (1,6:1) e que afeta primariamente a parótida (70%) e a submandibular (12%).[37][38][39] Está associada a mutação de HRAS em 85% dos casos.[37][40] Pode surgir de novo ou de um adenoma pleomórfico.[37][39]
Clinicamente, caracteriza-se como uma massa indolor de crescimento lento, mas em casos raros pode ocasionar paralisia do nervo facial e linfadenopatia, indicando transformação em alto grau.[37][41] Histologicamente, observa-se a presença de células epiteliais e mioepiteliais em arquitetura tecidual tubular, glandular ou sólida, com a presença de áreas císticas e papilares, ou até de matriz hialinizada; quando há transformação de alto grau (20%), normalmente se dá no componente epitelial com proliferação de células atípicas em padrão sólido ou em lençol, e presença de necrose.[37] Algumas variantes mais raras como oncocítica ou apócrina podem ser encontradas.[37] Diferenciação escamosa ou sebácea, ou em corpos de Verocay é rara.[37][42]
Possui bom prognóstico, exceto se de alto grau, e o tratamento de escolha é a ressecção cirúrgica com radioterapia adjuvante.[37][41]
Carcinoma ex-adenoma pleomórfico
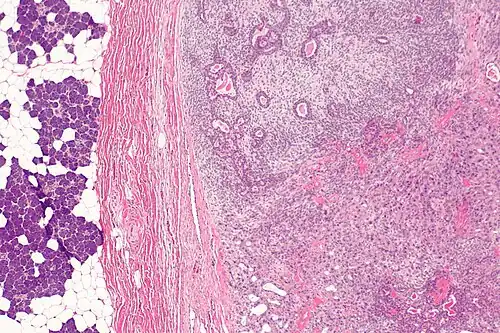
O carcinoma ex-adenoma pleomórfico é uma neoplasia que surge a partir de um adenoma pleomórfico que sofreu malignização, representando 11,6% das neoplasias malignas salivares.[43] É mais frequente na sétima década de vida, com ligeira predominância em homens, e afeta a parótida (77%) e a submandibular (18%) mais frequentemente.[43][44] Cerca de 5% dos adenomas pleomórficos sofrem malignização, com risco aumentado daqueles que são redicivantes ou de longa data: esse processo implica em mutações genéticas subsequentes, como de TP53, amplificação de HER2 e perda da expressão de PLAG1.[43][45][46]
Clinicamente se caracteriza como uma massa de longa data que passou por recente crescimento rápido, mas pode ocasionar dor, parestesia ou paralisia facial, assim como ulceração da pele e disfagia em casos avançados.[43][47] Na ressonância magnética, o componente benigno (encapsulado) tende a ter uma intensidade de sinal variável devido à natureza arquitetural do adenoma pleomórfico, enquanto o componente invasivo maligno apresenta baixa a média intensidade de sinal em T2 devido a hemorragia e necrose.[43][48] Histologicamente, apresenta-se como um adenoma pleomórfico (componente benigno) associado a um componente carcinomatoso que pode ser um carcinoma do ducto salivar, carcinoma mioepitelial (usualmente de baixo grau), adenocarcinoma (usualmente de alto grau) ou carcinoma epitelial-mioepitelial.[43]
O prognóstico depende da extensão da doença: a forma não invasiva ou minimamente invasiva possui bom prognóstico, enquanto doença altamente invasiva é mais desfavorável; componente carcinomatoso de carcinoma mioepitelial, tamanho, idade avançada, sexo masculino, invasão da cápsula e metástase são associados a pior prognóstico.[43][49] Disseminação linfonodal pode ocorrer em 30% dos casos, mas metástase é mais rara (4%).[43][50]
Carcinoma intraductal
O carcinoma intraductal é uma neoplasia maligna excepcionalmente rara de glândula salivar, tendo menos de 100 casos registrados.[51] Afeta mais mulheres do que homens (1,5:1), e especialmente a parótida (84,6%).[51] É usualmente caracterizada como uma massa assintomática, e seu aspecto histopatológico lembra um carcinoma ductal in situ de mama, sendo dividido em 3 variantes: do ducto intercalado (a mais comum), apócrina, e híbrida.[51] O tratamento consiste na cirurgia, mas devido a sua raridade, não há evidências de benefício na radioterapia.[51]
Ver também
Outros carcinomas de glândulas salivares incluem:[1]
- Carcinoma de células escamosas
- Carcinoma linfoepitelial
- Carcinoma mioepitelial
- Carcinoma mucoepidermoide
- Carcinoma secretório
- Sialoblastoma
- Carcinossarcoma
Referências
- ↑ a b c Żurek, Michał; Fus, Łukasz; Niemczyk, Kazimierz; Rzepakowska, Anna (1 de novembro de 2023). «Salivary gland pathologies: evolution in classification and association with unique genetic alterations». European Archives of Oto-Rhino-Laryngology (em inglês) (11): 4739–4750. ISSN 1434-4726. PMC 10562281
 . PMID 37439929. doi:10.1007/s00405-023-08110-w. Consultado em 9 de janeiro de 2025
. PMID 37439929. doi:10.1007/s00405-023-08110-w. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f Prosser, Natasha; Gupta, Ruta. «Basal cell adenocarcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Muller, S.; Barnes, L. (15 de dezembro de 1996). «Basal cell adenocarcinoma of the salivary glands. Report of seven cases and review of the literature». Cancer (12): 2471–2477. ISSN 0008-543X. PMID 8952553. Consultado em 9 de janeiro de 2025
- ↑ Robinson, Robert A. (março de 2021). «Basal Cell Adenoma and Basal Cell Adenocarcinoma». Surgical Pathology Clinics (1): 25–42. ISSN 1875-9157. PMID 33526221. doi:10.1016/j.path.2020.09.005. Consultado em 9 de janeiro de 2025
- ↑ Farrell, Tisha; Chang, Yilan L. (outubro de 2007). «Basal cell adenocarcinoma of minor salivary glands». Archives of Pathology & Laboratory Medicine (10): 1602–1604. ISSN 1543-2165. PMID 17922602. doi:10.5858/2007-131-1602-BCAOMS. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f Jassim, Treeva; Allison, Derek. «Sclerosing microcystic adenocarcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Rooper, Lisa M. (março de 2021). «Emerging Entities in Salivary Pathology: A Practical Review of Sclerosing Microcystic Adenocarcinoma, Microsecretory Adenocarcinoma, and Secretory Myoepithelial Carcinoma». Surgical Pathology Clinics (1): 137–150. ISSN 1875-9157. PMID 33526218. doi:10.1016/j.path.2020.10.003. Consultado em 9 de janeiro de 2025
- ↑ Tan, Gideon Ze Lin; Goh, Giap Hean; Loh, Kwok Seng; Petersson, Fredrik (outubro de 2021). «Sclerosing microcystic adenocarcinoma of the parotid gland - The first recorded case with histo-cytopathologic correlation and a brief review of the literature». Annals of Diagnostic Pathology. 151806 páginas. ISSN 1532-8198. PMID 34418769. doi:10.1016/j.anndiagpath.2021.151806. Consultado em 9 de janeiro de 2025
- ↑ Ide, Fumio; Kikuchi, Kentaro; Kusama, Kaoru (setembro de 2011). «Microcystic adnexal (sclerosing sweat duct) carcinoma of intraoral minor salivary gland origin: an extracutaneous adnexal neoplasm?». Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontics (3): 284–286. ISSN 1528-395X. PMID 21684772. doi:10.1016/j.tripleo.2011.02.050. Consultado em 9 de janeiro de 2025
- ↑ Zhang, Ranran; Cagaanan, Alain; Hafez, Gholam-Reza; Hu, Rong (junho de 2019). «Sclerosing Microcystic Adenocarcinoma: Report of a Rare Case and Review of Literature». Head and Neck Pathology (2): 215–219. ISSN 1936-0568. PMC 6513910
 . PMID 29987694. doi:10.1007/s12105-018-0945-z. Consultado em 9 de janeiro de 2025
. PMID 29987694. doi:10.1007/s12105-018-0945-z. Consultado em 9 de janeiro de 2025
- ↑ Wood, Andrew; Conn, Brendan I. (abril de 2018). «Sclerosing microcystic adenocarcinoma of the tongue: a report of 2 further cases and review of the literature». Oral Surgery, Oral Medicine, Oral Pathology and Oral Radiology (4): e94–e102. ISSN 2212-4411. PMID 29398516. doi:10.1016/j.oooo.2017.12.017. Consultado em 9 de janeiro de 2025
- ↑ a b c d e Mikula, Michael; Rooper, Lisa. «Microsecretory adenocarcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Bishop, Justin A.; Sajed, Dipti P.; Weinreb, Ilan; Dickson, Brendan C.; Bilodeau, Elizabeth A.; Agaimy, Abbas; Franchi, Alessandro; Khurram, Syed Ali; Da Forno, Philip (dezembro de 2021). «Microsecretory Adenocarcinoma of Salivary Glands: An Expanded Series of 24 Cases». Head and Neck Pathology (4): 1192–1201. ISSN 1936-0568. PMC 8633253
 . PMID 33982215. doi:10.1007/s12105-021-01331-7. Consultado em 9 de janeiro de 2025
. PMID 33982215. doi:10.1007/s12105-021-01331-7. Consultado em 9 de janeiro de 2025
- ↑ Rooper, Lisa M. (março de 2021). «Emerging Entities in Salivary Pathology: A Practical Review of Sclerosing Microcystic Adenocarcinoma, Microsecretory Adenocarcinoma, and Secretory Myoepithelial Carcinoma». Surgical Pathology Clinics (1): 137–150. ISSN 1875-9157. PMID 33526218. doi:10.1016/j.path.2020.10.003. Consultado em 9 de janeiro de 2025
- ↑ a b c d «:: Korean Academy Of Oral And Maxillofacial Pathology ::». journal.kaomp.org. doi:10.17779/kaomp.2019.43.5.006. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f Xu, Bin. «Polymorphous adenocarcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ a b c Soares, Ciro D; Morais, Thayná M L; Carlos, Roman; Jorge, Jacks; de Almeida, Oslei Paes; de Carvalho, Maria G F; Altemani, Albina M M (2018). «Sebaceous adenocarcinomas of the major salivary glands: a clinicopathological analysis of 10 cases». Histopathology (em inglês) (4): 585–592. ISSN 1365-2559. doi:10.1111/his.13664. Consultado em 9 de janeiro de 2025
- ↑ a b c d e Xu, Bin. «Adenoid cystic carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f g h Lahoutiharahdashti, Arash; Rao, Rema. «Acinic cell carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Sepúlveda, Ilson; Frelinghuysen, Michael; Platin, Enrique; Spencer, M. Loreto; Urra, Alexis; Ortega, Pablo (2015). «Acinic cell carcinoma of the parotid gland: a case report and review of the literature». Case Reports in Oncology (1): 1–8. ISSN 1662-6575. PMC 4327553
 . PMID 25759653. doi:10.1159/000371340. Consultado em 9 de janeiro de 2025
. PMID 25759653. doi:10.1159/000371340. Consultado em 9 de janeiro de 2025
- ↑ Al-Zaher, Nabil; Obeid, Amani; Al-Salam, Suhail; Al-Kayyali, Bassam Sulaiman (2009). «Acinic cell carcinoma of the salivary glands: a literature review». Hematology/Oncology and Stem Cell Therapy (1): 259–264. ISSN 1658-3876. PMID 20063555. doi:10.1016/s1658-3876(09)50035-0. Consultado em 9 de janeiro de 2025
- ↑ Lewis, J. E.; Olsen, K. D.; Weiland, L. H. (1 de janeiro de 1991). «Acinic cell carcinoma. Clinicopathologic review». Cancer (1): 172–179. ISSN 0008-543X. PMID 1985714. doi:10.1002/1097-0142(19910101)67:1<172::aid-cncr2820670129>3.0.co;2-x. Consultado em 9 de janeiro de 2025
- ↑ Bell, R. Bryan; Dierks, Eric J.; Homer, Louis; Potter, Bryce E. (julho de 2005). «Management and outcome of patients with malignant salivary gland tumors». Journal of Oral and Maxillofacial Surgery: Official Journal of the American Association of Oral and Maxillofacial Surgeons (7): 917–928. ISSN 0278-2391. PMID 16003616. doi:10.1016/j.joms.2005.03.006. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f Ely, Kim. «Clear cell carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Milchgrub, S.; Gnepp, D. R.; Vuitch, F.; Delgado, R.; Albores-Saavedra, J. (janeiro de 1994). «Hyalinizing clear cell carcinoma of salivary gland». The American Journal of Surgical Pathology (1): 74–82. ISSN 0147-5185. PMID 7506496. doi:10.1097/00000478-199401000-00007. Consultado em 9 de janeiro de 2025
- ↑ Tanguay, Jeff; Weinreb, Ilan (março de 2013). «What the EWSR1-ATF1 fusion has taught us about hyalinizing clear cell carcinoma». Head and Neck Pathology (1): 28–34. ISSN 1936-0568. PMC 3597151
 . PMID 23459838. doi:10.1007/s12105-013-0427-2. Consultado em 9 de janeiro de 2025
. PMID 23459838. doi:10.1007/s12105-013-0427-2. Consultado em 9 de janeiro de 2025
- ↑ Wang, Beverly; Brandwein, Margaret; Gordon, Ronald; Robinson, Robert; Urken, Mark; Zarbo, Richard J. (junho de 2002). «Primary salivary clear cell tumors--a diagnostic approach: a clinicopathologic and immunohistochemical study of 20 patients with clear cell carcinoma, clear cell myoepithelial carcinoma, and epithelial-myoepithelial carcinoma». Archives of Pathology & Laboratory Medicine (6): 676–685. ISSN 0003-9985. PMID 12033955. doi:10.5858/2002-126-0676-PSCCTA. Consultado em 9 de janeiro de 2025
- ↑ Milchgrub, S.; Gnepp, D. R.; Vuitch, F.; Delgado, R.; Albores-Saavedra, J. (janeiro de 1994). «Hyalinizing clear cell carcinoma of salivary gland». The American Journal of Surgical Pathology (1): 74–82. ISSN 0147-5185. PMID 7506496. doi:10.1097/00000478-199401000-00007. Consultado em 9 de janeiro de 2025
- ↑ Albergotti, W. Greer; Bilodeau, Elizabeth A.; Byrd, J. Kenneth; Mims, Mark M.; Lee, Stella; Kim, Seungwon (março de 2016). «Hyalinizing clear cell carcinoma of the head and neck: Case series and update». Head & Neck (3): 426–433. ISSN 1097-0347. PMID 25352039. doi:10.1002/hed.23902. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f g h i Jalaly, Jalal. «Salivary duct carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ a b Nakaguro, Masato; Tada, Yuichiro; Faquin, William C.; Sadow, Peter M.; Wirth, Lori J.; Nagao, Toshitaka (outubro de 2020). «Salivary duct carcinoma: Updates in histology, cytology, molecular biology, and treatment». Cancer Cytopathology (10): 693–703. ISSN 1934-6638. PMC 7541685
 . PMID 32421944. doi:10.1002/cncy.22288. Consultado em 9 de janeiro de 2025
. PMID 32421944. doi:10.1002/cncy.22288. Consultado em 9 de janeiro de 2025
- ↑ Williams, Lindsay; Thompson, Lester D. R.; Seethala, Raja R.; Weinreb, Ilan; Assaad, Adel M.; Tuluc, Madalina; Ud Din, Nasir; Purgina, Bibianna; Lai, Chi (maio de 2015). «Salivary duct carcinoma: the predominance of apocrine morphology, prevalence of histologic variants, and androgen receptor expression». The American Journal of Surgical Pathology (5): 705–713. ISSN 1532-0979. PMID 25871467. doi:10.1097/PAS.0000000000000413. Consultado em 9 de janeiro de 2025
- ↑ Weon, Young Cheol; Park, Sun-Won; Kim, Hyung-Jin; Jeong, Han-Sin; Ko, Young-Hyeh; Park, In Suh; Kim, Sung Tae; Baek, Chung Hwan; Son, Young-Ik (junho de 2012). «Salivary duct carcinomas: clinical and CT and MR imaging features in 20 patients». Neuroradiology (6): 631–640. ISSN 1432-1920. PMID 22307272. doi:10.1007/s00234-012-1014-z. Consultado em 9 de janeiro de 2025
- ↑ Motoori, Ken; Iida, Yumiko; Nagai, Yuichirou; Yamamoto, Seiji; Ueda, Takuya; Funatsu, Hiroyuki; Ito, Hisao; Yoshitaka, Okamoto (maio de 2005). «MR imaging of salivary duct carcinoma». AJNR. American journal of neuroradiology (5): 1201–1206. ISSN 0195-6108. PMC 8158590
 . PMID 15891184. Consultado em 9 de janeiro de 2025
. PMID 15891184. Consultado em 9 de janeiro de 2025
- ↑ Udager, Aaron M.; Chiosea, Simion I. (setembro de 2017). «Salivary Duct Carcinoma: An Update on Morphologic Mimics and Diagnostic Use of Androgen Receptor Immunohistochemistry». Head and Neck Pathology (3): 288–294. ISSN 1936-0568. PMC 5550399
 . PMID 28321773. doi:10.1007/s12105-017-0798-x. Consultado em 9 de janeiro de 2025
. PMID 28321773. doi:10.1007/s12105-017-0798-x. Consultado em 9 de janeiro de 2025
- ↑ «Treatment by Cancer Type». NCCN (em inglês). Consultado em 9 de janeiro de 2025
- ↑ a b c d e f g h Huang, Min Li; Gupta, Ruta. «Epithelial myoepithelial carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Gore, Mitchell R. (2018). «Epithelial-myoepithelial carcinoma: a population-based survival analysis». BMC ear, nose, and throat disorders. 15 páginas. ISSN 1472-6815. PMC 6097440
 . PMID 30127663. doi:10.1186/s12901-018-0063-2. Consultado em 9 de janeiro de 2025
. PMID 30127663. doi:10.1186/s12901-018-0063-2. Consultado em 9 de janeiro de 2025
- ↑ a b Seethala, Raja R.; Barnes, E. Leon; Hunt, Jennifer L. (janeiro de 2007). «Epithelial-myoepithelial carcinoma: a review of the clinicopathologic spectrum and immunophenotypic characteristics in 61 tumors of the salivary glands and upper aerodigestive tract». The American Journal of Surgical Pathology (1): 44–57. ISSN 0147-5185. PMID 17197918. doi:10.1097/01.pas.0000213314.74423.d8. Consultado em 9 de janeiro de 2025
- ↑ Urano, Makoto; Nakaguro, Masato; Yamamoto, Yoshinari; Hirai, Hideaki; Tanigawa, Maki; Saigusa, Natsuki; Shimizu, Akira; Tsukahara, Kiyoaki; Tada, Yuichiro (julho de 2019). «Diagnostic Significance of HRAS Mutations in Epithelial-Myoepithelial Carcinomas Exhibiting a Broad Histopathologic Spectrum». The American Journal of Surgical Pathology (7): 984–994. ISSN 1532-0979. PMID 30994537. doi:10.1097/PAS.0000000000001258. Consultado em 9 de janeiro de 2025
- ↑ a b Li, Bowen; Yang, Hongyu; Hong, Xia; Wang, Yufan; Wang, Feng (dezembro de 2017). «Epithelial-myoepithelial carcinoma with high-grade transformation of parotid gland: A case report and literature review». Medicine (49): e8988. ISSN 1536-5964. PMC 5728887
 . PMID 29245272. doi:10.1097/MD.0000000000008988. Consultado em 9 de janeiro de 2025
. PMID 29245272. doi:10.1097/MD.0000000000008988. Consultado em 9 de janeiro de 2025
- ↑ Seethala, Raja R.; Richmond, Jeffrey A.; Hoschar, Aaron P.; Barnes, E. Leon (junho de 2009). «New variants of epithelial-myoepithelial carcinoma: oncocytic-sebaceous and apocrine». Archives of Pathology & Laboratory Medicine (6): 950–959. ISSN 1543-2165. PMID 19492889. doi:10.5858/133.6.950. Consultado em 9 de janeiro de 2025
- ↑ a b c d e f g h Aivazian, Karina; Gupta, Ruta. «Carcinoma ex pleomorphic adenoma». Pathology Outlines. Consultado em 9 de janeiro de 2025
- ↑ Gupta, Avigeet; Koochakzadeh, Sina; Neskey, David M.; Nguyen, Shaun A.; Lentsch, Eric J. (2019). «Carcinoma ex pleomorphic adenoma: A review of incidence, demographics, risk factors, and survival». American Journal of Otolaryngology (6). 102279 páginas. ISSN 1532-818X. PMID 31471126. doi:10.1016/j.amjoto.2019.102279. Consultado em 9 de janeiro de 2025
- ↑ Hashimoto, Kazuki; Yamamoto, Hidetaka; Shiratsuchi, Hideki; Nakashima, Torahiko; Tamiya, Sadafumi; Nishiyama, Ken-ichi; Higaki, Yuichiro; Komune, Shizuo; Tsuneyoshi, Masazumi (maio de 2012). «HER-2/neu gene amplification in carcinoma ex pleomorphic adenoma in relation to progression and prognosis: a chromogenic in-situ hybridization study». Histopathology (6B): E131–142. ISSN 1365-2559. PMID 22486195. doi:10.1111/j.1365-2559.2012.04201.x. Consultado em 9 de janeiro de 2025
- ↑ de Brito, Beatriz Samara; Giovanelli, Natália; Egal, Erika Said; Sánchez-Romero, Celeste; Nascimento, Juliana de Souza do; Martins, Antonio Santos; Tincani, Álfio José; Del Negro, André; Gondak, Rogério de Oliveira (novembro de 2016). «Loss of expression of Plag1 in malignant transformation from pleomorphic adenoma to carcinoma ex pleomorphic adenoma». Human Pathology: 152–159. ISSN 1532-8392. PMID 27473265. doi:10.1016/j.humpath.2016.07.011. Consultado em 9 de janeiro de 2025
- ↑ Lüers, Jan-Christoffer; Wittekindt, Claus; Streppel, M.; Guntinas-Lichius, Orlando (2009). «Carcinoma ex pleomorphic adenoma of the parotid gland. Study and implications for diagnostics and therapy». Acta Oncologica (Stockholm, Sweden) (1): 132–136. ISSN 1651-226X. PMID 18607845. doi:10.1080/02841860802183604. Consultado em 9 de janeiro de 2025
- ↑ Kashiwagi, Nobuo; Murakami, Takamichi; Chikugo, Takaaki; Tomita, Yasuhiko; Kawano, Kiyoshi; Nakanishi, Katsuyuki; Mori, Kazunori; Tomiyama, Noriyuki (1 de abril de 2012). «Carcinoma ex pleomorphic adenoma of the parotid gland». Acta Radiologica (Stockholm, Sweden: 1987) (3): 303–306. ISSN 1600-0455. PMID 22287150. doi:10.1258/ar.2011.110389. Consultado em 9 de janeiro de 2025
- ↑ Brandwein, M.; Huvos, A. G.; Dardick, I.; Thomas, M. J.; Theise, N. D. (junho de 1996). «Noninvasive and minimally invasive carcinoma ex mixed tumor: a clinicopathologic and ploidy study of 12 patients with major salivary tumors of low (or no?) malignant potential». Oral Surgery, Oral Medicine, Oral Pathology, Oral Radiology, and Endodontics (6): 655–664. ISSN 1079-2104. PMID 8784897. doi:10.1016/s1079-2104(96)80071-0. Consultado em 9 de janeiro de 2025
- ↑ Patel, Evan J.; Oliver, Jamie R.; Liu, Cheng; Tam, Moses; Givi, Babak (fevereiro de 2021). «Outcomes of carcinoma ex pleomorphic adenoma compared to de novo adenocarcinoma of major salivary glands». Journal of Surgical Oncology (2): 446–455. ISSN 1096-9098. PMID 33145786. doi:10.1002/jso.26289. Consultado em 9 de janeiro de 2025
- ↑ a b c d Kim, Ely. «Intraductal carcinoma». Pathology Outlines. Consultado em 9 de janeiro de 2025