Evolução da peçonha das serpentes
_juvenile_eating_(14232058164).jpg)
| Parte de uma série sobre |
| Evolução |
|---|
 |
|
A peçonha em cobras [en] e alguns lagartos é uma forma de saliva que foi modificada ao longo de sua história evolutiva para se tornar peçonha.[1] Nas cobras, a peçonha evoluiu para matar ou subjugar presas, além de desempenhar outras funções relacionadas à dieta.[2] Embora as cobras ocasionalmente usem sua peçonha em autodefesa, acredita-se que isso não tenha influenciado fortemente sua evolução.[3] A evolução da peçonha é considerada responsável pela enorme expansão das cobras pelo globo.[4][5][6]
A história evolutiva da peçonha das cobras é objeto de debate. Historicamente, acreditava-se que ela havia evoluído uma única vez, na base dos Caenophidia [en], ou cobras derivadas. Estudos moleculares iniciados em 2006 sugeriram que a peçonha surgiu apenas uma vez em um suposto clado de répteis, chamado Toxicofera, há cerca de 170 milhões de anos.[7] Sob essa hipótese, a peçonha toxicoferana original era um conjunto simples de proteínas reunidas em um par de glândulas. Posteriormente, esse conjunto diversificou-se nas várias linhagens de toxicoferanos, incluindo Serpentes, Anguimorpha e Iguania, com algumas linhagens de cobras perdendo a capacidade de produzir peçonha.[8][9] A hipótese Toxicofera foi contestada por estudos em meados da década de 2010, incluindo uma pesquisa de 2015 que encontrou homólogos de proteínas da peçonha em diversos tecidos da píton-birmanêsa.[10][11] Assim, o estudo sugeriu que a peçonha evoluiu independentemente em diferentes linhagens de répteis, incluindo uma vez nas cobras caenofídias.[10] Acredita-se que a peçonha contendo a maioria das famílias de toxinas atuais estava presente no último ancestral comum dos Caenophidia, tendo sofrido ampla diversificação, acompanhada por mudanças na morfologia das glândulas de peçonha e sistemas de entrega.[12]
A evolução da peçonha das cobras é impulsionada por uma corrida armamentista evolutiva entre as proteínas da peçonha e a fisiologia das presas.[13] O mecanismo comum de evolução é a duplicação gênica seguida por seleção natural para características adaptativas.[14] As adaptações resultantes incluem peçonha mais tóxica para presas específicas em várias linhagens,[15][16][17] proteínas que pré-digerem presas[18] e um método para rastrear presas após a mordida.[19] Essas adaptações variadas também geraram debates sobre a definição de peçonha e cobras peçonhentas.[20] Mudanças na dieta de uma linhagem foram associadas à atrofia da peçonha.[8][9]
História evolutiva
A origem da peçonha é vista como o catalisador para a rápida diversificação das cobras no período Cenozóico,[21] especialmente para os Colubridae e sua colonização das Américas.[5] Estudiosos sugerem que essa expansão se deve à transição de um método mecânico para um bioquímico de subjugar presas.[22][23] As peçonhas das cobras atacam vias e processos biológicos que também são alvos de peçonhas de outros táxons; por exemplo, bloqueadores de canais de cálcio [en] foram encontrados em cobras, aranhas e caramujos da família Conidae, sugerindo que a peçonha exibe evolução convergente.[24] A peçonha é comum entre famílias de cobras derivadas.[13] Acredita-se que a peçonha com a maioria das famílias de toxinas atuais estava presente no último ancestral comum dos Caenophidia, também chamados de Colubroidea, tendo sofrido grande diversificação, acompanhada por mudanças nas glândulas de peçonha e sistemas de entrega, ligada à rápida radiação global das cobras avançadas.[12] As presas tubulares ou sulcadas que as cobras usam para injetar peçonha evoluíram várias vezes, sendo um exemplo de evolução convergente. As presas tubulares comuns às cobras de presas frontais evoluíram independentemente em Viperidae, Elapidae e Atractaspidinae.[25]
| Serpentes |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||
Acima está um cladograma adaptado de Fry et al. (2012) mostrando um subconjunto de eventos sugeridos de recrutamento de proteínas. [A]: 13 famílias de toxinas, incluindo 3FTx e metaloprotease. [B]: 2 famílias de toxinas, incluindo PLA2 Tipo IIA e a classe P-II de metaloproteases da peçonha de cobra. [C]: 2 famílias de toxinas, incluindo PLA2 Tipo IB.[26][27]
Até o uso do sequenciamento de DNA para criar árvores filogenéticas se tornar prático, as filogenias eram baseadas na morfologia. Essas filogenias tradicionais sugeriam que a peçonha surgiu em múltiplas linhagens entre os Squamata há cerca de 100 milhões de anos: nos Caenophidia e no gênero de lagarto Heloderma.[7][10][28] Estudos com sequências de genes nucleares entre meados dos anos 2000 e início dos 2010 encontraram proteínas de peçonha nos clados de lagartos Anguimorpha e Iguania semelhantes às das cobras, sugerindo que, junto com Serpentes, formavam um clado chamado "Toxicofera".[7][28] Isso levou à teoria de que a peçonha surgiu uma única vez na linhagem inteira há cerca de 170 milhões de anos, sendo descrita como um conjunto simples de proteínas reunidas em glândulas.[7] As peçonhas das diferentes linhagens então diversificaram-se e evoluíram independentemente, junto com seus meios de injeção.[7] Isso incluiu a evolução independente de sistemas de entrega de peçonha de presas frontais a partir de um sistema ancestral de presas traseiras.[29] A hipótese de origem única também sugere que os sistemas de peçonha atrofiaram ou foram perdidos independentemente em várias linhagens.[20] A posição filogenética de Iguania dentro de Toxicofera é apoiada por estudos moleculares, mas não por morfológicos.[30]
A "hipótese Toxicofera" foi posteriormente desafiada. Um estudo de 2014 encontrou homólogos de 16 proteínas da peçonha, usadas para sustentar a hipótese de origem única, expressas em altos níveis em vários tecidos corporais.[11] Os autores sugeriram que pesquisas anteriores, que consideravam proteínas da peçonha conservadas na linhagem Toxicofera, poderiam ter interpretado erroneamente a presença de genes "domésticos" genéricos, devido à amostragem limitada de tecidos. Assim, propuseram que a peçonha evoluiu independentemente em várias linhagens, incluindo antes da radiação das cobras "avançadas".[11] Um estudo de 2015 encontrou homólogos dos chamados genes "tóxicos" em vários tecidos de uma cobra não peçonhenta, a píton-birmanêsa (Python bivittatus), demonstrando fraquezas na análise apenas de transcriptomas (o RNA mensageiro total numa célula).[10] A equipe sugeriu que as pítons representavam um período na evolução das cobras antes do grande desenvolvimento da peçonha, com a expansão das famílias de genes da peçonha ocorrendo principalmente em cobras caenofídias altamente peçonhentas, indicando que a maior parte da evolução da peçonha ocorreu após essa linhagem se separar de outras cobras.[10] O debate sobre a hipótese Toxicofera é parcialmente impulsionado por discordâncias sobre a definição de peçonha.[10][31] Até 2022, a hipótese Toxicofera permanecia uma visão predominante.[32]
Mecanismos de evolução
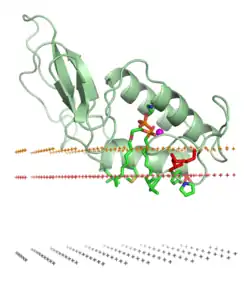
O principal mecanismo para a diversificação da peçonha é a duplicação de genes que codificam outros tecidos, seguida por sua expressão nas glândulas de peçonha, evoluindo então em várias proteínas da peçonha por seleção natural. Esse processo, conhecido como modelo de nascimento-e-morte, é responsável por vários eventos de recrutamento de proteínas na peçonha das cobras.[33][13] Essas duplicações ocorreram em diversos tipos de tecidos com funções ancestrais variadas. Exemplos notáveis incluem 3FTx, ancestralmente um neurotransmissor no cérebro, que se adaptou em uma neurotoxina que bloqueia receptores de acetilcolina, e fosfolipase A2 (PLA2) tipo IIA, envolvida ancestralmente em processos inflamatórios, que evoluiu para uma peçonha capaz de desencadear atividade de lipase e destruição tecidual.[21] A mudança na função do PLA2 foi bem documentada, com evidências de eventos de duplicação gênica associados ao surgimento de novas espécies de cobras.[34] A recombinação homóloga não alélica [en] induzida por invasão de transposons (ou recombinação entre sequências de DNA que são semelhantes, mas não são alelos) foi proposta como o mecanismo de duplicação dos genes PLA2 em cascavéis, explicando sua rápida evolução.[35] Essas proteínas da peçonha ocasionalmente também foram recrutadas de volta para genes teciduais.[36]
A duplicação gênica não é a única forma de diversificação da peçonha. Houve casos de novas proteínas da peçonha geradas por splicing alternativo. A cobra elapídea Bungarus fasciatus, por exemplo, possui um gene que é sofreu splicing alternativo para produzir tanto um componente da peçonha quanto uma proteína fisiológica.[36] A diversificação adicional pode ter ocorrido pela perda de genes de componentes específicos da peçonha. Por exemplo, acredita-se que o ancestral das cascavéis tinha genes PLA2 para uma neurotoxina heterodimérica agora encontrada em Crotalus scutulatus, mas esses genes estão ausentes em espécies modernas não neurotóxicas de cascavéis (Crotalus); os genes PLA2 para a miotoxina Lys49, supostamente presentes no ancestral comum das cascavéis, também foram perdidos várias vezes em linhagens recentes até as espécies atuais.[35] A perda de domínios também foi implicada na neofuncionalização da peçonha. A investigação da história evolutiva dos genes SVMP da peçonha de viperídeos revelou repetidas ocasiões de perda de domínios, acompanhadas por forte seleção positiva na maioria dos ramos filogenéticos onde isso ocorreu.[37] Toxinas da peçonha também evoluíram por "sequestro" ou "co-optação" de genes, ou seja, mudança na função de genes não relacionados. Um estudo de 2021 sugeriu que a co-optação explica a evolução da maioria dos tipos de toxinas, mas não das mais abundantes na peçonha das cobras.[27]
Eventos de recrutamento de proteínas ocorreram em diferentes pontos da história evolutiva das cobras. Por exemplo, a família de proteínas 3FTX está ausente na linhagem viperídea, sugerindo que foi recrutada para a peçonha após a separação das cobras viperídeas das demais colubróideas.[38] O PLA2 foi recrutado pelo menos duas vezes para a peçonha, uma em elapídeos e outra em viperídeos, exibindo evolução convergente dessa proteína em toxina.[39][40] Um estudo de 2019 sugeriu que a duplicação gênica permitiu que diferentes toxinas evoluíssem independentemente, possibilitando às serpentes experimentarem diferentes perfis de peçonha e explorar formulações eficazes, sendo uma das formas de diversificação ao longo de milhões de anos.[40] Esses eventos resultaram em uma peçonha extremamente complexa. A peçonha das cascavéis, por exemplo, inclui cerca de 40 proteínas distintas de diferentes famílias,[41] e outras peçonhas de cobras contêm mais de 100 proteínas diferentes.[22] A composição dessa mistura varia geograficamente e está relacionada às espécies de presas disponíveis em uma região.[17] A peçonha das cobras geralmente evolui muito rapidamente, com mudanças ocorrendo mais rápido na peçonha do que no resto do organismo.[42]
Pressão seletiva
Hipóteses antigas sobre a evolução da peçonha das cobras assumiam que a maioria injeta muito mais peçonha do que o necessário para matar suas presas, sugerindo que a composição da peçonha não estaria sujeita à seleção natural, conhecida como hipótese do "excesso".[43] No entanto, estudos recentes da história molecular da peçonha contradisseram isso, encontrando evidências de evolução adaptativa rápida em vários clados, incluindo as víboras dos gêneros Echis,[44] Sistrurus,[41] e Calloselasma,[45] bem como na diversificação das proteínas PLA2.[34] Há evidências filogenéticas de seleção positiva e taxas rápidas de ganho e perda de genes da peçonha em táxons de Sistrurus que se alimentam de diferentes presas.[46] Até 2019, havia evidências tanto de "excesso" em algumas linhagens quanto de evolução adaptativa rápida e uma corrida armamentista com a fisiologia das presas em muitas outras.[47]
Os genes que codificam proteínas da peçonha em alguns gêneros de cobras têm uma proporção de mutações sinônimas menor do que o esperado se a peçonha evoluísse por processos evolutivos neutros; a taxa de mutações não sinônimas, no entanto, foi encontrada mais alta em muitos casos, indicando seleção direcional.[34] Além disso, a produção de peçonha é metabolicamente custosa, o que cientistas sugeriram como evidência adicional de uma pressão seletiva para minimizar o volume necessário.[43] O uso de organismos-modelo, em vez de presas naturais, para estudar toxicidade foi sugerido como razão para a superestimação da hipótese do "excesso".[48] No entanto, o gênero de víboras Agkistrodon [en] é uma exceção; a composição da peçonha em Agkistrodon está relacionada à posição da espécie na filogenia, sugerindo que evoluiu principalmente por processos neutros (mutação e deriva genética), indicando variação significativa na pressão seletiva sobre diferentes peçonhas de cobras.[49]
Vários estudos encontraram evidências de que a peçonha e a resistência a ela em espécies de presas evoluíram em uma corrida armamentista coevolutiva.[43] Por exemplo, ratos-trocadores do gênero Neotoma têm alta resistência à peçonha de cascavéis, sugerindo que os ratos evoluíram em resposta à peçonha, renovando a pressão seletiva sobre as cobras.[41] Resistência a peçonhas de espécies de cobras predatórias simpátricas foi encontrada em enguias[50] e alguns tipos de esquilos.[51][52][53] Esses estudos sugerem uma corrida armamentista coevolutiva entre presa e predador, indicando outra pressão potencial sobre a peçonha para aumentar ou inovar em toxicidade. A pressão seletiva sobre a peçonha é vista como selecionando diversidade funcional nas proteínas da peçonha, tanto dentro de uma espécie quanto entre espécies.[54] Além da fisiologia das presas, há evidências de que a peçonha evoluiu em resposta à fisiologia de predadores.[13]
Além da dieta, outras pressões podem influenciar a composição da peçonha. Um estudo de 2019 encontrou que maior massa corporal e habitats ecológicos menores correlacionaram-se com maior produção de peçonha.[47] Outro estudo encontrou que clima e temperatura tinham correlações mais fortes com a peçonha do que dietas ou tipos de presas.[55] Embora cobras peçonhentas usem suas peçonhas em defesa (daí o problema de mordidas em humanos), não se sabe bem até que ponto a seleção natural para defesa impulsionou sua evolução. As peçonhas de Micrurus tener [en] e outras espécies de cobras-coral (Micrurus) contêm toxinas com atividade específica de indução de dor, sugerindo uma função defensiva.[56] Contudo, uma pesquisa com pacientes mordidos por diversas espécies peçonhentas mostrou que a dor após a maioria das mordidas tem início lento, argumentando contra uma seleção ampla para defesa.[3] O cuspe de peçonha exibido por algumas cobras cuspideiras é exclusivamente uma adaptação defensiva. Um estudo de 2021 mostrou que as peçonhas de todas as três linhagens dessas serpentes evoluíram convergentemente para níveis mais altos de ativação de neurônios sensoriais (ou seja, causam mais dor) do que as de cobras não cuspideiras, por ação sinérgica de citotoxinas e toxinas fosfolipase A2, indicando seleção para função defensiva.[57]
Diferentemente da composição e toxicidade para linhagens específicas, a produção de peçonha, ou a quantidade produzida por uma cobra individual, não varia com a massa corporal das presas, mas sim com a massa das cobras que a produzem, aumentando consistentemente com a hipótese de que as cobras investem uma proporção constante de sua saída metabólica na produção de peçonha, que é metabolicamente custosa.[47]
Adaptações funcionais
As cobras usam sua peçonha para matar ou subjugar presas, bem como para outras funções relacionadas à dieta, como digestão. A teoria científica atual sugere que a peçonha não é usada para defesa ou competição entre membros da mesma espécie, ao contrário de outros táxons. Assim, a evolução adaptativa na peçonha resultou em várias adaptações relacionadas a essas funções dietéticas que aumentam a aptidão das cobras que as possuem.[58][43][17] Isso também se reflete na variação da composição da peçonha dentro de uma espécie; a peçonha varia geograficamente, por idade e tamanho, provavelmente refletindo variações nas presas consumidas por diferentes grupos dentro da espécie.[13] A variação geográfica também está presente no nível de espécie; cobras insulares tendem a ter peçonhas menos complexas, enquanto as que vivem em habitats altamente produtivos têm peçonhas mais complexas, sugerindo um padrão biogeográfico.[59]
Toxicidade específica para presas

Peçonha tóxica apenas para certos táxons, ou fortemente tóxica apenas para certos táxons, foi encontrada em várias cobras, sugerindo que essas peçonhas evoluíram via seleção natural para subjugar presas preferidas. Exemplos incluem a cobra-dos-mangues (Boiga dendrophila [en]), com peçonha específica para aves,[48] os gêneros Echis e Sistrurus, e serpentes marinhas. A peçonha de Spilotes sulphureus [en] tem dois componentes: um tóxico para lagartos, mas não para mamíferos, e outro tóxico para mamíferos, mas não para lagartos.[60] Contudo, embora várias cobras possuam peçonha altamente tóxica para suas presas preferidas, a correlação inversa nem sempre é verdadeira: as peçonhas de várias cobras são tóxicas para táxons que elas não consomem em grandes proporções. A maioria das peçonhas, por exemplo, é altamente tóxica para lagartos, embora a proporção de presas lagartos varie entre espécies de cobras. Isso levou pesquisadores a sugerir que a toxicidade para um táxon é quase independente da toxicidade para outro táxon distantemente relacionado.[41]

As dietas naturais das cobras do gênero viperídeo Echis são altamente variadas, incluindo artrópodes, como escorpiões, e vertebrados. Diferentes espécies de Echis consomem quantidades variadas de artrópodes.[61] Um estudo de 2009 injetou escorpiões com peçonha de várias espécies de Echis e encontrou alta correlação entre a proporção de artrópodes consumidos em seu habitat natural e a toxicidade da peçonha para escorpiões.[44] Os pesquisadores também encontraram evidências de que a evolução de peçonha mais tóxica para artrópodes estava relacionada a um aumento na proporção de artrópodes na dieta, sugerindo coevolução entre dieta e peçonha. Uma filogenia do gênero construída com DNA mitocondrial mostrou que uma mudança na composição da peçonha no ancestral de todas as cobras Echis correlacionou-se com a transição para uma dieta baseada em artrópodes, enquanto outra mudança em uma linhagem mais recente correlacionou-se com uma dieta de vertebrados.[62] Apesar da maior toxicidade da peçonha das espécies consumidoras de artrópodes, ela não incapacitou ou matou presas mais rapidamente do que a de espécies com menos artrópodes na dieta. Assim, acredita-se que a peçonha evoluiu para minimizar o volume necessário, proporcionando um benefício adaptativo devido ao custo metabólico significativo de sua produção.[62] Esse padrão também é encontrado em outras linhagens.[63] Resultados semelhantes foram obtidos por um estudo de 2012 que constatou que a peçonha de espécies de Echis consumidoras de artrópodes era mais tóxica para gafanhotos do que a de espécies consumidoras de vertebrados.[64]
Um estudo de 2009 sobre a peçonha de quatro espécies de víboras Sistrurus encontrou variação significativa na toxicidade para camundongos, relacionada à proporção de pequenos mamíferos na dieta dessas espécies.[41] A ideia de que a peçonha de Sistrurus evoluiu para acomodar uma dieta baseada em mamíferos foi apoiada por análise filogenética, sugerindo que a diferença na toxicidade se deve à diferença na fisiologia muscular das várias presas.[41] Duas linhagens de cobras elapídeas, serpentes marinhas comuns e kraits marinhas Laticauda [en], colonizaram ambientes marinhos independentemente e mudaram para uma dieta simples baseada em peixes teleósteos.[17] Um estudo de 2005 encontrou que ambas as linhagens têm um conjunto de proteínas da peçonha muito mais simples do que seus parentes terrestres no continente australiano, que possuem uma dieta mais variada e complexa.[17] Esses achados foram confirmados por um estudo de 2012 que comparou as peçonhas de Toxicocalamus longissimus, uma espécie terrestre, e Hydrophis cyanocinctus [en], uma espécie marinha, ambas na subfamília Hydrophiinae. Apesar de serem próximas, a espécie marinha tinha um conjunto significativamente mais simples de proteínas da peçonha.[16] Ainda assim, as peçonhas das cobras marinhas estão entre as mais tóxicas conhecidas, possivelmente porque, incapazes de impedir a fuga das presas mordidas, suas peçonhas evoluíram para agir rapidamente.[65]
Pré-digestão de presas

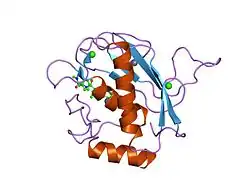
As várias subespécies do gênero de cascavéis Crotalus produzem peçonhas com duas funções conflitantes: imobilizar a presa após a mordida e auxiliar na digestão ao quebrar tecidos antes do consumo.[18] Como outros membros da família Viperidae, as peçonhas de Crotalus perturbam os processos homeostáticos das presas. No entanto, há uma ampla variedade de composições de peçonha entre as espécies de Crotalus. Um estudo de 2010 encontrou uma diferença de 100 vezes na atividade de metaloproteinase entre várias cobras, com Crotalus cerberus [en] apresentando a maior atividade e Crotalus concolor [en] a menor. Também houve uma variação de 15 vezes na atividade de protease, com C. concolor e C. cerberus tendo as maiores e menores atividades, respectivamente.[18]
A atividade de metaloproteinase causa hemorragia e necrose após a mordida, auxiliando na digestão. Já a atividade de proteases perturba a função de plaquetas e músculos e danifica membranas celulares, contribuindo para uma morte rápida da presa.[18] O estudo constatou que as peçonhas de Crotalus se dividiam em duas categorias: as que favoreciam metaloproteinases (Tipo I) e as que favoreciam proteases (Tipo II). Essas funções eram essencialmente mutuamente exclusivas; as peçonhas foram selecionadas com base em sua toxicidade ou potencial de amaciamento. Os pesquisadores hipotetizaram que a razão para essa dicotomia é que uma peçonha altamente neurotóxica, como a do tipo II, mata rapidamente, impedindo que a metaloproteinase, de ação mais lenta, digira tecidos.[18]
Rastreamento de presas mordidas

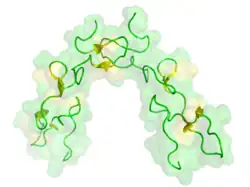
Outro exemplo de função adaptativa além da imobilização de presas é o papel da peçonha viperídea em permitir que a cobra rastreie uma presa mordida, um processo conhecido como "relocalização de presa". Essa adaptação importante permitiu às cascavéis evoluir o mecanismo de mordida de atacar e soltar, proporcionando um grande benefício ao minimizar o contato com presas potencialmente perigosas.[19] No entanto, isso exige que a cobra rastreie o animal mordido em um ambiente cheio de outros da mesma espécie. Um estudo de 2013 descobriu que cascavéis-diamante-ocidentais (Crotalus atrox) respondiam mais ativamente a carcaças de camundongos injetadas com peçonha bruta de cascavel. Quando os componentes da peçonha foram separados, as cobras reagiram a camundongos injetados com dois tipos de disintegrinas, concluindo que essas proteínas eram responsáveis por permitir o rastreamento ao alterar o odor do animal mordido.[19]
Atrofia baseada na dieta

A peçonha em várias linhagens de cobras parece ter atrofiado em resposta a mudanças na dieta.[7] Um estudo de 2005 na serpente-marinha-marmoreada (Aipysurus eydouxii [en]) encontrou que o gene para uma toxina três dedos na peçonha sofreu uma deleção de duas bases nucleotídicas, tornando a peçonha 50 a 100 vezes menos tóxica do que antes. Essa mudança correlacionou-se com a transição de uma dieta de peixes para uma quase exclusivamente de ovos de peixe, sugerindo que a adaptação removeu a pressão seletiva para manter uma peçonha altamente tóxica, permitindo mutações deletérias nos genes da peçonha.[17][66] Uma degradação semelhante da peçonha após a mudança para uma dieta baseada em ovos foi encontrada em Dasypeltis scabra [en], cuja dieta consiste inteiramente de ovos de aves, tornando a peçonha desnecessária. Isso levou biólogos a sugerir que, se a peçonha não é usada por uma espécie, ela é rapidamente perdida.[67]
Referências
- ↑ Hargreaves et al. (a) 2014.
- ↑ Casewell et al. 2013, pp. 218–220.
- ↑ a b Ward-Smith et al. 2020.
- ↑ Fry et al. 2012a, pp. 441–442.
- ↑ a b Wuster et al. 2008.
- ↑ Lomonte et al. (a) 2014, p. 326.
- ↑ a b c d e f Fry et al. 2012a, pp. 434–436.
- ↑ a b Fry et al. 2012a, pp. 424–436.
- ↑ a b Casewell et al. 2013, pp. 224–227.
- ↑ a b c d e f Reyes-Velasco et al. 2015.
- ↑ a b c Hargreaves et al. (b) 2014, pp. 153–155.
- ↑ a b Xie et al. 2022.
- ↑ a b c d e Casewell et al. 2020, pp. 570–581.
- ↑ Casewell et al. 2013, pp. 222–223.
- ↑ Barlow et al. 2009, pp. 2447–2448.
- ↑ a b Calvete et al. 2012, pp. 4094–4098.
- ↑ a b c d e f Li et al. 2005.
- ↑ a b c d e Mackessy 2010.
- ↑ a b c Saviola et al. 2013.
- ↑ a b Fry et al. 2012a, p. 443.
- ↑ a b Fry et al. 2012a.
- ↑ a b Lomonte et al. (a) 2014, pp. 326–327.
- ↑ Mackessy 2010, p. 1464.
- ↑ Casewell et al. 2013, pp. 225–227.
- ↑ Palci et al. 2021.
- ↑ Fry et al. 2012a, p. 435.
- ↑ a b Almeida et al. 2021.
- ↑ a b Sunagar & Abraham 2021.
- ↑ Fry & Wuster 2004, p. 870.
- ↑ Mount & Brown 2022, pp. 973–985.
- ↑ Hargreaves et al. (b) 2014.
- ↑ Rao et al. 2022.
- ↑ Casewell et al. 2013, p. 223.
- ↑ a b c Lynch 2007.
- ↑ a b Dowell et al. 2016.
- ↑ a b Casewell et al. 2013, p. 223–224.
- ↑ Casewell et al. 2011.
- ↑ Fry & Wuster 2004, p. 871.
- ↑ Fry et al. 2012b.
- ↑ a b Mikheyev & Barua 2019.
- ↑ a b c d e f Gibbs & Mackessy 2009.
- ↑ Lomonte et al. (a) 2014, p. 334.
- ↑ a b c d Barlow et al. 2009, p. 2443.
- ↑ a b Barlow et al. 2009, p. 2447.
- ↑ Casewell et al. 2013, p. 220.
- ↑ Gibbs & Rossiter 2008.
- ↑ a b c Healy & Carbone Jackson, pp. 527–537.
- ↑ a b Casewell et al. 2013, pp. 220–221.
- ↑ Lomonte et al. (b) 2014, pp. 112–114.
- ↑ Heatwole & Poran 1995.
- ↑ Biardi, Chien & Coss 2005.
- ↑ Biardi & Coss 2011.
- ↑ Pomento et al. 2016.
- ↑ Sanz et al. 2006, pp. 2098–2099.
- ↑ Zancolli et al. 2019.
- ↑ Bohlen 2011.
- ↑ Kazandjian et al. 2021.
- ↑ Casewell et al. 2013, pp. 219–220.
- ↑ Siqueira‐Silva et al. 2021, pp. 1978–1989.
- ↑ Modahl et al. 2018.
- ↑ Barlow et al. 2009, pp. 2444, 2447.
- ↑ a b Barlow et al. 2009, pp. 2446–2448.
- ↑ Casewell et al. 2013, pp. 223–225.
- ↑ Richards et al. 2012.
- ↑ Calvete et al. 2012, pp. 4092–4093.
- ↑ Calvete et al. 2012, pp. 4097–4098.
- ↑ Fry et al. 2008.
Bibliografia
- Almeida, Diego Dantas; Viala, Vincent Louis; Nachtigall, Pedro Gabriel; Broe, Michael; Gibbs, H. Lisle; Serrano, Solange Maria de Toledo; Moura-da-Silva, Ana Maria; Ho, Paulo Lee; Nishiyama-Jr, Milton Yutaka; Junqueira-de-Azevedo, Inácio L. M. (10 de maio de 2021). «Tracking the recruitment and evolution of snake toxins using the evolutionary context provided by the Bothrops jararaca genome». Proceedings of the National Academy of Sciences. 118 (20). Bibcode:2021PNAS..11815159A. ISSN 0027-8424. PMC 8157943
 . PMID 33972420. doi:10.1073/pnas.2015159118
. PMID 33972420. doi:10.1073/pnas.2015159118 - Barlow, A.; Pook, C.E.; Harrison, R.A.; Wuster, E.W. (2009). «Coevolution of diet and prey-specific venom activity supports the role of selection in snake venom evolution». Proceedings of the Royal Society B: Biological Sciences. 276 (1666): 2443–2449. PMC 2690460
 . PMID 19364745. doi:10.1098/rspb.2009.0048
. PMID 19364745. doi:10.1098/rspb.2009.0048 - Biardi, James E.; Chien, David C.; Coss, Richard G. (2005). «California ground squirrel (Spermophilus beecheyi) defenses against rattlesnake venom digestive and hemostatic toxins». Journal of Chemical Ecology. 31 (11): 2501–2518. Bibcode:2005JCEco..31.2501B. PMID 16273425. doi:10.1007/s10886-005-7610-1
- Biardi, JE; Coss, RG (2011). «Rock squirrel (Spermophilus variegatus) blood sera affects proteolytic and hemolytic activities of rattlesnake venoms». Toxicon. 57 (2): 323–331. Bibcode:2011Txcn...57..323B. PMID 21184770. doi:10.1016/j.toxicon.2010.12.011
- Bohlen, Christopher J. (17 de novembro de 2011). «A heteromeric Texas coral snake toxin targets acid-sensing ion channels to produce pain». Nature. 479 (7373). 414 páginas. Bibcode:2011Natur.479..410B. PMC 3226747
 . PMID 22094702. doi:10.1038/nature10607
. PMID 22094702. doi:10.1038/nature10607 - Calvete, J.J.; Ghezellou, P.; Paiva, O.; Matainaho, T.; Ghassempour, A.; Goudarzi, H.; Kraus, F.; Sanz, L.; Williams, D.J. (2012). «Snake venomics of two poorly known Hydrophiinae: Comparative proteomics of the venoms of terrestrial Toxicocalamus longissimus and marine Hydrophis cyanocinctus». Journal of Proteomics. 75 (13): 4091–4101. PMID 22643073. doi:10.1016/j.jprot.2012.05.026
- Casewell, N. R.; Wagstaff, S. C.; Harrison, R. A.; Renjifo, C.; Wuster, W. (4 de abril de 2011). «Domain Loss Facilitates Accelerated Evolution and Neofunctionalization of Duplicate Snake Venom Metalloproteinase Toxin Genes». Molecular Biology and Evolution. 28 (9): 2637–2649. ISSN 0737-4038. PMID 21478373. doi:10.1093/molbev/msr091
- Casewell, N.R.; Wuster, W.; Vonk, F.J.; Harrison, R.A.; Fry, B.G. (2013). «Complex cocktails: the evolutionary novelty of venoms». Trends in Ecology & Evolution. 28 (4): 219–229. Bibcode:2013TEcoE..28..219C. PMID 23219381. doi:10.1016/j.tree.2012.10.020
- Casewell, Nicholas R.; Jackson, Timothy N.W.; Laustsen, Andreas H.; Sunagar, Kartik (2020). «Causes and Consequences of Snake Venom Variation». Elsevier BV. Trends in Pharmacological Sciences. 41 (8): 570–581. ISSN 0165-6147. PMC 7116101
 . PMID 32564899. doi:10.1016/j.tips.2020.05.006
. PMID 32564899. doi:10.1016/j.tips.2020.05.006 - Dowell, Noah L.; Giorgianni, Matt W.; Kassner, Victoria A.; Selegue, Jane E.; Sanchez, Elda E.; Carroll, Sean B. (2016). «The Deep Origin and Recent Loss of Venom Toxin Genes in Rattlesnakes». Current Biology. 26 (18): 2434–2445. Bibcode:2016CBio...26.2434D. PMC 5207034
 . PMID 27641771. doi:10.1016/j.cub.2016.07.038
. PMID 27641771. doi:10.1016/j.cub.2016.07.038 - Gibbs, H. Lisle; Rossiter, Wayne (6 de fevereiro de 2008). «Rapid Evolution by Positive Selection and Gene Gain and Loss: PLA2 Venom Genes in Closely Related Sistrurus Rattlesnakes with Divergent Diets». Journal of Molecular Evolution (em inglês). 66 (2): 151–166. Bibcode:2008JMolE..66..151G. ISSN 0022-2844. PMID 18253686. doi:10.1007/s00239-008-9067-7
- Fry, B.G.; Casewell, N.R.; Wuster, W.; Vidal, N.; Young, B.; Jackson, T. N. W. (2012). «The structural and functional diversification of the Toxicofera reptile venom system». Toxicon. 60 (4): 434–448. Bibcode:2012Txcn...60..434F. PMID 22446061. doi:10.1016/j.toxicon.2012.02.013
- Fry, Bryan G.; Wuster, Wolfgang (2004). «Assembling an Arsenal: Origin and Evolution of the Snake Venom Proteome Inferred from Phylogenetic Analysis of Toxin Sequences». Molecular Biology and Evolution. 5 (21): 870–883. PMID 15014162. doi:10.1093/molbev/msh091
- Fry, Bryan G.; Scheib, Holger; Junqueira de Azevedo, Inacio de L.M.; Silva, Debora Andrade; Casewell, Nicholas R. (2012). «Novel transcripts in the maxillary venom glands of advanced snakes». Toxicon. 59 (7–8): 696–708. Bibcode:2012Txcn...59..696F. ISSN 0041-0101. PMID 22465490. doi:10.1016/j.toxicon.2012.03.005
- Fry, Bryan G.; Scheib, Holger; Van Der Weerd, Louise; Young, Bruce; McNaughtan, Judith; Ramjan, S. F. Ryan; Vidal, Nicolas; Poelmann, Robert E.; Norman, Janette A. (2008). «Evolution of an Arsenal». Molecular & Cellular Proteomics. 7 (2): 215–246. PMID 17855442. doi:10.1074/mcp.M700094-MCP200
- Gibbs, H.L.; Mackessy, S.P. (2009). «Functional basis of a molecular adaptation: Prey-specific toxic effects of venom from Sistrurus rattlesnakes». Toxicon. 53 (6): 672–679. Bibcode:2009Txcn...53..672G. PMID 19673082. doi:10.1016/j.toxicon.2009.01.034
- Hargreaves, Adam D.; Swain, Martin T.; Hegarty, Matthew J.; Logan, Darren W.; Mulley, John F. (1 de agosto de 2014). «Restriction and Recruitment—Gene Duplication and the Origin and Evolution of Snake Venom Toxins». Genome Biology and Evolution (em inglês). 6 (8): 2088–2095. ISSN 1759-6653. PMC 4231632
 . PMID 25079342. doi:10.1093/gbe/evu166
. PMID 25079342. doi:10.1093/gbe/evu166 - Hargreaves, Adam D.; Swain, Martin T.; Logan, Darren W.; Mulley, John F. (2014). «Testing the Toxicofera: Comparative transcriptomics casts doubt on the single, early evolution of the reptile venom system» (PDF). Toxicon. 92: 140–156. Bibcode:2014Txcn...92..140H. PMID 25449103. doi:10.1016/j.toxicon.2014.10.004. Consultado em 28 de março de 2025
- Healy, Kevin; Carbone, Chris; Jackson, Andrew L. (7 de janeiro de 2019). «Snake venom potency and yield are associated with prey-evolution, predator metabolism and habitat structure». Wiley. Ecology Letters. 22 (3): 527–537. Bibcode:2019EcolL..22..527H. ISSN 1461-023X. PMID 30616302. doi:10.1111/ele.13216. hdl:2262/92842
- Heatwole, Harold; Poran, Naomie S. (1995). «Resistances of sympatric and allopatric eels to sea snake venoms». Copeia. 1995 (1): 136–147. JSTOR 1446808. doi:10.2307/1446808
- Kazandjian, T. D.; Petras, D.; Robinson, S. D.; van Thiel, J.; Greene, H. W.; Arbuckle, K.; Barlow, A.; Carter, D. A.; Wouters, R. M.; Whiteley, G.; Wagstaff, S. C.; Arias, A. S.; Albulescu, L.-O.; Plettenberg Laing, A.; Hall, C.; Heap, A.; Penrhyn-Lowe, S.; McCabe, C. V.; Ainsworth, S.; da Silva, R. R.; Dorrestein, P. C.; Richardson, M. K.; Gutiérrez, J. M.; Calvete, J. J.; Harrison, R. A.; Vetter, I.; Undheim, E. A. B.; Wüster, W.; Casewell, N. R. (2021). «Convergent evolution of pain-inducing defensive venom components in spitting cobras» (PDF). Science. 371 (6527): 386–390. Bibcode:2021Sci...371..386K. ISSN 0036-8075. PMC 7610493
 . PMID 33479150. doi:10.1126/science.abb9303. Consultado em 28 de março de 2025
. PMID 33479150. doi:10.1126/science.abb9303. Consultado em 28 de março de 2025 - Li, M.; Fry, B.G.; Kini, R.M. (2005). «Eggs-only diet: Its implications for the toxin profile changes and ecology of the marbled sea snake (Aipysurus eydouxii)» (PDF). Journal of Molecular Evolution. 60 (1): 81–89. Bibcode:2005JMolE..60...81L. PMID 15696370. doi:10.1007/s00239-004-0138-0. Consultado em 28 de março de 2025
- Lomonte, B.; Fernandez, J.; Sanz, L.; Angulo, Y.; Sasa, M.; Gutierrez, J. M.; Calvete, J. J. (2014). «Venomous snakes of Costa Rica: Biological and medical implications of their venom proteomic profiles analyzed through the strategy of snake venomics». Journal of Proteomics. 105: 323–339. PMID 24576642. doi:10.1016/j.jprot.2014.02.020
- Lomonte, B.; Tsai, W. C.; Urena-Diaz, J. M.; Sanz, L.; Mora-Obando, D.; Sanchez, E. E.; Fry, B.G.; Gutierrez, J. M.; Gibbs, H. L.; Sovic, M.G.; Calvete, J.J. (2014). «Venomics of New World pit vipers: Genus-wide comparisons of venom proteomes across Agkistrodon». Journal of Proteomics. 96: 103–116. PMC 4294458
 . PMID 24211403. doi:10.1016/j.jprot.2013.10.036
. PMID 24211403. doi:10.1016/j.jprot.2013.10.036 - Lynch, V.J. (2007). «Inventing an arsenal: adaptive evolution and neofunctionalization of snake venom phospholipase A(2) genes». BMC Evolutionary Biology. 7 (1): 2. PMC 1783844
 . PMID 17233905. doi:10.1186/1471-2148-7-2
. PMID 17233905. doi:10.1186/1471-2148-7-2 - Mackessy, Stephen P. (2010). «Evolutionary trends in venom composition in the Western Rattlesnakes (Crotalus viridis sensu lato): Toxicity vs. tenderizers». Toxicon. 55 (8): 1463–1474. Bibcode:2010Txcn...55.1463M. PMID 20227433. doi:10.1016/j.toxicon.2010.02.028
- Palci, Alessandro; LeBlanc, Aaron R. H.; Panagiotopoulou, Olga; Cleuren, Silke G. C.; Mehari Abraha, Hyab; Hutchinson, Mark N.; Evans, Alistair R.; Caldwell, Michael W.; Lee, Michael S. Y. (11 de agosto de 2021). «Plicidentine and the repeated origins of snake venom fangs». The Royal Society. Proceedings of the Royal Society B: Biological Sciences. 288 (1956): 20211391. ISSN 0962-8452. PMC 8354744
 . PMID 34375553. doi:10.1098/rspb.2021.1391
. PMID 34375553. doi:10.1098/rspb.2021.1391 - Mikheyev, Alexander S.; Barua, Agneesh (2019). «Many Options, Few Solutions: Over 60 My Snakes Converged on a Few Optimal Venom Formulations». Molecular Biology and Evolution (em inglês). 36 (9): 1964–1974. PMC 6736290
 . PMID 31220860. doi:10.1093/molbev/msz125
. PMID 31220860. doi:10.1093/molbev/msz125 - Modahl, Cassandra M.; Mrinalini, null; Frietze, Seth; Mackessy, Stephen P. (2018). «Adaptive evolution of distinct prey-specific toxin genes in rear-fanged snake venom». Proceedings of the Royal Society B: Biological Sciences. 285 (1884). 20181003 páginas. PMC 6111164
 . PMID 30068680. doi:10.1098/rspb.2018.1003
. PMID 30068680. doi:10.1098/rspb.2018.1003 - Mount, Genevieve G; Brown, Jeremy M (22 de março de 2022). «Comparing Likelihood Ratios to Understand Genome-Wide Variation in Phylogenetic Support». Oxford University Press (OUP). Systematic Biology. 71 (4): 973–985. ISSN 1063-5157. PMID 35323986. doi:10.1093/sysbio/syac014
- Pomento, AM; Perry, BW; Denton, RD; Gibbs, HL; Holding, ML (2016). «No safety in the trees: Local and species-level adaptation of an arboreal squirrel to the venom of sympatric rattlesnakes». Toxicon. 118: 149–155. Bibcode:2016Txcn..118..149P. PMID 27158112. doi:10.1016/j.toxicon.2016.05.003
- Rao, Wei-qiao; Kalogeropoulos, Konstantinos; Allentoft, Morten E; Gopalakrishnan, Shyam; Zhao, Wei-ning; Workman, Christopher T; Knudsen, Cecilie; Jiménez-Mena, Belén; Seneci, Lorenzo; Mousavi-Derazmahalleh, Mahsa; Jenkins, Timothy P; Rivera-de-Torre, Esperanza; Liu, Si-qi; Laustsen, Andreas H (2022). «The rise of genomics in snake venom research: recent advances and future perspectives». Oxford University Press (OUP). GigaScience. 11. ISSN 2047-217X. PMC 8975721
 . PMID 35365832. doi:10.1093/gigascience/giac024
. PMID 35365832. doi:10.1093/gigascience/giac024 - Reyes-Velasco, Jacobo; Card, Daren C.; Andrew, Audra L.; Shaney, Kyle J.; Adams, Richard H.; Schield, Drew R.; Casewell, Nicholas R.; Mackessy, Stephen P.; Castoe, Todd A. (1 de janeiro de 2015). «Expression of Venom Gene Homologs in Diverse Python Tissues Suggests a New Model for the Evolution of Snake Venom». Molecular Biology and Evolution (em inglês). 32 (1): 173–183. ISSN 0737-4038. PMID 25338510. doi:10.1093/molbev/msu294
- Richards, D. P.; Barlow, A.; Wüster, W. (1 de janeiro de 2012). «Venom lethality and diet: Differential responses of natural prey and model organisms to the venom of the saw-scaled vipers (Echis)». Toxicon. 59 (1): 110–116. Bibcode:2012Txcn...59..110R. PMID 22079297. doi:10.1016/j.toxicon.2011.10.015
- Sanz, Libia; Gibbs, H. Lisle; Mackessy, Stephen P.; Calvete, Juan J. (2006). «Venom Proteomes of Closely Related Sistrurus rattlesnakes with Divergent Diets». Journal of Proteome Research. 5 (9): 2098–2112. CiteSeerX 10.1.1.506.9290
 . PMID 16944921. doi:10.1021/pr0602500
. PMID 16944921. doi:10.1021/pr0602500 - Saviola, A.J.; Chiszar, D.; Busch, C.; Mackessy, S.P. (2013). «Molecular basis for prey relocation in viperid snakes». BMC Biology. 11 (1). 20 páginas. PMC 3635877
 . PMID 23452837. doi:10.1186/1741-7007-11-20
. PMID 23452837. doi:10.1186/1741-7007-11-20 - Siqueira-Silva, Tuany; Lima, Luiz Antônio Gonzaga; Chaves-Silveira, Jônatas; Amado, Talita Ferreira; Naipauer, Julian; Riul, Pablo; Martinez, Pablo Ariel; Sheard, Catherine (27 de julho de 2021). «Ecological and biogeographic processes drive the proteome evolution of snake venom». Wiley. Global Ecology and Biogeography. 30 (10): 1978–1989. Bibcode:2021GloEB..30.1978S. ISSN 1466-822X. doi:10.1111/geb.13359. Consultado em 28 de março de 2025
- Sunagar, Kartik; Abraham, Siju V (3 de fevereiro de 2021). «The Curious Case of the "Neurotoxic Skink": Scientific Literature Points to the Absence of Venom in Scincidae». MDPI AG. Toxins. 13 (2): 114. ISSN 2072-6651. PMC 7913497
 . PMID 33546362. doi:10.3390/toxins13020114
. PMID 33546362. doi:10.3390/toxins13020114 - Wuster, Wolfgang; Peppin, Lindsay; Pook, Catherine E.; Walker, Daniel E. (2008). «A nesting of vipers: Phylogeny and historical biogeography of the Viperidae (Squamata: Serpentes)». Molecular Phylogenetics and Evolution. 49 (2): 445–459. Bibcode:2008MolPE..49..445W. PMID 18804544. doi:10.1016/j.ympev.2008.08.019
- Ward-Smith, Harry; Arbuckle, Kevin; Naude, Arno; Wüster, Wolfgang (2020). «Fangs for the memories? A survey of pain in snakebite patients does not support a strong role for defense in the evolution of snake venom composition». Toxins. 12 (3). 201 páginas. PMC 7150919
 . PMID 32235759. doi:10.3390/toxins12030201
. PMID 32235759. doi:10.3390/toxins12030201 - Xie, Bing; Dashevsky, Daniel; Rokyta, Darin; Ghezellou, Parviz; Fathinia, Behzad; Shi, Qiong; Richardson, Michael K.; Fry, Bryan G. (7 de janeiro de 2022). «Dynamic genetic differentiation drives the widespread structural and functional convergent evolution of snake venom proteinaceous toxins». Springer Science and Business Media LLC. BMC Biology. 20 (1): 4. ISSN 1741-7007. PMC 8742412
 . PMID 34996434. doi:10.1186/s12915-021-01208-9
. PMID 34996434. doi:10.1186/s12915-021-01208-9 - Zancolli, Giulia; Calvete, Juan J.; Cardwell, Michael D.; Greene, Harry W.; Hayes, William K.; Hegarty, Matthew J.; Herrmann, Hans-Werner; Holycross, Andrew T.; Lannutti, Dominic I.; Mulley, John F.; Sanz, Libia (13 de março de 2019). «When one phenotype is not enough: divergent evolutionary trajectories govern venom variation in a widespread rattlesnake species». Proceedings of the Royal Society B: Biological Sciences. 286 (1898). 20182735 páginas. PMC 6458317
 . PMID 30862287. doi:10.1098/rspb.2018.2735
. PMID 30862287. doi:10.1098/rspb.2018.2735
.jpg)