Fosfolipase A2
As fosfolipases A₂ (PLA₂) EC 3.1.1.4 são enzimas que libertam ácidos gordos ligados ao segundo carbono (posição sn-2) do glicerol. Esta fosfolipase reconhece especificamente o grupo acilo unido em sn-2 de fosfolípidos e hidrolisa cataliticamente a ligação, libertando ácido araquidónico e lisofosfolípidos. Por uma posterior modificação feita por ciclo-oxigenases, o ácido araquidónico converte-se em compostos ativos chamados eicosanoides. Entre os eicosanoides estão as prostaglandinas e os leucotrienos, que são considerados mediadores anti-inflamatórios e inflamatórios.[1]
As enzimas PLA₂ são encontradas vulgarmente em tecidos de mamíferos e em aracnídeos, insetos e no veneno de serpente.[2] Os venenos de serpentes e insetos são em grande parte compostos por melitina, que é um estimulante da PLA₂. Devido ao aumento da presença e da atividade da PLA₂ que se produz como resultado de uma mordida ou picada de certas serpentes ou insetos, o ácido araquidónico é libertado dos fosfolípidos de membrana de forma desproporcionada. O resultado é inflamação e dor no local afetado pela picada.[3] Há também fosfolipases A₂ procarióticas.
Tipos adicionais de fosfolipases são a fosfolipase A₁, fosfolipase B, fosfolipase C e fosfolipase D.[4]
Famílias
As fosfolipases A₂ incluem várias famílias de proteínas não relacionadas que têm uma atividade enzimática comum. Duas das mais notáveis famílias são as fosfolipases A₂ citosólicas e segregadas. Outras famílias são a da PLA₂ independente do Ca2+ (iPLA₂) e a da PLA₂ associada a lipoproteínas (lp-PLA₂), também chamada fator ativador das plaquetas acetil-hidrolase (PAF-AH).
Fosfolipases A₂ Segregadas (sPLA₂)
As formas extracelulares das fosfolipases A₂ foram isoladas de diferentes venenos (de serpes, abelhas e vespas), e de praticamente todos os tecidos de mamíferos estudados (incluindo o pâncreas e os rins) e também de bactérias. Para a sua atividade requerem Ca2+.
As sPLA₂ pancreáticas servem para a digestão inicial dos compostos fosfolipídicos das gorduras da dieta. As fosfolipases do veneno ajudam a imobilizar as presas ao promover a lise celular.
Em ratos, as sPLA₂ do grupo III estão implicadas na maturação dos espermatozoides,[5] e as do grupo X crê-se que estão implicadas na capacitação dos espermatozoides.[6]
A sPLA₂ promove a inflamação em mamíferos ao catalisar o primeiro passo da via do ácido araquidónico ao degradar fosfolípidos, o que resulta na formação de ácidos gordos incluindo o ácido araquidónico. Este ácido araquidónico é depois metabolizado para formar várias moléculas inflamatórias e tromboxénicas. Os níveis excessivos de sPLA₂ crê-se que contribuem para várias doenças inflamatórias, e promovem a inflamação vascular correlacionada com eventos coronários na doença coronária e a síndrome coronária aguda,[7] e possivelmente acaba por causar síndrome de dificuldade respiratória aguda[8] e a progressão da amigdalite[9]
Em crianças, os níveis excessivos de sPLA₂ foram associados à inflamação que se crê exacerbar a asma[10] e à inflamação da superfície celular (olho seco).[11]
O aumento da atividade da sPLA₂ observa-se no líquido cefalorraquidiano de pessoas com doença de Alzheimer e esclerose múltipla, e pode servir como marcador do aumento da permeabilidade da barreira hemato-raquidiana.[12]
Fosfolipases A₂ Citosólicas (cPLA₂)
As PLA₂ intracelulares (cPLA₂) são também dependentes de Ca, mas têm uma estrutura tridimensional completamente diferente e significativamente maior do que a PLA₂ segregada (mais de 700 resíduos). Incluem o domínio C2 e o domínio catalítico grande.
Estas fosfolipases estão implicadas em processos de sinalização celular, como a resposta inflamatória. O ácido araquidónico produzido é simultaneamente uma molécula de sinalização e o precursor de outras moléculas de sinalização denominadas eicosanoides. Entre estes estão os leucotrienos e as prostaglandinas. Alguns eicosanoides sintetizam-se a partir do diacilglicerol, libertado da bicamada lipídica pela fosfolipase C (ver abaixo).
As fosfolipases A₂ podem ser classificadas com base na homologia de sequências.[13]
PLA₂s Associadas a Lipoproteínas (lp-PLA₂)
Viaja pelo sangue associada a lipoproteínas, principalmente às LDL, e em menor medida (cerca de 20%) às HDL. É uma enzima produzida por células inflamatórias que hidrolisa fosfolípidos oxidados nas LDL.
A lp-PLA₂ é uma das várias PAF acetil-hidrolase (EC 3.1.1.47), que é segregada e catalisa a degradação do PAF a produtos inativos ao hidrolisar o grupo acetilo na posição sn-2, originando os produtos biologicamente inativos liso-PAF e acetato.[14]
O aumento dos níveis de lp-PLA₂ está associado a doenças cardíacas, e pode contribuir para a aterosclerose.[15]
Mecanismo
O mecanismo catalítico sugerido da sPLA2 pancreática é iniciado pelo complexo His-48/Asp-99/Cálcio (Ca2+) situado no sítio ativo. O ião Ca2+ polariza o oxigénio do grupo carbonilo em *sn*-2 e também se coordena com uma molécula de água catalítica, w5. A His-48 incrementa a nucleofilia da água catalítica por meio de uma ponte com uma segunda molécula de água, w6. Sugeriu-se que são necessárias duas moléculas de água para cobrir a distância entre a histidina catalítica e o grupo éster. A basicidade da His-48 crê-se ser potenciada por meio de uma ponte de hidrogénio com o Asp-99. Uma substituição de asparagina por His-48 mantém a atividade normal, uma vez que o grupo funcional amida da asparagina pode também funcionar diminuindo o pKa, ou constante de dissociação de ácido, da molécula de água que faz a ponte. O estado limitante é caracterizado pela degradação do composto intermédio tetraédrico constituído por um oxianião coordenado com cálcio. O papel do cálcio pode também ser duplicado por outros catiões relativamente pequenos como o cobalto e o níquel.[16] Antes de se tornar ativa na digestão, a pró-forma da PLA2 é ativada pela tripsina.
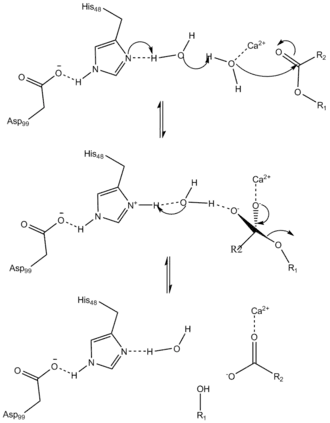
A PLA2 também pode ser caracterizada por ter um canal com uma parede hidrofóbica com resíduos de aminoácidos hidrofóbicos como a Fenilalanina (Phe), Leucina (Leu) e Tirosina (Tyr), que servem para se ligar ao substrato enzimático. Outros componentes da PLA2 são as sete pontes de dissulfeto que influenciam a regulação e o enovelamento estável da proteína.[16]
Regulação
Dada a importância da PLA2 na resposta inflamatória, a regulação desta enzima é essencial. A PLA2 é regulada por fosforilação e pelas concentrações de cálcio. A PLA2 é fosforilada pela MAPK no resíduo serina-505. Quando a fosforilação está acoplada a um influxo de iões cálcio, a PLA2 é estimulada e pode translocar-se para a membrana para começar a catálise.[17]
A fosforilação de PLA2 pode ser o resultado da ligação de um ligando a recetores, como são os seguintes:
- Receptor de 5-HT2 (de serotonina) [18]
- mGLUR1[18]
- Recetor bFGF[18]
- Recetor do IFN-α[18]
- Recetor do IFN-γ[18]
No caso de uma inflamação, a aplicação de glicocorticoides regula em alta (mediado a nível génico) a produção da proteína lipocortina, que inibe a PLA2 e reduz a resposta inflamatória.
Relevância em Doenças Neurológicas
Nas células do cérebro normais, a regulação da PLA2 explica o equilíbrio entre a conversão do ácido araquidónico em mediadores pro-inflamatórios e a sua reincorporação na membrana. Na ausência de uma regulação estrita da atividade da PLA2, é produzida uma quantidade desproporcionada de mediadores pro-inflamatórios. O stress oxidativo induzido e a neuroinflamação resultantes são análogos a doenças neurológicas como a doença de Alzheimer, epilepsia, esclerose múltipla e isquemia. Os lisofosfolípidos são outra classe de moléculas libertadas das membranas que são precursores, na via a montante, de fatores ativadores de plaquetas (PAF). Níveis anormais de potentes PAF estão associados a danos neurológicos. Um inibidor enzimático ideal teria como alvo específico a atividade da PLA2 nas membranas das células neurais que já estão sob stress oxidativo e inflamação potente. Assim, o uso de inibidores específicos da PLA2 do cérebro poderia ser uma abordagem farmacêutica para o tratamento de várias doenças associadas a traumas neurais.[19]
Um aumento da fosfolipase A2 foi também associado a doenças neuropsiquiátricas como a esquizofrenia e as perturbações globais do desenvolvimento (como o autismo), embora os mecanismos utilizados não sejam conhecidos.[20]
Isoenzimas
As isoenzimas da fosfolipase A2 humana são:
- Grupo I: PLA2G1B
- Grupo II: PLA2G2A, PLA2G2C
- Grupo III: PLA2G3
- Grupo IV: PLA2G4A, PLA2G4B, PLA2G4C, PLA2G4D
- Grupo V: PLA2G5
- Grupo VI: PLA2G6
- Grupo VII: PLA2G7
- Grupo X: PLA2G10
- Grupo XII: PLA2G12A, PLA2G12B
Além disso, as seguintes proteínas humanas contêm o domínio de fosfolipase A2:
Referências
- ↑ Dennis EA (May 1994). «Diversity of group types, regulation, and function of phospholipase A2». The Journal of Biological Chemistry. 269 (18): 13057–60. PMID 8175726 Verifique data em:
|data=(ajuda) - ↑ Nicolas JP, Lin Y, Lambeau G, Ghomashchi F, Lazdunski M, Gelb MH (Mar 1997). «Localization of structural elements of bee venom phospholipase A2 involved in N-type receptor binding and neurotoxicity». The Journal of Biological Chemistry. 272 (11): 7173–81. PMID 9054413. doi:10.1074/jbc.272.11.7173
- ↑ Argiolas A, Pisano JJ (Nov 1983). «Facilitation of phospholipase A2 activity by mastoparans, a new class of mast cell degranulating peptides from wasp venom» (PDF). The Journal of Biological Chemistry. 258 (22): 13697–702. PMID 6643447
- ↑ Cox, Michael; Nelson, David R.; Lehninger, Albert L (2005). Lehninger principles of biochemistry 4th ed. San Francisco: W.H. Freeman. ISBN 0-7167-4339-6
- ↑ Sato H, Taketomi Y, Isogai Y, Miki Y, Yamamoto K, Masuda S, Hosono T, Arata S, Ishikawa Y, Ishii T, Kobayashi T, Nakanishi H, Ikeda K, Taguchi R, Hara S, Kudo I, Murakami M (May 2010). «Group III secreted phospholipase A2 regulates epididymal sperm maturation and fertility in mice». The Journal of Clinical Investigation. 120 (5): 1400–14. PMC 2860917
 . PMID 20424323. doi:10.1172/JCI40493 Verifique data em:
. PMID 20424323. doi:10.1172/JCI40493 Verifique data em: |data=(ajuda) - ↑ Escoffier J, Jemel I, Tanemoto A, Taketomi Y, Payre C, Coatrieux C, Sato H, Yamamoto K, Masuda S, Pernet-Gallay K, Pierre V, Hara S, Murakami M, De Waard M, Lambeau G, Arnoult C (May 2010). «Group X phospholipase A2 is released during sperm acrosome reaction and controls fertility outcome in mice». The Journal of Clinical Investigation. 120 (5): 1415–28. PMC 2860919
 . PMID 20424324. doi:10.1172/JCI40494 Verifique data em:
. PMID 20424324. doi:10.1172/JCI40494 Verifique data em: |data=(ajuda) - ↑ Mallat Z, Lambeau G, Tedgui A (Nov 2010). «Lipoprotein-associated and secreted phospholipases A₂ in cardiovascular disease: roles as biological effectors and biomarkers». Circulation. 122 (21): 2183–200. PMID 21098459. doi:10.1161/CIRCULATIONAHA.110.936393
- ↑ De Luca D, Minucci A, Cogo P, Capoluongo ED, Conti G, Pietrini D, Carnielli VP, Piastra M (Jan 2011). «Secretory phospholipase A₂ pathway during pediatric acute respiratory distress syndrome: a preliminary study». Pediatric Critical Care Medicine. 12 (1): e20-4. PMID 20351613. doi:10.1097/PCC.0b013e3181dbe95e
- ↑ Ezzeddini R, Darabi M, Ghasemi B, Jabbari Moghaddam Y, Jabbari Y, Abdollahi S, Rashtchizadeh N, Gharahdaghi A, Darabi M, Ansarin M, Shaaker M, Samadi A, Karamravan J (Apr 2012). «Circulating phospholipase-A2 activity in obstructive sleep apnea and recurrent tonsillitis». International Journal of Pediatric Otorhinolaryngology. 76 (4): 471–4. PMID 22297210. doi:10.1016/j.ijporl.2011.12.026 Verifique data em:
|data=(ajuda) - ↑ Henderson WR, Oslund RC, Bollinger JG, Ye X, Tien YT, Xue J, Gelb MH (Aug 2011). «Blockade of human group X secreted phospholipase A2 (GX-sPLA2)-induced airway inflammation and hyperresponsiveness in a mouse asthma model by a selective GX-sPLA2 inhibitor». The Journal of Biological Chemistry. 286 (32): 28049–55. PMC 3151050
 . PMID 21652694. doi:10.1074/jbc.M111.235812 Verifique data em:
. PMID 21652694. doi:10.1074/jbc.M111.235812 Verifique data em: |data=(ajuda) - ↑ Wei Y, Epstein SP, Fukuoka S, Birmingham NP, Li XM, Asbell PA (Jun 2011). «sPLA2-IIa amplifies ocular surface inflammation in the experimental dry eye (DE) BALB/c mouse model». Investigative Ophthalmology & Visual Science. 52 (7): 4780–8. PMC 3175946
 . PMID 21519031. doi:10.1167/iovs.10-6350
. PMID 21519031. doi:10.1167/iovs.10-6350
- ↑ Chalbot S, Zetterberg H, Blennow K, Fladby T, Andreasen N, Grundke-Iqbal I, Iqbal K (Janeiro de 2011). «Blood-cerebrospinal fluid barrier permeability in Alzheimer's disease». Journal of Alzheimer's Disease. 25 (3): 505–15. PMC 3139450
 . PMID 21471645. doi:10.3233/JAD-2011-101959
. PMID 21471645. doi:10.3233/JAD-2011-101959
- ↑ Six DA, Dennis EA (Outubro de 2000). «The expanding superfamily of phospholipase A(2) enzymes: classification and characterization». Biochimica Et Biophysica Acta. 1488 (1-2): 1–19. PMID 11080672. doi:10.1016/S1388-1981(00)00105-0
- ↑ «Entrez Gene: PLA2G7 phospholipase A2, group VII (platelet-activating factor acetylhydrolase, plasma)»
- ↑ Wilensky RL, Shi Y, Mohler ER, Hamamdzic D, Burgert ME, Li J, Postle A, Fenning RS, Bollinger JG, Hoffman BE, Pelchovitz DJ, Yang J, Mirabile RC, Webb CL, Zhang L, Zhang P, Gelb MH, Walker MC, Zalewski A, Macphee CH (Outubro de 2008). «Inhibition of lipoprotein-associated phospholipase A2 reduces complex coronary atherosclerotic plaque development». Nature Medicine. 14 (10): 1059–66. PMC 2885134
 . PMID 18806801. doi:10.1038/nm.1870
. PMID 18806801. doi:10.1038/nm.1870
- ↑ a b Berg OG, Gelb MH, Tsai MD, Jain MK (setembro de 2001). «Interfacial enzymology: the secreted phospholipase A(2)-paradigm». Chemical Reviews. 101 (9): 2613–54. PMID 11749391. doi:10.1021/cr990139w.
See page 2640
- ↑ Leslie CC (julho de 1997). «Properties and regulation of cytosolic phospholipase A2». The Journal of Biological Chemistry. 272 (27): 16709–12. PMID 9201969. doi:10.1074/jbc.272.27.16709
- ↑ a b c d e Walter F., PhD. Boron (2003). Medical Physiology: A Cellular And Molecular Approaoch. [S.l.]: Elsevier/Saunders. p. 103. ISBN 1-4160-2328-3
- ↑ Farooqui AA, Ong WY, Horrocks LA (setembro de 2006). «Inhibitors of brain phospholipase A2 activity: their neuropharmacological effects and therapeutic importance for the treatment of neurologic disorders». Pharmacological Reviews. 58 (3): 591–620. PMID 16968951. doi:10.1124/pr.58.3.7
- ↑ Bell JG, MacKinlay EE, Dick JR, MacDonald DJ, Boyle RM, Glen AC (outubro de 2004). «Essential fatty acids and phospholipase A2 in autistic spectrum disorders». Prostaglandins, Leukotrienes, and Essential Fatty Acids. 71 (4): 201–4. PMID 15301788. doi:10.1016/j.plefa.2004.03.008