Ligando
- Este artigo trata sobre os ligandos em bioquímica. Para os ligandos em coordenação de metais em química inorgânica, ver Ligante (química inorgânica). :Não confundir com Ligante (aglomerante ou aglutinante)[1][2]
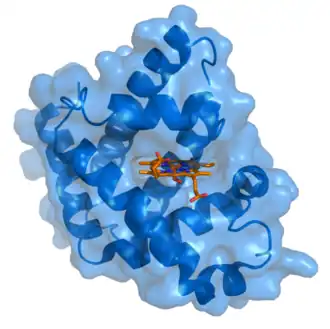
A mioglobina (azul) com o seu grupo prostético heme (laranja) ligado. O oxigénio é o ligando do grupo heme. Baseado em PDB - 1MBO.

Em bioquímica e farmacologia, um ligando[3] (do latim ligare, 'unir') é uma substância que forma um complexo com uma biomolécula (proteína ou ácido nucleico) para realizar uma função biológica, como a estabilização estrutural, catálise, modulação de uma atividade enzimática ou transmissão de um sinal. Na ligação proteína-ligando, o ligando é uma molécula que desencadeia um sinal ao ligar-se a um sítio de ligação na proteína alvo. Entre os ligandos estão, entre outros, os substratos, inibidores enzimáticos, ativadores, hormonas e neurotransmissores. Nos estudos de ligação ADN-ligando, o ligando pode ser uma pequena molécula, ião,[4] ou proteína[5] que se liga à dupla hélice do ADN.
A ligação do ligando ocorre por forças intermoleculares, como ligações iónicas, ligações de hidrogénio e forças de van der Waals. A ligação ou "ancoragem" ao receptor (a associação entre ambos) é geralmente reversível, pelo que a dissociação ocorre posteriormente. É raro nos sistemas biológicos que a ligação ocorra por meio de uma ligação covalente irreversível. Ao contrário do significado que ligando tem em metalorgânica e química inorgânica, em bioquímica é irrelevante que o ligando se ligue a um sítio metálico, mas isso ocorre em alguns casos, como na hemoglobina. Os ligandos podem ligar-se, entre outros, a enzimas, receptores de membrana ou intracelulares, canais iónicos, proteínas de transporte ou armazenamento, proteínas reguladoras, ou anticorpos.
A ligação do ligando a um receptor (proteína receptora) altera a sua forma tridimensional (conformação). O estado conformacional de uma proteína receptora determina o seu estado funcional. A tendência ou força de ligação ao seu receptor é denominada afinidade. A afinidade de ligação é determinada não só pelas interações diretas, mas também pelos efeitos do solvente, que pode ter um efeito indireto dominante na formação de ligações não covalentes na solução.[6] Os radioligandos são compostos rotulados com radioisótopos, que são utilizados in vivo como marcadores nos estudos com tomografia de emissão de positrões (PET) e para estudos de ligação de ligandos in vitro.
Afinidade da ligação entre o receptor e o ligando
As interações da maioria dos ligandos com os seus sítios de ligação podem ser caracterizadas em termos de afinidade de ligação. Em geral, a ligação de alta afinidade de ligandos deve-se a que as forças intermoleculares entre o ligando e o seu receptor são grandes, enquanto a ligação de baixa afinidade do ligando envolve menores forças intermoleculares entre o ligando e o seu receptor. Em geral, a ligação de alta afinidade implica que o ligando permanece mais tempo no seu sítio de ligação no receptor do que quando a afinidade de ligação é baixa. A alta afinidade de ligação dos ligandos aos receptores é muitas vezes importante fisiologicamente quando parte da energia de ligação pode ser utilizada para causar uma mudança conformacional no receptor, o que resulta numa alteração no comportamento de um canal iónico ou enzima associados.
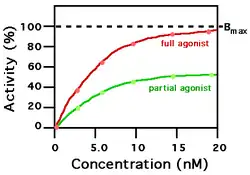
Um ligando que se pode ligar ao seu receptor, que altera a função do receptor e desencadeia uma resposta fisiológica é denominado um agonista para esse receptor. Os agonistas que se ligam a um receptor podem ser caracterizados pela quantidade de resposta fisiológica que é originada e pela concentração do agonista que é necessária para produzir a resposta fisiológica. Quando um ligando tem alta afinidade, isso significa que uma concentração relativamente baixa do ligando é suficiente para uma ocupação máxima do sítio de ligação ao ligando e desencadear uma resposta fisiológica. Quando um ligando tem baixa afinidade, isso significa que é necessária uma concentração relativamente alta do ligando para que o sítio de ligação apresente uma ocupação máxima e haja uma resposta fisiológica máxima. No exemplo do gráfico à direita, dois ligandos diferentes ligam-se ao mesmo sítio de ligação do receptor. Apenas um dos agonistas que se mostram pode estimular ao máximo o receptor e, assim, pode ser definido como um "agonista completo". Um agonista que só pode ativar parcialmente a resposta fisiológica é denominado "agonista parcial". Os ligandos que se ligam a um receptor mas não conseguem ativar a resposta fisiológica são "antagonistas" do receptor. Neste exemplo, a concentração na qual o agonista completo (curva vermelha) pode ativar o receptor à metade do valor máximo é de aproximadamente 5,0 nanomolar.
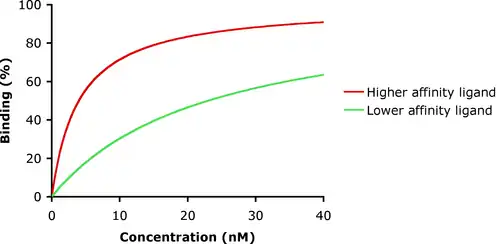
No exemplo à esquerda, são mostradas as curvas de ligação ao ligando para dois ligandos com diferentes afinidades de ligação. O ligando representado pela curva vermelha tem uma maior afinidade de ligação e uma menor constante de dissociação ou Kd do que o ligando representado pela curva verde. Se estes dois ligandos estivessem presentes ao mesmo tempo, ligar-se-ia mais quantidade do ligando de alta afinidade aos sítios de ligação ao receptor disponíveis. É assim que o monóxido de carbono pode competir com o oxigénio para se ligar à hemoglobina, originando um envenenamento por monóxido de carbono. A afinidade de ligação é geralmente determinada utilizando um ligando marcado radioactivamente, o que é conhecido como "ligando quente". Os experimentos de ligação competitiva de homólogos envolvem a competição pelo sítio de ligação entre um "ligando quente" e um "ligando frio" (ligando não marcado).[7] Os métodos sem marcação ou rotulagem, como a ressonância do plasmão de superfície e interferometria de polarização dual podem também quantificar a afinidade a partir de ensaios baseados na concentração, mas também a partir da cinética de associação e dissociação, e, no último caso, a mudança conformacional induzida pela ligação. Recentemente, foi desenvolvida a termoforese em microescala (MST), um método sem imobilização.[8] Este método permite a determinação da afinidade de ligação sem qualquer limitação da massa molecular do ligando.[9] Também é usada a mecânica estatística para o estudo quantitativo da afinidade de ligação ligando-receptor.[10]
Potência do fármaco e afinidade de ligação
Os dados de afinidade de ligação por si sós não determinam a potência global de um fármaco. A potência é o resultado das complexas interações da afinidade de ligação e da eficácia do ligando. A eficácia do ligando refere-se à capacidade do ligando de produzir uma resposta biológica após se ligar ao seu receptor alvo e a medida quantitativa dessa resposta. Esta resposta pode ser como agonista, antagonista, ou agonista inverso, dependendo da resposta fisiológica produzida.[11]
Seletivos e não seletivos
Os ligandos seletivos ligam-se a um ou poucos receptores, enquanto os ligandos não seletivos ligam-se a vários tipos de receptores. Isto é muito importante em farmacologia, já que os fármacos que não são seletivos tendem a apresentar mais efeitos adversos, porque se ligam a vários receptores além do receptor que gera os efeitos desejados.
Ligando bivalente
Os ligandos bivalentes consistem em duas moléculas conectadas. São utilizados em investigação científica para detetar receptores dímeros e investigar as suas propriedades. Os ligandos bivalentes são geralmente grandes e tendem a não ser do "tipo fármaco", o que limita a sua aplicabilidade clínica.[12][13]
Referências
- ↑ Dicionario Digalego ligante Arquivado em 2018-11-25 no Wayback Machine
- ↑ Definições no Dicionário da Real Academia Galega e no Portal das Palavras (em galego) para ligante.
- ↑ Dicionario Digalego ligando Arquivado em 2018-11-25 no Wayback Machine
- ↑ Teif V.B. (2005). «Ligand-induced DNA condensation: choosing the model». Biophysical Journal. 89 (4): 2574–2587. PMC 1366757
 . PMID 16085765. doi:10.1529/biophysj.105.063909
. PMID 16085765. doi:10.1529/biophysj.105.063909
- ↑ Teif VB, Rippe K. (2010). «Statistical-mechanical lattice models for protein-DNA binding in chromatin.». Journal of Physics: Condensed Matter. 22 (41). 414105 páginas. PMID 21386588. doi:10.1088/0953-8984/22/41/414105
- ↑ Baron, Riccardo; Setny, Piotr; Andrew Mccammon, J. (2010). «Water in Cavity-Ligand Recognition». Journal of the American Chemical Society. 132 (34): 12091–12097. PMC 2933114
 . PMID 20695475. doi:10.1021/ja1050082
. PMID 20695475. doi:10.1021/ja1050082
- ↑ Ver Curvas de ligação competitiva de homólogo Arquivado em 2007-12-19 no Wayback Machine, uma guia completa de regressão não linear, curvefit.com.
- ↑ Baaske P, Wienken CJ, Reineck P, Duhr S, Braun D (2010). «Optical Thermophoresis quantifies Buffer dependence of Aptamer Binding». Angew. Chem. Int. Ed. 49 (12): 1–5. PMID 20186894. doi:10.1002/anie.200903998. Resumo divulgativo – Phsyorg.com
- ↑ Wienken CJ; et al. (2010). «Protein-binding assays in biological liquids using microscale thermophoresis». Nature Communications. 1 (7). 100 páginas. Bibcode:2010NatCo...1E.100W. PMID 20981028. doi:10.1038/ncomms1093
- ↑ Vu-Quoc, L., [1], 2011.
- ↑ Kenakin, Terrance P. (2006). A pharmacology primer: theory, applications, and methods. [S.l.]: Academic Press. p. 79. ISBN 978-0-12-370599-0
- ↑ Shonberg, Jeremy; Scammells, Peter J.; Capuano, Ben (2011). «Design strategies for bivalent ligands targeting GPCRs». ChemMedChem. 6 (6): 963–74. PMID 21520422. doi:10.1002/cmdc.201100101
- ↑ Berque-Bestel, I; Lezoualc'h, F; Jockers, R (2008). «Bivalent ligands as specific pharmacological tools for G protein-coupled receptor dimers». Curr Drug Discov Technol. 5 (4): 312–8. PMID 19075611. doi:10.2174/157016308786733591