Mioglobina
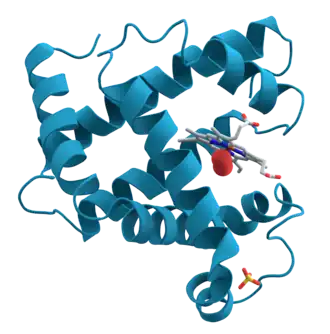
A mioglobina (Mb) é uma proteína globular presente nos vertebrados. Nos humanos, é formada por uma cadeia de 154 aminoácidos. Com um peso molecular de 16.700 daltons, é uma das proteínas mais simples que transporta oxigênio molecular (O2), sendo o principal transportador intracelular de oxigênio nos tecidos musculares, além de estocar oxigênio nos músculos. Entretanto, não realiza o transporte de oxigênio da mesma forma que a hemoglobina - à qual se assemelha estruturalmente. Isto porque, à diferença da hemoglobina, a mioglobina não tem ligações cooperativas com o oxigênio, por ser monomérica, isto é, formada de uma só subunidade.
Contém no seu núcleo porfírico um átomo de ferro. No seu core hidrofóbico, constituído basicamente de aminoácidos apolares, com exceção de duas histidinas, situa-se o grupo prostético hemo. Sua função depende de sua capacidade de ligar-se ao oxigênio e também de liberá-lo quando e onde for necessário. Possui apenas um grupo hemo - planar e "enterrado" em um bolso hidrofóbico.
A principal função da mioglobina é a transportação de oxigênio nos músculos dos mamíferos. É particularmente abundante nos músculos de mamíferos que mergulham como focas e baleias, pois é capaz de reter O2 por longos períodos, enquanto o animal está submerso. Os músculos desses animais possuem uma cor amarronzada devido à grande concentração de mioglobina. A cor vermelha e a abundância da mioglobina em certos músculos ou em certas espécies explicam a diferença da aparência entre carnes brancas e carnes vermelhas.
A mioglobina também está envolvida na degradação do óxido nítrico(NO), molécula muito reativa e oxidante produzido por ocasião do processo de respiração oxidativa. Seu teor no sangue aumenta sempre que há destruição muscular. Após uma lesão isquêmica da fibra muscular, a mioglobina é liberada precocemente na circulação, razão pela qual sua dosagem ajuda o médico no diagnóstico de infarto do miocárdio.[1]
Cor da carne
A Mioglobina contém um grupo hemo, o pigmento responsável pela cor da carne vermelha. A cor que a carne possui é em parte determinada pelo grau de oxidação da mioglobina. Na carne fresca crua, o átomo de ferro está em estado ferroso (Fe²⁺), ligado a uma molécula de dioxigénio O2. A carne cozinhada de forma suficiente é castanha porque o átomo de ferro está agora no estado de oxidação férrico (+3), ao perder um eletrão. Se a carne foi exposta a nitritos, permanece rosa porque o ferro está ligado ao óxido nítrico (NO), como nos presuntos curados. As carnes grelhadas podem adquirir tons rosa originados pela ligação do ferro a uma molécula de monóxido de carbono.[2] A carne crua embalada numa atmosfera de monóxido de carbono também mostra este mesmo fenómeno, e a sua superfície também mostra cor rosa, que é uma cor induzida artificialmente que pode persistir até um ano.[3][4]
Papel em doenças
A mioglobina é libertada dos músculos lesionados (rabdomiólise), que possuem uma concentração muito alta de mioglobina. A mioglobina libertada é filtrada pelos rins, mas é tóxica para o epitélio tubular renal e pode originar uma insuficiência renal aguda.[5] Na realidade, não é a mioglobina que é tóxica em si (é apenas uma pró-toxina), mas sim a porção ferri-hemato (heme + ferro) que se dissocia da mioglobina em ambientes ácidos (por exemplo, urina ácida, lisossomas).
A mioglobina é um marcador sensível que indica lesão muscular, sendo um marcador potencial para o enfarte do miocárdio em pacientes com Dor torácica.[6] No entanto, um nível elevado de mioglobina no sangue tem uma baixa especificidade para o enfarte agudo do miocárdio e outros sinais como a CK-MB, cTnT, ECG e outros sinais clínicos devem ser tidos em conta no diagnóstico.
Estrutura e ligações
A mioglobina pertence à superfamília das proteínas globinas, e como as outras globinas, é constituída por oito hélices alfa ligadas por laços (pregamento de globina). A mioglobina humana contém 154 aminoácidos.[8]
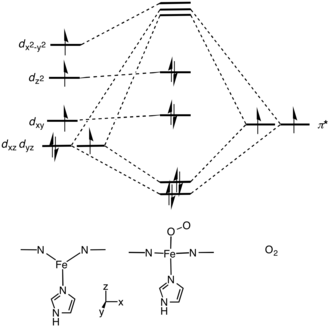
A mioglobina contém um anel porfirínico heme com um ião ferro no seu centro. Um grupo histidina proximal (His-94) está ligado diretamente ao ferro, e outro resíduo de histidina distal (His-65) está por perto na face oposta.[8] O imidazol distal da cadeia lateral da histidina não está ligado ao ferro, mas está disponível para interagir com o substrato O2. Esta interação favorece a ligação do O2, mas não a do monóxido de carbono (CO), o qual, apesar de tudo, se liga com uma força 240 vezes superior à do O2.
A ligação do O2 causa uma mudança estrutural substancial no centro de Fe, que encolhe o seu raio e se move para o centro do bolso N4. A ligação do O2 induz o "acoplamento de spin": a forma ferrosa desóxi do ferro com coordenação cinco tem um spin alto e a forma óxi com coordenação seis é de spin baixo e diamagnética.
Análogos sintéticos
Foram sintetizados muitos modelos de mioglobina como parte do grande interesse que despertaram os complexos de dioxigénio e metal de transição. Um exemplo bem conhecido é a porfirina de cerca de estacas, que consiste num complexo ferroso de um derivado estericamente maciço de tetrafenilporfirina.[9] Na presença de um ligando imidazol, este complexo ferroso liga-se reversivelmente ao O2. O substrato O2 adota uma geometria curvada, ocupando a sexta posição do centro de ferro. Uma propriedade chave deste modelo é a formação lenta do dímero μ-oxo, que é um estado diférrico inativo. Na natureza, estas vias de desativação são suprimidas pela matriz proteica que impede que haja uma aproximação muito estreita das montagens Fe-porfirina.[10]
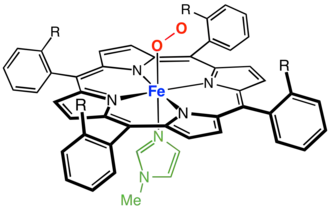
Um complexo de Fe porfirina de cerca de estacas, com os sítios de coordenação axial ocupados por metilimidazol (verde) e dioxigénio. Os grupos R flanqueiam o sítio de ligação do O2.
Referências
- ↑ Mioglobina é o marcador cardíaco que mais precocemente se altera no infarto agudo do miocárdio Arquivado em 17 de setembro de 2009, no Wayback Machine. Fleury Medicina e Saúde, 21 de junho de 2007.
- ↑ McGee H (2004). On Food and Cooking: The Science and Lore of the Kitchen. New York: Scribner. p. 148. ISBN 0-684-80001-2
- ↑ Fraqueza MJ, Barreto AS (Setembro de 2011). «Gas mixtures approach to improve turkey meat shelf life under modified atmosphere packaging: the effect of carbon monoxide». Poult. Sci. 90 (9): 2076–84. PMID 21844276. doi:10.3382/ps.2011-01366
- ↑ Associated Press (30 de outubro de 2007). «Meat companies defend use of carbon monoxide». Business. Minneapolis Star Tribune [ligação inativa] Parâmetro desconhecido
|data-acesso=ignorado (ajuda); Parâmetro desconhecido|url-arquivo=ignorado (ajuda); Parâmetro desconhecido|data-arquivo=ignorado (ajuda) - ↑ Naka T, Jones D, Baldwin I, Fealy N, Bates S, Goehl H, Morgera S, Neumayer HH, Bellomo R (Abril de 2005). «Myoglobin clearance by super high-flux hemofiltration in a case of severe rhabdomyolysis: a case report». Crit Care. 9 (2): R90–5. PMC 1175920
 . PMID 15774055. doi:10.1186/cc3034
. PMID 15774055. doi:10.1186/cc3034
- ↑ Weber M, Rau M, Madlener K, Elsaesser A, Bankovic D, Mitrovic V, Hamm C (Novembro de 2005). «Diagnostic utility of new immunoassays for the cardiac markers cTnI, myoglobin and CK-MB mass». Clin. Biochem. 38 (11): 1027–30. PMID 16125162. doi:10.1016/j.clinbiochem.2005.07.011
- ↑ Drago RS (1980). «Free radical reactions of transition metal systems». Coordination Chemistry Reviews. 32 (2): 97–110. doi:10.1016/S0010-8545(00)80372-0
- ↑ a b UniProt: P02144
- ↑ Collman JP, Brauman JI, Halbert TR, Suslick KS (Outubro de 1976). «Nature of O2 and CO binding to metalloporphyrins and heme proteins». Proc. Natl. Acad. Sci. U.S.A. 73 (10): 3333–7. Bibcode:1976PNAS...73.3333C. PMC 431107
 . PMID 1068445. doi:10.1073/pnas.73.10.3333
. PMID 1068445. doi:10.1073/pnas.73.10.3333
- ↑ Lippard SJ, Berg JM (1994). Principles of Bioinorganic Chemistry. Mill Valley, CA: University Science Books. ISBN 0-935702-73-3