Atividade enzimática

Ensaios enzimáticos são métodos laboratoriais para medir a atividade enzimática. São vitais para o estudo da cinética enzimática e da inibição enzimática. São predominantemente realizados por pesquisadores para identificar a presença ou quantidade de uma enzima específica num organismo, tecido ou amostra. Exemplos de tais enzimas incluem α-amilase, catalase, lacase, peroxidase, lisozima e enzimas fosfatase alcalina e luciferase. Diversos reagentes e metodologias estão amplamente disponíveis, o que permite a investigação de interações específicas enzima-substrato.[1][2][3]
Unidades de Enzima
A quantidade ou concentração de uma enzima pode ser expressa em quantidades molares, igual que com outros compostos químicos, ou em termos de atividade em unidades de enzima.
Atividade Enzimática
A atividade de uma enzima é uma medida da quantidade de enzima ativa presente e é assim dependente de várias condições físicas, as quais deveriam ser especificadas.
É calculada usando a seguinte fórmula:
onde
- = Atividade enzimática
- = Moles de substrato convertidos por unidade de tempo
- = Velocidade da reação
- = Volume de reação
A unidade do SI utilizada é o katal (kat), 1 katal = 1 mol s−1 (mol por segundo), mas esta é uma unidade excessivamente grande. Um valor mais prático e usado é o medido em unidades de enzima (U) = 1 μmol min−1 (micromol por minuto). 1 U corresponde a 16,67 nanokatals.[4]
A atividade enzimática dada em katals geralmente se refere à do substrato alvo considerado natural da enzima. A atividade enzimática pode também ser dada como a que apresenta com certos substratos padrão, como a gelatina, medida então em unidades de digestão de gelatina (GDU, pelas suas siglas em inglês), ou proteínas do leite, medida então em unidades de coagulação do leite (MCU, pelas suas siglas em inglês). As unidades GDU e MCU estão baseadas na rapidez com que um grama da enzima digere a gelatina ou as proteínas do leite, respetivamente. 1 GDU é igual aproximadamente a 1,5 MCU.[2]
O aumento da quantidade de substrato incrementa a velocidade da reação enzimática; porém, uma vez passado certo ponto, a velocidade da reação já não varia porque a quantidade de sítios ativos disponíveis na enzima permanece constante.
Atividade Específica
A atividade específica de uma enzima é outra medida comum. É a atividade de uma enzima por miligrama de proteína total (expresso em μmol min−1 mg−1). A atividade específica dá lugar a uma medida da pureza da enzima na mistura. São os micromoles de produto formados por uma enzima num determinado lapso de tempo (minutos) nas condições dadas por miligrama de proteínas totais. A atividade específica é igual à velocidade de reação multiplicada pelo volume de reação dividido pela massa de proteína total. A unidade do SI é o katal/kg, mas uma unidade mais prática é μmol/(mg*min).
A atividade específica é uma medida da processividade da enzima (a capacidade da enzima de processar), a uma concentração de substrato específica (geralmente saturante), e costuma ser constante para uma enzima pura.
Pode realizar-se um processo de titulação de um sítio ativo eliminando os erros que se originam pelas diferenças no cultivo de lotes e/ou o pregamento incorreto da enzima e outros assuntos similares. Esta é uma medida da quantidade de enzima ativa, calculada por, por exemplo, titulação da quantidade de sítios ativos presentes empregando um inibidor irreversível. A atividade específica deveria então ser expressa como μmol min−1 mg−1 de enzima ativa. Se conhecermos o peso molecular da enzima, o número de recâmbio ou de turnover, ou μmol de produto por segundo por μmol de enzima ativa, pode ser calculado a partir da atividade específica. O número de recâmbio pode ser visualizado como o número de vezes que cada molécula de enzima leva a cabo o seu ciclo catalítico por segundo.
Terminologia Relacionada
A velocidade de uma reação é a concentração de substrato que desaparece (ou de produto produzido) por unidade de tempo (mol L−1 s−1).
A % de pureza é 100 % \times (\text{atividade específica da amostra de enzima / atividade específica de enzima puro}). A amostra impura tem uma menor atividade específica porque parte da massa não é na realidade enzima. Se conhecermos a atividade específica de uma enzima pura a 100 %, então uma amostra impura terá uma menor atividade específica, o que permite calcular a pureza e depois obter um resultado claro.
Tipos de Ensaios
Todos os ensaios de enzimas medem o seu consumo de substrato ou a sua produção de produto com a passagem do tempo. Existem um grande número de métodos de medida das concentrações de substratos e produtos e muitas enzimas podem ser ensaiadas de várias maneiras. Os bioquímicos costumam estudar as reações catalisadas por enzimas usando quatro tipos de experimentos:[5]
- Experimentos de velocidade inicial. Quando se mistura uma enzima com um grande excesso de substrato, acumula-se o intermediário enzima-substrato numa rápida transição. Depois a reação atinge uma cinética de estado estável na qual os intermediários enzima-substrato permanecem aproximadamente constante com o tempo e a velocidade da reação muda de forma relativamente lenta. As velocidades são medidas durante um curto período de tempo depois de alcançar o estado quase estável, normalmente monitorizando a acumulação do produto com o tempo. Como as medidas se realizam durante um curto período de tempo e devido ao grande excesso de substrato, pode fazer-se a aproximação de que a quantidade de substrato livre é aproximadamente igual à quantidade de substrato inicial. O experimento de velocidade inicial é o experimento mais simples de realizar e analisar, estando relativamente livre de complicações como reações revertidas (back-reaction) e a degradação da enzima. É, por tanto, com diferença o tipo de experimento mais utilizado em cinética enzimática.
- Experimentos de curva de progresso. Nestes experimentos, os parâmetros cinéticos são determinados a partir de expressões das concentrações de espécies em função do tempo. A concentração dos substratos ou produtos é registada no tempo depois da rápida transição inicial e por um período o suficientemente longo para permitir que a reação se aproxime ao equilíbrio. Os experimentos de curva de progresso foram muito usados na etapa inicial da cinética enzimática, mas são menos comuns agora.
- Experimentos de cinética transiente. Nestes experimentos, rastreia-se o comportamento da reação durante a transição rápida inicial à medida que o intermediário chega ao período de cinética de estado estável. Estes experimentos são mais difíceis de realizar do que os dois mencionados antes porque requerem técnicas especializadas (como a fotólise flash de compostos aprisionados) ou a mistura rápida (como o fluxo interrompido, fluxo atemperado ou fluxo contínuo).
- Experimentos de relaxação. Nestes experimentos, perturba-se uma mistura em equilíbrio de enzima, substrato e produto, por exemplo por um salto de temperatura, de pressão ou de pH, e monitoriza-se o retorno ao equilíbrio. A análise destes experimentos deve considerar a reação reversível total. Além disso, os experimentos de relaxação são relativamente insensíveis a detalhes da mecânica e não são normalmente usados para a identificação do mecanismo, ainda que possam ser utilizados para isso sob as condições apropriadas.
Os ensaios de enzimas podem ser divididos em dois grupos de acordo com o seu método de amostragem: ensaios contínuos, nos quais o ensaio dá uma leitura contínua da atividade, e ensaios descontínuos, nos quais se tomam as amostras, a reação é detida e depois é determinada a concentração de substratos/produtos.

Ensaios Contínuos
Os ensaios contínuos são os mais convenientes, já que o ensaio dá a velocidade da reação sem que seja necessário nenhum trabalho adicional. Há muitos tipos de ensaios contínuos.
Espectrofotométrico
Em ensaios espectrofotométricos, seguem o curso da reação medindo uma alteração na quantidade de luz que absorve a solução do ensaio. Se esta luz está na região visível pode ver-se uma alteração de cor no ensaio, e estes ensaios denominam-se ensaios colorimétricos. O ensaio MTT, um ensaio redox no qual se usa uma tintura tetrazólio como substrato é um exemplo de ensaio colorimétrico.
Com frequência é usada luz UV, já que as coenzimas comuns NADH e NADPH absorvem luz UV nas suas formas reduzidas, mas não nas suas formas oxidadas. Uma oxidorredutase que usa NADH como substrato pode, portanto, ser ensaiada seguindo o decréscimo na absorvância UV ao comprimento de onda de 340 nm; à medida que o coenzima é consumido.[6]
Ensaios diretos e ensaios acoplados
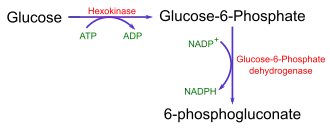
Mesmo quando a reação enzimática não causa uma alteração na absorvância de luz, ainda é possível usar um ensaio espectrofotométrico para a enzima utilizando um ensaio acoplado. Nestes ensaios, o produto de uma reação é utilizado como substrato de outra reação facilmente detetável. Por exemplo, a figura 1 mostra o ensaio acoplado para a enzima hexoquinase, que se pode fazer acoplando a sua produção de glicose 6-fosfato à produção de NADPH, empregando a enzima glicose-6-fosfato desidrogenase.
Fluorométrico
A fluorescência é produzida quando uma molécula emite luz de um comprimento de onda depois de absorver luz de outro comprimento de onda diferente. Os ensaios fluorométricos usam uma diferença na fluorescência do substrato em relação à do produto para medir a reação enzimática. Estes ensaios são em geral muito mais sensíveis do que os ensaios espectrofotométricos, mas podem ter interferências causadas por impurezas e pela inestabilidade de muitos compostos fluorescentes quando expostos à luz.
Um exemplo destes ensaios é outra vez o uso de coenzimas nucleótidos como o NADH e NADPH. As suas formas reduzidas são fluorescentes e as oxidadas não. As reações de oxidação podem, portanto, ser seguidas por uma diminuição na fluorescência, e as reações de redução por um incremento.[7] Também se dispõe de substratos sintéticos que liberam uma tintura fluorescente numa reação catalisada por uma enzima, como o 4-metilumbeliferil-β-D-galactosídeo para ensaiar a β-galactosidase ou o 4-metilumbeliferil-butirato para ensaiar a lipase de Candida rugosa.[8]
Calorimétrico

A calorimetria nos ensaios enzimáticos é a medida do calor liberado ou absorvido pelas reações químicas. Estes ensaios são muito gerais, já que muitas reações envolvem alguma alteração no calor e com o uso de um microcalorímetro não é preciso utilizar muita enzima ou substrato. Estes ensaios podem ser usados para medir reações que são impossíveis de ensaiar de nenhuma outra maneira.[9]
Quimioluminescente
A quimioluminescência é a emissão de luz por uma reação química. Algumas reações enzimáticas produzem luz e isto pode ser medido para detetar a formação de produto. Estes tipos de ensaio podem ser extremamente sensíveis, já que a luz produzida pode ser capturada por uma película fotográfica durante dias ou semanas, mas pode ser difícil de quantificar porque não se vai poder detetar toda a luz liberada pela reação.
A deteção da peroxidase do rábano picante por quimioluminescência enzimática é um método comum de deteção de anticorpos nos western blotting. Outro exemplo é a enzima luciferase, que se encontra em vaga-lumes e produz de forma natural luz a partir do seu substrato luciferina.
Dispersão da Luz
A dispersão da luz estática mede o produto da massa molar ponderada e a concentração de macromoléculas em solução. Dada uma concentração total fixada de uma ou mais espécies no tempo de medida, o sinal de dispersão é uma medida direta da massa molar ponderada da solução, que varia à medida que os complexos se formam ou dissociam. Portanto, as medidas quantificam a estequiometria dos complexos assim como a sua cinética. Os ensaios de dispersão de luz da cinética de proteínas são uma técnica muito geral que não requer uma enzima.
Termoforese à Microescala
A termoforese à microescala (MST, pelas suas siglas em inglês)[10] mede o tamanho, carga e entropia de hidratação de moléculas/substratos no equilíbrio.[11] O movimento termoforético de um substrato rotulado fluorescentemente muda significativamente à medida que é modificado por uma enzima. Esta atividade enzimática pode ser medida com um tempo de resolução alto em tempo real.[12] O consumo de material de todos os métodos ópticos de termoforese à microescala é muito baixo, só se necessitam 5 μL de volume de amostra e uma concentração 10nM de enzima para medir as constantes de velocidade enzimática para a atividade e a inibição. A termoforese à microescala permite medir a modificação de dois substratos diferentes ao mesmo tempo (multiplexação) se ambos os substratos estão rotulados com diferentes fluoróforos. Assim, podem ser realizados experimentos de competição de substratos.
Ensaios Descontínuos
Os ensaios descontínuos são aqueles nos quais as amostras de uma reação enzimática são tomadas a intervalos e é medida a quantidade de produção de produto ou consumo de substrato nestas amostras.
Radiométricos
Os ensaios radiométricos medem a incorporação de radioatividade em substratos ou a sua libertação dos substratos. Os isótopos radioativos que se usam mais frequentemente nestes ensaios são o 14C, o 32P, o 35S e o 125I. Como os isótopos radioativos permitem fazer uma rotulagem específica de um só átomo ou um substrato, estes ensaios são ambos extremamente sensíveis e específicos. São utilizados frequentemente em bioquímica e muitas vezes são a única maneira de medir uma reação específica em extratos crus (as complexas misturas de enzimas produzidas quando se lisam células).
A radioatividade costuma ser medida nestes procedimentos usando um contador de cintilação.
Cromatográfico
Os ensaios cromatográficos medem a formação de produto separando a mistura de reação nos seus componentes por cromatografia. Isto é feito normalmente por cromatografia líquida de alta pressão (HPLC, pelas suas siglas em inglês), mas pode também ser usada a técnica mais simples da cromatografia em camada fina. Embora esta estratégia possa necessitar grande quantidade de material, a sua sensibilidade pode ser incrementada rotulando os substratos/produtos com um marcador radioativo ou fluorescente. A sensibilidade do ensaio também se incrementou alterando os protocolos a instrumentos cromatográficos melhorados (por exemplo, cromatografia líquida de ultra-alta pressão) que funciona a pressão de bomba várias vezes maior que os instrumentos de HPLC (ver Cromatografia líquida de alto rendimento#Bomba de presión).[13]
Fatores que Afetam os Ensaios

Vários fatores afetam o resultado dos ensaios e uma revisão recente resume os diversos parâmetros que se devem monitorizar para realizar corretamente um ensaio.
Concentração de Sais
A maioria das enzimas não podem tolerar concentrações de sais extremamente altas. Os iões interferem com as ligações iónicas fracas das proteínas. As enzimas típicas são ativas a concentrações salinas de 1-500 mM Como é habitual, há exceções como nas algas halófilas e bactérias halófilas.
Efeitos da Temperatura
Todos os enzimas funcionam num intervalo de temperatura específico para o organismo. Os aumentos de temperatura geralmente produzem um incremento da velocidade de reação. Há um limite para este incremento, porque as temperaturas mais altas levam a um brusco decréscimo da velocidade da reação devido à desnaturação (alteração) da estrutura da proteína causada pela rutura de ligações fracas iónicas e de hidrogénio que estabilizavam a estrutura tridimensional do sítio ativo da enzima. A temperatura "ótima" para enzimas humanas costuma estar entre os 35 e os 40 °C. A temperatura média do corpo humano é 37 °C. As enzimas humanas comezan a desnaturar-se rapidamente a temperaturas por cima dos 40 °C. As enzimas das arqueas termófilas encontradas nas fontes termais são estáveis até aos 10040 °C.[14] Porém, a ideia de uma velocidade "ótima" de uma reação enzimática leva a confusão, já que a velocidade observada a qualquer temperatura é o produto de duas velocidades, a velocidade de reação e a velocidade de desnaturação. Se se vai usar um ensaio que meça a atividade durante um segundo, dará uma atividade alta a altas temperaturas, mas se se vai usar um ensaio que meça a formação de produto durante uma hora, dará uma atividade baixa a essas temperaturas.
Efeitos do pH
A maioria das enzimas são sensíveis ao pH e têm intervalos específicos de atividade. Todas têm um pH ótimo. O pH pode parar a atividade enzimática ao desnaturar a forma tridimensional da enzima ao romper ligações iónicas e de hidrogénio. A maioria das enzimas funcionam entre pH 6 e 8; mas a pepsina no estômago funciona melhor a pH 2 e a tripsina a pH 8.
Saturação de Enzima
Incrementar a concentração de substrato incrementa a velocidade da reação (atividade enzimática). Porém, a saturação da enzima limita a velocidade da reação. Uma enzima está saturada quando o sítio ativo de todas as moléculas está ocupado a maior parte do tempo. No ponto de saturação, a reação já não acelera mais, não importa quanto mais substrato seja adicionado. A gráfica da velocidade da reação chega a uma meseta.
Nível de Adensamento
O fato de haver uma grande quantidade de macromoléculas numa solução (está adensada) altera a velocidade da reação e a constante de equilíbrio das reações enzimáticas, por um efeito chamado adensamento macromolecular.[15]
Lista de Ensaios Enzimáticos
- Ensaio MTT (metil tiazol tetrazólio)
- Hidrólise de diacetato de fluoresceína
- para-Nitrofenilfosfato
Referências
- ↑ Nomenclature Committee of the International Union of Biochemistry (NC-IUB) (1979). «Units of Enzyme Activity». European Journal of Biochemistry. 97 (2): 319–20. doi:10.1111/j.1432-1033.1979.tb13116.x

- ↑ a b Rowlett, Russ (23 de novembro de 1998). «How Many? A Dictionary of Units of Measurement». Chapel Hill: University of North Carolina. Arquivado do original em 29 de agosto de 2018
- ↑ Schnell, S.; Chappell, M.J.; Evans, N.D.; Roussel, M.R. (2006). «The mechanism distinguishability problem in biochemical kinetics: The single-enzyme, single-substrate reaction as a case study». Comptes Rendus Biologies. 329 (1): 51–61. PMID 16399643. doi:10.1016/j.crvi.2005.09.005. Consultado em 5 de dezembro de 2023. Cópia arquivada em 26 de fevereiro de 2024
- ↑ Nomenclature Committee of the International Union of Biochemistry (NC-IUB) (1979). «Units of Enzyme Activity». European Journal of Biochemistry. 97 (2): 319–20. doi:10.1111/j.1432-1033.1979.tb13116.x
- ↑ Schnell, Santiago; Chappell, Michael J.; Evans, Neil D.; Roussel, Marc R. (19 de outubro de 2005). «The mechanism distinguishability problem in biochemical kinetics: The single-enzyme, single-substrate reaction as a case study». Comptes Rendus Biologies. 329 (1): 51–61. PMID 16399643. doi:10.1016/j.crvi.2005.09.005
- ↑ Bergmeyer, H.U. (1974). Methods of Enzymatic Analysis. 4. Nova York: Academic Press. pp. 2066–72. ISBN 0-89573-236-X
- ↑ Passonneau, Janet V.; Lowry, Oliver H. (1993). Enzymatic Analysis. A Practical Guide. Totowa NJ: Humana Press. pp. 85–110. ISBN 9780896032385
- ↑ Menden, Ariane (26 de julho de 2019). «A fast, miniaturised in-vitro assay developed for quantification of lipase enzyme activity». Journal of Enzyme Inhibition and Medicinal Chemistry. 34 (1): 1474–1480. PMC 6713963
 . PMID 31414611. doi:10.1080/14756366.2019.1651312
. PMID 31414611. doi:10.1080/14756366.2019.1651312
- ↑ Todd, Matthew J.; Gomez, Javier (setembro de 2001). «Enzyme Kinetics Determined Using Calorimetry: A General Assay for Enzyme Activity?». Analytical Biochemistry. 296 (2): 179–187. PMID 11554713. doi:10.1006/abio.2001.5218
- ↑ Wienken, Christoph J.; Baaske, Philipp; Rothbauer, Ulrich; Braun, Dieter; Duhr, Stefan (19 de outubro de 2010). «Protein-binding assays in biological liquids using microscale thermophoresis». Nature Communications. 1 (1): 100. Bibcode:2010NatCo...1..100W. PMID 20981028. doi:10.1038/ncomms1093
- ↑ Duhr, Stefan; Braun, Dieter (26 de dezembro de 2006). «Why molecules move along a temperature gradient». Proceedings of the National Academy of Sciences. 103 (52): 19678–19682. Bibcode:2006PNAS..10319678D. PMC 1750914
 . PMID 17164337. doi:10.1073/pnas.0603873103
. PMID 17164337. doi:10.1073/pnas.0603873103
- ↑ Asmari, Mufarreh; Michalcová, Lenka; Ibrahim, Adel Ehab; Glatz, Zdeněk; Wätzig, Hermann; El Deeb, Sami (julho de 2023). «Studying molecular interactions via capillary electrophoresis and microscale thermophoresis: A review». Electrophoresis. 44 (13–14): 1114–1142. PMID 37043774. doi:10.1002/elps.202200275
- ↑ Churchwell, M; Twaddle, N; Meeker, L; Doerge, D (25 de outubro de 2005). «Improving LC–MS sensitivity through increases in chromatographic performance: Comparisons of UPLC–ES/MS/MS to HPLC–ES/MS/MS». Journal of Chromatography B. 825 (2): 134–143. PMID 16002352. doi:10.1016/j.jchromb.2005.05.037
- ↑ Cowan, D.A. (novembro de 1997). «Thermophilic proteins: Stability and function in aqueous and organic solvents». Comparative Biochemistry and Physiology Part A: Physiology. 118 (3): 429–438. PMID 9406427. doi:10.1016/S0300-9629(97)00004-2
- ↑ Minton, Allen P. (abril de 2001). «The Influence of Macromolecular Crowding and Macromolecular Confinement on Biochemical Reactions in Physiological Media». Journal of Biological Chemistry. 276 (14): 10577–10580. PMID 11279227. doi:10.1074/jbc.R100005200