Cascavel-do-Mojave
Cascavel-do-Mojave
| |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estado de conservação | |||||||||||||||||||||
 Pouco preocupante (IUCN 3.1) [1] | |||||||||||||||||||||
| Classificação científica | |||||||||||||||||||||
| |||||||||||||||||||||
| Nome binomial | |||||||||||||||||||||
| Crotalus scutulatus (Kennicott, 1861) | |||||||||||||||||||||
| Sinónimos[2] | |||||||||||||||||||||
| |||||||||||||||||||||
Crotalus scutulatus é uma cobra altamente venenosa da família Viperidae, subfamília Crotalinae, encontrada nos desertos do sudoeste dos Estados Unidos e no interior do México. É talvez mais conhecida por produzir dois tipos de veneno distintos em diferentes populações.
É comumente conhecida como cascavel-do-Mojave.[3] Campbell e Lamar (2004) apresentam certa relutância para o nome em inglês Mohave rattlesnake (cascavel-do-Mojave), pois grande parte da distribuição da serpente está fora do deserto de Mojave.[4]
Duas subespécies são atualmente reconhecidas:[5] a subespécie amplamente distribuída Crotalus scutulatus scutulatus[6] e C. scutulatus salvini que ocorre em uma área relativamente pequena no interior do México.[7]
Holótipo e localidade
O holótipo de Crotalus scutulatus é o ANSP 7069, na coleção da Academia de Ciências Naturais da Filadélfia (anteriormente um dos dois espécimes do USNM 5027 no Instituto Smithsonian).[4][8][9] A localidade-tipo é "Fort Buchanan, Arizona". As ruínas de Fort Buchanan estão no atual condado de Santa Cruz, Arizona.[8][10]
Descrição
A Crotalus scutulatus cresce, em média, a um comprimento total (incluindo a cauda) inferior a 100 cm, com um comprimento máximo de 123,6 cm para machos e 92,2 cm para fêmeas.[11][12]
.jpg)
Não há uma única característica visual que identifique confiavelmente a C. scutulatus, e as identificações visuais mais precisas resultam da consideração cuidadosa de múltiplas características. A Crotalus scutulatus é amplamente simpátrica com a C. atrox (cascavel-diamante-ocidental), com a qual se assemelha bastante. A cor dorsal da C. scutulatus varia de tons de verde a marrons, cinzas e até amarelados. C. scutulatus apresenta uma fileira de manchas dorsais em forma de diamante, muito semelhantes às da C. atrox, mas sem a abundante pontuação escura, tanto grossa quanto fina, encontrada nas superfícies dorsais da C. atrox. Além disso, a C. scutulatus não possui as margens brancas nas bordas caudais dos “diamantes” dorsais, presentes na maioria das C. atrox. A faixa facial clara pós-ocular geralmente se inclina em direção ao pescoço e não intersecta com a boca na C. scutulatus, como ocorre na C. atrox. A cauda geralmente apresenta anéis claros e escuros alternados em ambas as espécies, com os anéis escuros frequentemente (mas nem sempre) sendo mais estreitos que os claros na C. scutulatus, e as cores geralmente são menos distintas que os anéis brancos brilhantes e pretos escuros da cauda da maioria das C. atrox. O segmento proximal do chocalho contém tecido vivo e geralmente é bicolor – amarelo e preto, ou totalmente amarelo, na C. scutulatus, mas totalmente preto (às vezes com um toque de branco) na C. atrox.[11][13]
As escamas frontais (entre as supraoculares) da C. scutulatus são relativamente grandes em comparação com outras cascavéis, como a C. atrox (mas veja C. molossus), e as escamas aumentadas se estendem para trás das escamas supraoculares em forma de leque, geralmente com uma margem bem definida. O número mínimo de escamas separando as supraoculares varia de duas a quatro na C. scutulatus. As escamas frontais na C. atrox são geralmente menores, mais numerosas, e não produzem o leque bem definido onde se integram às escamas atrás das frontais.[11][13]
| Comparação das características distintivas mais significativas entre C. scutulatus e outras cascavéis simpátricas comumente encontradas. Adaptado de Cardwell et al. 2022[13] | ||||
| Característica | Crotalus scutulatus | Crotalus atrox | Crotalus molossus* | Crotalus viridis |
| Cor esverdeada | Às vezes | Não | Às vezes | Frequentemente |
| Pontuação no padrão | Pouca ou nenhuma | Evidente, grossa e fina | Pouca ou nenhuma | Pouca ou nenhuma |
| Cor da cauda e anéis caudais | Anéis cinza escuro, preto ou marrom em fundo cinza claro ou branco | Anéis pretos de alto contraste em fundo branco | Cauda uniformemente preta, cinza ou marrom escura, com ocasionais anéis claros fracos | Anéis estreitos escuros e claros, mesmas cores do dorso, com pouco ou nenhum tom esbranquiçado |
| Segmento proximal do chocalho | Amarelo ou bicolor (amarelo e preto) | Preto com ocasional toque de branco | Preto | Preto |
| Faixa pós-ocular clara | Passa acima da boca | Intersecta com a boca | Ausente | Passa acima da boca |
| Escamas frontais | Grandes e irregulares, estendendo-se para a área parietal | Pequenas e granulares, indistintas da área parietal | Grandes e quadradas anteriormente, outras pequenas e uniformes | Pequenas e granulares, indistintas da área parietal |
| * Mesmas características que C. ornatus | ||||
Distribuição geográfica
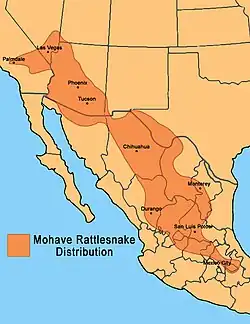
Esta cobra é encontrada em habitats áridos no sudoeste dos Estados Unidos, desde o deserto de Mojave nos condados de Los Angeles e San Bernardino, na Califórnia, através da maior parte do oeste e sul do Arizona (sudoeste da Mogollon Rim [en]), e do condado de El Paso ao sul, através da região de Big Bend, no oeste do Texas. Também ocorre ao norte até o condado de Lincoln, em Nevada, o condado de Washington, no sudoeste de Utah, e porções do extremo sul do Novo México. No México, é encontrada em Sonora, Chihuahua e ao sul, no Planalto Mexicano, até os estados do México, Puebla e Veracruz. É encontrada em desertos e outras áreas com vegetação xérica, desde o nível do mar até cerca de 2.500 m de altitude. Esta cobra também foi observada guardando o cume do Black Butte no Monte Shasta, Califórnia.[4]
Habitat
A Crotalus scutulatus é primariamente habitante de amplos vales desérticos ou encostas montanhosas mais baixas, sendo frequentemente encontrada em áreas com vegetação esparsa contendo predominantemente mato de creosoto (Larrea), sálvia (Ambrosia), algaroba (Prosopis), vários cactos (Cactaceae) e árvores de Josué (Yucca brevifolia), além de bosques de zimbro (Juniperus) e habitats de pastagem (Poaceae) em alguns locais. Em geral, a C. scutulatus tende a evitar áreas densamente vegetadas e extremamente rochosas, preferindo habitats relativamente planos, abertos e xéricos.[4]
Estado de conservação
A C. scutulatus é classificada como Pouco Preocupante (LC) na Lista Vermelha da IUCN de Espécies Ameaçadas (v 3.1, 2001).[14] As espécies são listadas como tal devido à sua ampla distribuição, população presumivelmente grande, ou porque é improvável que estejam diminuindo rapidamente o suficiente para se qualificar para uma categoria mais ameaçada. A tendência populacional era estável quando avaliada em 2007.[15]
Comportamento
A Crotalus scutulatus é mais ativa de abril a setembro. São predadoras de emboscada, alimentando-se principalmente de pequenos roedores e lagartos. O cortejo começa no final do verão/outono, é interrompido pelo inverno e retomado na primavera. As fêmeas dão à luz filhotes vivos, de dois a 17 (média de cerca de oito), de julho a setembro.[16][17][18][19]
Esta espécie não é conhecida por se reunir em tocas comunitárias e não precisa migrar sazonalmente entre tocas de inverno e áreas de forrageamento de verão, como algumas outras espécies que vivem em elevações e latitudes mais altas. Em vez disso, os indivíduos ocupam áreas de vida bem definidas durante todo o ano, abrigando-se durante o inverno e o calor do verão em tocas escavadas por animais como roedores, tartarugas e raposas-anãs.[11][19]
Como outras cascavéis, esta espécie é rotineiramente predada por predadores maiores, como coiotes, linces e aves de rapina. Como resultado, é tímida, críptica e não busca confrontos com criaturas maiores, incluindo humanos. Mas, como outras espécies de cascavéis, ela morde vigorosamente quando perturbada, especialmente se surpreendida ou quando não há vegetação ou toca próxima para onde possa escapar.[11][19]
Análises genéticas e morfológicas recentes
Análises genéticas robustas revelaram a estrutura populacional da C. scutulatus em toda a sua distribuição, correlacionando evidências genéticas de isolamento e contato secundário de subpopulações com eventos geológicos e climáticos correspondentes. Como resultado, quatro clados geneticamente distintos entre as atuais C. scutulatus foram descritos.[20]

A divergência mais antiga ocorreu na margem norte do Planalto Mexicano Central há cerca de 4,1 milhões de anos (MYA), separando a espécie em subpopulações do norte e do sul. Então, há cerca de 1,8 MYA, a subpopulação agora identificada como C. scutulatus salvini divergiu geneticamente dos animais no Planalto Mexicano Central. Mais recentemente, a subpopulação do norte foi dividida na Divisória Continental (Filtro de Cochise) há cerca de 1,5 MYA, criando o clado Mojave-Sonoran a oeste e o clado Chihuahuan a sudeste. Note-se que os limites entre esses clados correspondem a gradientes altitudinais onde mudanças climáticas durante os avanços e recuos glaciais do Pleistoceno provavelmente isolaram as subpopulações durante períodos frios, mas permitiram contato secundário e retomada do fluxo gênico durante períodos mais quentes, incluindo o presente.[20]
Essas análises indicam que o clado do Planalto Mexicano Central está mais próximo (ou seja, compartilhou um ancestral comum mais recentemente) da C. scutulatus salvini do que dos clados do norte (Mojave-Sonoran e Chihuahuan), sugerindo que a designação de salvini como uma subespécie de todas as outras C. scutulatus é problemática.[20]
Mais recentemente, características qualitativas, merísticas e morfométricas de 347 espécimes de C. scutulatus foram analisadas, concluindo que a espécie "é fenotipicamente coesa sem subgrupos discretos, e que a morfologia segue um gradiente contínuo no padrão de cor primário e traços merísticos ao longo do eixo principal de sua ampla distribuição", sugerindo que "múltiplos episódios de isolamento e contato secundário entre metapopulações durante o Pleistoceno foram suficientes para produzir populações genéticas distintas, que desde então experimentaram fluxo gênico para produzir variação clinal em fenótipos sem distinções discretas ou diagnosticáveis entre essas populações originais". Recomendou-se que, para fins taxonômicos, a Crotalus scutulatus "seja mantida como uma única espécie, embora seja possível que a C. s. salvini, que é morfologicamente a população mais distinta, possa representar um isolado periférico nas etapas iniciais de especiação".[23]
Veneno
Histórico
Por décadas, a mordida da C. scutulatus foi considerada extraordinariamente mortal, frequentemente descrita como a (ou “uma das”) cascavéis mais letais ou perigosas. Por exemplo: "o mais letal dos venenos de cascavéis norte-americanas";[24] "um dos venenos mais letais entre os répteis do mundo";[25] "uma serpente extremamente perigosa";[26] "provavelmente a serpente mais perigosa dos Estados Unidos";[27] e “considerada entre as serpentes mais venenosas da Terra”.[28]
Tais alegações são geralmente atribuídas à neurotoxina produzida pela maioria das populações de C. scutulatus nos Estados Unidos e no México, que foi relatada como capaz de causar paralisia respiratória tardia com pouco ou nenhum dano tecidual local. Essa neurotoxina foi isolada e descrita em 1975 e nomeada "toxina de Mojave".[29][30] Em 1978, uma área no centro-sul do Arizona foi identificada onde o veneno da C. scutulatus é significativamente menos letal para camundongos de laboratório do que o veneno do restante da distribuição da espécie. A variante mais letal (e mais amplamente distribuída) foi nomeada "veneno A" e a variante menos letal foi nomeada "veneno B". A diferença na letalidade foi posteriormente determinada pela ausência da toxina de Mojave na população de veneno B. Assim, o veneno A tornou-se conhecido como a variante neurotóxica e o veneno B como a variante não neurotóxica. Além da ausência da toxina de Mojave, o veneno B da C. scutulatus contém toxinas destruidoras de tecidos, predominantemente metaloproteinases, semelhantes aos venenos de muitas outras cascavéis. Alguns animais na zona de intergradação entre as populações de veneno A e B produzem veneno contendo tanto a toxina de Mojave quanto metaloproteinases significativas, sendo rotulados como "veneno A+B".[31][32][33][34][35][36]
Outros estudos observaram que os venenos de crotalíneos podem ser divididos geralmente em dois grupos dicotômicos que foram denominados “toxicidade vs. amaciadores” (neurotóxicos vs. destrutores de tecidos, respectivamente).[37] Os venenos mais tóxicos (letais para camundongos de laboratório) são dominados por neurotoxinas pré-sinápticas (das quais a toxina de Mojave é um homólogo), mas carecem de quantidades significativas de metaloproteinases hemorrágicas e serina proteases, enquanto os venenos “amaciadores” são dominados por componentes hemorrágicos e destrutores de tecidos, mas contêm pouco ou nenhum neurotoxina. No contexto mais amplo de todas os crotalíneos, os venenos mais comuns, contendo níveis mais altos de metaloproteinase e sem neurotoxinas significativas, foram denominados venenos “tipo I”, enquanto os venenos contendo altos níveis de neurotoxinas, mas sem componentes hemorrágicos e destrutores de tecidos, são chamados de “tipo II”.[37][38] Assim, o veneno A da C. scutulatus é um veneno tipo II, e o veneno B é um veneno tipo I.
Toxina de Mojave
A toxina de Mojave é uma potente β-neurotoxina pré-sináptica composta por duas subunidades peptídicas distintas.[39] A subunidade básica de fosfolipase A2 (PLA2) sozinha é levemente tóxica, enquanto a subunidade ácida não é tóxica por si só, mas ambas as subunidades devem estar presentes para constituir a toxina de Mojave. A subunidade básica está presente nos venenos de muitas espécies de Crotalus, incluindo C. adamanteus, C. pyrrhus, C. scutulatus, C. tigris [en] e C. viridis. A subunidade ácida é menos comumente distribuída e limitada a indivíduos em populações que também expressam a subunidade básica.[38][40][41]
Letalidade em humanos
Mortalidade
Estatísticas de mortalidade há muito mostram que há apenas cerca de 2 a 6 pessoas mortas por serpentes venenosas anualmente nos Estados Unidos, com a maioria das mortes relatadas nos estados do sudeste,[42][43] apesar da C. scutulatus ocorrer apenas no sudoeste, onde é comumente encontrada e responsável por muitas mordidas a cada ano. Assim, estatísticas dos Centros de Controle de Doenças[43] e da Associação Americana de Centros de Controle de Envenenamento[42] sugerem que as mordidas da C. scutulatus não são mais letais do que as mordidas de outras espécies de cascavéis.
Paralisia respiratória
A paralisia respiratória foi relatada em animais de laboratório na década de 1930 durante a comparação de venenos de crotalíneos norte-americanos, confirmando a paralisia respiratória e indicando extrema letalidade (ou seja, toxicidade) em pombos causada pelo veneno de C. scutulatus.[44][45][46] Numerosos estudos subsequentes, principalmente usando camundongos, confirmaram a letalidade relativa do veneno A da C. scutulatus em animais de laboratório. Em 1956, Laurence Klauber citou esses estudos em sua referência amplamente lida sobre cascavéis, adicionando “…se testes futuros da qualidade do veneno da C. s. scutulatus corroborarem as cifras de dose letal mediana (m.l.d.) agora disponíveis, esta pode se provar uma cascavel muito perigosa”.[47] Aparentemente por causa desses estudos iniciais em animais, advertências subsequentes abundaram sobre a extrema letalidade e o perigo de paralisia respiratória após mordidas da C. scutulatus.
Estudos clínicos recentes
Investigações recentes de mordidas de cascavéis em regiões onde C. scutulatus é comum lançaram dúvidas sobre a legitimidade das preocupações com extrema letalidade e insuficiência/paralisia respiratória em humanos. Um estudo retrospectivo de 3440 mordidas de cascavéis no Arizona relatadas ao Centro de Informações sobre Venenos e Drogas do Arizona (cobrindo todo o Arizona, exceto o condado de Maricopa) entre janeiro de 1999 e dezembro de 2020, não revelou relatos de insuficiência/paralisia respiratória neurotóxica.[48] Outro estudo retrospectivo de 289 mordidas de cascavéis tratadas em um hospital de referência terciária no condado de Maricopa entre julho de 1994 e novembro de 2000 também não encontrou relatos de insuficiência/paralisia respiratória neurotóxica.[49]
Esses achados publicados são consistentes com relatos anedóticos do sul da Califórnia, onde a C. scutulatus é a cascavel predominante em áreas planas de arbustos de creosoto no deserto de Mojave, onde todos os animais testados até agora expressaram veneno neurotóxico (tipo II/veneno A), e onde a C. atrox simpátrica não está presente para confundir a identificação da serpente. Uma busca na literatura por relatos de casos publicados (que não foi limitada em escopo, nem geograficamente nem temporalmente)[48] revelou apenas um caso de insuficiência respiratória neurotóxica.[50]
Embora os efeitos fisiológicos da toxina de Mojave sejam quase certamente dependentes da dose, muitas outras variáveis afetam como um organismo (pombo, camundongo de laboratório, esquilo, humano, etc.) é afetado, incluindo fatores como massa corporal do organismo, idade, saúde, comorbidades, alergias, perfil genético e muitos outros.
Prognóstico das vítimas de mordida
Embora a C. scutulatus seja capaz de infligir uma mordida potencialmente fatal, o prognóstico das vítimas de mordidas da C. scutulatus parece não ser pior do que o das vítimas mordidas por outras cascavéis de tamanho semelhante. Fatores que pioram o prognóstico de mordidas de víboras incluem atraso em alcançar cuidados médicos avançados, tamanho pequeno da vítima e tamanho grande da cobra.[48][51]
Soros antiofídicos
Ambos os soros antiofídicos disponíveis nos Estados Unidos são licenciados pela Administração de Alimentos e Medicamentos dos EUA para o tratamento de mordidas por todos os crotalíneos nativos, incluindo envenenamentos pela C. scutulatus.[52][53] Cada produto contém anticorpos produzidos contra os venenos de várias espécies cuidadosamente selecionadas. O veneno neurotóxico da C. scutulatus é usado na fabricação do CroFab®, enquanto o veneno de uma cascavel-mesoamericana ( C. simus) que expressa uma neurotoxina muito semelhante é usado na produção do Anavip®. Assim, ambos os produtos são projetados para serem eficazes contra envenenamentos neurotóxicos de C. scutulatus, e os venenos de outras espécies usados na produção de ambos os produtos são protetores contra mordidas de C. scutulatus tipo I/veneno B (não neurotóxico).
Subespécies
| Subespécie[5] | Autor taxonômico[5] | Distribuição geográfica[4] |
|---|---|---|
| C. scutulatus salvini | Günther, 1895 | México, de Hidalgo através de Tlaxcala e Puebla até o sudoeste de Veracruz |
| C. scutulatus scutulatus | Kennicott, 1861 | Estados Unidos, da Califórnia até o oeste do Texas e ao sul até Querétaro, no México |
O nome subespecífico, salvini, é em homenagem ao herpetologista inglês Osbert Salvin.[54]
Referências
- ↑ Mendoza-Quijano, F.; Hammerson, G.A. (2007). «Crotalus scutulatus». Lista Vermelha de Espécies Ameaçadas. 2007: e.T64332A12771270. doi:10.2305/IUCN.UK.2007.RLTS.T64332A12771270.en
 . Consultado em 16 de julho de 2025
. Consultado em 16 de julho de 2025
- ↑ McDiarmid RW, Campbell JA, Touré TA (1999). Snake Species of the World: A Taxonomic and Geographic Reference, vol. 1. Washington, District of Columbia: Herpetologists' League. 511 pp. ISBN 1-893777-00-6 (série). ISBN 1-893777-01-4 (volume).
- ↑ «Cascavel-do-Mojave (Crotalus scutulatus)». iNaturalist. Consultado em 16 de julho de 2025
- ↑ a b c d e Campbell JA, Lamar WW (2004). The Venomous Reptiles of the Western Hemisphere. Ithaca and London: Comstock Publishing Associates. 870 pp., 1,500 plates. ISBN 0-8014-4141-2.
- ↑ a b c «Crotalus scutulatus (Kennicott, 1861)». Integrated Taxonomic Information System. Consultado em 16 de julho de 2025
- ↑ Crother, BI; Bonett, RM; Boundy, J; Burbrink, FT; de Queiroz, K; Frost, DR; Highton, R; Iverson, JB; Jockusch, EL (2017). Scientific and Standard English names of Amphibians and reptiles of North America North of Mexico, With Comments Regarding Confidence in Our Understanding (PDF) 8th ed. [S.l.]: Society for the Study of Amphibians and Reptiles. pp. 64–65. ISBN 978-1-946681-00-3
- ↑ Gloyd, HK (1940). The Rattlesnakes – Genera Crotalus and Sistrurus. [S.l.]: Chicago Academy of Sciences. pp. 201–202
- ↑ a b Cardwell, MD; Gotte, SW; McDiarmid, RW; Gilmore, N; Poindexter, JA (2013). «Type specimen of Crotalus scutulatus (Chordata: Reptilia: Squamata: Viperidae) re-examined, with new evidence after more than a century of confusion». Proceedings of the Biological Society of Washington. 126 (1): 11–16. doi:10.1111/j.1469-7998.2007.00358.x
- ↑ McDiarmid, RC; Campbell, JA; Touré, TA (1999). Snake Species of the World. 1.. [S.l.]: The Herpetologists' League. pp. 293–295. ISBN 1-893777-01-4
- ↑ Cope, ED (1900). «The crocodilians, lizards, and snakes of North America». Annual Report of the Board of Regents of the Smithsonian Institution. [S.l.]: U.S. Government Printing Office. pp. 1158–1160
- ↑ a b c d e Cardwell, Mike (2020). The Mohave Rattlesnake and How It Became an Urban Legend. Rodeo, New Mexico: ECO Publishing. ISBN 978-1-938850-30-1
- ↑ Mrinalini; Hicks, JJ; Wüster, W (2016). «Crotalus scutulatus (Mohave Rattlesnake). Maximum size.». Herpetological Review. 46 (2): 271
- ↑ a b c Cardwell, M; Massey, D; Wüster, W (2022). «Mohave Rattlesnake (Crotalus scutulatus) Identification Revisited». Wilderness and Environmental Medicine. 33 (2): 210–218. PMID 35221167. doi:10.1016/j.wem.2022.01.003
 – via Elsevier Science Direct
– via Elsevier Science Direct
- ↑ Mendoza-Quijano, F. & Hammerson, G.A. (1 de março de 2007). «IUCN Red List of Threatened Species: Crotalus scutulatus». IUCN Red List of Threatened Species. Consultado em 16 de julho de 2025
- ↑ IUCN Red List categories and criteria, version 3.1, 2nd edition. [S.l.: s.n.] 2012. ISBN 978-2-8317-1435-6. Consultado em 16 de julho de 2025
- ↑ Klauber LM (1997). Rattlesnakes: Their Habitats, Life Histories, and Influence on Mankind. Second Edition. First printing in 1972. Berkeley: University of California Press. ISBN 0-520-21056-5.
- ↑ Schuett, GW; Carlisle, SL; Holycross, AT; O'Leile, JK; Hardy, DL; Van Kirk, EA; Murdoch, WJ (2002). «Mating system of male Mojave rattlesnakes (Crotalus scutulatus): Seasonal timing of mating, agonistic behavior, spermatogenesis, sexual segment of the kidney, and plasma sex steroids». In: Schuett, GW; Höggren, M; Douglas, ME; Greene, HW. Biology of the Vipers. [S.l.]: Eagle Mountain Publishing. pp. 515–532. ISBN 0-9720154-0-X
- ↑ Cardwell, MD (2008). «The reproductive ecology of Mohave rattlesnakes». Journal of Zoology. 274 (1): 65–76. doi:10.1111/j.1469-7998.2007.00358.x
- ↑ a b c Cardwell, MD (2016). «Mohave rattlesnake Crotalus scutulatus (Kennicott 1861)». In: Schuett; Feldner, MJ; Smith, CF; Reiserer, RS. Rattlesnakes of Arizona. 1 GW ed. Rodeo, New Mexico: ECO Publishing. pp. 563–605. ISBN 978-1-938850-18-9
- ↑ a b c Schield, Drew R.; Adams, Richard H.; Card, Daren C.; Corbin, Andrew B.; Jezkova, Tereza; Hales, Nicole R.; Meik, Jesse M.; Perry, Blair W.; Spencer, Carol L.; Smith, Lydia L.; García, Gustavo Campillo; Bouzid, Nassima M.; Strickland, Jason L.; Parkinson, Christopher L.; Borja, Miguel (2018). «Cryptic genetic diversity, population structure, and gene flow in the Mojave rattlesnake (Crotalus scutulatus)». Molecular Phylogenetics and Evolution. 127: 669–681. Bibcode:2018MolPE.127..669S. ISSN 1055-7903. PMID 29902574. doi:10.1016/j.ympev.2018.06.013
- ↑ Cardwell, Mike (2020). The Mohave Rattlesnake and How It Became an Urban Legend. Rodeo, New Mexico: ECO Publishing. ISBN 978-1-938850-30-1
- ↑ Schield, Drew R.; Adams, Richard H.; Card, Daren C.; Corbin, Andrew B.; Jezkova, Tereza; Hales, Nicole R.; Meik, Jesse M.; Perry, Blair W.; Spencer, Carol L.; Smith, Lydia L.; García, Gustavo Campillo; Bouzid, Nassima M.; Strickland, Jason L.; Parkinson, Christopher L.; Borja, Miguel (2018). «Cryptic genetic diversity, population structure, and gene flow in the Mojave rattlesnake (Crotalus scutulatus)». Molecular Phylogenetics and Evolution. 127: 669–681. Bibcode:2018MolPE.127..669S. ISSN 1055-7903. PMID 29902574. doi:10.1016/j.ympev.2018.06.013
- ↑ WATSON, JESSICA A.; SPENCER, CAROL L.; SCHIELD, DREW R.; BUTLER, BRETT O.; SMITH, LYDIA L.; FLORES-VILLELA, OSCAR; CAMPBELL, JONATHAN A.; MACKESSY, STEPHEN P.; CASTOE, TODD A.; MEIK, JESSE M. (7 de outubro de 2019). «Geographic variation in morphology in the Mohave Rattlesnake (Crotalus scutulatus Kennicott 1861) (Serpentes: Viperidae): implications for species boundaries». Zootaxa. 4683 (1): 129–143. ISSN 1175-5334. PMID 31715939. doi:10.11646/zootaxa.4683.1.7
- ↑ Russell, FE (1969). «Clinical aspects of snake venom poisoning in North America». Toxicon. 7 (1): 33–37. Bibcode:1969Txcn....7...33R. PMID 5804764. doi:10.1016/0041-0101(69)90160-3 – via Elsevier
- ↑ Wingert, WA; Chan, L (1988). «Rattlesnake bites in southern California and rationale for recommended treatment». Western Journal of Medicine. 148 (1): 37–44. PMC 1026007
 . PMID 3277335
. PMID 3277335
- ↑ Stebbins, R.C. (2003). A Field Guide to Western Reptiles and Amphibians. Boston: Houghton Mifflin & Co. pp. 416–417. ISBN 0-395-98272-3
- ↑ Ernst, CH; Ernst, EM (2012). Venomous Reptiles of the United States, Canada, and Northern Mexico. 2. Baltimore: Johns Hopkins University Press. pp. 218–232. ISBN 978-0-8018-9876-1
- ↑ Jones, LLC (2022). Venomous Animals of the United States and Mexico. Tucson: Rio Nuevo Publishers. pp. 435–440. ISBN 978-1940322087
- ↑ Bieber, AL; Tu, T; TU, AT (1975). «Studies of an acidic cardiotoxin isolated from the venom of Mojave rattlesnake (Crotalus scutulatus)». Biochimica et Biophysica Acta (BBA) - Protein Structure. 400 (1): 178–188. PMID 238654. doi:10.1016/0005-2795(75)90139-7 – via Elsevier
- ↑ Ho, C.L.; Lee, C.Y. (1981). «Presynaptic actions of Mojave toxin isolated from Mojave rattlesnake (Crotalus scutulatus) venom». Toxicon. 19 (6): 889–892. Bibcode:1981Txcn...19..889H. ISSN 0041-0101. PMID 7336451. doi:10.1016/0041-0101(81)90086-6
- ↑ Glenn, J.L.; Straight, R. (1978). «Mojave rattlesnake Crotalus scutulatus scutulatus venom: variation in toxicity with geographical origin». Toxicon. 16 (1): 81–84. Bibcode:1978Txcn...16...81G. ISSN 0041-0101. PMID 622731. doi:10.1016/0041-0101(78)90065-x
- ↑ Glenn, James L.; Straight, Richard C.; Wolfe, Martha C.; Hardy, David L. (1983). «Geographical variation in Crotalus scutulatus scutulatus (Mojave rattlesnake) venom properties». Toxicon. 21 (1): 119–130. Bibcode:1983Txcn...21..119G. ISSN 0041-0101. PMID 6342208. doi:10.1016/0041-0101(83)90055-7
- ↑ Glenn, James L.; Straight, Richard C. (1989). «Intergradation of two different venom populations of the Mojave rattlesnake (Crotalus scutulatus scutulatus) in Arizona». Toxicon. 27 (4): 411–418. Bibcode:1989Txcn...27..411G. ISSN 0041-0101. PMID 2499081. doi:10.1016/0041-0101(89)90203-1
- ↑ Wilkinson, JA; Glenn, JL; Straight, RC; Sites, JW (1991). «Distribution and generic variation in venom A and B populations of the Mojave rattlesnake (Crotalus scutulatus scutulatus) in Arizona». Herpetologica. 47 (1): 54–68. JSTOR 3892815
- ↑ Massey, DJ; Calvete, JJ; Sanchez, EE; Sanz, L; Richards, K; Curtis, R; Boesen, K (2012). «Venom variability and envenoming severity outcomes of the Crotalus scutulatus scutulatus (Mojave Rattlesnake) from Southern Arizona». Journal of Proteomics. 75 (9): 2576–2587. PMID 22446891. doi:10.1016/j.jprot.2012.02.035 – via Elsevier Science Direct
- ↑ Zancolli, G; Calvete, JJ; Cardwell, MD; Greene, HW; Hayes, WK; Hegarty, MJ; Herrmann, HW; Holycross, AT; Lannutti, DI; Mulley, JF; Sanz, L; Travis, ZD; Whorley, JR; Wüster, CE; Wüster, W (2019). «When one phenotype is not enough: divergent evolutionary trajectories govern venom variation in a widespread rattlesnake species». Proceedings of the Royal Society B: Biological Sciences (em inglês). 286 (1898). 20182735 páginas. ISSN 0962-8452. PMC 6458317
 . PMID 30862287. doi:10.1098/rspb.2018.2735
. PMID 30862287. doi:10.1098/rspb.2018.2735
- ↑ a b Mackessy, Stephen P. (2010). «Evolutionary trends in venom composition in the Western Rattlesnakes (Crotalus viridis sensu lato): Toxicity vs. tenderizers». Toxicon. 55 (8): 1463–1474. Bibcode:2010Txcn...55.1463M. ISSN 0041-0101. PMID 20227433. doi:10.1016/j.toxicon.2010.02.028
- ↑ a b Mackessy, SP (2008). «Venom composition in rattlesnakes: Trends and biological significance». In: Hayes, WK; Beaman, KR; Cardwell, MD; Bush, SP. The Biology of Rattlesnakes. [S.l.]: Loma Linda University Press. pp. 495–510. ISBN 978-159410-011-6
- ↑ Aird, S.D. et al. (1985). "Rattlesnake presynaptic neurotoxins: primary structures and evolutionary origin of the acidic subunit". Biochemistry 24: 7054–7058.
- ↑ Powell, RL; Lieb, CS; Rael, ED (2008). «Geographic distribution of Mojave toxin and Mojave toxin subunits among selected Crotalus species». In: Hayes, WK; Beaman, KR; Cardwell, MD; Bush, SP. The Biology of Rattlesnakes. [S.l.]: Loma Linda University Press. pp. 537–550. ISBN 978-159410-011-6
- ↑ Mackessy, SP (2021). «Reptile venoms and toxins – Unlimited opportunities for basic and applied research». In: Mackessy, SP. Handbook of Venoms and Toxins of Reptiles 2 ed. Boca Raton: CRC Press. pp. 3–18. ISBN 978-0367149741
- ↑ a b Greene, SC; Folt, J; Wyatt, K; Brandehoff, NP (2021). «Epidemiology of fatal snakebites in the United States 1989–2018». The American Journal of Emergency Medicine. 45: 309–316. ISSN 0735-6757. PMID 33046301. doi:10.1016/j.ajem.2020.08.083
- ↑ a b Forrester, JA; Weiser, TG; Forrester, JD (2018). «An Update on Fatalities Due to Venomous and Nonvenomous Animals in the United States (2008–2015)». Wilderness & Environmental Medicine. 29 (1): 36–44. ISSN 1080-6032. PMID 29373216. doi:10.1016/j.wem.2017.10.004
- ↑ Githens, TS (1935). «Studies on the venoms of North American pit vipers». The Journal of Immunology. 29 (2): 165–173. ISSN 0022-1767. doi:10.4049/jimmunol.29.2.165
- ↑ Githens, TS; Wolff, NO (1939). «The Polyvalency of Crotalidic Antivenins I. The influence of the composition of polyvalent antigens». The Journal of Immunology. 37 (1): 33–39. ISSN 0022-1767. doi:10.4049/jimmunol.37.1.33
- ↑ Githens, TS; Wolff, NO (1939). «The Polyvalency of Crotalidic Antivenins III. Mice as test animals for study of antivenins». The Journal of Immunology. 37 (1): 47–51. ISSN 0022-1767. doi:10.4049/jimmunol.37.1.47
- ↑ Klauber, LM (1956). Rattlesnakes - Their Habits, Life Histories and Influence on Mankind. 2. [S.l.]: University of California Press. 788 páginas
- ↑ a b c Smelski, G; Cardwell, M; Larsen, J (2023). «Neurotoxic respiratory failure absent following Arizona rattlesnake bites». Toxicon (em inglês). 224. 107034 páginas. Bibcode:2023Txcn..22407034S. PMID 36690088. doi:10.1016/j.toxicon.2023.107034

- ↑ Brooks, DE; Graeme, KA; Ruha, AM; Tanen, DA (2002). «Respiratory compromise in patients with rattlesnake envenomation». The Journal of Emergency Medicine. 23 (4): 329–332. ISSN 0736-4679. PMID 12480008. doi:10.1016/s0736-4679(02)00573-5
- ↑ Jansen, PW; Perkin, RM; Van Stralen, D (1992). «Mojave rattlesnake envenomation: Prolonged neurotoxicity and rhabdomyolysis». Annals of Emergency Medicine. 21 (3): 322–325. ISSN 0196-0644. PMID 1536496. doi:10.1016/s0196-0644(05)80898-4
- ↑ Gerardo, CJ; Vissoci, JRN; Evans, CS; Simel, DL; Lavonas, EJ (2019). «Does This Patient Have a Severe Snake Envenomation?: The Rational Clinical Examination Systematic Review». JAMA Surgery (em inglês). 154 (4): 346–354. ISSN 2168-6254. PMID 30758508. doi:10.1001/jamasurg.2018.5069
- ↑ «CroFab | Copperhead, Cottonmouth, and Rattlesnake Antivenom | CroFab.com». crofab.com. Consultado em 16 de julho de 2025
- ↑ «ANAVIP Home». ANAVIP® [crotalidae immune F(ab’)₂ (equine)] (em inglês). Consultado em 16 de julho de 2025
- ↑ Beolens, Bo; Watkins, Michael; Grayson, Michael (2011). The Eponym Dictionary of Reptiles. Baltimore: Johns Hopkins University Press. xiii + 296 pp. ISBN 978-1-4214-0135-5. (Crotalus scutulatus salvini, p. 232).