Diferenciação celular
Na biologia do desenvolvimento, diferenciação é o processo no qual as células vivas se "especializam", gerando uma diversidade celular capaz de realizar determinadas funções.
Estas células diferenciadas podem atuar isoladamente - como os gametas e as células sexuais dos organismos menores, como as bactérias. Ou podem agrupar-se em tecidos diferenciados, como o tecido ósseo e o muscular. Apesar de diferenciadas, as células mantêm o mesmo código genético da primeira célula (zigoto). A diferença está na ativação e inibição de grupos específicos de genes que determinarão a função de cada célula.
Esta especialização acarreta não só alterações da função, mas também da estrutura das células.
Este "agrupamento" foi realizado ao longo do processo evolutivo. A seguir, os metazoários "agruparam" diversos tecidos para formar órgãos diferenciados como o estômago, os órgãos sexuais etc. Estes, por sua vez, podem estar agrupados em aparelhos ou sistemas que, em conjunto, realizam determinada função vital, como é o caso do sistema digestivo.
O processo inverso também pode ocorrer. Células já especializadas, por algum motivo, podem perder a sua função, assumindo um estado de crescimento exagerado. Esse processo é denominado desdiferenciação e é o que ocasiona o surgimento de neoplasias.
Estágios da Diferenciação Celular
As mudanças que ocorrem na célula não são imediatas, mas são precedidas pelo processo de compromisso celular, na qual a célula possui um destino determinado e passará por grandes alterações. Assim, mesmo que uma célula ou tecido não sejam diferentes fenotipicamente das outras células ou tecidos que estão em estado de não comprometimento, o seu destino de desenvolvimento já está restrito.
O processo de compromisso celular pode ser dividido em dois estágios (Harrison 1933; Slack 1991). O primeiro é uma fase instável chamado de especificação. O destino da célula ou tecido é considerado especificado quando este é capaz de se diferenciar autonomamente em ambiente neutro (o ambiente é neutro em relação à via de desenvolvimento), como uma placa de Petri ou um tubo de ensaio. E ainda nesse estágio, o compromisso pode ser revertido. O segundo estágio de compromisso é a determinação. Uma célula ou tecido pode ser chamada de determinada quando é capaz de se diferenciar autonomamente mesmo quando é colocado em outra região do embrião. Se for capaz de diferenciar de acordo com o destino original, mesmo sob essas circunstâncias, pode-se assumir que o compromisso é irreversível.[1]
Especificação autônoma
Três modos básicos de compromisso foram descritos. O primeiro é chamado de especificação autônoma. Neste caso, se um blastômero particular for removido de um embrião no início do desenvolvimento, esse blastômero isolado irá produzir os mesmos tipos celulares que ele produziria se ainda fosse parte do embrião. E mais ainda, o embrião de onde foi retirado o blastômero perderá essas células e somente essas células, que seriam produzidas pelo blastômero retirado. A especificação autônoma dá origem a um padrão na embriogênese chamado de mosaico do desenvolvimento, pois o embrião parece uma construção de mosaico de peças independentes, com partes capazes de se auto-diferenciar. Embriões de invertebrados (especialmente de moluscos, anelídeos, e tunicados), geralmente possuem especificação autônoma para determinar o destino de suas células. Nesses embriões, determinantes morfogenéticos (certas proteínas ou RNAs mensageiros) são postos em diferentes regiões do citoplasma do ovo e são divididos em diferentes células de acordo com a divisão do embrião, sendo que os determinantes morfogenéticos especificam o tipo celular.
Especificação sincicial
Em embriões iniciais de insetos, a divisão celular não está completa. O núcleo se divide dentro do citoplasma do ovo, criando um multinucleado dentro do ovo. Um citoplasma que contém vários núcleos é chamado de sincício. O ovo citoplasmático, no entanto, não é uniforme. Em vez disso, o citoplasma do ovo anterior é marcadamente diferente do posterior. Aqui, a interação da especificação sincicial ocorre entre as diferentes partes de uma mesma célula, mas não entre elas.
Embriologistas experimentais mostraram que cada núcleo de Drosophila tem uma informação posicional dado por proteínas chamadas de morfógenos (do grego “doador de forma”).
Especificação condicional
O terceiro modo de comprometimento envolve interações entre células vizinhas. Neste tipo de especificação, cada célula tem, originalmente, a habilidade de se tornar qualquer uma dentre tantos tipos celulares. Entretanto, as interações de uma célula com outras células restringem o destino de uma ou mais participantes. Esse modo de comprometimento é chamado de especificação condicional porque o destino da célula depende das condições em que se encontra.
Se um blastômero for removido de um embrião, no início do desenvolvimento, que utiliza a especificação condicional, as células embrionárias remanescentes alteram seus destinos de modo que as funções das células que faltam sejam retomadas. Essa habilidade que células embrionárias têm de modificar seus destinos para compensar as partes que faltam é chamada de regulação. O blastômero isolado pode também dar origem a uma grande variedade de células (até gerar tipos celulares que a célula não faria se ainda fosse parte do embrião). Assim, a especificação condicional gera um padrão chamado de desenvolvimento regulador. O desenvolvimento regulador é visto na maioria dos embriões de vertebrados, e é crítico no desenvolvimento de gêmeos idênticos. Na formação dos gêmeos, as células no estágio de clivagem de um único embrião se divide em dois grupos, e cada grupo de células produz um indivíduo totalmente desenvolvido.
Mecanismos
Cada tipo celular especializado de um organismo expressa um subconjunto de todos os genes do seu genoma. Cada tipo celular define-se pelo seu padrão particular de regulação da expressão génica. A diferenciação celular é assim uma transição da célula de um tipo para outro e implica uma mudança de um padrão de expressão génica para outro.
A diferenciação celular durante o desenvolvimento pode ser entendida como o resultado de uma rede reguladora de genes. Um gene regulador e os seus módulos cis-reguladores são nós nesta rede reguladora de genes, que recebem sinais de entrada (input) e geram sinais de saída (output) noutras partes da rede.[1] A abordagem feita pela biologia de sistemas à biologia do desenvolvimento sublinha a importância de investigar o modo como interagem os mecanismos de desenvolvimento para produzir padrões previsíveis (morfogénese).
No entanto, propôs-se recentemente uma visão alternativa, baseada na expressão génica estocástica, na qual a diferenciação celular é o resultado de um processo de pressão seletiva darwiniana que ocorre entre as células. Neste quadro, as redes de genes e proteínas são o resultado de processos celulares e não a sua causa. Ver: darwinismo celular Arquivado em 2010-08-04 no Wayback Machine.
Geralmente, os processos celulares conservados evolutivamente implicados nos mecanismos celulares que controlam estas mudanças são apenas de alguns tipos. Os principais tipos de processos celulares que controlam a diferenciação celular baseiam-se na sinalização celular.
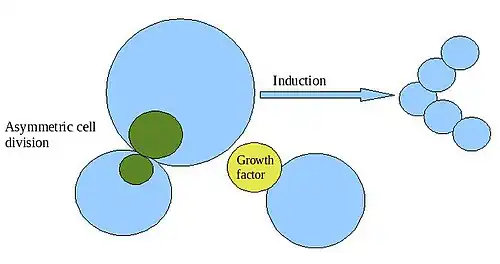
Muitas das moléculas sinalizadoras que transmitem informação de célula a célula durante o controlo da diferenciação celular denominam-se factores de crescimento. Embora os detalhes das vias de transdução de sinais específicas variem, estas vias partilham frequentemente as seguintes etapas gerais: Um ligando produzido por uma célula liga-se a um recetor no lado extracelular de outra célula, induzindo uma alteração conformacional no recetor. A forma do domínio citoplasmático do recetor muda, e o recetor adquire uma actividade enzimática. O recetor depois catalisa reacções que fosforilam outras proteínas, activando-as. Uma cascata de reacções de fosforilação activa finalmente um factor de transcrição dormente ou proteína citoesquelética, contribuindo assim para o processo de diferenciação na célula-alvo.[2]
As células e os tecidos podem variar em competência, isto é, na sua capacidade de responderem a sinais externos.[3]
A indução de sinais refere-se às cascatas de eventos de sinalização, durante os quais a célula ou os sinais dos tecidos são enviados a outra célula ou tecido para influenciar o seu desenvolvimento.[3] Yamamoto e Jeffery[4] investigaram o papel do cristalino na formação dos olhos dos peixes que habitam em cavernas e na superfície, que é um exemplo claro de indução.[3] Por meio de transplantes recíprocos, Yamamoto e Jeffery[4] verificaram que a vesícula do cristalino dos peixes de superfície pode induzir o desenvolvimento de outras partes do olho tanto nos peixes moradores de cavernas como de superfície, enquanto a vesícula do cristalino dos peixes de cavernas não o consegue fazer.[3]
Outro importante mecanismo enquadra-se na categoria das divisões celulares assimétricas, divisões que dão lugar a células-filhas com destinos de desenvolvimento distintos. As divisões celulares assimétricas podem ocorrer por causa de determinantes citoplasmáticos maternos expressos assimetricamente ou devido a sinalização.[3]
No primeiro destes mecanismos, criam-se células-filhas distintas durante a citocinese devido a uma distribuição desigual de moléculas reguladoras na célula progenitora; o citoplasma diferente que herda cada célula-filha dá lugar a um padrão distinto de diferenciação em cada uma. Um exemplo bem estudado de formação de padrão por divisão celular assimétrica é o padrão do eixo corporal de Drosophila.
As moléculas de ARN são um importante tipo de sinal de controlo intracelular da diferenciação. A base genética e molecular das divisões celulares assimétricas também foi estudada nas algas verdes do género Volvox, um sistema modelo para estudar como os organismos unicelulares podem evoluir para organismos pluricelulares.[3] Na espécie Volvox carteri, as 16 células do hemisfério anterior de um embrião de 32 células dividem-se assimetricamente, produzindo cada uma uma célula-filha grande e outra pequena. O tamanho da célula no final de todas as divisões celulares determina se esta se converterá numa célula germinal especializada ou numa célula somática.[3][5]
Controlo epigenético da diferenciação celular
Como cada célula de um organismo, independentemente do tipo, tem o mesmo genoma, a determinação do tipo celular deve ocorrer ao nível da expressão dos genes. Embora a regulação da expressão génica possa ocorrer por meio de elementos cis- ou trans-reguladores, como são os promotores e amplificadores (enhancers) dos genes, surge o problema de como se mantém este padrão de expressão ao longo de numerosas gerações de divisão celular.
Os processos epigenéticos desempenham um papel fundamental na regulação da decisão de destinar uma célula a ser uma célula estaminal, progenitora ou madura diferenciada. Este capítulo focar-se-á principalmente nas células estaminais de mamíferos.
Importância do controlo epigenético
Lister R. et. al., numa publicação de 2011, avaliaram a extensão e complexidade do papel dos processos epigenéticos na determinação da diferenciação que uma célula vai sofrer [6] mediante a programação epigenómica aberrante de células estaminais pluripotentes induzidas humanas (iPSCs).
Como se crê que as células estaminais pluripotentes induzidas mimetizam as células estaminais embrionárias (ESC) nas suas propriedades pluripotentes, deveriam existir poucas diferenças epigenéticas entre elas. Para verificarem esta previsão, os autores realizaram o perfil do genoma completo dos padrões de metilação do ADN em várias células estaminais embrionárias humanas, em iPSC, e em linhagens de células progenitoras.
No ensaio de Lister et al., reprogramaram-se células adiposas femininas, fibroblastos do pulmão e fibroblastos do prepúcio para um estado pluripotente induzido com os genes OCT4, SOX2, KLF4 e MYC. Compararam-se os padrões de metilação do ADN em ESCs, iPSCs e células somáticas, observando-se semelhanças significativas nos níveis de metilação entre células pluripotentes induzidas e embrionárias.
Cerca de 80% dos dinucleótidos CG nas ESCs e iPSCs estavam metilados, tal como estavam apenas 60% dos dinucleótidos CG nas células somáticas. Além disso, as células somáticas possuíam níveis mínimos de metilação de citosinas fora dos dinucleótidos CG, enquanto as células pluripotentes induzidas possuíam níveis de metilação semelhantes aos das células embrionárias, entre 0,5 e 1,5%. Assim, em correspondência com as suas respectivas actividades transcricionais,[6] os padrões de metilação do ADN, pelo menos ao nível genómico, são semelhantes em ESCs e em iPSCs.
Contudo, ao examinarem mais detidamente os padrões de metilação, descobriram que havia 1175 regiões de metilação diferencial em dinucleótidos CG entre pelo menos uma linhagem celular iPS ou ES. Comparando estas regiões de metilação diferencial com regiões de metilação de citosina nas células somáticas originais, 44-49% das regiões metiladas diferencialmente mostravam padrões de metilação das respectivas células somáticas progenitoras, enquanto 51-56% destas regiões eram diferentes tanto das linhagens celulares embrionárias como das progenitoras. A diferenciação induzida in vitro de linhagens iPSC apresentou transmissão de 88% e 46% de regiões hiper e hipometiladas diferencialmente, respectivamente.
Podem retirar-se duas conclusões deste estudo. A primeira, que o processo epigenético está fortemente implicado na determinação da diferenciação das células, como indicam os níveis semelhantes de metilação de citosina entre as células pluripotentes induzidas e as células estaminais embrionárias, o que concorda com os seus respectivos padrões de transcrição. Segundo, os mecanismos de desdiferenciação (e por extensão, diferenciação) são muito complexos e não podem ser duplicados facilmente, como indica o número significativo de regiões metiladas diferencialmente entre as linhagens celulares iPS e as ES.
Alguns dos mecanismos epigenéticos que se crê regularem a diferenciação celular explicam-se de seguida.
Mecanismos de regulação epigenética
Factores pioneiros (Oct4, Sox2, Nanog)
Três factores pioneiros de transcrição, OCT4, SOX2 e NANOG, o primeiro dos quais utilizado na reprogramação iPSC, expressam-se fortemente em células estaminais embrionárias indiferenciadas e são necessários para a manutenção da sua pluripotência.[7] Crê-se que o façam por meio de alterações da estrutura da cromatina, como a modificação de histonas e a metilação do ADN, para restringir ou permitir a transcrição dos genes-alvo.
Complexo repressivo Polycomb (PRC2)
No campo do silenciamento de genes, o complexo repressivo Polycomb 2, que é uma das duas classes da família de proteínas do grupo Polycomb (PcG), catalisa a di- e trimetilação da histona H3 na lisina 27 (H3K27me2/me3).[7][8] Ao ligar-se ao nucleossoma marcado com H3K27me2/3, o PRC1 (que também é um complexo da família de proteínas PcG) catalisa a mono-ubiquitinação da histona H2A na lisina 119 (H2AK119Ub1), bloqueando a actividade da ARN polimerase II e dando lugar a uma supressão transcricional.[7]
As células estaminais embrionárias com knockout para PcG não se diferenciam eficazmente nas três camadas germinais, e a deleção dos genes PRC1 e PRC2 produz um incremento da expressão de genes afiliados à linhagem e uma diferenciação fora do programa normal.[7] Presumivelmente, os complexos PcG são responsáveis pela repressão transcricional de genes que promovem a diferenciação e o desenvolvimento.
Grupo de proteínas Trithorax (TrxG)
Alternativamente, após receberem sinais de diferenciação, as proteínas PcG são recrutadas nos promotores de factores de transcrição de pluripotência. As células estaminais embrionárias deficientes em PcG podem começar a diferenciar-se, mas não conseguem manter o fenótipo diferenciado.[7] Simultaneamente, os genes que promovem a diferenciação e desenvolvimento são activados pelos reguladores da cromatina do grupo Trithorax (TrxG) e perdem a sua repressão.[7][8]
As proteínas TrxG são recrutadas em regiões com alta actividade transcricional, nas quais catalisam a trimetilação da histona H3 na lisina 4 (H3K4me3) e promovem a activação de genes por meio da acetilação de histonas.[8] Os complexos PcG e TrxG estabelecem uma competição directa e crê-se que são funcionalmente antagonistas, criando nos loci que promovem o desenvolvimento e diferenciação o que se denomina “domínio bivalente”, fazendo com que estes genes sensíveis sofram uma rápida indução ou repressão.[9]
Metilação do ADN
A regulação da expressão génica consegue-se ainda por meio de metilação do ADN, na qual a metilação mediada por ADN metiltransferase de resíduos de citosina em dinucleótidos CpG mantém a repressão herdável ao controlar a acessibilidade ao ADN.[9]
A maioria dos sítios CpG em células estaminais embrionárias não estão metilados e parecem estar associados a nucleossomas que transportam H3K4me3.[7] Após a diferenciação, um pequeno número de genes, como o OCT4 e o NANOG,[9] são metilados e os seus promotores reprimidos para impedir a sua futura expressão. As células estaminais embrionárias com metilação deficiente entram rapidamente em apoptose após a sua diferenciação in vitro.[7]
Posicionamento de nucleossomas
Embora a sequência de ADN de quase todas as células de um organismo seja a mesma, os padrões de ligação dos factores de transcrição e os padrões correspondentes de expressão génica são diferentes. Em grande medida, as diferenças na ligação de factores de transcrição são determinadas pela acessibilidade à cromatina dos seus sítios de ligação por meio de modificação de histonas e/ou factores pioneiros.
Em particular, é importante saber se um nucleossoma está a cobrir um sítio de ligação genómico ou não. Estudos recentes elucidaram o papel do posicionamento de nucleossomas durante o desenvolvimento de células estaminais.[10]
Papel da sinalização no controlo epigenético
Pensa-se que a sinalização celular influencia o processo epigenético que governa a diferenciação celular. Esta influência deveria existir, uma vez que é razoável pensar que a sinalização extrínseca pode levar a uma remodelação epigenética, tal como pode levar a mudanças na expressão génica por meio da activação ou repressão de diferentes factores de transcrição.
Dispõe-se de poucos dados directos sobre os sinais específicos que influenciam o epigenoma, e a maioria do nosso conhecimento actual consiste em especulações sobre candidatos plausíveis a reguladores da remodelação epigenética.[11] Neste artigo discutir-se-ão primeiro os principais candidatos que se crê estarem implicados na indução e manutenção das células estaminais embrionárias e da sua progenia diferenciada, vendo-se depois um exemplo de vias de sinalização específicas nas quais existe mais evidência directa deste papel na mudança epigenética.
O primeiro candidato principal é a via de sinalização Wnt. A via Wnt está implicada em todos os estádios de diferenciação, e o ligando Wnt3a pode substituir a sobreexpressão de c-Myc na geração de células estaminais pluripotentes induzidas.[11] Por outra parte, a alteração da ß-catenina, um componente da via de sinalização Wnt, dá lugar a uma diminuição da proliferação dos progenitores neurais.
Os factores de crescimento compõem o segundo maior conjunto de candidatos para serem reguladores epigenéticos da diferenciação celular. Estes morfógenos são fundamentais para o desenvolvimento e incluem as proteínas morfogenéticas do osso, os factores de crescimento transformantes (TGFs) e os factores de crescimento de fibroblastos (FGFs). Os TGFs e FGFs mantêm a expressão de OCT4, SOX2 e NANOG por uma sinalização a jusante das proteínas Smad.[11] A depleção de factores de crescimento promove a diferenciação de células estaminais embrionárias, enquanto os genes com cromatina bivalente podem tornar-se mais restritivos ou mais permissivos na sua transcrição.[11]
Outras vias de sinalização são também consideradas candidatos principais. As citocinas factores inibidores da leucemia estão associadas à manutenção das células estaminais embrionárias de rato em estado indiferenciado. Isto consegue-se por meio da activação nelas da via Jak-STAT3, a qual é necessária e suficiente para manter a pluripotência destas células estaminais embrionárias de rato.[12]
O ácido retinoico pode induzir a diferenciação das células embrionárias humanas e de rato,[11] e a sinalização Notch está implicada na proliferação e autorrenovação de células estaminais. Finalmente, a proteína Sonic hedgehog,[13] além do seu papel como morfógeno, promove a diferenciação de células estaminais embrionárias e a autorrenovação de células estaminais somáticas.[11]
O problema é que a possível intervenção destas vias de sinalização no controlo da diferenciação infere-se principalmente com base no seu papel no desenvolvimento e diferenciação celular. Embora a regulação epigenética seja necessária para dirigir a diferenciação celular, não é suficiente para este processo. A modulação directa da expressão génica por meio da modificação de factores de transcrição desempenha um papel chave que deve distinguir-se das mudanças epigenéticas herdáveis que podem persistir mesmo na ausência dos sinais ambientais originais.
Há apenas alguns exemplos actualmente de vias de sinalização que originem mudanças epigenéticas que alteram o destino da célula, e um deles é a expressão de Sonic hedgehog.
A expressão de Shh (Sonic hedgehog) regula positivamente a produção de Bmi1, um componente do complexo PcG, que reconhece a H3K27me3. Isto ocorre de um modo dependente de Gli, já que Gli1 e Gli2 são efectores de a jusante da via de sinalização Hedgehog. Em cultura, Bmi1 medeia a capacidade da via Hedgehog de promover a autorrenovação das células estaminais mamárias humanas.[14]
Tanto em humanos como em ratos, os investigadores mostraram que Bmi1 se expressa fortemente em células precursoras do grânulo cerebelar imaturo. Quando a Bmi1 sofre um knockout no rato, tal dá lugar a uma alteração do desenvolvimento cerebelar, produzindo-se reduções significativas na massa cerebral pós-natal juntamente com anomalias no controlo motor e no comportamento.[15] Um estudo separado mostrou uma diminuição significativa da proliferação de células estaminais neurais juntamente com um incremento da proliferação de astrocitos no rato Bmi nulo.[16]
Em resumo, o papel da sinalização no controlo epigenético do destino de diferenciação da célula em mamíferos é desconhecido em grande medida, mas há vários exemplos que indicam a provável existência de tais mecanismos.
Referências
- ↑ DeLeon SBT; EH Davidson (2007). «Gene regulation: Gene control network in development». Annual Review of Biophysics and Biomolecular Structure. 36: 191-212. doi:10.1146/annurev.biophys.35.040405.102002
- ↑ Knisely, Karen; Gilbert, Scott F. (2009). Developmental Biology 8th ed. Sunderland, Mass: Sinauer Associates. p. 147. ISBN 0-87893-371-9
- ↑ a b c d e f g Rudel and Sommer; The evolution of developmental mechanisms. Developmental Biology 264, 15-37, 2003 Rudel, D.; Sommer, R. J. (2003). "The evolution of developmental mechanisms". Developmental Biology 264 (1): 15–37. doi:10.1016/S0012-1606(03)00353-1. PMID 14623229.
- ↑ a b Yamamoto Y and WR Jeffery; Central role for the lens in cave fish eye degeneration. Science 289 (5479), 631-633, 2000 Yamamoto, Y.; Jeffery, W. R. (2000). "Central Role for the Lens in Cave Fish Eye Degeneration". Science 289 (5479): 631–633. Bibcode:2000Sci...289..631Y. doi:10.1126/science.289.5479.631. PMID 10915628.
- ↑ Kirk MM, A Ransick, SE Mcrae, DL Kirk; The relationship between cell size and cell fate in Volvox carteri. Journal of Cell Biology 123, 191-208, 1993 Kirk, M. M.; Ransick, A.; McRae, S. E.; Kirk, D. L. (1993). "The relationship between cell size and cell fate in Volvox carteri". Journal of Cell Biology 123 (1): 191–208. doi:10.1083/jcb.123.1.191. PMC 2119814. PMID 8408198.
- ↑ a b Lister R; et al. (2011). «Hotspots of aberrant epigenomic reprogramming in human induced pluripotent stem cells». Nature. 471 (7336): 68–73. Bibcode:2011Natur.471...68L. PMC 3100360
 . PMID 21289626. doi:10.1038/nature09798
. PMID 21289626. doi:10.1038/nature09798
- ↑ a b c d e f g h Christophersen NS, Helin K (2010). «Epigenetic control of embryonic stem cell fate». J Exp Med. 207 (11): 2287–95. PMC 2964577
 . PMID 20975044. doi:10.1084/jem.20101438
. PMID 20975044. doi:10.1084/jem.20101438
- ↑ a b c Guenther MG, Young RA (2010). «Repressive Transcription». Science. 329 (5988): 150–1. Bibcode:2010Sci...329..150G. PMC 3006433
 . PMID 20616255. doi:10.1126/science.1193995
. PMID 20616255. doi:10.1126/science.1193995
- ↑ a b c Meissner A (2010). «Epigenetic modifications in pluripotent and differentiated cells». Nat Biotechnol. 28 (10): 1079–88. PMID 20944600. doi:10.1038/nbt.1684
- ↑ Teif VB, Vainshtein Y, Caudron-Herger M, Mallm JP, Marth C, Höfer T, Rippe K. (2012). «Genome-wide nucleosome positioning during embryonic stem cell development». Nat Struct Mol Biol. 19 (11): 1185–92. PMID 23085715. doi:10.1038/nsmb.2419
- ↑ a b c d e f Mohammad HP, Baylin SB (2010). «Linking cell signaling and the epigenetic machinery». Nat Biotechnol. 28 (10): 1033–8. PMID 20944593. doi:10.1038/nbt1010-1033
- ↑ Niwa H, Burdon T, Chambers I, Smith A (1998). «Self-renewal of pluripotent embryonic stem cells is mediated via activation of STAT3». Genes Dev. 12 (13): 2048–60. PMC 316954
 . PMID 9649508. doi:10.1101/gad.12.13.2048
. PMID 9649508. doi:10.1101/gad.12.13.2048
- ↑ Identificou-se primeiro no gene de Drosophila hedgehog (ouriço), cujos mutantes estavam cobertos de dentículos e pareciam ouriços na etapa de embrião.
- ↑ Liu S; et al. (2006). «Hedgehog Signaling and Bmi-1 Regulate Self-renewal of Normal and Malignant Human Mammary Stem Cells». Cancer Res. 66 (12): 6063–71. PMID 16778178. doi:10.1158/0008-5472.CAN-06-0054
- ↑ Leung C; et al. (2004). «Bmi1 is essential for cerebellar development and is overexpressed in human medulloblastomas». Nature. 428 (6980): 337–41. Bibcode:2004Natur.428..337L. PMID 15029199. doi:10.1038/nature02385
- ↑ Zencak D; et al. (2005). «Bmi1 loss produces an increase in astroglial cells and a decrease in neural stem cell population and proliferation». J Neurosci. 25 (24): 5774–83. PMID 15958744. doi:10.1523/JNEUROSCI.3452-04.2005
Leitura adicional
- Knisely, Karen; Gilbert, Scott F. (2009). Developmental Biology (8th ed.). Sunderland, Mass: Sinauer Associates.
- Lodish, Harvey (2000) Mollecular Cell Biology (4th ed.).New York: W.H. Freeman.
- Becker, W.M. Kleinsmith, L.J. Hardin, J. & Bertoni,G.P. (2009) The World of the Cell (17th edition). Pearson Education, Inc.
- Guilak, Farshid; Cohen, Daniel M.; Estes, Bradley T.; Gimble, Jeffrey M.; Liedtke, Wolfgang; Chen, Christopher S. (2009-07-02). "Control of Stem Cell Fate by Physical Interactions with the Extracellular Matrix"
- Rabajante JF, Babierra AL (January 30, 2015)."Branching and oscillations in the epigenetic landscape of cell-fate determination".