Célula-tronco embrionária
Célula-tronco embrionária
| |
|---|---|
| Subclasse de | pluripotent stem cell, embryonic cell |
| Descobridor(a) | Martin Evans, Matthew Kaufman, Gail Roberta Martin |
| Cell Ontology | CL_0002322 |
| MeSH | D053595 |
| Foundational Model of Anatomy | 82841 |
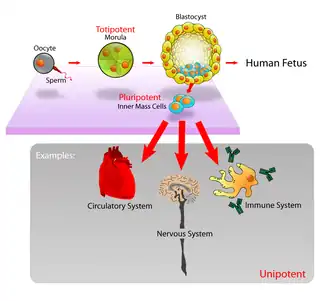
As células estaminais embrionárias (células ES ou ESC pelas suas siglas em inglês de embryonic stem cells) são células estaminais pluripotentes derivadas da massa celular interna de um blastocisto, o qual é um dos estádios iniciais do embrião pré-implantação.[1][2] Os embriões humanos chegam à fase de blastocisto aos 4 ou 5 dias após a fecundação, momento em que consistem em 50 a 150 células. Isolar um embrioblasto ou massa celular interna resulta na destruição do blastocisto, um processo que levanta questões éticas, tais como se os embriões em fase de pré-implantação deveriam ou não ter a mesma consideração moral que os embriões na fase de pós-implantação do desenvolvimento.[3][4]
Em 1981, duas equipes de pesquisa lideradas por Martin Evans e Matthew Kaufman, respectivamente, estabeleceram linhagens de células-tronco embrionárias do rato-doméstico in vitro no Departamento de Genética da Universidade de Cambridge, no Reino Unido.[5] O termo célula-tronco embrionária foi proposto pela primeira vez por Gail R. Martin , professora do Departamento de Anatomia da Universidade da Califórnia, São Francisco (UCSF) , num artigo publicado em dezembro daquele ano.[6] Em 1998, James Thomson, professor da Universidade de Wisconsin, e outros estabeleceram com sucesso linhagens de células-tronco embrionárias humanas. Em 2007, Martin Evans e outros dois cientistas receberam o Prêmio Nobel de Fisiologia ou Medicina.
Considera-se que as células estaminais embrionárias têm amplas perspetivas de aplicação em áreas como a medicina regenerativa, a engenharia de tecidos e os ensaios de fármacos. Contribuem também significativamente para a investigação básica em biologia do desenvolvimento. No entanto, devido a questões éticas, religiosas e legais (como o facto de os métodos actuais de isolamento de células estaminais embrionárias conduzirem inevitavelmente à morte do embrião), a investigação com células estaminais embrionárias (i.e., a clonagem terapêutica) está sujeita a certas restrições em vários países.[7][8][9] Os seus usos potenciais incluem o tratamento da diabetes e das doenças cardíacas.[9] As células estão a ser estudadas para uso em terapias clínicas, modelos de transtornos genéticos e reparação de ADN/celular. No entanto, também foram reportados efeitos adversos desta investigação e em processos clínicos, como tumores e respostas imunitárias indesejadas.[10]
Propriedades
As células estaminais embrionárias, derivadas do estádio de blastocisto de embriões de mamíferos iniciais, distinguem-se pela sua capacidade de se diferenciarem em qualquer tipo de célula embrionária e pela sua capacidade de autorrenovação. Estas características são as que as tornam valiosas para a investigação científica e médica. As células estaminais embrionárias têm um cariótipo normal, mantêm uma alta atividade de telomerase e exibem um notável potencial proliferativo a longo prazo.[11]
Pluripotência
As células estaminais embrionárias da massa celular interna possuem pluripotência, o que significa que podem diferenciar-se para gerar o ectoderma primitivo, que finalmente se diferencia durante a gastrulação em todos os derivados das três camadas germinativas primárias: ectoderma, endoderma e mesoderma. Estas camadas germinativas geram todos e cada um dos mais de 220 tipos celulares do corpo humano adulto. Quando lhes são fornecidos os sinais adequados, as células estaminais embrionárias formam inicialmente células precursoras que em seguida se diferenciam nos tipos celulares desejados. A pluripotência distingue as células estaminais embrionárias das células estaminais adultas, que são multipotentes e só podem produzir um número limitado de tipos celulares.
Autorrenovação e reparação de estruturas
Em condições definidas, as células estaminais embrionárias podem autorrenovar-se indefinidamente, permanecendo num estado indiferenciado. As condições de autorrenovação devem evitar que as células se agrupem e manter um ambiente que suporte um estado não especializado.[12] Tipicamente, isto é feito no laboratório utilizando meios que contêm soro e o Fator inibidor da leucemia ou suplementos de meios sem soro com dois fármacos inibidores ("2i"), o Inibidor de MEK PD03259010 e o Inibidor de GSK-3 CHIR99021.[13]
Crescimento
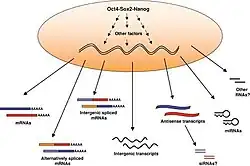
As células estaminais embrionárias dividem-se muito frequentemente devido a terem uma fase G1 encurtada no seu ciclo celular. Uma divisão celular rápida permite a estas células crescerem em número rapidamente, mas não em tamanho, o que é importante para o desenvolvimento inicial do embrião. Nas células estaminais embrionárias, as proteínas ciclina A e ciclina E envolvidas na Transição G1/S são expressas sempre e a um alto nível.[14] As quinases dependentes de ciclina como a CDK2, que promove a progressão do ciclo celular, estão sobre-ativadas, em parte devido à regulação negativa dos seus inibidores.[15] As proteínas do retinoblastoma que inibem o fator de transcrição E2F até que a célula esteja pronta para entrar na fase S estão hiperfosforiladas e inativadas nas células estaminais embrionárias, o que leva à expressão contínua de genes de proliferação.[14] Estas alterações resultam em ciclos acelerados de divisão celular. Embora uma fase G1 encurtada tenha sido ligada à manutenção da pluripotência,[16] as células estaminais embrionárias que crescem em condições $2i$ livres de soro expressam proteínas do retinoblastoma hipofosforiladas ativas e têm uma fase G1 alongada.[17] Apesar desta diferença no ciclo celular, quando comparadas com células estaminais embrionárias que crescem em meios contendo soro, estas células têm características pluripotentes semelhantes.[18] Os fatores de pluripotência Oct4 e Nanog desempenham um papel na regulação transcricional do ciclo celular das células estaminais embrionárias.[19][20]
Usos
Devido à sua plasticidade e capacidade potencialmente ilimitada de autorrenovação, foram propostas terapias com células estaminais para medicina regenerativa e substituição de tecidos após uma lesão ou doença. As células estaminais pluripotentes são promissoras para tratar diversas condições, como por exemplo as seguintes: lesões da medula espinhal, degeneração macular relacionada com a idade, diabetes, transtornos neurodegenerativos (como a doença de Parkinson), SIDA etc.[21] Além do seu potencial em medicina regenerativa, as células estaminais embrionárias proporcionam uma fonte alternativa de tecidos ou órgãos que serviriam como solução para a escassez de dadores para transplantes. No entanto, isto apresenta algumas controvérsias éticas (ver a secção de mais abaixo "Debate ético"). Juntamente com estes usos, as células estaminais embrionárias podem ser usadas para a investigação do desenvolvimento humano inicial, certas doenças genéticas e testes toxicológicos in vitro.[11]
Utilizações
De acordo com um artigo de 2002 na PNAS, "as células estaminais embrionárias humanas têm o potencial de se diferenciarem em vários tipos de células e, assim, podem ser úteis como fonte de células para o transplante ou engenharia de tecidos."[22]
No entanto, as células estaminais embrionárias não estão limitadas à engenharia de células e tecidos.
Terapias de substituição de células
A investigação atual está focada nas células estaminais embrionárias diferenciadas em diversos tipos celulares para um possível uso como células de terapia de substituição. Alguns dos tipos celulares que foram ou estão a ser desenvolvidos são os cardiomiócitos, neurónios, hepatócitos, células da medula óssea, células dos ilhéus de Langerhans pancreáticos e células endoteliais.[23] No entanto, a derivação de tais tipos celulares a partir de células estaminais embrionárias não está isenta de problemas, pelo que as investigações atuais estão centradas em superar estas barreiras. Por exemplo, realizam-se estudos para conseguir diferenciar células estaminais embrionárias em cardiomiócitos e para erradicar as suas propriedades imaturas que as distinguem dos cardiomiócitos adultos.[24]
Potencial clínico
- Foram obtidas células estaminais embrionárias diferenciadas em células produtoras de dopamina com a esperança de que estes neurónios possam ser usados no tratamento da doença de Parkinson.[25][26]
- As células estaminais embrionárias foram diferenciadas em células killer (NK) e do tecido ósseo.[27]
- Estuda-se o seu uso como tratamento alternativo para a diabetes. Por exemplo, D’Amour et al. conseguiram diferenciar células estaminais embrionárias em células que produzem insulina[28] e investigadores da Universidade Harvard conseguiram produzir grandes quantidades de células beta pancreáticas a partir de células estaminais embrionárias.[29]
- Um artigo publicado no European Heart Journal descreve um processo translacional para gerar células progenitoras cardíacas derivadas de células estaminais embrionárias para utilização em ensaios clínicos em pacientes com insuficiência cardíaca grave.[30]
Descoberta de fármacos
Além de se converterem numa alternativa importante para o transplante de órgãos, as células estaminais embrionárias estão também a ser utilizadas no campo da toxicologia e como crivos celulares para descobrir novas entidades químicas que possam ser desenvolvidas como fármacos de baixo peso molecular. Os cardiomiócitos derivados de células estaminais embrionárias são validados em modelos *in vitro* para testar respostas a fármacos e prever perfis de toxicidade.[23] Os cardiomiócitos derivados de células estaminais embrionárias respondem a estímulos farmacológicos e, portanto, podem ser utilizados para estimar a cardiotoxicidade, como nas Torsades de pointes (pontas torcidas nos picos do eletrocardiograma).[31]
Os hepatócitos derivados de células estaminais embrionárias são também modelos úteis que podem ser utilizados nos estádios pré-clínicos da descoberta de fármacos. Contudo, o desenvolvimento de hepatócitos a partir de células estaminais embrionárias tem muitas complicações e isto dificulta a capacidade de testar o metabolismo dos fármacos. Portanto, as investigações atuais estão dirigidas a estabelecer hepatócitos derivados de células estaminais embrionárias totalmente funcionais com atividade enzimática estável em fase I e II.[32]
Modelos de transtornos genéticos
Vários estudos novos começam a tratar a utilização de células estaminais embrionárias como modelos de transtornos genéticos. A modelagem de doenças genéticas tem sido alcançada manipulando geneticamente as células ou, mais recentemente, derivando linhas celulares de doenças identificadas por diagnóstico genético pré-natal. Esta estratégia pode ser muito valiosa no estudo de transtornos como a Síndrome do X frágil, a fibrose cística e outras doenças genéticas que não têm um sistema modelo fiável.
O investigador russo-americano Yury Verlinsky, especializado em genética embrionária e celular (citologia genética), desenvolveu métodos de testes de diagnóstico pré-natal para determinar transtornos cromossómicos e genéticos aplicáveis um mês e meio antes da amniocentese padrão. As técnicas são agora utilizadas por casais que vão ter filhos, especialmente se têm um histórico de anomalias genéticas ou em mulheres com mais de 35 anos (quando o risco de transtornos genéticos é maior). Além disso, como permitem aos pais selecionar um embrião sem transtornos genéticos, têm o potencial de salvar as vidas de irmãos que já tiveram transtornos e doenças semelhantes usando células procedentes dos filhos sem a doença.[33]
Reparação de danos no ADN
As células somáticas diferenciadas e as células estaminais embrionárias usam diferentes estratégias para lidar com os danos no ADN. Por exemplo, os fibroblastos humanos do prepúcio do pénis, um tipo de célula somática, usam a união de extremidades não homólogas (NHEJ), um processo de reparação de ADN propenso ao erro, como via principal para a reparação de roturas de dupla febra no ADN em todos os estádios do ciclo.[34] Devido à sua natureza propensa ao erro, o NHEJ geralmente produz mutações em descendentes clonais de células.
As células estaminais embrionárias usam uma estratégia diferente para lidar com as roturas de dupla febra.[35] Como as células estaminais embrionárias dão origem a todos os tipos de células de um organismo, incluindo as células da linha germinal, as mutações que se originam nas células estaminais embrionárias devido a defeitos na reparação do ADN são um problema mais grave do que nas células que se diferenciaram a partir de células somáticas. Consequentemente, é necessário que existam mecanismos robustos nas células estaminais embrionárias para reparar os danos no ADN adequadamente e, se a reparação falhar, para eliminar as células que tenham danos não reparados. Assim, as células estaminais embrionárias de ratinho usam predominantemente o processo de reparação recombinacional homóloga (HRR) de alta fidelidade para repararem as roturas de dupla febra.[35] Este tipo de reparação depende da interação das duas cópias irmãs do ADN formadas durante a fase S e que estão presentes juntas durante a fase G2 do ciclo celular. A HRR pode reparar com precisão as roturas de dupla febra num cromossoma ao usar informação intacta da molécula irmã de ADN. As células na fase G1 do ciclo celular (ou seja, depois da metafase/divisão celular, mas antes da próxima ronda de replicação) têm apenas uma cópia de cada molécula de ADN (ou seja, as moléculas irmãs não estão presentes). As células estaminais embrionárias de ratinho carecem do ponto de controlo de G1 e não sofrem uma paragem do ciclo celular ao sofrerem danos no ADN.[36] Em vez disso, sofrem uma morte celular programada (apoptose) em resposta aos danos no ADN,[37] A apoptose pode ser utilizada como uma estratégia de falha de segurança para eliminar células com danos no ADN não reparados para evitar as mutações e a progressão para o cancro.[38] Consistente com esta estratégia, as células estaminais embrionárias de ratinho têm uma frequência de mutação cerca de 100 vezes inferior à das células somáticas de ratinho isogénicas.[39]
Ensaio clínico em lesões medulares
Em janeiro de 2009, um ensaio clínico em fase I para o transplante de oligodendrócitos (um tipo celular do cérebro e medula espinhal) derivados de células estaminais embrionárias em indivíduos com lesão da medula espinhal recebeu a aprovação da FDA dos Estados Unidos, no que foi o primeiro ensaio mundial com células estaminais embrionárias humanas.[40] O estudo que levou a este avanço científico foi liderado por Hans Keirstead e colegas na Universidade da Califórnia, Irvine e apoiado pela Geron Corporation de Menlo Park, CA, financiado por Michael D. West. Um experimento prévio havia mostrado uma melhoria na recuperação locomotora em ratas com lesão da medula espinhal após 7 dias do transplante de células estaminais embrionárias que foram transformadas numa linhagem oligodendrocítica.[41] O estudo clínico em fase I foi desenhado para recrutar de 8 a 10 paraplégicos que tivessem tido a sua lesão não antes de duas semanas do início do ensaio, dado que as células devem ser injetadas antes que se forme tecido de cicatrização. Os investigadores enfatizaram que não se esperava que as injeções curassem completamente os pacientes e restaurassem toda a sua mobilidade. Baseando-se nos resultados de ensaios nos roedores, os investigadores especularam que se deveria produzir uma restauração das bainhas de mielina e um aumento da mobilidade. O primeiro ensaio foi desenhado principalmente para verificar a segurança destes procedimentos e, se tudo corresse bem, esperava-se que isso levasse a futuros estudos em pessoas com deficiências mais graves.[42] O ensaio foi provisoriamente paralisado em agosto de 2009 pela preocupação da FDA sobre a formação de um pequeno número de quistos microscópicos em vários modelos de ratas tratados, mas a paralisação foi levantada em julho de 2010.[43]
Em outubro de 2010, os investigadores recrutaram o primeiro paciente a quem foram administradas células estaminais embrionárias no Shepherd Center de Atlanta.[44] Estimava-se que seria necessário esperar vários meses para que as células estaminais se replicassem e a terapia GRNOPC1 pudesse ser avaliada.
Em novembro de 2011, a Geron anunciou que iria parar o ensaio e abandonar a investigação em células estaminais por razões financeiras, mas continuaria a monitorizar os pacientes existentes, e que estava a tentar encontrar um parceiro que continuasse a investigação.[45] Em 2013, a BioTime, liderada pelo Dr. Michael D. West, adquiriu todos os ativos relacionados com as células estaminais da Geron com a intenção de recomeçar o ensaio clínico sobre lesões da medula espinhal.[46]
A subvenção da Strategic Partnership III do CIRM (California Institute for Regenerative Medicine) fornecerá fundos à Asterias para financiar o seu próximo ensaio clínico com AST-OPC1 em lesionados medulares e para o desenvolvimento de produtos para refinar e escalar os seus métodos de fabricação para manter ensaios nas seguintes fases e, finalmente, para a sua comercialização. O acordo definitivo entre Asterias e o CIRM está condicionado a que o FDA aprove os ensaios.[47]
Preocupações e controvérsias
Efeitos adversos
A maior preocupação suscitada pelo transplante de células estaminais embrionárias em pacientes como terapia é a sua capacidade de formar tumores, incluindo os teratomas.[48] As questões de segurança foram o que motivou o FDA a paralisar provisoriamente o primeiro ensaio clínico com estas células, mas nele não se observaram tumores.
A principal estratégia para aumentar a segurança das células estaminais embrionárias para usos clínicos é diferenciá-las em tipos celulares específicos (por exemplo, neurónios, células musculares, do fígado etc.) que tiveram reduzida ou eliminada a sua capacidade de causar tumores. Após a diferenciação, as células são selecionadas por meio de uma citometria de fluxo para uma maior purificação. Prediz-se que as células estaminais embrionárias são inerentemente mais seguras que as células iPS criadas com vetores virais geneticamente integrados porque não são geneticamente modificadas com genes como o c-Myc, que estão ligados ao cancro. Não obstante, as células estaminais embrionárias expressam níveis muito altos de genes indutores de iPS e estes genes, incluindo o Myc, são essenciais para a autorrenovação e pluripotência das células estaminais embrionárias,[49] e as estratégias potenciais para melhorar a segurança eliminando a expressão de c-Myc dificilmente conservarão nelas o caráter de célula estaminal. Contudo, N-myc e L-myc induzem células iPS em vez de c-myc com eficiência similar.[50] Protocolos mais recentes para induzir a pluripotência contornam este problema completamente ao usarem ARN viral não integrados, como os vírus Sendai ou transfeção de ARNm.
Debate ético
Devido à natureza embrionária destas células estaminais, existem muitas opiniões controversas sobre o assunto. Como a colheita das células estaminais embrionárias requer a destruição de um embrião humano, o estatuto moral desse embrião entra em questão. Algumas pessoas argumentam que uma massa de células que constitui um embrião de 5 dias é demasiado jovem para lhe ser dado o estatuto de pessoa ou que os embriões, quando são doados por clínicas de fertilização in vitro (que é onde se obtêm normalmente os embriões para estas investigações), seriam de qualquer forma eliminados como resíduos médicos. Os oponentes a estas investigações consideram que esse embrião é uma vida humana, pelo que destruí-lo é um assassinato e que o embrião deve ser protegido com o mesmo ponto de vista ético que um ser humano mais desenvolvido.[51]
História
- 1964: Lewis Kleinsmith e G. Barry Pierce Jr. isolaram um só tipo de célula de um teratocarcinoma, um tumor que agora se sabe provém de uma célula germinativa.[52] Estas células foram isoladas do teratocarcinoma replicado e cresceram numa cultura celular como uma célula estaminal e são conhecidas agora como células de carcinoma embrionário. Embora as semelhanças em morfologia e potencial diferenciador (pluripotência) tenham levado ao uso de células estaminais embrionárias como modelo in vitro do desenvolvimento inicial dos ratos,[53] as células estaminais embrionárias têm mutações genéticas e frequentemente cariótipos anormais que se acumularam durante o desenvolvimento do teratocarcinoma. Estas aberrações genéticas salientam ainda mais a necessidade de poder cultivar células pluripotentes diretamente a partir da massa celular interna do embrião.

- 1981: as células estaminais embrionárias foram derivadas independentemente pela primeira vez de embriões de rato por dois grupos. Martin Evans e Matthew Kaufman do Departamento de Genética da Universidade de Cambridge publicaram primeiro em julho, descrevendo uma nova técnica para cultivar embriões de rato no útero para conseguir um aumento no número de células, permitindo a derivação de células estaminais embrionárias a partir desses embriões.[5] Gail R. Martin do Departamento de anatomia da Universidade da Califórnia, São Francisco, publicou o seu artigo em dezembro e cunhou o termo “célula estaminal embrionária”.[6] Esta investigadora demonstrou que os embriões podiam ser cultivados in vitro e que as células estaminais embrionárias podiam ser derivadas desses embriões.
- 1989: Mario R. Cappechi, Martin J. Evans e Oliver Smithies publicaram as suas investigações que detalham o seu isolamento e modificações genéticas de células estaminais embrionárias, criando o primeiro "rato knockout".[54] Ao criarem ratos knockout, esta publicação criou uma nova forma de estudar as doenças.
- 1998: uma equipa da Universidade de Wisconsin-Madison (James A. Thomson, Joseph Itskovitz-Eldor, Sander S. Shapiro, Michelle A. Waknitz, Jennifer J. Swiergiel, Vivienne S. Marshall e Jeffrey M. Jones) publicaram um artigo intitulado "Linhas de células estaminais embrionárias derivadas de blastocistos humanos". Estes investigadores não só criaram as primeiras células estaminais embrionárias, como reconheceram a sua pluripotência e a sua capacidade de autorrenovação. O resumo do artigo assinala a importância da descoberta nos campos da biologia do desenvolvimento e da descoberta de medicamentos.[55]
- 2001: o presidente dos Estados Unidos da América George W. Bush permitiu o financiamento federal de investigações com 60 linhas de células estaminais embrionárias já existentes na altura, mas não com as derivadas da criação de novas linhas.[56]
- 2006: os cientistas japoneses Shinya Yamanaka e Kazutoshi Takashi publicaram um artigo descrevendo a indução de células estaminais pluripotentes a partir de culturas de fibroblastos de rato. As células estaminais pluripotentes induzidas ou iPSCs foram uma grande descoberta, já que são praticamente idênticas às células estaminais embrionárias e poderiam ser usadas sem levantar polémicas morais.[57]
- Janeiro de 2009: o FDA norte-americano deu a sua aprovação para realizar o ensaio de fase I da Geron Corporation para o seu tratamento baseado em células estaminais embrionárias para as lesões da medula espinhal. As suas células estaminais derivavam das linhas permitidas pela administração de George W. Bush.[58]
- Março de 2009: uma ordem executiva assinada pelo presidente dos Estados Unidos da América Barack Obama, removeu as restrições sobre a alocação de fundos federais à investigação sobre células estaminais embrionárias impostas pela administração anterior.[59]
Técnicas e condições para a derivação e cultivo
Derivação de embriões humanos
Para realizar uma fertilização in vitro é necessário gerar múltiplos embriões. Os embriões em excesso não são usados clinicamente ou não são adequados para a sua implantação no paciente, e, portanto, podem ser doados com o consentimento do doador. As células estaminais embrionárias podem ser derivadas destes embriões provenientes de doações ou adicionalmente podem também ser extraídas de embriões clonados usando uma célula do paciente e um óvulo de um doador.[60] As células da massa celular interna do embrião (que são as células de interesse), presentes no estádio de blastocisto, são separadas do trofoectoderma, sendo estas últimas as células que se diferenciariam em tecidos extraembrionários. Para realizar a separação utilizam-se a imunocirurgia (o processo pelo qual os anticorpos se ligam ao trofoectoderma e são depois removidos por outra solução) e a dissecação mecânica. As células resultantes da massa celular interna são cultivadas sobre camadas de células que lhes darão suporte. As células da massa celular interna ligam-se e expandem-se mais para formar uma linha de células estaminais embrionárias humanas, que estão indiferenciadas. Estas células são alimentadas diariamente e são separadas enzimática ou mecanicamente a cada quatro a sete dias. Para que ocorra a diferenciação, a linha de células estaminais embrionárias humanas é removida das células que lhe servem de suporte para formar corpos embrionários, é cocultivada com um soro que contém os sinais necessários ou é enxertada num arcabouço tridimensional.[61]
Derivação de outros animais
As células estaminais embrionárias derivam das células da massa celular interna das fases iniciais do embrião, que são colhidas de um animal fêmea dador. Martin Evans e Matthew Kaufman relataram uma técnica que atrasa a implantação do embrião, o que permite que a massa celular interna aumente. Este processo inclui a extirpação dos ovários da mãe e a administração de doses de progesterona, alterando o ambiente hormonal, o que faz com que os embriões permaneçam livres no útero. Após 4 a 6 dias deste cultivo intrauterino, os embriões são colhidos e colocados a crescer em cultivo in vitro até que a massa celular interna forme “estruturas do tipo cilíndrico de ovos”, que são dissociadas em células simples e cultivadas sobre uma camada de fibroblastos tratados com mitomicina-C (para impedir a mitose dos fibroblastos). As linhas celulares clonais são criadas para que deem origem a um só tipo de célula. Evans e Kaufman demonstraram que as células que crescem a partir desses cultivos podiam originar teratomas e corpos embrioides e diferenciavam-se in vitro, tudo o que indica que as células são pluripotentes.[5]
Gail Martin derivou e cultivou as suas células estaminais embrionárias de forma diferente. Ela removeu os embriões da mãe dadora aproximadamente 76 horas após a cópula e cultivou-os durante toda uma noite num meio que continha soro. No dia seguinte, removeu a massa celular interna do blastocisto tardio usando microcirurgia. A massa celular interna extraída foi cultivada sobre fibroblastos tratados com mitomicina-C num meio que contém soro e com as condições necessárias. Passada aproximadamente uma semana, crescem as colónias de células. Estas células crescem em cultivo e demonstram ter características pluripotentes, como se demonstra pela sua capacidade de produzir teratomas, diferenciar-se in vitro, e formar corpos embrioides. Martin denominou estas células células estaminais embrionárias.[6]
Agora sabe-se que as células de alimentação (fibroblastos) fornecem o fator inibidor de leucemia e o soro fornece proteínas morfogenéticas ósseas (BMPs) que são necessárias para impedir que as células estaminais embrionárias se diferenciem.[62][63] Estes fatores são extremamente importantes para a eficiência das células estaminais embrionárias derivadas. Além disso, demonstrou-se que diferentes estirpes de ratos têm diferentes eficiências para isolar células estaminais embrionárias.[64] Os usos atuais das células estaminais embrionárias de rato incluem a geração de ratos transgénicos, incluindo os ratos knockout. Para o tratamento humano, não há necessidade de células pluripotentes específicas do paciente. A geração de células estaminais embrionárias humanas é mais difícil e apresenta questões éticas. Assim, além da investigação em células estaminais embrionárias humanas, muitos grupos estão a focar-se na geração de células estaminais pluripotentes induzidas (células iPS).[65]
Possível método para a derivação de uma nova linha celular
A 23 de agosto de 2006, a edição online da revista Nature publicou uma carta do Dr. Robert Lanza (diretor médico da Advanced Cell Technology de Worcester, MA) na qual se afirmava que a sua equipa tinha encontrado uma forma de extrair células estaminais embrionárias sem destruir o embrião.[66] Este feito técnico poderia permitir aos cientistas trabalhar com novas linhas de células estaminais embrionárias derivadas usando financiamento público nos Estados Unidos, onde o financiamento federal estava até então limitado às investigações com linhas de células estaminais embrionárias que tinham sido derivadas antes de agosto de 2001. Em março de 2009, esta limitação foi levantada.[67]
Células estaminais pluripotentes induzidas (iPS)
A tecnologia das iPSC foi iniciada pelo laboratório de Shinya Yamanaka em Quioto, Japão, que mostrou em 2006 que a introdução de quatro genes específicos que codificam fatores de transcrição poderia converter células adultas em células estaminais pluripotentes.[68] Foi galardoado em 2012 com o Prémio Nobel juntamente com John Gurdon "pela descoberta de que células maduras podem ser reprogramadas para se tornarem pluripotentes."[69]
Em 2007, demonstrou-se que células estaminais pluripotentes muito semelhantes a células estaminais embrionárias podem ser geradas pela introdução de três genes (Oct4, Sox2 e Klf4) em células diferenciadas.[70] A introdução destes genes "reprograma" células diferenciadas em células estaminais pluripotentes, o que permite a geração de células estaminais pluripotentes sem o embrião. Devido às preocupações éticas sobre as células estaminais embrionárias pela sua derivação de embriões, crê-se que a reprogramação destas células estaminais pluripotentes induzidas pode ser menos controversa. Tanto as células humanas como as de ratos podem ser reprogramadas por esta metodologia, gerando células estaminais pluripotentes humanas e de rato sem utilizar embriões.[71]
Isto pode permitir a geração de linhas de células estaminais embrionárias específicas de pacientes que poderiam ser utilizadas para terapias de substituição de células. Além disso, isto permitirá a geração de linhas celulares de células estaminais embrionárias a partir de pacientes com diversas doenças genéticas e fornecerá modelos muito valiosos para estudar essas doenças.
Contudo, como uma primeira indicação de que a tecnologia das células estaminais pluripotentes induzidas (iPS) pode alcançar curas rápidas, foi utilizada por uma equipa de investigação liderada por Rudolf Jaenisch do Instituto Whitehead para a Pesquisa Biomédica de Cambridge, Massachusetts, para curar ratos da anemia falciforme, conforme relatado na revista Science na sua edição online de 6 de dezembro de 2007.[72][73]
A 16 de janeiro de 2008, uma companhia sediada na Califórnia, Stemagen, anunciou que tinha criado os primeiros embriões humanos clonados maduros a partir de uma célula da pele colhida de adultos. Destes embriões podem ser obtidas células estaminais embrionárias que se correspondem geneticamente com os pacientes.[74]
Contaminação por reagentes usados em culturas celulares
A edição online da Nature Medicine publicou um estudo a 4 de janeiro de 2005 no qual se afirmava que as células estaminais embrionárias humanas disponíveis para o financiamento federal de investigações nos Estados Unidos estão contaminadas com moléculas não humanas provenientes do meio de cultura usado para as fazer crescer.[75] Uma técnica comum é usar células de rato e outras células animais para manter a pluripotência de células estaminais que se dividem ativamente. O problema foi descoberto quando se verificou que o ácido siálico não humano do meio de crescimento comprometia os usos potenciais das células estaminais embrionárias em humanos, segundo os cientistas da Universidade da Califórnia.[76]
Contudo, um estudo publicado na edição online do Lancet Medical Journal de 8 de março de 2005 detalhava informação sobre uma nova linha de células estaminais que foi derivada de embriões humanos em condições completamente isentas de células e de soro. Após mais de 6 meses de proliferação indiferenciada, estas células demonstraram o potencial de formar derivados das três camadas germinativas embrionárias tanto in vitro como em teratomas. Estas propriedades foram mantidas com sucesso (em mais de 30 passagens de cultivo) nas linhas de células estaminais estabelecidas.[77]
Referências
- ↑ Thomson; Itskovitz-Eldor, J; Shapiro, SS; Waknitz, MA; Swiergiel, JJ; Marshall, VS; Jones, JM (1998). «Blastocysts Embryonic Stem Cell Lines Derived from Human». Science. 282 (5391): 1145–1147. Bibcode:1998Sci...282.1145T. PMID 9804556. doi:10.1126/science.282.5391.1145
- ↑ «NIH Stem Cell Basics. What are embryonic stem cells?». Consultado em 25 de março de 2014. Arquivado do original em 31 de agosto de 2016
- ↑ Baldwing A (2009). «Morality and human embryo research. Introduction to the Talking Point on morality and human embryo research.». EMBO Reports. 10 (4): 299–300. PMC 2672902
 . PMID 19337297. doi:10.1038/embor.2009.37
. PMID 19337297. doi:10.1038/embor.2009.37
- ↑ Nakaya, Andrea C. (1 de agosto de 2011). Biomedical ethics. San Diego, CA: ReferencePoint Press. 96 páginas. ISBN 978-1601521576
- ↑ a b c Evans M, Kaufman M (1981). «Establishment in culture of pluripotent cells from mouse embryos». Nature. 292 (5819): 154–6. Bibcode:1981Natur.292..154E. PMID 7242681. doi:10.1038/292154a0
- ↑ a b c Martin G (1981). «Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells». Proc Natl Acad Sci USA. 78 (12): 7634–8. Bibcode:1981PNAS...78.7634M. PMC 349323
 . PMID 6950406. doi:10.1073/pnas.78.12.7634
. PMID 6950406. doi:10.1073/pnas.78.12.7634
- ↑ Baldwin, Thomas (abril de 2009). «Morality and human embryo research: Introduction to the Talking Point on morality and human embryo research». EMBO reports (em inglês). 10 (4): 299–300. ISSN 1469-221X. PMC 2672902
 . PMID 19337297. doi:10.1038/embor.2009.37
. PMID 19337297. doi:10.1038/embor.2009.37
- ↑ Nakaya, Andrea C. (1 de agosto de 2011). Biomedical ethics. San Diego, CA: ReferencePoint Press. 96 páginas. ISBN 160152157X
- ↑ a b «Introduction: What are stem cells, and why are they important?». National Institutes of Health. Consultado em 28 de outubro de 2018. Arquivado do original em 28 de outubro de 2018
- ↑ Carla A Herberts; Marcel SG Kwa; Harm PH Hermsen (2011). «Risk factors in the development of stem cell therapy». Journal of Translational Medicine. 9 (29). 29 páginas. PMC 3070641
 . PMID 21418664. doi:10.1186/1479-5876-9-29
. PMID 21418664. doi:10.1186/1479-5876-9-29
- ↑ a b Thomson, J. A.; Itskovitz-Eldor, J; Shapiro, S. S.; Waknitz, M. A.; Swiergiel, J. J.; Marshall, V. S.; Jones, J. M. (1998). «Embryonic Stem Cell Lines Derived from Human Blastocysts». Science. 282 (5391): 1145–7. Bibcode:1998Sci...282.1145T. PMID 9804556. doi:10.1126/science.282.5391.1145
- ↑ Ying; Nichols, J; Chambers, I; Smith, A (2003). «BMP Induction of Id Proteins Suppresses Differentiation and Sustains Embryonic Stem Cell Self-Renewal in Collaboration with STAT3». Cell. 115 (3): 281–292. PMID 14636556. doi:10.1016/S0092-8674(03)00847-X
- ↑ Martello, G.; Smith, A. (2014). «The nature of embryonic stem cells». Annual Review of Cell and Developmental Biology. 30: 647–75. PMID 25288119. doi:10.1146/annurev-cellbio-100913-013116
- ↑ a b Boward, B.; Wu, T.; Dalton, S. (2016). «Concise Review: Control of Cell Fate Through Cell Cycle and Pluripotency Networks». Stem Cells. 34 (6): 1427–36. PMC 5201256
 . PMID 26889666. doi:10.1002/stem.2345
. PMID 26889666. doi:10.1002/stem.2345
- ↑ White, J.; Stead, E.; Faast, R.; Conn, S.; Cartwright, P.; Dalton, S. (2005). «Developmental activation of the Rb-E2F pathway and establishment of cell cycle-regulated cyclin-dependent kinase activity during embryonic stem cell differentiation». Molecular Biology of the Cell. 16 (4): 2018–27. PMC 1073679
 . PMID 15703208. doi:10.1091/mbc.e04-12-1056
. PMID 15703208. doi:10.1091/mbc.e04-12-1056
- ↑ Singh, Amar M.; Dalton, Stephen (7 de agosto de 2009). «The cell cycle and Myc intersect with mechanisms that regulate pluripotency and reprogramming». Cell Stem Cell. 5 (2): 141–149. ISSN 1875-9777. PMC 2909475
 . PMID 19664987. doi:10.1016/j.stem.2009.07.003
. PMID 19664987. doi:10.1016/j.stem.2009.07.003
- ↑ Ter Huurne, Menno; Chappell, James; Dalton, Stephen; Stunnenberg, Hendrik G. (5 de outubro de 2017). «Distinct Cell-Cycle Control in Two Different States of Mouse Pluripotency». Cell Stem Cell. 21 (4): 449–455.e4. ISSN 1875-9777. PMC 5658514
 . PMID 28985526. doi:10.1016/j.stem.2017.09.004
. PMID 28985526. doi:10.1016/j.stem.2017.09.004
- ↑ Ying, Qi-Long; Wray, Jason; Nichols, Jennifer; Batlle-Morera, Laura; Doble, Bradley; Woodgett, James; Cohen, Philip; Smith, Austin (22 de maio de 2008). «The ground state of embryonic stem cell self-renewal». Nature. 453 (7194): 519–523. Bibcode:2008Natur.453..519Y. ISSN 1476-4687. PMC 5328678
 . PMID 18497825. doi:10.1038/nature06968
. PMID 18497825. doi:10.1038/nature06968
- ↑ Lee, J.; Go, Y.; Kang, I.; Han, Y. M.; Kim, J. (2010). «Oct-4 controls cell-cycle progression of embryonic stem cells». The Biochemical Journal. 426 (2): 171–81. PMC 2825734
 . PMID 19968627. doi:10.1042/BJ20091439
. PMID 19968627. doi:10.1042/BJ20091439
- ↑ Zhang, X.; Neganova, I.; Przyborski, S.; Yang, C.; Cooke, M.; Atkinson, S. P.; Anyfantis, G.; Fenyk, S.; Keith, W. N.; Hoare, S. F.; Hughes, O.; Strachan, T.; Stojkovic, M.; Hinds, P. W.; Armstrong, L.; Lako, M. (2009). «A role for NANOG in G1 to S transition in human embryonic stem cells through direct binding of CDK6 and CDC25A». The Journal of Cell Biology. 184 (1): 67–82. PMC 2615089
 . PMID 19139263. doi:10.1083/jcb.200801009
. PMID 19139263. doi:10.1083/jcb.200801009
- ↑ Mahla, Ranjeet (19 de julho de 2016). «Stem Cell Applications in Regenerative Medicine and Disease Therapeutics». International Journal of Cell Biology. 2016. 6940283 páginas. PMC 4969512
 . PMID 27516776. doi:10.1155/2016/6940283
. PMID 27516776. doi:10.1155/2016/6940283
- ↑ Levenberg, S. (2002). «Endothelial cells derived from human embryonic stem cells». Proceedings of the National Academy of Sciences. 99 (7): 4391–4396. Bibcode:2002PNAS...99.4391L. PMC 123658
 . PMID 11917100. doi:10.1073/pnas.032074999
. PMID 11917100. doi:10.1073/pnas.032074999
- ↑ a b Davila, JC; Cezar, GG; Thiede, M; Strom, S; Miki, T; Trosko, J (2004). «Use and application of stem cells in toxicology». Toxicological Sciences. 79 (2): 214–23. PMID 15014205. doi:10.1093/toxsci/kfh100
- ↑ Siu, CW; Moore, JC; Li, RA (2007). «Human embryonic stem cell-derived cardiomyocytes for heart therapies». Cardiovascular & Hematological Disorders Drug Targets. 7 (2): 145–52. PMID 17584049. doi:10.2174/187152907780830851
- ↑ Perrier, A. L. (2004). «Derivation of midbrain dopamine neurons from human embryonic stem cells». Proceedings of the National Academy of Sciences. 101 (34): 12543–12548. Bibcode:2004PNAS..10112543P. PMC 515094
 . PMID 15310843. doi:10.1073/pnas.0404700101
. PMID 15310843. doi:10.1073/pnas.0404700101
- ↑ Parish, CL; Arenas, E (2007). «Stem-cell-based strategies for the treatment of Parkinson's disease». Neuro-Degenerative Diseases. 4 (4): 339–47. PMID 17627139. doi:10.1159/000101892
- ↑ Waese, EY; Kandel, RA; Stanford, WL (2008). «Application of stem cells in bone repair». Skeletal Radiology. 37 (7): 601–8. PMID 18193216. doi:10.1007/s00256-007-0438-8
- ↑ d'Amour, KA; Bang, AG; Eliazer, S; Kelly, OG; Agulnick, AD; Smart, NG; Moorman, MA; Kroon, E; Carpenter, MK; Baetge, EE (2006). «Production of pancreatic hormone-expressing endocrine cells from human embryonic stem cells». Nature Biotechnology. 24 (11): 1392–401. PMID 17053790. doi:10.1038/nbt1259
- ↑ Colen, B.D. (9 October 2014) Giant leap against diabetes The Harvard Gazette, Retrieved 24 November 2014
- ↑ Menasché, Phillip; Vanneaux, Valérie; Fabreguettes, Jean-Roch; Bel, Alain; Tosca, Lucie; Garcia, Sylvie (21 de março de 2015). «Towards a clinical use of human embryonic stem cell derived-cardiac progenitors: a translational experience». European Heart Journal. 36 (12): 743–750. PMID 24835485. doi:10.1093/eurheartj/ehu192
- ↑ Jensen, J; Hyllner, J; Björquist, P (2009). «Human embryonic stem cell technologies and drug discovery». Journal of Cellular Physiology. 219 (3): 513–9. PMID 19277978. doi:10.1002/jcp.21732
- ↑ Söderdahl, T; Küppers-Munther, B; Heins, N; Edsbagge, J; Björquist, P; Cotgreave, I; Jernström, B (2007). «Glutathione transferases in hepatocyte-like cells derived from human embryonic stem cells». Toxicology in Vitro. 21 (5): 929–37. PMID 17346923. doi:10.1016/j.tiv.2007.01.021
- ↑ "Dr. Yury Verlinsky, 1943–2009: Expert in reproductive technology" Arquivado em 2009-08-08 no Wayback Machine Chicago Tribune, July 20, 2009
- ↑ Mao Z, Bozzella M, Seluanov A, Gorbunova V (setembro de 2008). «DNA repair by nonhomologous end joining and homologous recombination during cell cycle in human cells». Cell Cycle. 7 (18): 2902–6. PMC 2754209
 . PMID 18769152. doi:10.4161/cc.7.18.6679
. PMID 18769152. doi:10.4161/cc.7.18.6679
- ↑ a b Tichy ED, Pillai R, Deng L, et al. (novembro de 2010). «Mouse embryonic stem cells, but not somatic cells, predominantly use homologous recombination to repair double-strand DNA breaks». Stem Cells Dev. 19 (11): 1699–711. PMC 3128311
 . PMID 20446816. doi:10.1089/scd.2010.0058
. PMID 20446816. doi:10.1089/scd.2010.0058
- ↑ Hong Y, Stambrook PJ (outubro de 2004). «Restoration of an absent G1 arrest and protection from apoptosis in embryonic stem cells after ionizing radiation». Proc. Natl. Acad. Sci. U.S.A. 101 (40): 14443–8. Bibcode:2004PNAS..10114443H. PMC 521944
 . PMID 15452351. doi:10.1073/pnas.0401346101
. PMID 15452351. doi:10.1073/pnas.0401346101
- ↑ Aladjem MI, Spike BT, Rodewald LW, et al. (janeiro de 1998). «ES cells do not activate p53-dependent stress responses and undergo p53-independent apoptosis in response to DNA damage». Curr. Biol. 8 (3): 145–55. PMID 9443911. doi:10.1016/S0960-9822(98)70061-2
- ↑ Bernstein C, Bernstein H, Payne CM, Garewal H (junho de 2002). «DNA repair/pro-apoptotic dual-role proteins in five major DNA repair pathways: fail-safe protection against carcinogenesis». Mutat. Res. 511 (2): 145–78. PMID 12052432. doi:10.1016/S1383-5742(02)00009-1
- ↑ Cervantes RB, Stringer JR, Shao C, Tischfield JA, Stambrook PJ (março de 2002). «Embryonic stem cells and somatic cells differ in mutation frequency and type». Proc. Natl. Acad. Sci. U.S.A. 99 (6): 3586–90. Bibcode:2002PNAS...99.3586C. PMC 122567
 . PMID 11891338. doi:10.1073/pnas.062527199
. PMID 11891338. doi:10.1073/pnas.062527199
- ↑ «FDA approves human embryonic stem cell study - CNN.com». 23 de janeiro de 2009. Consultado em 1 de maio de 2010
- ↑ Keirstead HS, Nistor G, Bernal G, et al. (2005). «Human embryonic stem cell-derived oligodendrocyte progenitor cell transplants remyelinate and restore locomotion after spinal cord injury» (PDF). J. Neurosci. 25 (19): 4694–705. PMC 6724772
 . PMID 15888645. doi:10.1523/JNEUROSCI.0311-05.2005
. PMID 15888645. doi:10.1523/JNEUROSCI.0311-05.2005
- ↑ Reinberg, Steven (2009-01-23) FDA OKs 1st Embryonic Stem Cell Trial. The Washington Post
- ↑ Geron comments on FDA hold on spinal cord injury trial. geron.com (August 27, 2009)
- ↑ Vergano, Dan (11 de outubro de 2010). «Embryonic stem cells used on patient for first time». USA Today. Consultado em 12 de outubro de 2010
- ↑ Brown, Eryn (15 de novembro de 2011). «Geron exits stem cell research». LA Times. Consultado em 15 de novembro de 2011
- ↑ «Great news: BioTime Subsidiary Asterias Acquires Geron Embryonic Stem Cell Program». iPScell.com. 1 de outubro de 2013
- ↑ Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadascal - ↑ Knoepfler, Paul S. (2009). «Deconstructing Stem Cell Tumorigenicity: A Roadmap to Safe Regenerative Medicine». Stem Cells. 27 (5): 1050–6. PMC 2733374
 . PMID 19415771. doi:10.1002/stem.37
. PMID 19415771. doi:10.1002/stem.37
- ↑ Varlakhanova, Natalia V.; Cotterman, Rebecca F.; Devries, Wilhelmine N.; Morgan, Judy; Donahue, Leah Rae; Murray, Stephen; Knowles, Barbara B.; Knoepfler, Paul S. (2010). «Myc maintains embryonic stem cell pluripotency and self-renewal». Differentiation. 80 (1): 9–19. PMC 2916696
 . PMID 20537458. doi:10.1016/j.diff.2010.05.001
. PMID 20537458. doi:10.1016/j.diff.2010.05.001
- ↑ Wernig, Marius; Meissner, Alexander; Cassady, John P; Jaenisch, Rudolf (2008). «C-Myc is Dispensable for Direct Reprogramming of Mouse Fibroblasts». Cell Stem Cell. 2 (1): 10–2. PMID 18371415. doi:10.1016/j.stem.2007.12.001
- ↑ King, Nancy; Perrin, Jacob (7 de julho de 2014). «Ethical issues in stem cell research and therapy». Stem Cell Research & Therapy. 5 (4). 85 páginas. PMC 4097842
 . PMID 25157428. doi:10.1186/scrt474
. PMID 25157428. doi:10.1186/scrt474
- ↑ Kleinsmith LJ, Pierce GB Jr (1964). «Multipotentiality of Single Embryoncal Carcinoma Cells». Cancer Res. 24: 1544–51. PMID 14234000
- ↑ Martin GR (1980). «Teratocarcinomas and mammalian embryogenesis». Science. 209 (4458): 768–76. Bibcode:1980Sci...209..768M. PMID 6250214. doi:10.1126/science.6250214
- ↑ «The 2007 Nobel Prize in Physiology or Medicine - Advanced Information». Nobel Prize. Nobel Media
- ↑ Thompson, James A.; Itskovitz-Eldor, Joseph; Shapiro, Sander S.; Waknitz, Michelle A.; Swiergiel, Jennifer J.; Marshall, Vivienne S.; Jones, Jeffrey M. (6 de novembro de 1998). «Embryonic Stem Cell Lines Derived From Human Blastocyst». Science. 282 (5391): 1145–1147. Bibcode:1998Sci...282.1145T. PMID 9804556. doi:10.1126/science.282.5391.1145
- ↑ «President George W. Bush's address on stem cell research». CNN Inside Politics. CNN. 9 de agosto de 2001. Consultado em 4 de junho de 2020. Cópia arquivada em 13 de junho de 2018
- ↑ Yamanaka, Shinya; Takahashi, Kazutoshi (25 de agosto de 2006). «Induction of Pluripotent Stem Cells From Mouse Embryonic and Adult Fibroblast Cultures by Defined Factors». Cell. 126 (4): 663–676. PMID 16904174. doi:10.1016/j.cell.2006.07.024. hdl:2433/159777
- ↑ Wadman, Meredith (27 de janeiro de 2009). «Stem cells ready for primetime». Nature. 457 (7229). 516 páginas. PMID 19177087. doi:10.1038/457516a
- ↑ «Executive Order 13505—Removing Barriers To Responsible Scientific Research Involving Human Stem Cells» (PDF). Federal Register: Presidential Documents. 74 (46). 11 de março de 2009
- ↑ Mountford, JC (2008). «Human embryonic stem cells: origins, characteristics and potential for regenerative therapy». Transfus Med. 18 (1): 1–12. PMID 18279188. doi:10.1111/j.1365-3148.2007.00807.x
- ↑ Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, Marshall VS, Jones JM (1998). «Embryonic stem cell lines derived from human blastocysts». Science. 282 (5391): 1145–1147. Bibcode:1998Sci...282.1145T. PMID 9804556. doi:10.1126/science.282.5391.1145
- ↑ Smith AG, Heath JK, Donaldson DD, Wong GG, Moreau J, Stahl M, Rogers D (1988). «Inhibition of pluripotential embryonic stem cell differentiation by purified polypeptides». Nature. 336 (6200): 688–690. Bibcode:1988Natur.336..688S. PMID 3143917. doi:10.1038/336688a0
- ↑ Williams RL, Hilton DJ, Pease S, Willson TA, Stewart CL, Gearing DP, Wagner EF, Metcalf D, Nicola NA, Gough NM (1988). «Myeloid leukaemia inhibitory factor maintains the developmental potential of embryonic stem cells». Nature. 336 (6200): 684–687. Bibcode:1988Natur.336..684W. PMID 3143916. doi:10.1038/336684a0
- ↑ Ledermann B, Bürki K (1991). «Establishment of a germ-line competent C57BL/6 embryonic stem cell line». Exp Cell Res. 197 (2): 254–258. PMID 1959560. doi:10.1016/0014-4827(91)90430-3
- ↑ Takahashi K, Tanabe K, Ohnuki M, Narita M, Ichisaka T, Tomoda K, Yamanaka S (2007). «Induction of pluripotent stem cells from adult human fibroblasts by defined factors». Cell. 131 (5): 861–872. PMID 18035408. doi:10.1016/j.cell.2007.11.019. hdl:2433/49782
- ↑ Klimanskaya I, Chung Y, Becker S, Lu SJ, Lanza R (2006). «Human embryonic stem cell lines derived from single blastomeres». Nature. 444 (7118): 481–5. Bibcode:2006Natur.444..481K. PMID 16929302. doi:10.1038/nature05142
- ↑ US scientists relieved as Obama lifts ban on stem cell research, The Guardian, 10 March 2009
- ↑ Takahashi, K; Yamanaka, S (2006). «Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors». Cell. 126 (4): 663–76. PMID 16904174. doi:10.1016/j.cell.2006.07.024. hdl:2433/159777
- ↑ «The Nobel Prize in Physiology or Medicine – 2012 Press Release». Nobel Media AB. 8 de outubro de 2012
- ↑ Wernig, Marius; Meissner, Alexander; Foreman, Ruth; Brambrink, Tobias; Ku, Manching; Hochedlinger, Konrad; Bernstein, Bradley E.; Jaenisch, Rudolf (19 de julho de 2007). «In vitro reprogramming of fibroblasts into a pluripotent ES-cell-like state». Nature. 448 (7151): 318–324. Bibcode:2007Natur.448..318W. ISSN 1476-4687. PMID 17554336. doi:10.1038/nature05944
- ↑ «Embryonic stem cells made without embryos». Reuters. 21 de novembro de 2007
- ↑ Weiss, Rick (7 de dezembro de 2007). «Scientists Cure Mice Of Sickle Cell Using Stem Cell Technique: New Approach Is From Skin, Not Embryos». The Washington Post. pp. A02
- ↑ Hanna, J.; Wernig, M.; Markoulaki, S.; Sun, C.-W.; Meissner, A.; Cassady, J. P.; Beard, C.; Brambrink, T.; Wu, L.-C.; Townes, T. M.; Jaenisch, R. (2007). «Treatment of Sickle Cell Anemia Mouse Model with iPS Cells Generated from Autologous Skin». Science. 318 (5858): 1920–3. Bibcode:2007Sci...318.1920H. PMID 18063756. doi:10.1126/science.1152092
- ↑ Helen Briggs (17 de janeiro de 2008). «US team makes embryo clone of men». BBC. pp. A01
- ↑ Ebert, Jessica (24 de janeiro de 2005). «Human stem cells trigger immune attack». London: Nature Publishing Group. Nature News. doi:10.1038/news050124-1. Consultado em 27 de fevereiro de 2009. Arquivado do original em 24 de setembro de 2010
- ↑ Martin MJ, Muotri A, Gage F, Varki A (2005). «Human embryonic stem cells express an immunogenic nonhuman sialic acid». Nat. Med. 11 (2): 228–32. PMID 15685172. doi:10.1038/nm1181
- ↑ Klimanskaya I, Chung Y, Meisner L, Johnson J, West MD, Lanza R (2005). «Human embryonic stem cells derived without feeder cells». Lancet. 365 (9471): 1636–41. PMID 15885296. doi:10.1016/S0140-6736(05)66473-2
Ver também
Ligações externas
- Keller, Gordon (2005). Embryonic stem cell differentiation: emergence of a new era in biology and medicine. Genes & Development. doi:10.1101/gad.1303605
- Evans, Martin (2011). Discovering pluripotency: 30 years of mouse embryonic stem cells (PDF). Nature Reviews - Molecular Cell Biology
- Boiani, Michele (2005). Regulatory networks in embryo-derived pluripotent stem cells. Nature Reviwes - Molecular Cell Biology. doi:10.1038/nrm1744