Ácido siálico
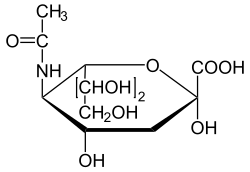
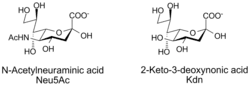
Ácido siálico é um termo genérico que se aplica aos derivados N- ou O-substituídos do ácido neuramínico, um monossacarídeo de 9 átomos de carbono do grupo dos açúcares ácidos.[1] Às vezes, o nome é utilizado especificamente para o membro mais comum do grupo, o ácido N-acetilneuramínico (Neu5Ac ou NANA).
Os ácidos siálicos estão amplamente distribuídos nos tecidos animais e em menor extensão em espécies de outros grupos de seres vivos como plantas, fungos e bactérias, principalmente fazendo parte de glicoproteínas e gangliosídeos. O grupo amino geralmente está substituído com um grupo acetil ou glicolilo, mas outras modificações já foram descritas. Os substituintes dos grupos hidroxilo são muito variáveis, e podem ser: grupos acetila, lactilo, metilo, sulfato, e fosfato.[2] O grupo ácido está ionizado a pH celular, o que lhes confere carga negativa, que é muito importante nas propriedades e funções destas moléculas.
O termo ácido siálico procede do grego σίαλον (sialon), saliva, e foi introduzido pelo bioquímico sueco Gunnar Blix em 1952. Nas mucinas e na saliva abundam os ácidos siálicos, que lhes dão as suas propriedades lubrificantes.
Estrutura
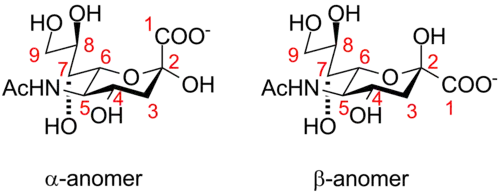
A numeração da estrutura dos ácidos siálicos começa no carbono do carboxilato e continua ao redor da cadeia no sentido horário. A configuração do anómero alfa é a que situa o carboxilato em posição axial.
Biossíntese
Em sistemas bacterianos os ácidos siálicos são sintetizados pela enzima ácido siálico aldolase. O substrato da enzima é a manose ou um derivado da manose, no qual a enzima insere três carbonos procedentes do piruvato originando o ácido siálico. Estas aldolases, juntamente com CMP-ácido siálico sintetases, e sialiltransferases podem ser utilizadas para a síntese quimioenzimática de derivados de ácidos siálicos.[3]
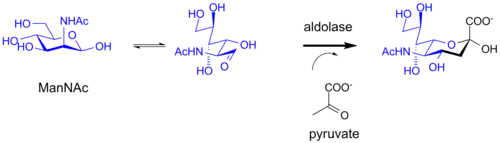
Nas células humanas o ácido N-acetilneuramínico sintetiza-se por epimerização da UDP-N-acetilglicosamina a N-acetilgalactosamina, que acaba dando lugar a N-acetilmanosamina-6-fosfato. Este último composto reage com o fosfoenolpiruvato para dar lugar ao ácido siálico, que, para poder entrar na rota de biossíntese de oligossacarídeos na célula, deve ser ativado por meio da adição de um nucleosídeo monofosfato, fornecido pela CMP, o que dá lugar à formação de «citidina monofosfato-ácido siálico» (CMP-ácido siálico). Nesta reação o CMP-ácido siálico sintetiza-se no núcleo celular das células animais, enquanto o resto dos açúcares ligados a nucleosídeos o fazem no citosol.[4]
Funções
As glicoproteínas ricas em ácidos siálicos (sialoglicoproteínas) ligam-se à selectina em humanos e outros organismos. É frequente que as células metastáticas de cancro expressem uma alta densidade de glicoproteínas ricas em ácidos siálicos.[5][6] Isso favorece a passagem destas células à circulação sanguínea.
As proteínas lectinas presentes em numerosas espécies têm uma grande afinidade por diferentes açúcares, incluindo os ácidos siálicos [7]; e são importantes em muitos processos patológicos [8]. Com frequência patógenos como vírus e bactérias identificam, graças aos ácidos siálicos, certas composições de açúcares específicos [7] que utilizam como alvos na superfície celular para iniciar a infeção em determinados tecidos [9][10][11]. As Siglecs, ou lectinas de tipo I, são uma família de lectinas que reconhecem especificamente o ácido siálico [12]. Pertencem à superfamília das imunoglobulinas.
Os ácidos siálicos também desempenham um importante papel nas infeções gripais em humanos. Os vírus da gripe (Orthomyxoviridae) têm glicoproteínas com atividade de hemaglutinina (HA) na sua superfície, que se ligam aos ácidos siálicos que se encontram na superfície dos eritrócitos humanos e nas membranas das células das vias respiratórias superiores. Esta é a base da hemaglutinação quando os vírus se misturam com células sanguíneas, e na entrada dos vírus nas células das vias aéreas superiores. Um exemplo que ilustra a importância dos ácidos siálicos na gripe é que os fármacos antivirais zanamivir e oseltamivir são inibidores da neuraminidase do vírus da gripe, que atua sobre os ácidos siálicos, que são o alvo molecular que permite que o vírus se adira às células que vai infetar.
Os oligossacarídeos ricos em ácidos siálicos de glicoconjugados como glicolípidos, glicoproteínas ou proteoglicanos que se encontram na superfície das membranas ajudam a manter hidratada a superfície das células. As regiões ricas em ácidos siálicos contribuem para criar uma carga negativa na superfície das células. Como a água é uma molécula polar com cargas parciais positivas (δ+) nos seus dois hidrogénios, é atraída pela superfície celular. Isto também contribui para a entrada de água na célula.
Os ácidos siálicos podem "ocultar" os antígenos de manose da superfície das células hospedeiras ou bactérias da lectina que se liga à manose.[13] Isto impede a ativação do sistema do complemento.
A união de ácidos siálicos em forma de ácidos polisiálicos é uma modificação pós-traducional incomum que ocorre nas moléculas de adesão celular neural, NCAM. Na sinapse, a forte carga negativa dos ácidos polisiálicos impede as ligações cruzadas de NCAM nas células [14].
Referências
- ↑ Varki Ajit, Roland Schauer (2008). Cold Spring Harbor Press, ed. in Essentials of Glycobiology. [S.l.: s.n.] pp. Ch. 14 [1]
- ↑ Schauer R. (2000). «Achievements and challenges of sialic acid research». Glycoconj. J. 17 (7–9): 485–499. PMID 11421344. doi:10.1023/A:1011062223612
- ↑ Hai Yu, Harshal Chokhawala, Shengshu Huang, and Xi Chen (2006). «One-pot three-enzyme chemoenzymatic approach to the synthesis of sialosides containing natural and non-natural functionalities». Nature Protocols. 1 (5): 2485–2492. PMC 2586341
 . PMID 17406495. doi:10.1038/nprot.2006.401
. PMID 17406495. doi:10.1038/nprot.2006.401
- ↑ Mathews, C. K.; Van Holde, K.E et Ahern, K.G (2003). Bioquímica 3 ed. [S.l.: s.n.] ISBN 84-7892-053-2
- ↑ John G. Collard et al. Cell Surface Sialic Acid and the Invasive and Metastatic Potential of T-Cell Hybridomas Cancer Research
- ↑ . Dennis, C. Waller, R. Timpl, V. Schirrmacher. Surface sialic acid reduces attachment of metastatic tumour cells to collagen type IV and fibronectin. Nature 300, 274 - 276 (18 November 1982); doi:10.1038/300274a0 doi:10.1038/300274a0
- ↑ a b Lis, H. & Sharon, N. (1998). Lectins: Carbohydrate-specific proteins that mediate cellular recognition. Chem. Rev. 98, 637-674.
- ↑ Sharon, N. (1996) Carbohydrate-lectin interactions in infectious disease. Adv. Exp. Med. Biol., 408, 1-8.
- ↑ Imberty, A., Mitchell, E.P. and Wimmerová, M. (2005) Structural basis for high affinity glycan recognition by bacterial and fungal lectins. Curr. Opin. Struct. Biol., 15, 525 - 534.
- ↑ Imberty, A. and Varrot, A. (2008) Microbial recognition of human cell surface glycoconjugates. Curr. Opin. Struct. Biol., 18, 567-576.
- ↑ Imberty, A., Wimmerova, M., Mitchell, E.P. and Gilboa-Garber, N. (2004) Structures of the lectins from Pseudomonas aeruginosa: Insights into molecular basis for host glycan recognition. Microb. Infect., 6, 222-229.
- ↑ Crocker, P.R. (2002) Siglecs: sialic-acid-binding immunoglobulin-like lectins in cell-cell interactions and signalling. Curr. Opin. Struct. Biol., 12, 609-615.
- ↑ The Microbial World. Lectures in Microbiology by Kenneth Todar PhD. University of Wisconsin-Madison. Department of Bacteriology. (2009). Chapter: Evasion of host defenses/Evading complement The Mechanisms of Bacterial Pathogenicity Arquivado em 2011-12-18 no Wayback Machine
- ↑ Bruce A.Cunningham, Stanley Hoffman, Urs Rutishauser, John J. Hemperly, Gerald M. Edelman. Proc. Natl Acad. Sci. USA Vol. 80, pp. 3116-3120, May 1983 Molecular topography of the neural cell adhesion molecule N-CAM: Surface orientation and location of sialic acid-rich and binding regions