Fator de transcrição
Factores de transcrição (TF) são proteínas que se ligam ao DNA de células eucarióticas para permitir que haja uma ligação entre a enzima RNA-polimerase e o DNA, permitindo assim a transcrição e a futura tradução.Qualquer proteína necessária para o início da transcrição, mas que não seja parte integrante do RNA polimerase.
As proteínas desses conjunto são classificadas em 3 tipos:
- TF I: proteínas que são imprescindíveis para a ligação a RNA-polimerase I, responsáveis pela transcrição de genes que resultam em RNAs ribossomais.
- TF II: proteínas que são imprescindíveis para a ligação a RNA-polimerase II, responsáveis pela transcrição de genes que resultam em RNAs mensageiros.
- TF III: proteínas que são imprescindíveis para a ligação a RNA-polimerase III, responsáveis pela transcrição de genes que resultam principalmente em RNAs transportadores.
Da mesma forma, essas proteínas podem inibir a transcrição.
Essas proteínas são essenciais na comunicação genética, controle da expressão genética, ver Redes Funcionais.
Uma característica definidora dos fatores de transcrição é que contêm um ou mais domínios de ligação ao ADN, que se ligam a sequências específicas de ADN adjacentes aos genes que regulam.[1][2] Outras proteínas, como coativadores, complexos de remodelação da cromatina, histona acetilases, histona desacetilases, cinases e metilases, também desempenham papéis cruciais na regulação da expressão genética, mas não possuem domínios de ligação ao ADN e, por esse motivo, não são classificados como fatores de transcrição.[3]
Conservação em diferentes organismos
Os fatores de transcrição são essenciais para a regulação da expressão genética e, como consequência, encontram-se em todos os seres vivos. O número de fatores de transcrição que um organismo possui aumenta com o tamanho do genoma, e genomas maiores tendem a ter mais fatores de transcrição por gene.[4]
Existem aproximadamente 2600 proteínas no genoma humano que contêm domínios de ligação ao ADN, e pensa-se que a maioria delas funcionam como fatores de transcrição.[5] Assim sendo, aproximadamente 10% dos genes do genoma codificam factores de transcrição, fazendo desta família de proteínas a mais extensa entre as proteínas humanas. Além disso, os genes são frequentemente ladeados por múltiplos locais de ligação para diferentes factores de transcrição, e a expressão eficiente de cada um destes genes requer a acção cooperativa de vários factores de transcrição diferentes (por exemplo, no caso dos factores nucleares dos hepatócitos). Portanto, a utilização combinada de um conjunto de aproximadamente 2000 factores de transcrição humanos explica facilmente a regulação particular de cada gene no genoma humano durante o desenvolvimento do organismo.[3]
Mecanismo
Os fatores de transcrição ligam-se a regiões amplificadoras (enhancers) ou a promotores do ADN adjacentes aos genes que regulam. Dependendo dos fatores de transcrição, a transcrição dos genes adjacentes é potenciada ou reduzida. Os fatores de transcrição utilizam diversos mecanismos para a regulação da expressão génica.[6] Estes mecanismos são:
- Estabilizam ou bloqueiam a ligação da ARN polimerase ao ADN.
- Catalisam a acetilação ou desacetilação das proteínas histonas. O fator de transcrição pode fazer isto diretamente ou recrutar outras proteínas graças a esta atividade catalítica. Muitos fatores de transcrição utilizam algum destes dois mecanismos opostos para regular a transcrição:[7]
- A atividade da histona acetiltransferase (HAT) acetila as histonas, o que debilita a associação do ADN com as histonas, o que faz com que o ADN seja mais acessível à transcrição, e, portanto, aumente a transcrição.
- A atividade da histona desacetilase (HDAC) desacetila as histonas, o que fortalece a associação do ADN com as histonas, e isto faz com que o ADN seja menos acessível à transcrição, e desse modo diminua a transcrição.
- Recrutam proteínas coativadoras ou correpressoras no complexo do ADN do fator de transcrição.[8]
Função
Os fatores de transcrição são um dos grupos de proteínas que leem e interpretam o projeto ou modelo ("blueprint") genético do ADN. Ligam-se ao ADN e ajudam a iniciar um programa que aumenta ou diminui a transcrição génica. São vitais para muitos processos celulares. A seguir indicam-se algumas das importantes funções e papéis biológicos nos quais estão envolvidos os fatores de transcrição:
Regulação da transcrição basal
Nos eucariotas, é necessária uma importante classe de fatores de transcrição chamados fatores de transcrição geral (GTFs) para que ocorra a transcrição.[9][10][11] Muitos destes fatores de transcrição geral não se ligam realmente ao ADN, mas são parte de um complexo de pré-iniciação da transcrição grande que interage diretamente com a ARN polimerase. Os fatores de transcrição geral mais comuns são: TFIIA, TFIIB, TFIID (ver também proteína de ligação à TATA), TFIIE, TFIIF, e TFIIH.[12] O complexo de pré-iniciação ligam-se a regiões promotoras do ADN a montante (na direção 5') do gene que regulam.
Potenciação diferencial da transcrição
Outros fatores de transcrição regulam diferencialmente a expressão de vários genes ao ligarem-se a regiões amplificadoras (*enhancers*) do ADN adjacentes aos genes regulados. Estes fatores de transcrição são fundamentais para garantir que os genes se expressam na célula correta no momento correto e na quantidade adequada, dependendo dos requisitos mutáveis do organismo.
Desenvolvimento
Muitos fatores de transcrição nos organismos multicelulares estão implicados no desenvolvimento.[13] Respondendo a sinais (estímulos), estes fatores de transcrição ativam ou desativam a transcrição dos genes apropriados, o qual, por sua vez, permite que ocorram mudanças na morfologia celular ou atividades necessárias para a determinação do destino da célula e a diferenciação celular. A família de fatores de transcrição Hox, por exemplo, é importante para uma adequada formação do padrão corporal em organismos tão diversos como as moscas da fruta e os humanos.[14][15] Outro exemplo é o fator de transcrição codificado pela região determinante do sexo do cromossoma Y (gene SRY), que desempenha um papel principal na determinação do sexo nos humanos.[16]
Resposta a sinais intercelulares
As células podem comunicar umas com as outras libertando moléculas que produzem cascatas de sinalização noutra célula recetora. Se o sinal requer o aumento ou diminuição da expressão de genes na célula recetora, frequentemente os fatores de transcrição estarão nas partes finais da cascata de sinalização.[17] A sinalização por meio de estrogénios é um exemplo de cascata de sinalização bastante curta que envolve o fator de transcrição receptor de estrogénios: Os estrogénios são segregados por tecidos como os ovários e a placenta, atravessam a membrana plasmática da célula recetora, e ligam-se ao receptor de estrogénios no citoplasma celular. O receptor de estrogénios depois dirige-se ao núcleo celular e ali liga-se aos seus sítios de ligação ao ADN, alterando a regulação transcricional dos genes associados.[18]
Resposta ao ambiente
Os fatores de transcrição não só atuam na parte final das cascatas de sinalização relacionadas com os estímulos biológicos, mas podem também atuar na parte final das cascatas implicadas nos estímulos do ambiente externo. São exemplos o factor de choque térmico (HSF), o qual aumenta a expressão de genes necessários para a sobrevivência a temperaturas altas,[19] o factor inducible da hipoxia (HIF), que aumenta a expressão dos genes necessários para a sobrevivência celular em ambientes baixos em oxigénio,[20] e a proteína de ligação ao elemento regulador de esteróis (SREBP), que ajuda a manter os níveis adequados de lípidos na célula.[21]
Controlo do ciclo celular
Muitos fatores de transcrição, especialmente alguns que são proto-oncogenes ou supressores de tumores, ajudam a regular o ciclo celular e determinam o tamanho que atingirá a célula e quando pode dividir-se para originar células-filhas.[22][23] Um exemplo é o oncogene Myc, o qual tem importantes papéis no crescimento celular e a apoptose.[24]
Patogénese
Os fatores de transcrição podem também ser utilizados para alterar a expressão génica numa célula hospedeiro para promover a patogénese. Um exemplo bem estudado disto são os efetores do tipo ativadores de transcrição (efetores TAl) segregados pela bactéria Xanthomonas. Quando se injetam em plantas, estas proteínas podem entrar no núcleo da célula da planta, ligar-se a sequências promotoras da planta, e ativar a transcrição de genes da planta que ajudam à infeção bacteriana.[25] Os efetores TAL contêm uma região repetida central na qual há uma relação simples entre a identidade de dois resíduos críticos nas sequências repetidas e bases da sequência do ADN no sítio de ligação do efetor TAL.[26][27] Esta propriedade provavelmente torna mais fácil que estas proteínas evoluam para competir melhor com os mecanismos de defesa da célula hospedeira.[28]
Regulação
É comum na biologia que os processos importantes tenham múltiplas camadas de regulação e controlo. Isto ocorre também com os fatores de transcrição. Os fatores de transcrição não só controlam o grau de transcrição para regular as quantidades de produtos génicos (ARN e proteínas) disponíveis para a célula, como também os próprios fatores de transcrição estão regulados (frequentemente por outros fatores de transcrição). A continuação faz-se uma breve sinopse de algumas das vias por meio das quais se regulam os fatores de transcrição:
Síntese
Os fatores de transcrição (como todas as proteínas) são transcritos a partir de um gene de um cromossoma a ARN, e depois o ARN é traduzido a proteínas. Qualquer destes passos pode ser regulado de modo que afete à produção (e deste modo à atividade) do fator de transcrição. Uma implicação interessante disto é que os fatores de transcrição podem regular-se a si mesmos. Por exemplo, num laço de retroalimentação negativa, os fatores de transcrição atuam como o seu próprio repressor: Se a proteína fator de transcrição se liga ao ADN do seu próprio gene, fará diminuir a sua própria produção. Este é um mecanismo que serve para manter um fator de transcrição em níveis baixos na célula.
Localização nuclear
Nos eucariotas, os fatores de transcrição, tal como a maioria das proteínas (umas poucas transcrevem-se nas mitocôndrias e cloroplastos), são codificados no núcleo celular, mas são depois traduzidas no citoplasma. Muitas proteínas que são ativas no núcleo contêm um sinal de localização nuclear que serve para as dirigir ao núcleo. Para muitos fatores de transcrição este é um ponto-chave na sua regulação.[29] Importantes classes de fatores de transcrição, como os receptores nucleares devem ligar-se primeiro a um ligando enquanto estão no citoplasma, para depois poderem ser deslocados ao núcleo.[29]
Ativação
Os fatores de transcrição podem ser ativados (ou desativados) por meio do seu domínio sensível ao sinal por diversos mecanismos entre os quais estão:
- Ligação a um ligando. A ligação a um ligando não só pode influir sobre em que parte da célula se deve localizar o fator de transcrição, mas também pode afetar ao estado de atividade do fator, e, portanto, à sua capacidade de ligação ao ADN ou a outros cofactores (caso, por exemplo, dos receptores nucleares).
- Fosforilação.[30][31] Muitos fatores de transcrição, como as proteínas STAT, devem ser fosforilados para que se possam ligar ao ADN.
- Interação com outros fatores de transcrição. Por exemplo, a homo- ou heterodimerização ou as proteínas correguladoras.
Acessibilidade ao sítio de ligação ao ADN
Nos eucariotas, o ADN está organizado juntamente com proteínas histonas formando partículas compactas, chamadas nucleossomas, nas quais cerca de 147 pares de bases do ADN dão duas voltas à volta de um octámero central de histonas. O ADN dos nucleossomas é inacessível para muitos fatores de transcrição. Alguns fatores de transcrição, denominados fatores pioneiros podem apesar de tudo ligar-se aos seus sítios de ligação ao ADN no ADN nucleossómico. Para a maioria dos outros fatores de transcrição, o nucleosoma deve ser ativamente removido por motores moleculares como os remodeladores da cromatina.[32] Alternativamente, o nucleosoma pode ser parcialmente desenrolado por flutuações térmicas que permitem um acesso temporário ao sítio de ligação do factor de transcrição. Em muitos casos os fatores de transcrição devem competir para se ligarem ao seu sítio de ligação ao ADN com outros fatores de transcrição e proteínas cromatínicas histonas e não histonas.[33] Pares de fatores de transcrição e outras proteínas podem ter papéis antagonistas (ativador contra repressor) na regulação de um mesmo gene.
Disponibilidade de outros cofactores/fatores de transcrição
A maioria dos fatores de transcrição não funcionam sozinhos. Frequentemente, para que ocorra a transcrição de um gene devem ligar-se às sequências reguladoras do ADN vários fatores de transcrição. Este conjunto de fatores de transcrição, por sua vez, recruta proteínas intermédias como os cofatores correguladores que permitem um recrutamento eficiente do complexo de pré-iniciação e a ARN polimerase. Assim, para que um só fator de transcrição inicie a transcrição, todas estas outras proteínas devem estar presentes também, e o fator de transcrição deve estar num estado em que possa ligar-se a elas se for preciso.
Estrutura

Os fatores de transcrição têm uma estrutura modular e contêm os seguintes domínios:[34]
- Dominio de ligação ao ADN (DBD), que se liga a sequências específicas do ADN, chamadas amplificadores (*enhancers*) ou promotores, que são adjacentes aos genes regulados. As sequências do ADN às quais se ligam os fatores de transcrição denominam-se frequentemente elementos de resposta.
- Domínio de transativação (TAD), que contém sítios de ligação para outras proteínas como os correguladores da transcrição. Estes sítios de ligação denominam-se frequentemente funções de ativação (AFs).[35]
- Um domínio sensível ao sinal opcional (SSD) (por exemplo, um domínio de ligação a um ligando), que é sensível a sinais externos e, em resposta a eles, transmite estes sinais ao resto do complexo de transcrição, causando um aumento ou diminuição da expressão do gene. Além disso, o domínio de ligação ao ADN e os domínios sensíveis ao sinal podem encontrar-se em proteínas separadas que se associam ao complexo de transcrição para regular assim a expressão génica.
Domínio de Transativação
Os domínios de transativação (TADs) são assim denominados pela sua composição em aminoácidos. Estes aminoácidos são essenciais para a sua atividade ou simplesmente os mais abundantes no TAD. A transativação pelo sistema do fator de transcrição Gal4 é mediada por aminoácidos de carácter ácido, e no sistema Gcn4 são os resíduos de carácter hidrofóbico que desempenham um papel similar. Desta forma, os domínios de transativação em Gal4 e Gcn4 denominam-se domínios de ativação ácidos ou hidrofóbicos, respetivamente.[36]
Um domínio de transativação de nove aminoácidos (9aaTAD) define um novo domínio comum a uma grande superfamília de fatores de transcrição eucarióticos representados por Gal4, Oaf1, Leu3, Rtg3, Pho4, Gln3, Gcn4 em leveduras, e por p53, NFAT, NF-κB e VP16 em mamíferos.[37] A predição de 9aa TADs (ácidos ou hidrofóbicos) está disponível online em ExPASy[38] e em EMBnet Spain[39]
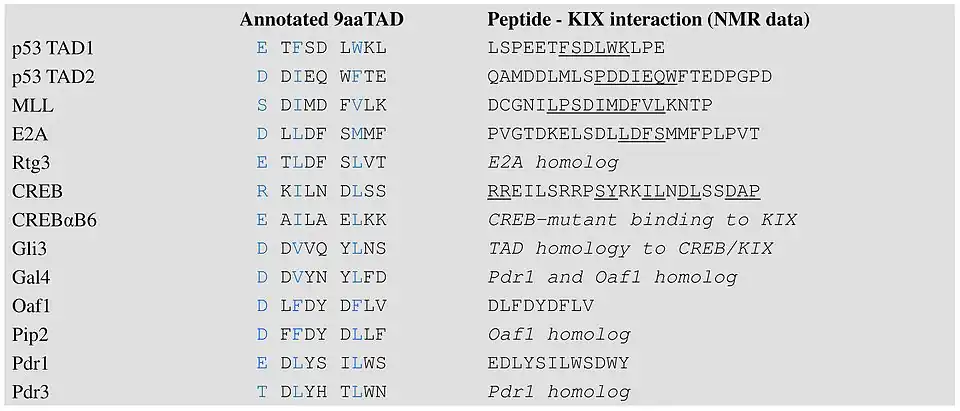
Os fatores de transcrição do tipo 9aaTAD p53, VP16, MLL, E2A, HSF1, NF-IL6, NFAT1 e NF-κB interagem diretamente com os coativadores gerais TAF9 e CBP/p300.[40] Os 9aaTADs de p53 interagem com TAF9, GCN5 e com múltiplos domínios de CBP/p300 (KIX, TAZ1, TAZ2 e IBiD).[41]
O domínio KIX dos coativadores gerais Med15(Gal11) interage com os fatores de transcrição do tipo 9aaTAD Gal4, Pdr1, Oaf1, Gcn4, VP16, Pho4, Msn2, Ino2 e P201.[42] Foram encontradas interações de Gal4, Pdr1 e Gcn4 com Taf9.[43] O 9aaTAD é um domínio de transativação comum que recruta múltiplos coativadores gerais como TAF9, MED15, CBP/p300 e GCN5.[44]
Domínio de ligação ao ADN
A porção (domínio) do fator de transcrição que se liga ao ADN é denominada domínio de ligação ao ADN (DBD). Abaixo está uma lista parcial de algumas das maiores famílias de domínios de ligação ao ADN/fatores de transcrição:
| Família | InterPro | Pfam | SCOP |
|---|---|---|---|
| hélice-alça-hélice básica[45] | IPR001092 | PF00010 | 47460 |
| cremalheira de leucina básica (bZIP)[46] | IPR004827 | PF00170 | 57959 |
| domínio efetor C-terminal dos reguladores da resposta bipartites | IPR001789 | PF00072 | 46894 |
| GCC box | 54175 | ||
| hélice-volta-hélice[47] | |||
| proteínas homeodomínio. Ligadas às sequências homeobox do ADN, as quais por sua vez codificam outros fatores de transcrição. As proteínas homeodomínio desempenham papéis críticos na regulação do desenvolvimento do organismo.[48] | IPR009057 | PF00046 | 46689 |
| do tipo do repressor lambda | IPR010982 | 47413 | |
| do tipo srf (fator de resposta sérico) | IPR002100 | PF00319 | 55455 |
| caixa apareada (paired box) [49] | |||
| hélice alada | IPR013196 | PF08279 | 46785 |
| dedos de zinco[50] | |||
| * dedos de zinco Cys2His2 multidomínio[51] | IPR007087 | PF00096 | 57667 |
| * Zn2/Cys6 | 57701 | ||
| * dedo de zinco do receptor nuclear Zn2/Cys8 | IPR001628 | PF00105 | 57716 |
Elementos de resposta
A sequência do ADN à qual se liga um fator de transcrição é chamada sítio de ligação do fator de transcrição ou elemento de resposta.[52]
Os fatores de transcrição interagem com os seus sítios de ligação utilizando uma combinação de atração eletrostática (como as pontes de hidrogénio) e forças de Van der Waals. Devido à natureza destas interações químicas, a maioria dos fatores de transcrição liga-se ao ADN de um modo específico de sequência. Contudo, nem todas as bases do sítio de ligação do fator de transcrição podem realmente interagir com o fator de transcrição. Além disso, algumas destas interações podem ser mais fracas do que outras. Assim, os fatores de transcrição não se ligam apenas a uma sequência, mas podem ligar-se a um conjunto de sequências muito similares, a cada uma delas com uma diferente força de interação.
Por exemplo, embora o sítio de ligação de consenso para a proteína de ligação à TATA (TBP) seja TATAAAA, o fator de transcrição da proteína de ligação à TATA pode também ligar-se a sequências similares como TATATAT ou TATATAA.
Dado que os fatores de transcrição podem ligar-se a um conjunto de sequências similares e estas sequências são geralmente curtas, podem aparecer por acaso sítios de ligação de fatores de transcrição potenciais se a sequência do ADN for suficientemente longa. No entanto, é improvável que um fator de transcrição se ligue a todas as sequências compatíveis do genoma da célula. Outras restrições, como a acessibilidade ao ADN da célula ou a disponibilidade de cofactores, pode também ajudar a determinar o local onde um fator de transcrição se ligará. Assim, dada a sequência genómica, é ainda difícil prever onde um fator de transcrição se ligará numa célula.
Pode obter-se uma especificidade de reconhecimento adicional utilizando mais do que um domínio de ligação ao ADN (por exemplo, sítios de ligação ao ADN em tandem no mesmo fator de transcrição ou através da dimerização de dois fatores de transcrição) que se ligam a duas ou mais sequências do ADN adjacentes.
Importância clínica
Os fatores de transcrição são importantes na medicina por duas razões: (1) as mutações nestes fatores podem estar associadas a determinadas doenças, e (2) os fatores podem ser o alvo de certos medicamentos.
Transtornos
Algumas doenças humanas estão associadas a mutações nos fatores de transcrição, devido aos seus importantes papéis no desenvolvimento, sinalização intercelular, e ciclo celular.[53]
Muitos fatores de transcrição são supressores de tumores ou oncogenes, e, as mutações ou a regulação anormal neles está associada ao cancro. Conhecem-se três grupos de fatores de transcrição que são importantes no cancro humano: (1) as famílias NF-kappaB e AP-1, (2) a família STAT e (3) os recetores de hormonas esteroides.[54]
A tabela indica alguns exemplos que foram bem estudados:
| Condição | Descrição | Locus |
|---|---|---|
| Síndrome de Rett | As mutações no fator de transcrição MECP2 estão associadas com a síndrome de Rett, um transtorno do desenvolvimento neural.[55][56] | Xq28 |
| Diabetes | Uma forma rara de diabetes chamada MODY (Maturity onset diabetes of the young) pode ser causada por mutações nos fatores nucleares do hepatócito (HNFs) [57] ou no fator-1 promotor da insulina (IPF1/Pdx1).[58] | múltiplo |
| Dispraxia verbal do desenvolvimento | As mutações no fator de transcrição FOXP2 estão associadas com a dispraxia verbal do desenvolvimento, uma doença na qual os afetados não conseguem coordenar com precisão os movimentos necessários para falar.[59] | 7q31 |
| Doenças autoimunes | As mutações no fator de transcrição FOXP3 causam uma forma rara de doença autoimune chamada IPEX.[60] | Xp11.23-q13.3 |
| Síndrome de Li-Fraumeni | Causado por mutações no supressor de tumores p53.[61] | 17p13.1 |
| Cancro da mama | A família de proteínas STAT é relevante no cancro da mama.[62] | múltiplo |
| Cancros múltiplos | A família HOX está implicada em vários tipos de cancro.[63] | múltiplo |
Alvos Potenciais de Medicamentos
Aproximadamente 10% dos fármacos prescritos atualmente têm como alvos diretos os fatores de transcrição da classe dos recetores nucleares.[64] Exemplos são o tamoxifen e bicalutamide para o tratamento do cancro da mama e do cancro da próstata, respetivamente, e vários tipos de anti-inflamatórios e esteroides anabólicos.[65]
Além disso, os fatores de transcrição são frequentemente modulados indiretamente por fármacos por meio de cascatas de sinalização. Nos tratamentos, seria possível visar outros fatores de transcrição menos explorados, como o NF-κB, com novos fármacos.[66][67][68][69] Acredita-se que os fatores de transcrição que não pertencem à família dos recetores nucleares são mais difíceis de atingir com pequenas moléculas terapêuticas, mas estão a ser feitos progressos na via de sinalização Notch.[70]
Análise
Existem diferentes tecnologias aplicáveis para a análise de fatores de transcrição. No nível genómico, são utilizadas comummente a sequenciação do ADN[71] e a pesquisa em bases de dados. A versão proteica concreta do fator de transcrição pode ser detetada utilizando anticorpos específicos. A amostra é detetada com a técnica de western blot. Utilizando o ensaio de retardo na mobilidade eletroforética (EMSA),[72] pode ser detetado o perfil de ativação do fator de transcrição. Uma abordagem multiplex para o estudo do perfil de ativação é o sistema de chip TF no qual vários fatores de transcrição podem ser detetados em paralelo. Esta tecnologia é baseada nas micromatrizes de ADN (microarrays), que fornecem a sequência específica de ligação ao ADN para o fator de transcrição na superfície da matriz.[73]
Classes
Como se descreve com mais detalhe abaixo, os fatores de transcrição podem ser classificados pelo seu (1) mecanismo de ação, (2) função reguladora, ou (3) homologia de sequências (e, portanto, semelhança estrutural) nos seus domínios de ligação ao ADN.
Classificação pelo mecanismo de ação
Há três classes de fatores de transcrição segundo o seu mecanismo de ação:
- Fatores de Transcrição Gerais. Estão envolvidos na formação de um complexo de pré-iniciação. Os mais comuns são: TFIIA, TFIIB, TFIID, TFIIE, TFIIF, e TFIIH. São ubíquos e interagem com a região núcleo (core) do promotor que rodeia o sítio de início da transcrição de todos os genes de classe II.[74]
- Fatores de Transcrição que atuam a montante (upstream). São proteínas que se ligam a montante (na direção 5') do sítio de iniciação e estimulam ou reprimem a transcrição. São, grosso modo, o mesmo que os fatores de transcrição específicos, porque variam consideravelmente dependendo da sequência de reconhecimento em que estão presentes na proximidade do gene.[75]
| Exemplos de Fatores de Transcrição Específicos[75] | |||
|---|---|---|---|
| Fator | Tipo estrutural | Sequência de reconhecimento | Liga-se como |
| SP1 | Dedo de zinco | 5'-GGGCGG-3' | Monómero |
| AP-1 | Cremalheira Básica | 5'-TGA(G/C)TCA-3' | Dímero |
| C/EBP | Cremalheira Básica | 5'-ATTGCGCAAT-3' | Dímero |
| Fator de Choque Térmico | Cremalheira Básica | 5'-XGAAX-3' | Trímero |
| ATF/CREB | Cremalheira Básica | 5'-TGACGTCA-3' | Dímero |
| c-Myc | Hélice-Alça-Hélice Básica | 5'-CACGTG-3' | Dímero |
| Oct-1 | Hélice-volta-hélice | 5'-ATGCAAAT-3' | Monómero |
| NF-1 | Novo | 5'-TTGGCXXXXXGCCAA-3' | Dímero |
Classificação Funcional
Os fatores de transcrição classificam-se de acordo com a sua função regulatória em:[3]
- I. Constitutivamente Ativos. Presentes em todas as células em todo o momento. Por exemplo: fatores de transcrição gerais, Sp1, NF1, CCAAT.
- II. Condicionalmente Ativos. Requerem ativação.
- II.A Do Desenvolvimento (específicos de células). A sua expressão está estreitamente controlada, mas, uma vez expressos, não requerem uma ativação adicional. Por exemplo: GATA, HNF, PIT-1, MyoD, Myf5, Hox, Hélice Alada.
- II.B Dependentes de Sinal. Requerem um sinal externo para a sua ativação.
- II.B.1 Dependentes de um Ligando Extracelular (endócrino ou parácrino). Por exemplo, os recetores nucleares.
- II.B.2 Dependentes de um Ligando Intracelular (autócrino). Ativados por pequenas moléculas intracelulares. Por exemplo: SREBP, p53, recetores nucleares órfãos.
- II.B.3 Dependentes de Recetores da Membrana Plasmática. Ativados por cascatas de sinalização de segundos mensageiros que originam a fosforilação do fator de transcrição.
- II.B.3.a Fatores Nucleares Residentes. Residem no núcleo sem ter em conta o estado de ativação em que se encontram. Por exemplo: CREB, AP-1, Mef2.
- II.B.3.b Fatores Citoplasmáticos Latentes. As formas inativas residem no citoplasma, mas quando são ativadas dirigem-se ao núcleo. Por exemplo: STAT, R-SMAD, NF-κB, Notch, TUBBY, NFAT.
Classificação estrutural
Os fatores de transcrição são classificados frequentemente com base na semelhança das suas sequências e, portanto, na estrutura terciária dos seus domínios de ligação ao ADN. Distinguem-se os seguintes grupos:[76][77][78]
- 1 Superclasse: Domínios básicos
- 1.1 Classe: Fatores de fecho de leucina (bZIP)
- 1.1.1 Família: componentes do tipo AP-1; como (c-Fos/c-Jun)
- 1.1.2 Família: CREB
- 1.1.3 Família: fatores do tipo C/EBP
- 1.1.4 Família: bZIP / PAR
- 1.1.5 Família: Fatores de ligação à caixa G de plantas
- 1.1.6 Família: Apenas ZIP
- 1.2 Classe: Fatores hélice-alça-hélice (bHLH)
- 1.2.1 Família: Fatores ubíquos (classe A)
- 1.2.2 Família: Fatores de transcrição miogénica (MyoD)
- 1.2.3 Família: Achaete-Scute
- 1.2.4 Família: Tal/Twist/Atonal/Hen
- 1.3 Classe: Fatores hélice-alça-hélice / fecho de leucina (bHLH-ZIP)
- 1.3.1 Família: Fatores ubíquos bHLH-ZIP, como USF (USF1, USF2); SREBP (SREBP)
- 1.3.2 Família: Fatores que controlam o ciclo celular, como c-Myc
- 1.4 Classe: NF-1
- 1.4.1 Família: NF-1 (A, B, C, X)
- 1.5 Classe: RF-X
- 1.5.1 Família: RF-X (1, 2, 3, 4, 5, ANK)
- 1.6 Classe: bHSH
- 1.1 Classe: Fatores de fecho de leucina (bZIP)
- 2 Superclasse: Domínios de ligação ao ADN coordenadores de zinco
- 2.1 Classe: tipo dedo de zinco Cys4 do receptor nuclear
- 2.1.1 Família: recetores de hormonas esteroides
- 2.1.2 Família: Fatores do tipo receptor de hormonas tiroides
- 2.2 Classe: Diversos dedos de zinco Cys4
- 2.2.1 Família: Fatores GATA
- 2.3 Classe: Domínio dedo de zinco Cys2His2
- 2.3.1 Família: Fatores ubíquos, como TFIIIA, Sp1
- 2.3.2 Família: Reguladores do ciclo celular / desenvolvimento, como Krüppel
- 2.3.4 Família: Fatores grandes com propriedades de ligação semelhantes a NF-6B
- 2.4 Classe: Cluster Cys6 cisteína-zinco
- 2.5 Classe: Dedos de zinco de composição alternada
- 2.1 Classe: tipo dedo de zinco Cys4 do receptor nuclear
- 3 Superclasse: Hélice-volta-hélice
- 3.1 Classe: Domínio homeo
- 3.1.1 Família: Apenas domínio homeo, como Ubx
- 3.1.2 Família: Fatores com domínio POU, como Oct
- 3.1.3 Família: Domínio homeo com região LIM
- 3.1.4 Família: Domínio homeo e motivos dedo de zinco
- 3.2 Classe: Caixa pareada (paired box)
- 3.2.1 Família: Pareada (paired) e domínio homeo
- 3.2.2 Família: Apenas domínio pareado
- 3.3 Classe: Fork head / hélice alada
- 3.3.1 Família: Reguladores de desenvolvimento, como forkhead
- 3.3.2 Família: Reguladores específicos de tecidos
- 3.3.3 Família: Fatores que controlam o ciclo celular
- 3.3.0 Família: Outros reguladores
- 3.4 Classe: Fatores de choque térmico
- 3.4.1 Família: HSF
- 3.5 Classe: Clusters de triptofano
- 3.5.1 Família: Myb
- 3.5.2 Família: Ets-type
- 3.5.3 Família: fatores regulatórios do interferão
- 3.6 Classe: Domínio TEA (fator de amplificador transcricional)
- 3.6.1 Família: TEA (TEAD1, TEAD2, TEAD3, TEAD4)
- 3.1 Classe: Domínio homeo
- 4 Superclasse: Fatores de armação beta com contactos no sulco menor
- 4.1 Classe: RHR (região de homologia Rel)
- 4.1.1 Família: Rel/anquirina; NF-kappaB
- 4.1.2 Família: Apenas anquirina
- 4.1.3 Família: NFAT (Nuclear Factor of Activated T-cells, ou fatores nucleares de células T ativadas), como NFATC1, NFATC2, NFATC3)
- 4.2 Classe: STAT
- 4.2.1 Família: STAT
- 4.3 Classe: p53
- 4.3.1 Família: p53
- 4.4 Classe: Caixa MADS
- 4.4.1 Família: Reguladores de diferenciação, como (Mef2)
- 4.4.2 Família: Respondedores de sinais externos, SRF (factor de resposta sérico)
- 4.4.3 Família: Reguladores metabólicos (ARG80)
- 4.5 Classe: Fatores de transcrição barril beta hélice alfa
- 4.6 Classe: Proteínas de ligação à TATA
- 4.6.1 Família: Proteínas de ligação à TATA (TBP)
- 4.7 Classe: HMG-box
- 4.7.1 Família: genes SOX, SRY
- 4.7.2 Família: TCF-1 (TCF1)
- 4.7.3 Família: relacionados com HMG2, SSRP1
- 4.7.5 Família: MATA
- 4.8 Classe: Fatores heteroméricos CCAAT
- 4.8.1 Família: Fatores heteroméricos CCAAT
- 4.9 Classe: Grainyhead
- 4.9.1 Família: Grainyhead
- 4.10 Classe: Fatores com domínio choque frio (Cold-shock domain)
- 4.10.1 Família: csd
- 4.11 Classe: Runt
- 4.11.1 Família: Runt
- 4.1 Classe: RHR (região de homologia Rel)
- 0 Superclasse: Outros fatores de transcrição
- 0.1 Classe: Proteínas punho de cobre
- 0.2 Classe: HMGI(Y) (HMGA1)
- 0.2.1 Família: HMGI(Y)
- 0.3 Classe: Domínio bolso (pocket)
- 0.4 Classe: Fatores tipo E1A
- 0.5 Classe: Fatores AP2/relacionados com EREBP
- 0.5.1 Família: AP2
- 0.5.2 Família: EREBP
- 0.5.3 Superfamília: AP2/B3
- 0.5.3.1 Família: ARF
- 0.5.3.2 Família: ABI
- 0.5.3.3 Família: RAV
Referências
- ↑ Mitchell PJ, Tjian R (1989). «Transcriptional regulation in mammalian cells by sequence-specific DNA binding proteins». Science. 245 (4916): 371–8. PMID 2667136. doi:10.1126/science.2667136
- ↑ Ptashne M, Gann A (1997). «Transcriptional activation by recruitment». Nature. 386 (6625): 569–77. PMID 9121580. doi:10.1038/386569a0
- ↑ a b c Brivanlou AH, Darnell JE (2002). «Signal transduction and the control of gene expression». Science. 295 (5556): 813–8. PMID 11823631. doi:10.1126/science.1066355
- ↑ van Nimwegen E (2003). «Leis de escala no conteúdo funcional dos genomas» 9 ed. Tendências Genet. pp. 479–84. PMID 12957540. doi:10.1016/S0168-9525(03)00203-8
- ↑ Babu MM, Luscombe NM, Aravind L, Gerstein M, Teichmann SA (2004). Curr. Opinião. Estrutura Biologia., ed. «Estrutura e evolução das redes regulatórias transcricionais». 14: 283–91. PMID 15193307. doi:10.1016/j.sbi.2004.05.004
- ↑ Gill G (2001). «Regulation of the initiation of eukaryotic transcription». Essays Biochem. 37: 33–43. PMID 11758455
- ↑ Narlikar GJ, Fan HY, Kingston RE (2002). «Cooperation between complexes that regulate chromatin structure and transcription». Cell. 108 (4): 475–87. PMID 11909519. doi:10.1016/S0092-8674(02)00654-2
- ↑ Xu L, Glass CK, Rosenfeld MG (1999). «Coactivator and corepressor complexes in nuclear receptor function». Curr. Opin. Genet. Dev. 9 (2): 140–7. PMID 10322133. doi:10.1016/S0959-437X(99)80021-5
- ↑ Robert O. J. Weinzierl (1999). Mechanisms of Gene Expression: Structure, Function and Evolution of the Basal Transcriptional Machinery. [S.l.]: World Scientific Publishing Company. ISBN 1-86094-126-5
- ↑ Reese JC (2003). «Basal transcription factors». Current opinion in genetics & development. 13 (2): 114–8. PMID 12672487. doi:10.1016/S0959-437X(03)00013-3
- ↑ Shilatifard A, Conaway RC, Conaway JW (2003). «The RNA polymerase II elongation complex». Annual review of biochemistry. 72: 693–715. PMID 12676794. doi:10.1146/annurev.biochem.72.121801.161551
- ↑ Thomas MC, Chiang CM (2006). «The general transcription machinery and general cofactors». Critical reviews in biochemistry and molecular biology. 41 (3): 105–78. PMID 16858867. doi:10.1080/10409230600648736
- ↑ Lobe CG (1992). «Transcription factors and mammalian development». Current topics in developmental biology. Current Topics in Developmental Biology. 27: 351–83. ISBN 978-0-12-153127-0. PMID 1424766. doi:10.1016/S0070-2153(08)60539-6
- ↑ Lemons D, McGinnis W (2006). «Genomic evolution of Hox gene clusters». Science. 313 (5795): 1918–22. PMID 17008523. doi:10.1126/science.1132040
- ↑ Moens CB, Selleri L (2006). «Hox cofactors in vertebrate development». Developmental biology. 291 (2): 193–206. PMID 16515781. doi:10.1016/j.ydbio.2005.10.032
- ↑ Ottolenghi C, Uda M, Crisponi L, Omari S, Cao A, Forabosco A, Schlessinger D (2007). «Determination and stability of sex». BioEssays : news and reviews in molecular, cellular and developmental biology. 29 (1): 15–25. PMID 17187356. doi:10.1002/bies.20515
- ↑ Pawson T (1993). «Signal transduction--a conserved pathway from the membrane to the nucleus». Developmental genetics. 14 (5): 333–8. PMID 8293575. doi:10.1002/dvg.1020140502
- ↑ Osborne CK, Schiff R, Fuqua SA, Shou J (2001). «Estrogen receptor: current understanding of its activation and modulation». Clin. Cancer Res. 7 (12 Suppl): 4338s–4342s; discussão 4411s–4412s. PMID 11916222
- ↑ Shamovsky I, Nudler E (2008). «New insights into the mechanism of heat shock response activation». Cell. Mol. Life Sci. 65 (6): 855–61. PMID 18239856. doi:10.1007/s00018-008-7458-y
- ↑ Benizri E, Ginouvès A, Berra E (2008). «The magic of the hypoxia-signaling cascade». Cell. Mol. Life Sci. 65 (7–8): 1133–49. PMID 18202826. doi:10.1007/s00018-008-7472-0
- ↑ Weber LW, Boll M, Stampfl A (2004). «Maintaining cholesterol homeostasis: sterol regulatory element-binding proteins». World J. Gastroenterol. 10 (21): 3081–7. PMID 15457548 Parâmetro desconhecido
|url-arquivo=ignorado (ajuda); Parâmetro desconhecido|data-arquivo=ignorado (ajuda); Parâmetro desconhecido|data-acesso=ignorado (ajuda); Parâmetro desconhecido|url-morta=ignorado (ajuda) - ↑ Wheaton K, Atadja P, Riabowol K (1996). «Regulation of transcription factor activity during cellular aging». Biochem. Cell Biol. 74 (4): 523–34. PMID 8960358. doi:10.1139/o96-056
- ↑ Meyyappan M, Atadja PW, Riabowol KT (1996). «Regulation of gene expression and transcription factor binding activity during cellular aging». Biol. Signals. 5 (3): 130–8. PMID 8864058. doi:10.1159/000109183
- ↑ Evan G, Harrington E, Fanidi A, Land H, Amati B, Bennett M (1994). «Integrated control of cell proliferation and cell death by the c-myc oncogene». Philos. Trans. R. Soc. Lond., B, Biol. Sci. 345 (1313): 269–75. PMID 7846125. doi:10.1098/rstb.1994.0105
- ↑ Boch J, Bonas U (2010). «XanthomonasAvrBs3 Family-Type III Effectors: Discovery and Function». Annual Review of Phytopathology. 48: 419–436. PMID 19400638. doi:10.1146/annurev-phyto-080508-081936
- ↑ Moscou MJ, Bogdanove AJ (2009). «A simple cipher governs DNA recognition by TAL effectors». Science. 326 (5959). 1501 páginas. Bibcode:2009Sci...326.1501M. PMID 19933106. doi:10.1126/science.1178817
- ↑ Boch J; Scholze H; Schornack S; et al. (2009). «Breaking the code of DNA binding specificity of TAL-type III effectors». Science. 326 (5959): 1509–12. PMID 19933107. doi:10.1126/science.1178811
- ↑ Voytas DF, Joung JK (2009). «Plant science. DNA binding made easy». Science. 326 (5959): 1491–2. PMID 20007890. doi:10.1126/science.1183604
- ↑ a b Whiteside ST, Goodbourn S (1993). «Signal transduction and nuclear targeting: regulation of transcription factor activity by subcellular localisation». Journal of Cell Science. 104 (4): 949–55. PMID 8314906
- ↑ Bohmann D (1990). «Transcription factor phosphorylation: a link between signal transduction and the regulation of gene expression». Cancer cells (Cold Spring Harbor, N.Y. : 1989). 2 (11): 337–44. PMID 2149275
- ↑ Weigel NL, Moore NL (2007). «Steroid Receptor Phosphorylation: A Key Modulator of Multiple Receptor Functions». Molecular Endocrinology. 21 (10): 2311–9. PMID 17536004. doi:10.1210/me.2007-0101
- ↑ Teif V.B., Rippe K. (2009). «Predicting nucleosome positions on the DNA: combining intrinsic sequence preferences and remodeler activities». Nucleic Acids Research. 37 (17): 5641–55. PMC 2761276
 . PMID 19625488. doi:10.1093/nar/gkp610
. PMID 19625488. doi:10.1093/nar/gkp610
- ↑ Teif V.B., Rippe K.; Rippe (2010). «Statistical-mechanical lattice models for protein-DNA binding in chromatin». Journal of Physics: Condensed Matter. 22 (41). 4105 páginas. Bibcode:2010JPCM...22O4105T. arXiv:1004.5514
 . doi:10.1088/0953-8984/22/41/414105
. doi:10.1088/0953-8984/22/41/414105
- ↑ Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadaspmid9570129 - ↑ Wärnmark A, Treuter E, Wright AP, Gustafsson J-Å (2003). «Activation functions 1 and 2 of nuclear receptors: molecular strategies for transcriptional activation». Mol. Endocrinol. 17 (10): 1901–9. PMID 12893880. doi:10.1210/me.2002-0384
- ↑ Ma J, Ptashne M (1987). «A new class of yeast transcriptional activators». Cell. 51 (1): 113–9. PMID 3115591. doi:10.1016/0092-8674(87)90015-8 Sadowski I, Ma J, Triezenberg S, Ptashne M (1988). «GAL4-VP16 is an unusually potent transcriptional activator». Nature. 335 (6190): 563–4. PMID 3047590. doi:10.1038/335563a0 Sullivan SM, Horn PJ, Olson VA, Koop AH, Niu W, Ebright RH, Triezenberg SJ (1998). «Mutational analysis of a transcriptional activation region of the VP16 protein of herpes simplex virus». Nucleic Acids Res. 26 (19): 4487–96. PMC 147869
 . PMID 9742254. doi:10.1093/nar/26.19.4487Gill G, Ptashne M (1987). «Mutants of GAL4 protein altered in an activation function». Cell. 51 (1): 121–6. PMID 3115592. doi:10.1016/0092-8674(87)90016-X Hope IA, Mahadevan S, Struhl K (1988). «Structural and functional characterization of the short acidic transcriptional activation region of yeast GCN4 protein». Nature. 333 (6174): 635–40. PMID 3287180. doi:10.1038/333635a0 Hope IA, Struhl K (1986). «Functional dissection of a eukaryotic transcriptional activator protein, GCN4 of yeast». Cell. 46 (6): 885–94. PMID 3530496. doi:10.1016/0092-8674(86)90070-X Drysdale CM, Dueñas E, Jackson BM, Reusser U, Braus GH, Hinnebusch AG (1995). «The transcriptional activator GCN4 contains multiple activation domains that are critically dependent on hydrophobic amino acids». Mol. Cell. Biol. 15 (3): 1220–33. PMC 230345
. PMID 9742254. doi:10.1093/nar/26.19.4487Gill G, Ptashne M (1987). «Mutants of GAL4 protein altered in an activation function». Cell. 51 (1): 121–6. PMID 3115592. doi:10.1016/0092-8674(87)90016-X Hope IA, Mahadevan S, Struhl K (1988). «Structural and functional characterization of the short acidic transcriptional activation region of yeast GCN4 protein». Nature. 333 (6174): 635–40. PMID 3287180. doi:10.1038/333635a0 Hope IA, Struhl K (1986). «Functional dissection of a eukaryotic transcriptional activator protein, GCN4 of yeast». Cell. 46 (6): 885–94. PMID 3530496. doi:10.1016/0092-8674(86)90070-X Drysdale CM, Dueñas E, Jackson BM, Reusser U, Braus GH, Hinnebusch AG (1995). «The transcriptional activator GCN4 contains multiple activation domains that are critically dependent on hydrophobic amino acids». Mol. Cell. Biol. 15 (3): 1220–33. PMC 230345 . PMID 7862116 Regier JL, Shen F, Triezenberg SJ (1993). «Pattern of aromatic and hydrophobic amino acids critical for one of two subdomains of the VP16 transcriptional activator». Proc. Natl. Acad. Sci. U.S.A. 90 (3): 883–7. PMC 45774
. PMID 7862116 Regier JL, Shen F, Triezenberg SJ (1993). «Pattern of aromatic and hydrophobic amino acids critical for one of two subdomains of the VP16 transcriptional activator». Proc. Natl. Acad. Sci. U.S.A. 90 (3): 883–7. PMC 45774 . PMID 8381535. doi:10.1073/pnas.90.3.883
. PMID 8381535. doi:10.1073/pnas.90.3.883
- ↑ Piskacek S, Gregor M, Nemethova M, Grabner M, Kovarik P, Piskacek M (2007). «Nine-amino-acid transactivation domain: establishment and prediction utilities». Genomics. 89 (6): 756–68. PMID 17467953. doi:10.1016/j.ygeno.2007.02.003;
Martin Piskacek, Nature Precedings http://precedings.nature.com/documents/3488/version/2 (2009);
Martin Piskacek, Nature Precedings http://precedings.nature.com/documents/3939/version/1 (2009);
Martin Piskacek, Nature Precedings http://precedings.nature.com/documents/3984/version/1 (2009) - ↑ «Cópia arquivada» Parâmetro desconhecido
|data-acesso=ignorado (ajuda); Parâmetro desconhecido|data-arquivo=ignorado (ajuda); Parâmetro desconhecido|url-morta=ignorado (ajuda); Parâmetro desconhecido|url-arquivo=ignorado (ajuda) - ↑ «Cópia arquivada». Arquivado do original em
|arquivourl=requer|arquivodata=(ajuda) Parâmetro desconhecido|data-acesso=ignorado (ajuda); Parâmetro desconhecido|dataarquivo=ignorado (ajuda) - ↑ Uesugi M, Verdine GL (1999). «The alpha-helical FXXΦΦ motif in p53: TAF interaction and discrimination by MDM2». Proc. Natl. Acad. Sci. U.S.A. 96 (26): 14801–6. PMC 24728
 . PMID 10611293. doi:10.1073/pnas.96.26.14801; Uesugi M, Nyanguile O, Lu H, Levine AJ, Verdine GL (1997). «Induced alpha helix in the VP16 activation domain upon binding to a human TAF». Science. 277 (5330): 1310–3. PMID 9271577. doi:10.1126/science.277.5330.1310; Choi Y, Asada S, Uesugi M (2000). «Divergent hTAFII31-binding motifs hidden in activation domains». J. Biol. Chem. 275 (21): 15912–6. PMID 10821850. doi:10.1074/jbc.275.21.15912; Lee CW, Arai M, Martinez-Yamout MA, Dyson HJ, Wright PE (2009). «Mapping the interactions of the p53 transactivation domain with the KIX domain of CBP». Biochemistry. 48 (10): 2115–24. PMC 2765525
. PMID 10611293. doi:10.1073/pnas.96.26.14801; Uesugi M, Nyanguile O, Lu H, Levine AJ, Verdine GL (1997). «Induced alpha helix in the VP16 activation domain upon binding to a human TAF». Science. 277 (5330): 1310–3. PMID 9271577. doi:10.1126/science.277.5330.1310; Choi Y, Asada S, Uesugi M (2000). «Divergent hTAFII31-binding motifs hidden in activation domains». J. Biol. Chem. 275 (21): 15912–6. PMID 10821850. doi:10.1074/jbc.275.21.15912; Lee CW, Arai M, Martinez-Yamout MA, Dyson HJ, Wright PE (2009). «Mapping the interactions of the p53 transactivation domain with the KIX domain of CBP». Biochemistry. 48 (10): 2115–24. PMC 2765525 . PMID 19220000. doi:10.1021/bi802055v; Goto NK, Zor T, Martinez-Yamout M, Dyson HJ, Wright PE (2002). «Cooperativity in transcription factor binding to the coactivator CREB-binding protein (CBP). The mixed lineage leukemia protein (MLL) activation domain binds to an allosteric site on the KIX domain». J. Biol. Chem. 277 (45): 43168–74. PMID 12205094. doi:10.1074/jbc.M207660200; Radhakrishnan I, Pérez-Alvarado GC, Parker D, Dyson HJ, Montminy MR, Wright PE (1997). «Solution structure of the KIX domain of CBP bound to the transactivation domain of CREB: a model for activator:coactivator interactions». Cell. 91 (6): 741–52. PMID 9413984. doi:10.1016/S0092-8674(00)80463-8; Zor T, Mayr BM, Dyson HJ, Montminy MR, Wright PE (2002). «Roles of phosphorylation and helix propensity in the binding of the KIX domain of CREB-binding protein by constitutive (c-Myb) and inducible (CREB) activators». J. Biol. Chem. 277 (44): 42241–8. PMID 12196545. doi:10.1074/jbc.M207361200; Brüschweiler S, Schanda P, Kloiber K, Brutscher B, Kontaxis G, Konrat R, Tollinger M (2009). «Direct observation of the dynamic process underlying allosteric signal transmission». J. Am. Chem. Soc. 131 (8): 3063–8. PMID 19203263. doi:10.1021/ja809947w; Liu GH, Qu J, Shen X (2008). «NF-kappaB/p65 antagonizes Nrf2-ARE pathway by depriving CBP from Nrf2 and facilitating recruitment of HDAC3 to MafK». Biochim. Biophys. Acta. 1783 (5): 713–27. PMID 18241676. doi:10.1016/j.bbamcr.2008.01.002; Bayly R, Murase T, Hyndman BD, Savage R, Nurmohamed S, Munro K, Casselman R, Smith SP, LeBrun DP (2006). «Critical role for a single leucine residue in leukemia induction by E2A-PBX1». Mol. Cell. Biol. 26 (17): 6442–52. PMC 1592826
. PMID 19220000. doi:10.1021/bi802055v; Goto NK, Zor T, Martinez-Yamout M, Dyson HJ, Wright PE (2002). «Cooperativity in transcription factor binding to the coactivator CREB-binding protein (CBP). The mixed lineage leukemia protein (MLL) activation domain binds to an allosteric site on the KIX domain». J. Biol. Chem. 277 (45): 43168–74. PMID 12205094. doi:10.1074/jbc.M207660200; Radhakrishnan I, Pérez-Alvarado GC, Parker D, Dyson HJ, Montminy MR, Wright PE (1997). «Solution structure of the KIX domain of CBP bound to the transactivation domain of CREB: a model for activator:coactivator interactions». Cell. 91 (6): 741–52. PMID 9413984. doi:10.1016/S0092-8674(00)80463-8; Zor T, Mayr BM, Dyson HJ, Montminy MR, Wright PE (2002). «Roles of phosphorylation and helix propensity in the binding of the KIX domain of CREB-binding protein by constitutive (c-Myb) and inducible (CREB) activators». J. Biol. Chem. 277 (44): 42241–8. PMID 12196545. doi:10.1074/jbc.M207361200; Brüschweiler S, Schanda P, Kloiber K, Brutscher B, Kontaxis G, Konrat R, Tollinger M (2009). «Direct observation of the dynamic process underlying allosteric signal transmission». J. Am. Chem. Soc. 131 (8): 3063–8. PMID 19203263. doi:10.1021/ja809947w; Liu GH, Qu J, Shen X (2008). «NF-kappaB/p65 antagonizes Nrf2-ARE pathway by depriving CBP from Nrf2 and facilitating recruitment of HDAC3 to MafK». Biochim. Biophys. Acta. 1783 (5): 713–27. PMID 18241676. doi:10.1016/j.bbamcr.2008.01.002; Bayly R, Murase T, Hyndman BD, Savage R, Nurmohamed S, Munro K, Casselman R, Smith SP, LeBrun DP (2006). «Critical role for a single leucine residue in leukemia induction by E2A-PBX1». Mol. Cell. Biol. 26 (17): 6442–52. PMC 1592826 . PMID 16914730. doi:10.1128/MCB.02025-05; García-Rodríguez C, Rao A (1998). «Nuclear factor of activated T cells (NFAT)-dependent transactivation regulated by the coactivators p300/CREB-binding protein (CBP)». J. Exp. Med. 187 (12): 2031–6. PMC 2212364
. PMID 16914730. doi:10.1128/MCB.02025-05; García-Rodríguez C, Rao A (1998). «Nuclear factor of activated T cells (NFAT)-dependent transactivation regulated by the coactivators p300/CREB-binding protein (CBP)». J. Exp. Med. 187 (12): 2031–6. PMC 2212364 . PMID 9625762. doi:10.1084/jem.187.12.2031; Mink S, Haenig B, Klempnauer KH (1997). «Interaction and functional collaboration of p300 and C/EBPbeta». Mol. Cell. Biol. 17 (11): 6609–17. PMC 232514
. PMID 9625762. doi:10.1084/jem.187.12.2031; Mink S, Haenig B, Klempnauer KH (1997). «Interaction and functional collaboration of p300 and C/EBPbeta». Mol. Cell. Biol. 17 (11): 6609–17. PMC 232514 . PMID 9343424; Piskacek S, Gregor M, Nemethova M, Grabner M, Kovarik P, Piskacek M (2007). «Nine-amino-acid transactivation domain: establishment and prediction utilities». Genomics. 89 (6): 756–68. PMID 17467953. doi:10.1016/j.ygeno.2007.02.003
. PMID 9343424; Piskacek S, Gregor M, Nemethova M, Grabner M, Kovarik P, Piskacek M (2007). «Nine-amino-acid transactivation domain: establishment and prediction utilities». Genomics. 89 (6): 756–68. PMID 17467953. doi:10.1016/j.ygeno.2007.02.003
- ↑ Teufel DP, Freund SM, Bycroft M, Fersht AR (2007). «Four domains of p300 each bind tightly to a sequence spanning both transactivation subdomains of p53». Proc. Natl. Acad. Sci. U.S.A. 104 (17): 7009–14. PMC 1855428
 . PMID 17438265. doi:10.1073/pnas.0702010104Teufel DP, Bycroft M, Fersht AR (2009). «Regulation by phosphorylation of the relative affinities of the N-terminal transactivation domains of p53 for p300 domains and Mdm2». Oncogene. 28 (20): 2112–8. PMC 2685776
. PMID 17438265. doi:10.1073/pnas.0702010104Teufel DP, Bycroft M, Fersht AR (2009). «Regulation by phosphorylation of the relative affinities of the N-terminal transactivation domains of p53 for p300 domains and Mdm2». Oncogene. 28 (20): 2112–8. PMC 2685776 . PMID 19363523. doi:10.1038/onc.2009.71Feng H, Jenkins LM, Durell SR, Hayashi R, Mazur SJ, Cherry S, Tropea JE, Miller M, Wlodawer A, Appella E, Bai Y (2009). «Structural Basis for p300 Taz2/p53 TAD1 Binding and Modulation by Phosphorylation». Structure. 17 (2): 202–10. PMC 2705179
. PMID 19363523. doi:10.1038/onc.2009.71Feng H, Jenkins LM, Durell SR, Hayashi R, Mazur SJ, Cherry S, Tropea JE, Miller M, Wlodawer A, Appella E, Bai Y (2009). «Structural Basis for p300 Taz2/p53 TAD1 Binding and Modulation by Phosphorylation». Structure. 17 (2): 202–10. PMC 2705179 . PMID 19217391. doi:10.1016/j.str.2008.12.009Ferreon JC, Lee CW, Arai M, Martinez-Yamout MA, Dyson HJ, Wright PE (2009). «Cooperative regulation of p53 by modulation of ternary complex formation with CBP/p300 and HDM2». Proc. Natl. Acad. Sci. U.S.A. 106 (16): 6591–6. PMC 2672497
. PMID 19217391. doi:10.1016/j.str.2008.12.009Ferreon JC, Lee CW, Arai M, Martinez-Yamout MA, Dyson HJ, Wright PE (2009). «Cooperative regulation of p53 by modulation of ternary complex formation with CBP/p300 and HDM2». Proc. Natl. Acad. Sci. U.S.A. 106 (16): 6591–6. PMC 2672497 . PMID 19357310. doi:10.1073/pnas.0811023106Gamper AM, Roeder RG (2008). «Multivalent Binding of p53 to the STAGA Complex Mediates Coactivator Recruitment after UV Damage». Mol. Cell. Biol. 28 (8): 2517–27. PMC 2293101
. PMID 19357310. doi:10.1073/pnas.0811023106Gamper AM, Roeder RG (2008). «Multivalent Binding of p53 to the STAGA Complex Mediates Coactivator Recruitment after UV Damage». Mol. Cell. Biol. 28 (8): 2517–27. PMC 2293101 . PMID 18250150. doi:10.1128/MCB.01461-07
. PMID 18250150. doi:10.1128/MCB.01461-07
- ↑ T. Fukasawa, M. Fukuma, K. Yano, and H. Sakurai, DNA Res 8 (1), 23 (2001); L. Badi and A. Barberis, Mol Genet Genomics 265 (6), 1076 (2001); Y. J. Kim, S. Bjorklund, Y. Li, M. H. Sayre, and R. D. Kornberg, Cell 77 (4), 599 (1994); Y. Suzuki, Y. Nogi, A. Abe, and T. Fukasawa, Mol Cell Biol 8 (11), 4991 (1988); J. S. Fassler and F. Winston, Mol Cell Biol 9 (12), 5602 (1989); J. M. Park, H. S. Kim, S. J. Han, M. S. Hwang, Y. C. Lee, and Y. J. Kim, Mol Cell Biol 20 (23), 8709 (2000); Z. Lu, A. Z. Ansari, X. Lu, A. Ogirala, and M. Ptashne, Proc Natl Acad Sci U S A 99 (13), 8591 (2002); M. J. Swanson, H. Qiu, L. Sumibcay et al., Mol Cell Biol 23 (8), 2800 (2003); G. O. Bryant and M. Ptashne, Mol Cell 11 (5), 1301 (2003); J. Fishburn, N. Mohibullah, and S. Hahn, Mol Cell 18 (3), 369 (2005); M. K. Lim, V. Tang, A. Le Saux, J. Schuller, C. Bongards, and N. Lehming, J Mol Biol 374 (1), 9 (2007); S. Lallet, H. Garreau, C. Garmendia-Torres, D. Szestakowska, E. Boy-Marcotte, S. Quevillon-Cheruel, and M. Jacquet, Molecular microbiology 62 (2), 438 (2006); M. Dietz, W. T. Heyken, J. Hoppen, S. Geburtig, and H. J. Schuller, Molecular microbiology 48 (4), 1119 (2003); T. Mizuno and S. Harashima, Mol Genet Genomics 269 (1), 68 (2003); J. K. Thakur, H. Arthanari, F. Yang et al., Nature 452 (7187), 604 (2008); J. K. Thakur, H. Arthanari, F. Yang, K. H. Chau, G. Wagner, and A. M. Naar, J Biol Chem 284 (7), 4422 (2009).
- ↑ J. Klein, M. Nolden, S. L. Sanders, J. Kirchner, P. A. Weil, and K. Melcher, J Biol Chem 278 (9), 6779 (2003).C. M. Drysdale, E. Duenas, B. M. Jackson, U. Reusser, G. H. Braus, and A. G. Hinnebusch, Mol Cell Biol 15 (3), 1220 (1995); E. Milgrom, R. W. West, Jr., C. Gao, and W. C. Shen, Genetics 171 (3), 959 (2005).
- ↑ Martin Piskacek, Nature Precedings http://precedings.nature.com/documents/3488/version/2 (2009); Martin Piskacek, Nature Precedings doi:10.1038/npre.2009.3939.1 (2009); S. Piskacek, M. Gregor, M. Nemethova, M. Grabner, P. Kovarik, and M. Piskacek, Genomics 89 (6), 756 (2007).
- ↑ Littlewood TD, Evan GI (1995). «Transcription factors 2: helix-loop-helix». Protein profile. 2 (6): 621–702. PMID 7553065
- ↑ Vinson C, Myakishev M, Acharya A, Mir AA, Moll JR, Bonovich M (2002). «Classification of Human B-ZIP Proteins Based on Dimerization Properties». Molecular and Cellular Biology. 22 (18): 6321–35. PMC 135624
 . PMID 12192032. doi:10.1128/MCB.22.18.6321-6335.2002
. PMID 12192032. doi:10.1128/MCB.22.18.6321-6335.2002
- ↑ Wintjens R, Rooman M (1996). «Structural classification of HTH DNA-binding domains and protein-DNA interaction modes». Journal of Molecular Biology. 262 (2): 294–313. PMID 8831795. doi:10.1006/jmbi.1996.0514
- ↑ Gehring WJ, Affolter M, Bürglin T (1994). «Homeodomain proteins». Annual review of biochemistry. 63: 487–526. PMID 7979246. doi:10.1146/annurev.bi.63.070194.002415
- ↑ Dahl E, Koseki H, Balling R (1997). «Pax genes and organogenesis». BioEssays : news and reviews in molecular, cellular and developmental biology. 19 (9): 755–65. PMID 9297966. doi:10.1002/bies.950190905
- ↑ Laity JH, Lee BM, Wright PE (2001). «Zinc finger proteins: new insights into structural and functional diversity». Current opinion in structural biology. 11 (1): 39–46. PMID 11179890. doi:10.1016/S0959-440X(00)00167-6
- ↑ Wolfe SA, Nekludova L, Pabo CO (2000). «DNA recognition by Cys2His2 zinc finger proteins». Annual review of biophysics and biomolecular structure. 29: 183–212. PMID 10940247. doi:10.1146/annurev.biophys.29.1.183
- ↑ Wang JC (2005). «Finding primary targets of transcriptional regulators». Cell Cycle. 4 (3): 356–8. PMID 15711128. doi:10.4161/cc.4.3.1521
- ↑ Semenza, Gregg L. (1999). Transcription factors and human disease. Oxford [Oxfordshire]: Oxford University Press. ISBN 0-19-511239-3
- ↑ Libermann TA, Zerbini LF (2006). «Targeting transcription factors for cancer gene therapy». Curr Gene Ther. 6 (1): 17–33. PMID 16475943. doi:10.2174/156652306775515501
- ↑ Moretti P, Zoghbi HY (2006). «MeCP2 dysfunction in Rett syndrome and related disorders». Curr. Opin. Genet. Dev. 16 (3): 276–81. PMID 16647848. doi:10.1016/j.gde.2006.04.009
- ↑ Chadwick LH, Wade PA (2007). «MeCP2 in Rett syndrome: transcriptional repressor or chromatin architectural protein?». Curr. Opin. Genet. Dev. 17 (2): 121–5. PMID 17317146. doi:10.1016/j.gde.2007.02.003
- ↑ Maestro MA, Cardalda C, Boj SF, Luco RF, Servitja JM, Ferrer J (2007). «Distinct roles of HNF1beta, HNF1alpha, and HNF4alpha in regulating pancreas development, beta-cell function and growth». Endocr Dev. 12: 33–45. PMID 17923767. doi:10.1159/000109603
- ↑ Al-Quobaili F, Montenarh M (2008). «Pancreatic duodenal homeobox factor-1 and diabetes mellitus type 2 (review)». Int. J. Mol. Med. 21 (4): 399–404. PMID 18360684
- ↑ Lennon PA, Cooper ML, Peiffer DA, Gunderson KL, Patel A, Peters S, Cheung SW, Bacino CA (2007). «Deletion of 7q31.1 supports involvement of FOXP2 in language impairment: clinical report and review». Am. J. Med. Genet. A. 143A (8): 791–8. PMID 17330859. doi:10.1002/ajmg.a.31632
- ↑ van der Vliet HJ, Nieuwenhuis EE (2007). «IPEX as a Result of Mutations in FOXP3». Clin. Dev. Immunol. 2007. 89017 páginas. PMC 2248278
 . PMID 18317533. doi:10.1155/2007/89017
. PMID 18317533. doi:10.1155/2007/89017
- ↑ Iwakuma T, Lozano G, Flores ER (2005). «Li-Fraumeni syndrome: a p53 family affair». Cell Cycle. 4 (7): 865–7. PMID 15917654. doi:10.4161/cc.4.7.1800
- ↑ http://ajp.amjpathol.org/cgi/content/full/165/5/1449 Arquivado em 2004-11-07 na Archive.today "Roles and Regulation of Stat Family Transcription Factors in Human Breast Cancer" 2004
- ↑ http://www.ias.surrey.ac.uk/reports/hox-report.html Arquivado em 2012-05-25 no Wayback Machine "Transcription factors as targets and markers in cancer" Workshop 2007
- ↑ Overington JP, Al-Lazikani B, Hopkins AL (2006). «How many drug targets are there?». Nature reviews. Drug discovery. 5 (12): 993–6. PMID 17139284. doi:10.1038/nrd2199
- ↑ Gronemeyer H, Gustafsson JA, Laudet V (2004). «Principles for modulation of the nuclear receptor superfamily». Nat Rev Drug Discov. 3 (11): 950–64. PMID 15520817. doi:10.1038/nrd1551
- ↑ Bustin SA, McKay IA (1994). «Transcription factors: targets for new designer drugs». Br. J. Biomed. Sci. 51 (2): 147–57. PMID 8049612
- ↑ Butt TR, Karathanasis SK (1995). «Transcription factors as drug targets: opportunities for therapeutic selectivity». Gene Expr. 4 (6): 319–36. PMID 7549464
- ↑ Papavassiliou AG (1998). «Transcription-factor-modulating agents: precision and selectivity in drug design». Mol Med Today. 4 (8): 358–66. PMID 9755455. doi:10.1016/S1357-4310(98)01303-3
- ↑ Ghosh D, Papavassiliou AG (2005). «Transcription factor therapeutics: long-shot or lodestone». Curr. Med. Chem. 12 (6): 691–701. PMID 15790306. doi:10.2174/0929867053202197
- ↑ Moellering RE, Cornejo M, Davis TN, Del Bianco C, Aster JC, Blacklow SC, Kung AL, Gilliland DG, Verdine GL, Bradner JE (2009). «Direct inhibition of the NOTCH transcription factor complex». Nature. 462 (7270): 182–8. PMC 2951323
 . PMID 19907488. doi:10.1038/nature08543. Resumo divulgativo – The Scientist
. PMID 19907488. doi:10.1038/nature08543. Resumo divulgativo – The Scientist
- ↑ EntrezGene database
- ↑ Wenta N, Strauss H, Meyer S, Vinkemeier U (2008). «Tyrosine phosphorylation regulates the partitioning of STAT1 between different dimer conformations». Proc Natl Acad Sci U S A. 105 (27): 9238–43. PMC 2453697
 . PMID 18591661. doi:10.1073/pnas.0802130105
. PMID 18591661. doi:10.1073/pnas.0802130105
- ↑ Sermeus A, Cosse JP, Crespin M, Mainfroid V, de Longueville F, Ninane N, Raes M, Remacle J, Michiels C (2008). «Hypoxia induces protection against etoposide-induced apoptosis: molecular profiling of changes in gene expression and transcription factor activity». Mol Cancer. 7. 27 páginas. PMC 2330149
 . PMID 18366759. doi:10.1186/1476-4598-7-27
. PMID 18366759. doi:10.1186/1476-4598-7-27
- ↑ Orphanides G, Lagrange T, Reinberg D (1996). «The general transcription factors of RNA polymerase II». Genes Dev. 10 (21): 2657–83. PMID 8946909. doi:10.1101/gad.10.21.2657
- ↑ a b Walter F., PhD. Boron (2003). Medical Physiology: A Cellular And Molecular Approaoch. [S.l.]: Elsevier/Saunders. pp. 125–126. ISBN 1-4160-2328-3
- ↑ Stegmaier P, Kel AE, Wingender E (2004). «Systematic DNA-binding domain classification of transcription factors». Genome informatics. International Conference on Genome Informatics. 15 (2): 276–86. PMID 15706513. Consultado em 5 de outubro de 2012. Arquivado do original em 19 de junho de 2013
- ↑ Matys V, Kel-Margoulis OV, Fricke E, Liebich I, Land S, Barre-Dirrie A, Reuter I, Chekmenev D, Krull M, Hornischer K, Voss N, Stegmaier P, Lewicki-Potapov B, Saxel H, Kel AE, Wingender E (2006). «TRANSFAC® and its module TRANSCompel®: transcriptional gene regulation in eukaryotes». Nucleic Acids Res. 34 (Database issue): D108–10. PMC 1347505
 . PMID 16381825. doi:10.1093/nar/gkj143
. PMID 16381825. doi:10.1093/nar/gkj143
- ↑ «TRANSFAC database». Consultado em 5 de agosto de 2007