Histona
As histonas são proteínas responsáveis por interagir com o DNA de modo a dispor da organização da dupla fita, nos três níveis de condensação, de modo favorável à célula, bem como também ter parte junto à modulação da expressão gênica, eis que, por exemplo, no caso dos nucleossomos, o primeiro nível de condensação do DNA, certas histonas compõem a “conta” da estrutura de “colar de contas”.
As histonas H2A, H2B, H3 e H4 compõem a “conta” do nucleossomo, enovelando uma fita de DNA, dificultando assim que a transcrição ocorra nos genes contidos na parte da fita enovelada nessa parte, em contrapartida com o “linker” DNA (DNA ligante), que está livre entre as “contas” de nucleossomo, para que favoreça a transcrição dos genes que contém. Esse processo de movimentação das “contas” do “colar de contas”, os nucleossomos em um sentido mais estrito, expõe regiões para transcrição mais fácil, enquanto “recolhe”, retira regiões do DNA antes do “linker” DNA, para compor as 1,7 voltas sobre o nucleossomo; tendo a atuação da histona H1, eis que ela não é a parte diretamente circundada pela fita de DNA, porém permanece relacionada ao nucleossomo interagindo com outros fatores para que ocorra tal movimentação do nucleossomo.
A histona H1 também desempenha um papel fundamental para que ocorra o empacotamento em “zig-zag” das fibras de cromatina de 30 nanômetros, o segundo grau de condensação do DNA, anterior à formação dos cromossomos, compostos por tais fibras ainda mais condensadas, sendo assim essencial para que ocorra a divisão celular.
Histonas de Archaea são semelhantes as dos eucariotos. [2]
Classes de histonas
A sequência de aminoácidos das histonas está muito conservada evolutivamente e estas podem ser agrupadas em cinco classes principais: H1/H5, H2A, H2B, H3 e H4.[1][2][3] Estes 5 tipos estão agrupados nas duas superclasses seguintes:
Histonas do octâmero ou histonas nucleares (core) – H2A, H2B, H3 e H4.
Histonas de união ou histonas de ligação (linker) – H1 e H5.
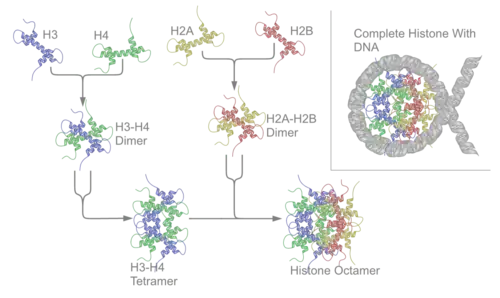
Cada uma das histonas core associa-se a outra igual, e depois agrupam-se todas para formar os octâmeros dos nucleossomas, originando uma espécie de carretel no qual se enrolam 147 pares de bases de ADN, formando uma super-hélice que se enrola para a esquerda e dá 1,65 voltas ao carretel.[4]
As histonas de ligação H1 unem-se ao nucleossoma e aos pontos de entrada e saída do ADN do octâmero, de maneira a fixarem o ADN no seu lugar,[5] o que permite a formação de uma estrutura de ordem superior. A mais básica dessas estruturas é a fibra de 10 nm da cromatina ou conformação em "colar de contas". Isto implica o enrolamento do ADN em torno dos nucleossomas deixando um trecho de ADN de aproximadamente 50 pares de bases que separa cada dois nucleossomas, chamado ADN ligador ou espaçador.
O conjunto das histonas montadas e o ADN chama-se cromatina. As estruturas de ordem superior que a cromatina pode formar são a fibra cromatínica de 30 nm (que forma um zigue-zague irregular) e a fibra de 100 nm, que se podem encontrar em células interfásicas. Durante a mitose e a meiose, uma maior condensação da cromatina origina os cromossomas, formados pelas interações entre os nucleossomas e outras proteínas reguladoras.
A seguinte é uma lista das proteínas histonas humanas:
| Superfamília | Família | Subfamília | Membros |
|---|---|---|---|
| Histonas de ligação (linker) | |||
| H1 | |||
| H1F | H1F0, H1FNT, H1FOO, H1FX | ||
| H1H1 | HIST1H1A, HIST1H1B, HIST1H1C, HIST1H1D, HIST1H1E, HIST1H1T | ||
| Histonas do octámero (core) | |||
| H2A | |||
| H2AF | H2AFB1, H2AFB2, H2AFB3, H2AFJ, H2AFV, H2AFX, H2AFY, H2AFY2, H2AFZ | ||
| H2A1 | HIST1H2AA, HIST1H2AB, HIST1H2AC, HIST1H2AD, HIST1H2AE, HIST1H2AG, HIST1H2AI, HIST1H2AJ, HIST1H2AK, HIST1H2AL, HIST1H2AM | ||
| H2A2 | HIST2H2AA3, HIST2H2AC | ||
| H2B | |||
| H2BF | H2BFM, H2BFO, H2BFS, H2BFWT | ||
| H2B1 | HIST1H2BA, HIST1H2BB, HIST1H2BC, HIST1H2BD, HIST1H2BE, HIST1H2BF, HIST1H2BG, HIST1H2BH, HIST1H2BI, HIST1H2BJ, HIST1H2BK, HIST1H2BL, HIST1H2BM, HIST1H2BN, HIST1H2BO | ||
| H2B2 | HIST2H2BE | ||
| H3 | |||
| H3A1 | HIST1H3A, HIST1H3B, HIST1H3C, HIST1H3D, HIST1H3E, HIST1H3F, HIST1H3G, HIST1H3H, HIST1H3I, HIST1H3J | ||
| H3A2 | HIST2H3C | ||
| H3A3 | HIST3H3 | ||
| H4 | |||
| H41 | HIST1H4A, HIST1H4B, HIST1H4C, HIST1H4D, HIST1H4E, HIST1H4F, HIST1H4G, HIST1H4H, HIST1H4I, HIST1H4J, HIST1H4K, HIST1H4L | ||
| H44 | HIST4H4 |
Funções
As histonas funcionam como a matriz na qual o DNA se enrola. Têm um papel importante na regulação dos genes. Por meio do seu enrolar exibir zonas de DNA ligante que são mais propícias à transcrição do que zonas que compõem o nucleossomo, bem como o seu “recolher” de DNA ligante implica em silenciamento. Ao compactarem o DNA, permitem que os genomas eucarióticos de grandes dimensões caibam dentro do núcleo das células. Podem sofrer modificações pós-traducionais. Estas modificações podem desempenhar um papel importante na regulação dos genes, de maneira epigenética. A regulação ocorre na caixa TATA.
Estrutura
As histonas são produzidas no citoplasma e importadas para o núcleo da célula. Ricas em lisina e arginina. São solúveis em água. Estão sujeitas a modificações pós-traducionais, essencialmente N-terminais, mas também nos domínios globulares. Exemplos de modicações deste tipo são: metilação, acetilação, fosforilação e ubiquitilação
Geralmente, os genes mais ativos têm menos histonas ligadas. Durante a interfase, as histonas estão intimamente associadas a genes inactivos.
A estrutura das histonas tem sido bem conservada em termos evolutivos, eis que ao desempenharem papeis tão vitais, estão sobre pressão de seleção estabilizadora. A mais conservada é a histona H4. [4]
História
As histonas foram descobertas em 1884 por Albrecht Kossel. A palavra "histona" é datada do fim do século XIX e deriva da palavra alemã "Histon", de origem incerta: talvez do grego histanai ou de histos. Até a decada de 1990, as histonas eram vistas somente como matriz para o enrolamento do material genético (DNA). Só a partir dessa altura foi descoberto o papel regulador das histonas.
Ver também
Referências
- ↑ Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadasNelson&Cox - ↑ Bhasin M, Reinherz EL, Reche PA (2006). «Recognition and classification of histones using support vector machine». J. Comput. Biol. 13 (1). PMID 16472024. doi:10.1089/cmb.2006.13.102 Parâmetro desconhecido
|páxinas=ignorado (ajuda) - ↑ Hartl, Daniel L., Freifelder, David Snyder, Leon A. (1988). Basic Genetics. [S.l.]: Jones and Bartlett Publishers - Boston. ISBN 0-86720-090-1
- ↑ Luger K, Mäder AW, Richmond RK, Sargent DF, Richmond TJ (1997). «Crystal structure of the nucleosome core particle at 2.8 A resolution». Nature. 389 (6648). PMID 9305837. doi:10.1038/38444 Parâmetro desconhecido
|páxinas=ignorado (ajuda) PDB 1AOI - ↑ Farkas, Daniel (1996). DNA simplified: the hitchhiker's guide to DNA. Washington, D.C: AACC Press. ISBN 0-915274-84-1
1. ALBERTS, Bruce et al. Biologia molecular da célula. Artmed Editora, 2010.
2. PEREIRA, Suzette L. et al. Archaeal nucleosomes. Proceedings of the National Academy of Sciences, v. 94, n. 23, p. 12633-12637, 1997.
3. ↑ Ir para:a b «Nucleossomo». Consultado em 1 de setembro de 20134. MARIÑO-RAMÍREZ, Leonardo et al. Histone structure and nucleosome stability. Expert review of proteomics, v. 2, n. 5, p. 719-729, 2005.