Suillus bovinus
Suillus bovinus
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Estado de conservação | |||||||||||||||||
 Pouco preocupante (IUCN 3.1) [1] | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Suillus bovinus (L.) Roussel (1806) | |||||||||||||||||
| Sinónimos[2] | |||||||||||||||||
| |||||||||||||||||
Suillus bovinus é uma espécie de cogumelo boleto do gênero Suillus na família Suillaceae. Um fungo comum nativo da Europa e Ásia, foi introduzido na América do Norte e na Austrália. Inicialmente descrito como Boletus bovinus por Carlos Lineu em 1753, recebeu seu nome binomial atual por Henri François Anne de Roussel em 1806. É um cogumelo comestível, embora não seja altamente valorizado.
O fungo cresce em florestas de coníferas em sua área nativa e em plantações de pinheiros em países onde se naturalizou. Forma associações ectomicorrízicas simbióticas com árvores vivas, envolvendo as raízes subterrâneas com bainhas de tecido fúngico, e às vezes é parasitado pelo cogumelo relacionado Gomphidius roseus [en]. Suillus bovinus produz basidiomas que carregam esporos, frequentemente em grande número, acima do solo. O cogumelo possui um píleo convexo cinza-amarelado ou ocre que atinge até 10 cm de diâmetro e se achata com a idade. Como outros boletos, apresenta tubos que se estendem para baixo a partir da parte inferior do píleo, em vez de lamelas; os esporos escapam na maturidade pelas aberturas dos tubos, ou poros. A superfície porada é amarela. O estipe, mais delgado que o de outros boletos Suillus, não possui anel.
Taxonomia
Suillus bovinus foi uma das muitas espécies descritas inicialmente em 1753 pelo "pai da taxonomia" Carlos Lineu, que, no segundo volume de sua obra Species Plantarum, deu-lhe o nome Boletus bovinus.[3] O epíteto específico deriva da palavra em latim bos, que significa "gado".[4] O fungo foi reclassificado (e tornou-se a espécie-tipo) do gênero Suillus pelo naturalista francês Henri François Anne de Roussel em 1796.[5] Suillus é um termo antigo para fungos, derivado da palavra "porco".[6] Lucien Quélet classificou-o como Viscipellis bovina em 1886.[7]
Em trabalhos publicados antes de 1987, a espécie era escrita completamente como Suillus bovinus (L.:Fr.) Kuntze, pois a descrição de Lineu havia sido sancionada em 1821 pelo "pai da micologia", o naturalista sueco Elias Magnus Fries. A data de início para todos os fungos havia sido estabelecida por acordo geral como 1º de janeiro de 1821, data do trabalho de Fries. Além disso, como a descrição de Roussel para Suillus também era anterior a isso, a autoridade para o gênero era atribuída a Otto Kuntze. A edição de 1987 do Código Internacional de Nomenclatura Botânica alterou as regras sobre a data de início e o trabalho primário para nomes de fungos, e os nomes agora podem ser considerados válidos até 1º de maio de 1753, data da publicação do trabalho de Lineu.[8]
Uma origem proposta para o nome científico é que cavaleiros medievais — que reverenciavam Tricholoma equestre — consideravam este cogumelo adequado apenas para vaqueiros, pois não era altamente valorizado.[9] A cor do cogumelo é semelhante à de uma vaca jersey.[10]
Uma amostragem genética limitada de espécies em um estudo de 1996 por Annette Kretzer e colegas mostrou que Suillus bovinus estava relacionada a uma linhagem que divergiu para S. punctipes, S. variegatus e S. tomentosus.[11] Um estudo de 2001 descobriu que não estava intimamente relacionada a outras espécies europeias, e que todas as populações testadas eram mais próximas umas das outras do que de qualquer outra, sendo, portanto, uma espécie coesa.[12]
O micologista tcheco Josef Šutara circunscreveu o gênero Mariaella em 1987, designando Mariaella bovina como espécie-tipo.[13] Mariaella continha espécies de Suillus na seção Fungosi. Estudos moleculares não apoiam a existência de Mariaella, sendo considerado sinônimo de Suillus.[14] Sinônimos mais antigos para S. bovinus incluem aqueles resultantes de transferências genéricas para Agaricus por Jean-Baptiste Lamarck em 1783, e o agora obsoleto Ixocomus por Lucien Quélet em 1888.[2]
Em 1951, Arthur Anselm Pearson descreveu a variedade Boletus bovinus var. viridocaerulescens,[15] que foi posteriormente transferida para Suillus por Rolf Singer em 1961.[16] Essa variante, coletada na Província do Cabo Ocidental, África do Sul, difere da forma principal pela reação de coloração da carne do píleo, que se torna verde-azulada escura ou clara ao ser machucada.[15] O Index Fungorum, no entanto, não reconhece a variedade como tendo significado taxonômico independente.[17]
Análise química de pigmentos e cromogênios mostrou que Suillus estava mais relacionado a Gomphidius [en] e Rhizopogon do que a outros boletos, e assim Suillus bovinus e seus aliados foram transferidos da Boletaceae para a família recém-circunscrita Suillaceae em 1997.[18] Estudos de filogenética molecular reforçaram o quão distantemente relacionados esses fungos estão de Boletus edulis e seus aliados.[19]
Descrição

O basidioma — coloquialmente chamado de cogumelo — de Suillus bovinus é menor e mais delicado que a maioria dos outros boletos.[9] O píleo é inicialmente convexo, depois plano com margem ondulada e é cinza-amarelado ou ocre com tom rosado em alguns espécimes. Varia de 3 a 10 cm de diâmetro e possui uma pileipellis pegajosa.[20] A carne é esbranquiçada, amarelada ou cor de argila e tem cheiro frutado.[20] Às vezes adquire tom rosado ao ser machucada;[9] a carne é esponjosa e emborrachada.[21] Como outros boletos, apresenta poros em vez de lamelas que compõem o himenóforo na parte inferior do píleo. Suillus bovinus possui uma camada porosa composta característica, consistindo em uma camada externa de poros grossos e angulares sobreposta a uma camada interna de poros mais finos.[22] Os poros são cinza a oliva-amarelados e geralmente decorrentes,[20] compreendendo tubos amarelos a oliva-amarelados que medem 0,3 a 1 cm de comprimento.[22] O estipe mede de 4 a 6 cm de altura, de cor semelhante à do píleo, e tende a ser mais estreito na base; com diâmetro de 0,5 a 0,8 cm,[20] é mais delgado que o de outros boletos.[9]
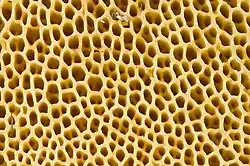
O esporada é de cor marrom-olivácea. Os esporos ovais a fusiformes têm dimensões de 8–10 por 3,5–4,5 μm.[20] Os basídios (células portadoras de esporos) são cilíndricos a estreitamente clavados, medindo 22,4–33,4 por 5,8–8,0 μm. Eles carregam quatro esterigmas (cada um sustentando um único esporo), que medem até 6,8 μm de comprimento. Cistídios estão presentes tanto nas extremidades dos tubos (queilocistídios) quanto nas faces dos tubos (pleurocistídios). Não há fíbulas nas hifas de Suillus bovinus. A pileipellis compreende hifas filamentosas e gelatinizadas com diâmetro de 2,6–5,0 μm.[23] O micélio apresenta tom rosado.[9]
A cor distinta do píleo e dos poros torna difícil confundi-la com outras espécies.[24] Frequentemente encontrada em habitats semelhantes está S. variegatus, embora essa espécie tenha píleo granular e poros oliva-escuros,[21] que são menores e não decorrentes. Também pode manchar de azul.[9]
Distribuição e habitat
Suillus bovinus é encontrada em bosques e plantações de coníferas em toda a Europa, incluindo regiões subalpinas nos Alpes, até altitudes de 800 m.[24] É comum na Lituânia, onde se associa ao pinheiro-silvestre (Pinus sylvestris), o único pinheiro nativo daquele país.[25] Solos preferidos de S. bovinus são frequentemente ácidos, arenosos ou às vezes calcários e de morena.[26] Na Ásia, foi registrada em Taiwan[27] e no Japão, onde se associa a Pinus densiflora.[28] Na China, foi registrada nas províncias de Anhui, Fujian, Guangdong, Hunan, Jiangxi e Zhejiang.[29]
Suillus bovinus foi introduzida em outras áreas. Na América do Norte, onde se acredita ter sido introduzida com Pinus sylvestris, é encontrada no leste dos Estados Unidos, incluindo Carolina do Norte, Pensilvânia, Vermont e as Montanhas Adirondack em Nova York.[30] Foi registrada infrequentemente sob P. sylvestris na Austrália,[31] onde foi encontrada até o sul de Queensland,[32] e em locais mais ao sul, incluindo Nova Gales do Sul e a Floresta de Kuitpo.[23] Foi registrada na Nova Zelândia.[33] Na África do Sul, cresce com Pinus radiata.[34]
Ecologia
Suillus bovinus é ectomicorrízica, formando associações simbióticas com árvores vivas ao envolver as raízes subterrâneas com bainhas de tecido fúngico. Trabalho de campo em florestas de pinheiros na Suécia analisando a estrutura populacional de Suillus bovinus descobriu que os cogumelos eram mais abundantes em florestas mais jovens e em áreas perturbadas, que continham um número maior de colônias — 700 a 5700 por hectare — em comparação com 30 a 120 colônias por hectare em povoamentos maduros. Colônias mais antigas em florestas maduras poderiam ter 17,5 m de diâmetro contra 1,7 a 5,3 m de diâmetro em florestas jovens.[26] Os basidiomas produzem um número enorme de esporos (estimado em um estudo finlandês em 240 milhões a 1,2 bilhão por cogumelo), dos quais apenas um pequeno número cresce com sucesso; acredita-se que esse grande número explique o maior número de colônias em florestas perturbadas e jovens, enquanto a disseminação vegetativa do fungo se torna mais importante em florestas estabelecidas.[35] Colônias de S. bovinus não se sobrepõem, o que indica que suprimem o crescimento umas das outras.[26] A mediana da expectativa de vida de uma colônia foi estimada em 36 anos.[36] Trabalho de campo realizado em florestas suecas de pinheiros sugeriu que S. variegatus suprimia o crescimento de S. bovinus, pois havia uma correlação negativa na ocorrência.[37]

Um estudo finlandês publicado em 1997 descobriu que comunidades bacterianas sob P. sylvestris sem micorrizas metabolizavam ácidos orgânicos e aminoácidos, enquanto comunidades entre S. bovinus metabolizavam manitol, um álcool de açúcar. Os micélios também estendiam o ambiente no solo em que as bactérias podiam crescer.[38] Um estudo experimental em Portugal mostrou que árvores de Pinus pinaster cresceram melhor após serem inoculadas com micélio de S. bovinus, Laccaria laccata e Lactarius deterrimus e esporos de Pisolithus tinctorius e Scleroderma citrinum. Esses fungos foram propostos como alternativa ao fertilizante químico na arboricultura de pinheiros.[39] Suillus bovinus demonstrou melhorar a tolerância de seu hospedeiro Pinus sylvestris a poluentes metálicos como cádmio e zinco,[40][41] embora não a compostos orgânicos perigosos como m-toluato.[40]
Um trabalho experimental em 1986 mostrou que Suillus bovinus poderia metabolizar proteínas e peptídeos diretamente, causando uma queda de nitrogênio em meios de crescimento, o que sugeriu que a espécie tem alguma atividade saprofítica.[42]
A relacionada Gomphidius roseus é encontrada exclusivamente com essa espécie e agora se pensa que seja parasita do micélio de Suillus bovinus.[43] Isso é evidenciado por exame microscópico, que mostra que G. roseus insere haustórios em células radiculares de plantas e não produz micélio significativo por si só. Além disso, G. roseus nunca é encontrada crescendo isoladamente, apenas com S. bovinus, embora esta última espécie seja encontrada sem a anterior.[43] Dicranophora fulva é um mofo amarelo que foi encontrado crescendo em basidiomas em decomposição de S. bovinus na Europa e nos Estados Unidos.[44]
Comestibilidade
O cogumelo Suillus bovinus tem sabor suave e é comestível, embora não seja altamente valorizado.[9] Quando cozido, libera muito líquido, que pode ser coletado e reduzido ou coado para fazer um molho. Seu sabor se intensifica ao ser desidratado.[45] A consistência macia e emborrachada de espécimes mais velhos — bem como sua propensão a infestações por larvas — os torna quase incomestíveis.[9] Os basidiomas fazem parte da dieta de verão tardio do esquilo-vermelho na Eurásia, que coleta os cogumelos e os armazena em bifurcações de árvores para um suprimento alimentar pronto após o início das geadas.[46] Há várias espécies de moscas que frequentemente usam basidiomas de S. bovinus para criar seus filhotes, incluindo Bolitophila rossica, Exechia separata, Exechiopsis indecisa, Pegomya deprimata e Pegohylemyia silvatica.[47]
Ver também
Referências
- ↑ Dahlberg, A. (2022) [errata version of 2019 assessment]. «Suillus bovinus». Lista Vermelha de Espécies Ameaçadas. 2019 (e.T122090785A223015509). doi:10.2305/IUCN.UK.2019-3.RLTS.T122090785A223015509.en
 . Consultado em 20 de novembro de 2025
. Consultado em 20 de novembro de 2025
- ↑ a b «Suillus bovinus (L.) Roussel 1806». MycoBank. International Mycological Association. Consultado em 6 de junho de 2011
- ↑ Linnaeus C. (1753). Species Plantarum (em latim). 2. Stockholm, Sweden: Laurentii Salvii. p. 1177. Consultado em 20 de novembro de 2025. Cópia arquivada em 6 de março de 2016
- ↑ Simpson DP. (1979). Cassell's Latin Dictionary 5th ed. London: Cassell. p. 79. ISBN 978-0-304-52257-6
- ↑ Roussell HFA. (1796). Flore du Calvados et terrains adjacents, composée suivant la méthode de Jussieu (em francês). Caen, France: L.-J. Poisson. p. 34
- ↑ Arora D. (1986). Mushrooms Demystified: A Comprehensive Guide to the Fleshy Fungi. Berkeley, USA: Ten Speed Press. p. 500. ISBN 978-0-89815-169-5
- ↑ Quélet L. (1886). Enchiridion fungorum in Europa media et praesertim in Gallia vigentium. Switzerland: O. Doin. p. 157. Consultado em 21 de novembro de 2025. Cópia arquivada em 10 de março de 2016
- ↑ Hawksworth DL. (2001). «The naming of fungi». In: McLaughlin DJ, McLaughlin EG. Systematics and Evolution. Part B. Col: The Mycota: A Comprehensive Treatise on Fungi as Experimental Systems for Basic and Applied Research. 7. Berlin, Germany: Springer. pp. 171–92 (see p. 181). ISBN 978-3-540-66493-2
- ↑ a b c d e f g h Lamaison JL, Polese JM (2005). The Great Encyclopedia of Mushrooms. Cologne, Germany: Könemann. p. 90. ISBN 978-3-8331-1239-3
- ↑ «Suillus bovinus, Bovine Bolete mushroom». www.first-nature.com. Consultado em 20 de novembro de 2025. Cópia arquivada em 3 de abril de 2019
- ↑ Kretzer A, Li Y, Szaro T, Bruns TD (1996). «Internal transcribed spacer sequences from 38 recognized species of Suillus sensu lato: Phylogenetic and taxonomic implications». Mycologia. 88 (5): 776–85. JSTOR 3760972. doi:10.2307/3760972
- ↑ Manian S, Sreenivasaprasad S, Bending GD, Mills PR (2001). «Genetic diversity and interrelationships among common European Suillus species based on ribosomal DNA sequences». FEMS Microbiology Letters. 204 (1): 117–21. PMID 11682189. doi:10.1111/j.1574-6968.2001.tb10873.x

- ↑ Šutara J. (1987). «Mariaella, a new boletaceous genus». Ceská Mykologie. 41 (2): 73–84. doi:10.33585/cmy.41202
- ↑ Watling R. (2008). A Manual and Source Book on the Boletes and their Allies. Col: Synopsis Fungorum. 24. Oslo, Norway: Fungiflora. p. 126. ISBN 978-82-90724-36-3
- ↑ a b Pearson AA. (1950). «Cape agarics and boleti». Transactions of the British Mycological Society. 33 (3–4): 276–314 (see p. 314). doi:10.1016/s0007-1536(50)80080-3. Consultado em 20 de novembro de 2025. Cópia arquivada em 23 de setembro de 2015
- ↑ Singer R. (1962). «Diagnoses Fungorum novorum Agaricalium II». Sydowia (em latim). 1 (1–6): 45–83 (see p. 82). Consultado em 20 de novembro de 2025. Cópia arquivada em 24 de setembro de 2015
- ↑ «Record details: Boletus bovinus var. viridocaerulescens A. Pearson». Index Fungorum. CAB International. Consultado em 20 de novembro de 2025. Cópia arquivada em 24 de setembro de 2015
- ↑ Besl H, Bresinsky A (1997). «Chemosystematics of Suillaceae and Gomphidiaceae (suborder Suillineae)». Plant Systematics and Evolution. 206 (1–4): 223–42. Bibcode:1997PSyEv.206..223B. doi:10.1007/BF00987949
- ↑ Binder M, Hibbett DS (2006). «Molecular systematics and biological diversification of Boletales». Mycologia. 98 (6): 971–81. PMID 17486973. doi:10.3852/mycologia.98.6.971
- ↑ a b c d e Phillips R (2006). Mushrooms. London: Pan MacMillan. p. 295. ISBN 978-0-330-44237-4
- ↑ a b Haas H. (1969). The Young Specialist Looks at Fungi. London: Burke. p. 52. ISBN 978-0-222-79409-3
- ↑ a b Laessoe T. (2002). Mushrooms. Col: Smithsonian Handbooks 2nd ed. London: Dorling Kindersley Adult. p. 200. ISBN 978-0-7894-8986-9
- ↑ a b Grgurinovic CA. (1997). Larger Fungi of South Australia. Adelaide: State Herbarium of South Australia. pp. 214–16. ISBN 978-0-7308-0737-7
- ↑ a b Nilsson S, Persson O (1977). Fungi of Northern Europe 1: Larger Fungi (Excluding Gill Fungi). London: Penguin Books. pp. 114–15. ISBN 978-0-14-063005-3
- ↑ Motiejūnaitė J, Kačergius A, Kasparavičius J (2013). «Preliminary studies on genetic diversity of ectomycorrhizal fungus Suillus bovinus in Lithuania». Botanica Lithuanica. 19 (2): 91–98. doi:10.2478/botlit-2013-0012


- ↑ a b c Dahlberg A, Stenlid J (1992). «Size, distribution and biomass of genets in populations of Suillus bovinus (L.: Fr.) Roussel revealed by somatic incompatibility». New Phytologist. 128 (2): 225–34. PMID 33874369. doi:10.1111/j.1469-8137.1994.tb04006.x

- ↑ Yeh KW, Chen ZC (1980). «The boletes of Taiwan» (PDF). Taiwania. 25 (1): 166–84 (see pp. 178–80). Consultado em 20 de novembro de 2025. Cópia arquivada (PDF) em 26 de novembro de 2015
- ↑ Zeller SM, Togashi K (1934). «The American and Japanese matsu-takes». Mycologia. 26 (9): 544–58. JSTOR 3754184. doi:10.2307/3754184. Consultado em 20 de novembro de 2025. Cópia arquivada em 23 de setembro de 2015
- ↑ Teng SC. (1996). Fungi of China 1st ed. Ithaca, New York: Mycotaxon. p. 405. ISBN 978-0-930845-05-6
- ↑ Bessette AR, Bessette A, Roody WC (2000). North American Boletes: A Color Guide to the Fleshy Pored Mushrooms. Syracuse, New York: Syracuse University Press. pp. 229–30. ISBN 978-0-8156-0588-1
- ↑ Leonard P, Batchelor D (outubro de 2010). «The slippery jack and how to find him: A field key to Suillus species in Australia and New Zealand» (PDF). Fungimap Newsletter (41): 4–8. Consultado em 20 de novembro de 2025. Cópia arquivada (PDF) em 28 de fevereiro de 2015
- ↑ Leonard P. (2012). «Fungi Key – Suillus». Queensland Mycological Society. Consultado em 20 de novembro de 2025. Cópia arquivada em 12 de agosto de 2015
- ↑ Segedin BP, Pennycook, SR (2001). «A nomenclatural checklist of agarics, boletes, and related secotioid and gasteromycetous fungi recorded from New Zealand.». New Zealand Journal of Botany. 39 (2): 285–348. Bibcode:2001NZJB...39..285S. doi:10.1080/0028825X.2001.9512739
- ↑ Dickinson C, Lucas J (1982). VNR Color Dictionary of Mushrooms. New York: Van Nostrand Reinhold. p. 150. ISBN 978-0-442-21998-7
- ↑ Dahlberg A, Stenlid J (1994). «Size, distribution and biomass of genets in populations of Suillus bovinus (L.: Fr.) Roussel revealed by somatic incompatibility». New Phytologist. 128 (2): 225–34. Bibcode:1994NewPh.128..225D. PMID 33874369. doi:10.1111/j.1469-8137.1994.tb04006.x

- ↑ Dahlberg A, Stenlid J (1990). «Population structure and dynamics in Suillus bovinus as indicated by spatial distribution of fungal clones». New Phytologist. 115 (3): 487–93. Bibcode:1990NewPh.115..487D. PMID 33874270. doi:10.1111/j.1469-8137.1990.tb00475.x
- ↑ Lukac M, Goldbold DL (2011). Soil Ecology in Northern Forests: A Belowground View of a Changing World. Cambridge, UK: Cambridge University Press. pp. 67–69. ISBN 978-1-139-50086-9. Consultado em 20 de novembro de 2025
- ↑ Timonen S, Jørgensen KS, Haahtela K, Sen R (1997). «Bacterial community structure at defined locations of Pinus sylvestris–Suillus bovinus and Pinus sylvestris–Paxillus involutus mycorrhizospheres in dry pine forest humus and nursery peat». Canadian Journal of Microbiology. 44 (6): 499–513. doi:10.1139/w98-035
- ↑ Sousa NR, Franco AR, Oliveira RS, Castro PM (2012). «Ectomycorrhizal fungi as an alternative to the use of chemical fertilisers in nursery production of Pinus pinaster». Journal of Environmental Management. 95 (Suppl. 1): S269–74. Bibcode:2012JEnvM..95S.269S. PMID 20702021. doi:10.1016/j.jenvman.2010.07.016. hdl:10400.14/5454

- ↑ a b Vosátka M, Rydlová J, Sudová R, Vohník M (2006). «Mycorrhizal fungi as helping agents in phytoremediation of degraded and contaminated soils». In: Mackova M, Dowling DN, Macek M. Phytoremediation and Rhizoremediation. Dordrecht, Germany: Springer Science & Business Media. p. 245. ISBN 978-1-4020-4999-6
- ↑ Adriaensen K, Vangronsveld J, Colpaert JV (2006). «Zinc-tolerant Suillus bovinus improves growth of Zn-exposed Pinus sylvestris seedlings». Mycorrhiza. 16 (8): 553–58. Bibcode:2006Mycor..16..553A. PMID 17033817. doi:10.1007/s00572-006-0072-7
- ↑ Abuzinadah RA, Read DJ (1986). «The role of proteins in the nitrogen nutrition of ectomycorrhizal plants. I. Utilization of peptides and proteins by ectomycorrhizal fungi». New Phytologist. 103 (3): 481–93. JSTOR 2434461. doi:10.1111/j.1469-8137.1986.tb02886.x
- ↑ a b Olsson PA, Munzenberger B, Mahmood S, Erland S (2000). «Molecular and anatomical evidence for a three-way association between Pinus sylvestris and the ectomycorrhizal fungi Suillus bovinus and Gomphidius roseus». Mycological Research (Submitted manuscript). 104 (11): 1372–78. doi:10.1017/S0953756200002823
- ↑ Volgmayr H, Krisai-Greilhuber I (1996). «Dicranophora fulva, a rare mucoraceous fungus growing on boletes». Mycological Research. 100 (5): 583–90. doi:10.1016/S0953-7562(96)80012-8

- ↑ Jordan P. (2015). Field Guide to Edible Mushrooms of Britain and Europe. London, United Kingdom: Bloomsbury Publishing. p. 99. ISBN 978-1-4729-2085-0
- ↑ Ognev SI. (1966). Mammals of the U.S.S.R. and Adjacent Countries. IV. Rodents. Jerusalem: Israel Program for Scientific Translations. pp. 314–15. Consultado em 20 de novembro de 2025. Cópia arquivada em 6 de março de 2016
- ↑ Hackman W, Meinander M (1979). «Diptera feeding as larvae on macrofungi in Finland» (PDF). Annales Zoologici Fennici. 16: 50–83 (see pp. 55–56). Consultado em 20 de novembro de 2025. Cópia arquivada (PDF) em 17 de novembro de 2015
Ligações externas
 Media relacionados com Suillus bovinus no Wikimedia Commons
Media relacionados com Suillus bovinus no Wikimedia Commons Dados relacionados com Suillus bovinus no Wikispecies
Dados relacionados com Suillus bovinus no Wikispecies

