Ectomicorriza
.jpg)
Uma ectomicorriza (do grego ἐκτός ektos, "externo", μύκης mykes, "fungo", e ῥίζα rhiza, "raiz"; abreviação EcM) é uma forma de relação simbiótica que ocorre entre um fungo simbionte, ou micobionte, e as raízes de várias espécies de plantas. O micobionte é frequentemente dos filos Basidiomycota e Ascomycota, e mais raramente do Zygomycota.[1] As ectomicorrizas se formam nas raízes de cerca de 2% das espécies de plantas,[1] geralmente plantas lenhosas, incluindo espécies das famílias das bétulas, dipterocarpos, mirtáceas, fagáceas, salicáceas, pinheiros e rosáceas.[2] A pesquisa sobre ectomicorrizas é cada vez mais importante em áreas como manejo de ecossistemas, restauração ecológica, silvicultura e agricultura.
Diferentemente de outras relações micorrízicas, como as micorrizas arbusculares e ericoides [en], os fungos ectomicorrízicos não penetram nas paredes celulares de seu hospedeiro. Em vez disso, formam uma interface totalmente intercelular conhecida como rede de Hartig, composta por hifas altamente ramificadas que formam uma treliça entre as células epidérmicas e corticais das raízes.
As ectomicorrizas distinguem-se de outras micorrizas pela formação de uma bainha hifal densa, conhecida como manto, que envolve a superfície da raiz.[3] Esse manto pode ter até 40 μm de espessura, com hifas que se estendem por vários centímetros no solo circundante. A rede de hifas auxilia a planta na absorção de nutrientes, incluindo água e minerais, frequentemente ajudando a planta hospedeira a sobreviver em condições adversas.[2] Em troca, o fungo simbionte obtém acesso a carboidratos.
Embora amostras de ectomicorrizas sejam geralmente coletadas no horizonte superficial do solo devido à maior densidade de raízes, sabe-se que ectomicorrizas ocorrem em raízes profundas de árvores (a uma profundidade superior a 2 metros), algumas atingindo pelo menos 4 m.[4]
Esporocarpos de fungos ectomicorrízicos bem conhecidos incluem a economicamente importante e comestível trufa (Tuber) e os mortais chapéu-da-morte, A. bisporigera, A. ocreata, A. verna e A. virosa.
Evolução
As simbioses micorrízicas são ubíquas em ecossistemas terrestres, e é possível que essas associações tenham facilitado a colonização terrestre pelas plantas. Há evidências paleobiológicas e moleculares de que as micorrizas arbusculares surgiram há pelo menos 460 milhões de anos.[5]
Plantas e fungos ectomicorrízicos (EcM) apresentam uma ampla distribuição taxonômica em todos os continentes (exceto na Antártida), sugerindo que a simbiose ectomicorrízica tem raízes evolutivas antigas.[1] A família Pinaceae é a mais antiga ainda existente na qual ocorre a simbiose com fungos EcM,[6] e fósseis dessa família datam de 156 milhões de anos.[7]
Propõe-se que o tipo de habitat e as funções distintas das diferentes micorrizas ajudem a determinar qual tipo de simbiose predomina em uma determinada área.[8] Nessa teoria, as simbioses EcM evoluíram em ecossistemas como florestas boreais, que são relativamente produtivas, mas nas quais o ciclo de nutrientes ainda é limitante. As ectomicorrizas têm uma capacidade intermediária de absorção de nutrientes, sendo mais eficientes que as micorrizas arbusculares e menos que as micorrizas ericoides, tornando-as úteis em situações de nutrientes intermediários.
Paleobiologia
Os fungos são compostos por tecidos moles, o que torna a fossilização difícil e a descoberta de fósseis fúngicos rara. No entanto, alguns espécimes excepcionalmente preservados foram encontrados no Chert de Princeton [en], do período Eoceno médio, na Colúmbia Britânica. Esses fósseis ectomicorrízicos mostram evidências claras de uma rede de Hartig, manto e hifas, demonstrando associações EcM bem estabelecidas há pelo menos 50 milhões de anos.[7]
O registro fóssil indica que as micorrizas arbusculares, mais comuns, formaram-se muito antes de outros tipos de simbioses entre fungos e plantas.[5][9][10] As ectomicorrizas podem ter evoluído com a diversificação das plantas e a evolução de coníferas e angiospermas. Assim, as micorrizas arbusculares podem ter sido uma força motriz na colonização terrestre pelas plantas, enquanto as ectomicorrizas podem ter surgido em resposta a uma maior especiação à medida que o clima da Terra se tornou mais sazonal e árido, ou simplesmente em resposta a habitats com deficiência nutricional.[10][11]
Estudos Moleculares
Análises moleculares e filogenéticas de linhagens fúngicas sugerem que os fungos EcM evoluíram e persistiram várias vezes a partir de ancestrais não EcM, como fungos saprófitos de húmus e madeira.[1] As estimativas variam de 7 a 16[6][12][13] até cerca de 66 evoluções independentes de associações EcM.[1] Alguns estudos sugerem que reversões ao estado ancestral de vida livre ocorreram,[12] mas isso é controverso.[6][10][13]
Morfologia
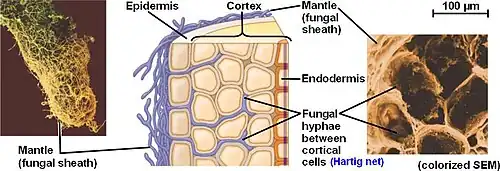
Como sugerido pelo nome, a biomassa do micossimbionte é majoritariamente externa à raiz da planta. A estrutura fúngica é composta principalmente por três partes: 1) as hifas intrarradiculares que formam a rede de Hartig; 2) o manto que forma uma bainha ao redor da ponta da raiz; e 3) as hifas extrarradiculares e estruturas relacionadas que se espalham pelo solo.
Rede de Hartig
A rede de Hartig é formada pelo crescimento de hifas (geralmente originadas da parte interna do manto circundante) para dentro da raiz do hospedeiro vegetal. As hifas penetram e crescem em uma direção transversal ao eixo da raiz,[14] formando assim uma rede entre as células externas do eixo da raiz. Nesta região, as células fúngicas e da raiz se tocam, e é onde ocorre a troca de nutrientes e carbono.[15]
A profundidade de penetração varia entre as espécies. Em Eucalyptus e Alnus, a rede de Hartig é confinada à epiderme, enquanto na maioria das gimnospermas as hifas penetram mais profundamente, até as células corticais ou a endoderme.[2] Em muitos tipos epidérmicos, ocorre o alongamento das células ao longo da epiderme, aumentando a superfície de contato entre o fungo e as células da raiz. A maioria dos tipos corticais de redes de Hartig não apresenta esse alongamento, sugerindo diferentes estratégias para aumentar o contato superficial entre as espécies.[2]
Manto
Uma bainha hifal, conhecida como manto, que frequentemente possui mais biomassa do que a interface da rede de Hartig, envolve a raiz. A estrutura do manto é variável, indo de uma rede frouxa de hifas a um arranjo estruturado e estratificado de tecido. Frequentemente, essas camadas lembram o tecido parenquimático vegetal e são chamadas de pseudoparenquimatosas.[15]
Como a raiz é envolvida pelo manto, seu desenvolvimento é frequentemente afetado. Parceiros fúngicos EcM caracteristicamente suprimem o desenvolvimento de pelos radiculares do simbionte vegetal.[15] Eles também podem aumentar a ramificação da raiz ao induzir citocininas na planta.[16] Esses padrões de ramificação podem se tornar tão extensos que um único manto consolidado pode envolver várias pontas de raízes ao mesmo tempo. Estruturas como essas são chamadas de ectomicorrizas tuberculadas ou coraloides.[15]
Os mantos de diferentes pares ectomicorrízicos frequentemente exibem características fenotípicas distintas, como cor, grau de ramificação e complexidade, que são usadas para ajudar a identificar o fungo, muitas vezes em conjunto com análises moleculares.[15] Esporocarpos também são úteis, mas nem sempre estão disponíveis.[2]
Hifas extrarradiculares e conexão

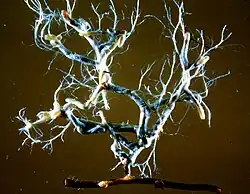
As hifas extrarradiculares se estendem para fora do manto no solo, compensando a supressão dos pelos radiculares ao aumentar a área de superfície efetiva da raiz colonizada. Essas hifas podem se espalhar individualmente ou em um arranjo agregado conhecido como rizomorfo. Esses órgãos hifais compostos podem ter uma ampla gama de estruturas. Alguns rizomorfos são simplesmente coleções lineares e paralelas de hifas. Outros têm uma organização mais complexa, por exemplo, as hifas centrais podem ser maiores em diâmetro do que outras hifas, ou as hifas podem crescer continuamente na ponta, penetrando em novas áreas de maneira que superficialmente lembra a atividade meristemática.[2]
Essa parte da ectomicorriza, chamada de micélio extrarradicular ou extramatricial, funciona amplamente como uma estrutura de transporte. Elas frequentemente se espalham por distâncias consideráveis, mantendo uma grande área de contato com o solo.[17] Alguns estudos mostraram uma relação entre as taxas de transporte de nutrientes e o grau de organização dos rizomorfos.[2][18] Os rizomorfos de diferentes tipos de EcM frequentemente têm diferentes tipos de organização e estratégias de exploração, observadas como diferentes estruturas e crescimento dentro do solo.[17] Essas diferenças também ajudam a identificar o fungo simbiótico.
As hifas que se estendem para fora no solo a partir de uma ectomicorriza podem infectar outras plantas próximas. Experimentos in vitro e estudos de campo mostram que isso pode levar à formação de redes micorrízicas que permitem o compartilhamento de carbono e nutrientes entre as plantas hospedeiras conectadas.[19][20][21] Por exemplo, o isótopo raro carbono-14 foi adicionado a uma árvore específica e posteriormente detectado em plantas e mudas próximas.[22] Um estudo observou uma transferência bidirecional de carbono entre Betula papyrifera [en] e Pseudotsuga menziesii, principalmente por meio das hifas da ectomicorriza.[23] No entanto, nem todas as plantas são compatíveis com todas as redes fúngicas, de modo que nem todas as plantas podem explorar os benefícios das conexões ectomicorrízicas estabelecidas.[22]
A conexão de nutrientes compartilhada por meio das redes micorrízicas foi sugerida como estando envolvida em outros processos ecológicos, como o estabelecimento de mudas, a sucessão ecológica florestal e outras interações planta-planta. Algumas micorrizas arbusculares demonstraram carregar sinais que alertam plantas na rede sobre ataques de insetos ou doenças.[24][25]
Esporocarpos

Diferentemente da maioria dos fungos micorrízicos arbusculares, os fungos ectomicorrízicos se reproduzem sexualmente e produzem esporocarpos visíveis em uma ampla variedade de formas.[1] O esporocarpo, comumente chamado de corpo frutífero, pode ser considerado uma extensão das hifas extrarradiculares. Suas paredes celulares e esporos são tipicamente compostos por carboidratos complexos e frequentemente incorporam uma grande quantidade de nitrogênio.[26] Muitos fungos EcM só conseguem formar esporocarpos e completar seus ciclos de vida ao participarem de uma relação EcM.
Os esporocarpos de muitas espécies assumem formas clássicas e bem reconhecidas, como cogumelos epígeos (desenvolvimento acima da superfície do solo) e trufas hipógeas (desenvolvimento abaixo da superfície do solo). A maioria desses produz propágulos microscópicos de cerca de 10 μm que podem se dispersar por longas distâncias por meio de diversos vetores, que variam de vento a animais fungívoros.[27] Sugere-se que os animais são atraídos por esporocarpos hipógeos devido ao seu alto teor de nutrientes, como nitrogênio, fósforo, minerais e vitaminas.[15] No entanto, outros argumentam que a disponibilidade de alimento em períodos específicos do ano é mais importante do que os nutrientes específicos.[26]
Pesquisas de esporocarpos têm sido utilizados para avaliar a composição da comunidade e a riqueza de espécies em muitos estudos. Contudo, esse método é imperfeito, pois os esporocarpos têm curta duração e podem ser difíceis de detectar.[28]
Fisiologia
Pré-simbiose
Para formar uma conexão ectomicorrízica, as hifas fúngicas devem primeiro crescer em direção às raízes da planta. Em seguida, devem envolver e penetrar as células da coifa radicular e infectá-las, permitindo a formação da rede de Hartig e estruturas associadas. Ambos os parceiros (planta e fungo) devem seguir uma sequência precisa de expressão gênica para que isso seja bem-sucedido. Há evidências de que a comunicação entre os parceiros na fase inicial da ectomicorriza ocorre, em alguns casos, por meio de compostos orgânicos voláteis produzidos apenas durante a fase de interação,[29] e que genes envolvidos em processos de secreção, crescimento apical e infecção mostram mudanças na expressão no início da fase de pré-contato.[30] Assim, um conjunto complexo de mudanças moleculares parece ocorrer mesmo antes do contato entre o fungo e a planta hospedeira.
As plantas hospedeiras liberam metabólitos na rizosfera que podem desencadear a germinação de esporos, o crescimento de hifas em direção à raiz e os primeiros passos da formação EcM.[31] Esses metabólitos incluem flavonoides, diterpenos, citocininas, hormônios e outros nutrientes. Alguns metabólitos liberados pelo hospedeiro demonstraram estimular o crescimento fúngico em Pisolithus, modificar o ângulo de ramificação das hifas e causar outras mudanças no fungo.[31] Alguns genes fúngicos parecem ser expressos antes do contato com a planta, sugerindo que sinais no solo podem induzir genes fúngicos importantes mesmo à distância da planta.[31]
Simbiose
Uma vez que as hifas fúngicas entram em contato com as células da coifa radicular, elas devem continuar a crescer em direção às células epidérmicas e se multiplicar para formar as camadas que eventualmente produzirão o manto. A produção do manto fúngico envolve a ativação de genes responsáveis pela tradução e crescimento celular, bem como aqueles responsáveis pela síntese e função da membrana celular, como as hidrofobinas.[32] Alguns polipeptídeos são encontrados apenas quando o fungo e a planta alcançam a simbiose; essas proteínas relacionadas à simbiose são chamadas ectomicorrizinas.[33]
Mudanças significativas na síntese de polipeptídeos e mRNA ocorrem rapidamente após a colonização pelo fungo, incluindo a produção de ectomicorrizinas.[2][34] Essas mudanças incluem a ativação de genes que podem ajudar na formação de novas membranas na interface simbiótica.[35] O efeito do manto na proliferação de raízes, desenvolvimento de pelos radiculares e ramificação dicotômica pode ser parcialmente imitado por exsudatos fúngicos, fornecendo um caminho para identificar as moléculas responsáveis pela comunicação.[31]
A rede de Hartig inicialmente se forma a partir da camada interna totalmente diferenciada do manto, e a penetração ocorre em uma frente ampla orientada perpendicularmente ao eixo da raiz,[14] digerindo através do espaço apoplástico. Algumas células vegetais respondem produzindo proteínas relacionadas ao estresse e à defesa, incluindo quitinases e peroxidases, que poderiam inibir a formação da rede de Hartig.[2][31] No entanto, a colonização extensiva da raiz ainda ocorre nessas plantas, e esses sinais de resistência parecem diminuir cerca de 21 dias após a colonização, sugerindo que os fungos EcM podem suprimir a resposta de defesa.[2]
À medida que o fungo e a planta se tornam intimamente conectados, eles começam a compartilhar nutrientes. Esse processo também é controlado por genes relacionados à simbiose. Por exemplo, a absorção de monossacarídeos em Amanita muscaria requer um transportador que é expresso apenas quando está em uma associação micorrízica. Quando o transportador é expresso, levando a um aumento na importação de açúcar pelo fungo, a planta hospedeira responde aumentando a disponibilidade de açúcar. O transporte de amônio e aminoácidos do fungo para a planta também é regulado.[32][35]
Absorção e troca de nutrientes
O nitrogênio é essencial na bioquímica vegetal, sendo necessário para a clorofila e todas as proteínas. Na maioria dos ecossistemas terrestres, o nitrogênio é escasso e está sequestrado em matéria orgânica difícil de decompor. Assim, os simbiontes fúngicos oferecem duas vantagens às plantas: o maior alcance de suas hifas em comparação com as raízes e uma maior capacidade de extrair nitrogênio da camada do solo onde a matéria orgânica está localizada.[15][36] A transferência líquida de nutrientes para as plantas requer que o nutriente atravesse três interfaces: 1) a interface solo-fungo, 2) a interface fungo-apoplasto, e 3) a interface apoplasto-célula radicular.[36] Estima-se que os fungos ectomicorrízicos recebam aproximadamente 15% do produto alimentar da produção primária da planta hospedeira e, em retorno, forneçam até 86% das necessidades de nitrogênio do hospedeiro.[27]
Alguns estudos mostraram que, se houver excesso de nitrogênio disponível devido ao uso humano de fertilizantes, as plantas podem desviar seus recursos da rede fúngica.[37][38] Isso pode representar problemas para o fungo, que pode não conseguir produzir esporocarpos,[37] e, a longo prazo, pode causar mudanças nos tipos de espécies fúngicas presentes no solo.[39] Em um estudo, a riqueza de espécies diminuiu drasticamente com o aumento dos aportes de nitrogênio, com mais de 30 espécies representadas em locais com baixo nitrogênio e apenas 9 em locais com alto nitrogênio.[40]
À medida que as hifas da região da rede de Hartig se tornam mais densamente compactadas, elas pressionam contra as paredes celulares das células radiculares da planta. Frequentemente, as paredes celulares fúngicas e vegetais tornam-se quase indistinguíveis onde se encontram, facilitando o compartilhamento de nutrientes.[41] Em muitas ectomicorrizas, as hifas da rede de Hartig não possuem divisões internas, criando uma estrutura multinuclear semelhante a uma célula de transferência que facilita o transporte inter-hifal.[36] As hifas apresentam uma alta concentração de organelas responsáveis pela produção de energia e proteína (mitocôndrias e retículo endoplasmático rugoso) em suas extremidades.[42] Há sinais de que transportadores nas membranas plasmáticas fúngicas e vegetais estão ativos, sugerindo uma troca bidirecional de nutrientes.[41]
A estrutura da rede EcM depende da disponibilidade de nutrientes. Quando a disponibilidade de nutrientes é baixa, o investimento na rede subterrânea é alto em relação ao crescimento acima do solo.[43] O fósforo é outro nutriente tipicamente limitante em muitos ecossistemas terrestres. Evidências sugerem que o fósforo é transferido principalmente como ortofosfato.[41] Algumas ectomicorrizas formadoras de tapetes contêm ribonucleases capazes de degradar rapidamente o DNA para obter fósforo dos núcleos celulares.[36]
Benefícios não nutricionais
As hifas extrarradiculares, particularmente os rizomorfos, também podem oferecer transporte inestimável de água. Frequentemente, esses desenvolvem-se em corredores especializados que se estendem muito além das raízes hospedeiras, aumentando a área funcional de acesso à água.[44][45] A bainha hifal que envolve as pontas das raízes também atua como uma barreira física, protegendo os tecidos vegetais de patógenos e predadores. Há também evidências de que metabólitos secundários produzidos pelos fungos atuam como mecanismos de defesa bioquímica contra fungos patogênicos, nematódeos e bactérias que podem tentar infectar a raiz micorrízica.[15][46] Muitos estudos também mostram que os fungos EcM permitem que as plantas tolerem solos com altas concentrações de metais pesados,[47][48][49] sais,[50][51] radionuclídeos e poluentes orgânicos persistentes.[15]
Ectendomicorriza
Embora a rede de Hartig se forme fora das células radiculares, a penetração das células corticais da planta ocorre ocasionalmente. Muitas espécies de fungos ectomicorrízicos podem funcionar tanto como ectomicorrizas quanto no modo penetrante típico das micorrizas arbusculares, dependendo do hospedeiro. Como essas associações representam uma forma de simbiose intermediária entre micorrizas arbusculares e ectomicorrizas, elas são chamadas ectendomicorrizas.[52]
Ecologia
Biogeografia e gradientes ambientais
Os fungos ectomicorrízicos são encontrados em ecossistemas boreais, temperados e tropicais, principalmente entre as famílias de plantas lenhosas dominantes.[27] Muitas das famílias fúngicas comuns em florestas temperadas (por exemplo, Russulaceae, Boletaceae, Thelephoraceae) também estão amplamente distribuídas no Hemisfério Sul e em florestas tropicais de dipterocarpos: embora as famílias de plantas sejam bastante diferentes em florestas temperadas e tropicais, os fungos ectomicorrízicos são relativamente semelhantes.[53] Os tipos de fungos EcM são afetados pelos tipos de solo, tanto em campo[54][55] quanto em laboratório.[56][57]
Para a maioria dos tipos de plantas e animais, a diversidade de espécies aumenta em direção ao equador. Isso é chamado de gradiente latitudinal de diversidade [en] (LGD).[58] Em contraste, há evidências de que os fungos EcM podem atingir a máxima diversidade na zona temperada.[27][59] Se for esse o caso, isso pode ser explicado por uma ou mais das seguintes hipóteses: 1) os fungos EcM podem ter evoluído em latitudes mais altas com hospedeiros Pinaceae e serem menos capazes de competir em climas tropicais; 2) as plantas hospedeiras dos EcM podem ser mais diversas em condições temperadas, e a estrutura do solo em regiões temperadas pode permitir maior diferenciação de nicho e acumulação de espécies; e 3) os hospedeiros EcM tropicais estão mais esparsamente distribuídos em pequenas ilhas florestais isoladas, o que pode reduzir o tamanho das populações e a diversidade dos fungos EcM.[59]
Especificidade do hospedeiro e respostas da comunidade
A maioria dos hospedeiros EcM apresenta baixos níveis de especificidade, podendo formar simbioses com muitos fungos distantes filogeneticamente.[60] Isso pode trazer benefícios evolutivos para a planta de duas maneiras: 1) as mudas da planta têm maior probabilidade de formar micorrizas em uma ampla variedade de habitats; e 2) a planta pode aproveitar diferentes fungos que variam em sua capacidade de acessar nutrientes.[61]
Os fungos EcM exibem diferentes níveis de especificidade para seus hospedeiros vegetais, e os custos e benefícios de sua especialização não são bem compreendidos.[62][63][64] Por exemplo, o grupo suilloide, um conjunto monofilético que contém os gêneros Suillus, Rhizopogon, Gomphidius [en] e outros, mostra um grau extremo de especificidade, com quase todos os seus membros formando ectomicorrizas com membros da família Pinaceae.[61] No entanto, muitos outros grupos fúngicos exibem uma ampla gama de hospedeiros.[65][66]
Plantas hospedeiras taxonomicamente relacionadas possuem comunidades de fungos EcM mais semelhantes do que táxons mais distantemente relacionados.[67] Da mesma forma, estudos filogenéticos moleculares mostraram que fungos derivados de um ancestral comum têm maior probabilidade de ter hospedeiros taxonomicamente relacionados.[12][68] A maturidade do ambiente hospedeiro, ou status sucessional, também pode afetar a variedade de comunidades fúngicas EcM presentes.[67] Outros fatores indiretos também podem influenciar a comunidade fúngica EcM, como a queda de folhas e a qualidade da serapilheira, que afetam os níveis de cálcio e o pH do solo.[69]
Papel na invasão

Plantas não nativas de uma área frequentemente requerem simbiontes micorrízicos para prosperar. A grande maioria das micorrizas arbusculares é inespecífica, e assim, plantas que interagem com essas micorrizas frequentemente se tornam invasoras rapidamente e com facilidade. No entanto, as simbioses ectomicorrízicas são frequentemente relativamente específicas. Em silvicultura exótica, fungos EcM compatíveis são frequentemente introduzidos no ambiente estranho para garantir o sucesso de plantações florestais.[70] Isso é mais comum em eucaliptos e pinheiros, que são árvores ectomicorrízicas obrigatórias em condições naturais.[70] Os pinheiros foram difíceis de estabelecer no hemisfério sul por essa razão,[71] e muitas plantações de Eucalyptus requereram inoculação com fungos EcM de seu ambiente nativo. Em ambos os casos, uma vez que as redes EcM foram introduzidas, as árvores conseguiram se naturalizar e começaram a competir com plantas nativas.[70]
Muitas espécies EcM, no entanto, co-invadem sem a ajuda de atividades humanas. A família Pinaceae frequentemente invade habitats junto com fungos EcM específicos dos gêneros Suillus e Rhizopogon.[62] Há também fungos formadores de ectomicorrizas com distribuições cosmopolitas que permitem que espécies vegetais não nativas se espalhem na ausência de seus fungos EcM específicos do ecossistema nativo.[62]
As plantas podem competir atacando as redes fúngicas umas das outras. Plantas nativas dominantes podem inibir fungos EcM nas raízes de plantas vizinhas,[72] e algumas plantas invasoras podem inibir o crescimento de fungos ectomicorrízicos nativos, especialmente se tornarem-se estabelecidas e dominantes. A erva-alheira (Alliaria petiolata) invasora e seu composto aleloquímico isotiocianato de benzila foram mostrados como inibidores do crescimento de três espécies de fungos EcM cultivados em mudas de pinheiro-branco.[73] Mudanças nas comunidades EcM podem ter efeitos drásticos na absorção de nutrientes e na composição da comunidade de árvores nativas, com ramificações ecológicas de longo alcance.[63]
Competição e outros simbiontes vegetais
A competição entre fungos ectomicorrízicos é um caso bem documentado de interações microbianas do solo [en].[74][75][76][77] Em alguns experimentos, o momento da colonização por fungos EcM concorrentes determinou qual espécie era dominante. Muitos fatores bióticos e abióticos podem mediar a competição entre fungos EcM, como temperatura, pH e umidade do solo, especificidade do hospedeiro e número de competidores, e esses fatores interagem de maneira complexa.[75][76] Há também algumas evidências de competição entre fungos EcM e fungos micorrízicos arbusculares. Isso é mais notado em espécies que podem hospedar tanto fungos EcM quanto micorrizas arbusculares em suas raízes.[78]
Algumas bactérias do solo, conhecidas como bactérias auxiliadoras de micorrizas (MHBs), demonstraram estimular a formação de EcM, a biomassa de raízes e brotos, e o crescimento fúngico.[79][80][81] Alguns argumentam que bactérias desse tipo deveriam ser consideradas um terceiro componente das micorrizas.[82] Outras bactérias inibem a formação ectomicorrízica.[80]
Interações com animais

Muitos fungos ectomicorrízicos dependem de mamíferos para a dispersão de seus esporos, particularmente fungos com esporocarpos hipógeos. Muitas espécies de pequenos mamíferos são micófagos, consumindo uma ampla gama de fungos, especialmente os esporocarpos. Os esporos são dispersos seja porque o esporocarpo é desenterrado e quebrado, seja após a ingestão e subsequente excreção. Alguns estudos sugerem que a passagem pelo trato digestivo de um animal promove a germinação dos esporos, embora para a maioria das espécies fúngicas isso não seja necessário.[83][84] Ao espalhar os esporos fúngicos, esses animais têm um efeito indireto na estrutura da comunidade vegetal.[26]
Outros esporocarpos são consumidos por invertebrados, como moluscos e larvas de moscas, alguns dos quais são até tolerantes à α-amanitina encontrada em chapéus-da-morte. No solo, nematódeos e colêmbolos também consomem tecido fúngico.[15] O fungo ectomicorrízico Laccaria bicolor foi encontrado atraindo e matando colêmbolos para obter nitrogênio, parte do qual pode então ser transferido para a planta hospedeira. Em um estudo, o pinheiro-branco inoculado com L. bicolor conseguiu derivar até 25% de seu nitrogênio de colêmbolos.[85]
Fungos comestíveis são importantes em sociedades ao redor do mundo. Trufas, boletos e cantarelos são conhecidos por sua importância culinária e econômica.[86]
Produção vegetal
Agricultura
Os fungos ectomicorrízicos não são predominantes em sistemas agrícolas e hortícolas. A maioria das plantas de cultivo economicamente relevantes que formam micorrizas tende a formá-las com fungos micorrízicos arbusculares.[87] Muitas práticas agrícolas modernas, como a lavoura, o uso intensivo de fertilizantes e fungicidas, são extremamente prejudiciais às micorrizas e ao ecossistema circundante. É possível que a agricultura afete indiretamente as espécies e habitats ectomicorrízicos próximos; por exemplo, o aumento da fertilização reduz a produção de esporocarpos.[88][89]
Silvicultura
Na silvicultura comercial, o transplante de árvores de cultivo para novos locais frequentemente requer um parceiro ectomicorrízico acompanhante. Isso é especialmente verdadeiro para árvores com alto grau de especificidade por seu micobionte, ou árvores que estão sendo plantadas longe de seu habitat nativo entre espécies fúngicas novas. Isso foi repetidamente demonstrado em plantações envolvendo árvores ectomicorrízicas obrigatórias, como espécies de Eucalyptus e Pinus.[70] O plantio em massa dessas espécies frequentemente requer um inóculo de fungos EcM nativos para que as árvores prosperem.[88]
Às vezes, espécies de plantações ectomicorrízicas, como pinheiros e eucaliptos, são plantadas e promovidas por sua capacidade de atuar como sumidouros de carbono atmosférico. No entanto, os fungos ectomicorrízicos dessas espécies também tendem a esgotar o carbono do solo, tornando esse uso de plantações controverso.[90][91]
Restauração
O papel das ectomicorrizas no suporte às suas plantas hospedeiras levou à sugestão de que fungos EcM poderiam ser usados em projetos de restauração ecológica destinados a restabelecer espécies vegetais nativas em ecossistemas perturbados por várias questões.[52][92] Como o desaparecimento de fungos micorrízicos de um habitat constitui um grande evento de perturbação do solo, sua reintrodução é uma parte importante do estabelecimento da vegetação e da restauração de habitats.[52]
Resiliência em ambientes desafiadores
Metais pesados
Os metais pesados são tóxicos para organismos vivos. Altas concentrações de metais pesados no solo, como zinco, cobre, cádmio, chumbo, níquel e cromo, afetam processos metabólicos básicos e podem levar a danos celulares e à morte. Alguns fungos ectomicorrízicos são tolerantes a metais pesados, com muitas espécies capazes de colonizar solos contaminados.[93] Há também casos de populações localmente adaptadas para tolerar ambientes químicos hostis.[93]
Os fungos apresentam mecanismos de desintoxicação para reduzir as concentrações de metais pesados em suas células. Esses mecanismos incluem a redução da absorção de metais pesados, o sequestro e armazenamento de metais pesados dentro da célula[48] e a excreção. A absorção de metais pesados pode ser reduzida por sorção e inativação metabólica na parede celular e no nível do apoplasto.[93] Os fungos ectomicorrízicos também têm a capacidade de se ligar a quantidades consideráveis de metais pesados.[93][94] Uma vez dentro da célula, os metais pesados podem ser imobilizados em complexos organometálicos, tornados solúveis, transformados em metalotioneínas, envolvidos no sequestro de metais e/ou armazenados em vacúolos em formas quimicamente inativas. Sistemas de desintoxicação antioxidante também podem estar presentes, reduzindo a produção de radicais livres e protegendo a célula fúngica.[95][96] Os fungos podem exportar metais do citoplasma para o apoplasto, um mecanismo que também ocorre em plantas.[97] Os fungos ectomicorrízicos também podem concentrar metais pesados em seus esporocarpos.[98] Diferenças genéticas entre populações crescendo em habitats tóxicos versus não tóxicos raramente foram relatadas, indicando que a tolerância a metais é generalizada. Nenhum táxon endêmico adaptado a metais foi documentado até o momento.[94][99] Há, no entanto, evidências de mudanças na comunidade associadas a metais pesados, com menor diversidade associada a locais contaminados.[100][101][102] Por outro lado, solos naturalmente ricos em metais pesados, como solos serpentinos [en], não parecem afetar a diversidade das comunidades de fungos ectomicorrízicos.[103]
Embora a tolerância generalizada a metais pareça ser a norma para fungos ectomicorrízicos, foi sugerido que alguns fungos, como Pisolithus tinctorius,[104] P. albus[105] e espécies do gênero Suillus[106][107][108] podem se adaptar a altos níveis de Al, Zn, Cd e Cu. Suillus luteus e S. bovinus são bons exemplos, com ecótipos conhecidos adaptados a Zn, Cd e Cu.[93][106][109][110]
Poluição e fitorremediação
Os fungos EcM demonstraram ter efeitos benéficos em vários tipos de ambientes poluídos, incluindo:
• Alta salinidade: Diversos estudos mostraram que certos fungos EcM podem ajudar seus hospedeiros a sobreviver em condições de alta salinidade do solo.[50][51][111]
• Radionuclídeos: Muitas espécies de fungos ectomicorrízicos, incluindo os Cortinariaceae, podem hiperacumular radionuclídeos.[112]
• Poluentes orgânicos: Algumas espécies EcM são capazes de decompor poluentes orgânicos persistentes (POPs), como organoclorados e bifenilas policloradas (PCBs). Produtos químicos que podem ser desintoxicados por fungos EcM, sozinhos ou em associação com sua planta hospedeira, incluem 2,4-diclorofenol e tetracloroetileno.[15][113]
Mudanças climáticas
As comunidades ectomicorrízicas podem ser afetadas pelo aumento de CO2 e os efeitos consequentes das mudanças climáticas. Em alguns estudos, níveis elevados de CO2 aumentaram o crescimento do micélio fúngico[114] e aumentaram a colonização radicular EcM.[115] Outras associações EcM mostraram pouca resposta ao CO2 elevado.[116]
O aumento das temperaturas também gera uma variedade de respostas, algumas negativas[117] e outras positivas.[54] A resposta EcM à seca é complexa, uma vez que muitas espécies fornecem proteção contra a dessecação das raízes e melhoram a capacidade das raízes de absorver água. Assim, os fungos EcM protegem suas plantas hospedeiras durante períodos de seca, embora eles próprios possam ser afetados ao longo do tempo.[116]
Conservação
À medida que a importância dos organismos subterrâneos para a produtividade, recuperação e estabilidade florestal se torna clara, a conservação de ectomicorrizas está ganhando atenção.[88] Muitas espécies de fungos EcM na Europa diminuíram, devido a fatores como redução da vitalidade das árvores, conversão de florestas para outros usos, poluição e acidificação dos solos florestais.[88][118] Argumenta-se que a conservação de ectomicorrizas requer a proteção de espécies em toda a sua gama de hospedeiros e habitats,[88] para garantir que todos os tipos de comunidades EcM sejam preservados.[28]
O Plano Florestal do Noroeste dos EUA, que regula o uso da terra em terras federais na região do Pacífico Noroeste dos Estados Unidos, inclui disposições para estudar fungos ameaçados e desenvolver estratégias para gerenciá-los e protegê-los. O Conselho Europeu para a Conservação de Fungos foi fundado em 1985 para promover a pesquisa e a atenção a fungos ameaçados.[119] Em 2018, o Conselho colaborou com o Kew Royal Botanic Gardens para produzir o Relatório sobre o estado dos fungos do mundo (State of the World's Fungi Report), 2018.[120]
As estratégias de conservação incluem a manutenção de: 1) plantas refúgio e hospedeiros reservatórios para preservar a comunidade fúngica EcM após a colheita; 2) árvores maduras para fornecer às mudas uma gama diversificada de fungos EcM; e 3) povoamentos de floresta primária que possuem macro e micro-habitats diversos e suportam comunidades fúngicas EcM variadas.[121] A preservação dos constituintes naturais do solo florestal e a retenção de detritos lenhosos e substratos também podem ser importantes. Em um estudo sobre mudas de abeto-de-douglas, a remoção de detritos do solo florestal e a compactação do solo reduziram a diversidade e a abundância de fungos EcM em 60%.[122] Algumas estratégias, como queimas controladas, têm efeitos diferentes em diferentes tipos de comunidades EcM, variando de negativos[123] a neutros ou positivos.[121][124]
Grandes coleções de culturas ex situ de fungos, incluindo fungos ectomicorrízicos, são mantidas em todo o mundo como uma garantia contra a perda genética. No entanto, essas coleções são incompletas.[125]
Referências
- ↑ a b c d e f Tedersoo, Leho; May, Tom W.; Smith, Matthew E. (2010). «Ectomycorrhizal lifestyle in fungi: global diversity, distribution, and evolution of phylogenetic lineages» (PDF). Mycorrhiza. 20 (4): 217–263. Bibcode:2010Mycor..20..217T. PMID 20191371. doi:10.1007/s00572-009-0274-x. Consultado em 22 de agosto de 2025. Arquivado do original (PDF) em 3 de março de 2016
- ↑ a b c d e f g h i j Smith, Sally E.; Read, David J. (26 de julho de 2010). Mycorrhizal Symbiosis. [S.l.]: Academic Press. ISBN 978-0-08-055934-6
- ↑ Hock, Bertold (2012). Fungal Associations. [S.l.]: Springer. ISBN 978-3-642-30826-0
- ↑ Robin, Agnès; Pradier, Céline; Sanguin, Hervé (16 de novembro de 2019). «How deep can ectomycorrhizas go? A case study on Pisolithus down to 4 meters in a Brazilian eucalypt plantation.». Mycorrhiza. 29 (6): 637–648. Bibcode:2019Mycor..29..637R. PMID 31732817. doi:10.1007/s00572-019-00917-y. hdl:11449/198164
 . Consultado em 22 de agosto de 2025. Cópia arquivada em 13 de fevereiro de 2023
. Consultado em 22 de agosto de 2025. Cópia arquivada em 13 de fevereiro de 2023
- ↑ a b Simon, Luc; Bousquet, Jean; Lévesque, Roger C.; Lalonde, Maurice (1993). «Origin and diversification of endomycorrhizal fungi and coincidence with vascular land plants». Nature. 363 (6424): 67–69. Bibcode:1993Natur.363...67S. doi:10.1038/363067a0
- ↑ a b c Hibbett, David S.; Matheny, P. Brandon (2009). «The relative ages of ectomycorrhizal mushrooms and their plant hosts estimated using Bayesian relaxed molecular clock analyses». BMC Biology. 7 (13). 13 páginas. PMC 2660285
 . PMID 19284559. doi:10.1186/1741-7007-7-13
. PMID 19284559. doi:10.1186/1741-7007-7-13
- ↑ a b LePage, Ben A.; Currah, Randolph S.; Stockey, Ruth A.; Rothwell, Gar W. (1997). «Fossil ectomycorrhizae from the Middle Eocene». American Journal of Botany. 84 (3): 410–412. JSTOR 2446014. PMID 21708594. doi:10.2307/2446014
- ↑ Read, David J. (1991). «Mycorrhizas in ecosystems». Experientia. 47 (4): 376–391. doi:10.1007/BF01972080
- ↑ Fitter, A. H.; Moyersoen, B. (1996). «Evolutionary trends in root-microbe symbioses». Philosophical Transactions of the Royal Society of London. Series B, Biological Sciences. 351 (1345): 1367–1375. Bibcode:1996RSPTB.351.1367F. doi:10.1098/rstb.1996.0120
- ↑ a b c Wang, B.; Qiu, Y.-L. (2006). «Phylogenetic distribution and evolution of mycorrhizas in land plants» (PDF). Mycorrhiza. 16 (5): 299–363. Bibcode:2006Mycor..16..299W. PMID 16845554. doi:10.1007/s00572-005-0033-6. Consultado em 22 de agosto de 2025. Arquivado do original (PDF) em 29 de outubro de 2013
- ↑ Allen, Michael F. The ecology of mycorrhizae. Cambridge University Press, 1991.
- ↑ a b c Hibbett, David S.; Gilbert, Luz-Beatriz; Donoghue, Michael J. (2000). «Evolutionary instability of ectomycorrhizal symbioses in basidiomycetes» (PDF). Nature. 407 (6803): 506–508. Bibcode:2000Natur.407..506H. PMID 11029000. doi:10.1038/35035065. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
- ↑ a b Bruns, Thomas D.; Shefferson, Richard P. (2004). «Evolutionary studies of ectomycorrhizal fungi: recent advances and future directions». Canadian Journal of Botany. 82 (8): 1122–1132. Bibcode:2004CaJB...82.1122B. doi:10.1139/b04-021 [ligação inativa]
- ↑ a b Blasius, D.; et al. (1986). «Hartig net structure and formation in fully ensheathed ectomycorrhizas». Nordic Journal of Botany. 6 (6): 837–842. Bibcode:1986NorJB...6..837B. doi:10.1111/j.1756-1051.1986.tb00487.x
- ↑ a b c d e f g h i j k Dighton, J. "Mycorrhizae." Encyclopedia of Microbiology (2009): 153–162.
- ↑ Giron, David; et al. (2013). «Cytokinins as key regulators in plant–microbe–insect interactions: connecting plant growth and defence» (PDF). Functional Ecology. 27 (3): 599–609. Bibcode:2013FuEco..27..599G. doi:10.1111/1365-2435.12042
 . Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 5 de março de 2016
. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 5 de março de 2016
- ↑ a b Agerer, Reinhard (2001). «Exploration types of ectomycorrhizae» (PDF). Mycorrhiza. 11 (2): 107–114. doi:10.1007/s005720100108. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 14 de novembro de 2012
- ↑ Kammerbauer, H; Agerer, R; Sandermann, H Jr (1989). «Studies on ectomycorrhiza. XXII. Mycorrhizal rhizomorphs of Thelephora terrestris and Pisolithus tinctorius in association with Norway spruce (Picea abies): formation in vivo and translocation of phosphate». Trees. 3 (2): 78–84. doi:10.1007/bf00191537
- ↑ Arnebrant, Kristina; et al. (1993). «Nitrogen translocation between Alnus glutinosa (L.) Gaertn. seedlings inoculated with Frankia sp. and Pinus contorta Doug, ex Loud seedlings connected by a common ectomycorrhizal mycelium». New Phytologist. 124 (2): 231–242. Bibcode:1993NewPh.124..231A. PMID 33874350. doi:10.1111/j.1469-8137.1993.tb03812.x

- ↑ He, Xinhua; et al. (2006). «Rapid nitrogen transfer from ectomycorrhizal pines to adjacent ectomycorrhizal and arbuscular mycorrhizal plants in a California oak woodland». New Phytologist. 170 (1): 143–151. Bibcode:2006NewPh.170..143H. PMID 16539611. doi:10.1111/j.1469-8137.2006.01648.x

- ↑ Nara, Kazuhide (2006). «Ectomycorrhizal networks and seedling establishment during early primary succession». New Phytologist. 169 (1): 169–178. Bibcode:2006NewPh.169..169N. PMID 16390428. doi:10.1111/j.1469-8137.2005.01545.x
- ↑ a b Amaranthus, M. P.; Perry, D. A. (1994). «The functioning of ectomycorrhizal fungi in the field: linkages in space and time». Plant and Soil. 159 (1): 133–140. Bibcode:1994PlSoi.159..133A. doi:10.1007/BF00000102
- ↑ Simard, Suzanne W.; et al. (1997). «Net transfer of carbon between ectomycorrhizal tree species in the field» (PDF). Nature. 388 (6642): 579–582. Bibcode:1997Natur.388..579S. doi:10.1038/41557
 . Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
- ↑ Babikova, Zdenka; et al. (2013). «Underground signals carried through common mycelial networks warn neighbouring plants of aphid attack» (PDF). Ecology Letters. 16 (7): 835–843. Bibcode:2013EcolL..16..835B. PMID 23656527. doi:10.1111/ele.12115. Consultado em 22 de agosto de 2025. Arquivado do original (PDF) em 21 de junho de 2015
- ↑ Xie, L. J.; et al. (2012). «Disease resistance signal transfer between roots of different tomato plants through common arbuscular mycorrhiza networks». The Journal of Applied Ecology. 23 (5): 1145
- ↑ a b c Johnson, Christopher N (1996). «Interactions between mammals and ectomycorrhizal fungi». Trends in Ecology & Evolution. 11 (12): 503–507. Bibcode:1996TEcoE..11..503J. PMID 21237938. doi:10.1016/S0169-5347(96)10053-7
- ↑ a b c d Peay, Kabir G.; et al. (2007). «A strong species–area relationship for eukaryotic soil microbes: island size matters for ectomycorrhizal fungi» (PDF). Ecology Letters. 10 (6): 470–480. Bibcode:2007EcolL..10..470P. PMID 17498146. doi:10.1111/j.1461-0248.2007.01035.x. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
- ↑ a b Gehring, Catherine A.; et al. (1998). «Ectomycorrhizal fungal community structure of pinyon pines growing in two environmental extremes» (PDF). Ecology. 79 (5): 1562–1572. doi:10.1890/0012-9658(1998)079[1562:efcsop]2.0.co;2. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 23 de janeiro de 2012
- ↑ Menotta, Michele; Gioacchini, Anna M.; Amicucci, Antonella; Buffalini, Michele; Sisti, Davide; Stocchi, Vilberto (2004). «Headspace solid-phase microextraction with gas chromatography and mass spectrometry in the investigation of volatile organic compounds in an ectomycorrhizae synthesis system». Rapid Communications in Mass Spectrometry (em inglês) (2): 206–210. ISSN 1097-0231. doi:10.1002/rcm.1314. Consultado em 23 de agosto de 2025
- ↑ Menotta, M.; et al. (2004). «Differential gene expression during pre-symbiotic interaction between Tuber borchii Vittad. and Tilia americana L». Current Genetics. 46 (3): 158–165. PMID 15258696. doi:10.1007/s00294-004-0518-4
- ↑ a b c d e Martin, Francis; et al. (2001). «Developmental cross talking in the ectomycorrhizal symbiosis: signals and communication genes». New Phytologist. 151 (1): 145–154. Bibcode:2001NewPh.151..145M. PMID 33873382. doi:10.1046/j.1469-8137.2001.00169.x

- ↑ a b Egerton-Warburton, L. M.; et al. (2003). «Mycorrhizal fungi». Encyclopedia of Soils in the Environment
- ↑ Hilbert, J. L.; Martin, F. (1988). «Regulation of gene expression in ectomycorrhizas». New Phytologist. 110 (3): 339–346. Bibcode:1988NewPh.110..339H. doi:10.1111/j.1469-8137.1988.tb00270.x

- ↑ Hilbert, Jean-Louis; Costa, Guy; Martin, Francis (1991). «Ectomycorrhizin synthesis and polypeptide changes during the early stage of eucalypt mycorrhiza development». Plant Physiology. 97 (3): 977–984. PMC 1081112
 . PMID 16668539. doi:10.1104/pp.97.3.977
. PMID 16668539. doi:10.1104/pp.97.3.977
- ↑ a b Morel, Mélanie; et al. (2005). «Identification of genes differentially expressed in extraradical mycelium and ectomycorrhizal roots during Paxillus involutus-Betula pendula ectomycorrhizal symbiosis». Applied and Environmental Microbiology. 71 (1): 382–391. Bibcode:2005ApEnM..71..382M. PMC 544268
 . PMID 15640212. doi:10.1128/aem.71.1.382-391.2005
. PMID 15640212. doi:10.1128/aem.71.1.382-391.2005
- ↑ a b c d Chalot, Michel; Brun, Annick (1998). «Physiology of organic nitrogen acquisition by ectomycorrhizal fungi and ectomycorrhizas». FEMS Microbiology Reviews. 22 (1): 21–44. PMID 9640645. doi:10.1111/j.1574-6976.1998.tb00359.x

- ↑ a b Högberg, Mona N.; et al. (2010). «Quantification of effects of season and nitrogen supply on tree below-ground carbon transfer to ectomycorrhizal fungi and other soil organisms in a boreal pine forest». New Phytologist. 187 (2): 485–493. Bibcode:2010NewPh.187..485H. PMID 20456043. doi:10.1111/j.1469-8137.2010.03274.x

- ↑ Wallander, H.; Ekblad, Alf; Bergh, J. (2011). «Growth and carbon sequestration by ectomycorrhizal fungi in intensively fertilized Norway spruce forests». Forest Ecology and Management. 262 (6): 999–1007. Bibcode:2011ForEM.262..999W. doi:10.1016/j.foreco.2011.05.035
- ↑ Lilleskov, E. A.; Hobbie, E. A.; Horton, T. R. (2011). «Conservation of ectomycorrhizal fungi: exploring the linkages between functional and taxonomic responses to anthropogenic N deposition» (PDF). Fungal Ecology. 4 (2): 174–183. Bibcode:2011FunE....4..174L. doi:10.1016/j.funeco.2010.09.008. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 29 de outubro de 2013
- ↑ Lilleskov, Erik A.; et al. (2002). «Belowground ectomycorrhizal fungal community change over a nitrogen deposition gradient in Alaska» (PDF). Ecology. 83 (1): 104–115. JSTOR 2680124. doi:10.2307/2680124. Consultado em 22 de agosto de 2025. Cópia arquivada (PDF) em 8 de janeiro de 2013
- ↑ a b c Smith, S. E.; Gianinazzi-Pearson, V.; Koide, R.; Cairney, J. W. G. (1 de fevereiro de 1994). «Nutrient transport in mycorrhizas: structure, physiology and consequences for efficiency of the symbiosis». Plant and Soil (em inglês) (1): 103–113. ISSN 1573-5036. doi:10.1007/BF00000099. Consultado em 26 de agosto de 2025
- ↑ Kottke, I.; Oberwinkler, F. (1987). «The cellular structure of the Hartig net: coenocytic and transfer cell-like organization». Nordic Journal of Botany. 7 (1): 85–95. Bibcode:1987NorJB...7...85K. doi:10.1111/j.1756-1051.1987.tb00919.x
- ↑ Hobbie, Erik A. (2006). «Carbon Allocation to Ectomycorrhizal Fungi Correlates with Belowground Allocation in Culture Studies». Ecology (em inglês) (3): 563–569. ISSN 1939-9170. doi:10.1890/05-0755. Consultado em 23 de agosto de 2025
- ↑ Duddridge, JA; Malibari, A; Read, DJ (1980). «Structure and function of mycorrhizal rhizomorphs with special reference to their role in water transport». Nature. 287 (5785): 834–836. Bibcode:1980Natur.287..834D. doi:10.1038/287834a0
- ↑ Brownlee, C.; Duddridge, J. A.; Malibari, A.; Read, D. J. (1983). «The structure and function of mycelial systems of ectomycorrhizal roots with special reference to their role in forming inter-plant connections and providing pathways for assimilate and water transport». Plant and Soil. 71 (1–3): 433–443. Bibcode:1983PlSoi..71..433B. doi:10.1007/BF02182684
- ↑ Schrey, Silvia D.; et al. (2012). «Production of fungal and bacterial growth modulating secondary metabolites is widespread among mycorrhiza-associated streptomycetes». BMC Microbiology. 12 (1). PMC 3487804
 . PMID 22852578. doi:10.1186/1471-2180-12-164
. PMID 22852578. doi:10.1186/1471-2180-12-164
- ↑ Colpaert, Jan V.; et al. (2011). «How metal-tolerant ecotypes of ectomycorrhizal fungi protect plants from heavy metal pollution» (PDF). Annals of Forest Science. 68 (1): 17–24. Bibcode:2011AnFSc..68...17C. doi:10.1007/s13595-010-0003-9
 . Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 29 de outubro de 2013
. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 29 de outubro de 2013
- ↑ a b Blaudez, Damien; Botton, Bernard; Chalot, Michel (2000). «Cadmium uptake and subcellular compartmentation in the ectomycorrhizal fungus Paxillus involutus». Microbiology. 146 (5): 1109–1117. PMID 10832638. doi:10.1099/00221287-146-5-1109

- ↑ Sell, Joachim; et al. (2005). «Contribution of ectomycorrhizal fungi to cadmium uptake of poplars and willows from a heavily polluted soil». Plant and Soil. 277 (1–2): 245–253. Bibcode:2005PlSoi.277..245S. doi:10.1007/s11104-005-7084-5. hdl:20.500.11850/30941
 . Consultado em 23 de agosto de 2025. Cópia arquivada em 16 de junho de 2021
. Consultado em 23 de agosto de 2025. Cópia arquivada em 16 de junho de 2021
- ↑ a b Bandou, E.; et al. (2006). «The ectomycorrhizal fungus Scleroderma bermudense alleviates salt stress in seagrape (Coccoloba uvifera L.) seedlings». Mycorrhiza. 16 (8): 559–565. Bibcode:2006Mycor..16..559B. PMID 17033816. doi:10.1007/s00572-006-0073-6
- ↑ a b Liang, Y. U.; et al. (2007). «Proteome analysis of an ectomycorrhizal fungus Boletus edulis under salt shock» (PDF). Mycological Research. 111 (8): 939–946. PMID 17716885. doi:10.1016/j.mycres.2007.06.005. Consultado em 23 de agosto de 2025. Arquivado do original em 29 de outubro de 2013
- ↑ a b c Quoreshi, A.M. (2008). The Use of Mycorrhizal Biotechnology in Restoration of Disturbed Ecosystem. In: Siddiqui, Z.A., Akhtar, M.S., Futai, K. (eds) Mycorrhizae: Sustainable Agriculture and Forestry. Springer, Dordrecht. doi:10.1007/978-1-4020-8770-7_13
- ↑ Peay, Kabir G.; et al. (2010). «Potential link between plant and fungal distributions in a dipterocarp rainforest: community and phylogenetic structure of tropical ectomycorrhizal fungi across a plant and soil ecotone». New Phytologist. 185 (2): 529–542. Bibcode:2010NewPh.185..529P. PMID 19878464. doi:10.1111/j.1469-8137.2009.03075.x

- ↑ a b Swaty, Randy L.; et al. (1998). «Temporal variation in temperature and rainfall differentially affects ectomycorrhizal colonization at two contrasting sites» (PDF). New Phytologist. 139 (4): 733–739. Bibcode:1998NewPh.139..733S. doi:10.1046/j.1469-8137.1998.00234.x. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 23 de janeiro de 2012
- ↑ Toljander, Jonas F.; et al. (2006). «Species composition of an ectomycorrhizal fungal community along a local nutrient gradient in a boreal forest». New Phytologist. 170 (4): 873–884. Bibcode:2006NewPh.170..873T. PMID 16684245. doi:10.1111/j.1469-8137.2006.01718.x

- ↑ Brearley, Francis Q (2006). «Differences in the growth and ectomycorrhizal community of Dryobalanops lanceolata (Dipterocarpaceae) seedlings grown in ultramafic and non-ultramafic soils». Soil Biology and Biochemistry. 38 (12): 3407–3410. Bibcode:2006SBiBi..38.3407B. doi:10.1016/j.soilbio.2006.05.012
- ↑ Brearley, Francis Q.; et al. (2007). «How does light and phosphorus fertilisation affect the growth and ectomycorrhizal community of two contrasting dipterocarp species?». Plant Ecology. 192 (2): 237–249. Bibcode:2007PlEco.192..237B. doi:10.1007/s11258-007-9325-6
- ↑ Delavaux, Camille S.; LaManna, Joseph A.; Myers, Jonathan A.; Phillips, Richard P.; Aguilar, Salomón; Allen, David; Alonso, Alfonso; Anderson-Teixeira, Kristina J.; Baker, Matthew E.; Baltzer, Jennifer L.; Bissiengou, Pulchérie; Bonfim, Mariana; Bourg, Norman A.; Brockelman, Warren Y.; Burslem, David F. R. P. (19 de outubro de 2023). «Mycorrhizal feedbacks influence global forest structure and diversity». Communications Biology (em inglês). 6 (1): 1066. ISSN 2399-3642. PMC 10587352
 . PMID 37857800. doi:10.1038/s42003-023-05410-z
. PMID 37857800. doi:10.1038/s42003-023-05410-z . hdl:2164/22248
. hdl:2164/22248
- ↑ a b Tedersoo, Leho; Nara, Kazuhide (2010). «General latitudinal gradient of biodiversity is reversed in ectomycorrhizal fungi». New Phytologist. 185 (2): 351–354. Bibcode:2010NewPh.185..351T. PMID 20088976. doi:10.1111/j.1469-8137.2009.03134.x

- ↑ Molina, Randy, Hugues Massicotte, and James M. Trappe. "Specificity phenomena in mycorrhizal symbioses: community-ecological consequences and practical implications." Mycorrhizal functioning: an integrative plant-fungal process (1992): 357–423.
- ↑ a b Bruns, Thomas D.; Bidartondo, Martin I.; Taylor, D. Lee (2002). «Host specificity in ectomycorrhizal communities: what do the exceptions tell us?». Integrative and Comparative Biology. 42 (2): 352–359. PMID 21708728. doi:10.1093/icb/42.2.352

- ↑ a b c Dickie, Ian A.; et al. (2010). «Co-invasion by Pinus and its mycorrhizal fungi». New Phytologist. 187 (2): 475–484. Bibcode:2010NewPh.187..475D. PMID 20456067. doi:10.1111/j.1469-8137.2010.03277.x

- ↑ a b Wolfe, Benjamin E.; Klironomos, John N. (2005). «Breaking new ground: soil communities and exotic plant invasion» (PDF). BioScience. 55 (6): 477–487. doi:10.1641/0006-3568(2005)055[0477:bngsca]2.0.co;2
 . Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 6 de abril de 2012
. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 6 de abril de 2012
- ↑ Borowicz, Victoria A.; Juliano, Steven A. (1991). «Specificity in host-fungus associations: Do mutualists differ from antagonists?». Evolutionary Ecology. 5 (4): 385–392. Bibcode:1991EvEco...5..385B. doi:10.1007/BF02214155
- ↑ Diédhiou, Abdala Gamby; et al. (2010). «Multi-host ectomycorrhizal fungi are predominant in a Guinean tropical rainforest and shared between canopy trees and seedlings». Environmental Microbiology. 12 (8): 2219–2232. Bibcode:2010EnvMi..12.2219D. PMID 21966915. doi:10.1111/j.1462-2920.2010.02183.x

- ↑ Massicotte, H. B.; et al. (1999). «Diversity and host specificity of ectomycorrhizal fungi forest sites by five host species». Canadian Journal of Botany. 77 (8): 1053–1076. doi:10.1139/b99-115
- ↑ a b Ishida, Takahide A.; Nara, Kazuhide; Hogetsu, Taizo (2007). «Host effects on ectomycorrhizal fungal communities: insight from eight host species in mixed conifer–broadleaf forests». New Phytologist. 174 (2): 430–440. Bibcode:2007NewPh.174..430I. PMID 17388905. doi:10.1111/j.1469-8137.2007.02016.x

- ↑ Den Bakker, Henk C.; et al. (2004). «Evolution and host specificity in the ectomycorrhizal genus Leccinum». New Phytologist. 163 (1): 201–215. Bibcode:2004NewPh.163..201D. PMID 33873790. doi:10.1111/j.1469-8137.2004.01090.x

- ↑ Aponte, Cristina; et al. (2010). «Indirect host effect on ectomycorrhizal fungi: Leaf fall and litter quality explain changes in fungal communities on the roots of co-occurring Mediterranean oaks» (PDF). Soil Biology and Biochemistry. 42 (5): 788–796. Bibcode:2010SBiBi..42..788A. doi:10.1016/j.soilbio.2010.01.014. hdl:10261/23231
 . Consultado em 23 de agosto de 2025. Arquivado do original (PDF) em 21 de junho de 2015
. Consultado em 23 de agosto de 2025. Arquivado do original (PDF) em 21 de junho de 2015
- ↑ a b c d Díez, Jesús (2005). «Invasion biology of Australian ectomycorrhizal fungi introduced with eucalypt plantations into the Iberian Peninsula» (PDF). Archived copy. Issues in Bioinvasion Science. 2005. [S.l.: s.n.] pp. 3–15. ISBN 978-1-4020-2902-8. doi:10.1007/1-4020-3870-4_2. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 8 de janeiro de 2013
- ↑ Richardson, David M., ed. Ecology and biogeography of Pinus. Cambridge University Press, 2000.
- ↑ Walker, John F.; et al. (1999). «Suppression of ectomycorrhizae on canopy tree seedlings in Rhododendron maximum L. (Ericaceae) thickets in the southern Appalachians» (PDF). Mycorrhiza. 9 (1): 49–56. Bibcode:1999Mycor...9...49W. doi:10.1007/s005720050262. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 11 de junho de 2010
- ↑ Wolfe, Benjamin E.; et al. (2008). «The invasive plant Alliaria petiolata (garlic mustard) inhibits ectomycorrhizal fungi in its introduced range». Journal of Ecology. 96 (4): 777–783. Bibcode:2008JEcol..96..777W. doi:10.1111/j.1365-2745.2008.01389.x

- ↑ Kennedy, Peter G.; Peay, Kabir G.; Bruns, Thomas D. (2009). «Root tip competition among ectomycorrhizal fungi: Are priority effects a rule or an exception?» (PDF). Ecology. 90 (8): 2098–2107. Bibcode:2009Ecol...90.2098K. PMID 19739372. doi:10.1890/08-1291.1. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 16 de outubro de 2023
- ↑ a b Kennedy, Peter (2010). «Ectomycorrhizal fungi and interspecific competition: species interactions, community structure, coexistence mechanisms, and future research directions». New Phytologist. 187 (4): 895–910. Bibcode:2010NewPh.187..895K. PMID 20673286. doi:10.1111/j.1469-8137.2010.03399.x
- ↑ a b Mamoun, M.; Olivier, J. M. (1993). «Competition between Tuber melanosporum and other ectomycorrhizal fungi under two irrigation regimes». Plant and Soil. 149 (2): 211–218. doi:10.1007/BF00016611
- ↑ Villeneuve, Normand; Le Tacon, François; Bouchard, Daniel (1991). «Survival of inoculated Laccaria bicolor in competition with native ectomycorrhizal fungi and effects on the growth of outplanted Douglasfir seedlings». Plant and Soil. 135 (1): 95–107. Bibcode:1991PlSoi.135...95V. doi:10.1007/BF00014782
- ↑ Chen, Y. L.; Brundrett, M. C.; Dell, B. (2000). «Effects of ectomycorrhizas and vesicular–arbuscular mycorrhizas, alone or in competition, on root colonization and growth of Eucalyptus globulus and E. urophylla». New Phytologist. 146 (3): 545–555. Bibcode:2000NewPh.146..545C. doi:10.1046/j.1469-8137.2000.00663.x
 . Consultado em 23 de agosto de 2025. Cópia arquivada em 25 de julho de 2020
. Consultado em 23 de agosto de 2025. Cópia arquivada em 25 de julho de 2020
- ↑ Founoune, Hassna; et al. (2002). «Mycorrhiza helper bacteria stimulate ectomycorrhizal symbiosis of Acacia holosericea with Pisolithus alba». New Phytologist. 153 (1): 81–89. Bibcode:2002NewPh.153...81F. doi:10.1046/j.0028-646X.2001.00284.x

- ↑ a b Bowen, G. D.; Theodorou, C. (1979). «Interactions between bacteria and ectomycorrhizal fungi». Soil Biology and Biochemistry. 11 (2): 119–126. Bibcode:1979SBiBi..11..119B. doi:10.1016/0038-0717(79)90087-7
- ↑ Garbaye, J (1994). «Tansley Review No. 76 Helper bacteria: a new dimension to the mycorrhizal symbiosis». New Phytologist. 128 (2): 197–210. Bibcode:1994NewPh.128..197G. PMID 33874371. doi:10.1111/j.1469-8137.1994.tb04003.x

- ↑ Bonfante, Paola; Anca, Iulia-Andra (2009). «Plants, mycorrhizal fungi, and bacteria: a network of interactions» (PDF). Annual Review of Microbiology. 63: 363–383. PMID 19514845. doi:10.1146/annurev.micro.091208.073504. hdl:2318/99264. Consultado em 23 de agosto de 2025. Arquivado do original (PDF) em 21 de junho de 2015
- ↑ Claridge, A. W.; et al. (1999). «Mycophagy by small mammals in the coniferous forests of North America: nutritional value of sporocarps of Rhizopogon vinicolor, a common hypogeous fungus». Journal of Comparative Physiology B. 169 (3): 172–178. PMID 10335615. doi:10.1007/s003600050208
- ↑ Cork, Steven J.; Kenagy, G. J. (1989). «Nutritional value of hypogeous fungus for a forest-dwelling ground squirrel». Ecology. 70 (3): 577–586. Bibcode:1989Ecol...70..577C. JSTOR 1940209. doi:10.2307/1940209
- ↑ Klironomos, John N.; Hart, Miranda M. (2001). «Food-web dynamics: Animal nitrogen swap for plant carbon». Nature. 410 (6829): 651–652. Bibcode:2001Natur.410..651K. PMID 11287942. doi:10.1038/35070643
- ↑ Yun, Wang; Hall, Ian R. (2004). «Edible ectomycorrhizal mushrooms: challenges and achievements» (PDF). Canadian Journal of Botany. 82 (8): 1063–1073. Bibcode:2004CaJB...82.1063Y. doi:10.1139/b04-051. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 29 de outubro de 2013
- ↑ Munyanziza, E.; Kehri, H. K.; Bagyaraj, D. J. (1997). «Agricultural intensification, soil biodiversity and agro-ecosystem function in the tropics: the role of mycorrhiza in crops and trees». Applied Soil Ecology. 6 (1): 77–85. Bibcode:1997AppSE...6...77M. doi:10.1016/S0929-1393(96)00152-7
- ↑ a b c d e Amaranthus, M.P. (1998). «The importance and conservation of ectomycorrhizal fungal diversity in forest ecosystems: lessons from Europe and the Pacific Northwest». US Department of Agriculture, Forest Service, Pacific Northwest Research Station (em inglês). Consultado em 23 de agosto de 2025
- ↑ Grant, Cynthia; et al. (2005). «Soil and fertilizer phosphorus: Effects on plant P supply and mycorrhizal development» (PDF). Canadian Journal of Plant Science. 85 (1): 3–14. doi:10.4141/p03-182. Consultado em 23 de agosto de 2025. Arquivado do original (PDF) em 22 de dezembro de 2014
- ↑ Scott, Neal A.; et al. (1999). «Soil carbon storage in plantation forests and pastures: land-use change implications». Tellus B. 51 (2): 326–335. Bibcode:1999TellB..51..326S. doi:10.1034/j.1600-0889.1999.00015.x
- ↑ Chapela, Ignacio H.; et al. (2001). «Ectomycorrhizal fungi introduced with exotic pine plantations induce soil carbon depletion» (PDF). Soil Biology and Biochemistry. 33 (12): 1733–1740. Bibcode:2001SBiBi..33.1733C. doi:10.1016/s0038-0717(01)00098-0. Consultado em 23 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
- ↑ Kernaghan, G.; et al. (2002). «In Vitro Selection of Boreal Ectomycorrhizal Fungi for Use in Reclamation of Saline-Alkaline Habitats» (PDF). Restoration Ecology. 10 (1): 43–51. Bibcode:1990reec.book.....J. doi:10.1046/j.1526-100x.2002.10105.x. Consultado em 25 de agosto de 2025. Cópia arquivada (PDF) em 21 de junho de 2015
- ↑ a b c d e Colpaert, J. (2011). «How metal-tolerant ecotypes of ectomycorrhizal fungi protect plants from heavy metal pollution». Annals of Forest Science. 68: 17–24. Bibcode:2011AnFSc..68...17C. doi:10.1007/s13595-010-0003-9
 . hdl:1942/11953
. hdl:1942/11953
- ↑ a b Blaudez, D.; Jacob, C.; Turnau, K.; Colpaert, J.V.; Ahonen-Jonnath, U.; Finlay, R.; Botton, B.; Chalot, M. (2000). «Differential responses of ectomycorrhizal fungi to heavy metals in vitro». Mycological Research. 104 (11): 1366–1371. doi:10.1017/s0953756200003166
- ↑ Gadd, G.M. (2004). «Microorganisms and heavy metal toxicity». Microbial Ecology. 4 (4): 303–317. PMID 24232222. doi:10.1007/bf02013274
- ↑ Bellion, M.; Courbot, M; Jacob, C.; et al. (2006). «Extracellular and cellular mechanism sustaining metal tolerance in ectomycorrhizal fungi». FEMS Microbiology Letters. 254 (2): 173–181. PMID 16445743. doi:10.1111/j.1574-6968.2005.00044.x
- ↑ Lasat, M.M.; Baker, A.J.M.; Kochian, L.V. (1998). «Altered Zn compartmentation in the root symplasm and stimulated Zn absorption into the leaf as mechanisms involved in Zn hyperaccumulation in Thlaspi caerulescens». Plant Physiology. 118 (3): 875–883. PMC 34798
 . PMID 9808732. doi:10.1104/pp.118.3.875
. PMID 9808732. doi:10.1104/pp.118.3.875
- ↑ Leyval, C.; Turnau, K.; Haselwandter, K. (1997). «Effect of heavy metal pollution on mycorrhizal colonization and function: physiological, ecological and applied aspects». Mycorrhiza. 7 (3): 139–153. Bibcode:1997Mycor...7..139L. doi:10.1007/s005720050174
- ↑ Southworth, D.; Tackleberry, L.E.; Massicotte, H.B. (2013). «Mycorrhizal ecology on serpentine soils». Plant Ecology and Diversity. 7 (3): 445–455. doi:10.1080/17550874.2013.848950
- ↑ Colpaert, J.V. 2008. Heavy metal pollution and genetic adaptations in ectomycorrhizal fungi. In: Avery S.V., Stratford M., Van West P. (eds) Stress in yeasts and filamentous fungi. Academic, Amsterdam, pp 157–174.
- ↑ Ruotsalainen, A.L.; Markkola, A.M.; Kozlov, M.V. (2009). «Mycorrhizal colonisation of mountain birch (Betula pubescens ssp czerepanovii) along three environmental gradients: does life in harsh environments alter plant–fungal relationships?». Environ Monit Assess. 148 (1–4): 215–232. Bibcode:2009EMnAs.148..215R. PMID 18327653. doi:10.1007/s10661-007-0152-y
- ↑ Staudenrausch, S.; Kaldorf, M.; Renker, C.; Luis, P.; Buscot, F. (2005). «Diversity of the ectomycorrhiza community at a uranium mining heap». Biol Fertil Soils. 41 (6): 439–446. Bibcode:2005BioFS..41..439S. doi:10.1007/s00374-005-0849-4
- ↑ Branco, S.; Ree, R. (2010). «Serpentine soils do not limit mycorrhizal fungal diversity». PLOS ONE. 5 (7): e11757. Bibcode:2010PLoSO...511757B. PMC 2909254
 . PMID 20668696. doi:10.1371/journal.pone.0011757
. PMID 20668696. doi:10.1371/journal.pone.0011757
- ↑ Egerton-Warburton, L.; Griffin, B. (1995). «Differential responses of Pisolithus tinctorius isolates to aluminium in vitro». Canadian Journal of Botany. 73 (8): 1229–1233. Bibcode:1995CaJB...73.1229E. doi:10.1139/b95-133
- ↑ Jourand, P.; Ducousso, M.; Loulergue-Majorel, C.; Hannibal, L.; Santoni, S.; Prin, Y.; Lebrun, M. (2010). «Ultramafic soils from New Caledonia structure Pisolithus albus in ecotype». FEMS Microbiology Ecology. 72 (2): 238–249. Bibcode:2010FEMME..72..238J. PMID 20199570. doi:10.1111/j.1574-6941.2010.00843.x

- ↑ a b Colpaert, J.V.; Vandenkoornhuyse, P.; Adriaensen, K.; Vangronsveld, J. (2000). «Genetic variation and heavy metal tolerance in the ectomycorrhizal basidiomycete Suillus luteus». New Phytologist. 147 (2): 367–379. Bibcode:2000NewPh.147..367C. doi:10.1046/j.1469-8137.2000.00694.x

- ↑ Colpaert, J.V.; Muller, L.A.H.; Lambaerts, M.; Adriaensen, K.; Vangronsveld, J. (2004). «Evolutionary adaptation to zinc toxicity in populations of Suilloid fungi». New Phytologist. 162 (2): 549–559. Bibcode:2004NewPh.162..549C. doi:10.1111/j.1469-8137.2004.01037.x

- ↑ Krznaric, E.; Verbruggen, N.; Wevers, J.H.L.; Carleer, R.; Vangronsveld, J.; Colpaert, J.V. (2009). «Cd-tolerant Suillus luteus: a fungal insurance for pines exposed to Cd». Environ Pollut. 157 (5): 1581–1588. Bibcode:2009EPoll.157.1581K. PMID 19211178. doi:10.1016/j.envpol.2008.12.030
- ↑ Adriaensen, K.; Vrålstad, T.; Noben, J.P.; Vangronsveld, J.; Colpaert, J.V. (2005). «Copper-adapted Suillus luteus, a symbiotic solution for pines colonizing Cu mine spoils». Appl Environ Microbiol. 71 (11): 7279–7284. Bibcode:2005ApEnM..71.7279A. PMC 1287625
 . PMID 16269769. doi:10.1128/aem.71.11.7279-7284.2005
. PMID 16269769. doi:10.1128/aem.71.11.7279-7284.2005
- ↑ Ruytinx, J.; Nguyen, H.; Van Hees, M.; De Beeck, O.; Vangronsveld, J.; Carleer, R.; Colpaert, J.V.; Adriaensen, K. (2013). «Zinc export results in adaptive zinc tolerance in the ectomycorrhizal basidiomycete Suillus bovinus». Metallomics. 5 (9): 1225–1233. PMID 23715468. doi:10.1039/c3mt00061c

- ↑ Luo, Zhi-Bin; et al. (2011). «The ectomycorrhizal fungus (Paxillus involutus) modulates leaf physiology of poplar towards improved salt tolerance». Environmental and Experimental Botany. 72 (2): 304–311. Bibcode:2011EnvEB..72..304L. doi:10.1016/j.envexpbot.2011.04.008
- ↑ Nikolova, Ivanka; Johanson, Karl J.; Dahlberg, Anders (1997). «Radiocaesium in fruitbodies and mycorrhizae in ectomycorrhizal fungi». Journal of Environmental Radioactivity. 37 (1): 115–125. Bibcode:1997JEnvR..37..115N. doi:10.1016/S0265-931X(96)00038-0
- ↑ Meharg, Andrew A.; Cairney, John WG (2000). «Ectomycorrhizas—extending the capabilities of rhizosphere remediation?» (PDF). Soil Biology and Biochemistry. 32 (11): 1475–1484. Bibcode:2000SBiBi..32.1475M. doi:10.1016/s0038-0717(00)00076-6. Consultado em 25 de agosto de 2025. Arquivado do original (PDF) em 21 de junho de 2015
- ↑ Fransson, Petra MA; Taylor, Andy FS; Finlay, Roger D. (2005). «Mycelial production, spread and root colonisation by the ectomycorrhizal fungi Hebeloma crustuliniforme and Paxillus involutus under elevated atmospheric CO2». Mycorrhiza. 15 (1): 25–31. PMID 14750001. doi:10.1007/s00572-003-0289-7
- ↑ Garcia, Maria O.; et al. (2008). «Mycorrhizal dynamics under elevated CO2 and nitrogen fertilization in a warm temperate forest» (PDF). Plant and Soil. 303 (1–2): 301–310. doi:10.1007/s11104-007-9509-9. Consultado em 25 de agosto de 2025. Cópia arquivada (PDF) em 30 de setembro de 2021
- ↑ a b Compant, Stéphane; Marcel; Der Heijden, GA Van; Sessitsch, Angela (2010). «Climate change effects on beneficial plant–microorganism interactions». FEMS Microbiology Ecology. 73 (2): 197–214. PMID 20528987. doi:10.1111/j.1574-6941.2010.00900.x

- ↑ Malcolm, Glenna M.; et al. (2008). «Acclimation to temperature and temperature sensitivity of metabolism by ectomycorrhizal fungi». Global Change Biology. 14 (5): 1169–1180. Bibcode:2008GCBio..14.1169M. doi:10.1111/j.1365-2486.2008.01555.x
- ↑ Arnolds, E. E. F. (1991). «Decline of ectomycorrhizal fungi in Europe». Agriculture, Ecosystems & Environment. 35 (2): 209–244. Bibcode:1991AgEE...35..209A. doi:10.1016/0167-8809(91)90052-y
- ↑ «European Council for the Conservation of Fungi». www.eccf.eu. Consultado em 25 de agosto de 2025. Cópia arquivada em 16 de julho de 2019
- ↑ Willis, Katherine J. (2018). «State of the World's Fungi». State of the World's Fungi (em inglês). Consultado em 16 de julho de 2019. Cópia arquivada em 13 de março de 2019
- ↑ a b Wiensczyk, A.,Gamiet, S., Durall, D., Jones, M., Simard, S. 2002. Ectomycorrhizae and forestry in British Columbia: A summary of current research and conservation strategies. Journal of Ecosystems and Management 2.1. Arquivado em 21 junho 2015 no Wayback Machine
- ↑ Amaranthus, Michael P., et al. Soil compaction and organic matter affect conifer seedling nonmycorrhizal and ectomycorrhizal root tip abundance and diversity. Forest Service research paper. No. PB—97-104301/XAB; FSRP-PNW—494. Forest Service, Portland, OR (United States). Pacific Northwest Research Station, 1996. [1] Arquivado em 16 outubro 2023 no Wayback Machine
- ↑ Dahlberg, Anders; et al. (2001). «Post-fire legacy of ectomycorrhizal fungal communities in the Swedish boreal forest in relation to fire severity and logging intensity». Biological Conservation. 100 (2): 151–161. Bibcode:2001BCons.100..151D. doi:10.1016/s0006-3207(00)00230-5
- ↑ Mah, Karen; et al. (2001). «The impacts of broadcast burning after clear-cutting on the diversity of ectomycorrhizal fungi associated with hybrid spruce seedlings in central British Columbia» (PDF). Canadian Journal of Forest Research. 31 (2): 224–235. Bibcode:2001CaJFR..31..224M. doi:10.1139/x00-158. Consultado em 25 de agosto de 2025. Cópia arquivada (PDF) em 4 de março de 2016
- ↑ Hawksworth, David L (1991). «The fungal dimension of biodiversity: magnitude, significance, and conservation». Mycological Research. 95 (6): 641–655. doi:10.1016/S0953-7562(09)80810-1
Ligações externas
- Mycorrhizal Associations: The Web Resource Ilustrações abrangentes e listas de plantas e fungos micorrízicos e não micorrízicos
- Mycorrhizas – a successful symbiosis Pesquisa de biossegurança em cevada geneticamente modificada
- International Mycorrhiza Society Sociedade Internacional de Micorrizas