Gesneriaceae
Gesneriaceae
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
Gloxinia perennis. | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Distribuição geográfica | |||||||||||||||||
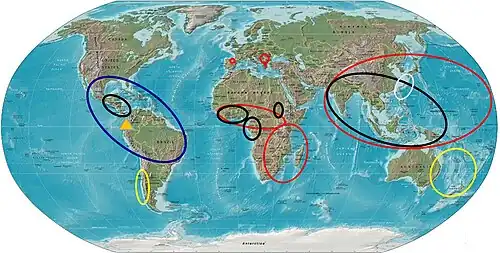
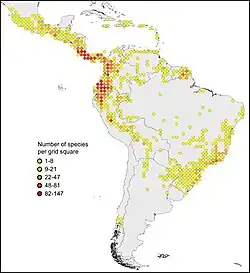 Distribuição e riqueza de espécies de Gesneriaceae no Novo Mundo com base em 48 000 ocorrências compiladas a partir do portal de dados do GBIF (http://data.gbif.org, novembro de 2011), Perret et al. (2006) e dados não publicados (A. Chautems). Observe a distribuição centrada nos Andes com uma concentração de espécies no norte dos Andes e na América Central e o centro secundário de diversidade na floresta atlântica brasileira. Ocorrências nos Andes temperados do Chile correspondem a espécies de Coronanthereae.
| |||||||||||||||||
| Subfamílias | |||||||||||||||||
| |||||||||||||||||
| Sinónimos | |||||||||||||||||






_(8611177560).jpg)
.jpg)
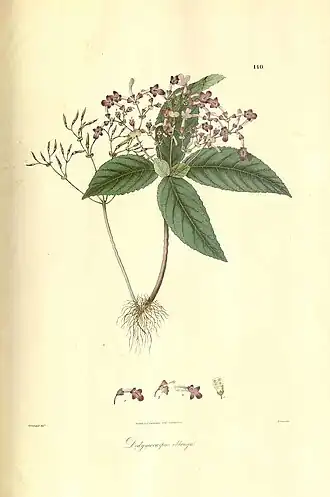
Gesneriaceae é uma família de plantas com flor, da ordem Lamiales, que agrupa cerca 3 540 espécies, repartidas por mais de 152 géneros.[3] A família tem distribuição natural nos trópicos e subtrópicos do Velho Mundo (quase todas espécies da subfamília Didymocarpoideae) e do Novo Mundo (a maioria das espécies da subfamília Gesnerioideae), com um número muito pequeno estendendo-se às regiões temperadas. Muitas espécies produzem flores coloridas e vistosas e são cultivadas como plantas ornamentais e plantas de interior.[4][5] A etimologia do nome da família é baseado no género Gesneria, que homenageia o naturalista e humanista suíço Conrad Gessner.[6]
Descrição
A família Gesneriaceae Rich. & Juss. ex DC. é uma família de plantas angiospérmicas da ordem Lamiales,[7] que inclui algumas das espécies mais conhecidas daquela ordem, como são as espécies dos géneros Gloxinia e Saintpaulia, também conhecida como violetas-africanas. A maioria das espécies apresenta hábito arbustivo ou subarbustivo, mas muitas são herbáceas ou, mais raramente, lianas. O agrupamento apresenta distribuição pantropical e pansubtropical. No Brasil existem 28 géneros, dos quais oito são endemismos, compreendendo 221 espécies.[8]
Morfologia
- Hábito e filotaxia
A maioria das espécies são herbáceas perenes ou subarbustos, mas algumas são arbustos lenhosos ou pequenas árvores. Algumas espécies apresentam raízes fibrosas, outras raízes tuberosas ou mesmo rizomas. O caule herbáceo ou lenhoso, ereto, escandente ou pendente.
A filotaxia foliar é geralmente oposta e decussada, mas em alguns grupos as folhas têm uma disposição espiralada, verticilada ou alterna. As folhas simples, sem estípulas, com margens inteiras ou serrilhadas, pecioladas ou subsésseis, cobertas, ou não, por densos tricomas.
- Inflorescências e flores
As inflorescências são folhosas ou rodeadas por brácteas, formando tirsos indeterminados com cortes axilares pareados, que às vezes são reduzidos a uma única flor, porém algumas flores não apresentam essa característica. Tal como acontece com outros membros da Lamiales, as flores têm uma corola em geral zigomórfica, cujas pétalas estão fundidas num tubo, e não existe nenhuma característica morfológica evidente que diferencie uma gesneriácea de qualquer outro membro da ordem Lamiales.[5] As gesneriáceas diferem contudo das famílias filogeneticamente mais próximas por terem uma estrutura de inflorescência invulgar, a «cimeira de flores emparelhadas», mas algumas gesneriáceas não possuem esta característica, e algumas outras Lamiales (como as Calceolariaceae e algumas Scrophulariaceae) partilham-na.
A família é caracterizada por flores bissexuais, zigomorfas, raramente actinomorfas, e diclamídeas, protândricas, ressupinadas ou não; corolas bi- ou tri-labiadas com quatro ou cinco pétalas fundidas, gamopétala; cálice com cinco lobos (sépalas), pouco unidas na base, às vezes até 1/3 ou quase a 1/2 do comprimento, verdes ou coloridas, inteiras ou dentadas, gamossépalo ou dialissépalo. Possui quatro estames, inclusos, raramente exsertos, epipétalos, ocasionalmente estéreis (estaminódios); estilete simples, estigma estomatomórfico ou bilobado. Anteras conadas, rimosas, epipétalos, em números de dois ou mais (raramente cinco), basifixa ou dorsifixa; ovário súpero ou ínfero com uma única câmara, bicarpelar, pluriovulados; placentação parietal ou semi-parietal (e.g. Sanango). A fórmula floral é:
O ovário pode ser súpero, semi-ínfero ou totalmente ínfero. As Gesneriaceae têm sido tradicionalmente separadas das Scrophulariaceae por terem um ovário unilocular em vez de bilocular, com placentação parietal em vez de axial.
- Frutos e sementes
Os frutos podem ser uma cápsula, seca ou carnuda, ou uma baga, de formas muito variadas, loculicidas (com fenda longitudinal), septicidas (com fenda transversal) ou que se abrem com uma tampa. Os frutos apresentam coloração que vai de muito vistosa a discreta.[9] Cada fruto contém muitas sementes, que são sempre pequenas e numerosas.[10][11]
As sementes, sempre minúsculas, têm forma fusiforme a elipsoidal ou ovóide e, por vezes, apresentam apêndices numa ou em ambas as extremidades.[10] Na maioria dos casos, as sementes contêm endosperma oleaginoso, composto por uma ou várias camadas. Contudo, nas Cyrtandroideae, não existe endosperma.[11]
O embrião é reto apresenta dois cotilédones iguais. Nas Gesneriaceae paleotropicais, após a germinação, um cotilédone cresce mais rapidamente do que o outro (embrião anisocótilo).[10]
- Detalhes de flores e frutos
-
 Bagas de Columnea orientandina.
Bagas de Columnea orientandina. -
 Ramonda myconi cujos frutos são cápsulas secas deiscente.
Ramonda myconi cujos frutos são cápsulas secas deiscente. -
 Na espécie Drymonia serrulata, o cálice resistente contém o fruto carnudo, que se abre quando maduro e liberta uma massa frutal com as sementes. A superfície interna vermelha da casca do fruto é particularmente notável.
Na espécie Drymonia serrulata, o cálice resistente contém o fruto carnudo, que se abre quando maduro e liberta uma massa frutal com as sementes. A superfície interna vermelha da casca do fruto é particularmente notável.
Sinecologia
Cerca de metade das espécies do Novo Mundo (ou seja, a subfamília Gesnerioideae) estão coadaptadas à polinização por aves, particularmente por beija-flores nas Américas. As espécies polinizadas por aves têm normalmente flores com dois lábios em tons de vermelho; exemplos podem ser encontrados nos géneros Asteranthera, Columnea e Sinningia. Entre os géneros do Velho Mundo, Aeschynanthus tem flores semelhantes.[12]
Alguns géneros da Ásia (como Aeschynanthus) e Américas (como Sarmienta) apresentam um estilo de vida epifítico. Outras espécies são saxícolas e crescem sobre rochas (como Aeschynanthus), obtendo suporte físico e nutrientes recorrendo aos musgos que se desenvolvem nesse mesmo habitat. Outras espécies apresentam hábitos hemiepifíticos (como Mitraria coccinea e Asteranthera ovata), rupícola e terrícola. Muitas dessas espécies toleram grande intensidade luminosa. Nas regiões montanhosas da Europa várias espécies crescem a grande altitude, tolerando invernos frios sob uma cobertura de neve.[13]
- Aparência típica das flores polinizadas por pássaros
-
 Asteranthera ovata
Asteranthera ovata -
.jpg) Columnea microphylla
Columnea microphylla -

-
 Aeschynanthus speciosus
Aeschynanthus speciosus
- Ecologia da polinização (ecologia floral)
Quase todas as espécies da família Gesneriaceae são fertilizadas por polinização cruzada. Para favorecer a polinização cruzada, as Gesneriaceae desenvolveram os seguintes mecanismos: protandria, em que o pólen amadurece e é liberado pelas anteras antes que os estigmas da mesma flor estejam prontos para receber pólen; protoginia, em que os estigmas ficam receptivos ao pólen e deixam de estar receptivos antes que o pólen amadureça e seja libertado pelas anteras na mesma flor; enantiostilia, que é uma posição esquerda-direita do estilete combinada com a posição oposta das anteras. A protândria predomina na família das Gesneriaceae. A protoginia parece ocorrer apenas em algumas espécies de Gesneria polinizadas por morcegos. A enantiostilia ocorre nos géneros Didymocarpus, Henckelia e Saintpaulia, já que nestes géneros as anteras permanecem numa posição fixa e afastada em relação ao estigma.[14]
- Flores polinizadas por pássaros
-
 Um beija-flor macho da espécie Chaetocercus berlepschi a sugar o néctar de uma flor de Kohleria spicata, realizando assim a polinização.
Um beija-flor macho da espécie Chaetocercus berlepschi a sugar o néctar de uma flor de Kohleria spicata, realizando assim a polinização. -
_001.jpg) As flores zigomórficas da Rhytidophyllum tomentosum contêm néctar em abundância.
As flores zigomórficas da Rhytidophyllum tomentosum contêm néctar em abundância. -
 Flor zigomórfica de Gasteranthus delphinioides com corola branca, cujo tubo se estreita na extremidade inferior.
Flor zigomórfica de Gasteranthus delphinioides com corola branca, cujo tubo se estreita na extremidade inferior.
A autopolinização facultativa ou obrigatória é conhecida ou presumida apenas em poucas espécies de Gesneriaceae (a autogamia, ocorre, por exemplo, em espécies dos géneros Epithema, Rhynchoglossum e Monophyllaea). Nestas espécies, as flores são geralmente pequenas e discretas e, muitas vezes, formam-se em grande quantidade. A frutificação é de quasetotal. Em poucos casos, as flores não se abrem e a fertilização ocorre nos botões florais (cleistogamia, por exemplo, em Streptocarpus nobilis e em Codonanthopsis dissimulata).[14]
Em quase todas as espécies da família Gesneriaceae, a polinização é feita por animais (zoofilia). As aves desempenham o papel principal na polinização, seguidos pelos insetos e morcegos.[14]
Nas espécies da região neotropical, predomina a ornitofilia, ou seja, a polinização é feita por aves. Cerca de 60 % da subfamília neotropical Gesnerioideae (ou seja, cerca de 1 000 espécies) são polinizadas por beija-flores (família Trochilidae). O centro de diversidade das espécies polinizadas por aves está na Colômbia e no Equador. Existem significativamente mais espécies epífitas do que terrícolas que são polinizadas por aves.[14]
As espécies ornitófilas são facilmente reconhecíveis pela forma tubular ou forma de prato da corola da flor, bem como pelas cores das flores, que apresentam tons de vermelho muito diferentes, mas geralmente brilhantes (do vermelho ao laranja e ao amarelo brilhante). Além disso, as flores para aves oferecem sempre néctar em abundância. A posição dos estames e do estigma garante que o pólen é removido da cabeça do pássaro e que a polinização ocorra quando este visitar a próxima flor.
Além das características das flores, outras características também desempenham um papel importante na atração dos beija-flor. Folhas grandes e coloridas nas inflorescências (por exemplo, em espécies de Drymonia) ou manchas e bordos vermelhos ou janelas translúcidas nas folhas (por exemplo, em Columnea sect. Collandra) servem para atrair os pássaros; nessas espécies, as flores são frequentemente relativamente discretas e escondidas nas folhas.
Em Columnea florida, observou-se que os beija-flor jovens e inexperientes das espécies Phaethornis longuemareus e Heliodoxa jacula primeiro se dirigem às janelas vermelhas translúcidas das folhas e depois passam alguns segundos a examinar diferentes partes da planta antes de encontrarem as flores; os espécimes experientes voam sobre as manchas vermelhas e depois mergulham rapidamente por baixo das folhas para alcançarem diretamente as flores nas axilas das folhas. A polinização por aves é muito menos comum nas Gesneriaceae do Velho Mundo (nos géneros Aeschynanthus e Agalmyla e em algumas espécies dos géneros Henckelia, Streptocarpus e Cyrtandra, que são polinizados maioritariamente por abelhas). Na África e na Ásia, as espécies de aves da família Nectariniidae e, em algumas áreas de Sulawesi à Nova Zelândia, da família Meliphagidae são consideradas polinizadoras.[14]
A polinização por morcegos (quiropterofilia) é conhecida apenas na região neotropical e desenvolveu-se várias vezes de forma independente em alguns géneros (como em espécies de Capanea, Drymonia, Kohleria, Gesneria, Rhytidophyllum, Sinningia e Paliavana). Nessas espécies, as corolas mais ou menos zigomorfas possuem tubos curtos e largos ou claramente acampanados. As suas corolas são amareladas ou esverdeadas com manchas castanhas ou violeta sujo. Nessas flores é produzido néctar em grandes quantidades. Observações sobre a polinização de Sinningia brasiliensis e Paliavana prasinata por espécies de morcegos filostomídeos (da família Phyllostomidae) e especialmente de morcegos florícolas (da subfamília Glossophaginae) descrevem que, para a polinização quiropterófila, são típicos a ântese durante a noite, o odor desagradável e o aumento noturno da secreção de néctar.[14]
Entre os insetos, as abelhas (Apidae) desempenham o papel mais importante. Nos neotrópicos, as abelhas do grupo géneros da tibo Euglossini são particularmente importantes, mas também as Anthophoridae, provavelmente as Xylocopinae e outras.[14] Cerca de 30 % das espécies da subfamília Gesnerioideae é polinizada por ambos os sexos (nas orquídeas, por exemplo, isso ocorre apenas pelos machos) das abelhas da tribo Euglossini. A polinização por borboletas parece ser rara, havendo relatos isolados de borboletas noturnas (mariposas).
Presume-se que a polinização seja feita por borboletas (lepidópteros diurnos), embora não haja registos de observação, quando as flores oferecem néctar e possuem corolas vermelhas ou azuis em forma de prato com tubos longos e estreitos e lóbulos planos (por exemplo, em algumas espécies dos géneros Achimenes, Sinningia e Episcia). As borboletas noturnas polinizam flores muito perfumadas com corolas brancas, creme a amarelas, com tubos longos e estreitos (por exemplo, Sinningia tubiflora). Outros visitantes das flores, como vespas e dípteros (Diptera), como mosquitos (Nematocera) e sirfídeos (Syrphidae), também podem estar envolvidos na polinização; no entanto, nenhuma espécie está especificamente adaptada a um desses polinizadores. As flores em forma de «buraco de fechadura» de algumas espécies de Streptocarpus, com tubos estreitos, lóbulos planos e pequenas aberturas laterais estreitas, são provavelmente visitadas por moscas de probóscide longa.[14]
O principal efeito para atrair os polinizadores é visual. As seguintes adaptações ecológicas das flores para atrair determinados polinizadores estã presentes nas Gesneriaceae: flores nectaríferas, com corolas zigomorfas, em que as pétalas mais ou menos coloridas estão fundidas numa corola tubular, muitas vezes longa; presença de um disco nectarífero para a secreção de néctar; néctar frequentemente recolhido numa protuberância especial na base do tubo da corola e o pólen é pegajoso.
Ocorrem também flores com nectário falso, que têm a aparência de flores com néctar, mas, se houver nectários, estes não são funcionais. Algumas espécies de Ornithoboea podem ser classificadas como flores com néctario falso. Devido aos cálices aplainados e à forma das corolas, as suas flores parecem flores de orquídeas; pode tratar-se, de facto, de um mimetismo das flores das orquídeas (talvez de Calanthe), mas, no mínimo, têm a forma de flores nectaríferas.
Outra adptaçção é a ocorrência de flores polínicas, qunado ass flores são inclinadas e as pétalas estão fundidas numa corola curta em forma de sino; por vezes têm cinco estames férteis e as anteras relativamente grandes, frequentemente de cor amarela ou laranja brilhante, que sobressaem mais ou menos do tubo da coroa e por vezes ficam unidas; nas anteras, a extremidade superior abre-se com poros ou fendas transversais e liberta pólen não pegajoso e pulverulento, que é espalhado pelo zumbido dos visitantes das flores. Nestas flores, os nectários não são funcionais ou estão reduzidos (como ocorre em Ramonda, Conandron, Didymocarpus cordatus, Bellonia, Niphaea, Phinea e Napeanthus).
Outra adptação é a presença de flores com pólen parcial ou totalmente falso. Neste caso, o pólen abundante é simulado pelas paredes amarelas das anteras (por exemplo, em Saintpaulia, as paredes amarelas e robustas das anteras permanecem atraentes durante muito mais tempo do que o período de presença do pólen. Por exemplo, a espécie Petrocosmea kerrii tem uma mancha amarela na coroa acima da antera; a Henckelia caerulea tem filamentos amarelos, mas as anteras verdadeiras têm uma cor que as oculta).
Outra forma de atarair polinizadores é a produção de flores perfumadas, mais conhecidas na Gloxinia perennis, mas que também ocorrem em Monopyle. Neste caso as pétalas estão fundidas num tubo coronal muito curto e largo e os osmóforos (tecidos produtores de perfume) estão presentes perto da base do tubo coronal, em vez dos nectários; os osmóforos consistem em células epidérmicas em paliçada, castanho-púrpura, que secretam pequenas gotas de terpenos, que são recolhidas pelas abelhas.[14]
A maioria das espécies da família Gesneriaceae tem flores inodoras, pelo menos todas as espécies polinizadas por pássaros. Algumas espécies de cerca de 15 géneros, especialmente da região neotropical, têm flores perfumadas. Há uma variedade surpreendente de aromas, que vão desde o doce semelhante ao mel, almiscarado, limão, cravo, repolho, carniça e outros. O perfume parece ser direcionado a determinados polinizadores. Na espécie Sinningia tubiflora, o perfume cítrico atrai mariposas, enquanto o perfume de couve da Capanea cf. grandiflora atrai morcegos. Também há relatos de perfume em algumas espécies paleotropicais, como a Streptocarpus vandeleurii.[14]
- Detalhes de flores e frutos
-
Flor em detalhe de Niphaea oblonga
-
 Flor de Gloxinia perennis
Flor de Gloxinia perennis -
 Enantiostilia numa variedade de Saintpaulia ionantha, onde o estilo está lateral em relação às anteras.
Enantiostilia numa variedade de Saintpaulia ionantha, onde o estilo está lateral em relação às anteras.
- Ecologia da dispersão
Os diásporos são as bagas ou, no caso dos frutos em cápsula, as sementes.[14]
Nas espécies com frutos em cápsula, as sementes minúsculas são espalhadas quando maduras e disseminadas pelo vento ou pela chuva. A disseminação de sementes com apêndices ocorre obviamente pelo vento. Na maioria das vezes, são espécies epífitas cujas sementes possuem pêlos como apêndices, que as ajudam, especialmente quando ficam húmidas, a aderir à casca dos ramos e ao tronco das árvores. Nas espécies com cauda de pelos, os pelos espalham-se em tempo seco e formam um pára-quedas. A grande eficácia da dispersão com caudas de pelos explica a ampla distribuição de Aeschynanthus sect. Polytrichium na Ásia e na Malésia.[14]
Nas espécies com bagas ou frutos carnudos, a dispersão é feita principalmente por aves (ornitocoria), pequenos mamíferos ou formigas (mirmecocoria).[14]
Para que as sementes sejam transportadas pelas formigas, existem diferentes adaptações, por exemplo, no género Codonanthe, algumas espécies possuem sementes invulgarmente grandes, com cerca de 3 milímetros de comprimento, que são revestidas na metade inferior por uma taça semelhante a um arilo, enquanto outras espécies possuem sementes multicelulares, hialinas, e outras espécies são típicas «plantas de formigueiro», nas quais o transporte de sementes pelas formigas foi documentado.
Os funículos aumentados, carnudos e brancos da Chrysothemis friedrichsthaliana contêm óleos gordurosos e oferecem às formigas algo semelhante a elaiossomas. Na espécie Rufodorsia minor, o transporte de sementes pelas formigas foi observado depois das bagas terem sido abertas, na maioria das vezes, por pássaros. As formigas são frequentemente disseminadoras secundárias de sementes, após os frutos, que são indeiscentes, serem abertos.[14]
Quando aves e pequenos mamíferos são responsáveis pela dispersão, trata-se de endocoria, a chamada dispersão digestiva, na qual as sementes passam pelo trato digestivo dos animais. Para atrair animais que comam os frutos ou partes deles com as sementes, as Gesneriaceae apresentam algumas adaptações. Para isso, as bagas maduras inteiras são atraentes ou, após a abertura dos frutos, é exibida uma massa de frutos. O cálice durável também pode funcionar como órgão de exibição.[14]
Distribuição
A distribuição de Gesneriaceae é pantropical e pansubtropical, estando presentes especialmente em áreas tropicais montanhosas, com poucas espécies em zonas de clima temperado. A maioria dessas espécies tem distribuição natural na América do Sul temperada, no sul da Europa e norte da China.[15]
A família Gesneriaceae possui uma ampla área de distribuição natural no Velho Mundo e no Novo Mundo. As espécies da família Gesneriaceae ocorrem principalmente nas regiões tropicais e subtropicais em todo o mundo. Algumas espécies ocorrem nas regiões temperadas da América do Sul, Europa, Himalaia e norte da China.[14]
Para sul, a área de distribuição total estende-se até ao sudeste da Austrália, Nova Zelândia e sul do Chile. As poucas espécies dos géneros Ramonda e Haberlea são remanescentes terciários nos Pirenéus e na Península Balcânica.
Existem cerca de 60 géneros na biorregião indo-malaia (incluindo o Afeganistão, Paquistão, sul da Ásia e sudeste asiático) e na Neotropis. Na África, existem cerca de nove géneros com cerca de 160 espécies, enquanto na Europa existem apenas três géneros com apenas seis espécies. Apenas cerca de nove géneros e 20 espécies existem exclusivamente no hemisfério sul. Os géneros Rhynchoglossum na Ásia, mas também com uma espécie na região neotropical, e Epithema, com uma espécie na África Ocidental, mas as outras 20 espécies na Ásia e no arquipélago indonésio, apresentam uma distribuição fortemente disjunta. Na China, existem cerca de 56 géneros (dos quais 25 apenas nessa região) e cerca de 442 espécies (das quais 354 são endémicas). Na Austrália, apenas cinco géneros são nativos, mas dois géneros monotípicos ocorrem apenas nessa região.
Na região neotropicam (Neotropis) ocorrem sete tribos com cerca de 60 géneros e mais de 1 200 espécies. Naquela região ocorrem os seguintes centros de diversidade: com mais de 400 espécies, a região da Colômbia ao Peru; com cerca de 250 espécies, a América Central; com mais de 200 espécies, o leste do Brasil; com cerca de 100 espécies, a Guiana; e com cerca de 100 espécies, o México tropical.[9]
No Brasil a família tem ocorrência confirmada em todos os estados, nos domínios fitogeográficos Amazônia, Caatinga, Cerrado, Mata Atlântica e Pampa.
Usos e cultivo
Alguns géneros da família são cultivados como plantas ornamentais, tanto em jardins como em interiores. Nesses géneros muitas espécies usadas como plantas ornamentais em casas e jardins, são objecto de horticultura. As espécies cultivadas mais comuns são: Sinningia speciosa, Streptocarpus ionanthus e Streptocarpus rexii.[17]
Entre os géneros que têm espécies que são cultivadas contam-se, nomeadamente, os seguintes: Aeschynanthus, Achimenes, Aeschynanthus, Columnea, Episcia, Gesneria, Gloxinia, Haberlea, Kohleria, Nematanthus (sin. Hypocyrta), Petrocosmea, Primulina, Ramonda, Smithiantha e Streptocarpus (prímulas-do-cabo). [12] Um dos membros mais conhecidos dos jardineiros são as violetas-africanas em especial as pertencentes ao grupo Streptocarpus secção Saintpaulia.
As gesneriáceas são para efeitos de cultivo geralmente divididas em três grupos, com base no facto de os seus caules serem ou não modificados em órgãos de armazenamento e na forma como isso ocorre: rizomatosas, tubérculos e espécies de raízes fibrosas, ou seja, aquelas que não possuem tais estruturas de armazenamento (embora todas as gesneriáceas tenham raízes fibrosas).
Para além da utilização como plantas ornamentais, quase nenhuma espécie da família Gesneriaceae é utilizada. Apenas se conhece que as folhas da Conandron ramondioides são cozidas e consumidas quando não há mais nada disponível.[18]
A maioria das Gesneriaceae, de acordo com a sua origem tropical, gosta de calor durante todo o ano. Muitas das espécies preferem locais claros e quentes, sem exposição direta ao sol. Existem muitos géneros, espécies e variedades da família Gesneriaceae que são adequados como plantas de interior (seleção):
- Saintpaulia, podem ser facilmente reproduzidas através de estacas foliares.
- Streptocarpus, podem ser facilmente reproduzidas através de estacas de folhas.
- Gloxínias (Sinningia speciosa (Lodd.) Hiern), formam tubérculos.
- Columnea, originalmente epífitas, são frequentemente cultivadas como «plantas suspensas».
- Episcia, plantas rastejantes.
- As flores-da-vergonha (Aeschynanthus), originalmente epífitas, são frequentemente cultivadas como plantas suspensas.
- Nematanthus (sin.: Hypocyrta Mart., p.p.)
- Achimenes, formam tubérculos e são fáceis de propagar através de estacas.
- Smithiantha, formam tubérculos.
- Chrysothemis
- Kohleria
- Codonanthe.
-
Híbrido de Saintpaulia-ionantha, com a típica cor azul.
-
 Streptocarpus sp.
Streptocarpus sp. -
 Achimenes sp.
Achimenes sp. -
 Episcia reptans.
Episcia reptans.
Conservação
Na Lista Vermelha de espécies ameaçadas da IUCN estavam registadas, em 2013, 152 espécies da família Gesneriaceae.[19] No entanto, na Austrália e na África do Sul, por exemplo, existem listas vermelhas nacionais cujas espécies não estão registadas na IUCN. Portanto, há muito mais espécies ameaçadas.
Taxonomia e filogenia











.jpg)

_Gesneraid_Family_(3073307484)_(2).jpg)










Sistemática e história botânica
A primeira publicação da família Gesneriaceae sob o nome «Gessnerieae» é atribuída a Louis Claude Marie Richard e Antoine Laurent de Jussieu em Augustin-Pyrame de Candolle: Essai sur les Propriétés Médicales des Plantes, 2.ª edição, p. 192, de 11 de maio de 1816. O género-tipo é Gesneria L.. São sinónimos taxonómicos para Gesneriaceae (Rich. & Juss.) ex DC.: Belloniaceae Martinov, Didymocarpaceae D.Don, Ramondaceae Godr., Besleriaceae Raf. e Cyrtandraceae Jack.
Gesneriaceae é um nome conservado (nomen conservandum),[2] o que significa que, embora tenham sido publicados anteriormente nomes alternativos menos utilizados para a família, o Código Internacional de Nomenclatura para Algas, Fungos e Plantas especifica este como o nome a ser utilizado. Foi publicado por Louis Claude Richard e Antoine Laurent de Jussieu em 1816.[1] O nome genérico «Gesneria» e, consequentemente, o nome da família Gesneriaceae, derivado deste, é uma homenagem ao naturalista e filósofo suíço Konrad Geßner, mais conhecido por Conrad Gessner ou Conradus Gesnerius (1516 — 1565).
Em 1829, Barthélemy Dumortier dividiu a família em duas tribos, com base no número de estames.[20] No entanto, o único género que colocou na sua tribo de dois estames, Columellia, está agora colocado na família separada Columelliaceae.[21] A publicação de Dumortier tem sido considerada como a primeira sobre a família por algumas fontes.[22]
Os botânicos que deram contribuições significativas para a sistemática da família são George Bentham, Robert Brown, B.L. Burtt, C.B. Clarke, Olive Mary Hilliard, Joseph Dalton Hooker, William Jackson Hooker, Karl Fritsch, Elmer Drew Merrill, Harold E. Moore Jr., John L. Clark, Conrad Vernon Morton, Henry Nicholas Ridley, Laurence Skog, W.T. Wang, Anton Weber e Hans Wiehler. A Gesneriad Society é uma sociedade internacional de horticultura dedicada à promoção, cultivo e estudo das Gesneriaceae.[23]
Dentro da ordem das Lamiales, as Gesneriaceae são a famílila filogeneticamente mais próximas das Calceolariaceae.
Filogenia
A partir de 1997, estudos de filogenética molecular levaram a mudanças extensas na classificação da família Gesneriaceae e seus géneros, muitos dos quais foram recircunscritos ou sinonimizados. Novas espécies ainda estão a ser descobertas, particularmente na Ásia, e podem alterar ainda mais os limites genéricos. Uma filogenia consensual usada para construir classificações da família em 2013 e 2020 é mostrada abaixo (ao nível das tribos). A família Calceolariaceae é mostrada como grupo irmão da família Gesneriaceae.[24][25]
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
Um estudo filogenómico publicado em 2021, que utilizou 418 genes nucleares, confirmou a monofilia de todas as subfamílias e tribos. Esse estudo permitiu resolver o género Peltanthera como grupo irmão de um clado de Calceolariaceae e Gesneriaceae. Dentro da subfamília das Gesnerioideae, descobriu-se que as Napeantheae, e não as Titanotricheae, eram o táxon irmão das restantes tribos. A posição das Titanotricheae variou de acordo com o método utilizado para construir o cladograma, o que os autores sugeriram ser devido a uma triagem incompleta da linhagem (efeito conhecido por Incomplete lineage sorting ou ILS) após uma rápida divergência. A posição filogenética do género Titanotrichum permanece indefinida.[26]
| Baseado em concatenação | Baseado em coalescência | ||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
|
O género Sanango nem sempre foi incluído na família Gesneriaceae. No entanto, estudos filogenéticos moleculares publicados até 2021 sugerem que aquele género pertence à família como o membro mais basal, sendo colocado na sua própria subfamília. Os estudos filogenéticos também mostram que o género Peltanthera está fora da família,[25][26] embora algumas fontes ainda o coloquem dentro da família Gesneriaceae.[27] O género Rehmannia também tem sido por vezes incluído na família, mas agora é posicionado na família Orobanchaceae.[28]
Nenhuma característica morfológica divide absolutamente as duas subfamílias principais (ou seja, forma uma sinapomorfia uniforme). As plântulas de Gesnerioideae têm cotilédones normais, do mesmo tamanho e forma (isocotilos). Os cotilédones das Didymocarpoideae são geralmente, mas nem sempre, diferentes em tamanho e forma (anisocotilos). Um cotilédone deixa de crescer e murcha, enquanto o outro continua a crescer, podendo até formar uma folha grande que é a única que a planta tem (Monophyllaea, alguns Streptocarpus). As flores das Gesnerioideae têm geralmente quatro estames férteis, raramente dois ou cinco. As flores Didymocarpoideae têm geralmente dois estames férteis, menos frequentemente quatro, raramente um ou cinco.[25]
Filogenia e evolução
Acredita-se que a subfamília Gesnerioidea tenha se diversificado entre 43 e 45 milhões de anos atrás. Gesneriaceae já foi dividida em duas famílias, a Gesneriaceae predominantemente neotropical e Didymocarpaceae palaeotropical (i.e. com ocorrência na África e Ásia tropical), devido principalmente a distinções na posição do ovário. Essas famílias foram agrupadas no final do século XIX.[29]
Recentemente estudos moleculares sobre os membros da família Scrophulariaceae propuseram que Calceolaria, Jovellana, Peltanthera e Sanango são espécies pertencente a Gesneriaceae[29]. Numa das revisões mais recentes baseadas em filogenia molecular,[30] foram reconhecidos três subfamílias em Gesneriaceae: Sanangoideae, Gesnerioideae e Didymocarpoideae.
Alguns estudos bioquímicos indicam uma relação próxima entre Plocospermataceae e Gesneriaceae, pois as duas famílias compartilham alguns compostos químicos como o cornosídeo, o qual também é encontrado em Tetrachondraceae.[29]
Outros estudos sistemáticos mostraram que Gesneriaceae não é um grupo relacionado com os demais da ordem Lamiales, porém recentemente foi sugerida uma relação de grupo-irmão de Gesneriaceae com Calceolariaceae.[31]
Vulgarmente, a família Gesneriaceae é dividida em três grupos com base nos caracteres morfológicos de suas raízes (i.e. rizomatoso, tuberoso ou “fibroso”, embora todas as Gesneriaceae tenham raízes fibrosas).
Subfamílias e géneros
A família das Gesneriaceae era dividida em quatro subfamílias antes de 2003/2004. De acordo com Anton Weber, num trabalho de 2004,[32] aquelas quatro subfamílias representavam quatro grupos informais, uma vez que não eram monofiléticas, mas tinham o mesmo número de tribos e géneros. Aquela era, portanto, apenas uma solução provisória, até que novas investigações permitissem estabelecer grupos monofiléticos. A partir de 2013, passaram novamente a existir quatro subfamílias, mas com um âmbito diferente do que existia antes de 2004.[33]
A família Gesneriaceae contém, dependendo do autor, entre 147 e 160 géneros, com de 3 200 a 3 870 espécies. Cerca de 40 géneros são monotípicos.[34] Antes de 2013, a família Gesneriaceae era dividida em doze tribos:
- Gesnereáceas didimocarpoides (segundo A. Weber 2004) — agora parte das subfamílias Didymocarpoideae ou Cyrtandroideae: o número cromossómico é muito variável. Teve de ser reclassificada após as investigações realizadas desde 1998. Aqui foram classificadas cerca de 82 géneros e cerca de 2 000 espécies. A antiga representação com quatro tribos (porém, três géneros não estavam classificados ao nível de tribo, estavam em incertae sedis) era a seguinte:
- Tribo Cyrtandreae Bartl.: Aqui estavam classificadas três géneros.
- Tribo Didymocarpeae Endl.
- Tribo Titanotricheae W.T.Wang: Aqui estava classificado apenas um género monotípico.
- Tribo Trichosporeae Nees: Aqui estavam classificadas cerca de cinco géneros.
- Gesnereáceas epitematoides (segundo A. Weber 2004) — até então subfamília Epithematoideae: gerlamente o número de cromossomas n = 10 (8-12). Aqui estava classificada apenas uma tribo. Distribuição: principalmente na Índia e no Sudeste Asiático; existe uma espécie na África Ocidental e uma espécie desde a América Central até ao Peru.:
- Tribo Klugieae Fritsch: Aqui estavam classificadas seis a sete espécies.
- Gesnereáceas gesnerioides (segundo Anton Weber 2004) — como por exemplo a extensão da subfamília Gesnerioideae: o número de cromossomas n = 6-16. Aqui eram classificadas seis tribos com cerca de 53 géneros e cerca de 1500 espécies do Novo Mundo (Neotropis). Muitos taxons são epífitas, na maioria das vezes polinizados e disseminados por aves:
- Tribo Beslerieae Bartl.: Aqui estavam classificadas cerca de oito géneros.[35]
- Tribo Napeantheae Wiehler: Aqui foi classificado apenas um género.
- Tribo Gesnerieae Dumort.: Aqui foram classificadas apenas dois géneros.
- Tribo Gloxinieae (G.Don) G.Don de acordo com E.H.Roalson et al. 2005[36]: Aqui estavam classificadas cerca de 20 géneros.
- Tribo Sinningieae Fritsch: As apenas três géneros; ocorrem principalmente no Brasil.
- Tribo Sphaerorrhizeae Roalson & Boggan: Aqui estava classificado apenas um género.
- Tribo Episcieae Endl.
- Gesnereáceas coronanteroides (segundo Anton Weber 2004) — anteriormente subfamília Coronatheroideae: são plantas lenhosas. O número de cromossomas é n = 37-45. Aqui foi classificada apenas uma tribo:
- Tribo Coronanthereae Fritsch: Aqui foram classificadas cerca de dez géneros, na sua maioria monotípicos, com cerca de 20 espécies e distribuição nas ilhas Salomão, Antilhas, Nova Caledónia e no sul da América do Sul.
Com base nas diferenças filogenéticas moleculares, morfológicas e biogeográficas, a família foi dividida em duas subfamílias principais: a subfamília Didymocarpoideae (anteriormente Cyrtandroideae), com todas as espécies, exceto uma, do Velho Mundo; e a subfamília Gesnerioideae, nativa das Américas, passando pelo Pacífico até a Austrália e sudeste da China. O género Sanango é colocado na sua própria subfamília, Sanangoideae. As duas subfamílias principais são divididas em tribos e subtribos.[25]
Os géneros aceites pela Plants of the World Online (PoWO) 2025 estão listados numa secção abaixo,[37] juntamente com a sua classificação numa das subfamílias e tribos por Weber. et al. (2020).[25] Desde Weber 2013, a família Gesneriaceae é novamente dividida em quatro subfamílias com múltiplas tribos e subtribos:[38][39][33]
- Subfamília Sanangoideae A.Weber, J.L.Clark & Mich.Möller
- Tribo Titanotricheae Yamaz. ex W.T.Wang:[39][33]
- Contém apenas um género monotípico:[33][33]
- Titanotrichum Soler.: Contém apenas uma espécie:
- Titanotrichum oldhamii (Hemsl.) Soler.: Originária de Fujian e Taiwan, passando pelas ilhas Ryūkyū até outras ilhas japonesas.
- Titanotrichum Soler.: Contém apenas uma espécie:
- Contém apenas um género monotípico:[33][33]
- Tribo Napeantheae Wiehler:[39][33]
- Contém apenas um género:[33]
- Napeanthus Gardner (sin.: Marssonia H.Karst.): As pelo menos 23 espécies estão amplamente distribuídas na região neotropical.
- Contém apenas um género:[33]
- Tribo Beslerieae Bartl.:[39] Dividida em duas subtribos:[33]
- Subtribo Anetanthinae A.Weber & J.L.Clark:[39] Contém cerca de cinco géneros:[33]
- Anetanthus Hiern ex Benth. & Hook. f.: As duas espécies Anetanthus gracilis Hiern e Anetanthus rubra L.E.Skog ocorrem no Peru, na Bolívia, na região central da Colômbia e no sudeste do Brasil.
- Cremospermopsis L.E.Skog & L.P.Kvist: As duas espécies Cremospermopsis cestroides (Fritsch) L.E.Skog & L.P.Kvist, e Cremospermopsis parviflora L.E.Skog & L.P.Kvist ocorrem nos departamentos colombianos de Antioquia e Bolívar, este último adjacente ao primeiro.
- Resia H.E.Moore: As duas espécies Resia ichthyoides Leeuwenb. e Resia nimbicola H.E.Moore ocorrem na Colômbia e na Venezuela.
- Shuaria D.A.Neill & J.L.Clark: Foi criado em 2010[33] e contém apenas uma espécie:
- Shuaria ecuadorica D.A.Neill & J.L.Clark: Esta pequena árvore, com apenas 3 a 5 metros de altura, cresce no sub-bosque da Cordilheira do Condor e na região amazónica do sudeste do Equador. Como os locais onde cresce são muito isolados, é considerada «espécie quase ameaçada» = «potencialmente em perigo».[40]
- Tylopsacas Leeuwenb.: Contém apenas uma espécie:
- Tylopsacas cuneata (Gleason) Leeuwenb.: Ocorre nas florestas de montanha do planalto da Guiana.
- Subtribo Besleriinae G.Don:[39] Contém cerca de quatro géneros com aproximadamente 240 espécies:[33]
- Besleria L.: As mais de 200 espécies estão amplamente distribuídas no Neotropis, com centros de biodiversidade nos Andes da Colômbia e do Equador. Muitas das espécies são endémicas, algumas delas em áreas pequenas.
- Cremosperma Benth.: As 20 a 25 espécies estão distribuídas desde o Panamá até aos Andes do Peru.
- Gasteranthus Benth.: As cerca de 35 espécies estão distribuídas desde a Guatemala e áreas adjacentes no México, Costa Rica e Panamá, passando pelo oeste da América do Sul até à Bolívia, com o centro de diversidade de espécies no oeste do Equador.
- Reldia Wiehler: As cerca de 60 espécies ocorrem principalmente em florestas de montanha ou, raramente, em florestas tropicais de planície, desde o Panamá até ao norte do Peru.
- Subtribo Anetanthinae A.Weber & J.L.Clark:[39] Contém cerca de cinco géneros:[33]
- Tribo Coronanthereae Fritsch[39] (sin.: Coronantheroid Gesneriaceae (segundo Anton Weber 2004), subfamília Coronatheroideae (segundo Wiehler 1983)): São plantas lenhosas. O número de cromossomas é n = 37-45. É dividida em três subtribos:[33]
- Subtribo Coronantherinae Fritsch:[39] Contém dois géneros:[33]
- Coronanthera C.B.Clarke: Das cerca de onze espécies, dez ocorrem na Nova Caledónia e uma nas ilhas Salomão.
- Rhabdothamnus Cunn.: Contém apenas uma espécie:
- Rhabdothamnus solandri Cunn.: Endemismo da ilha Norte da Nova Zelândia.
- Subtribo Mitrariinae Hanst.:[39] Contém quatro géneros monotípicos, ou seja, apenas quatro espécies, todas no hemisfério sul:[33]
- Asteranthera Hanst.: Contém apenas uma espécie:
- Asteranthera ovata Hanst.: Ocorre no sul do Chile e nas regiões vizinhas da Argentina.
- Fieldia Cunn.: Contém apenas uma espécie:
- Fieldia australis Cunn.: Ocorre nas florestas tropicais do sudeste da Austrália, em árvores ou rochas cobertas de musgo.
- Mitraria Cav.: Contém apenas uma espécie:
- Sarmienta Ruiz & Pav.: Contém apenas uma espécie:
- Sarmienta scandens (J.D.Brandis) Pers. (sin.: Sarmienta repens Ruiz & Pav. nom. illeg.): Ocorre nas florestas tropicais frias do sul do Chile e na ilha de Chiloé.
- Asteranthera Hanst.: Contém apenas uma espécie:
- Subtribo Negriinae V.L.Woo, J.F.Smith & Garn.-Jones:[39] Contém três géneros com cerca de quatro espécies[33] e, desde 2021, inclui mais um género monotípico.[41] Todas as cinco espécies ocorrem no hemisfério sul:
- Bopopia Munzinger & J.R.Morel: Foi criada em 2021 e contém apenas uma espécie:[41]
- Bopopia parviflora Munzinger & J.R.Morel: Endémica da Nova Caledónia.[41]
- Depanthus S.Moore: As duas espécies só ocorrem nas florestas montanhosas da Nova Caledónia.
- Lenbrassia G.W.Gillett: Contém apenas uma espécie:
- Lenbrassia australiana (C.T.White) G.W.Gillett: As duas variedades ocorrem no norte de Queensland, no nordeste da Austrália, na floresta tropical sobre granito, em altitudes entre 750 e 1100 metros.
- Negria F.Muell.: Contém apenas uma espécie:
- Negria rhabdothamnoides F.Muell.: Espécie endémica da ilha Lord Howe.
- Bopopia Munzinger & J.R.Morel: Foi criada em 2021 e contém apenas uma espécie:[41]
- Subtribo Coronantherinae Fritsch:[39] Contém dois géneros:[33]
- Tribo Gesnerieae Dumort.[39][33]
- Subtribo Columneinae Hanst.: Corresponde aproximadamente ao âmbito das tribos Episcieae anteriores.Endl.:[39][33]
- Alloplectus Mart.: s. str.: As apenas cerca de cinco espécies existentes estão distribuídas desde a Costa Rica até aos Andes da Colômbia, norte do Equador e Peru.
- Alsobia Hanst.: As duas espécies, Alsobia dianthiflora (H.E.Moore & R.G.Wilson) Wiehler e Alsobia punctata (Lindl.) Hanst., ocorrem no México, Guatemala e Costa Rica.
- Centrosolenia Benth.: Foi repristinado em 2016.[33] As cerca de 13 espécies ocorrem desde o norte da América do Sul até ao norte do Brasil.
- Christopheria J.F.Sm. & J.L.Clark: Foi criada em 2013 e contém apenas uma espécie:[33]
- Christopheria xantha (Leeuwenb.) J.F.Sm. & J.L.Clark: Ocorre no norte da América do Sul.
- Chrysothemis Decne. (sin.: Tussacia Benth., Tussacia Raf., Tussacia Klotzsch ex Beer, Tussacia Willd. ex Roem. & Schult.): As cerca de sete espécies estão distribuídas desde o Equador até a Guatemala, no centro do Brasil, nas Guianas, na Venezuela e nas Pequenas Antilhas.
- Cobananthus Wiehler: Contém apenas uma espécie:
- Cobananthus calochlamys (Donn. Sm.) Wiehler: Espécie endémica da região de Cobán, em Alta Verapaz, na Guatemala.
- Codonanthe (Mart.) Hanst. (sin.: Coccanthera K.Koch & Hanst., Comes Buc'hoz): Desde 2013, ela não contém mais 20 espécies, mas apenas cerca de nove no Brasil.[33]
- Codonanthopsis Mansf.: As cerca de 13 espécies existentes desde 2013 estão distribuídas pela região neotropical.[33]
- Columnea L. (sin.: Achimenes P.Browne non Pers., Aponoa Raf., Bucinella Wiehler, Collandra Lem., Eusynetra Raf., Glycanthes Raf., Kohlerianthus Fritsch, Pterygoloma Hanst., Stenanthus Oerst. ex Hanst., Stygnanthe Hanst., Vireya Raf.): s. l.: O âmbito do género é alvo de controvérsia: com cerca de 270 espécies s. l.; s. str.: 75 espécies, além de quatro géneros anteriores, incluindo Dalbergaria Tussac com cerca de 90 espécies, Tricantha Hook. com 75 espécies, Ortholoma (Benth.) Hanst. e Pentadenia Hanst.
- Corytoplectus Oerst.: As cerca de 15 espécies prosperam em altitudes mais elevadas da cordilheira ocidental, do Panamá à Bolívia, e na costa da Venezuela, bem como nas terras altas da Guiana.
- Cremersia Feuillet & L.E.Skog: Contém apenas uma espécie:
- Cremersia platula C.Feuillet & L.E.Skog: Esta espécie endémica ocorre apenas na Guiana Francesa.
- Crantzia Scop.: Foi reativada em 2005/2006 e contém duas a quatro espécies que, antes de 2005, estavam incluídas no género Alloplectus.[33] Ocorrem na região tropical do norte da América do Sul.
- Drymonia Mart.: As cerca de 140 espécies estão amplamente distribuídas.
- Episcia Mart.: As oito a nove espécies estão distribuídas do México ao Peru, no norte do Brasil e nas Guianas, por exemplo:
- Episcia lilacina Hanst.
- Glossoloma Hanst.: Reativado em 2005/2006.[33] As cerca de 28 espécies estão amplamente distribuídas na região neotropical, do México à Bolívia.
- Lampadaria Feuillet & L.E.Skog: Contém apenas uma espécie:
- Lampadaria rupestris Feuillet & L.E.Skog: Ocorre apenas na Guiana.
- Lembocarpus Leeuwenb.: Contém apenas uma espécie:
- Lembocarpus amoenus Leeuwenb.: Ocorre em florestas tropicais sobre granito no Suriname e na Guiana Francesa.
- Lesia J.L.Clark & J.F.Sm.: Criado em 2013, inclui apenas duas espécies da América do Sul tropical.[33]
- Nautilocalyx Hanst. (sin.: Physodeira Hanst., Skiophila Hanst., Nauticalyx Hort. ex Loud., Episcia subgen. Physodeira Hanst., Episcia sect. Nautilocalyx (Hanst.) Benth., Episcia sect. Skiophila (Hanst.) Benth., Episcia sect. Physodeira (Hanst.) Benth., Episcia sect. Episcia subsect. Centrosolenia (Benth.) Leeuwenb. p.p., Episcia sect. Episcia subsect. Physodeira (Hanst.) Leeuwenb., Episcia sect. Tarachanthus Leeuwenb., Episcia sect. Trichosperma Leeuwenb.): As mais de 70 espécies estão amplamente distribuídas na região neotropical, sendo que apenas no sudeste do Brasil não existe nenhuma espécie.
- Nematanthus Schrad. (sin.: Hypocyrta Mart. 1829, p.p.): As cerca de 30 espécies ocorrem no leste do Brasil.
- Neomortonia Wiehler: Desde 2013, contém apenas uma espécie:[33]
- Neomortonia rosea Wiehler: Ocorre desde a Costa Rica, passando pelo Panamá, até à Colômbia e ao Equador.
- Oerstedina Wiehler: As apenas três espécies estão distribuídas do México à América Central.
- Pachycaulos J.L.Clark & J.F.Sm.: Foi criado em 2013 e contém apenas uma espécie:[33]
- Pagothyra (Leeuwenb.) J.F.Sm. & J.L.Clark: Desde 2013, tem o estatuto de género e contém apenas uma espécie:[33]
- Pagothyra maculata (Hook. f.) J.F.Sm. & J.L.Clark: Ocorre no norte da América do Sul.
- Paradrymonia Hanst.:[33] Anteriormente, existiam entre 34 e 70 espécies, mas desde 2016 existem apenas cerca de 10 espécies, distribuídas desde a Costa Rica até ao Panamá e da Colômbia, Equador até à Bolívia, no norte do Brasil e nas Guianas.
- Rhoogeton Leeuwenb.: As duas a quatro espécies ocorrem na Venezuela e na Guiana.
- Rufodorsia Wiehler: As cerca de quatro espécies estão distribuídas desde a Nicarágua até ao Panamá.
- Trichodrymonia Oerst.: Foi repristinado em 2016.[33] As cerca de 29 espécies estão distribuídas na região neotropical.
- Subtribo Gesneriinae Oerst.[39]: Em 2020, contém quatro gêneros com mais de 100 espécies nas ilhas do Caribe, na Colômbia e na Venezuela:[33]
- Bellonia L.: Das duas espécies existentes, a Bellonia aspera L. ocorre em Cuba e a Bellonia spinosa Swartz em Hispaniola.
- Gesneria L.: As 46 a 60 espécies ocorrem nas ilhas das Caraíbas.
- Pheidonocarpa L.E.Skog: Contém apenas uma espécie:
- Pheidonocarpa corymbosa (Sw.) L.E.Skog: Ocorre apenas nas ilhas caribenhas de Cuba e Jamaica.
- Rhytidophyllum Mart.: As cerca de 20 espécies estão distribuídas pelas ilhas das Caraíbas, Colômbia e Venezuela.
- Subtribo Gloxiniinae G.Don (sin.: tribo Gloxinieae (G.Don) G.Don: Contém, de acordo com E.H.Roalson et al. 2005,[36] cerca de 20 géneros:[39][33]
- Achimenes Pers.: As cerca de 24 espécies estão distribuídas do México à Colômbia, incluindo as ilhas do Caribe.
- Amalophyllon Brandegee: Foi repristinado em 2008 e contém cerca de 13 espécies, que se distribuem desde o sul do México até à América Central e ao norte da América do Sul.
- Chautemsia A.O.Araujo & V.C.Souza: Foi criado em 2010 e contém apenas uma espécie:[33]
- Chautemsia calcicola A.O.Araujo & V.C.Souza: Ocorre no sudeste do Brasil.
- Diastema Benth.: As mais de 20 espécies estão distribuídas na região neotropical.
- Eucodonia Hanst.: As duas únicas espécies ocorrem no centro e sul do México.
- Gloxinella (H.E.Moore) Roalson & Boggan: Desde 2005, tem o estatuto de género[33] e contém apenas uma espécie:
- Gloxinella lindeniana (Regel) Roalson & Boggan: Durante muito tempo, esta espécie era conhecida apenas em cultura, com origem desconhecida, e foi redescoberta no Peru (Cajamarca).
- Gloxinia L'Hér. (sin.: Anodiscus Benth., Escheria Regel, Eucolum Salisb., Fiebrigia Fritsch, Fritschiantha Kuntze, Koellikeria Regel, Salisia Regel):[33] Desde 2005, existem apenas cerca de três espécies[33] e, desde 2020, cerca de cinco espécies na região neotropical, principalmente nos Andes.
- Gloxiniopsis Roalson & Boggan: Foi criada em 2005 e contém apenas uma espécie:[33]
- Gloxiniopsis racemosa (Benth.) Roalson & Boggan: Ocorre nos Andes da Colômbia.
- Goyazia Taub.: As duas únicas espécies ocorrem na região central do Brasil (Planalto).
- Heppiella Regel: As cerca de quatro espécies estão distribuídas desde o Peru até ao oeste da Venezuela.
- Kohleria Regel (sin.: Brachyloma Hanst., Calycostemma Hanst., Capanea Decne. ex Planch., Cryptoloma Hanst., Capanea Decne., Gesneria Mart. sect. Isoloma Benth., Giesleria Regel, Isoloma (Benth.) Decne. non J.Smith, Sciadocalyx Regel, Synepileana Baill., Tydaea Decne.):[33] O âmbito do género foi alvo de controvérsia e inclui cerca de 17 a 22 espécies. A sua origem é a cordilheira do Peru ao México, Venezuela, Trinidad e Guianas. O centro de diversidade situa-se na Colômbia.
- Mandirola Decne.: Foi reativada em 2005. As apenas três espécies estão distribuídas no Brasil.[33]
- Monopyle Moritz ex Benth.: As cerca de 17 espécies estão distribuídas desde a Bolívia até à Guatemala.
- Moussonia Regel: As cerca de onze espécies estão distribuídas desde o México até ao Panamá.
- Niphaea Lindl.: As cerca de cinco espécies ocorrem no México e na Guatemala.
- Nomopyle Roalson & Boggan: As duas únicas espécies ocorrem no Equador e no Peru.
- Pearcea Regel (incluindo Parakohleria Wiehler): As cerca de 17 espécies existentes atualmente estão distribuídas pelo norte da América do Sul.
- Phinaea Benth.: Anteriormente, continha entre 10 e 16 espécies, mas desde 2008 existem apenas três espécies.[33] Das três espécies restantes, uma ocorre desde o nordeste da Colômbia até ao norte do Brasil, no estado do Pará, outra ocorre desde o oeste até ao centro do México e uma é endémica do oeste de Cuba.
- Seemannia Regel: Foi reativado em 2005.[33] As cerca de quatro espécies estão distribuídas principalmente pelos Andes: Bolívia, norte da Argentina e sul do Peru. A Seemannia sylvatica chega até ao sul do Equador.
- Smithiantha Kuntze: As cerca de sete espécies estão distribuídas desde o centro e norte do México até à Guatemala.
- Solenophora Benth: As cerca de 16 espécies estão distribuídas pela América Central.
- Subtribo Ligeriinae Hanst.: Corresponde à antiga tribo Sinningieae Fritsch[39]: contém apenas três géneros,[33] que ocorrem principalmente no Brasil:
- Paliavana Vand.: As cerca de seis espécies estão distribuídas pelo leste e sudeste do Brasil.
- Sinningia Nees (sin.: Alagophyla Raf., Almana Raf., Biglandularia Seem., Corytholoma (Benth.) Decne., Dircaea Decne., Dolichodeira Hanst., Fimbrolina Raf., Gesnera Mart., Lietzia Regel, Ligeria Decne., Megapleilis Raf., Orthanthe Lem., Rechsteineria Regel, Rosanowia Regel, Stenogastra Hanst., Styrosinia Raf., Tapeinotes DC., Tapina Mart., Tulisma Raf., Anodiscus Benth. e Koellikeria Regel): As cerca de 65 espécies estão distribuídas na região neotropical, principalmente no sul e leste do Brasil. Incluindo a Sinningia speciosa (Lodd.) Hiern, designada por gloxinia por Gärtner.
- Vanhouttea Lem.: As cerca de oito espécies ocorrem no sudeste do Brasil.
- Subtribo Sphaerorrhizinae A.Weber & J.L.Clark (sin.: tribo Sphaerorrhizeae Roalson & Boggan):[39] Contém apenas um género:[33]
- Sphaerorrhiza Roalson & Boggan: Foi criado em 2005. [33] As duas espécies Sphaerorrhiza sarmentiana (Gardn. ex Hook.) Roalson & Boggan e Sphaerorrhiza burchellii (S.M.Phillips) Roalson & Boggan são comuns no Brasil.
- Subtribo Columneinae Hanst.: Corresponde aproximadamente ao âmbito das tribos Episcieae anteriores.Endl.:[39][33]
- Tribo Epithemateae C.B.Clarke (sin.: tribo Klugieae Fritsch):[39] Corresponde às anteriores «gerneriáceas epitematoides» segundo Anton Weber 2004, anteriormente a subfamília Epithematoideae: está dividida em quatro subtribos e contém sete géneros com cerca de 85 espécies. A área de distribuição estende-se principalmente da Índia ao Sudeste Asiático; uma espécie ocorrre na África Ocidental e outra espécie ocorre da América Central ao Peru. O número de cromossomas é geralmente n = 10 (8-12):[33]
- Subtribo Epithematinae DC. ex Meisn.[39] Contém apenas um género:[33]
- Epithema Blume: As cerca de vinte espécies existentes desde 2015, estão distribuídas pelo sul e sudeste da Ásia, bem como pela África Ocidental.
- Subtribo Loxoniinae A.DC.:[39] Contém três géneros:[33]
- Gyrogyne W.T.Wang: Contém apenas uma espécie:
- Gyrogyne subaequifolia W.T.Wang: Esta espécie endémica cresce em altitudes baixas na região ocidental de Guangxi, apenas em Bose e no condado de Xian.[10]
- Loxonia Jack: As cerca de três espécies estão distribuídas na Malésia ocidental: Sumatra, Península Malaia, Bornéu e Java.
- Stauranthera Benth.: As cerca de dez espécies estão distribuídas pelo Sudeste Asiático e pelas ilhas do Pacífico.
- Gyrogyne W.T.Wang: Contém apenas uma espécie:
- Subtribo Loxotidinae G.Don[39] Contém apenas um género:[33]
- Rhynchoglossum Blume (sin.: Antonia R.Br., Glossanthus Klein ex Benth., Klugia Schltdl., Loxotis R.Br. ex Benth.): Das cerca de 13 espécies, cerca de doze espécies estão distribuídas no sul e sudeste da Ásia, bem como nas ilhas do Pacífico, e uma espécie está distribuída na região neotropical.
- Subtribo Monophyllaeinae A.Weber & Mich.Möller:[39] Contém apenas dois géneros:[33]
- Monophyllaea R.Br.: As mais de 30 espécies estão distribuídas na Malésia, desde Sumatra até à Nova Guiné, e desde o sul da Tailândia e Luzon até Java.
- Whytockia W.W.Sm.: As cerca de seis espécies estão distribuídas pela China (cinco espécies) e Taiwan (uma espécie).
- Subtribo Epithematinae DC. ex Meisn.[39] Contém apenas um género:[33]
- Tribo Trichosporeae Nees: Corresponde em grande parte às anteriores «gesnereáceas didimocarpoides» segundo A. Weber 2004, anteriormente a subfamília Didymocarpoideae ou Cyrtandroideae.[39] Contém cerca de 71 géneros com cerca de 2400 espécies. Em 2020, os grupos de parentesco natural ainda não puderam ser suficientemente esclarecidos. Em 2020, foi feita uma divisão em dez subtribos, algumas das quais contêm apenas um género. São necessários mais estudos de genética molecular para um maior esclarecimento.[33]
- Subtribo Corallodiscinae A.Weber & Mich.Möller[39] Contém apenas um género:[33]
- Corallodiscus Batalin: As três a cinco espécies estão distribuídas pelo norte da Índia, Butão, Nepal, Sikkim, Tailândia e China (três espécies).
- Subtribo Didissandrinae A.Weber & Mich.Möller[39] Contém apenas dois géneros com cerca de dez espécies:[33]
- Didissandra C.B.Clarke: As cerca de oito espécies estão distribuídas na parte ocidental da Malésia.
- Tribounia D.J.Middleton: Foi criado em 2012[33] e contém apenas duas espécies presentes apenas na Tailândia.
- Subtribo Didymocarpinae G.Don[39] (sin.: Trichosporinae G.Don nom. reject., Cyrtandrinae G.Don, Liebigiinae A.DC., Aeschynanthinae A.DC. nom. cons., Lysionotinae A.DC., Oreocharidinae Fritsch): Em 2020, ela contém cerca de 35 gêneros com aproximadamente 1 900 espécies:[33]
- Aeschynanthus Jack (sin.: Euthamnus Schltr., Micraeschynanthus Ridl., Oxychlamys Schltr., Rheithrophyllum Hassk., Trichosporum D.Don.):[33] As cerca de 140 espécies estão distribuídas pela Ásia e pelas ilhas do Pacífico.
- Agalmyla Blume (sin.: Orithalia Blume nom. illeg., Orythia Endl., Dichrotrichum Reinw. ex De Vriese, Tetradema Schltr.): As cerca de 100 espécies estão distribuídas pela Malésia.
- Allocheilos W.T.Wang: As duas espécies ocorrem no sul da China: Allocheilos cortusiflorus W.T.Wang e Allocheilos guangxiensis H.Q. Wen, Y.G.Wei & S.H.Zhong em altitudes de cerca de 1400 metros no karst tropical do sudoeste de Guizhou (apenas em Xingyi Xian) e no leste de Yunnan (apenas em Luoping Xian) em altitudes de cerca de 100 metros em Guangxi.[10]
- Allostigma W.T.Wang: Contém apenas uma espécie:
- Allostigma guangxiense W.T.Wang: Endemismo do sul da China, na região autónoma de Guangxi.[10]
- Anna Pellegr.: As apenas três ou quatro espécies ocorrem na China e no norte do Vietname.
- Chayamaritia D.J.Middleton & Mich.Möller: Foi criado em 2015.[33] As duas únicas espécies ocorrem na Indochina.
- Billolivia D.J.Middleton: Foi criado em 2014[42][33] e inclui cerca de 15 espécies apenas no Vietname.
- Briggsiopsis K.Y.Pan: Foi criado em 1985 e contém apenas uma espécie:[43]
- Briggsiopsis delavayi (Franch.) K.Y.Pan: Ocorre em altitudes entre 200 e 1500 metros nas províncias do sul da China, Guizhou (apenas em Xishui Xian), sul de Sichuan e nordeste de Yunnan (apenas em Yanjin Xian).[10]
- Cathayanthe Chun: Contém apenas uma espécie:
- Cathayanthe biflora Chun: Esta espécie endémica cresce em altitudes de cerca de 2400 metros apenas na província chinesa de Hainan.[10]
- Chayamaritia D.J.Middleton & Mich.Möller: Foi criado em 2015[44][33] As duas únicas espécies, existentes no Sudeste Asiático, ocorrem apenas no Laos e na Tailândia.
- Conandron Sieb. & Zucc.: Contém apenas uma espécie:
- Codonoboea Ridl. (sin.: Platyadenia B.L.Burtt): As cerca de 129 espécies existentes desde 2011 estão distribuídas desde a Tailândia até ao oeste da Malésia.[45]
- Cyrtandra J.R.Forst. & G.Forst.: Com 550 a 650 espécies, é o género mais rico em espécies da família. A sua área de distribuição estende-se desde as Nicobar e o sul da Tailândia até à Malésia e as ilhas do Pacífico Sul, chegando ao Havaí.[33][46][47]
- Deinostigma W.T.Wang & Z.YuLi: Foi criada em 1992 e era monotípica, mas contém cerca de cinco espécies na China e no Vietname desde 2010 e cerca de oito espécies desde 2020.[33][48]
- Didymocarpus Wall. nom. cons. (sin.: Roettlera Vahl, Rottlera Vahl):[33] As cerca de 75 espécies estão distribuídas desde o norte e nordeste da Índia, Nepal e sul da China até ao sul da Península Malaia e no norte de Sumatra.
- Didymostigma W.T.Wang: Foi criado em 1984 e contém apenas duas ou três espécies comuns na China.
- Glabrella Mich.Möller & W.H.Chen: Foi criado em 2014.[33] As três espécies ocorrem no sul da China.
- Gyrocheilos W.T.Wang: As quatro espécies estão distribuídas pela China.
- Hemiboea C.B.Clarke (sin.: Metabriggsia W.T.Wang): As cerca de 23 espécies existentes anteriormente e as cerca de 40 espécies existentes desde 2011[33] estão distribuídas desde o Himalaia oriental até à China, Taiwan, sul do Japão e norte do Vietname.
- Henckelia Spreng. (sin.: Henckelia sect. Henckelia Weber & Burtt, Babactes DC. ex Meisn., Calosacme Wall., Ceratoscyphus Chun, Didymocarpus sect. Orthoboea Benth., Hemiboeopsis W.T.Wang, Chirita Buch.-Ham. ex D.Don, Chirita sect. Euchirita C.B.Clarke, Didymocarpus sect. Euchirita (C.B.Clarke) Chun, Gonatostemon Regel, Roettlera sect. Euchirita (C.B.Clarke) Fritsch): O género Henckelia tem um âmbito diferente desde Weber 2011,[45] que foi reduzido para cerca de 73 espécies em 2013. As espécies correspondentes ao âmbito de 2013 estão distribuídas desde o Sri Lanka, sul da Índia, Bangladesh, Assam, Nepal, Tibete, China, Taiwan, Mianmar, Tailândia, Vietname, Laos até à Malásia.[33]
- Hexatheca C.B.Clarke: As cerca de quatro espécies ocorrem em Bornéu (desde Kalimantan Ocidental e Sarawak até Sabah).
- Liebigia Endl. (sin.: Tromsdorffia Blume non Bernhardi nec Martius, Morstdorffia Steud., Chirita sect. Liebigia (Endl.) C.B.Clarke, Hypopteron Hassk. nom. inval., Bilabium Miq.): Foi reativado em 2011. As cerca de doze espécies ocorrem desde a Indonésia até Sumatra.[45][33]
- Loxostigma C.B.Clarke: As cerca de 13 espécies existentes desde 2014[33] estão distribuídas pela Índia, Butão, Nepal, Sikkim, Mianmar, China (sete espécies) e norte do Vietname.
- Lysionotus D.Don: As cerca de 25 espécies estão distribuídas pelo norte da Índia, Butão, Mianmar, Nepal, China, Laos, norte da Tailândia, norte do Vietname e sul do Japão.
- Metapetrocosmea W.T.Wang: Contém apenas uma espécie:
- Metapetrocosmea peltata (Merrill & W.Y.Chun) W.T.Wang: Ocorre em altitudes de 300 a 700 metros, apenas em Hainan.[10]
- Michaelmoelleria F.Wen, Z.B.Xin & T.V.Do: Foi criado em 2020 e contém apenas uma espécie:[49]
- Michaelmoelleria vietnamensis F.Wen, Z.B.Xin & T.V.Do: Foi descrita pela primeira vez em 2020. Até agora, só foi encontrada numa floresta de louros numa região montanhosa de granito, a uma altitude de 140 a 200 metros, no sul do Vietname.[49]
- Microchirita (C.B.Clarke) Y.Z.Wang (sin.: Chirita sect. Microchirita C.B.Clarke, Roettlera sect. Microchirita (C.B.Clarke) Fritsch, Didymocarpus sect. Microchirita (C.B.Clarke) Chun): Desde 2011, tem o estatuto de género.[45][33] As cerca de 39 espécies estão distribuídas pela Índia e pelo sul da China, passando pela Indochina até ao sudeste asiático.[45]
- Oreocharis Benth. (sin.: Ancylostemon Craib, Bournea Oliv., Briggsia Craib, Dasydesmus Craib, Dayaoshania W.T.Wang, Deinocheilos W.T.Wang, Isometrum Craib, Opithandra B.L.Burtt, Paraisometrum W.T.Wang, Perantha Craib, Schistolobos W.T.Wang, Thamnocharis W.T.Wang, Tremacron Craib):[33] As 19 a 28 espécies estão distribuídas no sul da China (27 espécies), Tailândia e Vietname.
- Petrocodon Hance (sin.: Calcareoboea C.Y.Wu, Dolicholoma D.Fang & W.T.Wang, Lagarosolen W.T.Wang, Paralagarosolen Y.G.Wei, Tengia W.Y.Chun): Até 2011, existiam apenas duas ou três espécies. Em 2011, algumas espécies de alguns géneros foram incluídas neste género: Calcareoboea C.Y.Wu, Dolicholoma D.Fang & W.T.Wang, Lagarosolen W.T.Wang, Paralagarosolen Y.G.Wei, Tengia W.Y.Chun e algumas espécies do género Didymocarpus.[50] Desde então, surgiram outras espécies. As cerca de 39 espécies existentes desde 2020 ocorrem principalmente na China e na Indochina e prosperam principalmente em locais de karst tropical.[51][52][53][54][55][56][33]
- Petrocosmea Oliv.: As cerca de 30 espécies estão distribuídas pela China (24 espécies), nordeste da Índia, Mianmar, Tailândia e sul do Vietname.
- Primulina Hance (sin.: Chirita sect. Gibbosaccus C.B.Clarke, Chiritopsis W.T.Wang, Deltocheilos W.T.Wang, Wentsaiboea D.Fang & D.H.Qin): O género anteriormente monotípico contém mais de 170 espécies desde 2015 e mais de 200 espécies desde 2019, algumas das quais anteriormente incluídas em Chirita, e muitas novas espécies foram descritas neste século. [45][57][33] A maioria das espécies ocorre na China, apenas cerca de 19 espécies ocorrem no Vietname. Muitas espécies ocorrem apenas em regiões de karst tropical.[58]
- Pseudochirita W.T.Wang: Desde 2021, inclui duas espécies[10], que 0c0rrem no karst tropical] em Guangxi e no norte do Vietname.
- Rachunia D.J.Middleton & C.Puglisi: Contém apenas uma espécie:[59][33]
- Rachunia cymbiformis D.J.Middleton: Foi descrita pela primeira vez em 2018 na Tailândia. Até agora, só é conhecida no local onde foi encontrada pela primeira vez, em Ban E Tong, no distrito de Thong Pha Phum, na província tailandesa de Kanchanaburi, perto da fronteira com Mianmar, a uma altitude de 900 metros. Ocorre na encosta, à sombra, numa floresta húmida e sempre-verde.[59]
- Raphiocarpus Chun: Das 15 espécies existentes desde 2022, nove ocorrem no norte e centro do Vietname e sete no sul e sudoeste da China; a espécie descrita pela primeira vez em 2022 ocorre em Hainan e no centro do Vietname. [60] Na Flora of China de 1998, este género ainda era monotípico.[10]
- Ridleyandra A.Weber & B.L.Burtt: Em 2017, inclui 31 espécies da Tailândia, passando pela Península Malaia, onde ocorrem cerca de 23 espécies, até Bornéu, com cerca de cinco espécies.[61]
- Sepikea Schltr. talvez seja um sinónimo de Cyrtandra. Contém apenas uma espécie:
- Sepikea cylindrocarpa Schltr.: Endemismo na região de Sepik, na Nova Guiné.
- Subtribo Jerdoniinae A.Weber & Mich.Möller[39] Contém apenas um género:[33]
- Jerdonia Wight: Contém apenas uma espécie:
- Jerdonia indica Wight: Esta espécie endémica cresce nas rochas das montanhas Nilghiri e Anamally, no sudoeste da Índia.
- Jerdonia Wight: Contém apenas uma espécie:
- Subtribo Leptoboeinae C.B.Clarke (sin.: Championiinae Fritsch)[39] Desde 2022, contém cerca de sete géneros.[33][62]
- Actinostephanus F.Wen, Y.G.Wei & L.F.Fu: Foi criado em 2022 e contém apenas uma espécie:[62]
- Actinostephanus enpingensis F.Wen, Y.G.Wei & Z.B.Xin: Foi descrita pela primeira vez em 2022. Até agora, só foi encontrada no distrito de Enping, na província chinesa de Guangdong. Cresce na camada herbácea de uma floresta de louros perene, a altitudes entre 170 e 250 metros.[62]
- Beccarinda Kuntze (sin.: Petrodoxa J.Anthony): As cerca de oito espécies estão distribuídas pelo nordeste da Índia (Assam), Birmânia, sul da China e Hainan (cinco espécies), Vietname (Tonkin) e Sumatra.
- Boeica C.B.Clarke (sin.: Boeicopsis H.W.Li): As cerca de doze espécies estão distribuídas no sul da China (sete espécies), no Butão, no norte e nordeste da Índia, em Mianmar, no norte do Vietname e no noroeste da Península Malaia.
- Championia Gardn.: Contém apenas uma espécie:
- Championia reticulata Gardn.: Esta espécie endémica ocorre apenas no Sri Lanka.
- Leptoboea Benth.: As cerca de três espécies estão distribuídas pelo norte da Índia, Butão, Sikkim, Mianmar, Tailândia e China.
- Platystemma Wall.: Contém apenas uma espécie:
- Platystemma violoides Wall.: Sie kommt im nördlichen Indien, Bhutan, Nepal und südlichen Tibet (nur im Nyalam Xian) vor.
- Rhynchotechum Blume (sin.: Cheilosandra Griff. ex Lindl., Chiliandra Griff., Corysanthera Wall. ex Endl., Isanthera Nees): As cerca de 13 espécies estão distribuídas pelo Sudeste Asiático e pelas ilhas do Pacífico.
- Actinostephanus F.Wen, Y.G.Wei & L.F.Fu: Foi criado em 2022 e contém apenas uma espécie:[62]
- Subtribo Litostigminae A.Weber & Mich.Möller[39] Contém apenas um género:[33]
- Litostigma Y.G.Wei, F.Wen & Mich.Möller: Foi criada em 2010 e inclui apenas duas espécies, desde o centro-sul da China até ao Vietname.[33]
- Subtribo Loxocarpinae A.DC.[39] Em 2020, contém cerca de 14 géneros:[33]
- Boea Lam.: As cerca de 14 espécies estão distribuídas pelo sul da China, nordeste da Índia, norte da Tailândia, Vietname, Filipinas, Sulawesi, Sumbawa, Flores, Nova Guiné, nas Ilhas Salomão, no arquipélago de Bismarck e Louisiade e na Austrália.
- Damrongia Kerr ex Craib: Foi reativada em 2010 e contém cerca de onze espécies, que ocorrem desde o sudeste da China até Mianmar, Tailândia, Malásia e Sumatra.[45][33]
- Dorcoceras Bunge: Foi reativada em 2016/7.[33] As cerca de seis espécies ocorrem desde Assam, passando pela Indochina, até à China e à Malésia central.
- Emarhendia Kiew, A.Weber & B.L.Burtt: Foi criado em 1998 e contém apenas uma espécie:
- Emarhendia bettiana (M.R.Hend.) Kiew, A.Weber & B.L.Burtt: Ocorre apenas na Península Malaia.
- Kaisupeea B.L.Burtt: Foi criado em 2001. As cerca de três espécies ocorrem em Mianmar e na Tailândia.
- Loxocarpus R.Br.: Foi reativado em 2013[33] e inclui cerca de 26 espécies na Malésia ocidental.
- Middletonia C.Puglisi: Foi criada em 2013.[33] Existem cerca de cinco espécies, desde o Himalaia oriental até à China e Indochina, passando pela Península Malaia.
- Orchadocarpa Ridl.: Contém apenas uma espécie:
- Orchadocarpa lilacina Ridl.: Ocorre em florestas montanhosas em solos ácidos na Península Malaia.
- Ornithoboea C.S.P.Parish ex C.B.Clarke (sin.: Brachiostemon Hand.-Mazz., Lepadanthus Ridl., Sinoboea Chun): As cerca de 17 espécies estão distribuídas desde a China (cerca de cinco espécies) até à Indochina (Malásia, leste de Mianmar, Tailândia e Vietname).
- Paraboea (C.B.Clarke) Ridl. s. l. (sin.: Buxiphyllum W.T.Wang & C.Z.Gao, Chlamydoboea Stapf, Dichiloboea Stapf, Phylloboea Benth., Trisepalum C.B.Clarke):[33] As cerca de 87 a 90 espécies existentes anteriormente e as cerca de 146 espécies existentes desde 2016 estão distribuídas pelo Butão, Mianmar, China, Vietname, Tailândia, Malásia, Indonésia e Filipinas.
- Rhabdothamnopsis Hemsl.: Contém apenas uma espécie:
- Somrania D.J.Middleton: Foi criado em 2012/3[33] e inclui apenas três espécies existentes apenas na Tailândia.
- Senyumia Kiew, A.Weber & B.L.Burtt: Foi criado em 1998. As duas espécies ocorrem apenas na Península Malaia.
- Spelaeanthus Kiew, A.Weber & B.L.Burtt: Foi criado em 1998 e contém apenas uma espécie:
- Spelaeanthus chinii Kiew, A.Weber & B.L.Burtt: Ocorre apenas na Península Malaia.
- Subtribo Ramondinae DC. ex Meisn.[39] Contém os dois ou três géneros existentes na Europa, com um total de cinco a seis géneros:[33]
- Haberlea Friv.: Dependendo do autor (Petrova et al. 2014), uma ou duas espécies são nativas da Europa. Este género é uma relíquia de tempos em que o clima tropical predominava na Europa.
- Jancaea Boiss.: Contém apenas uma espécie:
- Jancaea heldreichii (Boiss.) Boiss.: Esta espécie endémica ocorre apenas no Monte Olimpo, na Tessália, Grécia. Cresce em fendas rochosas sombreadas e húmidas em calcário, a altitudes entre 100 e, na maioria das vezes, 1000 a 2100 metros.
- Ramonda Rich.: As apenas três espécies ocorrem na Espanha e na Península Balcânica.
- Subtribo Streptocarpinae Ivanina[39] Contém apenas um género:[33]
- Streptocarpus Lindl. s l. (nach Nishii et al. 2015) (sin.: Acanthonema Hook. f., Carolofritschia Engl., Colpogyne B.L.Burtt, Hovanella A.Weber & B.L.Burtt, Linnaeopsis Engl., Nodonema B.L.Burtt, Saintpaulia H.Wendl., Schizoboea (Fritsch) B.L.Burtt, Trachystigma C.B.Clarke):[33] Desde Nishii et al. 2015, cerca de 180 espécies em dois subgéneros estão distribuídas principalmente na África tropical e sudeste, Madagáscar e Comores. É controverso se essa ampla concepção desse género é o conceito correto ou se ele deve ser dividido em géneros menores.[33]
- Subtribo Tetraphyllinae A.Weber & Mich.Möller[39] Contém apenas um género:[33]
- Tetraphyllum Griff. ex C.B.Clarke: Das três espécies, uma ocorre apenas no Vietname e outra provavelmente apenas no nordeste da Índia, havendo outras referências de ocorrência em Bangladesh, Mianmar e Tailândia.[33]
- Subtribo Corallodiscinae A.Weber & Mich.Möller[39] Contém apenas um género:[33]
- Tribo Titanotricheae W.T.Wang:
- Contém apenas um género monotípico:[33]
- Titanotrichum Soler.: Contém apenas uma espécie:
- Titanotrichum oldhamii (Hemsl.) Soler.: Originária de Fujian e Taiwan, passando pelas Ilhas Ryūkyū até outras ilhas japonesas.
- Titanotrichum Soler.: Contém apenas uma espécie:
- Contém apenas um género monotípico:[33]
- Híbridos de género
- Em géneros intimamente relacionados, é fácil produzir híbridos de género através de cruzamentos:[9]
- Seleção:
- ×Achimenantha = Achimenes × Smithiantha
- ×Achicodonia = Achimenes × Eucodonia
- ×Smithicodonia = Smithiantha × Eucodonia
- ×Gloxmannia = Gloxinia × Seemannia
- Seleção:
- Géneros transferidos
- Os seguintes géneros foram transferidos e já não pertencem à família Gesneriaceae:
- Classificadas em outras famílias das Lamiales:
- Brookea Benth. (pertence à família Plantaginaceae s. lat.)[33]
- Charadrophila Marloth (pertence à família Stilbaceae)[33]
- Cyrtandromea Zoll. (pertence à família Phrymaceae)[33] As cerca de doze espécies estão distribuídas na região neotropical.
- Cubitanthus Barringer: (pertence à família Linderniaceae)[33] Contém apenas uma espécie:
- Cubitanthus alatus (Cham. & Schltdl.) Barringer: Nativa do estado brasileiro da Bahia.
- Rehmannia Fisch. & C.Mey.: As cerca de nove espécies ocorrem apenas na China. (pertence à família Orobanchaceae)[63][64][33]
- Classificadas em outras famílias das Lamiales:
Lsta de géneros
- Acanthonema
- Achimenes
- Aeschynanthus
- Agalmyla
- Allocheilos
- Alloplectus
- Allostigma
- Alsobia
- Ancylostemon
- Anetanthus
- Anna
- Anodiscus
- Asteranthera
- Beccarinda
- Bellonia
- Besleria
- Boea
- Boeica
- Bournea
- Briggsia
- Briggsiopsis
- Bucinellina
- Calcareoboea
- Capanea
- Cathayanthe
- Championia
- Chirita
- Chiritopsis
- Chrysothemis
- Cobananthus
- Codonanthe
- Codonanthopsis
- Colpogyne
- Columnea
- Conandron
- Corallodiscus
- Coronanthera
- Corytoplectus
- Cremosperma
- Cubitanthus
- Crantzia
- Cyrtandra
- Dalbergaria
- Dayaoshania
- Deinocheilos
- Depanthus
- Diastema
- Dichrotrichum
- Didissandra
- Didymocarpus
- Didymostigma
- Diplolegnon
- Dolicholoma
- Drymonia
- Episcia
- Epithema
- Eucodonia
- Fieldia
- Gasteranthus
- Gesneria
- Glossoloma
- Gloxinella
- Gloxinia
- Gloxiniopsis
- Goyazia
- Gyrocheilos
- Gyrogyne
- Haberlea
- Hemiboea
- Hemiboeopsis
- Henckelia
- Heppiella
- Hexatheca
- Hygea
- Isometrum
- Jancaea
- Jerdonia
- Koellikeria
- Kohleria
- Kohlerianthus
- Lagarosolen
- Lembocarpus
- Lenbrassia
- Leptobaea
- Lietzia
- Linnaeopsis
- Loxocarpus
- Loxonia
- Loxostigma
- Lysionotus
- Mandirola
- Metabriggsia
- Metapetrocosmea
- Micraeschynanthus
- Mitraria
- Monophyllaea
- Monopyle
- Moussonia
- Napeanthus
- Nautilocalyx
- Negria
- Nematanthus
- Neomortonia
- Niphaea
- Nodonema
- Nomopyle
- Oerstedina
- Opithandra
- Orchadocarpa
- Oreocharis
- Ornithoboea
- Oxychlamys
- Paliavana
- Paraboea
- Paradrymonia
- Parakohleria
- Pearcea
- Petrocodon
- Pentadenia
- Petrocosmea
- Pheidonocarpa
- Phinaea
- Phyllobaea
- Phylloboea
- Platyadenia
- Platystemma
- Primulina
- Protocyrtandra
- Pseudochirita
- Ramonda
- Raphiocarpus
- Reldia
- Resia
- Rhabdothamnopsis
- Rhabdothamnus
- Rhoogeton
- Rhynchoglossum
- Rhynchotoechum
- Rhytidophyllum
- Rufodorsia
- Sarmienta
- Saintpaulia
- Schistolobos
- Schizoboea
- Seemannia
- Sepikea
- Sinningia
- Smithiantha
- Solenophora
- Sphaerorrhiza
- Stauranthera
- Streptocarpus
- Tengia
- Tetraphyllum
- Thamnocharis
- Titanotrichum
- Trachystigma
- Tremacron
- Trichantha
- Trisepalum
- Tylopsacas
- Vanhouttea
- Whytockia
Referências
- ↑ a b «Gesneriaceae Rich. & Juss.». The International Plant Names Index. Consultado em 13 de abril de 2021
- ↑ a b Wiersema, J.H.; Turland, N.J.; Barrie, F.R.; Greuter, W.; Hawksworth, D.L.; Herendeen, P.S.; Knapp, S.; Kusber, W.-H.; Li, D.-Z.; Marhold, K.; May, T.W.; McNeill, J.; Monro, A.M.; Prado, J.; Price, M.J.; Smith, G.F., eds. (2018). «Gesneriaceae». International Code of Nomenclature for algae, fungi, and plants (Shenzhen Code) adopted by the Nineteenth International Botanical Congress Shenzhen, China, July 2017: Appendices I–VII. Consultado em 12 de abril de 2021
- ↑ Christenhusz, M. J. M.; Byng, J. W. (2016). «The number of known plants species in the world and its annual increase». Phytotaxa. 261 (3): 201–217. doi:10.11646/phytotaxa.261.3.1

- ↑ «Gesneriaceae - plant family». Encyclopedia Britannica
- ↑ a b «Gesneriads». Encyclopedia of Life
- ↑ Hyam, R.; Pankhurst, R. J. (1995). Plants and their names: a concise dictionary. ISBN 978-0-19-866189-4. Oxford: Oxford University Press p. 209.
- ↑ «Lamiales». Encyclopædia Britannica, inc. Abril 28, 2017. Consultado em 14 de setembro de 2018
- ↑ «Gesneriaceae». Encyclopædia Britannica, inc. 23 de novembro de 2017. Consultado em 14 de setembro de 2018
- ↑ a b c A. Chautems, 2009: Neotropical Gesneriaceae bei Neotropikey – Interactive key and information resources for flowering plants of the Neotropics.
- ↑ a b c d e f g h i j k l m Wencai Wang, Kai-yu Pan, Zhen-yu Li, Anna L. Weitzman, Laurence E. Skog: Gesneriaceae. – texto idêntico ao da obra impressa. In: Wu Zheng-yi, Peter H. Raven (Hrsg.): Flora of China. Volume 18: Scrophulariaceae through Gesneriaceae. Science Press / Missouri Botanical Garden Press, Beijing / St. Louis 1998, ISBN 0-915279-55-X, p. 244 (inglês).
- ↑ a b Die Familie Gesneriaceae bei DELTA von L. Watson & M. J. Dallwitz.
- ↑ a b Morley, B. (1978). «Gesneriaceae». In: Heywood, V.H.; Moore, D.M.; Richardson, I.B.K.; Stearn, W.T. Flowering Plants of the World. ISBN 978-0-19-217674-5. Oxford University Press. pp. 246–248
- ↑ «The wonderful world of gesneriads». Consultado em 14 de setembro de 2018
- ↑ a b c d e f g h i j k l m n o p Anton Weber: Gesneriaceae: A Scientific Perspective
- ↑ «Gesneriaceae». Jardim Botânico do Rio de Janeiro. Consultado em 14 de setembro de 2018
- ↑ «Sistemática de plantas vasculares». Consultado em 14 de setembro de 2018
- ↑ «Centro de Estudos Ambientais e Paisagísticos». Consultado em 14 de setembro de 2018
- ↑ Conandron ramondioides bei Plants For A Future
- ↑ Busca por Gesneriaceae na Lista Vermelha das espécies ameaçadas da IUCN.
- ↑ Dumortier, B.-C. (1829). Analyse des Familles de Plantes: avec l'indication des principaux genres qui s'y rattachent (em francês). Tournay: J. Casterman. p. 30. OCLC 1116096010. Consultado em 13 de abril de 2021
- ↑ «Columellia Ruiz & Pav.». Plants of the World Online. Royal Botanic Gardens, Kew. Consultado em 13 de abril de 2021
- ↑ Angiosperm Phylogeny Group (2016). «An update of the Angiosperm Phylogeny Group classification for the orders and families of flowering plants: APG IV». Botanical Journal of the Linnean Society. 181 (1): 1–20. doi:10.1111/boj.12385

- ↑ «The Gesneriad Society». Consultado em 11 de abril de 2021
- ↑ Weber, A.; Clark, J. L.; Möller, M. (2013). «A new formal classification of Gesneriaceae». Selbyana. 31 (2): 68–94. JSTOR 24894283
- ↑ a b c d e Weber, A.; Middleton, D. J.; Clark, J. L.; Möller, M. (2020). «Keys to the infrafamilial taxa and genera of Gesneriaceae». Rheedea. 30 (1): 5–47. doi:10.22244/rheedea.2020.30.01.02

- ↑ a b Ogutcen, Ezgi; Christe, Camille; Nishii, Kanae; Salamin, Nicolas; Möller, Michael; Perret, Mathieu (2021). «Phylogenomics of Gesneriaceae using targeted capture of nuclear genes». Molecular Phylogenetics and Evolution. 157. Bibcode:2021MolPE.15707068O. PMID 33422648. doi:10.1016/j.ympev.2021.107068

- ↑ «Peltanthera Benth.». Plants of the World Online. Royal Botanic Gardens, Kew. Consultado em 9 agosto 2024
- ↑ «Rehmannia Libosch. ex Fisch. & C.A.Mey.». Plants of the World Online. Royal Botanic Gardens, Kew. Consultado em 11 de abril de 2021
- ↑ a b c Christenhusz, Maarten (2017). Plants of the World: An Illustrated Encyclopedia of Vascular Plants. Chicago: University of Chicago Press
- ↑ Weber; Clark; Möller, Anton; John; Michael (2013). «A new formal classification of Gesneriaceae». Michael. A new formal classification of Gesneriaceae. Selbyana
- ↑ Perret, Mathieu (2012). «Temporal and spatial origin of Gesneriaceae in the New World inferred from plastid DNA sequences». Temporal and spatial origin of Gesneriaceae in the New World inferred from plastid DNA sequences
- ↑ Anton Weber: Gesneriaceae. In: Joachim W. Kadereit (ed.): The Families and Genera of Vascular Plants. Volume 7: Flowering plants, Dicotyledons. Lamiales (except Acanthaceae including Avicenniaceae). Springer, Berlin / Heidelberg / New York 2004, ISBN 3-540-40593-3, pp. 63–158.
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al am an ao ap aq ar as at au av aw ax ay az ba bb bc bd be bf bg bh bi bj bk bl bm bn bo bp bq br bs bt bu bv bw bx by bz ca cb cc cd ce cf cg ch ci cj ck cl cm cn co cp cq cr cs Anton Weber, David John Middleton, John Littner Clark: Keys to the infrafamilial taxa and genera of Gesneriaceae. In: Rheedia: Journal of the Indian Association for Angiosperm Taxonomy, Volume 30, Issue 1, 2020, S. 05–47. doi:10.22244/rheedea.2020.30.01.02 Volltext-PDF.
- ↑ Anton Weber, Laurence E. Skog, 2007: Umfassende Webseite zur Familie der Gesneriaceae, da die Navigation der Hauptseite mindestens unter Firefox nicht funktioniert: Gattungs-Navigation.
- ↑ E. H. Roalson, John L. Clark: Phylogenetic patterns of diversification in the Beslerieae (Gesneriaceae), S. 251–268. In: A. K. Sharma, A. Sharma (Hrsg.): Plant Genome: Biodiversity and Evolution, Phanerograms 1C, Science Publishers, Enfield, New Hampshire, 2006.
- ↑ a b J. K. Boggan, L. E. Skog, E. A. Zimmer: Untangling Gloxinieae (Gesneriaceae). I. Phylogenetic patterns and generic boundaries inferred from nuclear, chloroplast, and morphological cladistic data sets. In: Taxon, Band 54, Nr. 2, 2005, S. 389–410.
- ↑ «Gesneriaceae Dumort.». Plants of the World Online. Royal Botanic Gardens, Kew. Consultado em 11 de abril de 2021
- ↑ The classification of Gesneriaceae bei Gesneriaceae Resource Centre = GRC.
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj Anton Weber, John Littner Clark, Michael Möller: A new formal classification of Gesneriaceae. In: Selbyana, Volume 31, Issue 2: Special Issue: Proceedings of the World Gesneriad Research Conference 2010, Marie Selby Botanical Gardens Inc., 2013, S. 68–94. PDF.
- ↑ John L. Clark, David A. Neill, Anton Weber, Jennifer A. Gruhn, Tuntiak Katan: Shuaria (Gesneriaceae), an Arborescent New Genus from the Cordillera del Cóndor and Amazonian Ecuador. In: Systematic Botany, Volume 35, Issue 3, 2010, S. 662–674: doi:10.1600/036364410792495917 bei BioOne.
- ↑ a b c Jérémie Morel, Jérôme Duminil and Jérôme Munzinger: Bopopia, A New Monotypic Genus of Gesneriaceae (Gesnerioideae, Coronanthereae) from New Caledonia. In: European Journal of Taxonomy, Volume 736, Issue 1, 2021, S. 82–101. doi:10.5852/ejt.2021.736.1253
- ↑ David John Middleton, H. Atkins, L. H. Truong, K. Nishii, Michael Möller: Billolivia, a new genus of Gesneriaceae from Vietnam with five new species. In: Phytotaxa, Volume 161, 2014, S. 241–269. doi:10.11646/phytotaxa.161.4.1
- ↑ K. Y. Pan: Acta Phytotaxonomica Sinica, Volume 23, Issue 3, 1985, p. 216.
- ↑ D. J. Middleton, K. Nishii, C. Puglisi, L. L. Forrest, M. Möller: Chayamaritia (Gesneriaceae: Didymocarpoideae), a new genus from southeast Asia. In: Plant Systematics and Evolution, Volume 301, Issue 7, 2015, S. 1947–1966. doi:10.1007/s00606-015-1213-2 PDF.
- ↑ a b c d e f g Anton Weber, David John Middleton, Alan Forrest, Ruth Kiew, Chung Lu Lim, Rafidah Abdul Rahman, Susanne Sontag, Pramote Triboun, Yi-Gang Wei, Tze Leong Yao, Michael Moeller: Molecular systematics and remodelling of Chirita and associated genera (Gesneriaceae). In: Taxon, Volume 60, Issue 3, 2011, S. 767–790, doi:10.1002/tax.603012.
- ↑ Warren Lambert Wagner, Antony J. Wagner, David H. Lorence: Revision of Cyrtandra (Gesneriaceae) in the Marquesas Islands. In: PhytoKeys, Volume 30, 2013, pp. 33–64. doi:10.3897/phytokeys.30.6147
- ↑ Melissa A. Johnson, John R. Clark, Warren L. Wagner, Lucinda A. McDade: A molecular phylogeny of the Pacific clade of Cyrtandra (Gesneriaceae) reveals a Fijian origin, recent diversification, and the importance of founder events. In: Molecular Phylogenetics and Evolution, Volume 116, 2017, p. 30. doi:10.1016/j.ympev.2017.07.004
- ↑ M. Möller, K. Nishii, H.J. Atkins, H. H. Kong, M. Kang, Y. G. Wei, F. Wen, X. Hong, D. J. Middleton: An expansion of the genus Deinostigma (Gesneriaceae). In: Gardens’ Bulletin Singapore, Volume 68, Issue 1, 2016, pp. 145–172. doi:10.3850/S2382581216000119
- ↑ a b Fang Wen, Zi-Bing Xin, Long-Fei Fu, Shu Li, Lan-Ying Su, Stephen Maciejewski, Zhang-Jie Huang, Truong Van Do, Yi-Gang Wei: Michaelmoelleria (Gesneriaceae), a new lithophilous dwelling genus and species with zigzag corolla tube from southern Vietnam. In: PhytoKeys, Volume 146, Mai 2020, S. 89–107. doi:10.3897/phytokeys.146.49731
- ↑ Anton Weber, Yi-Gang Wei, Carmen Puglisi, Fang Wen, Veronika Mayer, Michael Möller: A new definition of the genus Petrocodon (Gesneriaceae). In: Phytotaxa, Volume 23, Issue 1, 2011, S. 49–67. doi:10.11646/phytotaxa.23.1.3
- ↑ Xin Hong, S. B. Zhou, Fang Wen: Petrocodon villosus (Gesneriaceae), a new species from Guangxi, China. In: Blumea, Volume 59, Issue 1, 2014, S. 33–36. doi:10.3767/000651914X682378
- ↑ W. H. Chen, M. Möller, Y. M. Shui, H. Wang, J. B. Yang, G. Y. Li: Three new species of Petrocodon (Gesneriaceae), endemic to the limestone areas of Southwest China, and preliminary insights into the diversification patterns of the genus. In: Systematic Botany, Volume 39, Issue 1, 2014, S. 316–330. doi:10.1600/036364414X678189
- ↑ J. Guo, T. Meng, H. Pang, Q. Zhang: Petrocodon retroflexus sp. nov. (Gesneriaceae) from a karst cave in Guizhou, China. In: Nordic Journal of Botany, Volume 34, Issue 2, 2016, S. 159–164. doi:10.1111/njb.00941
- ↑ H. F. Cen, L. F. Fu, Fang Wen: Petrocodon urceolatus sp. nov. (Gesneriaceae) from Zhangjiajie city, northwestern Hunan Province, China. In: Nordic Journal of Botany, Volume 35, Issue 3, 2017, S. 334–338. doi:10.1111/njb.01333
- ↑ L. Chen, W. H. Chen, S. W. Guo, Fang Wen, Y. M. Shui: Petrocodon tenuitubus (Gesneriaceae), a new species from Southeast Yunnan, China. In: Guihaia, Volume 39, Issue 5, 2019, S. 574–580.
- ↑ Rui-Li Zhang, Shu Li, Stephen Maciejewski, Yi-Gang Wei: Petrocodon rubiginosus, a new species of Gesneriaceae from Guangxi, China. In: PhytoKeys, Volume 157, August 2020, S. 175–181. doi:10.3897/phytokeys.157.32270
- ↑ B. Ai, Y. Gao, X. Zhang, J. Tao, M. Kang, H. Huang: Comparative transcriptomeresources of eleven Primulina species, a group of ‘stone plants’ from a biodiversityhot spot. In: Molecular Ecology Resources, Volume 15, 2015, S. 619–632, doi:10.1111/1755-0998.12333
- ↑ Xin Hong, Jeremy Keene, Zhi-Jing Qiu, Fang Wen: Primulina anisocymosa (Gesneriaceae), a new species with a unique inflorescence structure from Guangdong, China. In: PeerJ. Januar 2019, 7, e6157. doi:10.7717/peerj.6157
- ↑ a b David John Middleton, Gillian S. Khew, Manop Poopath, Michael Möller, Carmen Puglisi: Rachunia cymbiformis, a new genus and species of Gesneriaceae from Thailand. In: Nordic Journal of Botany, Volume 36, Issue 11, November 2018, e01992. doi:10.1111/njb.01992 PDF.
- ↑ Zi-Bing Xin, Lang-Xing Yuan, Zhong-Yang Zhang, Quang Diep Dinh, Gang Lu, Stephen Maciejewski, Truong Van Do: Raphiocarpus sinovietnamicus (Gesneriaceae), a new species from southern China and central Vietnam. In: Nordic Journal of Botany, September 2022, e03716, S. 1–5. doi:10.1111/njb.03716
- ↑ Mat Yunoh Siti Munirah, Zaharil Dzulkafly: Ridleyandra merohmerea (Gesneriaceae), a new species from Kelantan, Peninsular Malaysia. In: PhytoKeys, Volume 89, 2017, S. 1–10. doi:10.3897/phytokeys.89.20344
- ↑ a b c Fang Wen, Zi-Bing Xin, Xin Hong, Lei Cai, Xiao-Yun Chen, Jun-Jie Liang, Hui-Feng Wang, Stephen Maciejewski, Yi-Gang Wei, Long-Fei Fu: Actinostephanus (Gesneriaceae), a new genus and species from Guangdong, South China. In: PhytoKeys, Volume 193, März 2022, S. 89–106. doi:10.3897/phytokeys.193.80715
- ↑ Z. Xi, Y. Z. Wang, James F. Smith: Familial placement and relations of Rehmannia and Triaenophora (Scrophulariaceae s.l.) inferred from five gene regions. In: American Journal of Botany, Volume 96, 2009, S. 519–530. doi:10.3732/ajb.0800195
- ↑ Zhi Xia, Yin-Zheng Wang, James F. Smith: Familial placement and relations of Rehmannia and Triaenophora (Scrophulariaceae s.l.) inferred from five gene regions. In: American Journal of Botany, Volume 96, 2009, S. 519–530: doi:10.3732/ajb.0800195
Bibliografia
- Die Familie Gesneriaceae bei der APWebsite. (Abschnitte Systematik und Beschreibung)
- Die Familie Gesneriaceae bei DELTA von L. Watson & M. J. Dallwitz. (Abschnitt Beschreibung)
- Anton Weber, Laurence E. Skog: The Genera of Gesneriaceae: Umfassende Webseite zur Familie der Gesneriaceae, 2. Auflage, ab 2007 laufend weiterbearbeitet, Institute of Botany, University of Vienna, Austria & Department of Systematic Biology, Botany, Smithsonian Institution, Washington D.C., USA. (Abschnitt Systematik)
- Anton Weber: Gesneriaceae. In: Joachim W. Kadereit (ed.): The Families and Genera of Vascular Plants. Volume 7: Flowering plants, Dicotyledons. Lamiales (except Acanthaceae including Avicenniaceae). Springer, Berlin / Heidelberg / New York 2004, ISBN 3-540-40593-3, pp. 63–158.
- Wencai Wang, Kai-yu Pan, Zhen-yu Li, Anna L. Weitzman, Laurence E. Skog: In: Wu Zheng-yi, Peter H. Raven (Hrsg.): Flora of China. Volume 18: Scrophulariaceae through Gesneriaceae. Science Press und Missouri Botanical Garden Press, Beijing und St. Louis 1998, ISBN 0-915279-55-X. Gesneriaceae., S. 244 – textgleich online wie gedrucktes Werk. (Abschnitte Systematik und Beschreibung)
- A. Chautems, 2009: Neotropical Gesneriaceae bei Neotropikey – Interactive key and information resources for flowering plants of the Neotropics. (Abschnitte Beschreibung und Systematik)
- Ron Myhr: The Gesneriad Reference Web.
- Laurence E. Skog, John K. Boggan: A new classification of the western hemisphere Gesneriaceae. In: Gesneriads, Volume 56, Issue 3, 2006, S. 12–19.
Bibliografia complementar
- Laurence E. Skog: Gesneriaceae in the 21st Century. In: Selbyana, Volume 25, Issue 2, 2005, S. 179–181.
- Z. Xu, B. L. Burtt, L. E. Skog, David John Middleton: A revision of Paraboea. In: Edinburgh Journal of Botany, Volume 65, Issue 2, 2008, S. 161–347. doi:10.1017/S0960428608005106
- E. H. Roalson, L. E. Skog, E. A. Zimmer: Untangling Gloxinieae (Gesneriaceae). II. Reconstructing biogeographic patterns and estimating divergence times among New World continental and island lineages. In: Systematic Botany, Volume 33, Issue 1, 2008, S. 159–175. doi:10.1600/036364408783887429
- Michael Möller, M. Pfosser, C. G. Jang, V. Mayer, A. Clark, M. L. Hollingsworth, M. H. J. Barfuss, Y. Z. Wang, M. Kiehn, Anton Weber: A preliminary phylogeny of the ‘Didymocarpoid Gesneriaceae’ based on three molecular data sets: incongruence with available tribal classifications. In: American Journal of Botany, Volume 96, 2009, S. 989–1010. doi:10.3732/ajb.0800291
- Y. G. Wei, Fang Wen, W. H. Chen, Y. M. Shui, Michael Möller: Litostigma, a new genus from China: a morphological link between basal and derived didymocarpoid Gesneriaceae. In: Edinburgh Journal of Botany, Volume 67, Issue 1, 2010, S. 161–184. doi:10.1017/S0960428609990291
- Michael Möller, A. Forrest, Y. G. Wei, Anton Weber: A molecular phylogenetic assessment of the advanced Asiatic and Malesian Didymocarpoid Gesneriaceae with focus on non-monophyletic and monotypic genera. In: Plant Systematics and Evolution, Volume 292, 2011, S. 223–248. doi:10.1007/s00606-010-0413-z
- Vincent L. Woo, Minde M. Funke, James F. Smith, Peter J. Lockhart, Philip J. Garnock-Jones: New World Origins of Southwest Pacific Gesneriaceae: Multiple Movements Across and Within the South Pacific, In: International Journal of Plant Sciences, Volume 172, Issue 3, 2011, S. 434–457: Online bei JSTOR.
- John L. Clark, Minde M. Funke, Aaron M. Duffy, James F. Smith: Phylogeny of a Neotropical Clade in the Gesneriaceae: More Tales of Convergent Evolution, In: International Journal of Plant Sciences, Volume 173, Issue 8, 2012, S. 894–916: doi:10.1086/667229
- David John Middleton, Michael Möller: Tribounia, a new genus of Gesneriaceae from Thailand. In: Taxon, Volume 61, Issue 6, 2012, S. 1286–1295.
- Mathieu Perret, Alain Chautems, Andréa Onofre De Araujo, Nicolas Salamin: Temporal and spatial origin of Gesneriaceae in the New World inferred from plastid DNA sequences. In: Botanical Journal of the Linnean Society, Volume 171, Issue 1, 2013, S. 61–79. doi:10.1111/j.1095-8339.2012.01303.x
- David Middleton, Hannah Atkins, Luu Hong Truong, Kanae Nishii, Michael Möller: Billolivia, a new genus of Gesneriaceae from Vietnam with five new species. In: Phytotaxa, Volume 161, Issue 4, 2014: doi:10.11646/phytotaxa.161.4.1
- S. M. Scott, David John Middleton: A revision of Ornithoboea (Gesneriaceae). In: Gardens’ Bulletin Singapore, Volume 66, Issue 1, 2014, S. 73–119.
- David John Middleton, Kanae Nishii, Carmen Puglisi, Laura L. Forrest, Michael Möller: Chayamaritia, (Gesneriaceae: Didymocarpoideae), a new genus from Southeast Asia. In: Plant Systematics and Evolution, Volume 301, 2015, S. 1–20. doi:10.1007/s00606-015-1213-2
- X. L. Yu, M. Li, J.J. Zhou, P. W. Li: Petrocodon hunanensis (Gesneriaceae), a new species identified by both morphological and molecular evidence from limestone area in Hunan, China. In: Phytotaxa, Volume 195, 2015, S. 65–72. doi:10.11646/phytotaxa.195.1.4
- Michael Möller, Y. G. Wei, Fang Wen, John L. Clark, Anton Weber: You win some you lose some: updated generic delineations and classification of Gesneriaceae—implications forthe family in China. In: Guihaia, Volume 36, 2016, S. 44–60.
- A. P. Janeesha, Michael Möller, Santhosh Nampy, Anton Weber: The Gesneriaceae of India: Consequences of updated generic concepts and new family classification. In: Rheedea, Volume 27, Issue 1, Juni 2017, S. 23–41. doi:10.22244/rheedea.2017.27.1.5
- M. L. Serrano-Serrano, J. Rolland, J. L. Clark, N. Salimin, M. Perret: Hummingbird pollination and the diversification of angiosperms: an old and successful association in Gesneriaceae. In: Proceedings of the Royal Society, Botany, Volume 284, 2017, 20162816. doi:10.1098/rspb.2016.2816
- W. B. Xu, J. Guo, B. Pan, Q. Zhang, Y. Liu: Diversity and distribution of Gesneriaceae in China. In: Guihaia, Volume 37, 2017, S. 1219–1226. doi:10.11931/guihaia.gxzw201707004 (in Chinesisch)
- Li-Hua Yang, Chen Feng, Mei-Zhen Xu, Zhi-Xia Sun, Ming Kang: Synopsis of Cytological Studies on Didymocarpoideae (Gesneriaceae) under New Classification System. In: Journal of Tropical and Subtropical Botany (Redai Yaredai Zhiwu Xuebao), Volume 27, Issue 5, 2019, S. 548–557.
- Fang Wen, S. Li, Z. Xin, L. F. Fu, X. Hong, L. Cai, J. Q. Qin, B. Pan, F. Z. Pan, Y. G. Wei: The updated plant list of Gesneriaceae in China under the new Chinese naming rules. In: Guangxi Sciences, Volume 26, Issue 1, 2019, S. 37–63. doi:10.13656/j.cnki.gxkx.20190225.002
- R. B. Zhang, T. Deng, L. F. Fu, S. Li, L. He, T. Deng, Q. L. Dou, Fang Wen: Petrocodon tongziensis (Gesneriaceae), a new species from limestone areas in Guizhou, China based on morphological and molecular evidence. In: Nordic Journal of Botany, c01774, 2019, S. 1–7. doi:10.1111/njb.01774
- S. Sirimongkol, J. A. N. Parnell, T. R. Hodkinson, David John Middleton, C. Puglisi: Five new species of Henckelia (Gesneriaceae) from Myanmar and Thailand. In: Thai Forest Bulletin, Botany, Volume 47, Issue 1, 2019, S. 38–54. doi:10.20531/tfb.2019.47.1.08
- Hannah J. Atkins, Gemma L. C. Bramley, Melissa A. Johnson, Abdulrokhman Kartonegoro, Kanae Nishii, Goro Kokubugata, Michael Moeller, Mark Hughes: A molecular phylogeny of Southeast Asian Cyrtandra (Gesneriaceae) supports an emerging paradigm for Malesian plant biogeography. In: Frontiers of Biogeography, Volume 12, Issue 1, 2020, e44814. doi:10.21425/F5FBG44184
- Ke Tan, Tao Lu, Ming-Xun Ren: Biogeography and evolution of Asian Gesneriaceae based on updated taxonomy. In: Y-M. Shui, W-H. Chen, Ming-Xun Ren, Fang Wen, X. Hong, Z-J. Qiu, Y-G. Wei, M. Kang (Hrsg.): Taxonomy of Gesneriaceae in China and Vietnam. In: PhytoKeys, Volume 157, August 2020, S. 7–26. doi:10.3897/phytokeys.157.34032
- Ke Tan, Tao Lu, Ming-Xun Ren: Gesneriaceae in China and Vietnam: Perfection of taxonomy based on comprehensive morphological and molecular evidence. In: Y-M. Shui, W-H. Chen, Ming-Xun Ren, Fang Wen, X. Hong, Z-J. Qiu, Y-G. Wei, M. Kang (Hrsg.): Taxonomy of Gesneriaceae in China and Vietnam. In: PhytoKeys, Volume 157, August 2020, S. 7–26. doi:10.3897/phytokeys.157.34032
- Alain Chautems, Domingos B.O.S. Cardoso, Mathieu Perret: Two new species of Sinningia (Gesneriaceae) endemic to Bahia, Brazil. In: Candollea, Volume 77, Issue 2, September 2022, S. 137–144. doi:10.15553/c2022v772a1
Ver também
Ligações Externas
- «Informação sobre Lamiales - Angiosperm Phylogeny Website» (em inglês)
- «Chave de identificação de famílias de angiospérmicas» (em inglês)
- «Imagens e descrição de famílias de angiospérmicas - segundo sistema Cronquist» (em inglês)
- World Checklist of Gesneriaceae
- Genera of Gesneriaceae
- Gesneriad Reference Web
- Gesneriaceae: A Scientific Overview, by Prof. Anton Weber (on the Gesneriad Reference Web)
- Gesneriaceae in Flora of China
- The Gesneriad Society (formerly the American Gloxinia and Gesneriad Society)
- Annotated Bibliography of the Gesneriaceae
- Phylogenetic relationships in the Gesnerioideae (Gesneriaceae) based on nrDNA ITS and cpDNA trnL-F and trnE-T spacer region sequences Arquivado em 2010-06-26 no Wayback Machine (link to abstract)
- Evolution of Cyrtandra (Gesneriaceae) in the Pacific Ocean: the origin of a supertramp clade
- Weber, A. 2004. Gesneriaceae and Scrophulariaceae: Robert Brown and now. Telopea 10(2): 543-571.
- Gesneriaceae: All you need to know about gesneriads. Arquivado em 2015-02-08 no Wayback Machine
- American Gloxinia and Gesneriad Society. (inglês)
- James F. Smith, 20. April 1998: Gesneriaceae em The Tree of Life Web Project. (inglês)
- Gesneriaceae no PacificBulbSociety. (inglês)