Cenários alternativos de abiogênese
Um cenário é um conjunto de conceitos relacionados pertinentes a origem da vida (abiogênese) ou biopoese, termo que tem origem no grego antigo e é formado pela junção das palavras bios (vida) e poiesis (criação), tal como o mundo ferro-enxofre. Muitos cenários alternativos de abiogênese tem sido propostas por cientistas de vários campos a partir da década de 1950, numa tentativa de explicar como os mecanismos complexos da vida poderiam ter surgido. Isso inclui hipóteses de ambientes antigos que podem ter sido favoráveis à origem da vida e possíveis mecanismos bioquímicos.
Um cenário
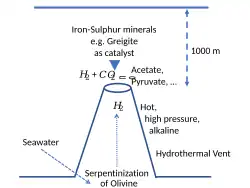
O bioquímico Nick Lane propôs um cenário possível para a origem da vida que integra muitas das evidências disponíveis da bioquímica, geologia, filogenia e experimentação:[1]
-
-
![Protocélulas em contato com uma fina barreira rochosa em uma fonte hidrotermal recebem um suprimento gratuito de energia do gradiente de pH.[2]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_2.svg.png) Protocélulas em contato com uma fina barreira rochosa em uma fonte hidrotermal recebem um suprimento gratuito de energia do gradiente de pH.[2]
Protocélulas em contato com uma fina barreira rochosa em uma fonte hidrotermal recebem um suprimento gratuito de energia do gradiente de pH.[2] -
![Protocélulas em uma fonte hidrotermal podem crescer adicionando ácidos graxos à sua membrana e outras substâncias orgânicas ao seu citoplasma.[3]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_3.svg.png) Protocélulas em uma fonte hidrotermal podem crescer adicionando ácidos graxos à sua membrana e outras substâncias orgânicas ao seu citoplasma.[3]
Protocélulas em uma fonte hidrotermal podem crescer adicionando ácidos graxos à sua membrana e outras substâncias orgânicas ao seu citoplasma.[3] -
![Nucleotídeos em uma protocélula em uma fonte hidrotermal podem polimerizar em sequências aleatórias de RNA. Qualquer um que tenha até mesmo uma leve atividade catalítica favorecerá o crescimento e a replicação de suas protocélulas, um começo para a seleção natural.[4]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_4.svg.png) Nucleotídeos em uma protocélula em uma fonte hidrotermal podem polimerizar em sequências aleatórias de RNA. Qualquer um que tenha até mesmo uma leve atividade catalítica favorecerá o crescimento e a replicação de suas protocélulas, um começo para a seleção natural.[4]
Nucleotídeos em uma protocélula em uma fonte hidrotermal podem polimerizar em sequências aleatórias de RNA. Qualquer um que tenha até mesmo uma leve atividade catalítica favorecerá o crescimento e a replicação de suas protocélulas, um começo para a seleção natural.[4] -
![Uma protocélula distante de uma fonte hidrotermal deve criar sua própria força protônica, como por exemplo, pela divisão do sulfeto de hidrogênio.[5]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_5.svg.png) Uma protocélula distante de uma fonte hidrotermal deve criar sua própria força protônica, como por exemplo, pela divisão do sulfeto de hidrogênio.[5]
Uma protocélula distante de uma fonte hidrotermal deve criar sua própria força protônica, como por exemplo, pela divisão do sulfeto de hidrogênio.[5] -
![A ferredoxina catalisa a divisão do sulfeto de hidrogênio, sua primeira sequência de aminoácidos repetida, talvez codificada por um código genético incompleto.[6]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_6.svg.png) A ferredoxina catalisa a divisão do sulfeto de hidrogênio, sua primeira sequência de aminoácidos repetida, talvez codificada por um código genético incompleto.[6]
A ferredoxina catalisa a divisão do sulfeto de hidrogênio, sua primeira sequência de aminoácidos repetida, talvez codificada por um código genético incompleto.[6] -
![A fotossíntese anoxigênica, usando sulfeto de hidrogênio, acabou com a necessidade de escasso hidrogênio.[6]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_7.svg.png) A fotossíntese anoxigênica, usando sulfeto de hidrogênio, acabou com a necessidade de escasso hidrogênio.[6]
A fotossíntese anoxigênica, usando sulfeto de hidrogênio, acabou com a necessidade de escasso hidrogênio.[6] -
![Os primeiros heterótrofos usavam a respiração do ciclo de Krebs; depois, a fotossíntese oxigenada proporcionou total independência da energia vulcânica.[6]](./_assets_/0c70a452f799bfe840676ee341124611/Abiogenesis_Scenario_8.svg.png) Os primeiros heterótrofos usavam a respiração do ciclo de Krebs; depois, a fotossíntese oxigenada proporcionou total independência da energia vulcânica.[6]
Os primeiros heterótrofos usavam a respiração do ciclo de Krebs; depois, a fotossíntese oxigenada proporcionou total independência da energia vulcânica.[6]
Ambientes
Muitos ambientes foram propostos para a origem da vida.
Salinidade flutuante: diluição e secagem
Harold Blum observou em 1957 que se cadeias de proto-ácidos nucleicos formam espontaneamente estruturas duplas, então não há como dissociá-las.[7]
A hipótese de Oparin-Haldane aborda a formação, mas não a dissociação, de polímeros de ácido nucleico e duplexos. Entretanto, os ácidos nucleicos são incomuns porque, na ausência de contra-íons (baixo teor de sal) para neutralizar as altas cargas nos grupos fosfato opostos, o duplexo de ácido nucleico se dissocia em cadeias simples.[8] As primeiras marés, impulsionadas pela proximidade da Lua, podem ter gerado ciclos rápidos de diluição (maré alta, sal baixo) e concentração (secagem na maré baixa, sal alto) que promoveram exclusivamente a replicação de ácidos nucleicos[8] através de um processo denominado reação em cadeia das marés (abreviado na literatura em inglês como TCR, tidal chain reaction).[9] Esta teoria foi criticada com base no facto de as primeiras marés poderem não ter sido tão rápidas,[10] embora a regressão dos valores atuais exija uma justaposição Terra-Lua em torno de dois Ga (bilhões de anos), para a qual não há evidências, e as primeiras marés podem ter ocorrido aproximadamente a cada sete horas.[11] Outra crítica é que apenas 2–3% da crosta terrestre pode ter sido exposta acima do mar até o final da evolução terrestre.[12]
A teoria da reação em cadeia de maré tem vantagens mecanicistas sobre a associação/dissociação térmica em fontes hidrotermais profundas porque requer que a montagem da cadeia (polimerização orientada por molde) ocorra durante a fase de secagem, quando os precursores estão mais concentrados, enquanto o ciclo térmico requer que a polimerização ocorra durante a fase fria, quando a taxa de montagem da cadeia é menor e os precursores provavelmente estão mais diluídos.
Lagos de água doce quente
Jack W. Szostak sugeriu que a atividade geotérmica oferece maiores oportunidades para a origem da vida em lagos abertos onde há um acúmulo de minerais. Em 2010, com base na análise espectral do mar e da água mineral quente, Ignat Ignatov e Oleg Mosin demonstraram que a vida pode ter se originado predominantemente na água mineral quente. Água mineral quente que contenha íons hidrogenocarbonato (bicarbonato) e cálcio tem o alcance mais otimizado.[13][14] Este caso é semelhante à origem da vida em fontes hidrotermais, mas com hidrogenocarbonato e íons de cálcio em água quente.[15][16] No pH de 9–11, as reações podem ocorrer na água do mar. De acordo com Melvin Calvin, certas reações de condensação-desidratação de aminoácidos e nucleotídeos em blocos individuais de peptídeos e ácidos nucleicos podem ocorrer na hidrosfera primária com pH 9–11 em um estágio evolutivo posterior.[17] Alguns desses compostos como ácido cianídrico (HCN) tem sido comprovados em experimentos de Miller. Este é o ambiente em que os estromatólitos tem sido criados. David Ward descreveu a formação de estromatólitos em água mineral quente no Parque Nacional de Yellowstone.[18] Em 2011, Tadashi Sugawara criou uma protocélula em água quente.[19]
Fontes geotérmicas
Bruce Damer e David Deamer argumentam que as membranas celulares não podem ser formadas em água do mar salgada e, portanto, devem ter se originado em ambientes de água doce, como piscinas reabastecidas por uma combinação de fontes geotérmicas e chuva. Antes da formação dos continentes, a única terra seca na Terra seriam ilhas vulcânicas, onde a água da chuva formaria lagoas onde os lipídios poderiam formar os primeiros estágios em direção às membranas celulares. Durante múltiplos ciclos úmido-seco, biopolímeros seriam sintetizados e encapsulados em vesículas após a condensação. Sulfeto de zinco e sulfeto de manganês nessas lagoas teriam catalisado compostos orgânicos por fotossíntese abiótica.[20] Pesquisas experimentais em fontes geotérmicas sintetizaram com sucesso polímeros e os encapsularam em vesículas após exposição à luz UV e múltiplos ciclos de úmidoseco.[21] Em temperaturas de 60 a 80 °C em campos geotérmicos, podem ocorrer reações bioquímicas.[22] Supõe-se que esses predecessores de células verdadeiras se comportaram mais como um superorganismo do que como estruturas individuais, onde as membranas porosas abrigariam moléculas que vazariam e entrariam em outras protocélulas. Somente quando as células verdadeiras tivessem evoluído elas se adaptariam gradualmente a ambientes mais salgados e entrariam no oceano.[23][24]
6 das 11 reações bioquímicas do ciclo rTCA podem ocorrer em água ácida quente rica em metais, o que sugere que reações metabólicas podem ter se originado neste ambiente, o que é consistente com a estabilidade aprimorada do fosfodiéster de RNA, ligações aminoacil-tRNA e peptídeos em condições ácidas.[25] Ciclos entre CO2 supercrítico e subcrítico em zonas de falhas tectônicas podem ter levado à integração de peptídeos e à estabilização de membranas lipídicas. Isso é sugerido como tendo impulsionado a evolução da proteína da membrana, pois mostrou que um peptídeo selecionado (H-Lys-Ser-Pro-Phe-Pro-Phe-Ala-Ala-OH) causa o aumento da permeabilidade da membrana à água.[26] David Deamer e Bruce Damer afirmam que a química prebiótica não requer irradiação ultravioleta, pois a química também poderia ter ocorrido em áreas sombreadas que protegiam as biomoléculas da fotólise.[27]
Fontes alcalinas marinhas profundas
Nick Lane acredita que nenhuma forma de vida conhecida poderia ter utilizado fotossíntese baseada em sulfeto de zinco, raios, síntese de pirita vulcânica ou radiação UV como fonte de energia. Em vez disso, ele sugere que as fontes alcalinas do fundo do mar têm mais probabilidade de ter sido uma fonte de energia para a vida celular inicial.[28] A serpentinização em fontes hidrotermais alcalinas produz metano e amônia.[29] Partículas minerais que têm propriedades semelhantes às enzimas em fontes hidrotermais profundas catalisariam compostos orgânicos a partir de fontes de CO2 dissolvido na água do mar.[30] Rochas porosas podem ter promovido reações de condensação de biopolímeros e atuar como um compartimento de estruturas membranosas, porém não se sabe como elas puderam promover a codificação e o metabolismo.[31] O acetilfosfato, que é prontamente sintetizado a partir do tioacetato, pode promover a agregação de adenosina monofosfato de até 7 monômeros, o que é considerado energeticamente favorecido na água devido às interações entre nucleobases. O acetilfosfato pode estabilizar a agregação de nucleotídeos na presença de Na+ e poderia possivelmente promover a polimerização em superfícies minerais ou diminuir a atividade da água.[32] Um gradiente externo de prótons dentro de uma membrana teria sido mantido entre o oceano ácido e a água do mar alcalina.[33][34] Os descendentes do último ancestral comum universal, bactérias e arqueas, eram provavelmente metanógenos e acetógenos.[35] Os primeiros microfósseis, datados de 4,28 a 3,77 Ga, foram encontrados em precipitados de fontes hidrotermais. Esses microfósseis sugerem que a vida celular inicial começou em fontes hidrotermais de águas profundas.[36] Reações exergônicas nesses ambientes podem ter fornecido energia livre que promoveu reações químicas propícias a biomoléculas prebióticas.[29]
Reações não enzimáticas da glicólise e da via da pentose fosfato podem ocorrer na presença de ferro ferroso a 70 °C, as reações produzem eritrose 4-fosfato, um precursor de aminoácido e ribose 5-fosfato, um precursor de nucleotídeo.[37] Pirimidinas são sintetizadas a partir da reação entre aspartato e fosfato de carbamoil a 60 °C e na presença de metais,[38] sugere-se que as purinas podem ser sintetizadas a partir da catálise de metais.[39] O monofosfato de adenosina também é sintetizado a partir de adenina, fosfato monopotássico ou pirofosfato e ribose em sílica a 70 °C.[40] Reações de aminações e transaminações redutivas catalisadas por íons minerais e metálicos de fontes hidrotermais alcalinas produzem aminoácidos.[39] Ácidos graxos de cadeia longa podem ser derivados do ácido fórmico ou do ácido oxálico durante síntese do tipo Fischer-Tropsch.[41] Carboidratos contendo um esqueleto de isopreno podem ser sintetizados a partir da reação formose. Os isoprenóides incorporados nas vesículas de ácidos graxos podem estabilizar as vesículas, o que se sugere ter impulsionado a divergência de lipídios bacterianos e arqueais.[42]
Cinzas vulcânicas no oceano
Geoffrey W. Hoffmann argumentou que um evento de nucleação complexo como origem da vida envolvendo polipeptídeos e ácidos nucléicos é compatível com o tempo e o espaço disponíveis nos oceanos primários da Terra.[43] Hoffmann sugere que as cinzas vulcânicas podem fornecer as muitas formas aleatórias necessárias no postulado evento de nucleação complexa. Este aspecto da teoria pode ser testado experimentalmente.
A biosfera profunda e quente de Gold
Nos anos 1970, Thomas Gold propôs a teoria de que a vida se desenvolveu primeiro não na superfície da Terra, mas vários quilômetros abaixo da superfície. Alega-se que a descoberta de vida microbiana abaixo da superfície de outro corpo no nosso Sistema Solar daria um crédito significativo a esta teoria.[44]
Hipótese da praia radioativa
Zachary Adam afirma que os processos de maré que ocorreram durante uma época em que a Lua estava muito mais próxima podem ter concentrado grãos de urânio e outros elementos radioativos no ponto mais alto das praias primordiais, onde podem ter sido responsáveis pela geração dos blocos de construção da vida.[45] De acordo com modelos de computador,[46] um depósito de tais materiais radioativos poderia mostrar a mesma reação nuclear autossustentável como o encontrado na jazida de minério de urânio Oklo no Gabão. Essa areia de praia radioativa pode ter fornecido energia suficiente para gerar moléculas orgânicas, como aminoácidos e açúcares de acetonitrila na água. O material radioativo monazita também liberou fosfato solúvel nas regiões entre os grãos de areia, tornando-o biologicamente "acessível". Assim, aminoácidos, açúcares e fosfatos solúveis podem ter sido produzidos simultaneamente, segundo Adam. Actinídeos radioativos, deixados para trás em alguma concentração pela reação, podem ter feito parte de complexos organometálicos. Esses complexos poderiam ter sido importantes catalisadores iniciais para processos vivos.
John Parnell sugeriu que tal processo poderia fornecer parte do "cadinho da vida" nos estágios iniciais de qualquer planeta rochoso úmido, desde que o planeta seja grande o suficiente para ter gerado um sistema de placas tectônicas que traz minerais radioativos para a superfície . Como se pensa que a Terra primitiva tinha muitas placas menores, poderia ter proporcionado um ambiente adequado para tais processos.[47]
O hiperciclo
No início dos anos 1970, Manfred Eigen e Peter Schuster examinou os estágios transitórios entre o caos molecular e um hiperciclo auto-replicante em uma sopa prebiótica.[48] Em um hiperciclo, o sistema de armazenamento de informação (possivelmente RNA) produz uma enzima, que catalisa a formação de outro sistema de informação, em sequência até o produto do último auxiliar na formação do primeiro sistema de informação. Tratados matematicamente, os hiperciclos poderiam criar quase-espécies, que através da seleção natural entrou em uma forma de evolução darwiniana. Um impulso à teoria do hiperciclo foi a descoberta de ribozimas capazes de catalisar suas próprias reações químicas. A teoria do hiperciclo requer a existência de compostos bioquímicos complexos, como os nucleotídeos, que não se formam nas condições propostas pelo experimento Miller–Urey.
Mundo ferro–enxofre
Nos anos 1980, o bioquímico alemão Günther Wächtershäuser e Karl Popper postulou a hipótese do mundo ferro–enxofre para a evolução de caminhos químicos pré-bióticos traçando a bioquímica atual para reações primordiais que sintetizam blocos de construção orgânicos a partir de gases.[49][50] Os sistemas de Wächtershäuser têm uma fonte interna de energia: sulfetos de ferro, como a pirita. A energia liberada pela oxidação desses sulfetos metálicos pode suportar a síntese de moléculas orgânicas. Tais sistemas podem ter evoluído para conjuntos autocatalíticos constituindo entidades auto-replicantes e metabolicamente ativas, anteriores às formas de vida modernas.[37] Experimentos com sulfetos em ambiente aquoso a 100 °C produziram um pequeno rendimento de dipeptídeos (0,4% a 12,4%) e um menor rendimento de tripeptídeos (0,10%). Entretanto, sob as mesmas condições, os dipeptídeos foram rapidamente decompostos.[51]
Vários modelos postulam um metabolismo primitivo, permitindo que a replicação do RNA surja posteriormente. A centralidade do ciclo de Krebs (ciclo do ácido cítrico) para a produção de energia em organismos aeróbicos e na captação de dióxido de carbono e íons de hidrogênio na biossíntese de substâncias químicas orgânicas complexas sugere que foi uma das primeiras partes do metabolismo a evoluir.[52] Concordantemente, geoquímicos Szostak e Kate Adamala demonstraram que a replicação não enzimática do RNA em protocélulas primitivas só é possível na presença de queladores de cátions fracos como ácido cítrico. Isto fornece mais evidências para o papel central do ácido cítrico no metabolismo primordial.[53] Russell propôs que "o propósito da vida é hidrogenar dióxido de carbono" (como parte de um cenário de “metabolismo primeiro”, em vez de “genética primeiro”).[54][55][37] O físico Jeremy England argumentou, a partir de considerações termodinâmicas gerais, que a vida terias sido inevitável.[56] Uma versão inicial dessa ideia foi a proposta de Oparin de 1924 para vesículas auto-replicantes. Nas décadas de 1980 e 1990, surgiram a teoria do mundo ferro-enxofre de Wächtershäuser e os modelos tioéster de Christian de Duve. Argumentos mais abstratos e teóricos para o metabolismo sem genes incluem o modelo matemático de Freeman Dyson e os conjuntos coletivamente autocatalíticos de Stuart Kauffman na década de 1980. O trabalho de Kauffman foi criticado por ignorar o papel da energia na condução de reações bioquímicas nas células.[57]
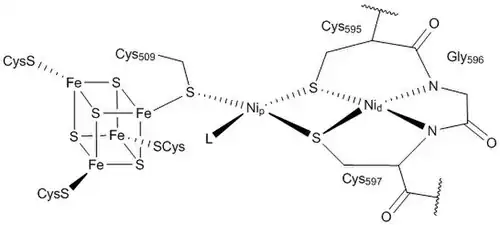
Uma via bioquímica de múltiplas etapas, como o ciclo de Krebs, não se auto-organizou apenas na superfície de um mineral; ela deve ter sido precedida por vias mais simples.[58] A via Wood–Ljungdahl (via redutiva da acetil-coenzima A ou acetyl-CoA) é compatível com a auto-organização em uma superfície de sulfeto de metal. Sua unidade enzimática chave (duas enzimas trabalhando juntas), monóxido de carbono desidrogenase/acetil-CoA sintase, contém aglomerados mistos de níquel-ferro-enxofre em seus centros de reação e catalisa a formação de acetil-CoA. No entanto, é termodinamicamente e cineticamente improvável que os compostos prebióticos tiolados e tioésteres se acumulem nas condições prebióticas presumidas das fontes hidrotermais.[59] Uma possibilidade é que cisteína e homocisteína podem ter reagido com nitrilas da reação de Strecker, formando polipeptídeos catalíticos ricos em tiol.[60]
Foi sugerido que a hipótese do mundo ferro-enxofre e a hipótese do mundo RNA não são mutuamente exclusivas, pois os processos celulares modernos envolvem tanto metabólitos quanto moléculas genéticas.[61]
Mundo de zinco
A hipótese do mundo de zinco (mundo Zn) de Armen Mulkidjanian estende a hipótese da pirita de Wächtershäuser.[62][63] A teoria do mundo Zn propõe que os fluidos hidrotermais ricos em H2S interagindo com a água fria do oceano primordial (ou "pequeno lago quente" de Darwin) precipitou partículas de sulfeto de metal. Os sistemas hidrotermais oceânicos têm uma estrutura zonal refletida em antigos depósitos maciços de minério de sulfeto vulcanogênico. Eles atingem muitos quilômetros de diâmetro e datam do Arqueano. Os mais abundantes são a pirita (FeS2), calcopirita (CuFeS2) e esfalerita (ZnS), com adições de galena (PbS) e alabandita (MnS). ZnS e MnS tem uma capacidade única de armazenar energia de radiação, e.g. da luz ultravioleta. Quando as moléculas replicantes estavam se originando, a pressão atmosférica primordial era alta o suficiente (>100 bar) para precipitar perto da superfície da Terra, e a irradiação ultravioleta era 10 a 100 vezes mais intensa que agora; daí as propriedades fotossintéticas mediadas por ZnS fornecendo as condições energéticas adequadas para a síntese de moléculas informacionais e metabólicas e a seleção de nucleobases fotoestáveis.[64]
A teoria do mundo Zn foi preenchida com evidências para a constituição iônica do interior das primeiras protocélulas. Em 1926, o bioquímico canadense Archibald Macallum notou a semelhança de fluidos corporais tais como sangue e linfa com a água do mar;[65] no entanto, a composição inorgânica de todas as células difere daquela da água do mar moderna, o que levou Mulkidjanian e colegas a reconstruir as "incubadoras" das primeiras células combinando a análise geoquímica com o escrutínio filogenômico dos requisitos de íons inorgânicos das células modernas. Os autores concluem que proteínas e sistemas funcionais ubíquos e, por inferência, primordiais, mostram afinidade e requisitos funcionais para K+, Zn2+, Mn2+ e [PO4]3−. A reconstrução geoquímica mostra que essa composição iônica não poderia ter existido no oceano, mas é compatível com sistemas geotérmicos interiores. No ambiente com pouco oxigênio, atmosfera primordial dominada por CO2, a química dos condensados de água próximos de campos geotérmicos assemelhar-se-ia ao meio interno das células modernas. Portanto, a evolução pré-celular pode ter ocorrido em ambientes superficiais "poças de Darwin" cobertas com minerais silicatos porosos misturados com sulfetos metálicos e enriquecidos em K+, Zn2+ e compostos fosforosos.[66][nota 1]
Argila
A hipótese da argila foi proposta por Graham Cairns-Smith em 1985.[67][68] Ela postula que moléculas orgânicas complexas surgiram gradualmente em superfícies de replicação não orgânicas preexistentes de cristais de silicato em contato com uma solução aquosa. O argilomineral montmorillonita tem sido demonstrado como catalisando a polimerização de RNA em solução aquosa de monômeros de nucleotídeos,[69] e a formação de membranas a partir de lipídios.[70] Em 1998, Hyman Hartman propôs que "os primeiros organismos eram argilas ricas em ferro auto-replicantes que fixavam dióxido de carbono em ácido oxálico e outros ácidos dicarboxílicos. Este sistema de fenótipo de replicação de argilas e seus metabolismos então evolui para a região rica em sulfeto da fonte termal adquirindo a capacidade de fixar nitrogênio. Finalmente, o fosfato foi incorporado ao sistema em evolução, o que permitiu a síntese de nucleotídeos e fosfolipídios."[71]
Bioquímica
Diferentes formas de vida com processos de origem variáveis podem ter surgido quase simultaneamente na Terra primitiva.[72] As outras formas podem estar extintas, tendo deixado fósseis característicos através de sua bioquímica diferente. Reações semelhantes ao metabolismo podem ter ocorrido naturalmente nos oceanos primitivos, antes que os primeiros organismos evoluíssem. Algumas dessas reações podem produzir RNA, e outras se assemelham a duas cascatas de reações essenciais do metabolismo: glicólise e a via da pentose fosfato, que fornecem precursores essenciais para ácidos nucleicos, aminoácidos e lipídios.[37][73]
Proteinoides de Fox
Ao tentar descobrir os estágios intermediários da abiogênese mencionados por Bernal, Sidney Fox nos anos 1950 e 1960 estudou a formação espontânea de estruturas de peptídeo sob condições plausivelmente primitivas da Terra. Em um de seus experimentos, ele permitiu que os aminoácidos secassem como se estivessem em uma poça em um local quente e seco em condições pré-bióticas: Em um experimento para criar condições adequadas para a formação da vida, Fox material vulcânico coletado de um cone de cinzas no Havaí. Ele descobriu que a temperatura sendo acima de 100 °C apenas 100 mm abaixo da superfície do cone de cinzas e sugeriu que este poderia ter sido o ambiente em que a vida foi criada—moléculas poderiam ter se formado e depois sido levadas pelas cinzas vulcânicas soltas para o mar. Ele colocou pedaços de lava sobre aminoácidos derivados de metano, amônia e água, esterilizou todos os materiais e cozinhou a lava sobre os aminoácidos por algumas horas em um forno de vidro. Uma substância marrom e pegajosa se formou sobre a superfície, e quando a lava foi encharcada em água esterilizada, um líquido espesso e marrom foi lixiviado. Ele descobriu que, à medida que secavam, os aminoácidos formavam polipeptídeos submicroscópicos longos, frequentemente reticulados, semelhantes a fios.[74]
Proteína amilóide
Uma teoria da origem da vida baseada em estruturas de folhas beta auto-replicantes foi proposta por Maury em 2009.[75][76] A teoria sugere que os catalisadores auto-replicantes e automontantes amiloides foram os primeiros polímeros informativos em um mundo primitivo pré-RNA. Os principais argumentos para a hipótese amiloide são baseados na estabilidade estrutural, nas propriedades autocatalíticas e catalíticas e na evolutividade dos sistemas informacionais baseados em folhas beta. Esses sistemas também corrigem erros[77] e são quiroseletivo.[78]
Primeira proteína que condensa substratos durante o ciclo térmico: termossíntese
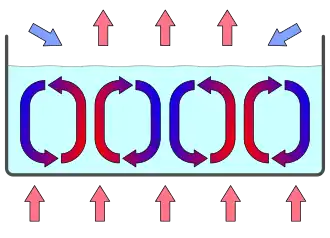
A hipótese da termossíntese considera a quimiosmose mais basal que a fermentação: a enzima ATP sintase, que sustenta a quimiosmose, é a enzima atualmente existente mais intimamente relacionada ao primeiro processo metabólico.[79][80] A hipótese da termossíntese nem sequer invoca um caminho: O mecanismo de mudança de ligação da ATP sintase assemelha-se a um processo de adsorção física que produz energia livre. O resultado seria a convecção, que traria um suprimento contínuo de reagentes para a protoenzima.[81] A primeira proteína descrita pode ser simples no sentido de que requer apenas uma sequência curta de resíduos de aminoácidos conservados, um sequenciador suficiente para a fenda catalítica apropriada.[82]
Mundo pré-RNA: A questão de evitar-se a necessidade da ribose
Um tipo diferente de ácido nucleico, tal como ácido nucleico peptídico, ácido treonucleico ou ácido glicolnucleico, poderia ter sido o primeiro a surgir como uma molécula auto-reprodutora, mais tarde substituída pelo RNA.[83][84] Larralde et al., afirmam que "a síntese prebiótica geralmente aceita de ribose, a reação da formose, produz numerosos açúcares sem qualquer seletividade".[85] Eles concluem que "a espinha dorsal do primeiro material genético não poderia conter ribose ou outros açúcares devido à sua instabilidade", o que significa que a ligação éster da ribose e do ácido fosfórico no RNA é propensa à hidrólise.[86]
Os ribonucleosídeos e nucleotídeos de pirimidina foram sintetizados por reações que contornam os açúcares livres e são montados passo a passo usando químicas nitrogenadas ou oxigenadas. Sutherland demonstrou rotas de alto rendimento para ribonucleotídeos de citidina e uridina a partir de pequenos fragmentos de 2 e 3 carbonos, tal como glicolaldeído, gliceraldeído ou gliceraldeído-3-fosfato, cianamida e cianoacetileno. Uma etapa desta sequência permite o isolamento de ribose aminooxazolina enantiopura se o excesso enantiomérico de gliceraldeído for 60% ou maior.[87] Isso pode ser visto como uma etapa de purificação prebiótica. A ribose aminooxazolina pode então reagir com cianoacetileno para dar ribonucleotídeo alfa citidina. A fotoanomerização com luz UV permite a inversão em torno do centro anomérico 1' para dar a estereoquímica beta correta.[88] Em 2009, eles mostraram que os mesmos blocos de construção simples permitem o acesso, por meio da elaboração de nucleobases controlada por fosfato, a nucleotídeos de pirimidina 2',3'-cíclicos diretamente, os quais podem polimerizar em RNA. Similar foto-sanitização pode criar fosfatos pirimidina-2',3'-cíclica.[89]
Autocatálise
Autocatalisador são substâncias que catalisam a produção de si mesmas e, portanto, são "replicadores moleculares". Os sistemas químicos autorreplicantes mais simples são autocatalíticos e normalmente contêm três componentes: uma molécula de produto e duas moléculas precursoras. A molécula de produto se junta às moléculas precursoras, que por sua vez produzem mais moléculas de produto a partir de mais moléculas precursoras. A molécula de produto catalisa a reação fornecendo um molde complementar que se liga aos precursores, unindo-os assim. Tais sistemas foram demonstrados tanto em macromoléculas biológicas quanto em pequenas moléculas orgânicas.[90]
Foi proposto que a vida surgiu inicialmente como redes químicas autocatalíticas.[91][92] Julius Rebek e colegas combinaram amino adenosina e ésteres pentafluorofenílicos com o éster triácido aminoadenosina autocatalisador (AATE, amino adenosine triacid ester). Um produto foi uma variante de AATE o qual catalisou sua própria síntese. Isso demonstrou que os autocatalisadores poderiam competir dentro de uma população de entidades com hereditariedade, uma forma rudimentar de seleção natural.[93]
Síntese baseada em cianeto de hidrogênio
Um projeto de pesquisa concluído em 2015 por John Sutherland e outros descobriram que uma rede de reações começando com cianeto de hidrogênio e sulfeto de hidrogênio, em correntes de água irradiadas por luz UV, poderiam produzir os componentes químicos de proteínas e lipídios, bem como os do RNA,[94] embora não produza uma ampla gama de outros compostos.[95] Os pesquisadores usaram o termo "cianossulfídico" para descrever essa rede de reações.[94]
Rotas químicas simuladas
Em 2020, químicos descreveram possíveis caminhos químicos de produtos químicos prebióticos não vivos para complexos bioquímicos que poderia dar origem a organismos vivos, com base em um novo programa de computador chamado AllChemy.[96]
Origem viral
Evidências para uma hipótese de "vírus primeiro", que pode apoiar teorias do mundo do RNA, foram sugeridas em 2015.[97][98] Uma das dificuldades para o estudo das origens dos vírus é sua alta taxa de mutação; esse é particularmente o caso de retrovírus de RNA como o HIV.[99] Um estudo de 2015 comparou estruturas de dobra de proteína através de diferentes ramos da árvore da vida, onde os pesquisadores podem reconstruir as histórias evolutivas das dobras e dos organismos cujos genomas codifica para essas dobras. Eles argumentam que as dobras de proteínas são melhores marcadores de eventos antigos, pois suas estruturas tridimensionais podem ser mantidas mesmo quando as sequências que codificam essas dobras começam a mudar.[97]
Assim, o repertório de proteínas virais retém traços de história evolutiva antiga que podem ser recuperados usando abordagens avançadas de bioinformática. Esses pesquisadores acham que "a pressão prolongada do genoma e a redução do tamanho das partículas eventualmente reduziram as virocélulas em vírus modernos (identificados pela perda completa da composição celular), enquanto outras linhagens celulares coexistentes se diversificaram em células modernas".[100] Os dados sugerem que os vírus se originaram de células antigas que coexistiram com os ancestrais das células modernas. Essas células antigas provavelmente continham genomas de RNA segmentados.[97][101]
Um modelo computacional (2015) mostrou que os capsídeos de vírus podem ter se originado no mundo do RNA e servido como um meio de transferência horizontal entre comunidades replicadoras. Essas comunidades não poderiam sobreviver se o número de parasitas genéticos aumentasse, com certos genes sendo responsáveis pela formação dessas estruturas e aqueles que favoreceram a sobrevivência de comunidades autorreplicantes.[102] O deslocamento desses genes ancestrais entre organismos celulares pode favorecer o surgimento de novos vírus durante a evolução.[103] Os vírus retêm um módulo de replicação herdado do estágio pré-biótico, pois ele está ausente nas células.[103] Então, isso é evidência de que os vírus podem se originar do mundo do RNA e também podem surgir diversas vezes na evolução por meio de escape genético nas células.[103]
Encapsulamento sem membrana
Gotas de poliéster
Tony Jia e Kuhan Chandru propuseram gotículas de poliéster sem membrana de formação espontânea na celularização inicial antes da inovação das vesículas lipídicas. A função da proteína dentro e a função do RNA na presença de certas gotículas de poliéster mostraram-se preservadas dentro das gotículas. As gotículas têm capacidade de andaime, permitindo que os lipídios se reúnam ao redor delas; isso pode ter evitado o vazamento de materiais genéticos.[104][105][106]
Microesferas proteinóides
Fox observou nos anos 1960 que os proteinóides poderiam formar estruturas semelhantes a células denominadas "microesferas proteinóides".[74] Os aminoácidos se combinaram para formar proteinoides, que formaram pequenos glóbulos. Não eram células; seus aglomerados e cadeias eram reminiscentes de cianobactérias, mas não continham ácidos nucleicos funcionais ou outras informações codificadas. Colin Pittendrigh afirmou em 1967 que "os laboratórios criarão uma célula viva dentro de dez anos", uma observação que refletia a típica ingenuidade contemporânea sobre a complexidade das estruturas celulares.[107]
Protocélula Jeewanu
Outro modelo de protocélula é o Jeewanu. Sintetizado pela primeira vez em 1963 a partir de minerais simples e compostos orgânicos básicos, expostos à luz solar, é relatado que possui algumas capacidades metabólicas, a presença de uma membrana semipermeável, aminoácidos, fosfolipídios, carboidratos e moléculas como o RNA.[108][109] No entanto, a natureza e as propriedades do Jeewanu ainda precisam ser esclarecidas. Interações eletrostáticas induzidas por peptídeos hidrofóbicos curtos, carregados positivamente, contendo 7 aminoácidos de comprimento ou menos podem anexar RNA a uma membrana de vesícula, a membrana celular básica.[110]
Mundo de RNA-DNA
Em 2020, coevolução de uma mistura de RNA-DNA baseada em diamidofosfato foi proposta.[111][112][113] As misturas de sequências de RNA-DNA, chamada quimeras, têm afinidade fraca e formam estruturas duplex mais fracas.[114] Isto é vantajoso num cenário abiótico e estas quimeras demonstraram replicar RNA e DNA – superando o problema de inibição do "produto-modelo", em que uma fita de RNA ou DNA puro é incapaz de se replicar de forma não enzimática porque se liga muito fortemente aos seus parceiros.[115] Isso poderia levar a uma amplificação catalítica cruzada abiótica de RNA e DNA. Uma rede de reação química contínua em água e sob radiação de alta energia pode gerar precursores para o RNA inicial.[116]
Em 2022, experimentos de evolução de RNA auto-replicante mostrou como o RNA pode ter evoluído para diversas moléculas complexas em condições de mundo de RNA. O RNA evoluiu para uma "rede replicadora composta por cinco tipos de RNAs com interações diversas", como cooperação para replicação de outros membros (múltiplas linhagens coexistentes de hospedeiros e parasitas).[117]
Notas
- ↑ Ver também Lankenau, Dirk-Henner (2011). «Two RNA Worlds: Toward the Origin of Replication, Genes, Recombination and Repair». In: Egel, Richard; Lankenau, Dirk-Henner; Mulkidjanian, Armen Y. Origins of Life: The Primal Self-Organization. Heidelberg: Springer. pp. 225–286. ISBN 978-3-642-21624-4. OCLC 733245537. doi:10.1007/978-3-642-21625-1, interligando o conceito de “dois mundos de RNA” e Davidovich, Chen; Belousoff, Matthew; Bashan, Anat; Yonath, Ada (setembro 2009). «The evolving ribosome: from non-coded peptide bond formation to sophisticated translation machinery». Research in Microbiology. 160 (7): 487–492. PMID 19619641. doi:10.1016/j.resmic.2009.07.004

Referências
- ↑ Lane 2023, pp. 121-123, 147–153, 166–167.
- ↑ Lane 2023, pp. 147–148.
- ↑ Lane 2023, pp. 147–148, 152–153.
- ↑ Lane 2023, p. 148.
- ↑ Lane 2023, pp. 148–150.
- ↑ a b c Lane 2023, pp. 166–167.
- ↑ Blum, Harold F. (1957). «On the origin of self-replicating systems». In: Rudnick, D. Rhythmic and Synthetic Processes in Growth. [S.l.]: Princeton University Press. pp. 155–170
- ↑ a b Lathe, Richard (2004). «Fast tidal cycling and the origin of life». Icarus. 168 (1): 18–22. Bibcode:2004Icar..168...18L. doi:10.1016/j.icarus.2003.10.018
- ↑ Lathe, Richard (2005). «Tidal chain reaction and the origin of replicating biopolymers». International Journal of Astrobiology. 4 (1): 19–31. Bibcode:2005IJAsB...4...19L. doi:10.1017/S1473550405002314
- ↑ Varga, P.; Rybicki, K.; Denis, C. (2006). «Comment on the paper "Fast tidal cycling and the origin of life" by Richard Lathe». Icarus. 180 (1): 274–276. Bibcode:2006Icar..180..274V. doi:10.1016/j.icarus.2005.04.022
- ↑ Lathe, R. (2006). «Early tides: Response to Varga et al». Icarus. 180 (1): 277–280. Bibcode:2006Icar..180..277L. doi:10.1016/j.icarus.2005.08.019
- ↑ Flament, Nicolas; Coltice, Nicolas; Rey, Patrice F. (2008). «A case for late-Archaean continental emergence from thermal evolution models and hypsometry». Earth and Planetary Science Letters. 275 (3–4): 326–336. Bibcode:2008E&PSL.275..326F. doi:10.1016/j.epsl.2008.08.029
- ↑ Ignatov, Ignat (2011). «Entropy and Time in Living Organisms». Archiv Euromedica. 1&2: 74–75
- ↑ Ignatov, Ignat (2021). «Origin of Life and Living Matter in Hot Mineral Water and Properties of Polar Molecules in the Primary Hydrosphere and Hydrothermal Ponds». Uttar Pradesh Journal of Zoology. 42 (6): 37–52
- ↑ Derekova, Anna; Sjoholm, Carsten; Mandeva, Rossica; Kambourova, Margarita (2007). «Anoxybacillus rupiences sp. Nov. a novel thermophylic bacterium isolated from Rupi basin (Bulgaria)». Extremophiles. 11 (4): 577–583. PMID 17505776. doi:10.1007/s00792-007-0071-4
- ↑ Strunecký, Otakar; Kopejtka, Karel; Goecke, Franz; Tomasch, Juergen; Lukavský, Jaromir; Neori, Amir; Kahe, Silke; Pieper, Dietmar; Pilarski, Plamen; Kaftan, David; Koblížek, Michal (2019). «High diversity of thermophilic cyanobacteria in Rupite hot spring identified by microscopy, Cultivation, Single-cell PCR and Amplicon sequencing». Extremophiles. 23 (9): 35–48. PMID 30284641. doi:10.1007/s00792-018-1058-z
- ↑ Calvin 1969
- ↑ Schirber, Michael (1 de março de 2010). «First Fossil-Makers in Hot Water». Astrobiology Magazine. Consultado em 19 de junho de 2015. Cópia arquivada em 14 de julho de 2015
- ↑ Kurihara, Kensuke; Tamura, Mieko; Shohda, Koh-ichiroh; Toyota, Taro; Suzuki, Kentaro; Sugawara, Tadashi (outubro de 2011). «Self-Reproduction of supramolecular giant vesicles combined with the amplification of encapsulated DNA». Nature Chemistry. 3 (10): 775–781. Bibcode:2011NatCh...3..775K. PMID 21941249. doi:10.1038/nchem.1127
- ↑ Mulkidjanian, Armen Y.; Bychkov, Andrew Yu.; Dibrova, Daria V.; Galperin, Michael Y.; Koonin, Eugene V. (3 de abril de 2012). «Origin of first cells at terrestrial, anoxic geothermal fields». Proceedings of the National Academy of Sciences. 109 (14): E821-30. PMC 3325685
 . PMID 22331915. doi:10.1073/pnas.1117774109
. PMID 22331915. doi:10.1073/pnas.1117774109
- ↑ Deamer, David (10 de fevereiro de 2021). «Where Did Life Begin? Testing Ideas in Prebiotic Analogue Conditions». Life. 11 (2). 134 páginas. Bibcode:2021Life...11..134D. PMC 7916457
 . PMID 33578711. doi:10.3390/life11020134
. PMID 33578711. doi:10.3390/life11020134
- ↑ Deamer, David; Weber, Arthur L. (1 de fevereiro de 2010). «Bioenergetics and Life's Origins». Cold Spring Harbor Perspectives in Biology (em inglês). 2 (2): a004929. ISSN 1943-0264. PMC 2828274
 . PMID 20182625. doi:10.1101/cshperspect.a004929
. PMID 20182625. doi:10.1101/cshperspect.a004929
- ↑ Damer, Bruce; Deamer, David (13 de março de 2015). «Coupled Phases and Combinatorial Selection in Fluctuating Hydrothermal Pools: A Scenario to Guide Experimental Approaches to the Origin of Cellular Life». Life. 5 (1): 872–887. Bibcode:2015Life....5..872D. PMC 4390883
 . PMID 25780958. doi:10.3390/life5010872
. PMID 25780958. doi:10.3390/life5010872
- ↑ Damer, Bruce; Deamer, David (1 de abril de 2020). «The Hot Spring Hypothesis for an Origin of Life». Astrobiology. 20 (4): 429–452. Bibcode:2020AsBio..20..429D. PMC 7133448
 . PMID 31841362. doi:10.1089/ast.2019.2045
. PMID 31841362. doi:10.1089/ast.2019.2045
- ↑ Muchowska, Kamila B.; Varma, Sreejith J.; Chevallot-Beroux, Elodie; Lethuillier-Karl, Lucas; Li, Guang; Moran, Joseph (2 de outubro de 2017). «Metals promote sequences of the reverse Krebs cycle». Nature Ecology & Evolution (em inglês). 1 (11): 1716–1721. ISSN 2397-334X. PMC 5659384
 . PMID 28970480. doi:10.1038/s41559-017-0311-7
. PMID 28970480. doi:10.1038/s41559-017-0311-7
- ↑ Mayer, Christian; Schreiber, Ulrich; Dávila, María J.; Schmitz, Oliver J.; Bronja, Amela; Meyer, Martin; Klein, Julia; Meckelmann, Sven W. (24 de maio de 2018). «Molecular Evolution in a Peptide-Vesicle System». Life (em inglês). 8 (2). 16 páginas. Bibcode:2018Life....8...16M. ISSN 2075-1729. PMC 6027363
 . PMID 29795023. doi:10.3390/life8020016
. PMID 29795023. doi:10.3390/life8020016
- ↑ Damer, Bruce; Deamer, David (13 de março de 2015). «Coupled Phases and Combinatorial Selection in Fluctuating Hydrothermal Pools: A Scenario to Guide Experimental Approaches to the Origin of Cellular Life». Life (em inglês). 5 (1): 872–887. Bibcode:2015Life....5..872D. ISSN 2075-1729. PMC 4390883
 . PMID 25780958. doi:10.3390/life5010872
. PMID 25780958. doi:10.3390/life5010872
- ↑ Martin, William F.; Sousa, Filipa L.; Lane, Nick (6 de junho de 2014). «Energy at life's origin». Science. 344 (6188): 1092–1093. Bibcode:2014Sci...344.1092M. ISSN 0036-8075. PMID 24904143. doi:10.1126/science.1251653
- ↑ a b María, Colín-García; Alejandro, Heredia; Guadalupe, Cordero; Camprubí, Antoni; Negrón-Mendoza, Alicia; Ortega-Gutiérrez, Fernando; Beraldi, Hugo; Ramos-Bernal, Sergio (2016). «Hydrothermal vents and prebiotic chemistry: a review» (em inglês). Boletín de la Sociedad Geológica Mexicana. Consultado em 5 de novembro de 2022
- ↑ «Origin of life: Chemistry of seabed's hot vents could explain emergence of life». ScienceDaily. Consultado em 1 de novembro de 2022
- ↑ West, Timothy; Sojo, Victor; Pomiankowski, Andrew; Lane, Nick (5 de dezembro de 2017). «The origin of heredity in protocells». Philosophical Transactions of the Royal Society B: Biological Sciences (em inglês). 372 (1735). 20160419 páginas. ISSN 0962-8436. PMC 5665807
 . PMID 29061892. doi:10.1098/rstb.2016.0419
. PMID 29061892. doi:10.1098/rstb.2016.0419
- ↑ Whicher, Alexandra; Camprubi, Eloi; Pinna, Silvana; Herschy, Barry; Lane, Nick (1 de junho de 2018). «Acetyl Phosphate as a Primordial Energy Currency at the Origin of Life». Origins of Life and Evolution of Biospheres (em inglês). 48 (2): 159–179. Bibcode:2018OLEB...48..159W. ISSN 1573-0875. PMC 6061221
 . PMID 29502283. doi:10.1007/s11084-018-9555-8
. PMID 29502283. doi:10.1007/s11084-018-9555-8
- ↑ Lane, Nick; Martin, William F. (21 de dezembro de 2012). «The Origin of Membrane Bioenergetics». Cell (em inglês). 151 (7): 1406–1416. ISSN 0092-8674. PMID 23260134. doi:10.1016/j.cell.2012.11.050

- ↑ Baaske, Philipp; Weinert, Franz M.; Duhr, Stefan; Lemke, Kono H.; Russell, Michael J.; Braun, Dieter (29 de maio de 2007). «Extreme accumulation of nucleotides in simulated hydrothermal pore systems». Proceedings of the National Academy of Sciences (em inglês). 104 (22): 9346–9351. ISSN 0027-8424. PMC 1890497
 . PMID 17494767. doi:10.1073/pnas.0609592104
. PMID 17494767. doi:10.1073/pnas.0609592104
- ↑ Martin, William; Russell, Michael J (29 de janeiro de 2003). «On the origins of cells: a hypothesis for the evolutionary transitions from abiotic geochemistry to chemoautotrophic prokaryotes, and from prokaryotes to nucleated cells.». Philosophical Transactions of the Royal Society B: Biological Sciences. 358 (1429): 59–85. ISSN 0962-8436. PMC 1693102
 . PMID 12594918. doi:10.1098/rstb.2002.1183
. PMID 12594918. doi:10.1098/rstb.2002.1183
- ↑ Dodd, Matthew S; Papineau, Dominic; Grenne, Tor; Slack, John F; Rittner, Martin; Pirajno, Franco; O'Neil, Jonathan; Little, Crispin T S (1 de março de 2017). «Evidence for early life in Earth's oldest hydrothermal vent precipitates». Nature. 543 (7643): 60–64. Bibcode:2017Natur.543...60D. ISSN 1476-4687. PMID 28252057. doi:10.1038/nature21377

- ↑ a b c d Keller, Markus A; Turchyn, Alexandra V; Ralser, Markus (25 de abril de 2014). «Non-enzymatic glycolysis and pentose phosphate pathway-like reactions in a plausible Archean ocean». Molecular Systems Biology. 10 (4). 725 páginas. ISSN 1744-4292. PMC 4023395
 . PMID 24771084. doi:10.1002/msb.20145228
. PMID 24771084. doi:10.1002/msb.20145228
- ↑ Yi, Jing; Kaur, Harpreet; Kazöne, Wahnyalo; Rauscher, Sophia A.; Gravillier, Louis-Albin; Muchowska, Kamila B.; Moran, Joseph (7 de junho de 2022). «A Nonenzymatic Analog of Pyrimidine Nucleobase Biosynthesis». Angewandte Chemie International Edition (em inglês). 61 (23): e202117211. ISSN 1433-7851. PMC 9325535
 . PMID 35304939. doi:10.1002/anie.202117211
. PMID 35304939. doi:10.1002/anie.202117211
- ↑ a b Harrison, Stuart A.; Palmeira, Raquel Nunes; Halpern, Aaron; Lane, Nick (1 de novembro de 2022). «A biophysical basis for the emergence of the genetic code in protocells». Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1863 (8). 148597 páginas. ISSN 0005-2728. PMID 35868450. doi:10.1016/j.bbabio.2022.148597

- ↑ Akouche, Mariame; Jaber, Maguy; Maurel, Marie-Christine; Lambert, Jean-Francois; Georgelin, Thomas (26 de junho de 2017). «Phosphoribosyl Pyrophosphate: A Molecular Vestige of the Origin of Life on Minerals». Angewandte Chemie International Edition (em inglês). 56 (27): 7920–7923. PMID 28558156. doi:10.1002/anie.201702633
- ↑ McCollom, Thomas M.; Ritter, Gilles; Simoneit, Bernd R. T. (1 de março de 1999). «Lipid Synthesis Under Hydrothermal Conditions by Fischer- Tropsch-Type Reactions». Origins of Life and Evolution of the Biosphere (em inglês). 29 (2): 153–166. Bibcode:1999OLEB...29..153M. ISSN 1573-0875. PMID 10227201. doi:10.1023/A:1006592502746
- ↑ Jordan, Sean F.; Nee, Eloise; Lane, Nick (6 de dezembro de 2019). «Isoprenoids enhance the stability of fatty acid membranes at the emergence of life potentially leading to an early lipid divide». Interface Focus (em inglês). 9 (6). 20190067 páginas. ISSN 2042-8898. PMC 6802135
 . PMID 31641436. doi:10.1098/rsfs.2019.0067
. PMID 31641436. doi:10.1098/rsfs.2019.0067
- ↑ Hoffmann, Geoffrey William (24 de dezembro de 2016). «A network theory of the origin of life». bioRxiv. doi:10.1101/096701
- ↑ Gold, Thomas (1992). «The Deep, Hot Biosphere». Proceedings of the National Academy of Sciences. 89 (13): 6045–6049. Bibcode:1992PNAS...89.6045G. PMC 49434
 . PMID 1631089. doi:10.1073/pnas.89.13.6045
. PMID 1631089. doi:10.1073/pnas.89.13.6045
- ↑ Dartnell, Lewis (12 de janeiro de 2008). «Did life begin on a radioactive beach?». New Scientist. 2638. 8 páginas. Consultado em 26 de junho de 2015. Cópia arquivada em 27 de junho de 2015
- ↑ Adam, Zachary (2007). «Actinides and Life's Origins». Astrobiology. 7 (6): 852–872. Bibcode:2007AsBio...7..852A. PMID 18163867. doi:10.1089/ast.2006.0066
- ↑ Parnell, John (dezembro de 2004). «Mineral Radioactivity in Sands as a Mechanism for Fixation of Organic Carbon on the Early Earth». Origins of Life and Evolution of Biospheres. 34 (6): 533–547. Bibcode:2004OLEB...34..533P. CiteSeerX 10.1.1.456.8955
 . PMID 15570707. doi:10.1023/B:ORIG.0000043132.23966.a1
. PMID 15570707. doi:10.1023/B:ORIG.0000043132.23966.a1
- ↑ Eigen, M.; Schuster, P. (1979). The Hypercycle: A Principle of Natural Self-Organization. Berlin; New York: Springer-Verlag. ISBN 978-0-387-09293-5. LCCN 79001315. OCLC 4665354
- ↑ Yue-Ching Ho, Eugene (Julho–setembro de 1990). «Evolutionary Epistemology and Sir Karl Popper's Latest Intellectual Interest: A First-Hand Report». Intellectus. 15: 1–3. OCLC 26878740. Cópia arquivada em 11 março 2012.
Popper, sendo "velho demais para trabalhar sozinho", como ele nos contou durante nossa visita em julho, está colaborando com um bioquímico alemão, Günther Wächtershäuser, na teoria da origem da vida.
- ↑ Popper, Karl R. (29 março 1990). «Pyrite and the origin of life». Nature. 344 (6265). 387 páginas. Bibcode:1990Natur.344..387P. doi:10.1038/344387a0

- ↑ Huber, Claudia; Wächtershäuser, Günter (31 julho 1998). «Peptides by Activation of Amino Acids with CO on (Ni,Fe)S Surfaces: Implications for the Origin of Life». Science. 281 (5377): 670–672. Bibcode:1998Sci...281..670H. PMID 9685253. doi:10.1126/science.281.5377.670
- ↑ Lane, Nick (2009). Life Ascending: The 10 Great Inventions of Evolution
 1st American ed. New York: W.W. Norton & Company. ISBN 978-0-393-06596-1. OCLC 286488326
1st American ed. New York: W.W. Norton & Company. ISBN 978-0-393-06596-1. OCLC 286488326
- ↑ Adamala, Katarzyna; Szostak, Jack W. (29 novembro 2013). «Nonenzymatic Template-Directed RNA Synthesis Inside Model Protocells». Science. 342 (6162): 1098–1100. Bibcode:2013Sci...342.1098A. PMC 4104020
 . PMID 24288333. doi:10.1126/science.1241888
. PMID 24288333. doi:10.1126/science.1241888
- ↑ Musser, George (23 setembro 2011). «How Life Arose on Earth, and How a Singularity Might Bring It Down». Observations. Consultado em 17 junho 2015. Arquivado do original (Blog) em 17 junho 2015
- ↑ Carroll, Sean (10 março 2010). «Free Energy and the Meaning of Life». Cosmic Variance. Discover. Consultado em 17 junho 2015. Arquivado do original (Blog) em 14 julho 2015
- ↑ England, Jeremy L. (28 setembro 2013). «Statistical physics of self-replication» (PDF). Journal of Chemical Physics. 139 (12). 121923 páginas. Bibcode:2013JChPh.139l1923E. PMID 24089735. arXiv:1209.1179
 . doi:10.1063/1.4818538. hdl:1721.1/90392. Arquivado do original (PDF) em 4 junho 2015
. doi:10.1063/1.4818538. hdl:1721.1/90392. Arquivado do original (PDF) em 4 junho 2015
- ↑ Fox, Ronald F. (dezembro 1993). «Review of Stuart Kauffman, The Origins of Order: Self-Organization and Selection in Evolution». Biophysical Journal. 65 (6): 2698–2699. Bibcode:1993BpJ....65.2698F. PMC 1226010
 . doi:10.1016/s0006-3495(93)81321-3
. doi:10.1016/s0006-3495(93)81321-3
- ↑ Orgel, Leslie E. (7 novembro 2000). «Self-organizing biochemical cycles». PNAS. 97 (23): 12503–12507. Bibcode:2000PNAS...9712503O. PMC 18793
 . PMID 11058157. doi:10.1073/pnas.220406697
. PMID 11058157. doi:10.1073/pnas.220406697
- ↑ Chandru, Kuhan; Gilbert, Alexis; Butch, Christopher; Aono, Masashi; Cleaves, Henderson James II (21 julho 2016). «The Abiotic Chemistry of Thiolated Acetate Derivatives and the Origin of Life». Scientific Reports. 6 (29883). 29883 páginas. Bibcode:2016NatSR...629883C. PMC 4956751
 . PMID 27443234. doi:10.1038/srep29883
. PMID 27443234. doi:10.1038/srep29883
- ↑ Vallee, Yannick; Shalayel, Ibrahim; Ly, Kieu-Dung; Rao, K. V. Raghavendra; Paëpe, Gael De; Märker, Katharina; Milet, Anne (8 novembro 2017). «At the very beginning of life on Earth: the thiol-rich peptide (TRP) world hypothesis». The International Journal of Developmental Biology. 61 (8–9): 471–478. PMID 29139533. doi:10.1387/ijdb.170028yv
 . Consultado em 16 abril 2018. Cópia arquivada em 27 janeiro 2023
. Consultado em 16 abril 2018. Cópia arquivada em 27 janeiro 2023
- ↑ Preiner, Martina; Asche, Silke; Becker, Sidney; et al. (26 fevereiro 2020). «The Future of Origin of Life Research: Bridging Decades-Old Divisions». Life. 10 (3). 20 páginas. Bibcode:2020Life...10...20P. ISSN 2075-1729. PMC 7151616
 . PMID 32110893. doi:10.3390/life10030020
. PMID 32110893. doi:10.3390/life10030020
- ↑ Mulkidjanian, Armen Y. (24 agosto 2009). «On the origin of life in the zinc world: 1. Photosynthesizing, porous edifices built of hydrothermally precipitated zinc sulfide as cradles of life on Earth». Biology Direct. 4. 26 páginas. PMC 3152778
 . PMID 19703272. doi:10.1186/1745-6150-4-26
. PMID 19703272. doi:10.1186/1745-6150-4-26
- ↑ Wächtershäuser, Günter (dezembro 1988). «Before Enzymes and Templates: Theory of Surface Metabolism». Microbiological Reviews. 52 (4): 452–484. PMC 373159
 . PMID 3070320. doi:10.1128/MMBR.52.4.452-484.1988
. PMID 3070320. doi:10.1128/MMBR.52.4.452-484.1988
- ↑ Mulkidjanian, Armen Y.; Galperin, Michael Y. (24 agosto 2009). «On the origin of life in the zinc world. 2. Validation of the hypothesis on the photosynthesizing zinc sulfide edifices as cradles of life on Earth». Biology Direct. 4. 27 páginas. PMC 2749021
 . PMID 19703275. doi:10.1186/1745-6150-4-27
. PMID 19703275. doi:10.1186/1745-6150-4-27
- ↑ Macallum, A. B. (1 abril 1926). «The Paleochemistry of the body fluids and tissues». Physiological Reviews. 6 (2): 316–357. doi:10.1152/physrev.1926.6.2.316
- ↑ Mulkidjanian, Armen Y.; Bychkov, Andrew Yu.; Dibrova, Daria V.; Galperin, Michael Y.; Koonin, Eugene V. (3 de abril de 2012). «Origin of first cells at terrestrial, anoxic geothermal fields». Proceedings of the National Academy of Sciences. 109 (14): E821-30. Bibcode:2012PNAS..109E.821M. PMC 3325685
 . PMID 22331915. doi:10.1073/pnas.1117774109
. PMID 22331915. doi:10.1073/pnas.1117774109
- ↑ Cairns-Smith, Graham (2 setembro 1982). Genetic Takeover and the Mineral Origins of Life. Cambridge: Cambridge University Press. ISBN 0-521-23312-7. OCLC 7875600
- ↑ Dawkins, Richard (1996). The Blind Watchmaker Reissue with a new introduction ed. New York: W.W. Norton & Company. pp. 148–161. ISBN 978-0-393-31570-7. OCLC 35648431
- ↑ Huang, Wenhua; Ferris, James P. (12 julho 2006). «One-Step, Regioselective Synthesis of up to 50-mers of RNA Oligomers by Montmorillonite Catalysis». Journal of the American Chemical Society. 128 (27): 8914–8919. PMID 16819887. doi:10.1021/ja061782k
- ↑ Subramaniam, Anand Bala; Wan, Jiandi; Gopinath, Arvind; Stone, Howard A. (2011). «Semi-permeable vesicles composed of natural clay». Soft Matter. 7 (6): 2600–2612. Bibcode:2011SMat....7.2600S. arXiv:1011.4711
 . doi:10.1039/c0sm01354d
. doi:10.1039/c0sm01354d
- ↑ Hartman, Hyman (1998). «Photosynthesis and the Origin of Life». Origins of Life and Evolution of Biospheres. 28 (4–6): 515–521. Bibcode:1998OLEB...28..515H. PMID 11536891. doi:10.1023/A:1006548904157
- ↑ Davies, Paul (dezembro 2007). «Are Aliens Among Us?» (PDF). Scientific American. 297 (6): 62–69. Bibcode:2007SciAm.297f..62D. doi:10.1038/scientificamerican1207-62. Consultado em 16 julho 2015. Cópia arquivada (PDF) em 4 março 2016.
…se a vida realmente surge prontamente sob condições terrestres, então talvez ela tenha se formado muitas vezes em nosso planeta natal. Para perseguir essa possibilidade, desertos, lagos e outros ambientes extremos ou isolados foram pesquisados em busca de evidências de formas de vida "alienígenas" — organismos que difeririam fundamentalmente de organismos conhecidos porque surgiram independentemente.
zero width space character character in|citação=at position 246 (ajuda) - ↑ Senthilingam, Meera (25 abril 2014). «Metabolism May Have Started in Early Oceans Before the Origin of Life». Wellcome Trust. Consultado em 16 junho 2015. Cópia arquivada em 17 junho 2015
- ↑ a b Walsh, J. Bruce. «Part 4: Experimental studies of the origins of life». Origins of life (Lecture notes). Tucson, AZ: University of Arizona. Consultado em 8 junho 2015. Cópia arquivada em 13 de janeiro de 2008
- ↑ Maury, C. P. (2009). «Self-propagating beta-sheet polypeptide structures as prebiotic informational entities:The amyloid world». Origins of Life and Evolution of Biospheres. 39 (2): 141–150. PMID 19301141. doi:10.1007/s11084-009-9165-6
- ↑ Maury, C. P. (2015). «Origin of Life. Primordial genetics: Information transfer in a pre-RNA world based on self-replicating beta-sheet amyloid conformers». Journal of Theoretical Biology. 382: 292–297. Bibcode:2015JThBi.382..292M. PMID 26196585. doi:10.1016/j.jtbi.2015.07.008

- ↑ Nanda, J.; Rubinov, B.; Ivnitski, D.; et al. (2017). «Emergence of native peptide sequences in prebiotic replication networks». Nature Communications. 8 (1). 343 páginas. Bibcode:2017NatCo...8..434N. PMC 5585222
 . PMID 28874657. doi:10.1038/s41467-017-00463-1
. PMID 28874657. doi:10.1038/s41467-017-00463-1
- ↑ Rout, S. K.; Friedmann, M. P.; Riek, R.; Greenwald, J. (2018). «A prebiotic templated-directed synthesis based on amyloids». Nature Communications. 9 (1): 234–242. PMC 5770463
 . PMID 29339755. doi:10.1038/s41467-017-02742-3
. PMID 29339755. doi:10.1038/s41467-017-02742-3
- ↑ Muller, Anthonie W. J. (7 agosto 1985). «Thermosynthesis by biomembranes: Energy gain from cyclic temperature changes». Journal of Theoretical Biology. 115 (3): 429–453. Bibcode:1985JThBi.115..429M. PMID 3162066. doi:10.1016/S0022-5193(85)80202-2
- ↑ Muller, Anthonie W. J. (1995). «Were the first organisms heat engines? A new model for biogenesis and the early evolution of biological energy conversion». Progress in Biophysics and Molecular Biology. 63 (2): 193–231. PMID 7542789. doi:10.1016/0079-6107(95)00004-7

- ↑ Muller, Anthonie W. J.; Schulze-Makuch, Dirk (1 abril 2006). «Sorption heat engines: Simple inanimate negative entropy generators». Physica A: Statistical Mechanics and its Applications. 362 (2): 369–381. Bibcode:2006PhyA..362..369M. arXiv:physics/0507173
 . doi:10.1016/j.physa.2005.12.003
. doi:10.1016/j.physa.2005.12.003
- ↑ Orgel, Leslie E. (1987). «Evolution of the Genetic Apparatus: A Review». Evolution of Catalytic Function. Col: Cold Spring Harbor Symposia on Quantitative Biology. 52. Cold Spring Harbor, NY: Cold Spring Harbor Laboratory Press. pp. 9–16. ISBN 978-0-87969-054-0. OCLC 19850881. PMID 2456886. doi:10.1101/SQB.1987.052.01.004 "Proceedings of a symposium held at Cold Spring Harbor Laboratory in 1987" (Anais de um simpósio realizado no Cold Spring Harbor Laboratory em 1987)
- ↑ Orgel, Leslie E. (17 novembro 2000). «A Simpler Nucleic Acid». Science. 290 (5495): 1306–1307. PMID 11185405. doi:10.1126/science.290.5495.1306
- ↑ Nelson, Kevin E.; Levy, Matthew; Miller, Stanley L. (11 abril 2000). «Peptide nucleic acids rather than RNA may have been the first genetic molecule». PNAS. 97 (8): 3868–3871. Bibcode:2000PNAS...97.3868N. PMC 18108
 . PMID 10760258. doi:10.1073/pnas.97.8.3868
. PMID 10760258. doi:10.1073/pnas.97.8.3868
- ↑ Larralde, Rosa; Robertson, Michael P.; Miller, Stanley L. (29 agosto 1995). «Rates of Decomposition of Ribose and Other Sugars: Implications for Chemical Evolution». PNAS. 92 (18): 8158–8160. Bibcode:1995PNAS...92.8158L. PMC 41115
 . PMID 7667262. doi:10.1073/pnas.92.18.8158
. PMID 7667262. doi:10.1073/pnas.92.18.8158
- ↑ Lindahl, Tomas (22 abril 1993). «Instability and decay of the primary structure of DNA». Nature. 362 (6422): 709–715. Bibcode:1993Natur.362..709L. PMID 8469282. doi:10.1038/362709a0
- ↑ Anastasi, Carole; Crowe, Michael A.; Powner, Matthew W.; Sutherland, John D. (18 setembro 2006). «Direct Assembly of Nucleoside Precursors from Two- and Three-Carbon Units». Angewandte Chemie International Edition. 45 (37): 6176–6179. PMID 16917794. doi:10.1002/anie.200601267
- ↑ Powner, Matthew W.; Sutherland, John D. (13 outubro 2008). «Potentially Prebiotic Synthesis of Pyrimidine β-D-Ribonucleotides by Photoanomerization/Hydrolysis of α-D-Cytidine-2'-Phosphate». ChemBioChem. 9 (15): 2386–2387. PMID 18798212. doi:10.1002/cbic.200800391
- ↑ Powner, Matthew W.; Gerland, Béatrice; Sutherland, John D. (14 maio 2009). «Synthesis of activated pyrimidine ribonucleotides in prebiotically plausible conditions». Nature. 459 (7244): 239–242. Bibcode:2009Natur.459..239P. PMID 19444213. doi:10.1038/nature08013
- ↑ Paul, Natasha; Joyce, Gerald F. (dezembro 2004). «Minimal self-replicating systems». Current Opinion in Chemical Biology. 8 (6): 634–639. PMID 15556408. doi:10.1016/j.cbpa.2004.09.005
- ↑ Kauffman, Stuart (1993). The Origins of Order: Self-Organization and Selection in Evolution. New York: Oxford University Press. chapter 7. ISBN 978-0-19-507951-7. LCCN 91011148. OCLC 23253930
- ↑ Dawkins, Richard (2004). The Ancestor's Tale: A Pilgrimage to the Dawn of Evolution. Boston: Houghton Mifflin. ISBN 978-0-618-00583-3. LCCN 2004059864. OCLC 56617123
- ↑ Tjivikua, T.; Ballester, Pablo; Rebek, Julius Jr. (janeiro 1990). «Self-replicating system». Journal of the American Chemical Society. 112 (3): 1249–1250. doi:10.1021/ja00159a057
- ↑ a b Patel, Bhavesh H.; Percivalle, Claudia; Ritson, Dougal J.; Duffy, Colm D.; Sutherland, John D. (abril 2015). «Common origins of RNA, protein and lipid precursors in a cyanosulfidic protometabolism». Nature Chemistry. 7 (4): 301–307. Bibcode:2015NatCh...7..301P. PMC 4568310
 . PMID 25803468. doi:10.1038/nchem.2202
. PMID 25803468. doi:10.1038/nchem.2202
- ↑ Patel et al. 2015, p. 302
- ↑ Wolos, Agnieszka; et al. (25 setembro 2020). «Synthetic connectivity, emergence, and self-regeneration in the network of prebiotic chemistry». Science. 369 (6511): eaaw1955. PMID 32973002. doi:10.1126/science.aaw1955. Consultado em 3 outubro 2020
- ↑ a b c Yates, Diana (25 setembro 2015). «Study adds to evidence that viruses are alive» (Nota de imprensa). Champaign, IL: University of Illinois at Urbana–Champaign. Consultado em 20 de outubro de 2015. Cópia arquivada em 19 novembro 2015
- ↑ Janjic, Aleksandar (2018). «The Need for Including Virus Detection Methods in Future Mars Missions». Astrobiology. 18 (12): 1611–1614. Bibcode:2018AsBio..18.1611J. doi:10.1089/ast.2018.1851
- ↑ Katzourakis, A. (2013). «Paleovirology: Inferring viral evolution from host genome sequence data». Philosophical Transactions of the Royal Society B: Biological Sciences. 368 (1626). 20120493 páginas. PMC 3758182
 . PMID 23938747. doi:10.1098/rstb.2012.0493
. PMID 23938747. doi:10.1098/rstb.2012.0493
- ↑ Arshan, Nasir; Caetano-Anollés, Gustavo (25 setembro 2015). «A phylogenomic data-driven exploration of viral origins and evolution». Science Advances. 1 (8): e1500527. Bibcode:2015SciA....1E0527N. PMC 4643759
 . PMID 26601271. doi:10.1126/sciadv.1500527
. PMID 26601271. doi:10.1126/sciadv.1500527
- ↑ Nasir, Arshan; Naeem, Aisha; Jawad Khan, Muhammad; et al. (dezembro 2011). «Annotation of Protein Domains Reveals Remarkable Conservation in the Functional Make up of Proteomes Across Superkingdoms». Genes. 2 (4): 869–911. PMC 3927607
 . PMID 24710297. doi:10.3390/genes2040869
. PMID 24710297. doi:10.3390/genes2040869
- ↑ Jalasvuori, M.; Mattila, S.; Hoikkala, V. (2015). «Chasing the Origin of Viruses: Capsid-Forming Genes as a Life-Saving Preadaptation within a Community of Early Replicators». PLOS ONE. 10 (5): e0126094. Bibcode:2015PLoSO..1026094J. PMC 4425637
 . PMID 25955384. doi:10.1371/journal.pone.0126094
. PMID 25955384. doi:10.1371/journal.pone.0126094
- ↑ a b c Krupovic, M.; Dolja, V.V.; Koonin, E.V. (julho 2019). «Origin of viruses: primordial replicators recruiting capsids from hosts» (PDF). Nature Reviews. Microbiology. 17 (7): 449–458. PMID 31142823. doi:10.1038/s41579-019-0205-6
- ↑ Jia, Tony Z.; Chandru, Kuhan; Hongo, Yayoi; Afrin, Rehana; Usui, Tomohiro; Myojo, Kunihiro; Cleaves, H. James (22 julho 2019). «Membraneless polyester microdroplets as primordial compartments at the origins of life». Proceedings of the National Academy of Sciences. 116 (32): 15830–15835. Bibcode:2019PNAS..11615830J. PMC 6690027
 . PMID 31332006. doi:10.1073/pnas.1902336116
. PMID 31332006. doi:10.1073/pnas.1902336116
- ↑ Chandru, Kuhan; Mamajanov, Irena; Cleaves, H. James; Jia, Tony Z. (janeiro 2020). «Polyesters as a Model System for Building Primitive Biologies from Non-Biological Prebiotic Chemistry». Life. 10 (1). 6 páginas. Bibcode:2020Life...10....6C. PMC 7175156
 . PMID 31963928. doi:10.3390/life10010006
. PMID 31963928. doi:10.3390/life10010006
- ↑ Guttenberg, Nicholas; Virgo, Nathaniel; Chandru, Kuhan; Scharf, Caleb; Mamajanov, Irena (13 novembro 2017). «Bulk measurements of messy chemistries are needed for a theory of the origins of life». Philosophical Transactions of the Royal Society A: Mathematical, Physical and Engineering Sciences. 375 (2109). 20160347 páginas. Bibcode:2017RSPTA.37560347G. PMC 5686404
 . PMID 29133446. doi:10.1098/rsta.2016.0347
. PMID 29133446. doi:10.1098/rsta.2016.0347
- ↑ Woodward, Robert J., ed. (1969). Our Amazing World of Nature: Its Marvels & Mysteries. Pleasantville, NY: Reader's Digest Association. 287 páginas. ISBN 978-0-340-13000-1. LCCN 69010418
- ↑ Grote, Mathias (setembro 2011). «Jeewanu, or the 'particles of life'» (PDF). Journal of Biosciences. 36 (4): 563–570. PMID 21857103. doi:10.1007/s12038-011-9087-0. Consultado em 15 de junho de 2015. Cópia arquivada (PDF) em 24 setembro 2015
- ↑ Gupta, V.K.; Rai, R.K. (agosto 2013). «Histochemical localisation of RNA-like material in photochemically formed self-sustaining, abiogenic supramolecular assemblies 'Jeewanu'». International Research Journal of Science & Engineering. 1 (1): 1–4. Consultado em 15 de junho de 2015. Cópia arquivada em 28 junho 2017
- ↑ Kamat, Neha P.; Tobé, Sylvia; Hill, Ian T.; Szostak, Jack W. (29 julho 2015). «Electrostatic Localization of RNA to Protocell Membranes by Cationic Hydrophobic Peptides». Angewandte Chemie International Edition. 54 (40): 11735–11739. PMC 4600236
 . PMID 26223820. doi:10.1002/anie.201505742
. PMID 26223820. doi:10.1002/anie.201505742
- ↑ Gibard, Clémentine; Bhowmik, Subhendu; Karki, Megha; Kim, Eun-Kyong; Krishnamurthy, Ramanarayanan (fevereiro 2018). «Phosphorylation, oligomerization and self-assembly in water under potential prebiotic conditions». Nature Chemistry. 10 (2): 212–217. ISSN 1755-4349. PMC 6295206
 . PMID 29359747. doi:10.1038/nchem.2878
. PMID 29359747. doi:10.1038/nchem.2878
- ↑ Gibard, Clémentine; Gorrell, Ian B.; Jiménez, Eddy I.; Kee, Terence P.; Pasek, Matthew A.; Krishnamurthy, Ramanarayanan (2019). «Geochemical Sources and Availability of Amidophosphates on the Early Earth». PMID 30989779. doi:10.1002/anie.201903808
- ↑ Krishnamurthy, Ramanarayanan; Jiménez, Eddy I.; Gibard, Clémentine (15 dezembro 2020). «Prebiotic Phosphorylation and Concomitant Oligomerization of Deoxynucleosides to form DNA». Angewandte Chemie. 60 (19): 10775–10783. PMID 33325148. doi:10.1002/anie.202015910
- ↑ Gavette, Jesse V.; Stoop, Matthias; Hud, Nicholas V.; Krishnamurthy, Ramanarayanan (2016). «RNA–DNA Chimeras in the Context of an RNA World Transition to an RNA/DNA World». Angewandte Chemie International Edition. 55 (42): 13204–13209. PMID 27650222. doi:10.1002/anie.201607919
- ↑ Bhowmik, Subhendu; Krishnamurthy, Ramanarayanan (novembro 2019). «The role of sugar-backbone heterogeneity and chimeras in the simultaneous emergence of RNA and DNA». Nature Chemistry. 11 (11): 1009–1018. Bibcode:2019NatCh..11.1009B. ISSN 1755-4349. PMC 6815252
 . PMID 31527850. doi:10.1038/s41557-019-0322-x
. PMID 31527850. doi:10.1038/s41557-019-0322-x
- ↑ Yi, Ruiqin; Tran, Quoc Phuong; Ali, Sarfaraz; Yoda, Isao; Adam, Zachary R.; Cleaves, H. James; Fahrenbach, Albert C. (16 junho 2020). «A continuous reaction network that produces RNA precursors». Proceedings of the National Academy of Sciences (em inglês). 117 (24): 13267–13274. Bibcode:2020PNAS..11713267Y. ISSN 0027-8424. PMC 7306801
 . PMID 32487725. doi:10.1073/pnas.1922139117
. PMID 32487725. doi:10.1073/pnas.1922139117
- ↑ Mizuuchi, Ryo; Furubayashi, Taro; Ichihashi, Norikazu (18 março 2022). «Evolutionary transition from a single RNA replicator to a multiple replicator network». Nature Communications. 13 (1). 1460 páginas. Bibcode:2022NatCo..13.1460M. PMC 8933500
 . PMID 35304447. doi:10.1038/s41467-022-29113-x
. PMID 35304447. doi:10.1038/s41467-022-29113-x
Fontes
- Calvin, Melvin (1969). Chemical Evolution: Molecular Evolution Towards the Origin of Living Systems on the Earth and Elsewhere. Oxford, UK: Clarendon Press. ISBN 978-0-19-855342-7. LCCN 70415289. OCLC 25220
- Lane, Nick (2023). Transformer: The Deep Chemistry of Life and Death. [S.l.]: Profile Books. ISBN 978-1-7881-6055-1