Dipeptídeo
Um dipeptídeo (ou dipéptido) é um composto orgânico derivado de dois aminoácidos. Os aminoácidos constituintes podem ser iguais ou diferentes. Quando diferentes, dois isômeros do dipeptídeo são possíveis, dependendo da sequência. Vários dipeptídeos são fisiologicamente importantes, e alguns são fisiológicos e comercialmente significativos. Um dipeptídeo bem conhecido é o aspartame, um adoçante artificial.[1]
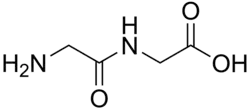
Dipeptídeos são sólidos brancos. Muitos são muito mais solúveis em água do que os aminoácidos originais.[1] Por exemplo, o dipeptídeo Ala-Gln tem a solubilidade de 586 g/L, mais de 10x a solubilidade de Gln (35 g/L). Dipeptídeos também podem apresentar diferentes estabilidades, e.g. com relação à hidrólise. Gln não resiste aos procedimentos de esterilização, enquanto este dipeptídeo não. Como os dipeptídeos são propensos à hidrólise, a alta solubilidade é explorada em infusões, i.e. para fornecer nutrição.[2]
Exemplos
Valor comercial
Cerca de seis dipeptídeos são de interesse comercial.[1]
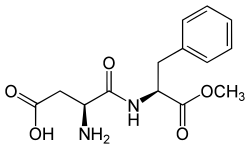
- Aspartame (N-L-α-aspartil-L-fenilalanina 1-metil éster) é um adoçante artificial.
- Carnosina (beta-alanil-L-histidina) e Anserina (beta-alanil-N-metil histidina) são altamente concentrados em músculo e tecidos cerebrais. São utilizados na medicina esportiva.
- Acetilcarnosina, prevenção de catarata
- Ala-Gln 3 Gly-Tyr, em infusão[2]
- Val-Tyr, antihipertensivo
Outros dipeptídeos
- Homoanserina (N-(4-aminobutiril)-L-histidina) é outro dipeptídeo identificado no cérebro e nos músculos de mamíferos.
- Difenilalanina é o bloco de construção mais estudado em nanotecnologia de peptídeos
- Quiotorfina (L-tirosil-L-arginina) é um dipeptídeo neuroactivo que desempenha um papel na regulação da dor no cérebro.
- ja (ou ofidina) (beta-alanil-N tau-metil histidina) foi identificado nos músculos de várias espécies de mamíferos (incluindo o homem), e as galinhas.
- Glorina (N-propionil-γ-L-glutamil-L-ornitina-δ-lac etil éster) é um dipeptídeo quimiotático para o bolor limoso Polysphondylium violaceum.
- Barettin (ciclo-[(6-bromo-8-en-triptofan)-arginina]) é um dipeptídeo cíclico da esponja marinha Geodia barretti.
- Pseudoprolina
- Dialanina é comumente usado como um modelo em dinâmica molecular.
- Xenortidas, isoladas da bactéria Xenorhabdus nematophila
Produção
Dipeptídeos sintéticos
Os dipeptídeos são produzidos pelo acoplamento de aminoácidos. O grupo amino de um aminoácido é tornado não nucleofílico (P em eq) e o grupo ácido carboxílico do segundo aminoácido é desativado como seu éster metílico. Os dois aminoácidos modificados são então combinados na presença de um agente de acoplamento, que facilita a formação da ligação amida.
- RCH(NHP)CO2H + R'CH(NH2)CO2CH3 → RCH(NHP)C(O)NH(CHR')CO2CH3 + H2O
Após essa reação de acoplamento, o grupo protetor da amina P e o éster são convertidos na amina livre e no ácido carboxílico, respectivamente.[3]
Para muitos aminoácidos, os grupos funcionais auxiliares são protegido. A condensação da amina e do ácido carboxílico para formar a ligação peptídica geralmente emprega agentes de acoplamento para ativar o ácido carboxílico.[4]
A síntese de peptídeos de azlactona de Bergmann é uma síntese orgânica clássica para a preparação de dipeptídeos.[1]
Biosíntese
Dipeptídeos são produzidos de polipeptídeos pela ação da enzima hidrolase dipeptidil peptidase.[5] As proteínas alimentares são digeridas em dipeptídeos e aminoácidos, sendo que os dipeptídeos são absorvidos mais rapidamente do que os aminoácidos, porque sua absorção envolve um mecanismo distinto. Os dipeptídeos ativam as células G encontradas no estômago para secretar gastrina.
Referências
- ↑ a b c d Yagasaki, M; Hashimoto, S (novembro 2008). «Synthesis and application of dipeptides; current status and perspectives». Applied Microbiology and Biotechnology. 81 (1): 13–22. PMID 18795289. doi:10.1007/s00253-008-1590-3
- ↑ a b Fürst, P; Pogan, K; Stehle, P (1997). «Glutamine dipeptides in clinical nutrition». Nutrition. 13 (7-8): 731–7. PMID 9263278. doi:10.1016/S0899-9007(97)83035-3
- ↑ Subirós-Funosas, AE; Albericio, F (2013). «Low-epimerization Peptide Bond Formation with Oxyma Pure: Preparation of Z-L-Phg-Val-OMe». Organic Syntheses. 90. 306 páginas. doi:10.15227/orgsyn.090.0306
- ↑ Suppo, JS; de Figueiredo, RM; Campagne, JM (2015). «Dipeptide Syntheses via Activated α-Aminoesters». Organic Syntheses. 92: 296–308. doi:10.15227/orgsyn.092.0296

- ↑ Steane, R. «Hydrolysis of a dipeptide». BioTopics. Consultado em 28 julho 2014