Suillellus luridus
Suillellus luridus
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Suillellus luridus (Schaeff.) Murrill (1909) | |||||||||||||||||
| Sinónimos[1][2] | |||||||||||||||||
| |||||||||||||||||
Suillellus luridus
| |
|---|---|
| Himênio poroso | |
| Píleo é convexo | |
| Lamela é adnata | |
| Estipe é nua | |
| A cor do esporo é marrom-oliváceo | |
| A relação ecológica é micorrízica | |
|
Comestibilidade: comestível
mas não recomendado |
Suillellus luridus (anteriormente Boletus luridus) é uma espécie de fungo da família Boletaceae, encontrado em florestas latifólia em solos calcários na Europa. Os basidiomas aparecem no verão e outono, podendo ser localmente abundantes. É um boleto robusto com um píleo marrom-oliva de até 20 cm de diâmetro, com poros pequenos laranja ou vermelhos na parte inferior (amarelos quando jovens). O estipe ocre robusto atinge de 8 a 14 cm de altura e de 1 a 3 cm de largura, apresentando uma rede vermelha. Como vários outros boletos de poros vermelhos, mancha-se de azul quando machucado ou cortado.
Embora comestível e saboroso quando cozido, pode causar desconforto gástrico se consumido cru. Também pode ser confundido com o venenoso Rubroboletus satanas; por isso, alguns guias recomendam evitar seu consumo. Quando ingerido com álcool, Suillellus luridus foi associado a reações adversas semelhantes às causadas pelo composto coprina, embora testes laboratoriais não tenham detectado coprina no fungo.
Descrita pela primeira vez em 1774, a espécie foi transferida para vários gêneros da família Boletaceae ao longo de sua história taxonômica, mantendo o nome original dado pelo botânico alemão Jacob Christian Schaeffer até ser transferida para o gênero Suillellus em 2014. Várias variedades, uma subespécie e uma forma foram descritas por micologistas europeus. Suillellus luridus é micorrízica, formando uma associação simbiótica com árvores latifólias, como carvalhos, castanheiros, bétulas e faias, e demonstrou ter um efeito de promoção de crescimento em coníferas em experimentos. Os cogumelos são altamente atrativos para insetos, frequentemente infestados, e várias espécies de dípteros foram registradas se alimentando deles. Análises químicas revelaram aspectos dos componentes do fungo, incluindo seus compostos voláteis de sabor, composições de ácidos graxos e aminoácidos, e a identidade dos compostos carotenoides responsáveis por sua cor.
Taxonomia e filogenia
Suillellus luridus foi descrita como Boletus luridus pelo botânico alemão Jacob Christian Schaeffer em 1774, em sua série sobre fungos da Baviera e do Palatinado, Fungorum qui in Bavaria et Palatinatu circa Ratisbonam nascuntur icones.[3] O epíteto específico vem do adjetivo latim luridus, que significa "pálido" ou "amarelado".[4] Boletus rubeolarius do botânico francês Pierre Bulliard, de 1791,[5] é um sinônimo heterotípico (baseado em um tipo diferente).[1] No ano seguinte, Johann Friedrich Gmelin o nomeou Boletus subvescus,[6] do latim sub ("quase" ou "sob")[7] e vescus ("comestível").[8] No entanto, este é um nomen nudum.[9] Vários sinônimos taxonômicos surgiram quando a espécie foi transferida para diferentes gêneros dentro da família Boletaceae por várias autoridades, incluindo Leccinum por Samuel Frederick Gray em 1821,[10] Tubiporus por Petter Karsten em 1881,[11] Dictyopus por Lucien Quélet em 1888,[12] e Suillellus por William Murrill em 1909.[1][13]

A variedade Boletus luridus var. erythropus, publicada como "beta" por Elias Magnus Fries em seu Systema Mycologicum de 1821,[14] é sinônima de Neoboletus luridiformis.[15] A variedade Boletus luridus var. rubriceps foi descrita originalmente na Espanha (como uma espécie de Tubiporus) por René Maire em 1937,[16] e posteriormente transferida formalmente para Boletus por Aurel Dermek em 1987.[17] Outras variedades de B. luridus incluem var. obscurus e var. rubromaculatus de Roman Schulz, publicados em 1924;[18] var. tenuipes de Josef Velenovský, de 1939, encontrada na República Tcheca;[19] e var. lupiniformis e var. queletiformis de Jean Blum, de 1969, descritas originalmente na França e na Espanha, respectivamente.[20] Boletus erythrentheron, originalmente descrito como uma espécie distinta por Jan Bezděk, foi recombinado como a variedade B. luridus var. erythrentheron por Albert Pilát e Dermek em 1979,[21] e finalmente como uma subespécie por Jiri Hlavácek em 1995.[22] Carmine Lavorato e Giampaolo Simonini definiram a forma primulicolor da Sardenha em 1997.[23] A variedade caucasicus de Rolf Singer, de 1947, posteriormente recombinada como uma espécie independente, Boletus caucasicus Singer ex. Alessio,[24] nunca foi validamente publicada e é um nomen nudum.[25] Boletus luridus f. sinensis, encontrado na província de Hainan, China, foi posteriormente elevado a espécie e transferido para outro gênero com o nome Neoboletus sinensis.[26]
Boletus luridus foi a espécie-tipo da seção Luridi do gênero Boletus, circunscrita por Fries em 1838.[27] Esta seção incluía tradicionalmente espécies com basidiomas médios a grandes, com estipes grossos e inchados, e poros minúsculos coloridos de vermelho, laranja ou, raramente, amarelo.[28] No entanto, investigações filogenéticas iniciais indicaram que Boletus é fortemente parafilético em sua delimitação tradicional. À medida que estudos posteriores resolveram relações filogenéticas e taxonômicas em maior detalhe, Boletus foi fragmentado e gêneros adicionais foram reconhecidos. Análises filogenéticas moleculares baseadas em sequências de DNA ribossômico por Manfred Binder e David Hibbett mostraram que B. luridus está relacionado a um grupo contendo B. torosus e B. luteocupreus (agora no gênero Imperator, I. torosus [en] e I. luteocupreus), com B. vermiculosus e Pulveroboletus ravenelii como parentes mais distantes.[29] Em outro estudo molecular de Mello e colegas,[30] B. luridus agrupou-se com Rubroboletus rhodoxanthus, enquanto análises genéticas adicionais em 2013 indicaram que B. luridus e alguns boletos de poros vermelhos fazem parte do clado dupainii (nomeado devido Rubroboletus dupainii), bastante distante do grupo central de Boletus edulis e seus parentes.[31] No entanto, análises mais refinadas baseadas em um maior número de sequências demonstraram que B. luridus e suas espécies aliadas formam um clado genérico distinto,[32] e desde 2014 o fungo foi colocado no gênero Suillellus.[33]
Descrição

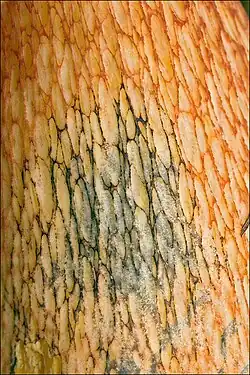
O basidioma é robusto e tem um píleo convexo almofadado, de cor amarelo-oliva a marrom-oliva, que pode atingir 20 cm de diâmetro.[34] A cor do píleo tende a escurecer com a idade, e regiões de vermelho, laranja, roxo, marrom ou verde-oliva podem estar presentes.[35] A superfície do píleo é finamente tomentosa (aveludada) no início, tornando-se mais lisa com a idade e viscosa em tempo úmido.[36] A superfície dos poros é inicialmente amarelo-laranja ou laranja, tornando-se laranja-avermelhada a às vezes vermelha, e mancha fortemente de azul quando machucada ou manipulada.[37][38] A superfície dos poros geralmente tem uma zona de cor mais clara cercando a margem, pois os poros tendem a escurecer a partir de seu ponto de fixação no estipe para fora.[35][39] Há 2 a 3 poros arredondados por milímetro, e os tubos têm de 1 a 2 cm de comprimento.[37] Os tubos são mais curtos ao redor da margem do píleo e próximos ao estipe, onde formam uma depressão circular. Inicialmente amarelo-pálidos, os tubos tornam-se amarelo-oliva e mancham de azul-esverdeado ao serem expostos ao ar.[35] Uma característica frequente é a presença de uma camada marrom-avermelhada entre os tubos e a carne (conhecida como linha de Bataille),[40] mas isso nem sempre está presente, e a carne sub-himenial pode ocasionalmente ser amarela ou cor de palha.[25] O estipe mede de 8 a 14 cm de altura e de 1 a 3 cm de largura, apresentando um padrão de reticulação alongada vermelho-laranja sobre um fundo mais claro amarelado, laranja ou ocre, frequentemente tornando-se mais escuro e vináceo em direção à base.[41][39] A carne é amarelada, às vezes com manchas vermelhas no píleo, mas quase sempre ruibarbo a vermelho-vináceo em direção à base do estipe, manchando de azul-escuro intenso quando machucada ou cortada. Há um leve odor azedo e o sabor é descrito como suave.[34][36] O micélio é de uma cor amarela incomum.[42]
A variedade queletiformis pode ser distinguida da forma principal pela descoloração avermelhada da base do estipe, tanto na superfície externa quanto na carne.[43] A variedade rubriceps tem um píleo vermelho-carmesim profundo, enquanto a var. lupiniformis tem píleo e poros amarelo-pálido ou ocre-suj, às vezes com tons rosados.[35]
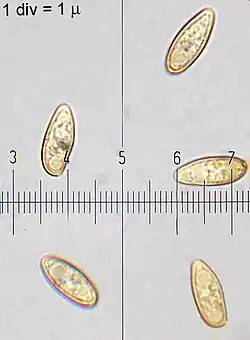
A esporada é oliva a marrom-olivácea. Sob o microscópio, os esporos são elípticos a fusiformes, medindo 11–15 μm de comprimento por 4,5–6,5 μm de largura, com um quociente médio de esporos de 2,2.[41][25] Os basídios (células portadoras de esporos) são claviformes, com quatro esporos, e medem 29,2–36,5 por 11,0–12,4 μm. Os cistídios nas laterais dos tubos (pleurocistídios) são fusiformes com o meio inchado e pescoços longos, medindo 33–48 por 7,3–13,5 μm; os queilocistídios (nas bordas dos poros) têm morfologia semelhante. A pileipellis é composta por hifas cilíndricas de 3,7–5,8 μm de largura, compactamente entrelaçadas, com as pontas hifais erguidas e dispostas em feixes. Em contraste, as hifas da carne do píleo são frouxamente entrelaçadas, cilíndricas e ramificadas, medindo 3,7–8,8 μm. As hifas não contêm fíbulas.[44]
Alguns testes químicos podem ajudar a identificar a espécie. Uma gota de hidróxido de potássio diluído na pileipellis mancha de vermelho-escuro a preto e amarelo-laranja na carne,[37] enquanto uma solução de sulfato ferroso torna a pileipellis amarela e depois verde-amarelada.[45] O reagente de Melzer torna a carne azul-escura, após o desbotamento da reação natural de azulamento quando ferida ou machucada.[37]
Espécies semelhantes
Suillellus mendax [en], descrita na Itália em 2014[25] e posteriormente confirmada em Chipre e na França,[46] é muito semelhante a S. luridus e encontrada sob as mesmas árvores hospedeiras. Produz basidiomas mais robustos com um píleo marcadamente tomentoso, tem uma reticulação menos pronunciada e frequentemente restrita à parte superior do estipe, e é encontrada principalmente em solos ácidos em vez de calcários. Microscopicamente, S. mendax tem esporos mais alongados, estreitamente fusiformes, medindo (12,4–)13,3–14,7(–15,5) por (4,5–)4,9–5,5(–5,7) μm, com um quociente de esporos maior de 2,7. Coleções do sul da Europa previamente classificadas como Boletus caucasicus com base em uma camada sub-himenial amarela (a linha de Bataille),[47] foram mostradas filogeneticamente como correspondendo a S. luridus ou S. mendax.[46] Como demonstrado por Vizzini e colegas,[25] o nome Boletus caucasicus foi publicado invalidamente (nomen nudum) e a linha de Bataille não é confiável para discriminar espécies no complexo Luridi, pois pode estar presente ou ausente em ambas S. luridus e S. mendax.
Outra espécie semelhante é Suillellus comptus, um boleto mediterrâneo com muitas características em comum com S. luridus e S. queletii.[48] Esta espécie incomum também é encontrada em solos calcários sob carvalhos, mas geralmente produz basidiomas mais esguios e de cores opacas, com uma reticulação rudimentar, incompleta ou, às vezes, completamente ausente, raramente se estendendo abaixo do ápice do estipe. Sob o microscópio, S. comptus tem esporos muito semelhantes a S. luridus, mas as hifas de sua pileipellis são mais frouxas e prostradas, correndo mais ou menos paralelas ao píleo.[38][25] Também no mesmo gênero, S. queletii compartilha com S. luridus uma base de estipe vinácea e carne que azuleia fortemente, mas carece completamente de reticulação no estipe.
O comestível Neoboletus luridiformis pode ser distinguido de S. luridus por seu píleo marrom escuro e ausência de reticulação no estipe; e cresce em solos arenosos associados a coníferas.[34] No gênero Rubroboletus, R. satanas também é encontrado em solos calcários, mas produz basidiomas maiores e mais robustos com um píleo pálido e reticulação de padrão diferente de S. luridus.[34][38] Sua carne não azuleia tão intensamente ao ser machucada ou cortada, enquanto cogumelos maduros frequentemente apresentam um odor de decomposição.[49] Outra espécie de poros vermelhos neste gênero, Rubroboletus rhodoxanthus, tem tons rosados característicos no píleo e uma reticulação muito densa, com padrão diferente. Quando cortada longitudinalmente, sua carne é amarelo-brilhante no estipe e azuleia apenas no píleo.[40][39]
Vários boletos extra-europeus compartilham uma aparência semelhante a S. luridus e foram fonte de confusão no passado. Suillellus hypocarycinus (encontrado na América do Norte) e Neoboletus subvelutipes (reportado na América do Norte e na Ásia e com posicionamento filogenético ainda incerto), podem ser semelhantes, mas carecem de reticulação no estipe.[37] Coletado inicialmente em Michigan, EUA, sob carvalhos, Boletus vinaceobasis se assemelha a S. luridus, mas tem esporos mais curtos e seus cistídios são marrom-escuros no reagente de Melzer.[50] A posição filogenética desta espécie também permanece não resolvida. Também na América do Norte, Rubroboletus pulcherrimus pode ser um pouco semelhante, mas tem um estipe mais robusto e poros vermelho-escuros.[51] A espécie chinesa Neoboletus sinensis, originalmente descrita como uma forma de S. luridus, mas agora colocada em um gênero diferente, tem esporos consideravelmente maiores, reportados como atingindo 12–17 por 5,5–7 μm.[26] Coleções muito semelhantes a S. luridus também foram registradas na Austrália, embora posteriormente renomeadas como Boletus barragensis, pois diferem no tamanho dos esporos e preferência por árvores da família Myrtaceae.[52][53]
Ecologia e distribuição
O fungo cresce em associação micorrízica com árvores latifoliadas, como carvalhos (Quercus), bétulas (Betula), castanheiras (Castanea) e faias (Fagus), em solos calcários.[34][25][46] Na República Tcheca, a variedade rubriceps foi reportada crescendo sob tílias (Tilia).[54] Suspeita-se também que seja um associado micorrízico de subarbustos do gênero Helianthemum.[55]
Estudos de campo indicam que o fungo, quando associado com mudas da conífera Cunninghamia lanceolata como parceiro micorrízico, aumenta a taxa de sobrevivência das mudas, promove seu crescimento em altura e diâmetro no solo, e eleva o conteúdo de clorofila nas folhas.[56] Um efeito semelhante de promoção de crescimento foi observado anteriormente com mudas de Pinus taiwanensis.[57] Esses efeitos benéficos no crescimento das plantas resultam de interações múltiplas entre o fungo, a planta hospedeira e micróbios do solo nativos, que aumentam a biomassa de carbono e a diversidade bacteriana na micorrizosfera.[58] Em um estudo comparando a resistência à salinidade de três fungos ectomicorrízicos comuns (os outros foram Suillus bovinus e S. luteus), S. luridus foi o mais tolerante a altas concentrações de sal, sendo um bom candidato para a inoculação de mudas de árvores a serem plantadas em solos salinos.[59]
Os basidiomas crescem isoladamente ou dispersos no solo,[37] de junho a novembro após chuvas de verão. S. luridus pode ocorrer em parques próximos a uma única árvore, embora seja muito raro em solos ácidos.[34]

A predileção de insetos por este fungo foi notada pela micologista britânica do século XIX, Anna Maria Hussey, que escreveu em 1847:
há muito poucos dos fungos de carne macia, todos os quais são viveiros de inúmeros insetos, tão apreciados quanto o venenoso Boletus luridus; ao quebrar um velho, ele é uma massa viva de larvas. Nosso presente objeto é tão rapidamente atacado por insetos que é muito raro encontrar espécimes desprovidos de vida agitada, e sendo um tipo muito comum e abundante, deve ser de grande utilidade na economia da existência dos insetos.[60]
Várias espécies de dípteros foram registradas se alimentando dos cogumelos, incluindo Phaonia boleticola, P. rufipalpis, Thricops diaphanus,[61] e, na América do Norte, Drosophila falleni, Pegomya mallochi, P. winthemi, Megaselia pygmaeoides e Muscina assimilis.[62] Em contraste, lesmas tendem a evitar consumir esta espécie.[63]
Com base em coleções verificadas filogeneticamente e estudos de DNA de distribuição micelial no solo, o fungo parece ser nativo da Europa e foi documentado até agora na Áustria, Chipre, Dinamarca, Estônia, França, Itália, Montenegro e Suécia.[64][65][66][67][25][46] Sua distribuição pode se estender a leste até o Mar Negro e regiões orientais da Anatólia na Turquia,[68][69] e ao sul até a Floresta Bar'am na região da Alta Galileia, no norte de Israel,[70] embora esses relatos precisem de verificação molecular.
Vários relatos extra-europeus podem ser encontrados na literatura anterior aos estudos de DNA, abrangendo Índia,[71] Paquistão,[72] Canadá,[44] Estados Unidos,[73] México,[74][75] Costa Rica,[76] China[77] e Taiwan,[57] mas esses não foram confirmados por testes moleculares e provavelmente representam táxons semelhantes mal identificados.[32][78]
Toxicidade/comestibilidade
De sabor suave, Suillellus luridus é frequentemente relatado como comestível após cozimento completo. É muito apreciado na França,[34][49] e comumente consumido na Itália, na República Tcheca, na Eslováquia e em outras partes da Europa.[79] No entanto, é necessária precaução ao escolher esta espécie para consumo, pois ela se assemelha a alguns boletos com reação de coloração azul que são venenosos, e alguns guias recomendam evitá-la completamente.[4] Se consumido cru ou insuficientemente cozido, sintomas de intoxicação gastrointestinal podem ocorrer dentro de 30 minutos a duas horas, incluindo náusea, vômito, cólicas abdominais e diarreia. A recuperação completa pode ser esperada dentro de 24 a 48 horas se as perdas de fluidos forem restauradas.[80]
Suillellus luridus foi suspeito de causar uma sensibilidade aumentada ao álcool semelhante à causada por Coprinopsis atramentaria, com sintomas gástricos. Um micologista alemão relatou ter sofrido sintomas após consumir álcool com este cogumelo excelente, se não fosse essa reação.[36][81] Um relatório de 1982 de três casos na Suíça incriminou ainda mais a espécie,[82] mas um estudo de 1994 lançou dúvidas sobre isso; os pesquisadores Ulrich Kiwitt e Hartmut Laatsch procuraram pelo composto coprina, semelhante ao dissulfiram, em S. luridus e espécies semelhantes, e não encontraram nenhum no suspeito histórico, mas encontraram indicações no raro Imperator torosus [en]. Eles concluíram que a explicação mais provável para incidentes históricos foi uma identificação errada de I. torosus com S. luridus, embora não pudessem descartar que S. luridus contenha um composto não identificado causador de reações relacionadas ao álcool.[83]
Química
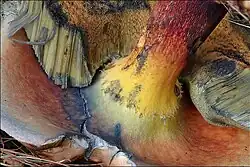
A composição dos compostos voláteis de sabor de Suillellus luridus consiste principalmente de ácido linoleico, com proporções menores de 1-butanol, 3-metil-1-butanol, ácido pentadecanoico, ácido palmítico, éster metílico de ácido linoleico e ácido heptadecanoico. Compostos de pirazina podem ser responsáveis pelo odor característico do cogumelo seco.[84] O principal esterol presente nos basidiomas é o ergosterol, com quantidades menores de compostos derivados relacionados.[85] Os principais ácidos graxos do cogumelo incluem ácido linoleico (53,4% do total de ácidos graxos), ácido oleico (24,1%) e ácido palmítico (10,2%). A arginina é o aminoácido livre encontrado em maior concentração (96,9 μM por grama de peso seco), seguido por glutamina (9,7) e alanina (8,2).[86]
O conteúdo de carotenoides dos basidiomas varia substancialmente entre o píleo, os tubos e o estipe. A parte superior do píleo, que contém 3,1 μg/g de carotenoide de peso fresco, tem predominantemente mutatocrome (47% dos carotenoides totais), 4-ceto-α-caroteno (40,2%) e δ-caroteno (6,4%). Os principais carotenoides nos tubos (totalizando 4,3 μg/g) incluem neurosporaxantina (31,1%), auroxantina (17,2%), 4-ceto-α-caroteno (17,1%) e rodopina (15,8%). O estipe (1,2 μg/g) contém principalmente auroxantina (32,5%), seguida por 4-ceto-α-caroteno (19,9%), β-zeacaroteno (18,5%) e rodopina (11,4%).[87] A mudança de cor observada com o machucado do tecido é causada pelos ácidos variegático e xerocômico, ambos os quais tornam-se azuis quando oxidados enzimaticamente ao serem expostos ao ar.[88]
Ver também
- Buchwaldoboletus lignicola
- Caloboletus calopus
- Caloboletus radicans
- Caloboletus rubripes
- Hortiboletus rubellus
- Pulveroboletus ravenelii
- Suillellus amygdalinus
- Suillus americanus
- Xerocomus subtomentosus
Referências
- ↑ a b c «GSD Species Synonymy: Suillellus luridus (Schaeff.) Murrill». Species Fungorum. CAB International. Consultado em 22 de outubro de 2025
- ↑ «Boletus luridus Schaeff., Fungorum qui in Bavaria et Palatinatu circa Ratisbonam nascuntur Icones, 4: 78, t. 107, 1774». MycoBank. International Mycological Association. Consultado em 22 de outubro de 2025
- ↑ Schaeffer JC. (1774). Fungorum qui in Bavaria et Palatinatu circa Ratisbonam nascuntur Icones (em latim e alemão). 4. Erlangen: Apud J.J. Palmium. p. 78; plate 107
- ↑ a b Nilson S, Persson O (1977). Fungi of Northern Europe 1: Larger Fungi (Excluding Gill-Fungi). [S.l.]: Penguin. p. 104. ISBN 0-14-063005-8
- ↑ Bulliard JBF. (1791). Herbier de la France (em francês). 11. Paris: Chez l'auteur, Didot, Debure, Belin. plate 490.1
- ↑ Gmelin JF. (1792). Systema Naturae (em latim). 2 13th ed. Leipzig: G.E. Beer. p. 1434
- ↑ Simpson DP. (1979) [1854]. Cassell's Latin Dictionary 5th ed. London: Cassell Ltd. pp. 574–75. ISBN 0-304-52257-0
- ↑ Nilson S, Persson O (1977). Fungi of Northern Europe 2: Gill-Fungi. [S.l.]: Penguin. p. 120. ISBN 0-14-063006-6
- ↑ «Boletus subvescus J.F. Gmel., Systema Naturae, 2: 1434, 1792». MycoBank. International Mycological Association. Consultado em 22 de outubro de 2025
- ↑ Gray SF. (1821). A Natural Arrangement of British Plants. 1. London: Baldwin, Cradock and Joy. p. 648
- ↑ Karsten PA. (1881). «Enumeratio Boletinearum et Polyporearum Fennicarum, systemate novo dispositarum». Revue Mycologique Toulouse (em latim). 3: 16–23
- ↑ Quélet L. (1886). Enchiridion Fungorum in Europa media et praesertim in Gallia Vigentium (em latim). Lutetia: Octave Dion. p. 160
- ↑ Murrill WA. (1909). «The Boletaceae of North America – 1». Mycologia. 1 (1): 4–18 (see p. 17). JSTOR 3753167. doi:10.2307/3753167
- ↑ Fries EM. (1821). Systema Mycologicum (em latim). 1. Lund: Ex Officina Berlingiana. p. 391
- ↑ «Boletus erythropus Pers., Annalen der Botanik (Usteri), 15: 23, 1795». MycoBank. International Mycological Association. Consultado em 22 de outubro de 2025
- ↑ Marie R. (1937). «Fungi Catalaunici: Series altera. Contributions a l'étude de la flore mycologique de la Catalogne». Publicacions del Instituto Botánico Barcelona (em francês). 3 (1): 1–128 (see p. 45)
- ↑ Dermek A. (1987). Boletes III. Col: Fungorum Rariorum Icones Coloratae. 16. Berlin: J. Cramer. pp. 1–23 (see p. 14). ISBN 978-3-443-69002-1
- ↑ Michael E, Schulz R (1924). Führer für Pilzfreunde: Systematisch geordnet und gänzlich neu bearbeitet von Roman Schulz (em alemão). 1 5th ed. Zwickau: Förster & Borries. plate 92
- ↑ Velenovský J. (1939). Novitates mycologicae (em latim). Prague: L. Souc̆ek. p. 158
- ↑ Petrak F; Commonwealth Mycological Institute (1970). «Boletus luridus». Index of Fungi. 3 (20): 546. ISSN 0019-3895. Arquivado do original em 3 de março de 2016
- ↑ Dermek A. (1979). Fungorum rariorum Icones coloratae. 9. [S.l.]: J. Cramer. pp. 1–34 (see p. 20). ISBN 978-3-7682-0416-3
- ↑ Hlavácek J. (1995). «Průzkum naší boletales, 29» [A survey of our Boletales, 29]. Mykologický Sborník (em checo). 72 (3): 83–90
- ↑ Lavorato C, Simonini G (1997). «Boletus flavosanguineus sp. nov.». Rivista di Micologia (em italiano). 40 (1): 37–51
- ↑ «Synonymy: Boletus caucasicus Singer ex Alessio, Boletus Dill. ex L. (Saronno): 175 (1985)». Species Fungorum. CAB International. Consultado em 22 de outubro de 2025
- ↑ a b c d e f g h Vizzini A, Simonini G, Ercole E, Voyron S (2014). «Boletus mendax, a new species of Boletus sect. Luridi from Italy and insights on the B. luridus complex». Mycol. Prog. 13 (1): 95–109. Bibcode:2014MycPr..13...95V. doi:10.1007/s11557-013-0896-4. hdl:2318/132875

- ↑ a b Lei QY, Zhou JJ, Wang QB (2009). «Notes on three bolete species from China». Mycosystema. 28 (1): 56–59. ISSN 1672-6472
- ↑ Fries EM. (1838). Epicrisis Systematis Mycologici seu Synopsis Hymenomycetum (em latim). Uppsala: Typographia Academica. p. 417
- ↑ Snell, Walter; Dick, Esther A. (1970). The Boleti of Northeastern North America. Lehre: J. Cramer. p. 79. ISBN 978-0-85486-016-6
- ↑ Binder M, Hibbett DS (2004). «Part 2: Figure 1C of the Proposed Research». Toward a Global Phylogeny of the Boletales. Clark University. Consultado em 22 de outubro de 2025. Arquivado do original em 25 de setembro de 2013
- ↑ Mello A, Ghignone S, Vizzini A, Sechi C, Ruiu P, Bonfante P (2006). «ITS primers for the identification of marketable boletes». Journal of Biotechnology. 121 (3): 318–29. PMID 16213623. doi:10.1016/j.jbiotec.2005.08.022
- ↑ Nuhn ME, Binder M, Taylor AF, Halling RE, Hibbett DS (2013). «Phylogenetic overview of the Boletineae». Fungal Biology. 117 (7–8): 479–511. PMID 23931115. doi:10.1016/j.funbio.2013.04.008
- ↑ a b Wu G, Feng B, Xu J, Zhu XT, Li YC, Zeng NK, Hosen MI, Yang ZL (2014). «Molecular phylogenetic analyses redefine seven major clades and reveal 22 new generic clades in the fungal family Boletaceae». Fungal Diversity. 69 (1): 93–115. doi:10.1007/s13225-014-0283-8
- ↑ Vizzini A. (2014). «Nomenclatural novelties» (PDF). Index Fungorum (188): 1. ISSN 2049-2375
- ↑ a b c d e f g Haas H. (1969). The Young Specialist Looks at Fungi. [S.l.]: Burke. p. 126. ISBN 0-222-79409-7
- ↑ a b c d Alessio CL. (1985). Boletus Dill. ex L. (sensu lato) (em italiano). Saronno: Biella Giovanna. pp. 169–74
- ↑ a b c Zeitlmayr L. (1976). Wild Mushrooms: An Illustrated Handbook. [S.l.]: Garden City Press, Hertfordshire. p. 102. ISBN 0-584-10324-7
- ↑ a b c d e f Bessette AR, Bessette A, Roody WC (2000). North American Boletes: A Color Guide to the Fleshy Pored Mushrooms. Syracuse: Syracuse University Press. pp. 126–27. ISBN 0-8156-0588-9
- ↑ a b c Muñoz JA. (2005). Fungi Europaei 2: Boletus s.l. Italy: Edizioni Candusso. ISBN 978-88-901057-6-0
- ↑ a b c Galli R. (2007). I Boleti. Atlante pratico-monographico per la determinazione dei boleti (em italiano) 3rd ed. Milano, Italy: Dalla Natura
- ↑ a b Michell K. (2006). Field Guide to Mushrooms and Other Fungi of Britain and Europe. London: New Holland Publisher. p. 30. ISBN 1-84537-474-6
- ↑ a b Phillips R. (2006). Mushrooms. London: Pan MacMillan. p. 281. ISBN 0-330-44237-6
- ↑ Ramsbottom J. (1953). Mushrooms & Toadstools. [S.l.]: Collins. p. 129. ISBN 1-870630-09-2
- ↑ Siquier JL, Salom JC (2008). «Contribució al coneixement micologic de les Illes Balears. XVI» (PDF). Revista Catalana de Micologia (em catalão). 30: 13–25 (see p. 15)
- ↑ a b Ammirati JA, Traquair JA, Horgen PA (1985). Poisonous Mushrooms of the Northern United States and Canada. Minneapolis: University of Minnesota Press. pp. 237; 240–41. ISBN 0-8166-1407-5
- ↑ Dickinson C, Lucas J (1982). VNR Color Dictionary of Mushrooms. [S.l.]: Van Nostrand Reinhold. p. 68. ISBN 978-0-442-21998-7
- ↑ a b c d Loizides M, Bellanger JM, Assyov B, Moreau PA, Richard F (2019). «Present status and future of boletoid fungi (Boletaceae) on the island of Cyprus: cryptic and threatened diversity unraveled by 10-year study.». Fungal Ecology. 41 (13): 65–81. doi:10.1016/j.funeco.2019.03.008
- ↑ Loizides M. (2011). «Quercus alnifolia: The indigenous Golden Oak of Cyprus and its fungi». Field Mycology. 12 (3): 81–88. doi:10.1016/j.fldmyc.2011.06.004

- ↑ Simonini G. (1992). «Boletus comptus sp. nov.». Rivista di Micologia. 35 (3): 195–208
- ↑ a b Lamaison JL, Polese JM (2005). The Great Encyclopedia of Mushrooms. Cologne: Könemann. p. 31. ISBN 3-8331-1239-5
- ↑ Smith AH, Thiers HD (1971). The Boletes of Michigan. Ann Arbor: University of Michigan Press. pp. 347–48. ISBN 0-472-85590-5
- ↑ Arora D. (1986). Mushrooms Demystified: A Comprehensive Guide to the Fleshy Fungi. Berkeley: Ten Speed Press. p. 528. ISBN 0-89815-169-4
- ↑ Watling R, Li TH (1999). Australian Boletes: A Preliminary Survey. [S.l.]: Royal Botanic Garden Edinburgh. p. 33. ISBN 1-872291-28-7
- ↑ Grgurinovic CA. (1997). Larger Fungi of Southern Australia. Adelaide: Botanic Gardens of Adelaide & State Herbarium. p. 229. ISBN 978-0-7308-0737-7
- ↑ Tichy H. (1998). «Hřib koloděj červenohlavý Boletus luridus var. rubriceps (R. Maire) roste v parku» [Boletus luridus var. rubriceps (R. Maire) growing in a park]. Mykologicky Sbornik (em checo e inglês). 75 (1): 20–21. ISSN 0374-9436
- ↑ Barden N. (2007). «Helianthemum grasslands of the Peak District and their possible mycorrhizal associates». Field Mycology. 8 (4): 119–26. doi:10.1016/S1468-1641(10)60384-2

- ↑ Wang YJ, Tang M, Guo Y, Zhang FF, Huang YH (2006). 外生菌根真菌对杉木的接种效应 [Inoculation effect of ectomycorrhizal fungi on Cunninghamia lanceolata]. Acta Botanica Boreali-Occidentalia Sinica (em chinês e inglês). 26 (9): 1900–04. ISSN 1000-4025
- ↑ a b Hu H-T. (1981). «Mycorrhizae of some important tree species grown at high elevation in Taiwan». National Science Council Monthly (em chinês). 9 (4): 303–34. ISSN 0250-1651
- ↑ Zhang HH, Tang M, Chen H, Zheng CL (2010). «Effects of inoculation with ectomycorrhizal fungi on microbial biomass and bacterial functional diversity in the rhizosphere of Pinus tabulaeformis seedlings». European Journal of Soil Biology. 46 (1): 55–61. Bibcode:2010EJSB...46...55Z. doi:10.1016/j.ejsobi.2009.10.005
- ↑ Sheng M, Chen H, Zhang FF (2009). «In vitro salinity resistance of three ectomycorrhizal fungi». Soil Biology and Biochemistry. 41 (5): 948–53. Bibcode:2009SBiBi..41..948T. doi:10.1016/j.soilbio.2008.12.007
- ↑ Hussey AM. (1847). Illustrations of British Mycology, Containing the Figures and Description of Funguses of Interest and Novelty Indigenous to Britain. ser. 1. London: Reeve, Brothers, King William Street, Strand. Description of plate XXIII
- ↑ Skidmore P. (1985). The Biology of the Muscidae of the World. Dordrecht & Boston: Springer. pp. 159, 493. ISBN 978-90-6193-139-3
- ↑ Bruns T. (1984). «Insect mycophagy in the Boletales: Fungivore diversity and the mushroom habitat». In: Wheeler Q, Blackwell M. Fungus-Insect Relationships: Perspectives in Ecology and Evolution. New York: Columbia University Press. pp. 91–129. ISBN 0-231-05694-X
- ↑ Elliott WT. (1922). «Some observations on the mycophagous propensities of slugs». Transactions of the British Mycological Society. 8 (1–2): 84–90. doi:10.1016/S0007-1536(22)80011-5
- ↑ Iotti M, Barbieri E, Stocchi V, Zambonelli A (2005). «Morphological and molecular characterisation of mycelia of ectomycorrhizal fungi in pure culture.». Fungal Diversity. 19: 1–68
- ↑ Nygren CM, Edqvist J, Elfstrand M, Heller G, Taylor A (2007). «Detection of extracellular protease activity in different species and genera of ectomycorrhizal fungi.». Mycorrhiza. 17 (3): 241–248. Bibcode:2007Mycor..17..241N. PMID 17216502. doi:10.1007/s00572-006-0100-7
- ↑ Krpata D, Peintner U, Langer I, Fitz WJ, Schweiger P (2008). «Ectomycorrhizal communities associated with Populus tremula growing on a heavy metal contaminated site». Mycological Research. 112 (9): 1069–1079. PMID 18692376. doi:10.1016/j.mycres.2008.02.004
- ↑ Osmundson TW, Robert VA, Schoch CL, Baker LJ, Smith A, Robich G, Mizzan L, Garbelotto MM (2013). «Filling gaps in biodiversity knowledge for macrofungi: contributions and assessment of an herbarium collection DNA barcode sequencing project.». PLOS ONE. 8 (4): 1–8. Bibcode:2013PLoSO...862419O. PMC 3640088
 . PMID 23638077. doi:10.1371/journal.pone.0062419
. PMID 23638077. doi:10.1371/journal.pone.0062419
- ↑ Demirel K, Uzun Y, Kaya A (2004). «Some poisonous fungi of East Anatolia» (PDF). Turkish Journal of Botany. 28 (1/2): 215–19. Arquivado do original (PDF) em 5 de maio de 2005
- ↑ Sesli E. (2007). «Preliminary checklist of macromycetes of the East and Middle Black Sea Regions of Turkey» (PDF). Mycotaxon. 99: 71–74
- ↑ Avizohar-Hershenzon Z, Binyamini N (1972). «Boletaceae of Israel: I. Boletus sect. Luridi». Transactions of the British Mycological Society. 59 (1): 25–30. doi:10.1016/s0007-1536(72)80037-8
- ↑ Kumar S, Sharma YP (2011). «Additions to boletes from Jammu and Kashmir». Journal of Mycology and Plant Pathology. 41 (4): 579–83
- ↑ Sarwar S, Khalid AN (2013). «Preliminary Checklist of Boletales in Pakistan» (PDF). Mycotaxon: 1–12
- ↑ Stack RW. (1981). «Rare mycorrhizal fungi fruiting in North Dakota in 1980». Proceedings of the North Dakota Academy of Science. 35: 44. ISSN 0096-9214
- ↑ Montoya A, Kong A, Estrada-Torres A, Cifuentes J, Caballero J (2004). «Useful wild fungi of La Malinche National Park, Mexico» (PDF). Fungal Diversity. 17: 115–43
- ↑ Pérez-Moreno J, Martínez-Reyes M, Yescas-Pérez A, Delgado-Alvarado A, Xoconostle-Cázares B (2008). «Wild mushroom markets in central Mexico and a case study at Ozumba». Economic Botany. 62 (3): 425–36. Bibcode:2008EcBot..62..425P. doi:10.1007/s12231-008-9043-6
- ↑ Halling RE, Mueller GM (2008). «Boletus luridus». New York Botanic Garden: Macrofungi of Costa Rica. New York Botanic Garden. Consultado em 22 de outubro de 2025
- ↑ Zhishu B, Zheng G, Taihui L (1993). The Macrofungus Flora of China's Guangdong Province (Chinese University Press). New York: Columbia University Press. p. 487. ISBN 962-201-556-5
- ↑ Wu G, Li YC, Zhu XT, Zhao K, Han LH, Cui YY, Li F, Xu JP, Yang ZL (2016). «One hundred noteworthy boletes from China». Fungal Diversity. 81: 25–188 [145]. doi:10.1007/s13225-016-0375-8
- ↑ Rubel W, Arora D (2008). «A study of cultural bias in field guide determinations of mushroom edibility using the iconic mushroom, Amanita muscaria, as an example». Economic Botany. 63 (3): 223–43. Bibcode:2008EcBot..62..223R. doi:10.1007/s12231-008-9040-9
- ↑ Tomalak M, Rossi E, Ferrini F, Moro PA (2011). «Negative aspects and hazardous effects of forest environment on human health». In: Nilsson K, et al. Forests, Trees and Human Health. New York: Springer. pp. 77–124 (see p. 101). ISBN 978-90-481-9805-4
- ↑ Flammer R. (1985). «Brechdurchfalle als Leitsymptom – Pilze und Alkohol» [Diarreia e vômito como principais sintomas - cogumelos e álcool]. Praxis (em alemão). 74 (37): 992–96. PMID 4059739
- ↑ Benjamin DR. (1995). Mushrooms: Poisons and Panaceas—A Handbook for Naturalists, Mycologists and Physicians. New York: WH Freeman and Company. p. 291. ISBN 0-7167-2649-1
- ↑ Kiwitt U, Laatsch H (1994). «Coprin in Boletus torosus: Beruht die angebliche Alkoholunverträglichkeit durch den Verzehr des Netzstieligen Hexenröhrlings (Boletus luridus) auf einer Verwechslung?» [Coprina em "Boletus torosus": a suposta hipersensibilidade ao álcool pela ingestão de "B. luridus" é causada por um erro?] (PDF). Zeitschrift für Mykologie (em alemão). 60 (2): 423–30. Consultado em 22 de outubro de 2025. Arquivado do original (PDF) em 13 de abril de 2014
- ↑ Li WW, Wu SM, Xu T (2009). 褐黄牛肝菌挥发性风味物质组成研究 [Volatile flavor composition of Boletus luridus Schaeff.: Fr.]. Journal of Shanghai Jiaotong University – Agricultural Science (em chinês e inglês). 27 (3): 300–04. doi:10.3969/j.issn.1671-9964.2009.03.022
- ↑ De Simone F, Senatore F, Sica D, Zollo F (1979). «Sterols from some basidiomycetes». Phytochemistry. 18 (9): 1572–73. Bibcode:1979PChem..18.1572D. doi:10.1016/S0031-9422(00)98504-2
- ↑ Dembitsky VM, Terent'ev AO, Levitsky DO (2010). «Amino and fatty acids of wild edible mushrooms of the genus Boletus». Records of Natural Products. 4 (4): 218–23. ISSN 1307-6167
- ↑ Czezuga B. (1978). «Investigations on carotenoids in fungi IV. Members of the Boletus genus». Qualitas Plantarum. 28 (1): 37–43. doi:10.1007/BF01092999
- ↑ Nelson SF. (2010). «Bluing components and other pigments of Boletes» (PDF). Fungi. 3 (4): 11–14
