Octaborano-12
Octaborano(12)
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
| Outros nomes | Octahidreto de octaboro nido-octaborano | ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
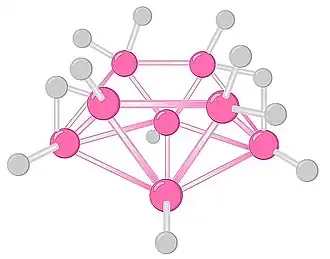
Octaborano(12) é um composto químico neutro pertencente à classe dos boranos, com a fórmula molecular B8H12. É um dos membros mais estudados da série de clusters de boro e hidrogênio, notável por sua estabilidade relativa em comparação a outros boranos neutros de tamanhos semelhantes.
Estrutura e ligação
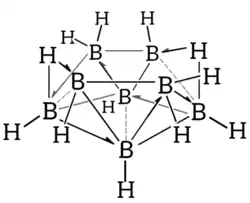
O octaborano(12) cristaliza como um sólido incolor e adota uma estrutura que pode ser descrita como um cluster do tipo nido, de acordo com as regras de contagem eletrônica de Wade–Mingos.[1]
O cluster apresenta uma forma de "tigela", com uma geometria que pode ser derivada conceitualmente de um poliedro closo B9H92- ao remover um vértice, resultando em uma estrutura aberta do tipo nido. Como todo borano, é um composto deficiente de elétrons, de forma que as ligações B-B no esqueleto do poliedro, não podem ser explicadas puramente como ligações covalentes convencionais, mas como um híbrido de ressonância envolvendo ligações comuns e ligações tricentradas com dois elétrons deslocalizadas por toda a estrutura. As pontes B-H-B também envolvem ligações do tipo tricentrada, enquanto as ligações B–H terminais são ligações covalentes normais.
Propriedades
O octaborano-12 é um sólido cristalino amarelado estável em condições ambientes, embora sensível à umidade e ao ar quando pulverizado. É solúvel em solventes orgânicos apolares, tais como éter, hexano e benzeno. Queima ao ar com uma chama verde brilhante característica dos compostos de boro, e sofre hidrólise em contato com a água formando ácido bórico e hidrogênio, mais rapidamente a quente. Diferente de boranos menores tais como diborano, tetraborano e pentaboranos, ele não inflama espontaneamente ao ar (embora ainda seja altamente inflamável) ou se hidrolisa rapidamente em água; é mais estável do que os respectivos boranos inferiores, mas menos que o decaborano-14. O octaborano-12 possui volatilidade moderada e pode sublimar sob vácuo. A decomposição térmica geralmente leva à formação de boranos menores e, em condições mais severas, à deposição de boro elementar.[2]
História da descoberta
O octaborano(12) foi primeiramente isolado e caracterizado em 1964 por Enrione, Boer e Lipscomb. Eles obtiveram cristais puros deste composto a partir de descargas elétricas em uma mistura de diborano (B2H6) e pentaborano (B5H9), e confirmaram sua composição e estrutura por difração de raios X de um cristal único mantido a baixas temperaturas.[3]
Síntese
O B8H12 pode ser obtido por pirólise ou fotólise de decaborano (B10H14), em processos nos quais há perda de fragmentos BH2 ou H2 e reestruturação do cluster.[4]
O octaborano(12) pode ser preparado pela pirolise de boranos menores:
Uma rota clássica envolve a decomposição térmica de pentaborano-11 ou hexaborano-10, que liberam hidrogênio e formam clusters maiores como B₈H₁₂.[5]
Outra rota envolve a desproporcionação de boranos em presença de catalisadores de metais de transição.
Aplicações
Embora não possua aplicações tecnológicas de grande escala, o octaborano(12) é importante em pesquisa de química inorgânica e organometálica. Seu estudo fornece informações sobre:
- os princípios de ligação em sistemas de cluster;
- mecanismos de conversão entre boranos de diferentes tamanhos;
- potenciais aplicações como precursores em deposição química de vapor (CVD) para obtenção de filmes de boro.
Segurança
O octaborano(12) é altamente tóxico e piroforicamente inflamável quando em pó. Apresenta um odor desagradável característico de boranos, mofado, intensamente amargo e reminiscente de chocolate amargo. Como muitos boranos, é altamente tóxico, agindo como neurotoxina.[6] Deve ser manipulado em sistemas fechados sob atmosfera inerte, preferencialmente de nitrogênio ou argônio. Em contato com ar, pode inflamar-se facilmente, liberando óxidos de boro e fumaça irritante. Pode explodir violentamente na presença de agentes oxidantes (como ácido nítrico, halogênios etc) ou mesmo de compostos como tetracloreto de carbono, clorofórmio e outros halocarbonos.
Ver também
- Boranos
- Decaborano
- Heptaborano-11
- Clusters de boro
Referências
- ↑ Housecroft, Catherine E.; Sharpe, Alan G. (2012). Inorganic Chemistry 4ª ed. Harlow: Pearson. ISBN 978-0-273-74275-3
- ↑ Greenwood, N. N.; Earnshaw, A. (1997). Chemistry of the Elements 2ª ed. Oxford: Butterworth-Heinemann. ISBN 978-0-7506-3365-9
- ↑ . "Preparation, Isolation and Structure of B₈H₁₂" .
- ↑ . "Polyhedral Boranes" DOI 10.1021/ja00876a043..
- ↑ https://ntrl.ntis.gov/NTRL/dashboard/searchResults/titleDetail/AD447710.xhtml
- ↑ https://pubs.acs.org/doi/10.1021/op068011l