Tetraborano
Tetraborano
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
| Nomes | |||||||||||||||
| Nome IUPAC | tetraborano(10) aracno-B4H10 | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
O Tetraborano, ou para ser mais preciso tetraborano-10 ou aracno-B4H10 foi o primeiro composto hidreto de boro a ser classificado por Stock e Messenez em 1912 e foi isolado pela primeira vez por Alfred Hock. Tem um ponto de ebulição relativamente baixo a 18°C sendo assim um líquido pouco abaixo da temperatura ambiente. O tetraborano gasoso apresenta um mau cheiro e é tóxico.
Estrutura [1]
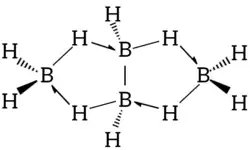
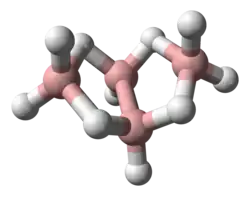
O tetraborano é um cluster de borano do tipo arachno, seguindo a fórmula geral BnHn+6. Sua molécula tem uma forma de borboleta, formada por dois átomos de boro centrais ligados diretamente entre si (cada um ligado também a um hidrogênio terminal), com dois outros boros mais distantes (ligados cada um a dois hidrogênios terminais), e quatro hidrogênios em ponte conectando os boros centrais aos distais, originando dois anéis cíclicos. O tetraborano é um composto deficiente em elétrons, de forma que resolve essa carência apelando para a formação de ligações tricentradas com dois elétrons para completar os octetos dos átomos de boro. Essas ligações tricentradas estão presentes nas quatro pontes B-H-B, que correspondem, cada uma, a uma única ligação covalente unindo os três átomos, cada uma com uma ordem de ligação de 0,66.
Reações e Segurança
O B4H10 é um composto altamente reativo. Ele é facilmente oxidado e, portanto, deve ser mantido sob vácuo. O tetraborano reage vigorosamente com a água para formar ácido bórico com liberação de gás hidrogênio:
B
4H
10 + 12H
2O → 4H
3BO
3 + 11H
2
Ele também inflama espontaneamente quando entra em contato com o oxigênio do ar, com uma chama verde brilhante característica do espectro de emissão do boro:
2B
4H
10 + 11O
2 → 4B
2O
3 + 10H
2O
Vapores de B
4H
10 reagem explosivamente em contato com ar ou oxigênio, bem como ácido nítrico.
Os boranos em geral (incluindo o tetraborano) têm sido considerados muito tóxicos e são biologicamente destrutivos. Um estudo que consiste de pequena exposição diária da substância química em coelhos e ratos resultou em fatalidade.[2]
Preparação
Tetraborano pode ser produzido através de uma reação entre um ácido e boretos de magnésio, alumínio e berílio, pela hidrólise do diboreto de magnésio, pela hidrogenação de haletos de boro em altas temperaturas e também pela pirólise do diborano. A hidrólise do boreto de magnésio foi uma das primeiras reações para dar um alto rendimento (14%) de tetraborano, além de outros boranos. O ácido fosfórico provou ser o mais eficiente na produção de B4H10 (com exceção do ácido clorídrico e do ácido sulfúrico) na reação com boreto de magnésio. Redução de halogenetos de boro com hidrogênio na presença de hidretos metálicos em altas temperaturas também produz tetraborano.[3]
- Este artigo foi inicialmente traduzido, total ou parcialmente, do artigo da Wikipédia em inglês cujo título é «Tetraborane».
Referências
- ↑ https://pubs.acs.org/doi/10.1021/ja01112a542
- ↑ «Cópia arquivada» (PDF). Consultado em 13 de outubro de 2011. Arquivado do original (PDF) em 27 de julho de 2011
- ↑ Dain, C. J., Downs, A. J., Laurenson, G. S., & Rankin, D. W. (1981). The Molecular Structure of Tetraborane(10) in the Gas Phase as determined by a Joint Analysis of Electron-diffraction and Microwave Data. Journal of the Chemical Society, 472-477.
Ver também
- Diborano
- Triborano
- Pentaborano
- Hexaborano-10
- Octaborano-12
- Nonaborano
- Decaborano
- Boreto de magnésio