Triborano
O triborano, mais especificamente triborano-7, é um composto químico instável de fórmula química B
3H
7, pertencente à classe dos boranos neutros, ou seja, hidretos de boro com estruturas de clusters.[1] É considerado um borano ’’nido’’, devido à geometria aberta do cluster formado pelos átomos de boro.[2]
Estrutura
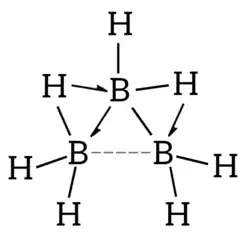
O triborano possui três átomos de boro formando um cluster triangular, em que os átomos de hidrogênio estão ligados de duas maneiras:[2]
- Hidrogênios terminais, ligados a um único átomo de boro.
- Hidrogênios ponte (B–H–B), unidos por ligações tricentradas com dois elétrons conectando pares de átomos de boro e estabilizando a estrutura do cluster.
A geometria do triborano segue a regra de Wade, típica de boranos pequenos, em que o número de átomos de hidrogênio determina se o cluster é “closo” (poliédrico fechado), “nido” (aberto) ou “arachno” (mais aberto).[1]
Esse composto é deficiente em elétrons, de forma que nem todas as ligações entre os átomos são ligações covalentes convencionais. Para completar o octeto, os átomos de boro recorrem a ligações 3c-2e para estabilizar a estrutura.[2]
Propriedades físicas e químicas
O triborano é um gás incolor altamente instável em condições ambientes, sendo extremamente sensível à umidade, oxigênio e calor. Ele reage espontaneamente com o oxigênio do ar, inflamando-se com uma chama verde brilhante. Também reage com a água formando ácido bórico e liberando gás hidrogênio.
Devido à sua instabilidade, raramente é isolado como composto puro, embora forme alguns adutos estáveis, por exemplo, com ligantes como a piridina (C
5H
5N–B
3H
7).[3], bem como sais sólidos como o Na[B
3H
8], contendo o ânion octaidrotriborato, B
3H–
8, formado ao reagir B
3H
7 com uma fonte de H–.[4] Normalmente, o triborano é detectado em fase gasosa ou como intermediário em reações de síntese de boranos maiores, tais como tetraborano (B
4H
10) ou pentaborano-9 (B
5H
9).
Apresenta reatividade elevada, característica de boranos pequenos, reagindo rapidamente com ar, água e agentes oxidantes. Essas reações podem ser vigorosas e muito exotérmicas, ou até mesmo explosivas.
Síntese e ocorrência
O triborano é geralmente formado como intermediário durante a síntese de outros boranos neutros, como por exemplo durante a pirólise do diborano.[5] Reações de decomposição térmica de boranos maiores ou descargas elétricas envolvendo hidretos de boro podem gerar espécies de B
3H
7 em fase gasosa, que rapidamente condensam para gerar outros boranos.
Importância e aplicações
O triborano não possui aplicações comerciais diretas devido à sua extrema instabilidade.
É relevante na química teórica e experimental de boranos, ajudando a compreender a estabilidade e geometria de clusters de boro, bem como a evolução das propriedades eletrônicas em boranos progressivamente maiores.[5]
Referências
- ↑ a b https://pubs.acs.org/doi/10.1021/acs.jpca.3c02747
- ↑ a b c https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Supplemental_Modules_and_Websites_%28Inorganic_Chemistry%29/Descriptive_Chemistry/Elements_Organized_by_Block/2_p-Block_Elements/Group_13%3A_The_Boron_Family/Z005_Chemistry_of_Boron_%28Z5%29/Boranes_and_Borohydrides
- ↑ https://pubs.rsc.org/en/content/articlelanding/2024/sc/d4sc03109a
- ↑ https://hal.science/hal-03887779/
- ↑ a b https://pubmed.ncbi.nlm.nih.gov/24020644/