Notação de meia-seta de Parkin
A notação de meia-seta proposta por Gerard Parkin (e precedida pela aplicação em contextos de Malcolm Green) é uma representação gráfica utilizada para descrever ligações três-centros dois elétrons (3c–2e), particularmente em química organometálica. Essa notação auxilia na contagem de elétrons e no entendimento da ligação em compostos onde a simples representação de ligações entre pares de átomos (2c–2e) se torna insuficiente.[1]
Conceito
A notação de meia-seta de Parkin é uma convenção gráfica introduzida por Gerard Parkin para representar ligações três-centros dois-elétrons (3c-2e) de forma consistente dentro do método de Classificação de Ligações Covalentes (CBC). Essa notação resolve a ambiguidade que surge quando se tenta descrever tais ligações apenas como traços, tais como uma ligação covalente convencional.
Em uma ligação 3c-2e, três átomos compartilham apenas dois elétrons. Como o par eletrônico já está envolvido em uma ligação, a representação por uma seta cheia (usada para indicar uma ligação dativa 2c-2e) seria enganosa. A meia-seta diferencia-se justamente por indicar que o par ligante é compartilhado com um terceiro centro atômico, e não que um par isolado está sendo doado.
Assim, a notação adota duas formas principais:
- Classe I (X–Z–X ou X–X–Z): cada átomo periférico (X) contribui com um elétron, e o centro (Z) fornece apenas um orbital vazio para recebê-los. Graficamente, representa-se a ligação X–Z com uma meia-seta que se projeta do segundo átomo X em direção ao átomo Z. Isso mostra que os dois elétrons da ligação já estão presentes, mas o orbital é compartilhado com um terceiro centro.
- Classe II (Z–L–Z): o átomo central (L) fornece os dois elétrons, que são simultaneamente compartilhados com dois átomos periféricos (Z). Nesse caso, desenham-se duas meia-setas, uma de L em direção a cada Z. Isso indica que o par eletrônico doador está localizado no centro, mas é deslocalizado para dois receptores.
A meia-seta, portanto, não representa a transferência de um par isolado de elétrons, como numa ligação coordenada clássica, mas sim a extensão de um par ligante previamente existente a um terceiro átomo. Essa distinção é importante na contagem eletrônica de complexos metálicos, permitindo evitar interpretações incorretas sobre o número de elétrons em torno do centro metálico e sobre a presença ou ausência de ligações metal–metal.
Classificação via CBC (Notação LXZ)
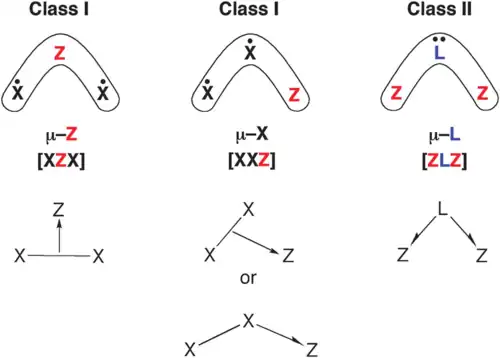
O método de Classificação de Ligações Covalentes (CBC), também chamado de notação LXZ, define ligantes com base na quantidade de elétrons doados ao átomo central:
- L: doa 2 elétrons
- X: doa 1 elétron
- Z: doa 0 elétrons (orbital vazio).
Ao aplicar ao contexto 3c–2e, a classificação se dá com base na contribuição da ponte:
Classe I (dois doadores) – Cada átomo periférico contribui com 1 elétron ([X–Z–X] ou [X–X–Z]). Um traço simples é desenhado unindo os dois átomos X e uma meia-seta é desenhada apontando de um dos átomos X para o átomo receptor Z, indicando que o par de elétrons está sendo compartilhado, mas originando-se do meio da ligação e não de um par isolado não-ligante.[3]
Classe II (doador único) – O átomo central contribui com o par completo de elétrons ([Z–L–Z]) .[3][4] Duas meia-setas saem do átomo central (L) rumo aos átomos Z com orbitais vazios, representando a doação de um único par de elétrons compartilhado com ambos os átomos externos (algo como uma "ligação dativa bifurcada").
A meia-seta evidencia a natureza especial dessa ligação.[5]
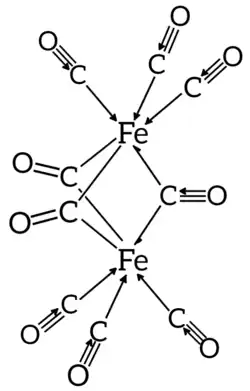
Esse modelo permite a contagem mais precisa de elétrons em centros metálicos e clusters de borano e ajuda a prever ordens de ligação metal–metal — como em complexos com ligantes carbonila em ponte simétrica, cuja descrição como derivados “cetônicos” pode falhar sem essa notação (como, por exemplo, em [Fe
2(CO)
9]).[5][3][4]
Exemplos notórios
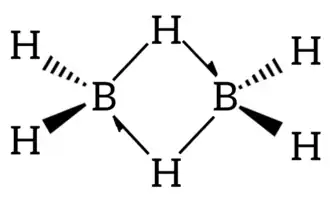
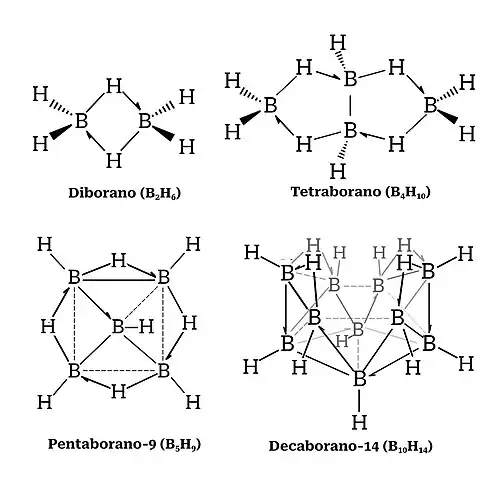
- Diborano (B
2H
6 ) e tetraborano (B
4H
10): as pontes B–H–B são representadas por traços e meia-setas na estrutura, ilustrando a natureza 3c-2e das ligações. Isto deixa bem claro que o hidrogênio não está formando duas ligações separadas, o que daria a entender se as conectividades fossem apresentadas como traços simples.
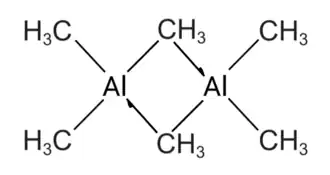
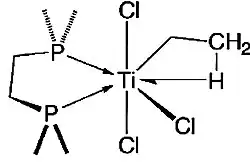
- Complexos metálicos com ligantes agósticos, carbonila, fosfinas ou outro ligante em ponte: exibem ligações 3c-2e que podem ser classificadas e representadas com meia-setas para tornar clara a contribuição eletrônica dos ligantes.
- Clusters de boro (como octacloreto de octaboro ou nonacloreto de nonaboro), onde múltiplas ligações tricentradas 3c-2e podem ser representadas por chaves de traço e meia-seta de Parkin em estruturas canônicas.
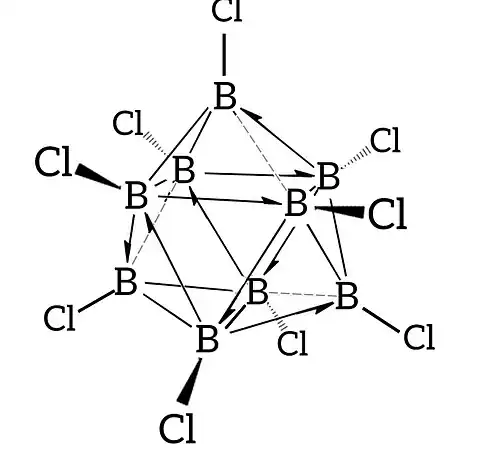
9Cl
9, mostrando as ligações tricentradas na gaiola poliédrica representadas pela notação de meia-seta.
Aplicações e importância

Compostos contendo ponte de hidreto (M–H–M): A notação de meia-seta permite contar corretamente os elétrons nos centros metálicos, evitando interpretações incorretas sobre ligação direta entre metais.
Complexos de ponte carbonila simétricos: A representação via m-L (ligante que doa o par completo) ajuda a explicar a ausência de ligação metal–metal, em casos onde contagens convencionais falham.[3][4]
Aplicação didática: Facilita a compreensão da regra dos 18 elétrons e de contagens de elétrons em química inorgânica e organometálica.[3]
Referências
- ↑ https://www.researchgate.net/figure/Half-arrow-structure-bonding-representations-for-symmetrically-bridging-and-monoagostic_fig36_232225251
- ↑ https://www.researchgate.net/figure/An-example-of-a-compound-that-features-a-3c-2e-interaction-with-a-m-L-bridge_fig3_232225251
- ↑ a b c d e https://www.cup.lmu.de/ac/kluefers/homepage/L/kc2/literature/3z2e_bonds_2012.pdf
- ↑ a b c https://pubs.rsc.org/en/content/articlelanding/2012/cc/c2cc35304k
- ↑ a b https://www.chemistryworld.com/news/three-centres-two-electrons-but-how-many-bonds/4010498.article
- ↑ Z. Dawoodi; M. L. H. Green; V. S. B. Mtetwa; K. Prout; A. J. Schultz; J. M. Williams; T. F. Koetzle (1986). «Evidence for Carbon–Hydrogen–Titanium Interactions: Synthesis and Crystal Structures of the Agostic alkyls [TiCl3(Me2PCH2CH2PMe2)R] (R = Et or Me)». J. Chem. Soc., Dalton Trans. (8): 1629. doi:10.1039/dt9860001629