Octacloreto de octaboro
Octacloreto de octaboro
| |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||
 | |||||||||||||
| Nomes | |||||||||||||
| Nome sistemático | octacloro-octaborano(8) | ||||||||||||
| Outros nomes | hipercloso-octacloro-octaborano Cloreto de boro (B8Cl8) (6CI,8CI) Octacloreto de octaboro Octacloro-octaborano Octacloro-octaborano(8) | ||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| |||||||||||||
| Página de dados suplementares | |||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||
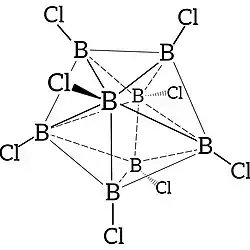
O octacloreto de octaboro ou octacloro-octaborano(8) é um composto químico com a estrutura molecular B
8Cl
8. Essa substância é um subcloreto de boro que apresenta uma estrutura molecular complexa em forma de gaiola poliédrica contendo ligações pouco convencionais entre os átomos de boro. Esse composto é um sólido verde-escuro, verde-preto, marrom escuro ou mesmo avermelhado dependendo do grau de pureza, da espessura da camada do material sólido ou da concentração da solução. É um dos compostos de subcloreto de boro mais estudados.
Estrutura
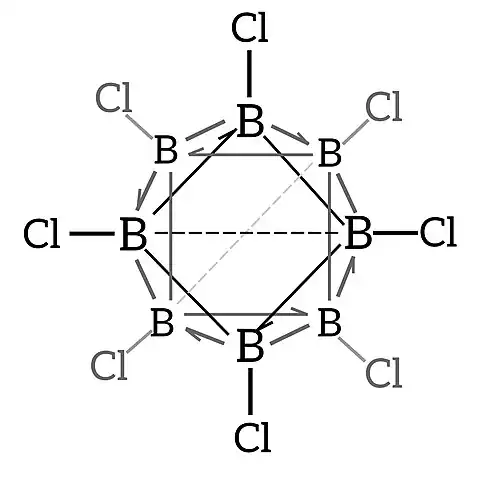
O cluster apresenta uma estrutura em forma de dodecaedro trigonal ou prisma triangular bicapado[2], que pode ser considerada como derivado de um prisma de base triangular com dois vértices adicionais sobre duas das três faces quadradas. Os oito átomos de boro se organizam nos vértices desse poliedro, e cada um está ligado a um átomo de cloro por uma ligação covalente simples B–Cl. Cada átomo de boro encontra-se ligado a quatro ou cinco boros vizinhos.
As ligações químicas entre os átomos de boro dentro do esqueleto poliédrico não podem ser explicadas em termos de ligações covalentes comuns (dois centros-dois elétrons, 2c-2e), pois cada átomo de boro possui apenas dois elétrons remanescentes para efetuar ligações (além do seu terceiro elétron já envolvido na ligação B–Cl), porém encontra-se ligado a quatro ou cinco boros vizinhos, fazendo com que cada boro se ligue a cinco ou seis átomos (contando o cloro). Caso essas ligações fossem ligações covalentes comuns, cada boro estaria realizando mais ligações do que o seu octeto permite (que seria no máximo quatro), o que não é possível para elementos do segundo período. Além disso, com apenas três elétrons de valência, o boro não tem elétrons suficientes para completar o seu octeto apenas realizando ligações covalentes convencionais dentro do esqueleto poliédrico. Portanto, as ligações dentro dessa gaiola são melhor descritas em termos de ligações tricentradas com dois elétrons (3c-2e), em que um único par de elétrons é compartilhado entre três átomos em vez de dois, ou seja, uma única ligação que une 3 átomos. Esse tipo de ligação é frequente em compostos contendo átomos deficientes em elétrons,[3] e não violam a regra do octeto.
O octacloreto de octaboro pode ser considerado como um derivado completamente clorado do composto hipotético hipercloso-octaborano(8) (B
8H
8), que, por sua vez, seria um derivado por oxidação da espécie química dianiônica estável B
8H2–
8. Embora o octaborano(8) neutro (e outros hiperclosoboranos) não seja uma espécie química estável (devido à sua estrutura eletrônica antiaromática), seus derivados per-halogenados tais como B
8Cl
8 e B
8Br
8 são compostos estáveis devido à doação parcial de densidade eletrônica dos pares de elétrons não-ligantes dos átomos de halogênio para o núcleo poliédrico por ressonância, o que confere ao poliedro de átomos de boro um certo caráter aromático estabilizador (coisa que não é possível no borano neutro parental, já que o hidrogênio não tem pares de elétrons não-ligantes para doar).[carece de fontes]
Estudos em solução mostraram que a molécula de B
8Cl
8 é altamente fluxional, sofrendo rearranjos frequentes das ligações entre os boros em sua gaiola poliédrica.[4]
Síntese
O octacloreto de octaboro é produzido a partir do aquecimento de uma solução de B
2Cl
4 em tetracloreto de carbono (CCl
4) rigorosamente puro e seco a 50°C ao longo de duas semanas seguido de evaporação do solvente e sublimação a vácuo do resíduo sólido obtido[5]. Esta é a única rota de síntese conhecida que produz esse composto com um alto rendimento.[6]
- 8B
2Cl
4 → B
8Cl
8 + 8BCl
3
O octacloreto de octaboro também pode ser produzido a partir da passagem de uma descarga elétrica através do vapor de tetracloreto de diboro a baixa pressão, sendo co-gerado junto com vários outros clusters de subcloretos de boro, tais como B
4Cl
4, B
9Cl
9, B
10Cl
10 e B
11Cl
11. No entanto, o rendimento é baixo e a separação é difícil.[7]
Propriedades
O composto é um sólido cristalino verde-escuro quando puro. No entanto, quando depositado sobre uma superfície (geralmente por ressublimação), essa cor pode variar conforme a espessura da camada: camadas mais finas apresentam cor verde-escura; uma espessura um pouco maior tende a apresentar uma cor mais próxima ao castanho-preto ou preto-esverdeado enquanto camadas ainda mais espessas podem apresentar uma cor vermelha. Um fenômeno semelhante é observado em soluções de diferentes concentrações em diclorometano, com soluções mais diluídas (0,01 mol/L) sendo verdes mudando para preto-marrom ou mesmo avermelhada em alta concentração.[5]
O octacloreto de octaboro é um composto relativamente instável frente a reações de rearranjo induzido pelo calor. Ao ser aquecido, parte do composto pode ser convertida em outros oligômeros maiores por redistribuição, como os compostos B
9Cl
9, B
10Cl
10 e B
11Cl
11. Essas reações também podem ser induzidas por meio de algumas reações colaterais enquanto o octacloreto reage com traços de água, oxigênio ou agentes redutores. Amostras envelhecidas de B
8Cl
8 frequentemente estão contaminadas com os clusters maiores já descritos, bem como o ânion radicalar roxo.[5]
Traços de umidade ou compostos redutores presentes na solução podem levar à formação do ânion-radical de cor púrpura intensa, fazendo com que amostras impuras ou antigas de octacloreto de octaboro apresentem a cor roxa. A presença dos clusters maiores (como o B
9Cl
9 amarelo-laranja) juntamente com o octacloreto verde e o radical roxo podem fazer com que as amostras impuras tenham cor marrom ou preta.[5]
O octacloreto de octaboro é um sólido volátil que sofre sublimação a temperaturas moderadas. No entanto, sofre decomposição para outros agregados em temperaturas mais elevadas. Um método comum de purificação é a sublimação a vácuo na ausência de ar. Esse composto é solúvel em solventes orgânicos apróticos e inertes, tais como tetracloreto de carbono, clorofórmio, diclorometano, pentano e benzeno. Não reage com esses solventes quando estes se encontram rigorosamente puros, anidros e livres de alguns estabilizantes como o etanol, penteno, ciclohexeno etc; caso contrário, na presença desses compostos, ele reage com eles, sendo reduzido para o ânion radicalar e tornando a cor da solução em roxa. Também reage com a umidade do ar dando essa mesma coloração. No entanto, B
8Cl
8 não reage com HCl anidro gasoso ou dissolvido em solventes como o clorofórmio.[5] Essas reações ainda não são bem compreendidas.
Embora seja um dos clusters de oligômeros de "monocloreto de boro" mais estudados, ainda se conhece relativamente pouco sobre a química desse composto e dados sobre ele são escassos na literatura científica. Um dos motivos é a grande dificuldade de síntese e purificação dessa substância, bem como sua relativa instabilidade. A síntese do composto é complicada e exige a decomposição cuidadosa do tetracloreto de diboro em tetracloreto de carbono a 90°C em condições controladas ao longo de vários dias. Octacloreto de octaboro é sempre produzido em pequenas quantidades e não possui aplicações comerciais. Sua importância é geralmente restrita à pesquisa científica.
Reações
O octacloreto de octaboro é um forte agente oxidante: o composto neutro B
8Cl
8 de cor verde pode ser facilmente reduzido por agentes redutores como o íon iodeto (I–) em duas etapas, produzindo o íon-radical livre de cor púrpura intensa B
8Cl
8•– excepcionalmente estável, bem como o diânion incolor B
8Cl2–
8.[4][5]
- B
8Cl
8 + 2e–
B
8Cl
8•– + e–
B
8Cl2–
8
Soluções de B
8Cl
8 em tetracloreto de carbono ou clorofórmio são sensíveis a traços de umidade, mudando sua cor de esverdeado para roxo escuro na presença de traços de água, mesmo a umidade do ar.[5] O mecanismo da reação não é bem compreendido. É proposto que nessa reação, parte dos clusters de octacloreto de octaboro é hidrolisada pela água com liberação de gás hidrogênio, o qual reduz as moléculas do cluster neutro restante em solução para suas formas aniônicas.[6] Algumas reações possíveis são apresentadas:[8]
B
8Cl
8 + 24H
2O → 8H
3BO
3 + 8HCl + 8H
2
B
8Cl
8 + H
2 → B
8Cl2–
8 + 2H+
B
8Cl2–
8 + B
8Cl
8 2B
8Cl
8•-
A reação do B
8Cl
8 com alcenos em solução (como o ciclohexeno) também causa essa mudança de cor, e o mecanismo provável para essa ocorrência é a oxidação em um elétron da ligação dupla do alceno com a formação de um radical carbocátion (que sofre reações de dismutação e rearranjos subsequentes) e do ânion radical B
8Cl
8•–.[4] Muitas dessas reações leva também à formação de clusters maiores tais como B
9Cl
9, B
10Cl
10 e B
11Cl
11, que são impurezas comuns em amostras de octacloreto de octaboro.[4] No entanto, B
8Cl
8 não reage com alcanos e benzeno.[5]
- B
8Cl
8 + H
3C—CH=CH
2 → ‹H
3C—CH+—CH
2•› + [B
8Cl
8]•-
B
8Cl
8 é susceptível a sofrer reações de recombinação consigo mesmo para formar outros agregados de subcloretos de boro. Essa reação é induzida por aquecimento, luz, exposição ao ar e umidade. Tais reações de redistribuição formam outros compostos de clusters maiores tais como B
9Cl
9, B
10Cl
10 e B
11Cl
11.
- 9B
8Cl
8 → 8B
9Cl
9 - 10B
8Cl
8 → 8B
10Cl
10 - 11B
8Cl
8 → 8B
11Cl
11
Produtos de redução
Ao reagir com agentes redutores, o octacloreto de octaboro atua como um oxidante de um ou dois elétrons, podendo receber um elétron para formar a espécie aniônica radicalar [B
8Cl
8]•– de cor roxa profunda, ou receber dois elétrons para formar o diânion incolor muito estável e aromático [B
8Cl
8]2–.[6] A espécie dianiônica é um derivado direto por cloração completa do ânion closoborano B
8H2–
8.
O diânion incolor é bastante estável devido à sua ressonância aromática, e essa estabilidade é a força motriz que torna a redução do octacloreto de octaboro não-aromático para o diânion aromático um processo muito favorável, o que torna B
8Cl
8 um forte agente oxidante. Essa espécie aniônica é muito mais estável ao ar e água, não sofrendo hidrólise ou oxidação, ao contrário do composto parental.
No entanto, a forma radicalar semi-reduzida B
8Cl
8•– é uma espécie química notoriamente estável, podendo ocorrer em soluções ou mesmo ser isolada como sais estáveis.[6] Esse ânion radical é muito mais estável ao ar e à água do que o octacloreto de octaboro neutro. Sua intensa cor púrpura e a presença desse produto de redução em amostras de B
8Cl
8 menos puro (bem como a presença de outros compostos como o B
9Cl
9 laranja) é o motivo da inconsistência da descrição da cor real do B
8Cl
8 na literatura, que já foi referida como marrom, vermelha, verde, roxa ou preta (o composto puro é verde-escuro).[6]
Ver também
Referências
- ↑ https://pubs.aip.org/aip/jcp/article-abstract/31/3/601/75896/Molecular-and-Crystal-Structure-of-B8Cl8-I?redirectedFrom=fulltext
- ↑ https://pubs.acs.org/doi/10.1021/ja01553a065
- ↑ https://chem.libretexts.org/Bookshelves/Inorganic_Chemistry/Inorganic_Chemistry_(LibreTexts)/15%3A_Parallels_between_Main_Group_and_Organometallic_Chemistry/15.04%3A_Cluster_Compounds/15.4.01%3A_Boranes
- ↑ a b c d https://chemistry-europe.onlinelibrary.wiley.com/doi/10.1002/ejic.202100777
- ↑ a b c d e f g h ResearchGate https://www.researchgate.net › 355... Synthesis and Properties of the Octaboron Cluster Series hypercloso‐B8Cl8 ...
- ↑ a b c d e https://d-nb.info/1246119889/34
- ↑ https://pubs.acs.org/doi/10.1021/ja01142a542
- ↑ http://168.160.2.5/Archives/browse.do?action=viewDetail&articleID=bd5fac76bab241e0&navig=9565bcbb40dbfbe9&navigator=category&flag=byWord&subjectCode=null&searchfrom=null