Heptaborano-11
Heptaborano(11)
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
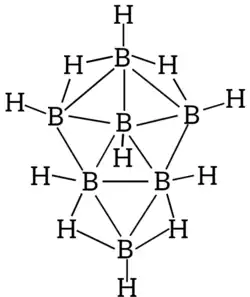
Heptaborano(11) é um composto químico pertencente à classe dos boranos, com fórmula molecular B7H11. Assim como outros boranos intermediários, apresenta estrutura eletronicamente deficiente e ligações multicêntricas características, descritas pela teoria de Wade–Mingos.[1][2]
Estrutura e ligação
O B7H11 é considerado um borano nido, derivado estruturalmente do closo-B8H82− pela remoção de um vértice. Sua estrutura contém ligações 3c–2e, conferindo estabilidade relativa, embora inferior a boranos mais pequenos (como B2H6) ou mais estáveis (como B10H14).[1]
Síntese
O heptaborano(11) não é encontrado comercialmente, sendo obtido apenas em laboratório sob condições controladas. Pode ser preparado por degradação térmica ou pirolítica de boranos maiores, como B10H14 (decaborano), resultando em misturas de boranos intermediários (B9H15, B8H12, B7H11).[3]
Propriedades
- Líquido incolor a amarelado, volátil e inflamável.
- Reage lentamente com água, liberando hidrogênio e ácido bórico.
- Apresenta odor característico, similar ao do decaborano, que lembra mofo ou chocolate amargo.
- Baixa estabilidade térmica: decompõe-se em temperaturas próximas à ebulição.
Heptaborano-11 é notável por sua baixa estabilidade: ele é difícil de isolar, existindo mais como um intermediário elusivo na formação de outros boranos. É menos estável que outros clusters de boranos próximos tais como o pentaborano-9, o hexaborano-10 e o octaborano-12. Ele rapidamente sofre quebra e rearranjo para formar outros boranos, bem como boro elementar e hidrogênio. Oxida-se muito facilmente e pode explodir na presença de oxigênio, oxidantes e haletos orgânicos.
Riscos e segurança
O B7H11 é um composto relativamente instável e altamente perigoso: é muito inflamável e pirofórico, podendo inflamar-se espontaneamente ao contato com o ar. Também é extremamente tóxico por inalação e absorção cutânea, causando irritações respiratórias, efeitos neurológicos graves e possível dano hepático.[4] Sua manipulação exige manuseio sob atmosfera inerte (argônio ou nitrogênio seco) e uso de proteção individual especializada.
Aplicações
Não possui aplicações práticas comerciais devido à sua instabilidade e toxicidade. É principalmente um composto de interesse acadêmico para o estudo da química dos clusters de boro.
Ver também
- Boranos
- Decaborano
- Octaborano-12
- Teoria de Wade–Mingos
Referências
- ↑ a b Grimes, R. N. Carboranes. 3rd Edition. Academic Press, 2016.
- ↑ Housecroft, C. E.; Sharpe, A. G. Inorganic Chemistry. 4th Edition. Pearson, 2012.
- ↑ Shriver, D. F.; Weller, M.; Overton, T.; Rourke, J.; Armstrong, F. Inorganic Chemistry. 4th Edition. W. H. Freeman, 2006.
- ↑ Weintraub, R. L.; Sweet, J. A.; Goldsmith, R. H. "Toxicity of Boron Hydrides." AMA Archives of Industrial Health, 1962, 25(6), 408–414.