Nucleosídeo trifosfato
Um nucleosídeo trifosfato, ou trifosfato de nucleosídeo, é uma molécula contendo uma base nitrogenada ligado a um açúcar de 5 carbonos (ribose ou desoxirribose), com três grupos fosfato ligados ao açúcar.[1] É um exemplo de um nucleotídeo. Eles são os precursores moleculares de ambos DNA e RNA, que são cadeias de nucleotídeos feitas através dos processos de replicação do DNA e transcrição.[2] Nucleosídeos trifosfatos também servem como fonte de energia para reações celulares[3] e estão envolvidos em vias de sinalização.[4]
Nucleosídeos trifosfatos não podem ser bem absorvidos, pelo que se sintetizam dentro da célula.[5] As vias de síntese são distintas dependendo do nucleósido trifosfato concreto que se vai formar, mas como têm importantes funções, a sua síntese é estritamente regulada em todos os casos.[6] Os análogos de nucleosídeo também pode ser usados para tratar infecções virais.[7] Por exemplo, azidotimidina (AZT) é um análogo de nucleosídeo usado para prevenir e tratar HIV/AIDS.[8]
Nomes
O termo nucleosídeo faz referência a uma molécula formada por uma base nitrogenada unida a um açúcar de 5 carbonos (ribose ou desoxirribose).[1] Os nucleótidos são nucleosídeos que estão ligados covalentemente a um grupo fosfato, o qual pode estar constituído, dependendo da definição utilizada, por um ácido fosfórico só,[9] ou por dous ou três.[10] Para proporcionar información sobre o número de fosfatos, os nucleótidos son denominados nucleosídeos monofosfato, difosfato ou trifosfato.[10][11] Por tanto, os nucleosídeos trifosfato são considerados tradicionalmente como um tipo de nucleótido.[10][12][11] Para a discussão da definição de nucleótido, ver a página nucleótido (existe certa ambiguidade entre a definição da IUPAC e os usos tradicionais em bioquímica, já que a IUPAC denomina nucleótidos só aos nucleosídeos monofosfato).[9]
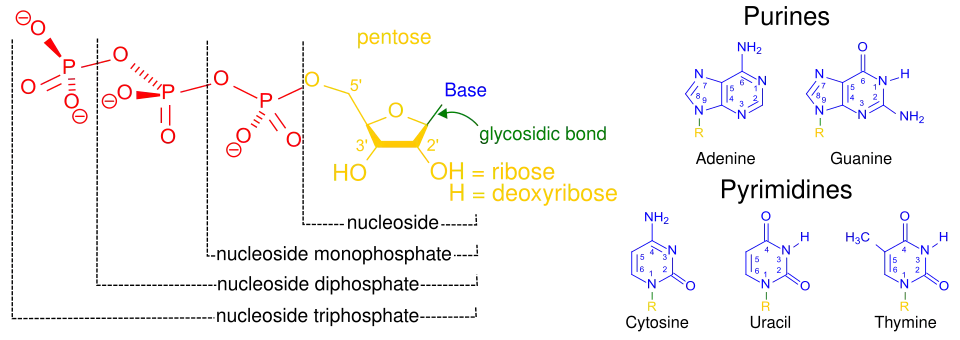
O nome dos nucleosídeos fosfato abrevia-se geralmente com uma sigla de três letras, que são 4 ou 5 no caso dos desoxi- ou didesoxinucleosídeos fosfato). A primeira letra indica a identidade da base nitrogenada (por exemplo, A por adenina, G por guanina), a segunda letra indica o número de fosfatos (mono, di, tri), e a terceira é P, que indica fosfato.[13] Os nucleosídeos trifosfato que contêm ribose como açúcar abrevia-se convencionalmente como NTPs, enquanto que os que contêm desoxirribose abrevia-se como dNTPs. Por exemplo, dATP seria a desoxirribose adenosina trifosfato. Os NTPs originam os nucleosídeos monofosfato que são as unidades que formam o ARN, e os dNTPs originam os nucleosídeos monofosfato que formam o ADN.[14] Os carbonos do açúcar de um nucleosídeo trifosfato numeram-se à volta do anel carbonado no sentido dos ponteiros do relógio empezando polo do grupo carbonilo original do açúcar. Convencionalmente, os números que indicam os carbonos do açúcar levam o símbolo prima (‘) para os distinguir dos carbonos da base nitrogenada. A base nitrogenada está ligada ao carbono 1’ por meio de uma ligação N-glicosídica e o grupo fosfato está ligado covalentemente ao carbono 5’ do açúcar por ligação fosfodiéster (ou às vezes ao 3'[9]). Os fosfatos estão ligados entre si por ligações anidro ácidas (ou fosfoanidro).[15] O primeiro fosfato ligado ao açúcar denomina-se α (fosfato alfa), o segundo é o β (beta) e o terceiro é o γ (gama).[16]
Síntese do ADN e ARN
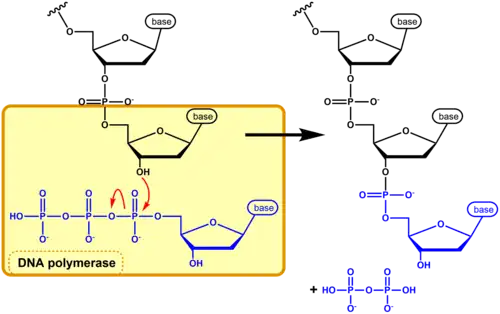
Os processos celulares da replicação do ADN e transcrição envolvem a síntese de ADN e ARN, respetivamente. A síntese de ADN usa dNTPs como substratos, enquanto que a síntese de ARN usa NTPs.[2] Os NTPs non se podem converter directamente en dNTPs. O ADN contém quatro bases nitrogenadas diferentes: adenina, guanina, citosina e timina. O ARN contém também adenina, guanina e citosina, mas no lugar de timina tem uracilo.[17] Por tanto, a síntese de ADN requer como substratos dATP, dGTP, dCTP e dTTP, enquanto que a de ARN necessita ATP, GTP, CTP e UTP.
A síntese de ácidos nucleicos é catalisada polos enzimas ADN polimerase, que realiza a síntese de ADN, ou ARN polimerase, que realiza a síntese de ARN.[18] Estes enzimas criam uma ligação covalente entre o grupo hidroxilo livre (-OH) do carbono 3’ do açúcar de uma cadeia de nucleótidos em crescimento e o fosfato α do carbono 5’ do seguinte (d)NTP, libertando juntos os fosfatos β e γ em forma de pirofosfato (PPi).[19] Isto resulta na formação de uma ligação fosfodiéster entre os dous (d)NTPs. A libertação do PPi proporciona a energia necessária para que a reação ocorra.[19] A síntese de ácidos nucleicos realiza-se na direção 5’-3’.
Metabolismo dos nucleosídeos trifosfato
Dada a sua importância na célula, a síntese e degradação de nucleosídeos trifosfato está sob um estreito controlo.[6] Este capítulo centra-se no metabolismo dos nucleosídeos trifosfato em humanos, mas o processo está muito conservado entre as espécies.[20] Os nucleosídeos trifosfato dos alimentos não se podem absorver bem, assim que todos os nucleosídeos trifosfato têm de ser formados de novo.[21] A síntese de ATP e GTP (purinas) é distinta da síntese de CTP, dTTP e UTP (pirimidinas). Tanto a síntese de purinas como a das pirimidinas utilizam o fosforribosil pirofosfato (PRPP) como molécula de início.[22]
A conversão de NTPs em dNTPs só pode ser realizada na forma de difosfatos. A um NTP remove-se-lhe um fosfato, convertindo-o num NDP, depois é convertido num dNDP por um enzima chamado ribonucleótido redutase, depois adiciona-se de novo um fosfato para dar lugar a um dNTP.[23]
Síntese de Purinas
A base nitrogenada hipoxantina é montada diretamente com o PRPP.[24] Isto origina um nucleótido chamado inosina monofosfato (IMP). O IMP converte-se depois num precursor do AMP ou do GMP. Uma vez que se formam o AMP ou o GMP, podem ser fosforilados pelo ATP originando as formas difosfato e trifosfato.[25]
A síntese de purinas é regulada por inibição alostérica da formação de IMP realizada pelos nucleótidos de adenina e guanina.[26] O AMP e o GMP também inibem competitivamente a formação dos seus precursores a partir de IMP.[27]
Síntese de Pirimidinas
A base nitrogenada orotato sintetiza-se independentemente do PRPP.[27] Depois o orotato liga-se covalentemente ao PRPP, originando o nucleótido orotato monofosfato (OMP).[28] O OMP converte-se em UMP, o qual pode ser depois fosforilado pelo ATP a UDP e UTP. O UTP pode depois converter-se em CTP por meio de uma reação de desaminação.[29] O dTTP forma-se indiretamente a partir de dUDP ou dCDP.[22]
A síntese de pirimidinas é regulada pela inibição da síntese de orotato pelo UDP e UTP. Além disso, o PRPP e o ATP são também ativadores alostéricos da síntese de orotato.[30]
Ribonucleótido Redutase
A ribonucleótido redutase (RNR) é o enzima responsável pela conversão de NTPs em dNTPs. Como os dNTPs se usam na replicação do ADN, a atividade da RNR está muito regulada.[6] O enzima RNR somente pode processar NDPs, pelo que os NTPs são primeiramente desfosforilados a NDPs antes da sua conversão em dNDPs.[31] Os dNDPs são depois refosforilados. A RNR tem dous subunidades e 3 sítios para a ligação de moléculas: o sítio catalítico, o sítio de atividade (A) e o sítio de especificidade (S).[31] O sítio catalítico é onde tem lugar a reação de passagem do NDP a dNDP; o sítio de atividade determina se o enzima está ativo ou não, e o sítio de especificidade determina que reação terá lugar no sítio catalítico.
Ao sítio de atividade pode ligar-se o ATP ou o dATP.[32] Quando se liga o ATP, a RNR está ativa. Quando se ligam o ATP ou o dATP ao sítio S, a RNR catalisa a síntese de dCDP e dUDP a partir de CDP e UDP. O dCDP e o dUDP podem depois dar lugar indiretamente a dTTP. O dTTP ligado ao sítio S determina a síntese de dGDP a partir de GDP, e a ligação de dGDP ao sítio S promove a síntese de dADP a partir de ADP.[33] O dADP é depois fosforilado para dar dATP, o qual se pode ligar ao sítio A e inativar a RNR.[32]
Outras funções nas células
O ATP como fonte de energia celular
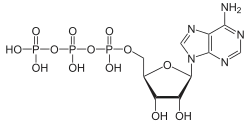
O ATP é a molécula que funciona como fonte de energia primária da célula.[34] Embora seja sintetizado pela via metabólica descrita anteriormente, é produzido principalmente durante a respiração celular[35] e fotossíntese[36] pela ATP sintase. A ATP sintase acopla a síntese de ATP a partir de ADP e fosfato com um gradiente eletroquímico gerado pelo bombeamento de protões através da membrana mitocondrial interna (na respiração celular) ou da membrana tilacoidal (na fotossíntese e fosforilação fotossintética).[37] Este gradiente eletroquímico é necessário porque a formação de ATP é energeticamente desfavorável.
A hidrólise do ATP a ADP e Pi ocorre como se segue:[38]
Esta reação é energeticamente favorável e liberta 30,5 kJ/mol de energia.[3] Na célula esta reação é frequentemente acoplada a reações desfavoráveis para proporcionar a enerxía que a torna possível.[39] O GTP é utilizado ocasionalmente para o acoplamento de energia de forma similar.[40]
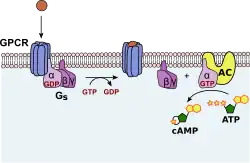
Transdução de sinais do GTP
O GTP é essencial para a transdução de sinais, especialmente com a proteína G. As proteínas G estão acopladas a um receptor ligado à membrana celular.[4] Este complexo completo denomina-se receptor acoplado à proteína G (GPCR). As proteínas G podem ligar-se ao GDP ou ao GTP. Quando se ligam ao GDP, as proteínas G estão inativas. Quando um ligando se liga ao GPCR, desencadeia-se uma alteração alostérica na proteína G, causando que o GDP saia e seja substituído por GTP.[41] O GTP ativa a subunidade alfa da proteína G, causando que esta se dissocie da proteína G e atue como efetor a jusante.[41]
Análogos de nucleosídeos
Podem ser utilizados análogos de nucleosídeos para tratar infeções virais.[42]Os análogos de nucleosídeos são nucleosídeos estruturalmente similares (análogos) aos nucleosídeos usados na síntese de ADN e ARN.[43] Uma vez que estes análogos de nucleosídeos entram na célula, podem ser fosforilados por um enzima viral. Os nucleótidos resultantes são suficientemente similares aos nucleótidos normais do ADN ou ARN para serem incorporados nas cadeias em crescimento de ADN ou ARN durante a sua síntese, mas não têm um grupo 3' OH disponível para atacar o seguinte nucleótido, causando a terminação da cadeia.[44] Isto pode ser explorado para usos terapêuticos em infeções virais porque a ADN polimerase viral reconhece certos análogos de nucleótidos mais facilmente do que a ADN polimerase eucariota.[42] Por exemplo, a azidotimidina é utilizada no tratamento da VIH/SIDA.[8] Alguns análogos de nucleosídeos menos seletivos podem ser utilizados como agentes quimioterápicos para tratar o cancro,[45] como a citosina arabinosa (ara-C) no tratamento de certas formas de leucemia.[7]
Contudo, a resistência a análogos de nucleosídeos é comum e deve-se frequentemente a uma mutação no enzima que fosforila o nucleosídeo depois da entrada na célula.[7] Isto é algo comum com os análogos de nucleosídeos utilizados para tratar a VIH/SIDA.[46]
Referências
- ↑ a b «Nucleotides and Bases - Genetics Generation». Genetics Generation. 11 de novembro de 2017
- ↑ a b Chargaff E (2 de dezembro de 2012). The Nucleic Acids. [S.l.]: Elsevier. ISBN 9780323144773
- ↑ a b «Khan Academy». Overview of ATP Hydrolysis. Consultado em 11 de novembro de 2017. Arquivado do original em 1 de dezembro de 2017
- ↑ a b «GPCR». Scitable. 2014
- ↑ «Eating DNA: Dietary Nucleotides in Nutrition». The call of the Honeyguide. 9 de abril de 2014. Consultado em 11 de novembro de 2017
- ↑ a b c Wyngaarden, JB (1976). «Regulation of purine biosynthesis and turnover». Advances in Enzyme Regulation. 14: 25–42. PMID 184697. doi:10.1016/0065-2571(76)90006-6
- ↑ a b c Galmarini CM, Mackey JR, Dumontet C (2001). «Nucleoside analogues: mechanisms of drug resistance and reversal strategies». Leukemia. 15 (6): 875–90. PMID 11417472. doi:10.1038/sj.leu.2402114
- ↑ a b «Zidovudine Monograph for Professionals - Drugs.com». Drugs.com. Consultado em 30 de novembro de 2017
- ↑ a b c IUPAC Gold book nucleotide
- ↑ a b c Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J (2000). Structure of Nucleic Acids. [S.l.: s.n.]
Nucleotides are nucleosides that have one, two, or three phosphate groups esterified at the 5′ hydroxyl. (Os nucleótidos são nucleosídeos que têm um, dous ou três grupos fosfato esterificados no hidroxilo 5').
- ↑ a b Secrist JA (maio de 2001). «Nucleoside and nucleotide nomenclature» (PDF). Current Protocols in Nucleic Acid Chemistry. Appendix 1: A.1D.1–A.1D.3. PMID 18428808. doi:10.1002/0471142700.nca01ds00. hdl:2027.42/143595
- ↑ Bruce Alberts et al. Biología molecular de la célula. Omega. Páginas 58, 62, 63. ISBN: 84-282-0752-86. Citação: "Los nucleótidos pueden actuar como transportadores de enerxía química. Sobre todo, el éster trifosfato de la adenina, ATP". ("Os nucleótidos podem atuar como transportadores de energia química. Sobretudo, o éster trifosfato da adenina, ATP").
- ↑ «Nomenclature of Nucleosides». www.biochem.uthscsa.edu. Consultado em 11 de novembro de 2017. Cópia arquivada em 22 de setembro de 2019
- ↑ «From DNA to RNA to protein, how does it work?». Science Explained. Consultado em 11 de novembro de 2017
- ↑ «Numbering convention for nucleotides». www.biosyn.com. Consultado em 11 de novembro de 2017
- ↑ «SparkNotes: DNA Replication and Repair: The Chemistry of the Addition of Substrates of DNA Replication». www.sparknotes.com. Consultado em 11 de novembro de 2017
- ↑ «Do You Know the Differences Between DNA and RNA?». ThoughtCo. Consultado em 11 de novembro de 2017
- ↑ «Difference Between DNA Polymerase and RNA Polymerase». 24 de dezembro de 2011. Consultado em 11 de novembro de 2017
- ↑ a b Lodish H, Berk A, Zipursky SL, Matsudaira P, Baltimore D, Darnell J (2000). Nucleic Acid Synthesis. [S.l.: s.n.]
- ↑ Samant S, Lee H, Ghassemi M, Chen J, Cook JL, Mankin AS, Neyfakh AA (fevereiro de 2008). «Nucleotide biosynthesis is critical for growth of bacteria in human blood». PLOS Pathogens. 4 (2): e37. PMC 2242838
 . PMID 18282099. doi:10.1371/journal.ppat.0040037
. PMID 18282099. doi:10.1371/journal.ppat.0040037
- ↑ Berg JM, Tymoczko JL, Stryer L (2002). Nucleotide Biosynthesis. [S.l.: s.n.]
- ↑ a b «Nucleotide Metabolism: Nucleic Acid Synthesis». themedicalbiochemistrypage.org. Consultado em 15 de novembro de 2017
- ↑ Stubbe J (1990). «Ribonucleotide reductases: amazing and confusing» (PDF). The Journal of Biological Chemistry. 265 (10): 5329–32. PMID 2180924. doi:10.1016/S0021-9258(19)39357-3
- ↑ Berg J, Tymoczko JL, Stryer L (2002). Purine Bases Can Be Synthesized de Novo or Recycled by Salvage Pathways. [S.l.: s.n.]
- ↑ «Purine Synthesis : Synthesis of Purine RiboNucleotides». BiochemDen.com. 16 de março de 2016. Consultado em 15 de novembro de 2017
- ↑ Berg JM, Tymoczko JL, Stryer L (2002). Key Steps in Nucleotide Biosynthesis Are Regulated by Feedback Inhibition. [S.l.: s.n.]
- ↑ a b Nierlich DP, Magasanik B (1965). «Regulation of purine ribonucleotide synthesis by end product inhibition. the effect of adenine and guanine ribonucleotides on the 5'-phosphoribosyl-pyrophosphate amidotransferase of aerobacter aerogenes». The Journal of Biological Chemistry. 240: 358–65. PMID 14253438. doi:10.1016/S0021-9258(18)97657-X
- ↑ Moffatt BA, Ashihara H (abril de 2002). «Purine and pyrimidine nucleotide synthesis and metabolism». The Arabidopsis Book. 1: e0018. PMC 3243375
 . PMID 22303196. doi:10.1199/tab.0018
. PMID 22303196. doi:10.1199/tab.0018
- ↑ «Pyrimidine Metabolism». www.cliffsnotes.com. Consultado em 15 de novembro de 2017
- ↑ Lane AN, Fan TW (fevereiro de 2015). «Regulation of mammalian nucleotide metabolism and biosynthesis». Nucleic Acids Research. 43 (4): 2466–85. PMC 4344498
 . PMID 25628363. doi:10.1093/nar/gkv047
. PMID 25628363. doi:10.1093/nar/gkv047
- ↑ a b Kolberg M, Strand KR, Graff P, Andersson KK (junho de 2004). «Structure, function, and mechanism of ribonucleotide reductases». Biochimica et Biophysica Acta. 1699 (1–2): 1–34. PMID 15158709. doi:10.1016/j.bbapap.2004.02.007
- ↑ a b Ahmad MF, Dealwis CG (2013). «The Structural Basis for the Allosteric Regulation of Ribonucleotide Reductase». Oligomerization in Health and Disease. Col: Progress in Molecular Biology and Translational Science. 117. [S.l.: s.n.] pp. 389–410. ISBN 9780123869319. PMC 4059395
 . PMID 23663976. doi:10.1016/B978-0-12-386931-9.00014-3
. PMID 23663976. doi:10.1016/B978-0-12-386931-9.00014-3
- ↑ Fairman JW, Wijerathna SR, Ahmad MF, Xu H, Nakano R, Jha S, Prendergast J, Welin RM, Flodin S, Roos A, Nordlund P, Li Z, Walz T, Dealwis CG (março de 2011). «Structural basis for allosteric regulation of human ribonucleotide reductase by nucleotide-induced oligomerization». Nature Structural & Molecular Biology. 18 (3): 316–22. PMC 3101628
 . PMID 21336276. doi:10.1038/nsmb.2007
. PMID 21336276. doi:10.1038/nsmb.2007
- ↑ «ATP». Scitable
- ↑ «Mitochondria, Cell Energy, ATP Synthase». Scitable
- ↑ «ATP Synthesis». Plants in Action. Consultado em 12 de novembro de 2017. Cópia arquivada em 24 de julho de 2021
- ↑ Jonckheere AI, Smeitink JA, Rodenburg RJ (março de 2012). «Mitochondrial ATP synthase: architecture, function and pathology». Journal of Inherited Metabolic Disease. 35 (2): 211–25. PMC 3278611
 . PMID 21874297. doi:10.1007/s10545-011-9382-9
. PMID 21874297. doi:10.1007/s10545-011-9382-9
- ↑ Dittrich M, Hayashi S, Schulten K (outubro de 2003). «On the mechanism of ATP hydrolysis in F1-ATPase». Biophysical Journal. 85 (4): 2253–66. Bibcode:2003BpJ....85.2253D. PMC 1303451
 . PMID 14507690. doi:10.1016/S0006-3495(03)74650-5
. PMID 14507690. doi:10.1016/S0006-3495(03)74650-5
- ↑ «ATP: Adenosine Triphosphate». courses.lumenlearning.com-US. Consultado em 12 de novembro de 2017 Texto " Boundless Biology" ignorado (ajuda)
- ↑ Carvalho AT, Szeler K, Vavitsas K, Åqvist J, Kamerlin SC (setembro de 2015). «Modeling the mechanisms of biological GTP hydrolysis». Archives of Biochemistry and Biophysics. Special issue in computational modeling on biological systems. 582 (Supplement C): 80–90. PMID 25731854. doi:10.1016/j.abb.2015.02.027
- ↑ a b «G protein-coupled receptor (GPCR)». Encyclopedia Britannica. Consultado em 12 de novembro de 2017 Texto " biochemistry" ignorado (ajuda)
- ↑ a b «Nucleoside Analogues». Molecules. Consultado em 13 de novembro de 2017
- ↑ Jordheim LP, Durantel D, Zoulim F, Dumontet C (junho 2013). «Advances in the development of nucleoside and nucleotide analogues for cancer and viral diseases». Nature Reviews. Drug Discovery. 12 (6): 447–64. PMID 23722347. doi:10.1038/nrd4010
- ↑ Ewald B, Sampath D, Plunkett W (outubro de 2008). «Nucleoside analogs: molecular mechanisms signaling cell death». Oncogene. 27 (50): 6522–37. PMID 18955977. doi:10.1038/onc.2008.316
- ↑ Galmarini CM, Mackey JR, Dumontet C (julho de 2002). «Nucleoside analogues and nucleobases in cancer treatment». The Lancet. Oncology. 3 (7): 415–24. PMID 12142171. doi:10.1016/s1470-2045(02)00788-x
- ↑ Menéndez-Arias L (junho de 2008). «Mechanisms of resistance to nucleoside analogue inhibitors of HIV-1 reverse transcriptase». Virus Research. 134 (1–2): 124–46. PMID 18272247. doi:10.1016/j.virusres.2007.12.015