Desmetilase
Desmetilases são enzimas que removem grupos metil (CH3) de ácidos nucleicos, proteínas (especialmente histonas) e outras moléculas. As desmetilases são proteínas epigenéticas importantes, pois regulam a transcrição do genoma ao controlar a metilação de DNA e histonas, influenciando, assim, o estado da cromatina em loci gênicos específicos.
Desmetilação de lisina em histonas
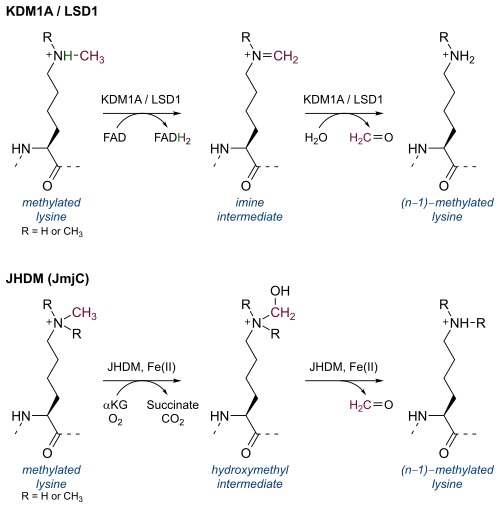
A metilação de histona [en] era inicialmente considerada um processo praticamente irreversível, pois a meia-vida da metilação de histonas era aproximadamente igual à meia-vida das próprias histonas.[1] A histona lisina desmetilase LSD1 (posteriormente classificada como KDM1A) foi identificada em 2004 como um homólogo da amina oxidase nuclear.[2] Existem duas classes principais de histona lisina desmetilases, definidas por seus mecanismos: amina oxidases [en] dependentes de flavina adenina dinucleotídeo (FAD) e hidroxilases dependentes de α-cetoglutarato [en].
As histona lisina desmetilases possuem diversos domínios responsáveis pelo reconhecimento de histonas, ligação ao DNA, ligação a substratos de aminoácido metilado e atividade catalítica. Esses incluem:
- Domínios de amina oxidase dependentes de FAD, contendo o sítio catalítico ativo de KDM1
- Domínios Jumonji-C, contendo o sítio catalítico ativo de KDM2 a KDM8[3][4]
- Domínios Jumonji-N, responsáveis pela estabilidade conformacional do domínio Jumonji-C
- Domínios SWIRM (SWI3P, RSC8P e Moira), propostos como sítios de ancoragem para substratos de histonas e responsáveis pela estabilidade da cromatina
- Domínios de dedo de zinco PHD, CXXC e C5HC2, responsáveis pelo reconhecimento e ligação a histonas
As histona lisina desmetilases são classificadas de acordo com seus domínios e especificidades de substrato. Os substratos de lisina são identificados por sua posição na sequência de aminoácidos da histona correspondente e pelo estado de metilação (por exemplo, H3K9me3 refere-se à histona 3 lisina 9 trimetilada).
_with_domains_highlighted.png)
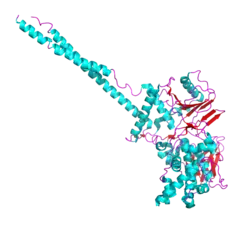
- KDM1
- Os homólogos KDM1 incluem KDM1A [en] e KDM1B [en]. KDM1A desmetila H3K4me1/2 e H3K9me1/2, enquanto KDM1B desmetila H3K4me1/2. A atividade de KDM1 é crucial para a embriogênese e a diferenciação celular tecido-específica, além do crescimento de oócitos.[1] A deleção do gene para KDM1A afeta o crescimento e a diferenciação de células-tronco embrionárias e é universalmente letal em ratos knockout.[5][6] A expressão do gene KDM1A é observada como aumentada em alguns cânceres,[7][8] tornando a inibição de KDM1A uma possível abordagem epigenética para o tratamento do câncer.[9][10][11] Por outro lado, KDM1B está mais envolvida no desenvolvimento de oócitos. A deleção desse gene leva à letalidade por efeito materno em camundongos.[12] Ortólogos de KDM1 em Drosophila melanogaster e Caenorhabditis elegans parecem funcionar de maneira semelhante a KDM1B, em vez de KDM1A.[13][14]
- KDM2
- Os homólogos KDM2 incluem KDM2A [en] e KDM2B [en]. KDM2A e KDM2B desmetilam H3K4me3 e H3K36me2/3. KDM2A pode promover ou inibir funções tumorais, enquanto KDM2B está envolvida na oncogênese.[1] KDM2A e KDM2B possuem domínios de dedo de zinco CXXC, responsáveis pela ligação a ilhas CpG não metiladas, e acredita-se que possam se ligar a muitos elementos regulatórios de genes na ausência de fatores de transcrição específicos.[15] A superexpressão de KDM2B foi observada em linfomas e adenocarcinomas humanos, enquanto a subexpressão de KDM2B foi observada em câncer de próstata e glioblastoma. Além disso, KDM2B demonstrou prevenir senescência em algumas células por meio de expressão ectópica.[16]
- KDM3
- Os homólogos KDM3 incluem KDM3A [en], KDM3B [en] e KDM3C [en]. Eles desmetilam H3K9me1/2. KDM3A está envolvida na espermatogênese e em funções metabólicas, mas as atividades de KDM3B e KDM3C não são especificamente conhecidas.[1] Estudos de knockdown de KDM3A em camundongos resultaram em infertilidade masculina e obesidade de início adulto. Estudos adicionais indicaram que KDM3A pode regular genes dependentes de receptor de androgênio e genes envolvidos na pluripotência, sugerindo um papel potencial na tumorigênese.[17]
- KDM4
- Os homólogos KDM4 incluem KDM4A [en], KDM4B [en], KDM4C [en], KDM4D [en], KDM4E e KDM4F. KDM4A, KDM4B e KDM4C desmetilam H3K9me2/3, H3K9me3 e H3K36me2/3, enquanto KDM4D, KDM4E e KDM4F desmetilam H3K9me2/3. KDM4A, KDM4B, KDM4C e KDM4D estão envolvidos na tumorigênese, mas as atividades de KDM4E e KDM4F não são especificamente conhecidas.[1] A regulação positiva de KDM4B foi observada em meduloblastoma, e a amplificação de KDM4C foi documentada em carcinoma escamoso de esôfago, meduloblastoma e câncer de mama.[18][19][20][21] Outros dados de expressão gênica também sugeriram que KDM4A, KDM4B e KDM4C estão superexpressos em câncer de próstata.[22]
- KDM5
- Os homólogos KDM5 incluem KDM5A [en], KDM5B [en], KDM5C [en] e KDM5D [en]. eles desmetilam H3K4me2/3.[1] A família KDM5 parece regular funções-chave de desenvolvimento, incluindo diferenciação celular, função mitocondrial e progressão do ciclo celular.[23][24][25][26][27][28] KDM5B e KDM5C também interagem com proteínas PcG, envolvidas na repressão transcricional. Mutações de KDM5C no cromossomo X foram observadas em pacientes com deficiência intelectual ligada ao X.[29] A depleção de homólogos de KDM5C em D. rerio resultou em defeitos no padrão cerebral e morte de células neuronais.[30]
- KDM6
- A família KDM6 inclui KDM6A [en], KDM6B [en] e KDM6C [en]. KDM6A e KDM6B desmetilam H3K27me2/3, e KDM6C desmetila H3K27me3. KDM6A e KDM6B possuem características supressoras de tumores. Knockdowns de KDM6A em fibroblastos levam a um aumento imediato na população de fibroblastos. KDM6B expresso em fibroblastos induz oncogenes da via Ras/Raf/MEK/ERK.[31] Mutações pontuais de KDM6A foram identificadas como uma causa da síndrome de Kabuki [en], um distúrbio congênito que resulta em deficiência intelectual.[32][33] A deleção de KDM6A em D. rerio resulta em expressão reduzida de genes HOX, que regulam o padrão corporal [en] durante o desenvolvimento.[34] Em estudos mamíferos, KDM6A também regula genes HOX.[35][36] Mutações de KDM5B afetam o desenvolvimento gonadal em C. elegans.[35] Outros estudos mostraram que a expressão de KDM6B é regulada positivamente em macrófagos ativados e expressa dinamicamente durante a diferenciação de células-tronco.[37][38]
Desmetilação de ésteres
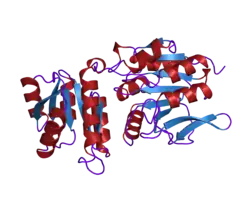
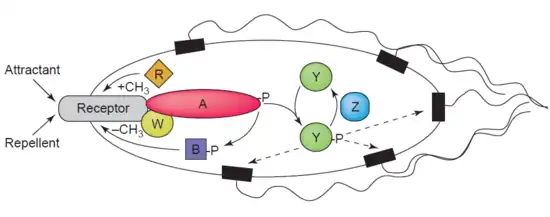
Outro exemplo de desmetilase é a proteína-glutamato metilesterase [en], também conhecida como proteína CheB (EC 3.1.1.61), que desmetila MCPs (Metil-aceptores de Quimiotaxia Proteínas) por hidrólise de ligações éster carboxílicas. A associação de um receptor de quimiotaxia com um agonista leva à fosforilação da proteína CheB. A fosforilação de CheB aumenta sua atividade catalítica de desmetilação de MCPs, resultando na adaptação da célula a estímulos ambientais.[39] Os MCPs respondem a atrativos e repelentes extracelulares em bactérias como Escherichia coli na regulação da quimiotaxia. A CheB é mais especificamente chamada de metilesterase, pois remove grupos metil de resíduos de metilglutamato [en] localizados nos MCPs por hidrólise, produzindo glutamato acompanhado da liberação de metanol.[40]
A CheB é de particular interesse para pesquisadores, pois pode ser um alvo terapêutico para mitigar a propagação de infecções bacterianas.[41]
Ver também
Referências
- ↑ a b c d e f Pedersen MT, Helin K (Nov 2010). «Histone demethylases in development and disease». Trends in Cell Biology. 20 (11): 662–71. PMID 20863703. doi:10.1016/j.tcb.2010.08.011
- ↑ Shi Y, Lan F, Matson C, Mulligan P, Whetstine JR, Cole PA, Casero RA, Shi Y (Dezembro de 2004). «Histone demethylation mediated by the nuclear amine oxidase homolog LSD1». Cell. 119 (7): 941–53. PMID 15620353. doi:10.1016/j.cell.2004.12.012

- ↑ Mosammaparast N, Shi Y (2010). «Reversal of histone methylation: biochemical and molecular mechanisms of histone demethylases». Annual Review of Biochemistry. 79: 155–79. PMID 20373914. doi:10.1146/annurev.biochem.78.070907.103946
- ↑ Aprelikova O, Chen K, El Touny LH, Brignatz-Guittard C, Han J, Qiu T, Yang HH, Lee MP, Zhu M, Green JE (Abril de 2016). «The epigenetic modifier JMJD6 is amplified in mammary tumors and cooperates with c-Myc to enhance cellular transformation, tumor progression, and metastasis». Clin Epigenetics. 8 (38): 38. PMC 4831179
 . PMID 27081402. doi:10.1186/s13148-016-0205-6
. PMID 27081402. doi:10.1186/s13148-016-0205-6
- ↑ Wang J, Hevi S, Kurash JK, Lei H, Gay F, Bajko J, Su H, Sun W, Chang H, Xu G, Gaudet F, Li E, Chen T (Jan 2009). «The lysine demethylase LSD1 (KDM1) is required for maintenance of global DNA methylation». Nature Genetics. 41 (1): 125–9. PMID 19098913. doi:10.1038/ng.268
- ↑ Wang J, Scully K, Zhu X, Cai L, Zhang J, Prefontaine GG, Krones A, Ohgi KA, Zhu P, Garcia-Bassets I, Liu F, Taylor H, Lozach J, Jayes FL, Korach KS, Glass CK, Fu XD, Rosenfeld MG (Abril de 2007). «Opposing LSD1 complexes function in developmental gene activation and repression programmes». Nature. 446 (7138): 882–7. Bibcode:2007Natur.446..882W. PMID 17392792. doi:10.1038/nature05671
- ↑ Kahl P, Gullotti L, Heukamp LC, Wolf S, Friedrichs N, Vorreuther R, Solleder G, Bastian PJ, Ellinger J, Metzger E, Schüle R, Buettner R (Dezembro de 2006). «Androgen receptor coactivators lysine-specific histone demethylase 1 and four and a half LIM domain protein 2 predict risk of prostate cancer recurrence». Cancer Research. 66 (23): 11341–7. PMID 17145880. doi:10.1158/0008-5472.CAN-06-1570
- ↑ Lim S, Janzer A, Becker A, Zimmer A, Schüle R, Buettner R, Kirfel J (Mar 2010). «Lysine-specific demethylase 1 (LSD1) is highly expressed in ER-negative breast cancers and a biomarker predicting aggressive biology». Carcinogenesis. 31 (3): 512–20. PMID 20042638. doi:10.1093/carcin/bgp324
- ↑ Metzger E, Wissmann M, Yin N, Müller JM, Schneider R, Peters AH, Günther T, Buettner R, Schüle R (Setembro de 2005). «LSD1 demethylates repressive histone marks to promote androgen-receptor-dependent transcription». Nature. 437 (7057): 436–9. Bibcode:2005Natur.437..436M. PMID 16079795. doi:10.1038/nature04020
- ↑ Schulte JH, Lim S, Schramm A, Friedrichs N, Koster J, Versteeg R, Ora I, Pajtler K, Klein-Hitpass L, Kuhfittig-Kulle S, Metzger E, Schüle R, Eggert A, Buettner R, Kirfel J (Mar 2009). «Lysine-specific demethylase 1 is strongly expressed in poorly differentiated neuroblastoma: implications for therapy». Cancer Research. 69 (5): 2065–71. PMID 19223552. doi:10.1158/0008-5472.CAN-08-1735

- ↑ Wang Y, Zhang H, Chen Y, Sun Y, Yang F, Yu W, Liang J, Sun L, Yang X, Shi L, Li R, Li Y, Zhang Y, Li Q, Yi X, Shang Y (Agosto de 2009). «LSD1 is a subunit of the NuRD complex and targets the metastasis programs in breast cancer». Cell. 138 (4): 660–72. PMID 19703393. doi:10.1016/j.cell.2009.05.050

- ↑ Ciccone DN, Su H, Hevi S, Gay F, Lei H, Bajko J, Xu G, Li E, Chen T (Setembro de 2009). «KDM1B is a histone H3K4 demethylase required to establish maternal genomic imprints». Nature. 461 (7262): 415–8. Bibcode:2009Natur.461..415C. PMID 19727073. doi:10.1038/nature08315
- ↑ Rudolph T, Yonezawa M, Lein S, Heidrich K, Kubicek S, Schäfer C, Phalke S, Walther M, Schmidt A, Jenuwein T, Reuter G (Abril de 2007). «Heterochromatin formation in Drosophila is initiated through active removal of H3K4 methylation by the LSD1 homolog SU(VAR)3-3». Molecular Cell. 26 (1): 103–15. PMID 17434130. doi:10.1016/j.molcel.2007.02.025

- ↑ Di Stefano L, Ji JY, Moon NS, Herr A, Dyson N (Maio de 2007). «Mutation of Drosophila Lsd1 disrupts H3-K4 methylation, resulting in tissue-specific defects during development». Current Biology. 17 (9): 808–12. PMC 1909692
 . PMID 17462898. doi:10.1016/j.cub.2007.03.068
. PMID 17462898. doi:10.1016/j.cub.2007.03.068
- ↑ Blackledge NP, Zhou JC, Tolstorukov MY, Farcas AM, Park PJ, Klose RJ (Abril de 2010). «CpG islands recruit a histone H3 lysine 36 demethylase». Molecular Cell. 38 (2): 179–90. PMC 3098377
 . PMID 20417597. doi:10.1016/j.molcel.2010.04.009
. PMID 20417597. doi:10.1016/j.molcel.2010.04.009
- ↑ He J, Kallin EM, Tsukada Y, Zhang Y (Nov 2008). «The H3K36 demethylase Jhdm1b/Kdm2b regulates cell proliferation and senescence through p15(Ink4b)». Nature Structural & Molecular Biology. 15 (11): 1169–75. PMC 2612995
 . PMID 18836456. doi:10.1038/nsmb.1499
. PMID 18836456. doi:10.1038/nsmb.1499
- ↑ Loh YH, Zhang W, Chen X, George J, Ng HH (Outubro de 2007). «Jmjd1a and Jmjd2c histone H3 Lys 9 demethylases regulate self-renewal in embryonic stem cells». Genes & Development. 21 (20): 2545–57. PMC 2000320
 . PMID 17938240. doi:10.1101/gad.1588207
. PMID 17938240. doi:10.1101/gad.1588207
- ↑ Ehrbrecht A, Müller U, Wolter M, Hoischen A, Koch A, Radlwimmer B, Actor B, Mincheva A, Pietsch T, Lichter P, Reifenberger G, Weber RG (Mar 2006). «Comprehensive genomic analysis of desmoplastic medulloblastomas: identification of novel amplified genes and separate evaluation of the different histological components». The Journal of Pathology. 208 (4): 554–63. PMID 16400626. doi:10.1002/path.1925
- ↑ Liu G, Bollig-Fischer A, Kreike B, van de Vijver MJ, Abrams J, Ethier SP, Yang ZQ (Dezembro de 2009). «Genomic amplification and oncogenic properties of the GASC1 histone demethylase gene in breast cancer». Oncogene. 28 (50): 4491–500. PMC 2795798
 . PMID 19784073. doi:10.1038/onc.2009.297
. PMID 19784073. doi:10.1038/onc.2009.297
- ↑ Northcott PA, Nakahara Y, Wu X, Feuk L, Ellison DW, Croul S, Mack S, Kongkham PN, Peacock J, Dubuc A, Ra YS, Zilberberg K, McLeod J, Scherer SW, Sunil Rao J, Eberhart CG, Grajkowska W, Gillespie Y, Lach B, Grundy R, Pollack IF, Hamilton RL, Van Meter T, Carlotti CG, Boop F, Bigner D, Gilbertson RJ, Rutka JT, Taylor MD (Abril de 2009). «Multiple recurrent genetic events converge on control of histone lysine methylation in medulloblastoma». Nature Genetics. 41 (4): 465–72. PMC 4454371
 . PMID 19270706. doi:10.1038/ng.336
. PMID 19270706. doi:10.1038/ng.336
- ↑ Yang ZQ, Imoto I, Fukuda Y, Pimkhaokham A, Shimada Y, Imamura M, Sugano S, Nakamura Y, Inazawa J (Setembro de 2000). «Identification of a novel gene, GASC1, within an amplicon at 9p23-24 frequently detected in esophageal cancer cell lines». Cancer Research. 60 (17): 4735–9. PMID 10987278
- ↑ «The putative oncogene GASC1 demethylates tri- and dimethylated lysine 9 on histone H3». Nature. 442 (7100): 307–11. Jul 2006. Bibcode:2006Natur.442..307C. PMID 16732293. doi:10.1038/nature04837
- ↑ Lee N, Erdjument-Bromage H, Tempst P, Jones RS, Zhang Y (Mar 2009). «The H3K4 demethylase lid associates with and inhibits histone deacetylase Rpd3». Molecular and Cellular Biology. 29 (6): 1401–10. PMC 2648242
 . PMID 19114561. doi:10.1128/MCB.01643-08
. PMID 19114561. doi:10.1128/MCB.01643-08
- ↑ Benevolenskaya EV, Murray HL, Branton P, Young RA, Kaelin WG (Jun 2005). «Binding of pRB to the PHD protein RBP2 promotes cellular differentiation». Molecular Cell. 18 (6): 623–35. PMID 15949438. doi:10.1016/j.molcel.2005.05.012

- ↑ Lopez-Bigas N, Kisiel TA, Dewaal DC, Holmes KB, Volkert TL, Gupta S, Love J, Murray HL, Young RA, Benevolenskaya EV (Agosto de 2008). «Genome-wide analysis of the H3K4 histone demethylase RBP2 reveals a transcriptional program controlling differentiation». Molecular Cell. 31 (4): 520–30. PMC 3003864
 . PMID 18722178. doi:10.1016/j.molcel.2008.08.004
. PMID 18722178. doi:10.1016/j.molcel.2008.08.004
- ↑ Pasini D, Hansen KH, Christensen J, Agger K, Cloos PA, Helin K (Maio de 2008). «Coordinated regulation of transcriptional repression by the RBP2 H3K4 demethylase and Polycomb-Repressive Complex 2». Genes & Development. 22 (10): 1345–55. PMC 2377189
 . PMID 18483221. doi:10.1101/gad.470008
. PMID 18483221. doi:10.1101/gad.470008
- ↑ van Oevelen C, Wang J, Asp P, Yan Q, Kaelin WG, Kluger Y, Dynlacht BD (Nov 2008). «A role for mammalian Sin3 in permanent gene silencing». Molecular Cell. 32 (3): 359–70. PMC 3100182
 . PMID 18995834. doi:10.1016/j.molcel.2008.10.015
. PMID 18995834. doi:10.1016/j.molcel.2008.10.015
- ↑ Zeng J, Ge Z, Wang L, Li Q, Wang N, Björkholm M, Jia J, Xu D (Mar 2010). «The histone demethylase RBP2 Is overexpressed in gastric cancer and its inhibition triggers senescence of cancer cells». Gastroenterology. 138 (3): 981–92. PMID 19850045. doi:10.1053/j.gastro.2009.10.004
- ↑ Jensen LR, Amende M, Gurok U, Moser B, Gimmel V, Tzschach A, Janecke AR, Tariverdian G, Chelly J, Fryns JP, Van Esch H, Kleefstra T, Hamel B, Moraine C, Gecz J, Turner G, Reinhardt R, Kalscheuer VM, Ropers HH, Lenzner S (Fevereiro de 2005). «Mutations in the JARID1C gene, which is involved in transcriptional regulation and chromatin remodeling, cause X-linked mental retardation». American Journal of Human Genetics. 76 (2): 227–36. PMC 1196368
 . PMID 15586325. doi:10.1086/427563
. PMID 15586325. doi:10.1086/427563
- ↑ Iwase S, Lan F, Bayliss P, de la Torre-Ubieta L, Huarte M, Qi HH, Whetstine JR, Bonni A, Roberts TM, Shi Y (Mar 2007). «The X-linked mental retardation gene SMCX/JARID1C defines a family of histone H3 lysine 4 demethylases». Cell. 128 (6): 1077–88. PMID 17320160. doi:10.1016/j.cell.2007.02.017

- ↑ Agger K, Cloos PA, Rudkjaer L, Williams K, Andersen G, Christensen J, Helin K (Maio de 2009). «The H3K27me3 demethylase JMJD3 contributes to the activation of the INK4A-ARF locus in response to oncogene- and stress-induced senescence». Genes & Development. 23 (10): 1171–6. PMC 2685535
 . PMID 19451217. doi:10.1101/gad.510809
. PMID 19451217. doi:10.1101/gad.510809
- ↑ Lederer D, Grisart B, Digilio MC, Benoit V, Crespin M, Ghariani SC, Maystadt I, Dallapiccola B, Verellen-Dumoulin C (Jan 2012). «Deletion of KDM6A, a histone demethylase interacting with MLL2, in three patients with Kabuki syndrome». American Journal of Human Genetics. 90 (1): 119–24. PMC 3257878
 . PMID 22197486. doi:10.1016/j.ajhg.2011.11.021
. PMID 22197486. doi:10.1016/j.ajhg.2011.11.021
- ↑ Miyake N, Mizuno S, Okamoto N, Ohashi H, Shiina M, Ogata K, Tsurusaki Y, Nakashima M, Saitsu H, Niikawa N, Matsumoto N (Jan 2013). «KDM6A point mutations cause Kabuki syndrome». Human Mutation. 34 (1): 108–10. PMID 23076834. doi:10.1002/humu.22229

- ↑ Lan F, Bayliss PE, Rinn JL, Whetstine JR, Wang JK, Chen S, Iwase S, Alpatov R, Issaeva I, Canaani E, Roberts TM, Chang HY, Shi Y (Outubro de 2007). «A histone H3 lysine 27 demethylase regulates animal posterior development». Nature. 449 (7163): 689–94. Bibcode:2007Natur.449..689L. PMID 17851529. doi:10.1038/nature06192
- ↑ a b Agger K, Cloos PA, Christensen J, Pasini D, Rose S, Rappsilber J, Issaeva I, Canaani E, Salcini AE, Helin K (Outubro de 2007). «UTX and JMJD3 are histone H3K27 demethylases involved in HOX gene regulation and development». Nature. 449 (7163): 731–4. Bibcode:2007Natur.449..731A. PMID 17713478. doi:10.1038/nature06145
- ↑ «The histone demethylase UTX enables RB-dependent cell fate control». Genes & Development. 24 (4): 327–32. Fevereiro de 2010. PMC 2816731
 . PMID 20123895. doi:10.1101/gad.1882610
. PMID 20123895. doi:10.1101/gad.1882610
- ↑ De Santa F, Totaro MG, Prosperini E, Notarbartolo S, Testa G, Natoli G (Setembro de 2007). «The histone H3 lysine-27 demethylase Jmjd3 links inflammation to inhibition of polycomb-mediated gene silencing». Cell. 130 (6): 1083–94. PMID 17825402. doi:10.1016/j.cell.2007.08.019

- ↑ Burgold T, Spreafico F, De Santa F, Totaro MG, Prosperini E, Natoli G, Testa G (2008). «The histone H3 lysine 27-specific demethylase Jmjd3 is required for neural commitment». PLOS ONE. 3 (8): e3034. Bibcode:2008PLoSO...3.3034B. PMC 2515638
 . PMID 18716661. doi:10.1371/journal.pone.0003034
. PMID 18716661. doi:10.1371/journal.pone.0003034
- ↑ a b Vladimirov N, Løvdok L, Lebiedz D, Sourjik V (Dezembro de 2008). «Dependence of bacterial chemotaxis on gradient shape and adaptation rate». PLOS Computational Biology. 4 (12): e1000242. Bibcode:2008PLSCB...4E0242V. PMC 2588534
 . PMID 19096502. doi:10.1371/journal.pcbi.1000242
. PMID 19096502. doi:10.1371/journal.pcbi.1000242
- ↑ Park SY, Borbat PP, Gonzalez-Bonet G, Bhatnagar J, Pollard AM, Freed JH, Bilwes AM, Crane BR (Maio de 2006). «Reconstruction of the chemotaxis receptor-kinase assembly». Nature Structural & Molecular Biology. 13 (5): 400–7. PMID 16622408. doi:10.1038/nsmb1085
- ↑ West AH, Martinez-Hackert E, Stock AM (Jul 1995). «Crystal structure of the catalytic domain of the chemotaxis receptor methylesterase, CheB». Journal of Molecular Biology. 250 (2): 276–90. PMID 7608974. doi:10.1006/jmbi.1995.0376