Anaptychia ciliaris
Anaptychia ciliaris
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
.jpg) | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Anaptychia ciliaris (L.) Flot. (1850) | |||||||||||||||||
| Sinónimos[1] | |||||||||||||||||
Lista
| |||||||||||||||||
Anaptychia ciliaris é uma espécie de líquen fruticoso da família Physciaceae [en].[2] Encontrada predominantemente no norte da Europa, sua distribuição se estende até a Rússia europeia, o Cáucaso, a Europa Central e Meridional, as Ilhas Canárias e partes da Ásia. Mencionada pela primeira vez na literatura botânica pelo italiano Fabio Colonna em 1606, a espécie foi formalmente descrita por Carl Linnaeus em 1753, que destacou suas características físicas distintas, como a cor cinzenta, a forma foliar incomum com segmentos lineares semelhantes a franjas e a presença de estruturas semelhantes a pelos (cílios). Este líquen é adaptável em relação aos substratos, crescendo principalmente em cascas de árvores e, menos comumente, em rochas. Ao longo da história, a espécie foi utilizada em investigações científicas iniciais sobre a estrutura e o desenvolvimento dos líquens. Botânicos como Joseph Pitton de Tournefort e Johann Hedwig realizaram observações sobre sua estrutura. Estudos mais recentes exploraram suas potenciais atividades biológicas, incluindo propriedades antibacterianas, inseticidas e antioxidantes. A. ciliaris tem sido usada em pesquisas para monitoramento da poluição atmosférica, incluindo a detecção de poluição do ar após o acidente nuclear de Chernobyl. Além de sua importância científica, o líquen teve várias aplicações práticas. Por exemplo, no século XVII, foi um dos ingredientes do "Pó de Chipre", usado como produto de higiene pessoal e cosmético.
Anaptychia ciliaris é facilmente reconhecível por seu talo fruticoso (arbustivo), que varia de cor entre branco-acinzentado e cinza-amarronzado, tornando-se esverdeado quando úmido, e por seus cílios grandes e distintivos. O líquen pode formar colônias extensas, compostas por indivíduos vizinhos, cada um fixado ao substrato em um único ponto, com lobos estreitos, chamados lacínias, crescendo para fora. Essas lacínias, cobertas por pelos finos, dividem-se repetidamente em ramos iguais. Estruturas reprodutivas circulares (apotécios) com discos marrons aparecem na superfície do talo. A anatomia interna de A. ciliaris o torna sensível a poluentes atmosféricos, exibindo mudanças visíveis em sua forma quando exposto a essas condições. Duas espécies de algas verdes do gênero Trebouxia [en] foram identificadas como os fotobiontes (parceiros fotossintéticos) deste líquen.
Taxonomia

De acordo com Annie Lorrain Smith [en], a espécie Anaptychia ciliaris foi mencionada pela primeira vez na literatura botânica em 1606 por Fabio Colonna em sua obra Ekphrasis, conhecida por suas ilustrações detalhadas de plantas feitas com gravuras em cobre.[3]
Foi formalmente descrita como uma nova espécie em 1753 por Carl Linnaeus, sob o nome Lichen ciliaris. Linnaeus descreveu-a como um líquen de aparência de certa forma ereta, foliar, cinzenta, com segmentos lineares semelhantes a franjas e ciliados (com estruturas semelhantes a pelos, ou cílios). Ele comparou-a a um musgo arbóreo com bordas peludas e pequenas estruturas em forma de escudo (apotécios). Linnaeus citou várias referências que descreviam o líquen de maneira semelhante, destacando seu tamanho maior, características peludas e aparência protegida. Ele observou que este líquen é encontrado em árvores na Europa.[4] Julius von Flotow [en] é creditado por transferir o táxon para o gênero Anaptychia [en] em 1850.[5] Um espécime ilustrado por Johann Jacob Dillenius em 1742 foi selecionado como lectótipo por Syo Kurokawa em sua monografia de 1962 sobre o gênero Anaptychia.[6]
Anaptychia ciliaris é a espécie-tipo do gênero Anaptychia.[7] Este gênero foi proposto por Gustav Wilhelm Körber em 1848 como um substituto para o nome Hagenia, sugerido por Franz Gerhard Eschweiler em 1824, mas já em uso para um gênero de plantas. Körber descreveu o gênero Anaptychia da seguinte forma (traduzido do latim): "Apotécios delimitados por um talo ressupinado (o talo ascendente é canalizado)".[8] Embora ele não tenha designado uma espécie-tipo, A. ciliaris foi posteriormente indicada como tal por Louis Pfeiffer em 1872.[7]
Subtáxons
Várias subespécies (subsp.), variedades (var.) e formas (f.) do líquen foram descritas; o Index Fungorum lista 44 desses subtáxons em maio de 2025.[9] A lista a seguir é representativa, mas não exaustiva:
- f. ciliaris
Esta é a forma nominada, na qual os picnídios (estruturas reprodutivas assexuadas) são raros ou ausentes, e as margens dos apotécios são distintamente lacinuladas (franjadas ou rasgadas).[6]
- f. agropia (Ach.) Boist. (1903)[10]
Nesta forma, os picnídios são raros ou ausentes, e as margens dos apotécios são crenadas (onduladas) ou quase inteiras (isto é, lisas e não lobadas ou dentadas).[6]
- f. verrucosa (Ach.) Boist. (1903)[10]
Nesta forma, os picnídios são numerosos; possui verrugas (pequenas protuberâncias semelhantes a verrugas) que são da mesma cor do talo ou ligeiramente mais escuras.[6]
- f. melanosticta (Ach.) Boberski (1886)
Nesta forma, os picnídios são numerosos; as verrugas variam de marrom-escuro a marrom-enegrecido.[6]
- f. nigrescens (Bory) Zahlbr. (1931)[11]
Nesta forma, as lacínias têm menos de 2 mm de largura.[6]
- subsp. mamillata (Taylor) D.Hawks. & P.James (1980)[12]
Comparada à variedade nominada, a subsp. mamillata tem lobos mais estreitos (cerca de 2 mm de largura), com coloração que varia de cinza-escuro a marrom quando seca, até verde-oliva escuro quando úmida, e não apresenta pruína na superfície do talo.[13]
- var. melanosticta (Ach.) Boistel (1903)[10]
Esta variedade é marrom-escura com uma superfície superior esparsamente peluda e é encontrada principalmente em rochas à beira-mar, especialmente em rochas frequentadas por aves.[14]
Em 1962, Kurokawa identificou cinco formas de Anaptychia ciliaris.[6] No entanto, em 1973, ele considerou que essas distinções eram apenas variações de características causadas por diferentes condições ambientais, julgando-as taxonomicamente insignificantes. Ele as agrupou subsequentemente como sinônimos.[15] Essa perspectiva é compartilhada pelo Species Fungorum, que não reconhece esses subtáxons como tendo importância taxonômica individual e os categoriza sob uma sinonímia coletiva.[1] A maioria dessas classificações não foi avaliada usando filogenética molecular contemporânea. Uma exceção é a var. melanosticta de regiões costeiras. Análises de DNA sugerem que ela pode ser distinta o suficiente para ser considerada uma espécie própria, pois surgiu como um táxon irmão em relação a outras amostras testadas de A. ciliaris.[16]
Descrição
.jpg)
A forma de crescimento de Anaptychia ciliaris combina características de líquens foliosos (semelhantes a folhas) e fruticosos (arbustivos). Como muitas espécies fruticosas, este líquen se fixa ao substrato em um único ponto. Suas frondes, semelhantes aos lobos de líquens foliosos, ficam próximas ao substrato, com estruturas superior e inferior distintas em uma organização dorsiventral. Essa estrutura inclui um córtex superior fibroso de hifas bem compactadas e uma camada algal com fotobiontes intercalados entre o córtex e as hifas mais soltas da medula. O córtex inferior é composto por hifas alinhadas mais ou menos paralelamente à superfície. A superfície superior do líquen é acinzentada, e a inferior pode ser acinzentada ou esbranquiçada,[17] ambas tornando-se verdes quando úmidas.[18]
Este líquen forma fixações frouxas ao substrato, permitindo o desenvolvimento de colônias grandes, com até 15 cm ou mais de diâmetro. Essas colônias são compostas por indivíduos vizinhos, cada um com estruturas lineares e alongadas (lacínias) que se ramificam dicotomicamente (em partes aproximadamente iguais) de forma repetida. As lacínias geralmente têm uma orientação ascendente. Sua largura chega a cerca de 2 mm, com espessura de aproximadamente 300 μm. Elas parecem planas ou ligeiramente convexas e são cobertas por pelos finos e macios (pubescência).[6] O córtex fibroso externo confere resistência estrutural às lacínias, ajudando-as a manter uma orientação ereta.[19] Numerosos cílios laterais claros estão presentes ao longo das margens das lacínias.[13] Eles variam de cinza-escuro a preto e podem atingir até 15 mm de comprimento.[14] Às vezes, esses cílios longos formam hapterons — órgãos de fixação aéreos especializados com hifas altamente adesivas. Ao entrar em contato com superfícies próximas, muitas vezes outro lobo do próprio talo, esses hapterons induzem ramificação e criam uma bainha espalhada, levando ao entrelaçamento.[20]
Na superfície inferior das lacínias, o talo não possui córtex e parece mais claro que a superfície superior. A face inferior apresenta veios irregulares e é adornada com rizinas (estruturas de fixação semelhantes a raízes) ao longo das margens, da mesma cor do talo. Essas rizinas medem entre 1 e 6 mm de comprimento e podem ser simples ou ocasionalmente ramificadas nas extremidades. O córtex superior das lacínias tem espessamento irregular, e sua superfície inferior apresenta contornos flexuosos, ocasionalmente se estendendo para baixo até a face inferior do talo. A camada de fotobionte, com células de 10–15 μm de diâmetro, é frequentemente interrompida pelo córtex superior, resultando em um padrão descontínuo. A camada medular é geralmente muito fina e pode até ser evanescente em algumas regiões.[6]
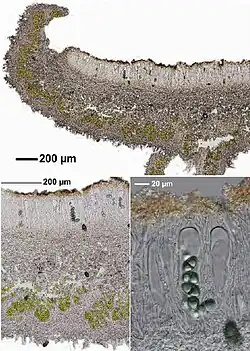
Os apotécios, estruturas reprodutivas, estão presentes no talo. Essas estruturas são geralmente laminais (espalhadas pela superfície do talo) e podem ser estipitados (com um estipe) ou um tanto sésseis (diretamente no talo). Seus diâmetros variam de 2 a 5 mm. Suas margens são lacinuladas (rasgadas), com lacínulas ciliadas nas bordas. O disco dos apotécios é marrom ou marrom-escuro, inicialmente coberto por uma pruína branca que pode desaparecer. O himênio do receptáculo, com 150–200 μm de altura, torna-se azul quando tingido com iodo. Seu córtex é irregularmente espessado e resistente à coloração por iodo. Os ascos cilíndricos ou clavados medem cerca de 120 por 30 μm e geralmente contêm entre quatro e oito esporos. Os esporos são marrom-escuros, elipsoides com extremidades arredondadas e ligeiramente contraídos no centro; medem 17–23 por 28–43 μm, com paredes finas e uniformemente espessadas.[6] Inicialmente, os esporos são ovais e preenchidos com substâncias granulares e mucosas. Eventualmente, uma partição central se forma, dividindo o conteúdo e resultando em um estado de duas células.[21]
Nenhum produto liquênico foi identificado em Anaptychia ciliaris, e ele não reage a nenhum dos testes químicos padrões usados para identificar líquens.[6]
A morfologia de A. ciliaris muda quando exposta a concentrações adversas de poluentes atmosféricos. Ele para de produzir cílios, os lobos tornam-se mais curtos e a superfície superior desenvolve uma textura verrucosa.[22]
Fotobionte
A espécie de alga verde Trebouxia arboricola [en] foi o primeiro fotobionte de Anaptychia ciliaris identificado.[23] Um estudo simultâneo corroborou essa associação e sugeriu a natureza inespecífica de A. ciliaris ao incorporar algas de líquens adjacentes. O espécime de A. ciliaris estudado foi obtido de casca de árvore próxima a Xanthoria parietina e Pleurosticta acetabulum [en]. O DNA ribossômico do espaçador interno transcrito do fotobionte correspondeu de perto às sequências dos fotobiontes desses líquens vizinhos, sugerindo que compartilham as mesmas algas.[24] Anaptychia ciliaris realiza reprodução sexual por meio da produção de esporos meióticos. Em líquens, esse modo reprodutivo dispersa os simbiontes individualmente, levando a novas formações simbióticas. Esse processo facilita a diversidade genética e possíveis mudanças simbióticas entre diferentes espécies.[25]
Em 2014, outra espécie do gênero Trebouxia foi demonstrada como parceira de Anaptychia ciliaris. Trebouxia decolorans é uma alga verde haploide comum e amplamente distribuída, conhecida por formar associações simbióticas com vários fungos formadores de líquens. Primers de microssatélites, projetados especificamente para investigar a estrutura genética e a diversidade desse fotobionte,[26] foram usados para esclarecer a diversidade genética intratalo de T. decolorans. Isso revelou a presença de múltiplas linhagens de fotobiontes geneticamente distintas dentro dos talos do fungo. Particularmente em A. ciliaris, a principal fonte de diversidade de fotobionte parece ser mutações somáticas intratalinas, possivelmente devido à longa vida do fungo em comparação com o micobionte, permitindo tempo suficiente para o acúmulo de mutações.[25]
Espécies semelhantes
A espécie africana que vive sobre musgos, Anaptychia ethiopica, assemelha-se muito a A. ciliaris, a ponto de seus autores a considerarem uma versão sorediada dessa espécie. Ela é conhecida apenas nas montanhas da Etiópia, em altitudes acima de 3.500 m.[27]
Habitat e distribuição

Anaptychia ciliaris possui uma distribuição ampla, mas predominantemente no Hemisfério Norte, abrangendo Europa, partes da Ásia e Norte da África, sendo notavelmente ausente na América do Norte. Encontrada principalmente no norte da Europa, sua distribuição se estende para o leste até a Rússia europeia, o Cáucaso,[6] e o nordeste da Rússia (Murmansk).[28] Está presente também na Europa Central e Meridional e nas Ilhas Canárias. Na África, está estabelecida em Marrocos,[29] e há registros no Sudão.[30] Na Ásia, os registros são esporádicos.[31] Na China, espécimes foram coletados em Xinjiang, Gansu, Shaanxi e Hebei, em altitudes acima de 1.800 m.[32] Anaptychia ciliaris esteve entre os três líquens mais abundantes na pesquisa de biodiversidade de 2018 no Parque Natural do Lago Abant, na Turquia.[33] Em contraste, o norte da Alemanha[34] e o Reino Unido observaram um declínio em avistamentos. É rara na Irlanda e quase extinta no nordeste da Inglaterra.[13] Até 2010, a Escócia registrou A. ciliaris em apenas quatro locais, com sua escassez atribuída à poluição do ar e ao declínio da população de olmos, afetada pela doença do olmo holandês.[35] Há um século atrás, era mais comum no Reino Unido, geralmente prosperando em árvores em parques e ao longo de estradas cultivadas.[36] Amplamente distribuída na Finlândia, é abundante em áreas povoadas, presente em parques, alamedas e bordas de campos, além de ocorrer em falésias à beira-mar.[14]
Anaptychia ciliaris adaptou-se a crescer em vários substratos. Sobre cascas, foi frequentemente registrada em Quercus rotundifolia, Quercus pyrenaica e Ulmus. Menos comumente, aparece em Pinus sylvestris, P. nigra, Juniperus oxycedrus,[37] Acer pseudoplatanus e Fagus sylvatica.[38] Na Dinamarca, seus hospedeiros habituais são Fraxinus e Tilia.[22] Com menos frequência, é encontrada em rochas calcárias e ácidas, e em lápides.[13] Uma característica marcante de A. ciliaris é sua preferência por luz difusa.[39]
Na Polônia, Anaptychia ciliaris está entre as seis espécies ameaçadas listadas na Lista Vermelha Nacional.[40] Na área da Planície do Leste Europeu em Moscou, é uma espécie incomum e está listada no Red Data Book of the Moscow Region de 2018. É encontrada principalmente nas florestas de bétulas com gramíneas e pântanos da região, com sua presença limitada atribuída à poluição do ar de Moscou.[41] A Lista Vermelha Regional da Áustria também classifica A. ciliaris como ameaçada.[38] Outrora comum na Alta Áustria, seu declínio se deve à menor disponibilidade de substratos preferidos, como cascas maduras, cobertas de musgo, fertilizadas e impregnadas de poeira. Práticas contemporâneas frequentemente resultam na remoção de árvores antes que suas cascas atinjam uma consistência adequada para A. ciliaris.[42]
A literatura histórica norte-americana ocasionalmente menciona a presença de A. ciliaris, mas tais referências são equívocos. Esses casos referem-se a Anaptychia setifera, e A. ciliaris não é nativa do continente.[43]
Biomonitoramento
.jpg)
Alguns líquens, incluindo Anaptychia ciliaris, são excelentes bioindicadores devido à sua sensibilidade a mudanças ambientais e capacidade de acumular poluentes atmosféricos, tornando-os ferramentas valiosas para monitoramento da qualidade do ar e da saúde ambiental.
Na Dinamarca e no norte da Alemanha, foi desenvolvido um método para avaliar as emissões de dióxido de enxofre (SO₂) usando a saúde e a fertilidade de líquens indicadores como A. ciliaris.[22] Da mesma forma, Inglaterra e País de Gales adotaram uma escala que classifica zonas de 0 (mais poluída) a 10 (menos poluída), com A. ciliaris geralmente encontrado em zonas acima de 7, correspondendo a níveis de SO₂ em torno de 40 microgramas por metro cúbico.[44] Historicamente comum nos Países Baixos no século XIX, A. ciliaris sofreu um declínio significativo ao longo do século XX. No entanto, espécimes saudáveis foram inesperadamente encontrados em 2010 em freixos jovens em Brabante do Norte, um ressurgimento atribuído à redução da poluição do ar e ao aquecimento climático.[45]
Monitorar a degradação da clorofila em feofitina em A. ciliaris provou ser eficaz para detectar poluição do ar. Sua capacidade de crescer em diferentes substratos aumenta sua utilidade no biomonitoramento. Na França, A. ciliaris foi usada para medir emissões de chumbo e cádmio de um incinerador de resíduos sólidos municipais.[46] Também foi empregado na Grécia para avaliar níveis de metais pesados em áreas poluídas[47] e perto de uma usina de lignito.[48]
Na Suécia, A. ciliaris também tem um histórico de ser usada no monitoramento da poluição atmosférica.[49] Após o desastre nuclear de Chernobyl, desempenhou um papel significativo no biomonitoramento de precipitação radioativa no ar, com atividade de césio-137 detectada em Anaptychia ciliaris alcançando até 14.560 becquerels por quilograma.[50]
Usos
No século XVII, o "Pó de Chipre" era usado como um pó cosmético (um pó fino, frequentemente perfumado, usado para higiene pessoal e fins cosméticos) para branquear, perfumar e limpar os cabelos. Era uma mistura de orzela‑do‑reino [en], Anaptychia ciliaris e espécies de Usnea [en], perfumada com âmbar gris ou almíscar, combinada com óleo essencial de rosas, jasmim ou flores de laranjeira.[51]
Na região de Ar Kaweit, no leste do Sudão, o líquen, conhecido localmente como bakour, era misturado com outras plantas e queimado para repelir insetos.[30]
Pesquisa
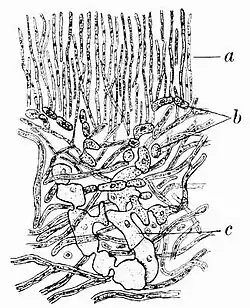
Historicamente, o líquen Anaptychia ciliaris desempenhou um papel significativo em várias explorações científicas sobre a estrutura e fisiologia dos líquens. Inicialmente, o botânico francês Joseph Pitton de Tournefort teria observado os esporos grandes e de cor escura característicos do líquen.[53] Em 1849,[54] Holle detalhou o desenvolvimento de hifas a partir de esporos de líquens, usando A. ciliaris como objeto de estudo.[55] Em 1850 e 1851, o líquen foi utilizado pelo botânico alemão Hermann Itzigsohn para demonstrar a existência de picnídios.[21] Em 1853,[56] Julius Ferdinand Speerschneider, outro botânico alemão, relatou a divisão das células do fotobionte (na época chamadas de gonídios) em seções úmidas do talo.[57] Ele descobriu que, em ar úmido, as hifas se decompunham em dois meses, enquanto as algas prosperavam, crescendo e se dividindo rapidamente. Posteriormente, pequenas estruturas verde-claras emergiam no centro do talo em decomposição, evoluindo para primórdios de líquen.[57]
Mais informações sobre a estrutura dos líquens vieram quando Reginald Heber Howe, Jr. apresentou o córtex do líquen como um exemplo de córtex "fibroso" — um tipo de tecido caracterizado por hifas longas, delgadas e raramente ramificadas, crescendo paralelamente à superfície.[58] O briologista alemão Johann Hedwig, no século XVIII, expandiu essas descobertas. Em sua obra de 1784, Fundamentum Historiae Naturalis Muscorum Frondosorum, descreveu e retratou os apotécios de Anaptychia ciliaris, esporos septados escuros e picnídios. Ele identificou pequenos corpos associados ao organismo, medindo cerca de 50 μm de comprimento e 24 μm de espessura, como "semina"[59] — termo que Erik Acharius substituiu por "esporos" em 1803.[60]
No século seguinte, a pesquisa sobre Anaptychia ciliaris avançou ainda mais. Pierre Augustin Dangeard, em 1894, estudou a origem e o desenvolvimento de ascos em líquens, usando Anaptychia ciliaris como modelo.[61] René Maire explorou a biologia celular observando a divisão nuclear em um esporo antes da formação do septum.[36] As aplicações práticas do líquen também foram investigadas. Em 1825, Joseph Placide Alexandre Léorier documentou a técnica pioneira de Roy de Tonnerre para produzir álcool a partir de líquens, notavelmente Anaptychia ciliaris. Essa inovação foi notável porque os líquens, ao contrário de frutas ou grãos, geralmente não possuem os açúcares abundantes usados como matéria-prima na produção tradicional de álcool.[62]
Pesquisas descobriram várias atividades biológicas potenciais de Anaptychia ciliaris. Seus extratos, testados por efeitos antibacterianos e inseticidas contra certas bactérias patogênicas e larvas do mosquito Culiseta longiareolata, mostraram propriedades larvicidas moderadas.[63] Em testes contra patógenos bacterianos de peixes, A. ciliaris demonstrou efeitos antibacterianos, particularmente contra Aeromonas hydrophila, Streptococcus agalactiae, Enterococcus faecalis e Lactococcus garvieae [en].[64] Os metabólitos ativos em A. ciliaris, incluindo vários antioxidantes, variam em presença e concentração dependendo do substrato arbóreo.[65]
Crescimento em cultura
O micobionte de Anaptychia ciliaris pode ser cultivado em cultura axênica (pura). Há mais de 100 anos, o ficologista finlandês Harry Warén descreveu o parceiro fúngico de A. ciliaris cultivado a partir de esporos, notando seu micélio compacto e grandes células globulares, erroneamente acreditadas como contendo clorofila.[66][67] Pesquisadores podem iniciar o crescimento de esporos colocando apotécios perto de uma placa de Petri invertida, permitindo que esporos maduros sejam ejetados sobre o meio de crescimento e comecem a germinar.[68] Os esporos de Anaptychia ciliaris geralmente se fixam ao meio de crescimento como unidades isoladas, em vez de em grupos, uma característica também observada em outras espécies de líquens e típica de certas famílias de líquens. Anaptychia ciliaris é notável por sua liberação consistente de esporos em condições de laboratório. Essa liberação constante torna A. ciliaris ideal para estudar a reprodução e o desenvolvimento de líquens em culturas apossimbióticas. Nessas condições, os pesquisadores cultivam o componente fúngico separadamente de seu parceiro algal, permitindo uma análise detalhada das características e comportamento individuais do fungo. Em média, esses esporos levam de seis a sete dias para iniciar a germinação.[69]
Anaptychia ciliaris mostra variabilidade na produção de esporos, refletindo seu ciclo de vida heterotálico. Isso contribui para a diversidade genética, um fator importante na adaptabilidade da espécie. Nas fases iniciais de crescimento, a presença de fontes de carbono aumenta o desenvolvimento filamentoso do micobionte. Essas descobertas alinham-se com a taxa de crescimento lenta característica do líquen e sua capacidade de suportar apotécios de diferentes idades em um único talo, contribuindo ainda mais para a variação genética. A morfologia, o metabolismo e a pigmentação de Anaptychia ciliaris são particularmente influenciados por açúcares e álcoois de açúcar, variando significativamente em diferentes meios de cultura.[69]
Interações entre espécies
Anaptychia ciliaris faz parte de uma rede de relações ecológicas, servindo como hospedeiro para vários organismos liquenícolas, que são espécies que vivem sobre líquens e frequentemente os parasitam. Entre os fungos que parasitam A. ciliaris está Tremella anaptychiae, uma espécie descrita em 2017. Esse fungo produz basidiomas esféricos ou tuberculados, variando de cor entre creme, rosado, acastanhado ou enegrecido, e é encontrado na Itália, Macedônia, Espanha (incluindo as Ilhas Canárias), Suécia[31] e Grécia. Catillaria mediterranea, um líquen com talo reduzido,[70] e Monodictys anaptychiae, um hifomiceto [en] raro, também crescem sobre A. ciliaris. Monodictys anaptychiae pode ser exclusivo de A. ciliaris; a infecção causa danos à superfície do talo e descoloração.[71][72] No Reino Unido, a subespécie mamillata de Anaptychia ciliaris frequentemente exibe pequenos pontos pretos em seus lobos, resultado do parasitismo por Stigmidium hageniae.[13] Além disso, A. ciliaris está sujeito a infecção por outros fungos liquenícolas, como Pronectria tincta.[73]
Referências
- ↑ a b «Synonymy. Current Name: Anaptychia ciliaris (L.) Flot., Jber. schles. Ges. vaterl. Kultur 28: 119 (1850)». Species Fungorum. Consultado em 15 de março de 2025
- ↑ «Anaptychia ciliaris (L.) Flot.». Catalogue of Life. Species 2000: Leiden, the Netherlands. Consultado em 15 de março de 2025
- ↑ Smith 1921, p. 3.
- ↑ Linnaeus, C. (1753). Species Plantarum (em latim). 2. Estocolmo: Lars Salvius. p. 1144
- ↑ Flotow, J.V. (1850). «Lichenes florae silesiae. Zweiter Artikel». Jahresbericht der Schlesischen Gesellschaft für Vaterländische Kultur (em alemão). 28: 119
- ↑ a b c d e f g h i j k l Kurokawa, Syo (1962). A Monograph of the Genus Anaptychia. Col: Nova Hedwigia. Weinheim: J. Cramer. pp. 10–14. ISBN 978-3-443-51089-3
- ↑ a b «Record Details: Anaptychia Körb., Grundriss Krypt.-Kunde: 197 (1848)». Index Fungorum. Consultado em 15 de março de 2025
- ↑ Körber, Gustav Wilhelm (1848). Grundriss der Kryptogamen-Kunde. Zur Orientirung beim Studium der kryptogamischen Pflanzen, sowie zum Gebrauch bei seinen Vorlesungen [Esboço da ciência das criptógamas. Para orientação durante o estudo das plantas criptogâmicas, bem como para uso em suas palestras] (em alemão). Breslau: Verlag von Eduard Trewendt. p. 87
- ↑ «Search term: Anaptychia ciliaris». Index Fungorum. Consultado em 15 de março de 2025
- ↑ a b c Boistel, Alphonse (1903). Nouvelle flore des lichens pour la détermination facile des espèces sans microscope et sans réactifs (em francês). 2. Paris: Librairie Générale de l'enseignement. p. 49
- ↑ Zahlbruckner, A. (1931). Catalogus Lichenum Universalis. 7. Leipzig: Borntraeger. p. 714
- ↑ Hawksworth, D.L.; James, P.W.; Coppins, B.J. (1980). «Checklist of British lichen-forming, lichenicolous and allied fungi». The Lichenologist. 12 (1): 1–115 [106]. doi:10.1017/s0024282980000035
- ↑ a b c d e Edwards, B.; Purvis, O.W. (2009). «Anaptychia Körb (1848)». In: Smith, C.W.; Aptroot, A.; Coppins, B.J.; Fletcher, F.; Gilbert, O.L.; James, P.W.; Wolseley, P.A. The Lichens of Great Britain and Ireland 2nd ed. London: The Natural History Museum. p. 147. ISBN 978-0-9540418-8-5
- ↑ a b c Stenroos, Soili; Ahti, Teuovo; Lohtander, Katileena; Myllys, Leena (2011). Suomen jäkäläopas [Guia de líquens da Finlândia] (em finlandês). Helsinque: Kasvimuseo, Luonnontieteellinen keskusmuseo. pp. 57–58. ISBN 978-952-10-6804-1. OCLC 767578333
- ↑ Kurokawa, S. (1973). «Supplementary notes on the genus Anaptychia». Journal of the Hattori Botanical Laboratory. 37: 563–607
- ↑ Lohtander, Katileena; Ahti, Teuvo; Stenroos, Soili; Urbanavichus, Gennadii (2008). «Is Anaptychia monophyletic? A phylogenetic study based on nuclear and mitochondrial genes». Annales Botanici Fennici. 45 (1): 55–60. doi:10.5735/085.045.0106
- ↑ Smith 1921, p. 99–100.
- ↑ Smith 1921, p. 246.
- ↑ Smith 1921, p. 103.
- ↑ Smith 1921, p. 94.
- ↑ a b Lindsay, W. Lauder (1856). A Popular History of British Lichens. Londres: Lovell Reeve. pp. 145–146
- ↑ a b c Søchting, Ulrik; Ramkar, Knur (1982). «The epiphytic lichen zones in rural Denmark and Schleswig-Holstein». Nordic Journal of Botany. 2 (2): 171–181. doi:10.1111/j.1756-1051.1982.tb01178.x
- ↑ Dahlkild, Åsa; Källersjö, Mari; Lohtander, Katileena; Tehler, Anders (2001). «Photobiont diversity in the Physciaceae (Lecanorales)». The Bryologist. 104 (4): 527–536. doi:10.1639/0007-2745(2001)104[0527:pditpl]2.0.co;2
- ↑ Helms, Gert; Friedl, Thomas; Rambold, Gerhard; Mayrhofer, Helmut (2001). «Identification of photobionts from the lichen family Physciaceae using algal-specific ITS rDNA sequencing». The Lichenologist. 33 (1): 73–86. Bibcode:2001ThLic..33...73H. doi:10.1006/lich.2000.0298
- ↑ a b Dal Grande, Francesco; Alors, David; Divakar, Pradeep K.; Bálint, Miklós; Crespo, Ana; Schmitt, Imke (2014). «Insights into intrathalline genetic diversity of the cosmopolitan lichen symbiotic green alga Trebouxia decolorans Ahmadjian using microsatellite markers». Molecular Phylogenetics and Evolution. 72: 54–60. Bibcode:2014MolPE..72...54D. PMID 24412431. doi:10.1016/j.ympev.2013.12.010
- ↑ Dal Grande, Francesco; Beck, Andreas; Singh, Garima; Schmitt, Imke (2013). «Microsatellite primers in the lichen symbiotic alga Trebouxia decolorans (Trebouxiophyceae)». Applications in Plant Sciences. 1 (3): 1–4. PMC 4105286
 . PMID 25202529. doi:10.3732/apps.1200400
. PMID 25202529. doi:10.3732/apps.1200400
- ↑ Swinscow, T.D.V.; Krog, Hildur (1976). «The genera Anaptychia and Heterodermia in East Africa». The Lichenologist. 8 (2): 103–138. doi:10.1017/s0024282976000212
- ↑ Jury, S.L. (2013). «Lichens collected during the fifth "Iter Mediterraneum" in Morocco, 8–27 June, 1992» (PDF). Bocconea. 26: 145–149. doi:10.7320/bocc26.145
- ↑ a b Crawford, Stuart D. (2019). «Lichens used in traditional medicine». In: Ranković, Branislav. Lichen Secondary Metabolites. Bioactive Properties and Pharmaceutical Potential 2 ed. [S.l.]: Springer Nature Switzerland. p. 67. ISBN 978-3-030-16813-1
- ↑ a b Zamora, Juan Carlos; Diederich, Paul; Millanes, Ana M.; Wedin, Mats (2017). «An old familiar face: Tremella anaptychiae sp. nov. (Tremellales, Basidiomycota)». Phytotaxa. 307 (4): 254–262. doi:10.11646/phytotaxa.307.4.3
- ↑ Chen, Jian-bin; Wang, Da-peng (1999). «The lichen family Physciaceae (Ascomycota) in China I. The genus Anaptychia». Mycotaxon. 73: 335–342
- ↑ Yavuz, Mustafa; Çobanoğlu, Gülşah (2018). «Lichen diversity of Gölcük Nature Park (Isparta), including new records for Turkey». Muzeul Olteniei Craiova. Oltenia. Studii şi comunicări. Ştiinţele Naturii. 34 (2): 57–66
- ↑ Wirth, Volkmar (1995). Die Flechten Baden-Württembergs [Os líquens de Baden-Württemberg] (em alemão). Stuttgart (Hohenheim): Balogh Scientific Books. p. 42. ISBN 978-3-8001-3325-3
- ↑ «Rare species found at fourth site». BBC News. 2010. Consultado em 15 de março de 2025
- ↑ a b Smith 1921, p. 189.
- ↑ Manrique, E.; Redondo, F.; Izco, F. (1989). «Estimation of chlorophyll degradation into phaeophytin in Anaptychia ciliaris as a method to detect air pollution». Lazaroa. 11: 141–148
- ↑ a b Türk, R.; Hafellner, J. (1999). Niklfeld, H., ed. Rote Liste gefährdeter Flechten (Lichenes) Österreichs. 2. Fassung [Lista vermelha de líquens ameaçados (Lichenes) da Áustria. 2ª edição]. Col: Rote Listen gefährdeter Pflanzen Österreichs 2 Auflage (em alemão). 10. Graz: Grüne Reihe des Bundesministeriums für Umwelt, Jugend und Familie. pp. 187–228
- ↑ Smith 1921, p. 243.
- ↑ Matwiejuk, A. (2015). «Lichens of the Supraśl town (Podlasie, north-eastern Poland)». Steciana. 19 (3): 133–142. doi:10.12657/steciana.019.015

- ↑ Chernenkova, Tatiana V.; Belyaeva, Nadezhda G.; Suslova, Elena G.; Aristarkhova, Ekaterina A.; Kotlov, Ivan P. (2023). «Patterns of the red-listed epiphytic species distribution in coniferous-deciduous forests of the Moscow Region». Geography, Environment, Sustainability. 16 (1): 119–131. doi:10.24057/2071-9388-2022-101

- ↑ Türk, Roman; Wittmann, Helmut; Pilsl, Peter (1982). «Ergebnisse der floristischen Flechtenkartierung in Oberösterreich – ein erster Überblick» [Resultados do mapeamento florístico de líquens na Alta Áustria – Uma primeira visão geral] (PDF). Stapfia (em alemão). 10: 121–137
- ↑ Lewis, Christopher J. (2019). «Heterodermia leucomela (L.) Poelt discovered in Ontario, Canada for the first time in over 150 years». Evansia. 36 (2): 30–38. doi:10.1639/0747-9859-36.2.30
- ↑ Gilbert, O.P. (1973). «Lichens and air pollution». In: Ahmadjian, Vernon; Hale, Mason. The Lichens. New York/London: Academic Press. pp. 466–467. ISBN 978-0-12-044950-7
- ↑ Aptroot, André (2011). «Wimpermos (Anaptychia ciliaris) vestigt zich weer in Nederland». Buxbaumiella (em neerlandês). 88: 26–27
- ↑ Gombert, S.; J., Asta (1998). «The effect of refure incinerator fumes on the lead and cadmium content of experimentally exposed corticolous lichens». Water, Air, & Soil Pollution. 104: 29–40. Bibcode:1998WASP..104...29G. doi:10.1023/A:1004965131303
- ↑ Sawidis, T.; Chettri, M.K.; Zachariadis, G.A.; Stratis, J.A.; Seaward, M.R.D. (1995). «Heavy metal bioaccumulation in lichens from Macedonia in northern Greece». Toxicological & Environmental Chemistry. 50 (1–4): 157–166. Bibcode:1995TxEC...50..157S. doi:10.1080/02772249509358211
- ↑ Riga-Karandinos, A.N.; Karandinos, M.G (1998). «Assessment of air pollution from a lignite power plant in the plain of Megalopolis (Greece) using as biomonitors three species of lichens; impacts on some biochemical parameters of lichens». Science of the Total Environment. 215 (1–2): 167–183. Bibcode:1998ScTEn.215..167R. doi:10.1016/s0048-9697(98)00119-3
- ↑ Borg, Lars; Aronsson, Margita (2004). «Population size and ecology of Pleurosticta acetabulum, Anaptychia ciliaris and Ramalina fraxinea in avenues and churchyards in Kalmar County, SE Sweden» (PDF). Graphis Scripta. 16 (2): 37–42
- ↑ Papastefanou, C.; Manolopoulou, M.; Sawidis, T. (1989). «Lichens and mosses: Biological monitors of radioactive fallout from the Chernobyl reactor accident». Journal of Environmental Radioactivity. 9 (3): 199–207. Bibcode:1989JEnvR...9..199P. doi:10.1016/0265-931x(89)90044-1
- ↑ Shukla, Ila; Azmi, Lubna; Gautam, Arti; Shukla, Shashi Kant; Rao, ChV (2018). «Lichens are the next promising candidates for medicinally active compounds». International Journal of Phytopharmacy. 8 (4): 31–38
- ↑ Baur, Erwin (1904). «Untersuchungen über die Entwickelungsgeschichte der Flechtenapothecien I.». Botanische Zeitung (em alemão). 62: 21–44
- ↑ Smith 1921, p. 155.
- ↑ Holle, G. von (1849). Zur Entwicklungsgeschichte von Borrera ciliaris. Inaugural-Dissertation [Sobre a história de desenvolvimento de Borrera ciliaris. Dissertação inaugural]. Göttingen: Huth
- ↑ Smith 1921, p. 46.
- ↑ Speerschneider, J. (1853). «Zur Entwickelungsgeschichte der Hagenia ciliaris» [Sobre a história de desenvolvimento de Hagenia ciliaris]. Botanische Zeitung (em alemão). 11: 705–711, 721–730
- ↑ a b Smith 1921, p. 24.
- ↑ Smith 1921, p. 85.
- ↑ Smith 1921, p. 156.
- ↑ Smith 1921, p. 184.
- ↑ Smith 1921, p. 185.
- ↑ Smith 1921, p. 411.
- ↑ Cetin, O.T.; Akarsu, M.; Burunkaya, E.; Kesmez, O.; Arpac, E.; Cetin, H. (2013). «Mosquito larvicidal and antibacterial activities of different solvent extracts of Anaptychia ciliaris subsp. ciliaris». Egyptian Journal of Biological Pest Control. 23 (2): 287–290
- ↑ Tas, I.; Yildirim, A.B.; Ozyigitoglu, G.C.; Turker, H.; Turker, A.U. (2019). «Lichens as a promising natural antibacterial agent against fish pathogens». Bulletin of the European Association of Fish Pathologists. 39 (1): 40–48
- ↑ Gulnara, Badridze; Chkhubianishvili, Eva; Rapava, Luara; Kikvidze, Medea; Chigladze, Lali; Tsiklauri, Nino; Tsilosani, Ketevan; Kupradze, Inga; Chanishvili, Shota (2019). «Active metabolites of some lichens growing in Georgia». Journal of Biodiversity and Environmental Sciences. 15 (6): 1–15
- ↑ Warén, Harry (1920). «Reinkulturen von Flechtengonidien» [Culturas puras de gonídios de líquens]. Öfversigt af Finska vetenskaps-societetens förhandlingar (em alemão). 61: 1–79
- ↑ Warén, H. (1921). «Beobachtungen bei Kultur von Flechtenhyphen» [Observações sobre a cultura de hifas de líquens]. Öfversigt af Finska vetenskaps-societetens förhandlingar (em alemão). 62: 1–9
- ↑ Crittenden, P.D.; David, J.C.; Hawksworth, D.L.; Campbell, F.S. (1995). «Attempted isolation and success in the culturing of a broad spectrum of lichen-forming and lichenicolous fungi». New Phytologist. 130 (2): 267–297. doi:10.1111/j.1469-8137.1995.tb03048.x

- ↑ a b Molina, M. Carmen; Divakar, Pradeep K.; González, Natalia (2015). «Success in the isolation and axenic culture of Anaptychia ciliaris (Physciaceae, Lecanoromycetes) mycobiont». Mycoscience. 56 (4): 351–358. doi:10.1016/j.myc.2014.10.003

- ↑ Brackel, Wolfgang von; Döbbeler, Peter (2020). «An addition to the knowledge of lichenicolous fungi of Greece with a key to the lichenicolous fungi on Collema s. l.». Folia Cryptogamica Estonica. 57: 147–152. doi:10.12697/fce.2020.57.13

- ↑ Hawksworth, D.L. (1994). «Notes on British lichenicolous fungi: VII». The Lichenologist. 26 (4): 337–347. Bibcode:1994ThLic..26..337H. doi:10.1006/lich.1994.1028
- ↑ Wedin, Mats (1993). «Concentric bodies in conidia of Monodictys anaptychiae (Hyphomycetes)». The Lichenologist. 25 (2): 203–206. Bibcode:1993ThLic..25..203W. doi:10.1006/lich.1993.1027
- ↑ Diederich, Paul; Lawrey, James D.; Ertz, Damien (2018). «The 2018 classification and checklist of lichenicolous fungi, with 2000 non-lichenized, obligately lichenicolous taxa». The Bryologist. 121 (3): 340–425 [382]. doi:10.1639/0007-2745-121.3.340
Literatura citada
- Smith, Annie Lorrain (1921). Lichens. Col: Cambridge Botanical Handbooks. Londres: Cambridge University Press