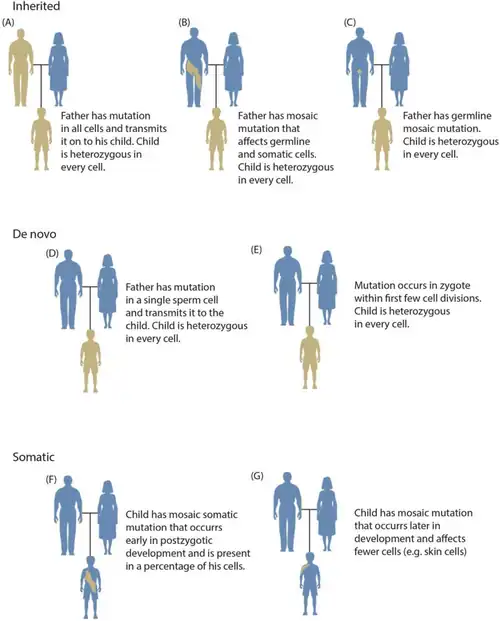
Mutação somática
Uma mutação somática é uma alteração na sequência de DNA de uma célula somática de um organismo multicelular com células reprodutivas dedicadas, ou seja, qualquer mutação que ocorre em uma célula que não seja um gameta, célula germinativa ou gametócito. Diferentemente das mutações germinativas, que podem ser transmitidas aos descendentes de um organismo, as mutações somáticas geralmente não são passadas para os descendentes. Essa distinção é menos clara em plantas, que não possuem uma linhagem germinativa dedicada, e em animais que podem se reproduzir assexuadamente por mecanismos como brotamento, como ocorre em membros do gênero Hydra da classe dos cnidários.
Embora as mutações somáticas não sejam transmitidas aos descendentes do organismo, elas estarão presentes em todos os descendentes de uma célula dentro do mesmo organismo. Muitos cânceres resultam do acúmulo de mutações somáticas.
Fração de células afetadas
O termo somático refere-se geralmente às células do corpo, em contraste com as células reprodutivas (linhagem germinativa), que dão origem ao óvulo ou espermatozoide. Em mamíferos, por exemplo, as células somáticas compõem os órgãos internos, pele, ossos, sangue e tecido conjuntivo.[1]
Na maioria dos animais, a separação entre células germinativas e células somáticas (desenvolvimento germinativo [en]) ocorre nas fases iniciais do desenvolvimento. Após essa segregação no embrião, qualquer mutação fora das células germinativas não pode ser transmitida aos descendentes do organismo.
No entanto, as mutações somáticas são passadas para todos os descendentes de uma célula mutada dentro do mesmo organismo. Assim, uma grande parte do organismo pode carregar a mesma mutação, especialmente se ela ocorrer nas fases iniciais do desenvolvimento.[2] As mutações somáticas que ocorrem mais tarde na vida de um organismo podem ser difíceis de detectar, pois podem afetar apenas uma única célula, como um neurônio pós-mitótico;[3][4] avanços em sequenciamento de célula única [en] são, portanto, ferramentas importantes para o estudo de mutações somáticas.[5] Tanto o DNA nuclear quanto o DNA mitocondrial de uma célula podem acumular mutações; mutações somáticas mitocondriais têm sido implicadas no desenvolvimento de algumas doenças neurodegenerativas.[6]
Exceções à herança

Há muitas exceções à regra de que mutações somáticas não podem ser herdadas pelos descendentes. Muitos organismos não dedicam uma linhagem germinativa separada durante o desenvolvimento inicial. Plantas e animais basais, como esponjas e corais, geram gametas a partir de células-tronco pluripotentes em tecidos somáticos adultos.[7][8] Em plantas com flores, por exemplo, as células germinativas podem surgir de células somáticas adultas no meristema floral. Outros animais sem uma linhagem germinativa designada incluem tunicados e platelmintos.[9]
As mutações somáticas também podem ser transmitidas aos descendentes em organismos que se reproduzem assexuadamente, sem a produção de gametas. Por exemplo, animais do gênero Hydra da classe dos cnidários podem se reproduzir assexuadamente por meio do mecanismo de brotamento (também podem se reproduzir sexualmente). Em hidras, um novo broto se desenvolve diretamente a partir de células somáticas da hidra parental.[10] Uma mutação presente no tecido que dá origem ao organismo filha seria transmitida a esse descendente.
Muitas plantas se reproduzem naturalmente por reprodução vegetativa — crescimento de uma nova planta a partir de um fragmento da planta parental — propagando mutações somáticas sem a etapa de produção de sementes. Humanos induzem artificialmente a reprodução vegetativa por meio de enxertia e estacas.
Causas
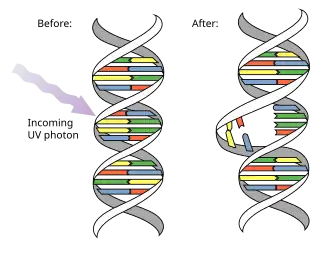
Assim como nas mutações germinativas, as mutações em células somáticas podem surgir devido a fatores endógenos, incluindo erros durante a replicação e reparo do DNA, e exposição a espécies reativas de oxigênio produzidas por processos celulares normais. As mutações também podem ser induzidas por contato com mutagênicos, que podem aumentar a taxa de mutação.
A maioria dos mutagênicos atua causando danos ao DNA — alterações na estrutura do DNA, como dímeros de pirimidina, ou quebra de uma ou ambas as fitas de DNA. Os processos de reparo de DNA podem remover danos ao DNA que, caso contrário, durante a replicação do DNA, causariam mutações. A mutação resulta de danos quando erros no mecanismo de reparo de DNA causam alterações na sequência de nucleotídeos, ou se a replicação ocorre antes que o reparo esteja completo.
Os mutagênicos podem ser físicos, como radiação de raios UV e raios X, ou químicos — moléculas que interagem diretamente com o DNA — como metabólitos [en] de benzo[a]pireno, um potente carcinógeno encontrado na fumaça de tabaco [en].[11] Mutagênicos associados a cânceres são frequentemente estudados para aprender sobre o câncer e sua prevenção.
Frequência de mutação
Pesquisas sugerem que a frequência de mutações [en] é geralmente maior em células somáticas do que em células da linhagem germinativa;[12] além disso, há diferenças nos tipos de mutação observados na linhagem germinativa e no soma.[13] Há variação na frequência de mutação entre diferentes tecidos somáticos dentro do mesmo organismo[13] e entre espécies.[2]
Milholland et al. (2017) examinaram a taxa de mutação de fibroblastos dérmicos [en] (um tipo de célula somática) e células germinativas em humanos e camundongos. Eles mediram a taxa de variantes de nucleotídeo único (SNVs), a maioria das quais é consequência de erro de replicação. Tanto em termos de carga mutacional (total de mutações presentes em uma célula) quanto de taxa de mutação por divisão celular (novas mutações a cada mitose), as taxas de mutação somática foram mais de dez vezes maiores que as da linhagem germinativa, em humanos e camundongos.
Em humanos, a carga mutacional em fibroblastos foi mais de vinte vezes maior que na linhagem germinativa (2,8 × 10−7 comparado com 1,2 × 10−8 mutações por par de bases). Ajustado para diferenças no número estimado de divisões celulares, a taxa de mutação de fibroblastos foi cerca de 80 vezes maior que a da linhagem germinativa (respectivamente, 2,66 × 10−9 vs. 3,3 × 10−11 mutações por par de bases por mitose).[2]
A disparidade na taxa de mutação entre a linhagem germinativa e os tecidos somáticos provavelmente reflete a maior importância da integridade genética na linhagem germinativa do que no soma.[12] A variação na frequência de mutação pode ser devido a diferenças nas taxas de dano ao DNA ou a diferenças no processo de reparo de DNA como resultado de níveis elevados de enzimas de reparo de DNA.[13]
Em Abril de 2022, foi relatado que a maioria dos mamíferos tem aproximadamente o mesmo número de mutações ao final de sua vida, de modo que aqueles com expectativa de vida semelhante terão taxas de mutação somática semelhantes, enquanto aqueles que vivem menos/mais terão uma taxa de mutações somáticas maior/menor, respectivamente.[14][15]
Neurônios
Neurônios pós-mitóticos acumulam mutações somáticas a uma taxa constante ao longo da vida, e essa taxa é aproximadamente semelhante às taxas de mutação de tecidos mitoticamente ativos.[16] As mutações em neurônios podem surgir como consequência de dano endógeno ao DNA [en] e da reparação um tanto imprecisa desse dano, que ocorre constantemente nas células.[16]
Hipermutação somática
Como parte da resposta imune adaptativa, as células B produtoras de anticorpos experimentam uma taxa de mutação muitas vezes maior que a taxa normal de mutação. A taxa de mutação nas sequências codificantes de ligação ao antígeno dos genes de imunoglobulinas é até 1.000.000 de vezes maior do que em linhagens celulares fora do sistema linfóide. Um passo importante na maturação de afinidade, a hipermutação somática ajuda as células B a produzir anticorpos com maior afinidade pelo antígeno.[17]
Doenças
As mutações somáticas acumulam-se nas células de um organismo à medida que ele envelhece e a cada rodada de divisão celular; o papel das mutações somáticas no desenvolvimento do câncer é bem estabelecido, e o acúmulo de mutações somáticas está implicado na biologia do envelhecimento.[4]
Mutações em células-tronco neurais (especialmente durante a neurogênese)[18] e em neurônios pós-mitóticos levam à heterogeneidade genômica dos neurônios — referida como "mosaicismo cerebral somático".[3] O acúmulo de mutações relacionadas à idade em neurônios pode estar ligado a doenças neurodegenerativas, incluindo a Doença de Alzheimer, mas a associação ainda não foi comprovada. A maioria das células do sistema nervoso central em adultos é pós-mitótica, e mutações em adultos podem afetar apenas um único neurônio. Diferentemente do câncer, onde as mutações resultam em proliferação clonal, mutações somáticas prejudiciais podem contribuir para doenças neurodegenerativas por morte celular.[19] A avaliação precisa da carga de mutação somática em neurônios, portanto, permanece difícil.
Papel na carcinogênese
Se uma mutação ocorre em uma célula de um organismo, essa mutação estará presente em todos os descendentes dessa célula dentro do mesmo organismo. O acúmulo de certas mutações ao longo de gerações de células somáticas é parte do processo de transformação maligna, de célula normal a célula cancerosa.
Células com mutações heterozigóticas de perda de função (uma cópia funcional de um gene e uma cópia mutada) podem funcionar normalmente com a cópia não mutada até que a cópia funcional seja espontaneamente mutada somaticamente. Esse tipo de mutação ocorre frequentemente em organismos vivos, mas é difícil medir a taxa. Medir essa taxa é importante para prever a taxa com que as pessoas podem desenvolver câncer.
Ver também
Referências
- ↑ Campbell, Neil A., 1946-2004. (2009). Biology. Reece, Jane B. 8th ed. San Francisco: Pearson Benjamin Cummings. ISBN 978-0-8053-6844-4. OCLC 174138981
- ↑ a b c Milholland, Brandon; Dong, Xiao; Zhang, Lei; Hao, Xiaoxiao; Suh, Yousin; Vijg, Jan (9 de Maio de 2017). «Differences between germline and somatic mutation rates in humans and mice». Nature Communications. 8. 15183 páginas. Bibcode:2017NatCo...815183M. ISSN 2041-1723. PMC 5436103
 . PMID 28485371. doi:10.1038/ncomms15183
. PMID 28485371. doi:10.1038/ncomms15183
- ↑ a b Verheijen, Bert M.; Vermulst, Marc; van Leeuwen, Fred W. (2018). «Somatic mutations in neurons during aging and neurodegeneration». Acta Neuropathologica (em inglês). 135 (6): 811–826. ISSN 0001-6322. PMC 5954077
 . PMID 29705908. doi:10.1007/s00401-018-1850-y
. PMID 29705908. doi:10.1007/s00401-018-1850-y
- ↑ a b Zhang, Lei; Vijg, Jan (23 de Novembro de 2018). «Somatic Mutagenesis in Mammals and Its Implications for Human Disease and Aging». Annual Review of Genetics. 52: 397–419. ISSN 0066-4197. PMC 6414224
 . PMID 30212236. doi:10.1146/annurev-genet-120417-031501
. PMID 30212236. doi:10.1146/annurev-genet-120417-031501
- ↑ Gawad, Charles; Koh, Winston; Quake, Stephen R. (2016). «Single-cell genome sequencing: current state of the science». Nature Reviews Genetics (em inglês). 17 (3): 175–188. ISSN 1471-0056. PMID 26806412. doi:10.1038/nrg.2015.16
- ↑ Schon, Eric A.; DiMauro, Salvatore; Hirano, Michio (2012). «Human mitochondrial DNA: roles of inherited and somatic mutations». Nature Reviews. Genetics. 13 (12): 878–890. ISSN 1471-0056. PMC 3959762
 . PMID 23154810. doi:10.1038/nrg3275
. PMID 23154810. doi:10.1038/nrg3275
- ↑ Schoen, Daniel J.; Schultz, Stewart T. (2 de Novembro de 2019). «Somatic Mutation and Evolution in Plants». Annual Review of Ecology, Evolution, and Systematics. 50 (1): 49–73. ISSN 1543-592X. doi:10.1146/annurev-ecolsys-110218-024955

- ↑ Radzvilavicius, Arunas L.; Hadjivasiliou, Zena; Pomiankowski, Andrew; Lane, Nick (20 de Dezembro de 2016). «Selection for Mitochondrial Quality Drives Evolution of the Germline». PLOS Biology. 14 (12): e2000410. ISSN 1544-9173. PMC 5172535
 . PMID 27997535. doi:10.1371/journal.pbio.2000410
. PMID 27997535. doi:10.1371/journal.pbio.2000410
- ↑ Seipel, Katja; Yanze, Nathalie; Schmid, Volker (2004). «The germ line and somatic stem cell gene Cniwi in the jellyfish Podocoryne carnea.». The International Journal of Developmental Biology (em inglês). 48 (1): 1–7. ISSN 0214-6282. PMID 15005568. doi:10.1387/ijdb.15005568

- ↑ Otto, Joann J.; Campbell, Richard D. (1977). «Budding in Hydra attenuata: Bud stages and fate map». Journal of Experimental Zoology (em inglês). 200 (3): 417–428. ISSN 0022-104X. PMID 874446. doi:10.1002/jez.1402000311
- ↑ Armstrong, Ben; Hutchinson, Emma; Unwin, John; Fletcher, Tony (2004). «Lung Cancer Risk after Exposure to Polycyclic Aromatic Hydrocarbons: A Review and Meta-Analysis». Environmental Health Perspectives (em inglês). 112 (9): 970–978. ISSN 0091-6765. PMC 1247189
 . PMID 15198916. doi:10.1289/ehp.6895
. PMID 15198916. doi:10.1289/ehp.6895
- ↑ a b Murphey, Patricia; McLean, Derek J.; McMahan, C. Alex; Walter, Christi A.; McCarrey, John R. (2013). «Enhanced Genetic Integrity in Mouse Germ Cells». Biology of Reproduction. 88 (1). 6 páginas. ISSN 0006-3363. PMC 4434944
 . PMID 23153565. doi:10.1095/biolreprod.112.103481
. PMID 23153565. doi:10.1095/biolreprod.112.103481
- ↑ a b c Chen, Chen; Qi, Hongjian; Shen, Yufeng; Pickrell, Joseph; Przeworski, Molly (2017). «Contrasting Determinants of Mutation Rates in Germline and Soma». Genetics (em inglês). 207 (1): 255–267. ISSN 0016-6731. PMC 5586376
 . PMID 28733365. doi:10.1534/genetics.117.1114
. PMID 28733365. doi:10.1534/genetics.117.1114
- ↑ Cagan, Alex; Baez-Ortega, Adrian; Brzozowska, Natalia; Abascal, Federico; Coorens, Tim H. H.; Sanders, Mathijs A.; Lawson, Andrew R. J.; Harvey, Luke M. R.; Bhosle, Shriram; Jones, David; Alcantara, Raul E. (21 de Abril de 2022). «Somatic mutation rates scale with lifespan across mammals». Nature (em inglês). 604 (7906): 517–524. Bibcode:2022Natur.604..517C. ISSN 0028-0836. PMC 9021023
 . PMID 35418684. doi:10.1038/s41586-022-04618-z
. PMID 35418684. doi:10.1038/s41586-022-04618-z
- ↑ «Mutations across species reveal clues to ageing». BBC News (em inglês). 13 de Abril de 2022. Consultado em 20 de Abril de 2022
- ↑ a b Abascal F, Harvey LMR, Mitchell E, Lawson ARJ, Lensing SV, Ellis P, Russell AJC, Alcantara RE, Baez-Ortega A, Wang Y, Kwa EJ, Lee-Six H, Cagan A, Coorens THH, Chapman MS, Olafsson S, Leonard S, Jones D, Machado HE, Davies M, Øbro NF, Mahubani KT, Allinson K, Gerstung M, Saeb-Parsy K, Kent DG, Laurenti E, Stratton MR, Rahbari R, Campbell PJ, Osborne RJ, Martincorena I. Somatic mutation landscapes at single-molecule resolution. Nature. 2021 May;593(7859):405-410. doi: 10.1038/s41586-021-03477-4. Epub 28 de Abril de 2021. PMID 33911282
- ↑ Teng, Grace; Papavasiliou, F. Nina (2007). «Immunoglobulin Somatic Hypermutation». Annual Review of Genetics (em inglês). 41 (1): 107–120. ISSN 0066-4197. PMID 17576170. doi:10.1146/annurev.genet.41.110306.130340
- ↑ Bae, Taejeong; Tomasini, Livia; Mariani, Jessica; Zhou, Bo; Roychowdhury, Tanmoy; Franjic, Daniel; Pletikos, Mihovil; Pattni, Reenal; Chen, Bo-Juen; Venturini, Elisa; Riley-Gillis, Bridget (2 de Fevereiro de 2018). «Different mutational rates and mechanisms in human cells at pregastrulation and neurogenesis». Science (em inglês). 359 (6375): 550–555. Bibcode:2018Sci...359..550B. ISSN 0036-8075. PMC 6311130
 . PMID 29217587. doi:10.1126/science.aan8690
. PMID 29217587. doi:10.1126/science.aan8690
- ↑ Leija-Salazar, M.; Piette, C.; Proukakis, C. (2018). «Review: Somatic mutations in neurodegeneration» (PDF). Neuropathology and Applied Neurobiology (em inglês). 44 (3): 267–285. PMID 29369391. doi:10.1111/nan.12465