Dímero de pirimidina
Dímero de pirimidina é um composto orgânico formado por duas bases pirimidínicas sucessivas ou espacialmente próximas numa seqüência de DNA, unidas por uma ligação covalente. É um composto relativamente estável, resistente a ação de agentes químicos e enzimas. Sua formação está condicionada a agentes externos, e portanto é considerado um dano ao material genético, e sua presença pode impedir o processo de replicação do DNA, causando morte celular.
Os dímeros de pirimidina são formados principalmente mediante a ação de radiação ionizante. A radiação promove a quebra das ligações entre as pirimidinas e as purinas na fita oposta e a pronta união entre as pirimidinas adjacentes, ou próximas entre si por ocasião de uma dobra na cadeia. A estabilidade desta nova ligação faz com que as duas fitas do DNA percam permanentemente o contato entre si nos pontos onde os dímeros são formados, prejudicando a codificação de RNA e comprometendo as funções da célula ainda em intérfase. No momento da replicação celular, a enzima DNA-Polimerase é a responsável pelo reconhecimento e correção de danos nas fitas de DNA, bem como pela sua separação e síntese de novas fitas. No entanto, esta enzima é incapaz de corrigir os dímeros de pirimidina, bem como de reconhecer estas bases pirimidínicas no momento da separação das fitas e da polimerização de novas fitas, virtualmente paralisando todo o processo de replicação de maneira irreversível. O DNA então se torna inoperante, causando a morte celular.
Os dímeros de pirimidina são lesões moleculares produzidas no ADN formadas por bases timina ou citosina (bases pirimidínicas) adjacentes, que se unem entre si de forma anormal formando dímeros. Estas lesões são causadas por reações fotoquímicas com a luz ultravioleta (UV).[1][2]
A luz ultravioleta induz a formação de ligações covalentes por reações localizadas em ligações duplas C=C .[3] No ARN bicatenário, podem também acumular-se dímeros de uracilo como resultado da radiação ultravioleta (UV).
Dois produtos comuns da irradiação UV são os dímeros de pirimidina ciclobutano (CPDs, entre os quais se incluem os dímeros de timina) e os fotoprodutos 6,4. Estas lesões pré-mutagénicas alteram a estrutura do ADN e consequentemente inibem as polimerases e fazem com que a replicação se detenha. Os dímeros podem ser reparados por fotorreativação ou reparação por excisão de nucleótidos, mas os dímeros que não são reparados são mutagénicos. Os dímeros de pirimidina são uma causa importante de melanomas em humanos.
Tipos de Dímeros
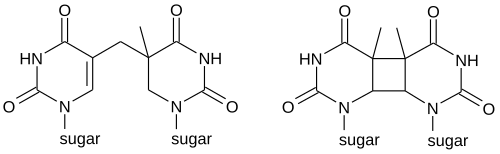
Um dímero de pirimidina ciclobutano (CPD) contém um anel de quatro membros originado pelo acoplamento de ligações duplas C=C das pirimidinas.[4][5][6] Estes dímeros interferem com o emparelhamento de bases durante a replicação do ADN, originando mutações.
Os fotoprodutos 6,4 ou 6,4 pirimidina-pirimidonas, surgem com uma frequência 3 vezes menor do que os dímeros de pirimidina ciclobutano, mas são mais mutagénicos.[7]
Foi estudada a enzima bacteriana fotoproduto de esporo liase (ou SP liase), que proporciona outra via enzimática para reparar os fotodímeros de timina, na qual se requer S-adenosilmetionina.[8]
Mutagénese
Os enzimas ADN polimerases de translesão introduzem frequentemente mutações em dímeros de pirimidina, tanto em procariotas (mutagénese de resposta SOS) como em eucariotas. Embora os dímeros de pirimidina ciclobutano timina-timina (dímeros TT) sejam as lesões mais frequentes causadas pela luz UV, as polimerases de translesão tendem a introduzir adeninas (A), de modo que os dímeros TT são frequentemente replicados corretamente. Por outro lado, as citosinas (C) envolvidas nos dímeros de pirimidina ciclobutano tendem a ser desaminadas, induzindo uma transição de C para T.[9]
Reparação do ADN
Os dímeros de pirimidina introduzem alterações conformacionais locais na estrutura do ADN, as quais permitem o reconhecimento da lesão pelos enzimas reparadores.[10]
Na maioria dos organismos (exceto os mamíferos placentários como os humanos) podem ser reparados por **fotorreativação**.[11] A fotorreativação é um processo de reparação no qual uns enzimas fotoliases revertem diretamente os dímeros de pirimidina ciclobutano por reações fotoquímicas. As lesões na cadeia do ADN são reconhecidas por estes enzimas, o que é seguido pela absorção de comprimentos de onda >$300 \text{ nm}$ (ou seja, luz solar e fluorescência), que impulsiona a catálise. Esta absorção permite que ocorram as reações fotoquímicas, o que resulta na eliminação de dímeros de pirimidina, que voltam ao seu estado original.[12]
A reparação por excisão de nucleótidos é um mecanismo mais geral de reparação de lesões no ADN. Este processo excisa os dímeros de pirimidinas ciclobutano, e sintetiza novo ADN para substituir a região que rodeia a lesão na molécula.[12] Na doença genética humana xeroderma pigmentoso está ausente o mecanismo de reparação por excisão de nucleótidos, e isto resulta numa descoloração da pele e muitos tumores ao expor a pele à luz ultravioleta. Os dímeros de pirimidina não reparados em humanos podem originar melanomas.[13]
Referências
- ↑ David S. Goodsell (2001). «The Molecular Perspective: Ultraviolet Light and Pyrimidine Dimers». The Oncologist. 6 (3): 298–299. PMID 11423677. doi:10.1634/theoncologist.6-3-298. Consultado em 11 de março de 2015. Cópia arquivada em 30 de abril de 2009
- ↑ E. C. Friedberg, G. C. Walker, W. Siede, R. D. Wood, R. A. Schultz and T. Ellenberger (2006). DNA repair and mutagenesis. Washington: ASM Press. p. 1118. ISBN 978-1-55581-319-2
- ↑ S. E. Whitmore, C. S. Potten, C. A. Chadwick, P. T. Strickland, W. L. Morison (2001). «Effect of photoreactivating light on UV radiation-induced alterations in human skin». Photodermatol. Photoimmunol. Photomed. 17 (5): 213–217. PMID 11555330. doi:10.1034/j.1600-0781.2001.170502.x
- ↑ R. B. Setlow (1966). «Cyclobutane-Type Pyrimidine Dimers in Polynucleotides». Science. 153 (3734): 379–386. PMID 5328566. doi:10.1126/science.153.3734.379
- ↑ Expert reviews in molecular medicine (2 de dezembro de 2002). «Structure of the major UV-induced photoproducts in DNA.» (PDF). Cambridge University Press. Consultado em 11 de março de 2015. Arquivado do original (PDF) em 21 de março de 2005
- ↑ Christopher Mathews and K.E. Van Holde (1990). Biochemistry 2nd ed. [S.l.]: Benjamin Cummings Publication. p. 1168. ISBN 978-0-8053-5015-9
- ↑ Van Holde, K. E.; Mathews, Christopher K. (1990). Biochemistry. Menlo Park, Calif: Benjamin/Cummings Pub. Co. ISBN 0-8053-5015-2
- ↑ Jeffrey M. Buis, Jennifer Cheek, Efthalia Kalliri, and Joan B. Broderick (2006). Characterization of an Active Spore Photoproduct Lyase, a DNA Repair Enzyme in the Radical S-Adenosylmethionine Superfamily. Journal of Biological Chemistry. 281. [S.l.: s.n.] pp. 25994–26003. PMID 16829680. doi:10.1074/jbc.M603931200
- ↑ J. H. Choi, A. Besaratinia ,D. H. Lee, C. S. Lee, G. P. Pfeifer (2006). The role of DNA polymerase iota in UV mutational spectra. Mutat. Res. 599. [S.l.: s.n.] pp. 58–65. PMID 16472831. doi:10.1016/j.mrfmmm.2006.01.003
- ↑ Kemmink Johan, Boelens Rolf, Koning Thea M.G., Kaptein Robert, Van , der Morel Gijs A., Van Boom Jacques H. (1987). «Conformational Changes in the oligonucleotide duplex d(GCGTTGCG)*d(GCGAAGCG) induced by formation of a cis-syn thymine dimer». European Journal of Biochemistry. 162: 31–43. PMID 3028790. doi:10.1111/j.1432-1033.1987.tb10538.x
- ↑ Essen LO, Klar T (2006). «Light-driven DNA repair by photolyases». Cell Mol Life Sci. 63 (11): 1266–77. PMID 16699813. doi:10.1007/s00018-005-5447-y
- ↑ a b Friedberg, Errol C. (23 de xaneiro de 2003) "DNA Damage and Repair". Nature 421, 436-439. doi:10.1038/nature01408
- ↑ Vink Arie A., Roza Len (2001). «Biological consequences of cyclobutane pyrimidine dimers». Journal of Photochemistry and Photobiology B: Biology. 65 (2–3): 101–104. doi:10.1016/S1011-1344(01)00245-7