Reparação por excisão de nucleótidos
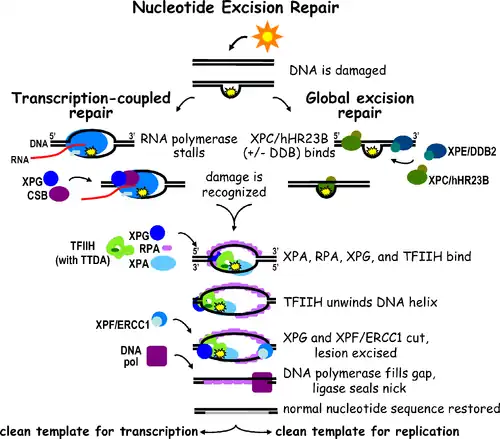
A reparação por excisão de nucleótidos (abreviado como NER) é um mecanismo de reparação de ADN.[2] Os danos no ADN ocorrem constantemente devido à exposição a certos produtos químicos, como agentes intercalantes, radiação e outros agentes mutagénicos. Existem três vias de reparação por excisão para reparar danos no ADN de cadeia simples, nomeadamente: reparação por excisão de nucleótidos (NER), reparação por excisão de bases (BER) e reparação por incompatibilidade de ADN (MMR). Embora a via BER possa reconhecer lesões específicas não volumosas no ADN, apenas consegue corrigir bases danificadas que são removidas por glicosidases específicas. Da mesma forma, a via de reparação por incompatibilidade apenas tem como alvo os pares de bases de Watson-Crick.
A reparação por excisão de nucleótidos (NER) é um mecanismo de excisão particularmente importante que remove os danos no ADN induzidos pela luz ultravioleta (UV). Os danos no ADN induzidos por UV resultam em adutos de ADN volumosos; Estes adutos são principalmente dímeros de timina e 6,4-fotoprodutos. O reconhecimento do dano resulta na remoção de um pequeno segmento de ADN de cadeia simples contendo a lesão. O ADN de cadeia simples intacto permanece no local e é utilizado pela ADN polimerase como molde para sintetizar uma curta sequência complementar. A ligação final que completa a NER e forma o DNA de dupla fita é realizada pela DNA ligase. A NER pode ser dividida em duas subvias: NER genómica global (GG-NER ou GGR) e NER acoplada à transcrição (TC-NER ou TCR). As duas subvias diferem na forma como reconhecem os danos no ADN, mas partilham o mesmo processo de incisão, reparação e ligação da lesão.
A importância da NER é evidenciada pelas graves doenças humanas resultantes de mutações genéticas congénitas que afetam as proteínas da NER. O Xeroderma pigmentoso e o Síndrome de Cockayne são dois exemplos de doenças associadas à NER.
Reparação por excisão de nucleótidos em eucariotas
A reparação por excisão de nucleótidos é mais complexa em eucariotas do que em procariotas, mas o princípio geral é semelhante. Existem 9 proteínas principais envolvidas na NER em células de mamíferos. Nas deficiências de certas proteínas que causam doenças, os nomes das proteínas estão associados aos das doenças. Os nomes das proteínas XPA, XPB, XPC, XPD, XPE, XPF e XPG são derivados de хeroderma pigmentoso, enquanto que CSA e CSB são proteínas ligadas à síndrome de Cockayne. Além disso, as proteínas ERCC1, RPA, RAD23A, RAD23B e outras estão também envolvidas na reparação por excisão de nucleótidos. Uma lista mais completa de proteínas envolvidas na reparação por excisão de nucleótidos pode ser encontrada em abaixo.
A reparação por excisão de nucleótidos pode ser dividida em duas subvias: NER genómica global (GG-NER) e NER acoplada à transcrição (TC-NER). Três conjuntos distintos de proteínas estão envolvidos no reconhecimento de danos no ADN em cada subvia. Após o reconhecimento do dano, que é distinto em cada uma, as subvias convergem para as etapas de incisão dupla, reparação e ligação.
Reconhecimento de danos
NER Genómica Global (GG-NER)
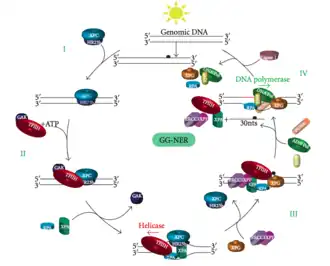
Reparações genómicas globais de NER Danos tanto na fita transcrita como na não transcrita de ADN em genes ativos e inativos em todo o genoma. Este processo não depende da transcrição. Esta via emprega diversas proteínas "sensoras de danos", como o complexo de ligação ao dano do DNA (DDB) e o XPC-Rad23B, que varrem constantemente o genoma e reconhecem distorções na dupla hélice: o complexo XPC-Rad23B é responsável pelo reconhecimento de distorções, enquanto DDB1 e DDB2 (XPE) também podem reconhecer alguns tipos de danos causados pela luz UV. Além disso, o XPA desempenha uma função de reconhecimento de danos que ainda não está bem definida. Após a identificação dos locais danificados, as seguintes proteínas de reparação são então recrutadas para o ADN danificado para verificar a presença de danos, clivar o ADN danificado em redor da lesão e, em seguida, preencher a área de reparação.
Doenças associadas ao GG-NER
As mutações na maquinaria do GG-NER são responsáveis por muitas doenças genéticas, tais como: xeroderma pigmentoso (XP): fotossensibilidade grave, elevadas taxas de cancro em zonas do corpo expostas ao sol, como a pele.
Reparação acoplada à transcrição (TC-NER)
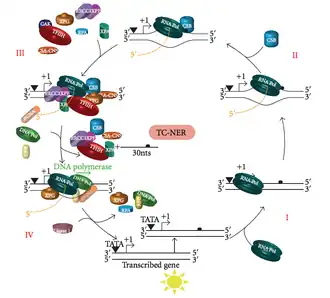
Em qualquer momento, a maior parte do genoma de um organismo não está a sofrer transcrição. Existe uma diferença na eficiência da NER entre regiões transcricionalmente silenciosas e ativas do genoma. Para muitos tipos de lesões, a NER repara as cadeias transcritas de genes transcricionalmente ativos mais rapidamente do que as cadeias não transcritas e o ADN transcricionalmente silencioso.
A TC-NER e a GG-NER diferem apenas nas fases iniciais do reconhecimento de danos no ADN. A principal diferença entre a TC-NER e a GG-NER é que a TC-NER não requer proteínas XPC ou DDB para o reconhecimento da distorção em células de mamíferos. Em vez disso, a TC-NER é iniciada quando a RNA polimerase fica retida numa lesão de ADN: a RNA polimerase bloqueada serve como sinal de reconhecimento de danos, substituindo a necessidade de complexos XPC-RAD23B e DDB com propriedades de reconhecimento de distorção. As proteínas CS (CSA e CSB) ligam-se a alguns tipos de danos no ADN no lugar do XPC-Rad23B.
Outros mecanismos de reparação são possíveis, mas são menos precisos e eficientes.
Doenças associadas à TC-NER
A TC-NER é iniciada quando a RNA polimerase fica retida numa lesão no ADN, e os complexos proteicos auxiliam a polimerase a reverter. As mutações que afetam a maquinaria da TC-NER são responsáveis por múltiplas doenças genéticas, tais como:
- Tricotiodistrofia: alguns indivíduos são fotossensíveis, ictiose, atraso mental/físico.
- Síndrome de Cockayne: fotossensibilidade, atraso mental, características semelhantes à proxerose, microcefalia.
Incisão dupla
A enzima-chave envolvida na dupla excisão é o fator de transcrição II H (TFIIH). Em primeiro lugar, o TFIIH e o XPG são recrutados para o local do dano no ADN (o XPG estabiliza o TFIIH). As subunidades TFIIH XPD e XPB atuam como helicases 5’-3’ e 3’-5’, respetivamente, e ajudam a desenrolar o ADN e a gerar uma junção entre o ADN de cadeia dupla e de cadeia simples em torno da bolha de transcrição. Para além de estabilizar o TFIIH, o XPG possui também atividade de endonuclease; corta o dano no ADN do lado 3’, enquanto a proteína heterodimérica XPF–ERCC1 corta do lado 5’. A incisão dupla provoca a remoção de ADN de cadeia simples com uma lacuna de cadeia simples de 25 a ~30 nucleótidos. Os oligonucleótidos de "pequeno ADN contendo dano excisado" (sedDNA) são inicialmente libertados do duplex em complexo com TFIIH, mas depois dissociam-se de forma ATP-dependente e ligam-se à RPA. A inibição da síntese e ligação de ADN que preenchem as lacunas resulta na acumulação de sedDNAs ligados à RPA na célula.
A proteína de replicação A (RPA) e a XPA são as duas últimas proteínas associadas ao principal complexo de reparação do NER. Estas duas proteínas já estão presentes antes da ligação da TFIIH, uma vez que estão envolvidas na verificação de danos no ADN. Podem também proteger o ADN de fita simples. Após a verificação, a incisão é feita no lado 5' e a reparação do ADN começa antes da incisão no lado 3'. Isto ajuda a reduzir o ADN de cadeia simples que é exposto durante o processo de reparação.
Reparação e ligação
O fator de replicação C (RFC) transporta o antigénio nuclear de célula em proliferação (PCNA) para a cadeia de ADN. Isto permite que as ADN polimerases envolvidas na reparação (δ, ε e/ou κ) copiem as cadeias não danificadas através de translocação. A DNA ligase I e a aba de endonuclease 1 ou o complexo ligase-III-XRCC1 selam a lacuna para completar a NER.
A NER nos procariontes: proteínas Uvr

O processo de reparação por excisão de nucleótidos é controlado em Escherichia coli pelo complexo enzimático da endonuclease UvrABC, que consiste em quatro proteínas Uvr: UvrA, UvrB, UvrC e a helicase de ADN II (por vezes designada por UvrD neste complexo). Em primeiro lugar, um complexo UvrA-UvrB revê o ADN, no qual a subunidade UvrA é responsável pelo reconhecimento de distorções na hélice, causadas, por exemplo, por dímeros de pirimidina. Quando o complexo reconhece tais distorções, a subunidade UvrA abandona o complexo e, de seguida, chega uma proteína UvrC, que se liga ao monómero UvrB e, assim, forma um novo dímero UvrBC. A UvrB cliva uma ligação fosfodiéster localizada 4 nucleótidos a jusante do local de dano no ADN, e a UvrC cliva uma ligação fosfodiéster localizada 8 nucleótidos a montante, criando um segmento clivado de 12 nucleótidos. A DNA helicase II (ou UvrD) chega então e remove o segmento clivado, quebrando ativamente as ligações de hidrogénio entre as bases complementares. A lacuna resultante é então preenchida utilizando a DNA polimerase I e a DNA ligase. O processo básico de clivagem é muito semelhante nas células eucarióticas, mas nestas células há geralmente mais proteínas envolvidas. O que acontece na E. coli é um exemplo simples.[5]
O modo TC-NER também existe nas bactérias e é mediado pela proteína TRCF (Mfd). A TRCF é uma SF2 ATPase que utiliza a hidrólise de ATP para se translocar para o ADN de cadeia dupla a montante da bolha de transcrição e translocar a RNA polimerase para a frente, iniciando assim a dissociação do complexo de alongamento da RNA polimerase ternária. A TRCF também recruta a maquinaria de reparação por excisão de nucleótidos Uvr(A)BC por interação física direta com a subunidade UvrA.
A NER e o cancro

Embora os estudos históricos tenham produzido resultados conflituantes, a variação genética ou mutação nos genes de reparação por excisão de nucleótidos pode ter impacto no risco de cancro ao afetar a eficiência da reparação. polimorfismos de nucleótidos únicos (SNPs) e SNPs codificantes não sinónimos (nsSNPs) estão presentes em níveis muito baixos (<1%) na população humana.[7] Se localizadas em genes NER ou sequências regulatórias, tais mutações podem afetar negativamente a capacidade de reparação do ADN, resultando num aumento da probabilidade de desenvolvimento de cancro. Embora o impacto funcional de todos os polimorfismos não esteja caracterizado, sabe-se que alguns polimorfismos nos genes de reparação do ADN ou nas suas sequências reguladoras induzem alterações fenotípicas e estão implicados no desenvolvimento do cancro.[8] Um estudo de caso de cancro do pulmão encontrou uma fraca associação entre os polimorfismos específicos do SNP do NER e o risco de cancro do pulmão.[9] Os resultados indicam que algumas variações polimórficas herdadas nos genes NER causam predisposição para o cancro do pulmão e, potencialmente, para outros tipos de cancro.
A disfunção do NER leva a polimorfismos do ADN
Dois genes importantes na via NER, nos quais se verificou que os polimorfismos têm um impacto funcional e fenotípico, são os genes XPD e XPC.[10] O XPD, também chamado de ERCC2, serve para abrir o ADN em redor do local do dano durante a NER, para além de outras atividades transcricionais. Estudos demonstraram que os polimorfismos no exon 10 (G>A)(Asp312Asn) e no exão 23 (A>T)(Lys751Gln) estão ligados à predisposição genética para vários tipos de cancro.[11][12] O gene XPC é responsável pela codificação de uma proteína que reconhece o ADN durante a porção inicial da via NER. Este gene pode apresentar polimorfismos no íntron 9 e SNPs no éxon 15, que também têm sido correlacionados com o risco de cancro. Um polimorfismo de inserção/deleção bialélico (AT) no íntron 9 do gene XPC está associado a um risco aumentado de cancro de pele, mama e próstata.[12][13][14] especialmente nas populações do norte da Índia.
Impacto no prognóstico do cancro
O estudo do cancro hereditário xeroderma pigmentoso (XP) ajudou a identificar vários genes que codificam proteínas na via NER, dois dos quais são XPC e XPD. O xeroderma pigmentoso é causado por uma deficiência homozigótica que afeta a reparação de danos no ADN por UV (TC-NER), o que aumenta o risco de cancro de pele do paciente em 1000 vezes. Em doentes heterozigóticos, o risco de cancro é esporádico, mas pode ser previsto com base numa estimativa analítica de polimorfismos no xeroderma pigmentoso relacionados com genes de reparação do ADN purificados a partir de linfócitos.[15] Num estudo das taxas de recidiva em cancros colorretais de alto risco em estádio II e III, o polimorfismo 2251A>C no XPD (ERCC2) foi significativamente correlacionado com a recidiva precoce após tratamento de quimioterapia.[16] Os efeitos dos genes NER polimórficos são aditivos e, quanto maior a frequência de variantes, maior o risco de cancro.[15][16][17]
Referências
- ↑ Fuss JO, Cooper PK (Junho de 2006). «DNA repair: dynamic defenders against cancer and aging». PLoS Biol. 4 (6): e203. PMC 1475692
 . PMID 16752948. doi:10.1371/journal.pbio.0040203
. PMID 16752948. doi:10.1371/journal.pbio.0040203
- ↑ Carroll SB; Wessler SR; Griffiths AJFl; Lewontin RC (2008). Introduction to genetic analysis. New York: W.H. Freeman and CO. pp. 534. ISBN 0-7167-6887-9
- ↑ a b Le May N, Egly JM, Coin F (2010). «True lies: the double life of the nucleotide excision repair factors in transcrição e reparo de DNA». J Nucleic Acids. 2010. PMC 2915888
 . PMID 20725631. doi:10.4061/2010/616342
. PMID 20725631. doi:10.4061/2010/616342
- ↑ Morita R, Nakane S, Shimada A, et al. (2010). «Molecular mechanisms of the whole DNA repair system: a comparison of bacterial and eukaryotic systems». J Nucleic Acids. 2010. 179594 páginas. PMC 2957137
 . PMID 20981145. doi:10.4061/2010/179594
. PMID 20981145. doi:10.4061/2010/179594
- ↑ Truglio JJ, Croteau DL, Van Houten B, Kisker C (Fevereiro de 2006). «Prokaryotic nucleotide excision repair: the UvrABC system». Chem. Rev. 106 (2): 233–52. PMID 16464004. doi:10.1021/cr040471u
- ↑ Zhang Y, Rohde LH, Wu H (junho de 2009). «Involvement of nucleotide excision and mismatch repair mechanisms in double strand break repair». Curr. Genomics. 10 (4): 250–8. PMC 2709936
 . PMID 19949546. doi:10.2174/138920209788488544
. PMID 19949546. doi:10.2174/138920209788488544
- ↑ Kwok PY, Gu Z (December 1999). «Single nucleotide polymorphism libraries: why and how are we building them?». Mol Med Today. 5 (12): 538–43. PMID 10562720. doi:10.1016/S1357-4310(99)01601-9 Verifique data em:
|data=(ajuda) - ↑ Karahalil B, Bohr V, Wilson D (October 2012). «Impact of DNA polymorphisms in key DNA base excision repair proteins on cancer risk». Hum Exp Toxicol. 31 (10): 981–1005. PMID 23023028. doi:10.1177/0960327112444476 Verifique data em:
|data=(ajuda) - ↑ Sakoda LC, Loomis MM, Doherty JA, Julianto L, Barnett MJ, Neuhouser ML, Thornquist MD, Weiss NS, Goodman GE, Chen C (2012). «Germ line variation in nucleotide excision repair genes and lung cancer risk in smokers». Int J Mol Epidemiol Genet. 3 (1): 1–17. PMC 3316453
 . PMID 22493747
. PMID 22493747
- ↑ Hou SM, Fält S, Angelini S, Yang K, Nyberg F, Lambert B, Hemminki K (Abril de 2002). «The XPD variant alleles are associated with increased aromatic DNA adduct level and lung cancer risk». Carcinogenesis. 23 (4): 599–603. PMID 11960912. doi:10.1093/carcin/23.4.599
- ↑ Wang M, Gu D, Zhang Z, Zhou J, Zhang Z (2009). «XPD polymorphisms, cigarette smoking, and bladder cancer risk: a meta-analysis». J. Toxicol. Environ. Health Part A. 72 (11–12): 698–705. PMID 19492231. doi:10.1080/15287390902841029
- ↑ a b Mittal RD, Mandal RK (January 2012). «Genetic variation in nucleotide excision repair pathway genes influence prostate and bladder cancer susceptibility in North Indian population». Indian J Hum Genet. 18 (1): 47–55. PMC 3385179
 . PMID 22754221. doi:10.4103/0971-6866.96648 Verifique data em:
. PMID 22754221. doi:10.4103/0971-6866.96648 Verifique data em: |data=(ajuda) - ↑ Blankenburg S, König IR, Moessner R, Laspe P, Thoms KM, Krueger U, Khan SG, Westphal G, Berking C, Volkenandt M, Reich K, Neumann C, Ziegler A, Kraemer KH, Emmert S (junho de 2005). «Assessment of 3 xeroderma pigmentosum group C gene polymorphisms and risk of cutaneous melanoma: a case-control study». Carcinogenesis. 26 (6): 1085–90. PMID 15731165. doi:10.1093/carcin/bgi055
- ↑ Shore RE, Zeleniuch-Jacquotte A, Currie D, Mohrenweiser H, Afanasyeva Y, Koenig KL, Arslan AA, Toniolo P, Wirgin I (maio de 2008). «Polymorphisms in XPC and ERCC2 genes, smoking and breast cancer risk». Int. J. Cancer. 122 (9): 2101–5. PMID 18196582. doi:10.1002/ijc.23361
- ↑ a b Qiao Y, Spitz MR, Guo Z, Hadeyati M, Grossman L, Kraemer KH, Wei Q (Novembro de 2002). «Rapid assessment of repair of ultraviolet DNA damage with a modified host-cell reactivation assay using a luciferase reporter gene and correlation with polymorphisms of DNA repair genes in normal human lymphocytes». Mutat. Res. 509 (1–2): 165–74. PMID 12427537. doi:10.1016/S0027-5107(02)00219-1
- ↑ a b Huang MY, Fang WY, Lee SC, Cheng TL, Wang JY, Lin SR (2008). «ERCC2 2251A>C genetic polymorphism was highly correlated with early relapse in high-risk stage II and stage III colorectal cancer patients: a preliminary study». BMC Cancer. 8. 50 páginas. PMC 2262891
 . PMID 18267032. doi:10.1186/1471-2407-8-50
. PMID 18267032. doi:10.1186/1471-2407-8-50
- ↑ Spitz MR, Wu X, Wang Y, Wang LE, Shete S, Amos CI, Guo Z, Lei L, Mohrenweiser H, Wei Q (fevereiro de 2001). «Modulation of nucleotide excision repair capacity by XPD polymorphisms in lung cancer patients». Cancer Res. 61 (4): 1354–7. PMID 11245433