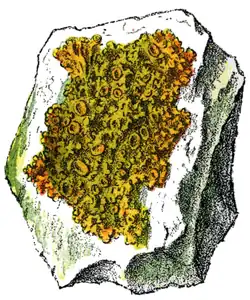
Xanthoria parietina
Xanthoria parietina
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
_-_Flickr_-_hedera.baltica.jpg) Talos amarelo-alaranjados de Xanthoria parietina crescendo em casca de árvore, cercados por Physcia adscendens (acinzentado) e algas Trentepohlia | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Xanthoria parietina (L.) Th.Fr (1860) | |||||||||||||||||
| Sinónimos[1][2] | |||||||||||||||||
Lista
| |||||||||||||||||
Xanthoria parietina é um líquen comum e amplamente distribuído, pertencente à família Teloschistaceae. É um líquen folioso reconhecido por sua coloração vibrante, que varia de amarelo a laranja, e por sua notável adaptabilidade ambiental. Descrito pela primeira vez por Carl Linnaeus em 1753, é um dos líquens mais estudados, contribuindo significativamente para o entendimento científico da biologia dos líquens. Diferentemente de muitos líquens sensíveis à poluição, X. parietina prospera em diversos habitats, incluindo rochas costeiras, muros urbanos e cascas de árvores, mesmo em áreas com altos níveis de poluição atmosférica e excesso de nitrogênio. Sua estrutura é composta por pequenos lóbulos sobrepostos, geralmente com menos de 8 cm de diâmetro, com coloração que varia de laranja brilhante em locais expostos ao sol a amarelo-esverdeado em ambientes sombreados.
O líquen representa uma parceria simbiótica com algas verdes do gênero Trebouxia [en]. Sua cor laranja-amarelada característica é devida à parietina, um pigmento do tipo antraquinona que se acumula na camada cortical externa, funcionando como um protetor solar natural, protegendo o parceiro algal de luz excessiva e radiação ultravioleta. Diferentemente de muitos líquens que se reproduzem por estruturas vegetativas especializadas, X. parietina depende principalmente da reprodução sexual por meio de ascomas em forma de taça (apotécios), que podem liberar até 50 esporos por minuto em condições úmidas. Quando os esporos fúngicos germinam, inicialmente formam associações preliminares com algas livres no ambiente. Além disso, o fungo pode recrutar células algais compatíveis de talos liquênicos vizinhos, extraindo esses parceiros para estabelecer uma relação simbiótica completa.
Nativo da Europa, partes da Ásia e da costa norte-africana, X. parietina tem uma distribuição mais limitada e predominantemente costeira na América do Norte e na Austrália, onde evidências genéticas sugerem uma introdução mediada por humanos. Nas últimas décadas, expandiu-se para o interior dessas regiões, especialmente em ambientes urbanos e áreas afetadas por poluição agrícola, aplicação de sal nas estradas (como agente antiderrapante no inverno) e deposição de nitrogênio. O líquen cresce lentamente, com uma média de 2,6 mm por ano, mas possui uma notável capacidade regenerativa, com fragmentos capazes de se desenvolverem em novos talos. Participa de uma complexa rede de interações ecológicas, hospedando pelo menos 41 espécies de fungos liquenícolas, enquanto certos gastrópodes e rotíferos microscópicos contribuem para sua dispersão biológica ao consumir e excretar esporos viáveis.
A espécie apresenta alta diversidade genética, mesmo em populações locais, com padrões distintos associados à localização geográfica e ao tipo de substrato. Essa variabilidade genética, combinada com associações flexíveis com diferentes linhagens de fotobiontes, contribui para seu sucesso ecológico. X. parietina é utilizada como bioindicador para monitoramento da qualidade do ar devido à sua capacidade de acumular contaminantes ambientais. Historicamente, foi empregada na medicina tradicioinal para tratar icterícia e como fonte de corante natural para tecidos. Mais recentemente, tornou-se objeto de pesquisa em astrobiologia, sobrevivendo a ambientes semelhantes aos de Marte, vácuo espacial, radiação cósmica e frio extremo. Essa resiliência estabeleceu X. parietina como um organismo-modelo em monitoramento ambiental e pesquisas de exploração espacial.
Sistemática
Taxonomia histórica
A história taxonômica de Xanthoria parietina começa em 1753 com Carl Linnaeus, que a descreveu como Lichen parietinus em sua obra seminal Species Plantarum.[3] Em sua breve diagnose, Linnaeus caracterizou-a como um líquen folioso com lóbulos amarelados e curvados, citando a ilustração anterior de Dillenius e notando sua ampla distribuição europeia em paredes, rochas e madeira.[4] Os espécimes originais de Linnaeus de Lichen parietinus estão preservados no Herbário Linneano, ambos rotulados com o número 25 de Species Plantarum. Esses espécimes causaram confusão taxonômica, pois um corresponde a Rusavskia elegans [en] (anteriormente Xanthoria elegans), enquanto o outro apresenta características semelhantes a Xanthoria ectaneoides. Um espécime separado de sua coleção Flora Suecica foi posteriormente reatribuído a X. parietina. Devido a essas inconsistências, taxonomistas designaram a ilustração citada por Linnaeus de Dillenius (1742) como lectótipo, com um espécime correspondente no Herbário de Oxford designado como epítipo.[3]
Os primeiros liquenologistas reclassificaram a espécie em diferentes gêneros. Por exemplo, Erik Acharius (1803) referiu-se a ela como Parmelia parietina em sua obra Methodus.[5] Giuseppe De Notaris (1847) listou-a como Physcia parietina. Johannes M. Norman (1852) tratou-a no gênero Teloschistes (um gênero relacionado de líquens alaranjados), chamando-a de Teloschistes parietinus.[6]
O gênero moderno Xanthoria foi estabelecido por Theodor Fries. Em 1860, ele recombinou formalmente a espécie como Xanthoria parietina. Em seu tratamento, Fries reconheceu uma forma distinta, que chamou de Xanthoria aureola, distinguindo-a da forma mais comum de X. parietina. Ele descreveu aureola como uma forma primária e fundamental da espécie, particularmente prevalente em regiões árticas, diferindo do típico X. parietina pela cor, talo rígido e preferência por habitats expostos. Fries também citou Acharius, que considerava aureola um intermediário entre Xanthoria elegans (agora Rusavskia elegans) e X. parietina.[7] Essas distinções podem ter contribuído para interpretações taxonômicas posteriores que reconheceram Xanthoria aureola como uma espécie distinta.
Xanthoria parietina é a espécie-tipo do gênero Xanthoria. O lectótipo designado para Xanthoria parietina é a ilustração citada por Linnaeus de Dillenius (1742).[3] Devido à sua reclassificação em diferentes gêneros, Xanthoria parietina acumulou muitos sinônimos na literatura. Além das transferências genéricas, várias táxons infraspecíficos (formas, variedades ou subespécies) foram descritas, particularmente em relação a variantes morfológicas. O nome Xanthoria parietina var. ectanea, originalmente descrito por Erik Acharius em 1810,[8] tem uma história longa e variada, aparecendo em múltiplas combinações dentro de Parmelia, Physcia, Teloschistes e Xanthoria, antes de ser reconhecido em diferentes categorias como variedade, forma ou subespécie.[2] Outra variação, Xanthoria parietina var. convexa, foi descrita por Veli Räsänen em 1944,[9] embora sua significância taxonômica tenha sido menos amplamente reconhecida.[2]
Os taxonomistas agora reconhecem várias táxons, outrora classificadas como variantes infraspecíficas de Xanthoria parietina, como espécies distintas:
- f. antarctica (Vain.) Hue (1915) é agora Polycauliona antarctica[10]
- f. ectaneoides (Nyl.) Boistel (1903) é agora Xanthoria ectaneoides[11]
- f. ectaniza Boistel (1903) é agora Rusavskia ectaniza[12]
- f. polycarpa (Hoffm.) Arnold (1881) é agora Polycauliona polycarpa[13]
- subsp. calcicola (Oxner) Clauzade & Cl.Roux (1985) é agora Xanthoria calcicola [en][14]
- subsp. phlogina (Ach.) Sandst. (1912) é agora Scythioria phlogina[15]
- var. aureola (Ach.) Th.Fr. (1860) é agora Xanthoria aureola [en][16]
- var. australis Zahlbr. (1917) é agora Jackelixia australis[17]
- var. contortuplicata (Ach.) H.Olivier (1894) é agora Xanthaptychia contortuplicata[18]
- var. incavata (Stirt.) Js. Murray (1960) é agora Dufourea incavata[19]
- var. lobulata (Flörke) Rabenh. (1870) é agora Seawardiella lobulata[20]
- var. mandschurica Zahlbr. (1931) é agora Zeroviella mandschurica[21]
- var. rutilans (Ach.) Maheu & A.Gillet (1924) é agora Xanthoria rutilans[22]
|
Xanthoria coomae, descrita em Nova Gales do Sul em 2007,[23] e Xanthoria polessica, descrita em Belarus em 2013,[24] foram posteriormente avaliadas como sinônimos de Xanthoria parietina.[1]
Relações filogenéticas e estudos moleculares
A taxonomia moderna coloca X. parietina na família Teloschistaceae [en], ordem Teloschistales, dentro da classe Lecanoromycetes (Ascomycota liquenizados).[25] Está intimamente relacionada a outros líquens alaranjados, como os dos gêneros Caloplaca, Teloschistes e outros membros do clado Xanthorioide da Teloschistaceae. Estudos moleculares ajudaram a esclarecer suas relações filogenéticas. Por exemplo, análises de sequências de DNA forneceram evidências de que X. parietina é geneticamente distinta de Xanthoria aureola, outro líquen costeiro amarelo que por vezes foi considerado apenas uma variedade ou forma de X. parietina. O estudo confirmou que X. aureola é uma espécie distinta, não coespecífica com X. parietina.[26]
Estudos microscópicos estabeleceram Xanthoria parietina como a espécie protótipo para o asco do tipo "Teloschistes", uma categoria estrutural caracterizada por uma camada externa apicamente espessada, fortemente amiloide, e um ápice em forma de domo que se divide longitudinalmente durante a liberação de esporos. Esse tipo de asco, originalmente descrito em membros de Xanthoria, Teloschistes e gêneros relacionados, difere do tipo Lecanora por não possuir um mecanismo de descarga especializado, dependendo de uma ruptura simples para a liberação de esporos. Investigações iniciais de microscopia eletrônica de X. parietina ajudaram a esclarecer a natureza funcional desse asco e sua distinção de outros tipos de asco encontrados em fungos liquenizados.[27]
Nomenclatura
A etimologia do nome atual está enraizada em sua aparência e habitat. Xanthoria deriva do grego xănthós, que significa "amarelo", com o sufixo genérico oria ("relativo a"), aludindo à cor laranja-amarelada brilhante do líquen.[28] O epíteto específico parietina vem do latim parietina ("de paredes"), referindo-se à sua ocorrência frequente em muros. Assim, o nome Xanthoria parietina significa essencialmente "líquen amarelo de paredes", uma descrição apropriada para este líquen laranja comum.[29]
Descrição

O corpo vegetativo do líquen, o talo, é folioso e geralmente tem menos de 8 cm de largura. Os lóbulos do talo têm 1–4 mm de diâmetro (raramente até 7 mm) e são achatados.[30] Em populações africanas, os lóbulos tendem a ser menores que os de áreas temperadas, geralmente com 0,5–2,0 mm de largura.[31] A superfície superior varia entre tons de amarelo, laranja ou amarelo-esverdeado, tornando-se quase verde em situações sombreadas. A superfície inferior é branca, possui um córtex e raras rizinas ou hapterons pálidos que ajudam a fixar o talo ao substrato. As estruturas reprodutivas vegetativas, sorédios e isídios [en], estão ausentes nesta espécie.[30] X. parietina reproduz-se principalmente por reprodução sexual por meio de apotécios. Os apotécios geralmente se desenvolvem a 2–4 mm da borda de crescimento do talo e levam de 12 a 18 meses para atingir a maturidade. Os apotécios maduros medem entre 1,5 e 2,6 mm de diâmetro, embora em casos raros possam chegar a 4,3 mm. Podem compor de 0 a 87% do peso seco do talo, com a maioria dos talos dedicando 10–30% de sua biomassa a essas estruturas reprodutivas. Os apotécios podem liberar esporos a uma taxa de até 50 por minuto em condições úmidas. A produção de apotécios parece ser independente da orientação do talo (norte, sul, leste ou oeste), o que significa que a exposição à luz solar não influencia significativamente o esforço reprodutivo.[32]
A "pele" externa do líquen, o córtex, é composta por hifas fúngicas densamente compactadas e serve para proteger o talo da perda de água por evaporação e dos efeitos nocivos de altos níveis de irradiação. Em X. parietina, a espessura dos talos varia dependendo do habitat em que cresce. Os talos são muito mais finos em locais sombreados do que em locais expostos ao sol, o que protege as algas que não toleram altas intensidades de luz.[33]
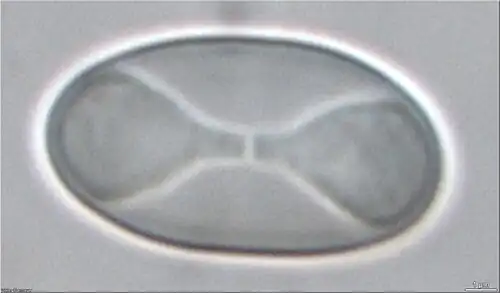
Os esporos produzidos por X. parietina são hialinos (incolores e translúcidos), elipsoides e geralmente medem 13–16 por 7–9 μm. Como todos os líquens da família Teloschistaceae, são polariloculares, ou seja, divididos em dois componentes (lóculos) separados por um septo central com uma perfuração. Esse septo varia de 3 a 8 μm de largura.[34]
| Características microscópicas de Xanthoria parietina: (Apotécio único) Apotécio maduro mostrando o disco (superfície superior do himênio) laranja-amarelado cercado por uma margem talina; (Apotécio seccionado) Corte transversal de um apotécio revelando o himênio laranja-amarelado, células de algas verdes na margem e tecido fúngico hialino de suporte; (Ilustração) Seção vertical de um apotécio mostrando paráfises (a), ascos com esporos polariloculares (b) e hipotécio (camada de tecido sob o himênio) (c); (Esporo) Visão em alta magnificação de um esporo polarilocular (escala: 1 μm) com seu característico septo central e perfuração, típico da família Teloschistaceae. |
Espécies semelhantes
Xanthoria parietina pode ser confundida com várias espécies relacionadas, particularmente X. aureola e X. calcicola. Evidências moleculares confirmam que essas são espécies distintas, embora compartilhem semelhanças morfológicas. X. aureola foi historicamente considerada sinônima de X. parietina, mas agora é reconhecida como uma espécie distinta. Comparada a X. parietina, X. aureola tem um talo mais espesso (média de 320 μm vs. 236 μm), lóbulos mais estreitos no ponto mais largo (média de 2,3 mm vs. 2,9 mm) e uma superfície superior áspera com cristais visíveis, em vez de lisa. As partes centrais de X. aureola são cobertas por lobos sobrepostos, crenulados a em forma de tira. Geralmente produz menos apotécios e apresenta uma preferência ecológica por rochas costeiras, enquanto X. parietina ocorre em vários substratos.[35]
Xanthoria calcicola difere de X. parietina por sua superfície superior áspera com cristais, partes centrais cobertas por isídios grossos ou projeções semelhantes a papilas, e cor laranja-amarelada opaca em comparação com o amarelo brilhante de X. parietina. Geralmente apresenta apotécios esparsos quando presentes (versus abundantes em X. parietina), margens talinas de apotécios que variam de lisas a ásperas ou crenuladas, uma quimossíndrome distinta (um conjunto de metabólitos secundários relacionados) e preferência por substratos calcários, como muros de pedra, raramente crescendo em casca de árvore. Análises moleculares mostram que X. calcicola e X. aureola são mais próximas entre si do que de X. parietina, embora permaneçam espécies geneticamente distintas com características morfológicas e preferências ecológicas diferentes. A presença de cristais na superfície superior é uma característica-chave que distingue tanto X. aureola quanto X. calcicola de X. parietina, que tem uma superfície superior lisa.[35]
Outra espécie semelhante, Rusavskia elegans, possui lóbulos convexos menores, medindo até 1,3 mm de largura.[34]
Fotobionte
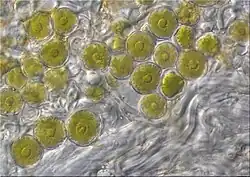
Os parceiros fotossintéticos, ou fotobiontes, de X. parietina pertencem ao gênero de algas verdes Trebouxia, incluindo Trebouxia arboricola e T. irregularis. Essas algas também existem independentemente na natureza, ocorrendo em cascas colonizadas e não colonizadas por líquens.[36] Um estudo constatou que o fotobionte ocupa 7% do volume do talo em X. parietina.[37] A densidade de pigmentação no córtex superior varia, regulando a exposição à luz das algas. O fotobionte Trebouxia ajusta sua atividade fotossintética sazonalmente, suportando X. parietina em ambientes ensolarados. À medida que a luz solar aumenta na primavera, o fotobionte reduz os níveis de clorofila e produz pigmentos protetores para dissipar o excesso de luz como calor. As concentrações de clorofila são mais baixas na primavera e atingem o pico no inverno, equilibrando a absorção de luz e a fotoproteção ao longo do ano.[38]
X. parietina associa-se a diversos fotobiontes. Geralmente se associa a Trebouxia decolorans quando cresce em casca e a T. arboricola em rocha. Mesmo em populações locais, fotobiontes geneticamente distintos frequentemente coexistem em talos adjacentes. Um estudo identificou 36 genótipos algais em 38 amostras epífitas de um único local. Apesar de T. decolorans ser considerada de reprodução assexuada, várias linhagens algais por vezes ocorrem dentro de um único talo, sugerindo troca de fotobiontes ou fusão de talos. Essa diversidade pode contribuir para a adaptabilidade de X. parietina em ambientes variados.[39]
Embora algas livres sejam abundantes, X. parietina associa-se seletivamente com espécies de Trebouxia. Proteínas fúngicas, incluindo proteínas de ligação algal, podem mediar essa seleção ao reconhecer fotobiontes compatíveis. Essas proteínas interagem especificamente com as paredes celulares de Trebouxia, sugerindo um mecanismo bioquímico para reconhecimento de parceiros.[40] Bubrick e Galun (1980) identificaram uma proteína em X. parietina que se liga seletivamente às paredes celulares de seu fotobionte cultivado, com força de ligação correlacionada aos níveis de polissacarídeos ácidos. Essa interação pode ser crucial durante a resíntese do líquen, pois X. parietina se propaga por esporos fúngicos e deve recrutar novos fotobiontes do ambiente.[41]
Imagens de células vivas revelaram uma rede mitocondrial dinâmica (condrioma) em Trebouxia recém-isolada de X. parietina.[42] As descobertas sugerem que as mitocôndrias podem ser moldadas pelo estado liquenizado e contribuir para a troca de energia com o parceiro fúngico. Elas também parecem desempenhar um papel nas respostas ao estresse, como a tolerância à dessecação, geralmente estudada em relação ao cloroplasto. Essas descobertas podem ajudar a esclarecer as interações fisiológicas na simbiose liquênica.
Química
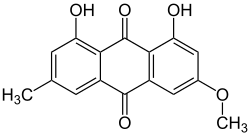
Como muitos líquens, Xanthoria parietina produz diversos metabólitos secundários (substâncias liquênicas), principalmente pigmentos antraquinônicos que conferem sua cor vibrante. O composto dominante, a parietina, é uma antraquinona laranja-amarelada que se acumula no córtex externo.[43] A parietina representa cerca de 2,1% do peso seco do talo e forma uma camada hidrofóbica no córtex superior, acima da camada algal.[44] Ela é depositada como pequenos cristais no córtex superior, onde protege o fotobionte. A síntese de parietina é estimulada pela radiação UV-B[43] e por fotossintatos do simbionte Trebouxia.[45] Além de proteger contra a radiação UV, a parietina atua como uma barreira contra toxinas ambientais, especialmente metais pesados.[44]
A parietina não apenas confere a X. parietina sua cor laranja brilhante, mas também a protege da luz visível (400–500 nm). A remoção experimental da parietina levou a um aumento da fotoinibição, especialmente em talos hidratados, confirmando sua função protetora. No entanto, quando dessecados, X. parietina permaneceu fototolerante, sugerindo que adaptações estruturais também contribuem para sua resistência à luz.[46] Além de seu papel na fotoproteção, a parietina aumenta a tolerância à dessecação, estabilizando membranas celulares e modificando o córtex superior para melhorar a retenção de água.[47]
A parietina é altamente eficaz na proteção contra UV, absorvendo a radiação UV-B com pico em 288 nm. Essa característica é particularmente benéfica em habitats intensos em UV, como falésias costeiras e regiões alpinas. Experimentos confirmam que a luz UV-B é necessária para a síntese de parietina — em condições controladas, talos expostos apenas à radiação fotossinteticamente ativa regeneraram 12% de sua parietina, enquanto aqueles expostos a UV-B restauraram 35%.[48] Apesar dos níveis mais baixos de UV-B em ambientes árticos, X. parietina mantém altas concentrações de parietina, sugerindo que outros fatores ambientais regulam sua produção.[48] Estudos de campo sazonais mostram que os níveis de parietina em Xanthoria parietina seguem um ciclo anual. Em populações naturais, as concentrações foram mais baixas no inverno e quase dobraram no solstício de verão. Esse padrão reflete as mudanças sazonais na radiação UV-B, sugerindo que a síntese de parietina é rapidamente aumentada na primavera para proteger o fotobionte do excesso de luz e diminui mais gradualmente no outono, à medida que a irradiação diminui.[49]
Além da parietina, X. parietina produz várias antraquinonas relacionadas, incluindo falacinol, falacinal, emodina e ácido parietínico. Falacinol e falacinal são antraquinonas menores, enquanto a emodina é outro pigmento laranja encontrado em alguns líquens. Esses compostos contribuem para o perfil químico de X. parietina e foram investigados em estudos fitoquímicos. Pesquisas recentes (2023) exploraram X. parietina como uma fonte natural de antraquinonas para a síntese de derivados farmacêuticos, como antraquinonas O-metiladas e aciladas.[50] X. parietina também produz o metabólito secundário 2-metoxi-4,5,7-trihidroxi-antraquinona,[51] além de tocoferol e ergosterol.[52]
Além das antraquinonas, X. parietina contém pigmentos adicionais, incluindo carotenoides como mutatoxantina, que contribuem para suas capacidades fotoprotetoras. O conteúdo total de carotenoides em X. parietina pode atingir até 94,7 mg/g de peso seco, significativamente maior do que em algumas espécies relacionadas, indicando um forte investimento em mecanismos de proteção contra luz. Além disso, a síntese de antraquinonas em X. parietina está ligada à sua relação simbiótica com algas Trebouxia — o ribitol, um carboidrato fornecido pelo fotobionte, demonstrou aumentar significativamente a produção de parietina quando fornecido em cultura.[48]

Na liquenologia, testes químicos simples in situ são usados para detectar certos compostos e X. parietina apresenta resultados claros devido aos seus pigmentos antraquinônicos. Um teste padrão é o teste K (usando solução de hidróxido de potássio). Em X. parietina, a aplicação de KOH no córtex produz uma reação púrpura intensa (K+ púrpura). Isso é uma indicação clássica de antraquinonas como a parietina — o KOH faz com que a parietina forme um sal púrpura (uma mudança de cor distinta). Outros resultados de testes químicos para este líquen são negativos: C–, KC– e P–.
Além de seus pigmentos antraquinônicos, Xanthoria parietina contém pequenas quantidades de oxalato de cálcio, um metabólito secundário comum em muitos líquens, particularmente aqueles que crescem em substratos calcários. No entanto, ao contrário de espécies estritamente calcícolas, como Caloplaca heppiana e Lecanora calcarea, que acumulam grandes quantidades de oxalato de cálcio, X. parietina apresenta apenas traços menores desse composto. Isso sugere que, embora X. parietina tolere habitats calcários, não depende da produção extensiva de oxalato para regulação de cálcio ou modificação do substrato na mesma medida que calcícolas obrigatórias.[53]
Adaptações fisiológicas
Xanthoria parietina regula o balanço hídrico enquanto mantém a troca gasosa, permitindo-lhe tolerar condições de umidade variáveis. Essa adaptação deve-se em grande parte à proteína hidrofobina de classe I XPH1, que se auto-organiza em uma camada de bastonetes hidrofóbicos nas hifas fúngicas nas camadas medular e algal do talo.[54] A camada de hidrofobina previne o encharcamento, preservando espaços aéreos essenciais para a difusão de CO2 e O2. Diferentemente do córtex externo hidrofílico, que absorve água, as hifas fúngicas são revestidas por uma barreira hidrofóbica, garantindo troca gasosa contínua mesmo em chuva ou alta umidade. Essa característica é especialmente benéfica em ambientes costeiros e ripários, onde a umidade frequente poderia interromper o metabolismo.[54][55]
A estrutura do talo de Xanthoria parietina consiste em aproximadamente 7% de células algais, 43% de tecido fúngico, 18% de espaços aéreos e 34% de matriz extracelular, que pode incluir glucano ou liquenano. Os espaços aéreos reduzem a resistência à difusão de CO2, melhorando a fotossíntese mesmo quando as paredes fúngicas estão saturadas de água.[37]
A proteína XPH1 forma um revestimento estável e insolúvel que aumenta a resiliência do líquen. Ela contém um domínio de fecho de leucina, provavelmente auxiliando na agregação em interfaces ar-água para prevenir a infiltração de líquidos. A microscopia eletrônica de fratura por congelamento revela que a camada de hidrofobina reveste as paredes celulares fúngicas e algais, formando uma barreira protetora entre os parceiros simbióticos e o ambiente.[55] Em X. parietina, o XPH1 é expresso continuamente, ao contrário de fungos não liquenizados, onde as hidrofobinas aparecem apenas em estágios específicos. Culturas de laboratório do micobionte cultivadas sem seu fotobionte não produzem XPH1, indicando que sua síntese depende da simbiose.[54][55]
A camada de hidrofobina também aumenta a resistência à dessecação, repelindo o excesso de umidade e evitando saturação prolongada, permitindo que o líquen se recupere rapidamente da desidratação. Isso é especialmente crítico em habitats expostos com ciclos frequentes de umedecimento e secagem.[54][55] A camada de hidrofobina pode ajudar na tolerância à poluição atmosférica, particularmente à resistência a metais pesados, criando uma barreira protetora que reduz a exposição fúngica a partículas tóxicas. Isso pode explicar por que X. parietina prospera em ambientes urbanos e industriais onde outros líquens têm dificuldade.[54]
Reprodução e dispersão

Muitos líquens se dispersam por propágulos vegetativos simbióticos, como sorédios, isídios ou blastídios, mas X. parietina não possui essas estruturas e deve restabelecer seu estado simbiótico a cada ciclo reprodutivo. Em vez disso, ácaros oribatídeos — Trhypochtonius tectorum e Trichoribates trimaculatus — servem como vetores, consumindo X. parietina e dispersando seus esporos viáveis e células do fotobionte por meio de suas fezes. Isso facilita a dispersão de curta e longa distância.[56]
Apesar da falta de propágulos vegetativos especializados, X. parietina demonstra estratégias reprodutivas sofisticadas que superam os desafios da reprodução sexual em líquens. Quando esporos fúngicos germinantes se espalham pelo substrato, eles primeiro formam associações com algas não simbióticas comuns (como Pleurococcus), criando um estágio preliminar de "proto-líquen". Essa rede ampla aumenta a probabilidade de encontrar o fotobionte Trebouxia necessário para o desenvolvimento adequado do talo. Além disso, o micobionte pode extrair parceiros algais adequados dos sorédios de outros líquens, particularmente espécies de Physcia que frequentemente crescem ao lado de X. parietina e contêm fotobiontes compatíveis.[57]
Uma vez estabelecido o contato com células compatíveis de Trebouxia, o micobionte forma estruturas especializadas chamadas complexos haustoriais que permitem uma troca eficiente de nutrientes. Esses haustórios intraparietais, que penetram parcialmente na parede celular algal, mas não na membrana celular, permitem o deslocamento de curto alcance de células do fotobionte e criam caminhos para a translocação de carboidratos das algas fotossintéticas para o fungo. Diferentemente de muitos outros líquens, X. parietina pode formar vários haustórios por célula algal, com cada haustório desenvolvido por uma única hifa ou várias hifas fúngicas trabalhando juntas, aumentando a eficiência da relação simbiótica.[58]
Xanthoria parietina segue um ciclo de vida de quatro estágios com 13 estados de desenvolvimento. Após a germinação do esporo, o crescimento progride por prototalo (apenas hifas fúngicas), proterotalo (associação algal inicial) e estágios juvenis, eventualmente formando um talo folioso. Em talos jovens, as apotécios cobrem cerca de metade da margem do talo, mas em talos maduros, ocupam apenas cerca de 1/16 da margem. Essa diminuição indica que, à medida que o líquen amadurece, a área relativa dedicada às estruturas reprodutivas diminui em comparação com o tamanho total do talo. As condições ambientais influenciam fortemente o desenvolvimento — talos em áreas poluídas ou urbanas frequentemente não completam seu ciclo de vida, enquanto aqueles em habitats limpos atingem a maturidade total.[59]
O sucesso reprodutivo varia conforme o substrato — talos em choupos produzem mais apotécios e esporos do que aqueles em outras espécies. Além disso, o micobionte pode se associar a algas não nativas (por exemplo, Pleurococcus) antes de estabelecer seu simbionte típico Trebouxia ou Pseudotrebouxia, permitindo a colonização em diferentes substratos.[59]
Xanthoria parietina cresce a uma taxa média de cerca de 2,6 mm por ano, embora o crescimento varie com o habitat. Ambientes submontanos úmidos suportam crescimento mais rápido (6–7 mm/ano), enquanto regiões costeiras mais secas retardam a expansão. O crescimento atinge o pico em estações frias e úmidas (outono/inverno) e diminui em condições quentes e secas, como em climas mediterrâneos. O crescimento lento de X. parietina influencia sua longevidade e dispersão. Sem absorção ativa de água, a alta demanda evaporativa limita o metabolismo, especialmente em regiões expostas ao vento e de baixa altitude, onde a dessecação retarda a expansão do talo e reduz o sucesso dos propágulos. Em contraste, a alta umidade suporta um crescimento radial constante, permitindo persistência a longo prazo, acumulação de biomassa e liberação contínua de esporos. Ventos fortes tanto prejudicam quanto auxiliam X. parietina. Embora a exposição ao vento desidrate os talos e retarde o crescimento, também dispersa fragmentos de talo, que servem como propágulos vegetativos na ausência de estruturas especializadas, complementando a dispersão baseada em esporos.[60]
Xanthoria parietina libera e germina esporos durante todo o ano, embora a germinação seja mais rápida no verão (4–5 dias) e mais lenta no inverno. A germinação ideal ocorre em pH 6, mas os esporos toleram pH de 3 a 7. O sucesso da germinação e o desenvolvimento do micobionte são influenciados por múltiplos fatores ambientais. O substrato afeta o sucesso — a germinação é maior em ágar do que em lâmina de água.[61] Em laboratório, os esporos de X. parietina germinam melhor em meios de cultura líquidos, particularmente malte-extrato de levedura, que fornece carboidratos, aminoácidos e vitaminas essenciais. Temperaturas mais altas aceleram a germinação, com 23°C promovendo a formação de colônias mais rapidamente do que 19°C. A exposição à luz é desnecessária para o crescimento fúngico inicial — culturas no escuro desenvolvem redes miceliais mais saudáveis e extensas.[62]
A morfologia do micobionte em desenvolvimento fornece percepções sobre a simbiose inicial. In vitro, X. parietina forma hifas septadas e ramificadas, que posteriormente desenvolvem estruturas lobadas, assemelhando-se a talos liquênicos iniciais. A microscopia eletrônica de varredura revela uma rede de hifas densa e entrelaçada, potencialmente facilitando interações com o fotobionte durante a liquenização natural. Essas adaptações suportam a capacidade regenerativa de X. parietina e o estabelecimento simbiótico em ambientes variados.[62]
Embora X. parietina não possua propágulos vegetativos especializados, tem uma capacidade regenerativa que aumenta seu sucesso ecológico. Talos mais velhos, cobertos por apotécios, se desprendem ao longo de rachaduras induzidas pela seca, enquanto as margens mais jovens permanecem fixas. Quando fragmentos pousam em substratos adequados, regeneram novos lóbulos ao longo das margens de feridas, atuando como propágulos naturais. Estudos de campo mostram um aumento de 150% no tamanho laminar em apenas 13 meses em talos em regeneração. Em um experimento de cinco anos, X. parietina manteve 50% de cobertura do substrato, apesar de perder 90% de sua área inicial de talo, pois o crescimento compensou essas perdas. A renovação total (crescimento + perda) excedeu 170%, destacando seu ciclo de vida dinâmico.[63]
A regeneração é impulsionada por células fúngicas e algais em divisão ativa dentro de áreas maduras do talo, permitindo novo crescimento a partir de praticamente qualquer parte do líquen, incluindo margens de discos apoteciais. Essa adaptação é particularmente evidente em X. parietina e algumas espécies de Teloschistales, proporcionando uma vantagem ecológica significativa sobre líquens que não possuem propágulos vegetativos nem alta capacidade regenerativa.[63] Essa dispersão baseada em fragmentação contribui para a resiliência e ampla distribuição da espécie.[64]
Habitat e distribuição
Xanthoria parietina é uma espécie cosmopolita, relatada na Austrália, África, Ásia, América do Norte e em grande parte da Europa.[65] No leste da América do Norte e na Europa, é mais frequentemente encontrada em locais costeiros, e no sul de Ontário, Canadá, seu reaparecimento foi atribuído ao aumento da deposição de nitrato associada a desenvolvimentos industriais e agrícolas.[66]
A espécie mostra uma forte preferência por habitats costeiros, onde se beneficia da deposição de aerossóis marinhos. Em Maine, EUA, X. parietina é abundante em lápides próximas ao oceano, mas diminui drasticamente no interior. Torna-se rara além de 40 km da costa no sudoeste de Maine e 130 km no interior do leste de Maine. Esse padrão de distribuição no interior é amplamente influenciado pela deposição de nutrientes derivados do mar, particularmente cloreto e sódio, transportados para o interior pelo vento e precipitação.[67]
Na América do Norte, a espécie era historicamente limitada principalmente a regiões costeiras — ao longo da costa atlântica de Terra Nova e Labrador a Pensilvânia, na costa do Pacífico da Califórnia ao Noroeste do Pacífico, e em uma pequena parte da costa do Golfo no Texas. No Noroeste do Pacífico, sua faixa tradicional foi descrita como a oeste das Cascatas, do Vale do Willamette à região de Puget Sound. Desde o início dos anos 2000, no entanto, a espécie foi documentada em várias cidades do interior em Idaho, Washington e partes do oeste de Montana. Essas ocorrências no interior estão predominantemente associadas a ambientes urbanos, particularmente em arboretos e parques em árvores ornamentais plantadas, sugerindo dispersão mediada por humanos.[68] Essas expansões de alcance documentadas identificaram X. parietina como uma das poucas espécies de líquens que se tornaram comprovadamente invasivas em novos territórios, principalmente por meio de vias de introdução hortícola.[29] Pesquisas indicam que X. parietina está sendo transportada para o interior em mudas de viveiros de regiões costeiras, conforme evidenciado por sua presença em plantas de viveiros comerciais e ausência em plantas lenhosas naturais em áreas não perturbadas fora dessas cidades.[68]
A direção do vento desempenha um papel crítico na definição da extensão para o interior de X. parietina. Ventos de sudoeste nos meses mais quentes carregam aerossóis marinhos mais para o interior, enquanto tempestades do leste contribuem com deposição adicional de sal marinho por meio da precipitação. A influência desses aerossóis é evidente em cemitérios de Maine: X. parietina é mais frequente em cemitérios abertos expostos aos ventos predominantes, em comparação com cemitérios arborizados, que bloqueiam ou capturam sais marinhos transportados pelo ar, e têm frequências significativamente menores do líquen.[67]
.jpg)
Nas últimas décadas, populações no interior de X. parietina foram descobertas no sul de Ontário, sugerindo uma expansão além de sua faixa tradicionalmente costeira. Antes considerada extinta na região, a espécie foi redescoberta crescendo em árvores em vários locais no interior. Essa ocorrência no interior levanta questões sobre se o líquen se restabeleceu após uma longa ausência ou persistiu indetectado por décadas. A expansão pode estar ligada ao aumento da deposição de nitrogênio por escoamento agrícola e poluição do ar, que criam condições favoráveis para líquens nitrófilos como X. parietina. Outro fator possível em sua disseminação no interior é o uso generalizado de sal nas estradas, para evitar derrapagens, em Ontário nos últimos 50–70 anos. Como X. parietina prospera em ambientes costeiros ricos em sal, a deposição de sal nas estradas pode ter fornecido um habitat artificial, imitando as condições químicas das regiões marítimas. O líquen é frequentemente encontrado perto de rodovias e em árvores crescendo ao longo de valas de drenagem que recebem escoamento de campos fertilizados, apoiando ainda mais o papel do enriquecimento antropogênico de nutrientes em seu estabelecimento no interior.[66]
O líquen cresce em uma variedade de substratos e em diversos habitats. É encontrado em florestas de madeira de lei em vales amplos de baixa elevação e ocorre esporadicamente em Populus e outras madeiras duras em zonas ripárias de áreas agrícolas e povoadas.[30] Coloniza preferencialmente as partes superiores dos troncos (cerca de 70% da altura total da árvore), onde a casca é mais jovem e mais exposta à luz solar.[69] Também é abundante em construções rurais e em rochas imediatamente acima da marca de água alta em zonas costeiras, e em praias rochosas forma tipicamente uma faixa distinta na zona supralitorânea entre espécies mais halófilas abaixo e espécies terrestres acima.[70] O enriquecimento de nutrientes por fezes de aves aumenta a capacidade de X. parietina de crescer em rocha.[71] A espécie demonstra versatilidade de substrato e até foi registrada crescendo sobre chumbo em lápides incisas com chumbo na Inglaterra.[72]
A espécie demonstra resiliência ecológica por meio de sua capacidade regenerativa. Diferentemente de muitos líquens foliosos que mostram controle posicional estrito de crescimento limitado às margens do talo, X. parietina pode iniciar novo crescimento a partir de praticamente qualquer porção danificada de seu talo. Essa capacidade de se recuperar de danos físicos ou fragmentação permite que persista em habitats perturbados onde outros líquens podem não conseguir se restabelecer.[64]
Registros adicionais indicam que formas morfológicas distintas ocorrem em habitats antropogênicos. Uma forma granulosa (anteriormente conhecida como Xanthoria aureola) foi registrada predominantemente em telhados no sudeste da Inglaterra.[73]
Ecologia
Xanthoria parietina demonstra uma gama de adaptações fisiológicas e morfológicas que facilitam sua sobrevivência em diversos habitats. Populações em habitats mais secos e expostos produzem hidrocarbonetos de cadeia mais longa (alcanos), enquanto aquelas em regiões mais úmidas e frias sintetizam alcanos de cadeia mais curta — uma resposta que ajuda a reduzir a perda de água, semelhante às adaptações vistas em plantas vasculares.[74] Sua morfologia do talo é plástica; formas em leitos de riachos úmidos tendem a ser semi-eretas e laranja-amareladas, enquanto aquelas em locais secos e expostos ao sol são mais compactas e laranja escuro. Essas diferenças parecem ser induzidas pelas condições ambientais, e não por diferenças genéticas.[75]

A sobrevivência do líquen está intimamente ligada à sua dependência da umidade atmosférica. Sem estruturas especializadas de absorção de água, como raízes ou estômatos, X. parietina absorve umidade ambiental para atividade metabólica. Quando a umidade diminui, o líquen entra em um estado dormente, suspendendo a fotossíntese até que a umidade retorne. Essa estratégia poiquilohídrica permite suportar períodos prolongados de seca, embora o crescimento e a reprodução sejam amplamente confinados a condições úmidas. Em climas mais úmidos, a hidratação contínua suporta o metabolismo contínuo e a expansão mais rápida do talo.[60] Fatores ambientais — temperatura do ar, vento e demanda evaporativa — influenciam sua fisiologia: temperaturas mais altas aceleram a perda de água, e ventos fortes e secos intensificam a dessecação, particularmente em regiões costeiras de baixa altitude; por outro lado, ventos moderados com umidade adequada podem melhorar a troca gasosa e aumentar temporariamente a eficiência fotossintética. Esse equilíbrio entre disponibilidade de umidade e movimento do ar é um determinante chave das taxas de crescimento do líquen em diferentes habitats.[60]
O talo de X. parietina progride por estágios ontogenéticos distintos que refletem suas adaptações ecológicas. Nas fases juvenil e imatura, o líquen estabelece sua forma foliosa e desenvolve uma estrutura homeomérica com uma crosta superior protetora. À medida que avança para estágios virginais, a forma característica de roseta se forma. Durante o período generativo, as apotécios se desenvolvem gradualmente, passando de uma distribuição central esparsa em talos jovens para um arranjo mais concentrado em regiões centrais e periféricas em espécimes de meia-idade; essas taxas de desenvolvimento variam com as condições ambientais, com formação ideal em habitats bem iluminados com níveis moderados de nutrientes.[59]
A competição ecológica influencia ainda mais a estrutura e morfologia da população. Em regiões onde várias espécies de líquens nitrófilos coexistem, X. parietina frequentemente forma uma relação codominante na colonização inicial, mas sua maior tolerância à poluição e ao enriquecimento de nutrientes pode eventualmente levar a uma maior dominância em habitats alterados. Essa dinâmica é refletida nas proporções variadas de estágios ontogenéticos, com distribuições etárias equilibradas em ambientes menos perturbados e representação desproporcional em ambientes estressados.[59] Em substratos rochosos, o líquen coloniza superfícies por meio de hifas emergindo de seu córtex inferior, em vez de rizinas; pode penetrar fissuras minerais — especialmente em rochas calcárias — e em substratos mais macios, como calcarenito, suas hifas podem se estender de 1 a 2 mm abaixo da superfície, promovendo a fragmentação mineral. Em rochas mais duras, como andesito, o líquen permanece majoritariamente ligado à superfície, contribuindo principalmente para a desagregação mecânica, em vez de intemperismo químico.[76]
Como uma espécie nitrófila, X. parietina prospera em ambientes ricos em nutrientes. A entrada moderada de nutrientes estimula o crescimento, embora níveis excessivos eventualmente reduzam as taxas de crescimento. Consequentemente, é frequentemente abundante em áreas afetadas por escoamento hídrico em áreas agrícolas, poleiros de aves e deposição de nitrogênio atmosférico,[77] onde o enriquecimento de nutrientes pode alterar as estruturas das comunidades liquênicas, reduzindo as espécies sensíveis a ácidos. O guano de aves, rico no composto ureia, geralmente exclui a maioria dos líquens desses habitats; no entanto, X. parietina alcança um dos maiores conteúdos de nitrogênio relatados, em parte devido à sua alta atividade de urease, que converte ureia em CO2 e NH4.[78]
Relações com nitrogênio
Xanthoria parietina é altamente adaptável a ambientes ricos em nitrogênio, com talos contendo entre 11 e 43 mg/g de nitrogênio (peso seco), uma faixa mais ampla do que a maioria dos outros líquens com algas verdes.[79] A espécie mantém o equilíbrio metabólico ao redirecionar a alocação de recursos entre seus parceiros fúngico e algal, destinando mais recursos ao fotobionte em condições de alto nitrogênio. Diferentemente de espécies sensíveis ao nitrogênio, X. parietina mantém padrões de crescimento consistentes, independentemente da concentração de nitrogênio, permitindo que prospere em áreas agrícolas e centros urbanos.[80] Essa adaptação a ambientes com alto nitrogênio explica sua associação frequente com eutrofização[81][82] e sua presença comum perto de fazendas e instalações de gado.[83]
Experimentos de transplante perto de uma fazenda de porcos na Dinamarca demonstraram ainda mais sua capacidade de acumulação de nitrogênio. Talos de líquen expostos a altos níveis de amoníaco aumentaram rapidamente seu conteúdo de nitrogênio, atingindo aproximadamente 2,1% em um mês, enquanto amostras posicionadas a 300 metros de distância mantiveram níveis mais baixos (cerca de 1,6%). Amostras in situ coletadas ao longo de um transecto exibiram uma forte correlação linear entre o conteúdo de nitrogênio do talo e o logaritmo das concentrações de amoníaco ambiental.[84] Pesquisas adicionais sugerem que a tolerância ao nitrogênio de X. parietina pode estar ligada a adaptações osmóticas, em vez de uma preferência direta por nitrogênio. É principalmente halotolerante e xerofítica, com valores osmóticos celulares significativamente mais altos do que os de espécies não nitrófitas. Isso permite que absorva água de soluções concentradas, incluindo depósitos de nitrato de amônio, explicando seu sucesso em áreas urbanas poluídas por nitrogênio e em climas mediterrâneos costeiros ou secos, onde os níveis de nitrogênio são baixos.[85]
Genética populacional



Estudos genéticos de Xanthoria parietina revelaram diferenciação significativa entre populações, com variação genética estruturada tanto pela distância geográfica quanto pelo tipo de substrato. Populações crescendo em casca de árvore mostram maior diversidade genética do que aquelas em superfícies rochosas, embora não haja evidências de fluxo gênico restrito entre populações no mesmo tipo de substrato, mesmo quando separadas por distâncias de até 25 km. Apesar dessas diferenças genéticas, não foi observada variação morfológica ou química correspondente.[65]
Em escalas espaciais finas, X. parietina exibe alta diversidade genética dentro de populações locais, com até 90% da variação genética ocorrendo dentro, e não entre, populações.[86] Estudos usando marcadores genéticos da região espaçadora intergênica e espaçador interno transcrito revelam diversidade significativa mesmo entre indivíduos próximos.[87] Pesquisas na ilha de Storfosna, Noruega, sugerem que a adaptação local de longo prazo a habitats de casca ou rocha levou a variantes genéticas específicas de habitat, moldando a estrutura populacional geral.[35]
Embora populações locais possam ter diversidade genética limitada, populações de diferentes regiões geográficas mostram diferenciação genética significativa. Por exemplo, populações antárticas de Rusavskia elegans (previamente conhecida como Xanthoria elegans) de locais a apenas 5–15 km de distância diferiram por um nucleotídeo. Em contraste, aquelas separadas por 660 km apresentaram uma divergência de 14,2% em suas sequências de DNA. Padrões semelhantes em outras espécies de Xanthoria sugerem que, apesar da variação limitada dentro de populações locais, a dispersão de longa distância e a deriva genética contribuem para a diferenciação regional e a adaptação ecológica.[88]
Em escalas espaciais mais amplas, as populações de X. parietina mostram um padrão de isolamento por distância — as diferenças genéticas aumentam com a separação geográfica.[89] Um estudo genético global usando DNA polimórfico amplificado aleatoriamente-PCR identificou apenas dois grandes clusters genéticos em todo o mundo: um no sudoeste da Europa (Península Ibérica, Ilhas Baleares e Ilhas Canárias) e outro abrangendo Europa, América do Norte, Austrália e Nova Zelândia. A alta similaridade entre amostras da Austrália/Nova Zelândia e da Europa indica que a espécie foi introduzida por humanos no Hemisfério Sul, possivelmente por transporte de videiras ou pedras de lastro de navios.[90] Uma introdução humana semelhante foi sugerida para o líquen no Vale Willamette povoado do oeste dos Estados Unidos,[30] e em Ontário, onde pode ter chegado em árvores de viveiro.[34]
A alta diversidade genética observada em X. parietina tem várias implicações práticas para sua ecologia e conservação. Essa diversidade provavelmente suporta a adaptabilidade da espécie a diferentes ambientes — de rochas costeiras a árvores urbanas e áreas poluídas. A alta variação genética dentro de populações locais fornece material para seleção natural, permitindo adaptação a condições mutáveis, incluindo níveis de poluição e mudanças climáticas. As diferentes estruturas genéticas entre os parceiros fúngico e algal sugerem que X. parietina obtém vantagens ecológicas ao se associar a parceiros algais localmente adaptados, melhorando sua capacidade de colonizar habitats diversos. Do ponto de vista da conservação, essa diversidade genética ajuda a prever como a espécie pode responder a mudanças ambientais e identifica grupos populacionais potencialmente importantes para a gestão da biodiversidade. A estrutura genética também revela padrões de disseminação assistida por humanos, conforme mostrado pela similaridade entre populações europeias e do Hemisfério Sul.[89]
Embora X. parietina seja homotálica (autofértil), estudos genéticos revelam que frequentemente cruza com outros indivíduos. Isso representa uma estratégia reprodutiva nova chamada "unissexualidade" — uma forma de homotalismo onde indivíduos de um único tipo sexual ainda podem se envolver em reprodução sexual com outros.[91] Análises genéticas de X. parietina e seu parceiro algal Trebouxia decolorans mostram estruturas populacionais contrastantes. O componente fúngico exibe alta mistura genética e pouca estrutura entre populações. Em contraste, o parceiro algal mostra diferenças genéticas claras entre populações, consistentes com sua reprodução principalmente assexuada. Isso sugere que o sucesso de X. parietina em diversos habitats pode vir, em parte, de sua capacidade de se associar a diferentes fotobiontes localmente adaptados. Quando comparado a líquens fruticulosos, como Evernia mesomorpha e Ramalina menziesii [en], X. parietina mostra diferenças genéticas mais fortes entre populações dentro da mesma paisagem. Isso indica que X. parietina tem troca genética mais limitada entre populações próximas do que se pensava anteriormente, possivelmente devido à especialização de habitat.[89]
As investigações moleculares sobre os locus do tipo sexual (MAT) revelaram ainda mais as estratégias reprodutivas de Xanthoria. Embora X. parietina seja homotálica — possuindo apenas um gene MAT1-2 (embora truncado) —, espécies como X. polycarpa são heterotálicas, com idiomorfos MAT distintos (regiões genéticas de tipo de acasalamento diferentes). Essas diferenças na estrutura do sistema de acasalamento podem afetar significativamente a genética populacional, influenciando os níveis de diversidade genética, fluxo gênico e, em última análise, os processos de especiação dentro do gênero.[92]
Tolerância à poluição
Xanthoria parietina é altamente resistente à poluição atmosférica, incluindo metais pesados, compostos de nitrogênio e ozônio. Experimentos de laboratório demonstraram que tolera a exposição a contaminantes atmosféricos e íons bissulfitos com pouco ou nenhum dano.[93] Também é resistente à contaminação por metais pesados[94] e à poluição por nitrogênio.[95] Os mecanismos subjacentes a essa tolerância envolvem múltiplos sistemas protetores. A camada de parietina no córtex superior atua como uma barreira hidrofóbica, reduzindo a penetração de íons metálicos tóxicos nas células do fotobionte. Estudos experimentais mostraram que talos deficientes em parietina experimentam maior estresse fisiológico quando expostos a metais pesados.[44] A parietina também contribui para a tolerância ao ozônio; experimentos de fumigação revelaram que amostras contendo parietina recuperaram a eficiência fotossintética e a integridade da clorofila mais rapidamente do que aquelas sem ela, sugerindo uma função antioxidante além de seu papel como pigmento de proteção contra luz. Além disso, os níveis de espécies reativas de oxigênio induzidos pela exposição ao ozônio foram significativamente mais altos em amostras deficientes em parietina, reforçando seu papel na mitigação do estresse oxidativo.[96] O estado de hidratação de X. parietina influencia sua sensibilidade ao ozônio. Talos secos sofrem menos danos e se recuperam mais rapidamente do que os hidratados, provavelmente porque a troca gasosa reduzida limita a penetração do ozônio. Esse fator ajuda a explicar a resiliência do líquen em climas mediterrâneos, onde frequentemente permanece dessecado durante períodos de alta poluição por ozônio.[96]
Ambos os parceiros simbióticos contribuem para a desintoxicação dentro do talo. O fotobionte é particularmente vulnerável à toxicidade de metais devido ao seu delicado maquinário fotossintético, mas mitiga os danos por meio da síntese de fitoquelatinas — peptídeos ricos em enxofre derivados de glutationa que se ligam e sequestram íons metálicos. Esses compostos servem como uma defesa secundária quando os metais penetram a barreira de parietina. O micobionte também auxilia na tolerância a metais por meio da imobilização de metais na parede celular e da produção de compostos antioxidantes.[44] Outros mecanismos protetores incluem tamponamento de pH, alto conteúdo de potássio e propriedades antioxidantes da parietina. O líquen também apresenta respostas de desintoxicação induzidas, incluindo a conversão de dióxido de enxofre tóxico em sulfato não tóxico, aumento da produção de glutationa, síntese aprimorada de prolina e arginina e melhoria da desintoxicação de espécie reativa de oxigénio.[93] Essas adaptações ajudam a manter funções fisiológicas estáveis em ambientes poluídos: sua clorofila permanece intacta, a atividade fotossintética diminui apenas moderadamente, as membranas celulares mantêm a integridade com vazamento mínimo de eletrólitos e os níveis de ATP permanecem constantes. Essas características permitem que X. parietina persista em ambientes poluídos onde muitas outras espécies de líquens declinam.[97]
Resposta à poluição e estresse ambiental
Registros históricos indicam que X. parietina persistiu em Londres apesar da grave poluição do ar, mesmo quando muitos outros líquens desapareceram. Estudos de mapeamento do meio do século XX revelaram que sua distribuição correlacionava-se com áreas de concentrações moderadas de dióxido de enxofre, mas estava ausente das zonas mais poluídas do centro de Londres, sugerindo que, embora resistente a contaminantes atmosféricos, possui um limite superior de tolerância.[98] No entanto, é sensível a certos poluentes, como demonstrado após o derramamento de óleo de Torrey Canyon, quando a contaminação por óleo e dispersantes tóxicos causaram mortalidade generalizada em rochas costeiras. Talos afetados perderam sua pigmentação laranja característica, indicando dano químico que interferiu na atividade enzimática e proteica, levando, em última análise, ao desprendimento da superfície rochosa.[99] O dispersante BP 1002, usado durante os esforços de limpeza, foi posteriormente considerado altamente tóxico para a vida marinha e líquens costeiros. Em X. parietina, seus componentes surfactantes romperam as membranas celulares algais, reduzindo a atividade fotossintética e acelerando a deterioração do talo.[100]
A poluição afeta tanto a estrutura populacional quanto o desenvolvimento de X. parietina. Houve um declínio na densidade populacional com o aumento dos níveis de poluição; um estudo documentou aproximadamente 47 talos por árvore em zonas levemente poluídas, em comparação com 12 em áreas moderadamente poluídas e 9 em regiões severamente poluídas.[59] Em ambientes não poluídos, o líquen completa seu ciclo de vida, atingindo a maturidade e a velhice. No entanto, em áreas urbanas poluídas, frequentemente morrem antes de alcançar esses estágios de desenvolvimento posteriores. Efeitos morfológicos da poluição incluem talos menores, menos apotécios e de tamanho reduzido, e menor aderência ao substrato em estágios de desenvolvimento posteriores.[59] Em vez de acelerar o desenvolvimento sob estresse, como algumas espécies de plantas fazem, X. parietina exibe um desenvolvimento retardado de indivíduos pré-generativos e eliminação de indivíduos generativos menos tolerantes. Sua tolerância à poluição também varia com a disponibilidade de luz; condições ideais parecem ser em áreas com baixa poluição e boa iluminação, onde indivíduos generativos jovens dominam e a capacidade reprodutiva é mais alta.[59]
A espécie também demonstra alta tolerância a metais. Um mecanismo chave é a imobilização de metais tóxicos no apoplasto (o espaço extracelular entre a parede celular e a membrana plasmática), impedindo sua entrada em células vivas.[101] Além disso, produz peptídeos tiólicos protetores, aumenta a produção de antioxidantes e mantém a integridade da membrana sob estresse metálico. Estudos de laboratório indicam sensibilidade diferencial a vários metais, com maior tolerância a cádmio e níquel, mas menor a cobre e mercúrio.[101] Também mostra resiliência à exposição a pesticidas, persistindo em jardins não tratados, mas declinando em pomares semi-intensivos e desaparecendo em pomares intensivamente pulverizados.[102] Essas respostas fisiológicas a diversos poluentes tornam esta espécie valiosa para aplicações de monitoramento ambiental.[103][104]
Interações com espécies
Fungos liquenícolas

Xanthoria parietina hospeda uma gama diversificada de fungos liquenícolas — fungos que vivem em líquens. Até 2017, pelo menos 41 espécies de fungos liquenícolas foram relatadas em X. parietina, incluindo parasitas obrigatórios e colonizadores facultativos. Exemplos incluem Athelia arachnoidea, Catillaria nigroclavata e Capronia suijae. Enquanto alguns desses fungos podem ser patogênicos, outros colonizam o líquen sem causar danos óbvios ao talo.[105]
Em alguns casos, múltiplos fungos liquenícolas e saprófitos podem formar comunidades complexas em talos em decomposição de X. parietina. Um estudo na Áustria documentou dez espécies fúngicas diferentes colonizando simultaneamente talos liquênicos danificados. O mais visualmente evidente foi Xanthoriicola physciae [en], enquanto o hifomiceto dematiáceo Cladosporium macrocarpum foi o colonizador mais abundante, cobrindo grandes áreas do talo e apotécios com filamentos escuros e algodonosos. Este fungo causa descoloração visível e irregularidade dos discos apoteciais antes de eventualmente destruir a estrutura do líquen. Outros parasitas notáveis incluíram Lichenoconium xanthoriae, Lichenodiplis poeltii e Pyrenochaeta xanthoriae. O altamente destrutivo Marchandiomyces aurantiacus forma crostas laranja pálidas distintas na superfície do líquen, encolhendo o talo até um filme frágil e branqueado que adere ao substrato antes da decomposição completa.[106]
.jpg)
Entre esses, o fungo recentemente descrito (2023) Tremella parietinae é encontrado exclusivamente em X. parietina, onde induz a formação de galhas convexas, laranja a amarelas, dentro do himênio de seus apotécios. Este fungo é conhecido em vários países europeus — incluindo Áustria, Espanha e Suécia — e provavelmente tem uma distribuição mais ampla onde quer que seu hospedeiro ocorra. Outro fungo liquenícola, Tremella occultixanthoriae, parasita X. parietina, mas se desenvolve na superfície inferior do talo e produz basídios de quatro células. Ambos os fungos pertencem a um complexo mais amplo de espécies de Tremella que se especializam em infectar líquens Teloschistaceae, frequentemente com especificidade estrita de hospedeiro.[107]
Alguns fungos saprófitos comuns, não tipicamente associados a líquens, também foram encontrados colonizando X. parietina. Estes incluem Epicoccum nigrum [en], aparecendo como montes hemisféricos roxo-escuros na superfície dos discos apoteciais, e Periconia digitata, que forma cabeças esféricas pedunculadas distintas, assemelhando-se a pequenos alfinetes nas apotécios e no talo. As condições ambientais que desencadeiam tal colonização fúngica extensa permanecem incertas, embora fatores como cobertura prolongada de neve, alta pluviosidade ou outros estressores ambientais possam inicialmente enfraquecer o líquen, tornando-o suscetível à invasão fúngica.[106]
Outro fungo liquenícola é Arthonia parietinaria, que por muito tempo foi identificado erroneamente como Arthonia molendoi ou A. epiphyscia. Esta espécie forma ascomas pretos foscos, dispostos em grandes grupos de até 20–30 (às vezes 50) na superfície do talo de X. parietina, incluindo suas margens apoteciais e himênios. Diferentemente de A. molendoi (que infecta principalmente Rusavskia elegans), A. parietinaria parece estar restrita ao grupo X. parietina e é amplamente distribuída pela Europa, oeste da Ásia e norte da África. O fungo atua como um comensal ou parasita fraco, causando nenhum dano significativo ao tecido do hospedeiro fora dos pontos de infecção, embora grupos maiores de ascomas possam causar leve descoloração do talo hospedeiro.[108]
O impacto bioquímico do fungo liquenícola Xanthoriicola physciae em seu hospedeiro foi investigado usando espectroscopia Raman. Essa técnica revelou que o fungo destrói pigmentos fotoprotetores essenciais — como parietina e carotenoides — vitais para proteger o líquen da luz solar intensa. Além disso, a detecção de escitonemina — um pigmento tipicamente produzido por cianobactérias e conhecido por proteção UV — nos tecidos infectados implica colonização secundária por cianobactérias.[109]
Interações com gastrópodes e dispersão
Xanthoria parietina serve tanto como fonte de alimento quanto como abrigo para certos gastrópodes. O caracol Balea perversa [en] usa o líquen para abrigo e nutrição.[110] Da mesma forma, outros gastrópodes, como Helicigona lapicida, alimentam-se de Xanthoria parietina. Esse pastoreio pode contribuir para a dispersão do líquen: células do fotobionte de X. parietina sobrevivem parcialmente à passagem pelo trato digestivo do caracol, retendo alguma atividade fotossintética mesmo após a digestão. Essa sobrevivência levanta a possibilidade de que a herbivoria por caracóis possa facilitar a reliquenização — seja recombinando simbiontes sobreviventes do mesmo talo ou misturando fotobiontes e micobiontes de diferentes indivíduos em depósitos fecais.[111] No entanto, a digestão reduz significativamente a viabilidade do fotobionte, com a fluorescência do fotobionte (uma medida da atividade fotossintética) diminuindo em 41–44% após a passagem pelo intestino do caracol. Embora algumas células permaneçam intactas, frequentemente sofrem danos morfológicos (incluindo cloroplastos encolhidos e distâncias aumentadas entre a parede celular e a membrana), deixando incerto se os fotobiontes sobreviventes podem estabelecer novos líquens efetivamente sem esporos fúngicos ou hifas viáveis.[111]
Interações com microfauna
As apotécios de Xanthoria parietina também hospedam animais microscópicos. Membros do gênero de rotíferos Philodina foram observados alimentando-se dos esporos do líquen presentes nas superfícies apoteciais. Rotíferos individuais podem acumular várias dezenas de esporos, e ao ingerir 20 ou mais esporos, cerca de 15% permanecem viáveis e capazes de germinar após a excreção. Essas descobertas indicam que os rotíferos podem atuar como vetores de dispersão, desalojando e liberando esporos viáveis em novos locais.[112]
Papéis competitivos e ecológicos
Além dessas interações, Xanthoria parietina frequentemente cresce sobre outros líquens epilíticos sem afetar seus fotobiontes. Também suporta comunidades microbianas sob seu talo, provavelmente se beneficiando de micro-habitats criados por suas estruturas de fixação.[76] Além disso, Xanthoria parietina desempenha um papel no ciclo biogeoquímico ao promover o intemperismo de rochas por meio da penetração e adesão de hifas. Suas interações com minerais como quartzo, feldspato e muscovita contribuem para a quebra mineral, particularmente em substratos ricos em carbonato.[76]
Por fim, o líquen compete com outros líquens foliosos. Em configurações experimentais, mostrou equivalência competitiva com Parmelia caperata, mas foi superado por Parmelia saxatilis em algumas condições. Em misturas de três espécies, no entanto, X. parietina frequentemente obteve uma vantagem competitiva — possivelmente devido à sua tolerância a níveis elevados de nitrogênio. Sua capacidade de prosperar em ambientes ricos em nutrientes pode permitir que supere espécies acidófitas em habitats influenciados por insumos agrícolas ou atmosféricos de nitrogênio.[77]
Quando compete com outros líquens, X. parietina tipicamente forma relações codominantes, em vez de deslocar completamente outras espécies, particularmente em estágios iniciais de colonização. Estudos de campo mostram que, quando talos de X. parietina fazem fronteira com outros líquens, como espécies de Physcia [en], nenhum deles cresce distintamente sobre o outro, mas seus lóbulos marginais se misturam.[63] A coocorrência frequente de X. parietina com espécies de Physcia de cor cinza pode representar mais do que uma simples coabitação. Pesquisas sugerem que, durante a reprodução, esporos fúngicos de X. parietina podem se envolver em uma forma de parasitismo reprodutivo (um tipo de simbiose onde um microrganismo altera a reprodução de um hospedeiro) ao "roubar" parceiros algais de líquens Physcia, que contêm as mesmas espécies algais. Essa estratégia de compartilhamento algal proporciona uma vantagem reprodutiva, pois os esporos fúngicos germinantes de X. parietina podem evitar o processo incerto de encontrar algas livres compatíveis.[113]
No entanto, a espécie se envolve em um padrão de sucessão ecológica de longo prazo. Estudos acompanhando comunidades liquênicas ao longo de cinco anos descobriram que espécies de Physcia (como Physcia adscendens e P. caesia) são relativamente de curta duração, geralmente desenvolvendo-se e desaparecendo em cerca de dois anos, enquanto populações de X. parietina persistiram durante todo o período. Eventualmente, em locais abrigados ou úmidos, briófitas (particularmente espécies de Orthotrichum) tendem a invadir e crescer sobre superfícies cobertas por líquens — representando o padrão normal de sucessão em situações de dossel. A capacidade regenerativa de X. parietina permite que mantenha sua presença por mais tempo do que muitas outras espécies de líquens durante esse processo sucessional, mas eventualmente é substituída por musgos de crescimento vigoroso na maioria dos habitats abrigados.[63]
Usos
Medicina tradicional
Xanthoria parietina tem uma longa história de uso na medicina tradicional em várias culturas. Em Andaluzia, Espanha, este líquen era conhecido como flor de piedra ("flor de pedra") ou rompepiedra ("quebra-pedra"). Curandeiros tradicionais espanhóis o utilizavam para vários propósitos: tratar queixas menstruais quando preparado como uma decocção em vinho, abordar distúrbios renais e dores de dente quando feito em decocções à base de água, e servir como um analgésico geral. Também o incorporavam em xaropes para tosse junto com vários ingredientes vegetais.[114]
Na medicina tradicional europeia durante a era moderna inicial, X. parietina era fervido com leite para tratar icterícia, frequentemente junto com Polycauliona candelaria.[114] Essa aplicação exemplifica a Doutrina das assinaturas [en] — um sistema de crenças que plantas que se assemelham a partes do corpo poderiam tratar doenças dessas partes — uma vez que a cor amarelo-laranja do líquen era considerada indicativa de sua eficácia contra o amarelamento da pele na icterícia.[115]
Na medicina tradicional chinesa, era conhecido como shí huáng yī ("roupas amarelas de pedra") e valorizado por suas propriedades antibacterianas. O uso medicinal generalizado de líquens, incluindo X. parietina, foi amplamente abandonado por volta de 1800, e essas aplicações representam remédios populares históricos, em vez de tratamentos baseados em evidências.[114]
Tingimento
Xanthoria parietina tem sido usado como uma fonte de corante natural por séculos. Evidências históricas indicam que civilizações antigas reconheceram as propriedades de tingimento deste líquen. Em uma publicação de 1934, Reginald Campbell Thompson analisou textos assírios antigos que mencionam líquens e tingimento. Thompson observou que o "líquen amarelo de parede" era "afirmado dar uma boa cor amarela ou laranja, se fixado com alume". A análise de Thompson dessas tábuas antigas sugere que o conhecimento do uso de líquens com alume como mordente existia na Mesopotâmia antiga. O alume (um mineral natural contendo sulfato de alumínio) era um mordente usado com este líquen principalmente para fixar o corante aos tecidos. Thompson observa que "a descoberta do alume foi um dos eventos mais importantes na história do tingimento." X. parietina era valorizado por sua acessibilidade, crescendo facilmente em troncos de árvores e paredes, e sua capacidade de produzir tons consistentes de amarelo a laranja quando processado adequadamente com mordentes.[116]
A parietina é responsável pelas propriedades de tingimento do líquen, e a parietina isolada pura produz as mesmas características de cor que extratos de líquen inteiro. Quando processado usando diferentes métodos de extração e mordentes, este líquen produz uma gama diversificada de cores. Extrações em água fervente produzem tons dourado-marrom, amarelo e caramelo, enquanto processos de fermentação com amoníaco a 10% resultam em tons roxo-rosa, laranja e rosa.[117] O método POD (foto-oxidado), que envolve expor o material do líquen à luz solar em uma solução alcalina ao longo do tempo, pode extrair corantes azuis ou roxos de X. parietina.[118]
O alume provou ser particularmente eficaz como mordente para corantes de X. parietina, permitindo que as cores naturais se desenvolvam completamente enquanto aumentam sua permanência. Os mordentes funcionam criando uma ponte química entre o corante natural e a fibra, formando ligações fortes que garantem a resistência da cor à lavagem e ao desbotamento.[117]
Pesquisas modernas expandiram além das aplicações tradicionais de tingimento, focando na parietina. Este composto hidrofóbico serve como um agente fotoprotetor natural para o líquen. Estudos recentes exploraram o potencial da parietina em nanotecnologia, particularmente na síntese sustentável de nanopartículas de prata com propriedades antimicrobianas.[119]
Pesquisa
Histórica
Em 1888, o botânico francês Gaston Bonnier demonstrou evidências experimentais iniciais para a simbiose liquênica por meio de seu trabalho com X. parietina (então chamada Parmelia parietina). Ele relatou a criação de talos liquênicos artificiais substituindo o parceiro algal natural do organismo (Protococcus viridis) por diferentes espécies de algas, incluindo Protococcus botryoides e a alga vermelha filamentosa Trentepohlia abietina.[120] Embora seus métodos prenunciassem técnicas microbiológicas modernas e representassem um passo significativo para a época, avaliações modernas notam limitações críticas. Suas fontes algais não eram verdadeiramente isoladas (vindo de outros talos liquênicos), e seus "líquens sintetizados" apenas vagamente se assemelhavam a espécimes naturais, mostrando hifas fúngicas envolvendo células algais, mas faltando a verdadeira morfologia liquênica.[29]
Em 1967, Richardson conduziu experimentos de transplante iniciais com X. parietina que ajudaram a estabelecer métodos para estudar a adaptabilidade dos líquens. Usando uma técnica nova de fixar talos liquênicos a novos substratos com cola de resina, o estudo alcançou uma taxa de sobrevivência de 96% em espécimes transplantados. Quando espécimes costeiros (var. ectanea) foram movidos para telhados de fazendas em Oxford, mostraram mudanças morfológicas significativas dentro de 18 meses, incluindo um aumento na largura do lóbulo de 0,8 mm para 2,4 mm. O estudo também demonstrou que a produção de parietina poderia se adaptar às condições locais dentro de seis meses, com espécimes transplantados eventualmente igualando os níveis de pigmento das populações nativas. Esta pesquisa inicial ajudou a estabelecer que, enquanto algumas características morfológicas permanecem estáveis independentemente do ambiente, outras mostram plasticidade significativa em resposta a novas condições. A técnica de transplante provou ser valiosa para estudar tanto relações taxonômicas quanto adaptações ecológicas em líquens, ajudando a estabelecer a base para estudos experimentais futuros.[121]
Em 1986, pesquisadores realizaram a primeira resíntese completa em laboratório de X. parietina a partir de seus componentes fúngico e algal separados. O experimento envolveu isolar esporos fúngicos e células algais, cultivá-los separadamente e, em seguida, permitir que se recombinassem em um substrato de ágar. Após 8–12 meses, os simbiontes formaram novos talos liquênicos de 2–5 mm de diâmetro, completos com apotécios. Embora esses líquens criados artificialmente mostrassem uma estrutura básica semelhante a espécimes naturais, diferiam em alguns aspectos, incluindo pigmentação mais pálida e a ausência de alguns produtos liquênicos característicos. Essa conquista representou um avanço no entendimento da biologia liquênica, pois a síntese bem-sucedida de líquens em laboratório havia sido um desafio por mais de um século.[122]
Biomonitoramento
Xanthoria parietina é um bioindicador eficaz para rastrear tendências de poluição do ar e acumulação de metais pesados ao longo do tempo. Um estudo de sete anos na Itália Adriática mediu nove metais pesados (Cd, Cr, Ni, Pb, V, Cu, Zn, Fe, Al) em 51 locais, revelando padrões de poluição espacial e temporal. Durante o estudo, os níveis de Cr, Ni, Zn, Fe e Al aumentaram, provavelmente devido a emissões industriais e veiculares, enquanto os níveis de Pb diminuíram, refletindo a eliminação gradual da gasolina com chumbo. O estudo também identificou pontos críticos de poluição, com níveis elevados de vanádio perto de refinarias de petróleo (um marcador de combustão de combustíveis fósseis) e concentrações mais altas de cobre e zinco em áreas urbanas, provavelmente devido ao tráfego e à indústria. Análises estatísticas mostraram que Al, Fe, Cr e Ni estavam ligados a emissões industriais e poeira do solo ressuspensa, enquanto Cd, Zn, Cu e V estavam associados a atividades de refinarias de petróleo e transporte de poluentes de longa distância. Essa capacidade de diferenciar fontes de poluição torna X. parietina uma ferramenta valiosa para forense ambiental e atribuição de fontes de poluição.[103]
Além do mapeamento de poluição, X. parietina é usado em avaliações de risco à saúde ambiental, identificando áreas com acumulação persistente de metais pesados que podem indicar maior exposição humana a contaminantes transportados pelo ar. Uma vantagem do biomonitoramento com líquens é que ele oferece uma alternativa econômica às redes de qualidade do ar, que exigem equipamentos e infraestrutura especializados. Como os líquens acumulam poluentes ao longo do tempo, permitem amostragem espacial de alta densidade, mesmo em áreas sem estações de monitoramento automatizadas. Isso torna X. parietina particularmente útil para avaliações retrospectivas de poluição e monitoramento ambiental de longo prazo. As descobertas do estudo da Itália Adriática apoiam seu papel como uma ferramenta confiável para rastrear tendências de poluição, identificar fontes de poluentes e informar estratégias de planejamento ambiental e saúde pública.[103]
Influências ambientais na taxa de crescimento têm implicações importantes para estudos de biomonitoramento que usam X. parietina para avaliar a qualidade do ar. Como o líquen acumula poluentes ao longo do tempo, diferenças nas taxas de crescimento entre populações podem afetar as medições de carga de poluentes. Talos em ambientes úmidos e mais frios podem acumular contaminantes a uma taxa menor do que aqueles em habitats mais secos e quentes, simplesmente devido a diferenças no crescimento e efeitos de diluição. Consequentemente, esforços de biomonitoramento baseados em líquens devem considerar as condições climáticas locais para garantir comparações precisas dos níveis de poluição atmosférica entre regiões.[60]
Astrobiologia e pesquisa espacial

A resiliência extrema de Xanthoria parietina a tornou um foco de astrobiologia e pesquisa de exposição espacial. Líquens estão entre as formas de vida mais tolerantes ao estresse, e X. parietina, com suas fortes defesas contra UV, foi testada para sobrevivência em condições espaciais e semelhantes às de Marte. Experimentos de laboratório simulando condições do espaço exterior (alto vácuo, radiação UV cósmica) expuseram o líquen a 10–14 dias de estresse extremo. O líquen sobreviveu, permaneceu metabolicamente ativo e retomou o crescimento após o tratamento, provando sua viabilidade a curto prazo em ambientes espaciais.[124] Testes de laboratório demonstraram ainda a tolerância extraordinária do líquen ao frio, com amostras secas sobrevivendo à imersão em nitrogênio líquido a temperaturas abaixo de -182°C.[29]
Com base nessas descobertas, X. parietina foi testada sob condições marcianas simuladas em um estudo de 2023. As amostras foram expostas por 30 dias a baixa pressão, uma atmosfera rica em CO2, mudanças extremas de temperatura e alta radiação UV. A saúde do líquen foi monitorada usando fluorescência de clorofila e análise estrutural. Ele sobreviveu aos 30 dias completos, reteve a capacidade fotossintética e manteve a integridade estrutural, embora as amostras expostas a UV mostrassem eficiência reduzida e alguma degradação de pigmentos. Dada essa resiliência, os pesquisadores sugeriram X. parietina como candidato para exposição espacial de longo prazo, como na Estação Espacial Internacional ou satélites.[123]
Um estudo de 2024 examinou ainda mais a resiliência fisiológica de X. parietina em condições marcianas simuladas. Após 30 dias, a eficiência fotossintética caiu 85% em amostras expostas a UV e 46% em amostras não expostas a UV. No entanto, 24 horas após o retorno a condições semelhantes às da Terra, a fotossíntese começou a se recuperar, demonstrando a capacidade de X. parietina reparar seu sistema fotossintético após exposição extrema prolongada.[125]
A recuperação parece estar ligada à produção de antioxidantes. Em condições semelhantes às de Marte, o estresse oxidativo aumentou os níveis de antioxidantes, protegendo contra os raios UV e as flutuações de temperatura. Ao longo de 30 dias, os níveis de antioxidantes diminuíram à medida que o líquen neutralizava as espécies reativas de oxigênio, indicando uma resposta adaptativa que apoia a sobrevivência em ambientes extremos.[125]
X. parietina minimiza o metabolismo em condições extremas. No estudo de simulação de Marte, a eficiência do fotossistema II diminuiu sob estresse de UV, mas permaneceu ativa. As amostras com proteção UV tiveram melhor desempenho, sugerindo que, sem exposição à radiação, X. parietina poderia sobreviver ao frio e à baixa pressão semelhantes aos de Marte. A espectroscopia Raman revelou a degradação dos carotenoides e da parietina após a exposição prolongada aos raios UV, mas permaneceu pigmento suficiente para proteger as células vitais, deixando a estrutura do líquen intacta.[123]
Referências
- ↑ a b Tsurykau, Andrei; Bely, Pavel; Arup, Ulf (2020). «Molecular phylogenetic analyses reveal two new synonyms of Xanthoria parietina». Plant and Fungal Systematics. 65 (2): 620–623. doi:10.35535/pfsyst-2020-0033

- ↑ a b c «GSD Species Synonymy. Current Name: Xanthoria parietina (L.) Th. Fr., Lich. arct. (Uppsala): 67 (1860)». Species Fungorum. Consultado em 22 de agosto de 2025
- ↑ a b c Jørgensen, Per M.; James, Peter W.; Jarvis, Charles E. (1994). «Linnaean lichen names and their typification». Botanical Journal of the Linnean Society. 115 (4): 261–405. doi:10.1111/j.1095-8339.1994.tb01784.x
- ↑ Linnaeus, Carl (1753). Species Plantarum (em latim). 2. Stockholm: Impensis Laurentii Salvii. p. 1143
- ↑ Acharius, Erik (1803). Methodus qua Omnes Detectos Lichenes Secundum Organa Carpomorpha ad Genera, Species et Varietates Redigere atque Observationibus Illustrare Tentavit Erik Acharius [Um método pelo qual Erik Acharius tentou classificar todos os líquens conhecidos de acordo com suas estruturas de corpos frutíferos em gêneros, espécies e variedades, e ilustrá-los com observações] (em latim). Stockholm: F.D.D. Ulrich. p. 213
- ↑ Norman, J.M. (1852). «Conatus praemissus redactionis novae generum nonnullorum Lichenum in organis fructificationes vel sporis fundatae» [A preliminary attempt at a new revision of certain genera of lichens based on their fruiting bodies or spores]. Nytt Magazin for Naturvidenskapene (em latim). 7: 213–252
- ↑ Fries, Th.M. (1860). Lichenes Arctoi Europae Groenlandiaeque hactenus cogniti [The Arctic lichens of Europe and Greenland known thus far] (em latim). [S.l.: s.n.] p. 167
- ↑ Acharius, Erik (1810). Lichenographia Universalis [Universal Lichenography] (em latim). Gottingen: Apud Iust. Frid. Danckwerts. p. 464
- ↑ Räsänen, V. (1944). «Lichenes novi I» [New lichens I]. Annales Botanici Societatis Zoologicae-Botanicae Fennicae "Vanamo" (em latim). 20 (3): 1–34 [12]
- ↑ «Record Details: Xanthoria parietina f. antarctica (Vain.) Hue, Deux. Expéd. Antarct. Franç., 1908-10, Lichens: 44 (1915)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina f. ectaneoides (Nyl.) Boistel, Nouv. Fl. Lich. (Paris) 2: 71 (1903)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina f. ectaniza Boistel, Nouv. Fl. Lich. (Paris) 2: 71 (1903)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina f. polycarpa (Hoffm.) Arnold, Verh. Kaiserl.-Königl. zool.-bot. Ges. Wien 30: 121 (1881) [1880]». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina subsp. calcicola (Oxner) Clauzade & Cl. Roux, Bull. Soc. bot. Centre-Ouest, Nouv. sér., num. spec. 7: 830 (1985)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina subsp. phlogina (Ach.) Sandst., Abh. naturw. Ver. Bremen 21(1): 223 (1912)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. aureola (Ach.) Th. Fr., Lich. arct. (Uppsala): 67 (1860)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. australis Zahlbr., K. svenska Vetensk-Akad. Handl., ny följd 57(no. 6): 49 (1917)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. contortuplicata (Ach.) H. Olivier, Rev. Bot. 12: 94 (1894)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. incavata (Stirt.) Js. Murray, Trans. Roy. Soc. N.Z. 88: 202 (1960)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. lobulata (Flörke) Rabenh., Krypt.-Fl. Sachsen, Abth. 2 (Breslau): 282 (1870)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. mandschurica Zahlbr., Annls mycol. 29: 85 (1931)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ «Record Details: Xanthoria parietina var. rutilans (Ach.) Maheu & A. Gillet, Mém. Soc. Sci. Nat. Maroc. 8(2): 281 (1924)». Index Fungorum. Consultado em 22 de agosto de 2025
- ↑ Kondratyuk, S.Y.; Kärnefelt, I.; Elix, J.A.; Thell, A. (2007). «Contributions to the Teloschistaceae of Australia». Bibliotheca Lichenologica. 96: 157–174
- ↑ Kondratyuk, S.; Yatsyna, A.P.; Lőkös, L.; Galanina, I.; Moniri, M.H.; Hur, J.-S. (2013). «Three new Xanthoria and Rusavskia species (Teloschistaceae, Ascomycota) from Europe». Acta Botanica Hungarica. 55 (3–4): 351–365. doi:10.1556/ABot.55.2013.3-4.10
- ↑ «Xanthoria parietina (L.) Th. Fr.». Catalogue of Life. Species 2000: Leiden, the Netherlands. Consultado em 26 de agosto de 2025
- ↑ Lindblom, Louise; Ekman, Stefan (2005). «Molecular evidence supports the distinction between Xanthoria parietina and X. aureola (Teloschistaceae, lichenized Ascomycota)». Mycological Research. 109 (2): 187–199. doi:10.1017/S0953756204001790
- ↑ Honegger, R. (1978). «The ascus apex in lichenized fungi I. The Lecanora-, Peltigera- and Teloschistes-types» (PDF). The Lichenologist. 10 (1): 47–67. doi:10.1017/S0024282978000079
- ↑ Ulloa, Miguel; Aguirre-Acosta, Elvira (2020). Illustrated Generic Names of Fungi. [S.l.]: APS press. p. 398. ISBN 978-0-89054-618-5
- ↑ a b c d e Lücking, Robert; Spribille, Toby (2024). The Lives of Lichens. Princeton: Princeton University Press. pp. 22–23; 36; 88; 255. ISBN 978-0-691-24727-4
- ↑ a b c d McCune, Bruce; Geiser, Linda (2023). Macrolichens of the Pacific Northwest 3 ed. Corvallis: Oregon State University Press. p. 470. ISBN 978-0-87071-251-7
- ↑ Swinscow, Thomas Douglas Victor; Krog, Hildur (1988). Macrolichens of East Africa. London: British Museum (Natural History). p. 358. ISBN 978-0-565-01039-3
- ↑ Pentecost, A.; Rose, C.I. (1985). «Apothecium production in Xanthoria parietina». The Lichenologist. 17 (1): 33–38. doi:10.1017/S0024282985000056
- ↑ Galun, Margalith (1988). CRC Handbook of Lichenology, Volume I. Boca Raton: CRC. p. 105. ISBN 978-0-8493-3581-5
- ↑ a b c McMullin, R. Troy (2023). Lichens. The Macrolichens of Ontario and the Great Lakes Region of the United States. [S.l.]: Firefly Books. p. 552. ISBN 978-0-228-10369-1
- ↑ a b c Lindblom, Louise; Ekman, Stefan (2006). «Genetic variation and population differentiation in the lichen-forming ascomycete Xanthoria parietina on the island Storfosna, central Norway». Molecular Ecology. 15 (6): 1545–1559. PMID 15839102. doi:10.1111/j.1365-294X.2006.02880.x
- ↑ Bubrick, P.; Galun, Margalith; Frensdorff, A. (1984). «Observations on free-living Trebouxia De Puymaly and Pseudotrebouxia Archibald, and evidence that both symbionts from Xanthoria parietina (L.) can be found free-living in nature». The New Phytologist. 97 (3): 455–462. JSTOR 2432333. doi:10.1111/j.1469-8137.1984.tb03611.x

- ↑ a b Collins, C.R.; Farrar, J.F. (1978). «Structural resistances to mass transfer in the lichen Xanthoria parietina». New Phytologist. 81 (1): 71–83. doi:10.1111/j.1469-8137.1978.tb01605.x
- ↑ Vrablíková, Hana; McEvoy, Maria; Solhaug, Knut Asbjørn; Barták, Milos; Gauslaa, Yngvar (2006). «Annual variation in photoacclimation and photoprotection of the photobiont in the foliose lichen Xanthoria parietina». Journal of Photochemistry and Photobiology B: Biology. 83 (3): 151–162. doi:10.1016/j.jphotobiol.2005.12.019
- ↑ Nyati, Shyam; Werth, Silke; Honegger, Rosmarie (2013). «Genetic diversity of sterile cultured Trebouxia photobionts associated with the lichen-forming fungus Xanthoria parietina visualized with RAPD-PCR fingerprinting techniques» (PDF). The Lichenologist. 45 (6): 825–840. doi:10.1017/S0024282913000546
- ↑ Galun, Margalith; Bubrick, P.; Frensdorff, A. (1984). «Initial stages in fungus-alga interaction». The Lichenologist. 16 (2): 103–110. doi:10.1017/S0024282984000281
- ↑ Bubrick, P.; Galun, Margalith (1980). «Proteins from the lichen Xanthoria parietina which bind to phycobiont cell walls. Correlation between binding patterns and cell wall cytochemistry». Protoplasma. 104 (1–2): 167–173. doi:10.1007/BF01279379
- ↑ Brickley, Mark R. (2017). «Development of a live cell imaging method for mitochondria in Trebouxia photobionts». The Lichenologist. 49 (3): 275–286. doi:10.1017/S0024282917000160
- ↑ a b Solhaug, Knut Asbjorn; Gauslaa, Yngvar; Nybakken, Line; Bilger, Wolfgang (2003). «UV-induction of sun-screening pigments in lichens». New Phytologist. 158 (1): 91–100. doi:10.1046/j.1469-8137.2003.00708.x

- ↑ a b c d Kalinowska, Renata; Bačkor, Martin; Pawlik-Skowrońska, Barbara (2015). «Parietin in the tolerant lichen Xanthoria parietina (L.) Th. Fr. increases protection of Trebouxia photobionts from cadmium excess». Ecological Indicators. 58: 132–138. doi:10.1016/j.ecolind.2015.05.055
- ↑ Solhaug, K.A.; Gauslaa, Y. (2004). «Photosynthates stimulate the UV-B induced fungal anthraquinone synthesis in the foliose lichen Xanthoria parietina». Plant, Cell and Environment. 27 (2): 167–176. doi:10.1111/j.1365-3040.2003.01129.x

- ↑ Gauslaa, Yngvar; Solhaug, Knut Asbjørn (2004). «Photoinhibition in lichens depends on cortical characteristics and hydration». The Lichenologist. 36 (2): 133–143. doi:10.1017/S0024282904014045
- ↑ Daminova, Amina G.; Leksin, Ilya Y.; Khabibrakhmanova, Venera R.; Gurjanov, Oleg P.; Galeeva, Ekaterina I.; Trifonova, Tatyana V.; Khamatgalimov, Ayrat R.; Beckett, Richard P.; Minibayeva, Farida V. (2024). «The roles of the anthraquinone parietin in the tolerance to desiccation of the lichen Xanthoria parietina: physiology and anatomy of the pale and bright-orange thalli». International Journal of Molecular Sciences. 25 (13): e7067. PMC 11240919
 . PMID 39000176. doi:10.3390/ijms25137067
. PMID 39000176. doi:10.3390/ijms25137067
- ↑ a b c Pedišius, Vilmantas (2020). «UV-B absorbing and bioactive secondary compounds in lichens Xanthoria elegans and Xanthoria parietina: A review». Czech Polar Reports. 10 (2): 252–262. doi:10.5817/CPR2020-2-19

- ↑ Gauslaa, Yngvar; McEvoy, Maria (2005). «Seasonal changes in solar radiation drive acclimation of the sun-screening compound parietin in the lichen Xanthoria parietina». Basic and Applied Ecology. 6 (1): 75–82. doi:10.1016/j.baae.2004.10.003
- ↑ Avan, İlker; Akbulut, Volkan Mustafa (2023). «Synthesis and antioxidant evaluation of O-methylated emodacidamides: starting from parietin, a secondary metabolite of lichen Xanthoria parietina». Chemistry & Biodiversity. 20 (1): e202200771. doi:10.1002/cbdv.202200771
- ↑ Ivanova, V.; Schlegel, R.; Gräfe, U. (2000). «2-Methoxy-4,5,7-trihydroxy-anthraquinone, a new lichen metabolite produced by Xanthoria parietina». Pharmazie. 55 (10): 785–786. PMID 11082848
- ↑ DaSelva, E.J.; Englund, B. (1974). «Occurrence of tocopherol and ergosterol in Swedish lichens». The Lichenologist. 6 (1): 96–99. doi:10.1017/S0024282974000053
- ↑ Syers, J.K.; Birnie, A.C.; Mitchell, B.D. (1967). «The calcium oxalate content of some lichens growing on limestone». The Lichenologist. 3 (3): 409–414. doi:10.1017/S0024282967000416
- ↑ a b c d e Scherrer, Sandra; De Vries, Onno M.H; Dudler, Robert; Wessels, Joseph G.H; Honegger, Rosmarie (2000). «Interfacial self-assembly of fungal hydrophobins of the lichen-forming ascomycetes Xanthoria parietina and X. ectaneoides». Fungal Genetics and Biology. 30 (1): 81–93. doi:10.1006/fgbi.2000.1205
- ↑ a b c d Scherrer, Sandra; Haisch, Annette; Honegger, Rosmarie (2002). «Characterization and expression of XPH1, the hydrophobin gene of the lichen-forming ascomycete Xanthoria parietina». New Phytologist. 154 (1): 175–184. doi:10.1046/j.1469-8137.2002.00351.x

- ↑ Meier, Franz A.; Scherrer, Sandra; Honegger, Rosmarie (2008). «Faecal pellets of lichenivorous mites contain viable cells of the lichen-forming ascomycete Xanthoria parietina and its green algal photobiont, Trebouxia arboricola». Biological Journal of the Linnean Society. 76 (2): 259–268. doi:10.1111/j.1095-8312.2002.tb02087.x

- ↑ Ott, Sieglinde (1987). «Sexual reproduction and developmental adaptations in Xanthoria parietina». Nordic Journal of Botany. 7 (2): 219–228. doi:10.1111/j.1756-1051.1987.tb00933.x
- ↑ Honegger, R. (1990). Mycobiont-photobiont interactions in adult thalli and in axenically resynthesized pre-thallus stages of Xanthoria parietina (Teloschistales, lichenized Ascomycetes). Col: Bibliothecia Lichenologica. 38. Berlin/Stuttgart: J. Cramer. pp. 191–208
- ↑ a b c d e f g Suetina, Yu. G. (2001). «Ontogeny and population structure of Xanthoria parietina (L.) Th. Fr. under different ecological conditions». Russian Journal of Ecology. 32 (3): 185–190. doi:10.1023/A:1011362227901
- ↑ a b c d Fortuna, Lorenzo; Tretiach, Mauro (2018). «Effects of site-specific climatic conditions on the radial growth of the lichen biomonitor Xanthoria parietina». Environmental Science and Pollution Research. 25 (34): 34017–34026. doi:10.1007/s11356-018-3155-z
- ↑ Chrismas, M. (1980). «Ascospore discharge and germination in Xanthoria parietina». The Lichenologist. 12 (3): 403–405. doi:10.1017/S0024282980000345
- ↑ a b Cristian, Diana; Brezeanu, Aurelia (2013). «Xanthoria parietina (L). Th. Fr. mycobiont isolation by ascospore discharge, germination and development in "in vitro" culture» (PDF). Oltenia, Studii şi comunicări, Seria Ştiinţele Naturii. 29 (2): 58–63
- ↑ a b c d Honegger, Rosmarie; Concni, S.; Kutasi, Verena (1996). «Field studies on growth and regenerative capacity in the foliose macrolichen Xanthoria parietina (Teloschistales, Ascomycotina)». Botanica Acta. 109 (3): 187–193. doi:10.1111/j.1438-8677.1996.tb00562.x
- ↑ a b Honegger, Rosmarie (1996). «Experimental studies of growth and regenerative capacity in the foliose lichen Xanthoria parietina». New Phytologist. 133 (4): 573–581. doi:10.1111/j.1469-8137.1996.tb01926.x

- ↑ a b Lindblom, Louise; Ekman, Stefan (2007). «New evidence corroborates population differentiation in Xanthoria parietina». The Lichenologist. 39 (3): 259–271. PMID 16629810. doi:10.1017/S0024282907006780
- ↑ a b Brodo, Irwin M.; Lewis, Chris; Craig, Brian (2007). «Xanthoria parietina, a coastal lichen, rediscovered in Ontario». Northeastern Naturalist. 14 (2): 300–306. doi:10.1656/1092-6194(2007)14[300:XPACLR]2.0.CO;2
- ↑ a b Hinds, James W. (1995). «Marine influence on the distribution of Xanthoria parietina, X. elegans, and X. ulophyllodes on marble gravestones in Maine». The Bryologist. 98 (3): 402–410. JSTOR 3243380. doi:10.2307/3243380
- ↑ a b Fraser, Shannon J.; Bowman, E. A.; Gianopulos, Nikolas G.; Newcombe, George (2016). «Xanthoria parietina in the Inland Pacific Northwest». North American Fungi. 11 (2): 1–12
- ↑ Ellegård Larsen, Hanne Marie; Hansen, Eric Steen; Nord-Larsen, Thomas; Rasmussen, Hanne Nina (2020). «Deciduous trees as lichen phorophytes: biodiversity and colonization patterns under common garden conditions». The Lichenologist. 52 (3): 221–232. doi:10.1017/S0024282920000018
- ↑ Fletcher, A. (1973). «The ecology of maritime (supralittoral) lichens on some rocky shores of Anglesey». The Lichenologist. 5 (5–6): 401–422. doi:10.1017/S0024282973000460
- ↑ Armstrong, R.A. (1984). «The influence of bird droppings and uric acid on the radial growth of five species of saxicolous lichens». Environmental and Experimental Botany. 24 (1): 95–99. doi:10.1016/0098-8472(84)90065-0
- ↑ Hickmott, M. (1980). «Lichens on lead». The Lichenologist. 12 (3): 405–406. doi:10.1017/S0024282980000357
- ↑ Hill, D.J.; Woolhouse, H.W. (1966). «Aspects of the autecology of Xanthoria parietina agg.». The Lichenologist. 3 (2): 207–214. doi:10.1017/S0024282966000227
- ↑ Piervittori, R.; Usai, L.; Alessio, F.; Maffei, M. (1996). «Surface N-alkane variability in Xanthoria parietina». The Lichenologist. 28 (1): 79–87. doi:10.1006/lich.1996.0007
- ↑ Fahselt, Dianne; Krol, Marianna (1989). «Biochemical comparison of two ecologically distinctive forms of Xanthoria elegans in the Canadian High Arctic». The Lichenologist. 21 (2): 135–146. doi:10.1017/S0024282989000253
- ↑ a b c Souza-Egipsy, Virginia; Wierzchos, Jacek; García-Ramos, Jose Vicente; Ascaso, Carmen (2002). «Chemical and ultrastructural features of the lichen-volcanic/sedimentary rock interface in a semiarid region (Almería, Spain)». The Lichenologist. 34 (2): 155–167. doi:10.1006/lich.2001.0371

- ↑ a b Welch, A.R.; Gillman, M.P.; John, E.A. (2006). «Effect of nutrient application on growth rate and competitive ability of three foliose lichen species». The Lichenologist. 38 (2): 177–186. doi:10.1017/S0024282906004555
- ↑ Nash III, Thomas H. (2008). «11.Nitrogen, its metabolism and potential contribution to ecosystems». In: Nash III, Thomas H. Lichen Biology 2nd ed. Cambridge, UK: Cambridge University Press. p. 221. ISBN 978-0-521-69216-8
- ↑ Gaio-Oliveira, Gisela; Dahlman, Lena; Palmqvist, Kristin; MáGuas, Cristina (2005). «Responses of the lichen Xanthoria parietina (L.) Th. Fr. to varying thallus nitrogen concentrations». The Lichenologist. 37 (2): 171–179. doi:10.1017/S0024282904014598
- ↑ Larsen Vilsholm, René; Wolseley, Pat A.; Søchting, Ulrik; Chimonides, P. Jim (2009). «Biomonitoring with lichens on twigs». The Lichenologist. 41 (2): 189–202. doi:10.1017/S0024282909007208
- ↑ Gaio-Oliveira, Gisela; Dahlman, Lena; Palmqvist, Kristin; Mguas, Cristina (2004). «Ammonium uptake in the nitrophytic lichen Xanthoria parietina and its effects on vitality and balance between symbionts». The Lichenologist. 36 (1): 75–86. doi:10.1017/S0024282904014124
- ↑ van Herk, C.M. (1999). «Mapping of ammonia pollution with epiphytic lichens in the Netherlands». The Lichenologist. 31 (1): 9–20. doi:10.1006/lich.1998.0138
- ↑ Frati, L.; Santoni, S.; Nicolardi, V.; Gaggi, C.; Brunialti, G.; Guttova, A.; Gaudino, S.; Pati, A.; Pirintsos, S.A.; Loppi, S. (2007). «Lichen biomonitoring of ammonia emission and nitrogen deposition around a pig stockfarm». Environmental Pollution. 146 (2): 311–316. PMID 16777293. doi:10.1016/j.envpol.2006.03.029
- ↑ Olsen, Henrik Brinkmann; Berthelsen, Kasper; Andersen, Helle Vibeke; Søchting, Ulrik (2010). «Xanthoria parietina as a monitor of ground-level ambient ammonia concentrations». Environmental Pollution. 158 (2): 455–461. doi:10.1016/j.envpol.2009.08.025
- ↑ Frahm, Jan-Peter; Janßen, Anne-Maike; Schumacher, Judith; Thönnes, Daniela; Hensel, Stephanie; Heidelbach, Birgit; Erler, David (2009). «Das Nitrophytenproblem bei epiphytischen Flechten – eine Synthese» [The nitrogen problem of epiphytic lichens – a synthesis] (PDF). Archive for Lichenology. 5: 1–8
- ↑ Itten, Beatriz; Honegger, Rosmarie (2010). «Population genetics in the homothallic lichen-forming ascomycete Xanthoria parietina». The Lichenologist. 42 (6): 751–761. doi:10.1017/S0024282910000411

- ↑ Lindblom, Louise (2009). «Sample size and haplotype richness in population samples of the lichen-forming ascomycete Xanthoria parietina». The Lichenologist. 41 (5): 529–535. doi:10.1017/S0024282909008743
- ↑ Dyer, P.S.; Murtagh, G.J. (2001). «Variation in the ribosomal ITS-sequence of the lichens Buellia frigida and Xanthoria elegans from the Vestfold Hills, Eastern Antarctica». The Lichenologist. 33 (2): 151–159. doi:10.1006/lich.2000.0306
- ↑ a b c Werth, Silke (2010). «Population genetics of lichen-forming fungi – a review». The Lichenologist. 42 (5): 499–519. doi:10.1017/S0024282910000125

- ↑ Honegger, Rosmarie; Zippler, Undine; Scherrer, Sandra; Dyer, Paul S. (2004). «Genetic diversity in Xanthoria parietina (L.) Th. Fr. (lichen-forming ascomycete) from worldwide locations». The Lichenologist. 36 (6): 381–390. doi:10.1017/S002428290401477X
- ↑ Wyczanska, Maja; Wacker, Karoline; Dyer, Paul S.; Werth, Silke (2023). «Local-scale panmixia in the lichenized fungus Xanthoria parietina contrasts with substantial genetic structure in its Trebouxia photobionts». The Lichenologist. 55 (2): 69–79. doi:10.1017/S002428292300004X

- ↑ Scherrer, Sandra; Zippler, Undine; Honegger, Rosmarie (2005). «Characterisation of the mating-type locus in the genus Xanthoria (lichen-forming ascomycetes, Lecanoromycetes)». Fungal Genetics and Biology. 42 (12): 976–988. PMID 16266815. doi:10.1016/j.fgb.2005.09.002
- ↑ a b Silberstein, L.; Siegel, B.Z.; Siegel, S.M.; Mukhtar, A.; Galun, M. (1996). «Comparative studies on Xanthoria parietina, a pollution resistant lichen, and Ramalina duriaei, a sensitive species. I. Effects of air pollution on physiological processes». The Lichenologist. 28 (4): 355–365. doi:10.1006/lich.1996.0033
- ↑ Backor, M.; Fahselt, D.; Davidson, R.D.; Wu, C.T. (2003). «Effects of copper on wild and tolerant strains of the lichen photobiont Trebouxia erici (Chlorophyta) and possible tolerance mechanisms». Archives of Environmental Contamination and Toxicology. 45 (2): 159–167. PMID 14565572. doi:10.1007/s00244-002-0134-6
- ↑ Munzi, S.; Cruz, C.; Branquinho, C.; Pinho, P.; Leith, I.D.; Sheppard, L.J. (2014). «Can ammonia tolerance amongst lichen functional groups be explained by physiological responses?». Environmental Pollution. 187: 206–209. PMID 24485905. doi:10.1016/j.envpol.2014.01.009
- ↑ a b Vannini, Andrea; Paoli, Luca; Ceccarelli, Sara; Sorbo, Sergio; Basile, Adriana; Carginale, Vincenzo; Nali, Cristina; Lorenzini, Giacomo; Pica, Mario; Loppi, Stefano (2017). «Physiological and ultrastructural effects of acute ozone fumigation in the lichen Xanthoria parietina: the role of parietin and hydration state». Environmental Science and Pollution Research. 25 (9): 8104–8112. doi:10.1007/s11356-017-9545-9
- ↑ Silberstein, L.; Siegel, B.Z.; Siegel, S.M.; Mukhtar, A.; Galun, M. (1996). «Comparative studies on Xanthoria parietina, a pollution resistant lichen, and Ramalina duriaei, a sensitive species. II. Evaluation of possible air pollution-protection mechanisms». The Lichenologist. 28 (4): 367–383. doi:10.1006/lich.1996.0034
- ↑ Laundon, J.R. (1967). «A study of the lichen flora of London». The Lichenologist. 3 (3): 277–327. doi:10.1017/S0024282967000362
- ↑ Ranwell, D.S. (1968). «Lichen mortality due to 'Torrey Canyon' oil and decontamination measures». The Lichenologist. 4 (1): 55–56. doi:10.1017/S0024282968000071
- ↑ Brown, D.H. (1973). «Toxicity studies on the components of an oil-spill emulsifier using Lichina pygmaea and Xanthoria parietina». Marine Biology. 18 (4): 291–297. doi:10.1007/BF00347791
- ↑ a b Dzubaj, Alexander; Bačkor, Martin; Tomko, Jaroslav; Peli, Evelin; Tuba, Zoltán (2008). «Tolerance of the lichen Xanthoria parietina (L.) Th. Fr. to metal stress». Ecotoxicology and Environmental Safety. 70 (2): 319–326. doi:10.1016/j.ecoenv.2007.04.002
- ↑ Bartók, Katalin (1999). «Pesticide usage and epiphytic lichen diversity in Romanian orchards». The Lichenologist. 31 (1): 21–25. doi:10.1006/lich.1998.0160
- ↑ a b c Brunialti, G.; Frati, L. (2007). «Biomonitoring of nine elements by the lichen Xanthoria parietina in Adriatic Italy: A retrospective study over a 7-year time span». Science of the Total Environment. 387 (1–3): 289–300. PMID 17716704. doi:10.1016/j.scitotenv.2007.06.033
- ↑ Loppi, Stefano; Paoli, Luca; Gaggi, Carlo (2006). «Diversity of epiphytic lichens and Hg contents of Xanthoria parietina thalli as monitors of geothermal air pollution in the Mt. Amiata area (central Italy)». Journal of Atmospheric Chemistry. 53 (2): 93–105. doi:10.1007/s10874-006-6648-y
- ↑ Tsurykau, Andrei; Etayo, Javier (2017). «Capronia suijae (Herpotrichiellaceae, Eurotiomycetes), a new fungus on Xanthoria parietina from Belarus, with a key to the lichenicolous species growing on Xanthoria s. str.». The Lichenologist. 49 (1): 1–12. doi:10.1017/S0024282916000530
- ↑ a b Etayo, Javier; Berger, Franz (2009). «About a fast developing community of lichenicolous deuteromycetes decaying Xanthoria parietina» (PDF). Österreichische Zeitschrift für Pilzkunde. 18: 111–115
- ↑ Freire-Rallo, Sandra; Diederich, Paul; Millanes, Ana M.; Wedin, Mats (2023). «Five new species in the Tremella caloplacae complex». The Lichenologist. 55 (5): 223–239. doi:10.1017/S0024282923000154

- ↑ Fleischhacker, Antonia; Grube, Martin; Frisch, Andreas; Obermayer, Walter; Hafellner, Josef (2016). «Arthonia parietinaria – A common but frequently misunderstood lichenicolous fungus on species of the Xanthoria parietina-group». Fungal Biology. 120 (11): 1341–1353. doi:10.1016/j.funbio.2016.06.009
- ↑ Edwards, Howell G.M.; Seaward, Mark R.D.; Preece, Tom F.; Jorge-Villar, Susana E.; Hawksworth, David L. (2017). «Raman spectroscopic analysis of the effect of the lichenicolous fungus Xanthoriicola physciae on its lichen host». Symbiosis. 71 (1): 57–63. doi:10.1007/s13199-016-0447-2. hdl:10454/10042

- ↑ Baur, Bruno; Baur, Anette (2007). «Xanthoria parietina as a food resource and shelter by the land snail Balea perversa» (PDF). The Lichenologist. 29 (1): 99–102. doi:10.1017/S0024282997000145
- ↑ a b Froberg, Lars; Björn, Lars Olof; Baur, Anette; Baur, Bruno (2001). «Viability of lichen photobionts after passing through the digestive tract of a land snail» (PDF). The Lichenologist. 33 (6): 543–545. doi:10.1006/lich.2001.0355
- ↑ Pyatt, F.B. (1968). «The occurrence of a rotifer on the surfaces of apothecia of Xanthoria parietina». The Lichenologist. 4 (1): 74–75. doi:10.1017/S0024282968000125
- ↑ Zonka, Vincent (2023). Lichens. Toward a Minimal Resistance. Hoboken, New Jersey: Polity Press. p. 205. ISBN 978-1-5095-5345-7
- ↑ a b c Crawford, S. (2019). «Lichens used in traditional medicine». In: Ranković, B. Lichen Secondary Metabolites. Bioactive Properties and Pharmaceutical Potential 2 ed. [S.l.]: Springer Nature Switzerland AG. pp. 31–97. ISBN 978-3-030-16813-1. doi:10.1007/978-3-030-16814-8_2
- ↑ Coppins, B.J.; Watling, Roy (1995). «Lichenized and non-lichenized fungi: folklore and fact». Botanical Journal of Scotland. 47 (2): 249–261. doi:10.1080/03746609508684832
- ↑ Thompson, R. Campbell (1934). «An Assyrian chemist's Vade-mecum». Journal of the Royal Asiatic Society. 66 (4): 771–785. doi:10.1017/S0035869X00112626
- ↑ a b Mendili, Mohamed; Khadhri, Ayda; Sabatini, Francesca; Degano, Ilaria; Aschi-Smiti, Samira (2024). «Parietin, the vibrant natural dye in Xanthoria parietina». Chemistry & Biodiversity. 21 (1): e202301357. doi:10.1002/cbdv.202301357
- ↑ Casselman, Karen Diadick (2001). Lichen Dyes: The New Source Book. Mineola, NY, US: Dover Publications. p. 34. ISBN 978-0-486-41231-3
- ↑ Ali, Sikander; Moazzam, Alisha; Mirza, Saima Shahzad; Mahmood, Majid; Ahmed, Sibtain; Ahmad, Muhammad Usman; Rivera, Gildardo; Asif, Akhtar Rasool; Arshad, Muhammad; Shahzad, Mirza Imran; William, Kaynat; Sharif, Sundas (2025). «Exploring green synthesis of parietin-mediated silver nanoparticles using γ-ray induced Xanthoria parietina foliose extracts for antibacterial potential». Results in Chemistry. 13: e101961. doi:10.1016/j.rechem.2024.101961

- ↑ Bonnier, Gaston (1888). «Germination des spores des lichens sur les protonemas des mousses et sur des algues differentes des gonidies du lichen» [Germination of lichen spores on moss protonemata and on algae different from the lichen gonidia]. Comptes rendus hebdomadaires des séances et mémoires de la Société de biologie. 8 (em francês). 40 (5): 541–543
- ↑ Richardson, D.H.S. (1967). «The transplantation of lichen thalli to solve some taxonomic problems in Xanthoria parietina (L.) Th. Fr.». The Lichenologist. 3 (3): 386–391. doi:10.1017/S0024282967000398
- ↑ Bubrick, P.; Galun, Margalith (1986). «Spore to spore resynthesis of Xanthoria parietina». The Lichenologist. 18 (1): 47–49. doi:10.1017/S0024282986000051
- ↑ a b c Lorenz, Christian; Bianchi, Elisabetta; Poggiali, Giovanni; Alemanno, Giulia; Benesperi, Renato; Brucato, John Robert; Garland, Stephen; Helbert, Jörn; Loppi, Stefano; Lorek, Andreas; Maturilli, Alessandro; Papini, Alessio; de Vera, Jean-Pierre; Baqué, Mickaël (2023). «Survivability of the lichen Xanthoria parietina in simulated Martian environmental conditions». Scientific Reports. 13 (1): e4893. PMC 10039903
 . PMID 36966209. doi:10.1038/s41598-023-32008-6
. PMID 36966209. doi:10.1038/s41598-023-32008-6
- ↑ Lorenz, Christian; Bianchi, Elisabetta; Benesperi, Renato; Loppi, Stefano; Papini, Alessio; Poggiali, Giovanni; Brucato, John Robert (2022). «Survival of Xanthoria parietina in simulated space conditions: vitality assessment and spectroscopic analysis». International Journal of Astrobiology. 21 (3): 137–153. doi:10.1017/S1473550422000076
 . hdl:2158/1281253
. hdl:2158/1281253
- ↑ a b Lorenz, Christian; Arena, Carmen; Vitale, Ermenegilda; Bianchi, Elisabetta; Poggiali, Giovanni; Alemanno, Giulia; Benesperi, Renato; Brucato, John Robert; Garland, Stephen; Helbert, Jörn; Loppi, Stefano; Lorek, Andreas; Maturilli, Alessandro; Papini, Alessio; de Vera, Jean-Pierre; Baqué, Mickaël (2024). «Resilience of Xanthoria parietina under Mars-like conditions: photosynthesis and oxidative stress response» (PDF). Planta. 259 (1): e25. doi:10.1007/s00425-023-04290-1