Fungo liquenícola
_Arnold_624105.jpg)
Um fungo liquenícola é um membro de um grupo especializado de fungos que vivem exclusivamente em líquens como seus organismos hospedeiros. Esses fungos, que abrangem mais de 2.000 espécies conhecidas distribuídas em 280 gêneros, exibem uma ampla gama de estratégias ecológicas, incluindo parasitismo, comensalismo e mutualismo. Eles podem ser encontrados em diversos ambientes ao redor do mundo, desde regiões tropicais até polares, desempenhando papéis importantes na ecologia dos líquens e na biodiversidade. Os fungos liquenícolas são classificados em vários grupos taxonômicos, com a maioria pertencendo aos Ascomycota e uma menor proporção aos Basidiomycota. Suas interações com os líquens hospedeiros variam de parasitismo leve a patogenicidade severa, às vezes causando danos significativos às comunidades de líquens.
Embora o estudo dos fungos liquenícolas remonte ao século XVIII, as últimas décadas testemunharam avanços significativos por meio de métodos modernos de pesquisa, incluindo técnicas moleculares, metagenômica e imagem avançada. Esses fungos apresentam diferentes níveis de especificidade ao hospedeiro, com algumas espécies restritas a um único gênero ou espécie de líquen, enquanto outras podem colonizar múltiplos hospedeiros. Um subgrupo único, conhecido como líquens liquenícolas, inicia seu ciclo de vida como parasitas, mas eventualmente se torna liquenizado por meio de um processo chamado cleptossimbiosis. Fatores ecológicos e ambientais, como altitude, disponibilidade de micro-habitats e especificidade ao hospedeiro, influenciam a diversidade e a distribuição dos fungos liquenícolas.
O estudo dos fungos liquenícolas apresenta desafios únicos devido ao seu tamanho microscópico e à associação íntima com seus hospedeiros. Os pesquisadores utilizam diversos métodos, desde técnicas tradicionais de cultura até abordagens moleculares avançadas. O isolamento e o cultivo desses fungos podem ser difíceis, frequentemente exigindo meios de cultura especializados e condições de crescimento específicas. Métodos moleculares revolucionaram o campo, permitindo identificação e análise filogenética mais precisas. No entanto, distinguir hifas estranhas dentro do talo do líquen do micobionte propriamente dito (o componente fúngico do líquen) permanece um desafio significativo.
Pesquisas recentes ampliaram o entendimento sobre os fungos liquenícolas, particularmente em grupos como mucoromicetos e o gênero Cladophialophora. Esses estudos não apenas revelaram novas espécies, mas também destacaram o potencial dos líquens como refúgios para organismos fúngicos especializados. Avanços nas técnicas de isolamento, cultivo e análises moleculares avançaram significativamente o campo.
Definição e características
Os fungos liquenícolas são um grupo especializado de fungos que vivem exclusivamente em líquens como seus organismos hospedeiros. O termo "liquenícola" vem do latim, com "líquen" referindo-se ao hospedeiro e "cola" significando "habitante".[1] Esses fungos são distintos do componente fúngico dos próprios líquens, que são conhecidos como fungos liquenizados.[2] O estudo dos fungos liquenícolas remonta ao século XVIII, antes do reconhecimento dos líquens como organismos simbióticos.[3]
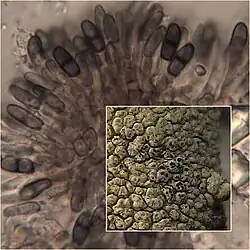
Os fungos liquenícolas representam um grupo altamente diverso, com mais de 2.000 espécies conhecidas em 280 gêneros, refletindo uma ampla gama de estratégias ecológicas e relações com seus hospedeiros líquens. Em 1981, já estimava-se que poderia haver até 300 gêneros e 1.000 espécies de fungos liquenícolas.[3] Essas relações variam amplamente, incluindo parasitismo, onde o fungo prejudica o líquen; comensalismo, onde o fungo se beneficia sem afetar o líquen; e mutualismo, onde ambos os organismos se beneficiam.[1] Os talos dos líquens fornecem um habitat complexo e variado para os fungos liquenícolas, caracterizado por gradientes biológicos que variam de partes em crescimento ativo a partes em decomposição. Essa diversidade dentro de um único talo cria um espectro de microambientes, que podem contribuir para a diversificação das estratégias de vida fúngica. Por exemplo, certos fungos associados a líquens especializam-se em colonizar camadas epinecrais ou epicórtex, estruturas sem células hospedeiras vivas. Outros preferem partes em decomposição dos líquens, conectando estilos de vida necróticos a saprófitos. A presença desses gradientes biológicos dentro dos talos dos líquens pode atuar como um catalisador para a evolução e adaptação dos fungos liquenícolas, potencialmente explicando a ampla gama de relações ecológicas observadas, do comensalismo ao parasitismo. Essa complexidade no habitat dos líquens levou alguns pesquisadores a sugerirem que os líquens podem servir como um "berço" para a evolução fúngica, promovendo o desenvolvimento de diversas estratégias de vida fúngica.[4]
Alguns fungos liquenícolas são patogênicos, enquanto outros são saprófitos, decompondo tecidos mortos de líquens. Alguns fungos liquenícolas eventualmente se tornam liquenizados, integrando-se à estrutura do líquen.[1] Os fungos liquenícolas podem ser não-liquenizados ou liquenizados, obrigatórios ou facultativos, e podem ou não induzir sintomas no hospedeiro.[5] Eles fazem parte do complexo microbioma [en] associado aos líquens, que inclui bactérias, algas e outros fungos.[6]
Os basidiomicetos liquenícolas, que representam cerca de 5% de todos os fungos liquenícolas conhecidos até 2018, incluem tanto homobasidiomicetos quanto heterobasidiomicetos.[7] Os homobasidiomicetos geralmente possuem basídios (estruturas produtoras de esporos) sem septos (partições internas) e basidiomas não gelatinosos, enquanto os heterobasidiomicetos possuem basídios septados e basidiomas gelatinosos.[7]
Morfológicamente, os fungos liquenícolas podem assumir formas diversas. Eles podem produzir esporocarpos visíveis na superfície do líquen hospedeiro ou existir como hifas dentro do talo do hospedeiro. Algumas espécies podem causar estruturas semelhantes a galhas ou outras deformações em seus hospedeiros.[3]
Até 2018, havia 2.319 espécies reconhecidas de fungos liquenícolas, incluindo cerca de 1.250 espécies de ascomicetos liquenícolas em 280 gêneros e 62 espécies de basidiomicetos liquenícolas em 10 gêneros.[8] Eles podem ser categorizados em três grupos principais:[8]
- Espécies obrigatoriamente liquenícolas (2.000 táxons)
- Líquens liquenícolas (257 táxons)
- Táxons facultativamente liquenícolas (62 táxons)
Avanços nas técnicas moleculares e maior exploração aumentaram significativamente a diversidade conhecida de basidiomicetos liquenícolas, quase dobrando a contagem de espécies de 2018 a 2022.[7]
Diversidade e classificação
A diversidade conhecida de fungos liquenícolas aumentou significativamente nos últimos anos. Esse crescimento reflete um ressurgimento do interesse em fungos liquenícolas no final do século XX.[3] Por exemplo, Clauzade e Roux compilaram 457 espécies em 1976,[9] número que aumentou para 686 espécies até 1989.[10] Em 1997, havia 894 espécies obrigatoriamente liquenícolas aceitas. Até 2018, esse número cresceu para mais de 1.800,[8] com uma taxa rápida de descoberta. Cerca de 1.170 táxons infragenéricos foram adicionados desde 1990.[5]
Os basidiomicetos liquenícolas, um grupo diverso dentro dos Basidiomycota, são encontrados principalmente nas subdivisões Agaricomycotina e Pucciniomycotina. Essas subdivisões abrangem uma ampla gama de formas fúngicas, incluindo aquelas que produzem esporocarpos complexos e também formas mais simples, frequentemente parasitas.[7]
Dentro da Agaricomycotina, as espécies liquenícolas estão presentes em duas classes. Nos Agaricomycetes, as espécies liquenícolas são encontradas em cinco ordens: Agaricales, Atheliales, Boletales, Cantharellales e Corticiales. Nos Tremellomycetes, as espécies liquenícolas são encontradas em duas de suas cinco ordens: Filobasidiales e Tremellales. Dentro da Pucciniomycotina, as espécies liquenícolas são encontradas em três classes: Agaricostilbomycetes, Cystobasidiomycetes e Microbotryomycetes.[7]
Até 2018, havia 93 espécies conhecidas de basidiomicetos liquenícolas (mais 7 táxons facultativamente liquenícolas).[8] Estudos publicados desde então relataram a descoberta de muitas novas espécies e até novos gêneros. Até 2022, o número de espécies conhecidas quase dobrou, chegando a quase 200.[7] Para contextualizar essa diversidade, as estimativas de 300 gêneros e 1.000 espécies de fungos liquenícolas (em 1981) podem ser comparadas com os 150 gêneros e 700 espécies de Gasteromycetes, ou 90 gêneros e 600 espécies de Pezizales.[3]

A descrição do novo gênero Crittendenia em Pucciniomycotina representa um desenvolvimento taxonômico significativo, pois redefine a classificação de várias espécies parasitas específicas de hospedeiros anteriormente colocadas em Chionosphaera.[13] Outro avanço é o reconhecimento de vários complexos de espécies, como Syzygospora physciacearum e Tremella parmeliarum [en], que foram divididos em várias espécies distintas, frequentemente com alta especificidade ao hospedeiro.[7]
As espécies liquenícolas também são encontradas entre os fungos negros, um grupo caracterizado por micélios de cor escura devido à melanina em suas paredes celulares. Esses fungos, conhecidos por sua capacidade de colonizar habitats extremos, incluindo talos de líquens, são representados pelo gênero Cladophialophora. Em 2023, nove novas espécies de Cladophialophora foram descritas a partir de líquens coletados na China, exemplificando a descoberta contínua de novos fungos liquenícolas. Essas espécies foram isoladas dos tecidos medulares de vários hospedeiros líquens, sugerindo potenciais relações biotróficas ou comensais. Cladophialophora representa uma linhagem significativa de fungos liquenícolas, com muitas espécies provavelmente ainda por serem descobertas. Esta pesquisa destaca a diversidade dos fungos liquenícolas e o papel dos líquens como refúgios para esses organismos especializados.[14]
Uma análise biológica dos gêneros de fungos liquenícolas revela tendências distintas. Uma proporção significativa de gêneros com representantes liquenícolas é exclusivamente liquenícola, enquanto outros incluem espécies saprófitas ou formadoras de líquens. Por exemplo, entre os Hyphomycetes liquenícolas, 43% dos gêneros são restritos a líquens, enquanto para os Coelomycetes liquenícolas, esse número sobe para 75%.[3]
Embora o número de espécies conhecidas de basidiomicetos liquenícolas tenha aumentado significativamente nos últimos anos, acredita-se que muitas espécies ainda não foram descobertas. Essas estimativas são baseadas em análises de especificidade ao hospedeiro, lacunas de conhecimento atuais e a taxa de descoberta de novas espécies. O número real de espécies pode ser ainda maior, especialmente em regiões e grupos taxonômicos pouco explorados.[7] Alguns pesquisadores estimam que o número total de espécies de fungos liquenícolas pode potencialmente atingir 3.000.[5]
Taxonomia e nomenclatura
A taxonomia e a nomenclatura dos fungos liquenícolas mudaram significativamente com a adoção do princípio "um fungo – um nome" no Código Internacional de Nomenclatura para Algas, Fungos e Plantas (Código de Melbourne). Este princípio tem implicações importantes para a classificação e nomeação de fungos liquenícolas.[5] Sob as novas regras, todos os nomes fúngicos legítimos são tratados igualmente para estabelecer prioridade, independentemente do estágio do ciclo de vida. Essa mudança é significativa para os fungos liquenícolas, pois muitas espécies foram anteriormente descritas separadamente em seus estados sexuais (teleomorfos) e assexuais (anamorfo).[5]
A implementação desse princípio levou a várias mudanças taxonômicas. Quando teleomorfos e anamorfos geneticamente idênticos possuem nomes diferentes, o nome mais antigo tem prioridade, a menos que o nome mais recente seja conservado. Para espécies conhecidas apenas em seu estado anamórfico, se o teleomorfo é descoberto, a espécie é descrita ou combinada no gênero teleomórfico apropriado, mesmo que os caracteres teleomórficos não sejam mencionados. Espécies anamórficas reconhecidas como não descritas são agora colocadas em gêneros teleomórficos quando sua posição filogenética é conhecida, em vez de em gêneros anamórficos separados.[5]
Essas mudanças reorganizaram vários grupos de fungos liquenícolas. Por exemplo, o gênero Vouauxiomyces, que incluía anamorfos de espécies de Abrothallus, foi reduzido a sinônimo de Abrothallus.[5] Vários fungos liquenícolas semelhantes a Phoma [en] foram descobertos como pertencentes a várias linhagens dentro dos Dothideomycetes e foram reclassificados de acordo. Por exemplo, algumas espécies anteriormente colocadas em Phoma são agora reconhecidas como membros de Didymocyrtis na Phaeosphaeriaceae.[5]
Essas mudanças taxonômicas e nomenclaturais apresentam desafios, mas também oportunidades para uma classificação mais precisa e filogeneticamente informada dos fungos liquenícolas. No entanto, é necessária cautela ao descrever novos gêneros, pois nomes podem já existir em sinonímia genérica tradicional.[5]
Ecologia e relações com o hospedeiro

Os fungos liquenícolas exibem diversas relações ecológicas com seus hospedeiros líquens, variando de parasitismo prejudicial a comensalismo neutro e interações potencialmente benéficas (mutualísticas). A especificidade ao hospedeiro, as condições ambientais e a adaptabilidade fúngica moldam coletivamente essas relações. Embora muitos fungos liquenícolas sejam parasitas, outros estabelecem relações comensais ou potencialmente mutualísticas. Algumas espécies, os líquens liquenícolas, podem até desenvolver seus próprios talos liquenizados usando o fotobionte do líquen hospedeiro.[8] Certos fungos liquenícolas podem desempenhar papéis importantes na ciclagem de nutrientes dentro do talo do líquen, potencialmente beneficiando o hospedeiro ao degradar e reciclar partes mais antigas do líquen.[6] Além disso, esses fungos podem estar envolvidos na decomposição de matéria orgânica morta, contribuindo para a dinâmica geral de nutrientes da comunidade de líquens. A extensão e a significância dessas funções ecológicas potenciais ainda estão sendo investigadas, mas destacam as relações complexas e potencialmente mutualísticas que podem existir entre fungos liquenícolas e seus hospedeiros líquens. Essas descobertas sugerem que o impacto ecológico dos fungos liquenícolas pode ser mais nuançado e potencialmente benéfico do que anteriormente compreendido, contribuindo para a saúde e longevidade das comunidades de líquens em diversos ambientes.[4]
Tipos de relações ecológicas
Os fungos liquenícolas podem ser amplamente classificados em dois tipos principais com base em seu impacto no hospedeiro:[15]
- Necrotróficos: Esses fungos têm um efeito devastador sobre o micobionte do líquen (micoparasitas), o fotobionte (parasitas de algas) ou ambos.
- Habitantes não destrutivos: Esses fungos esporulam abundantemente sem causar danos significativos ao parceiro fúngico ou fotoautotrófico do talo hospedeiro. Embora às vezes chamados de parassimbiontes ou comensais, são melhor considerados como parasitas leves, pois ainda consomem nutrientes do talo.
Especificidade ao hospedeiro e distribuição
.jpg)
A especificidade ao hospedeiro é um fator crucial na distribuição e ecologia dos fungos liquenícolas. Estima-se que 95% das espécies se associem a apenas uma única espécie ou gênero de líquen, sugerindo potenciais relações coevolutivas.[15] Esse alto grau de especificidade tem implicações evolutivas significativas, indicando adaptações de longo prazo entre fungos e seus hospedeiros líquens. No entanto, o alcance da especificidade ao hospedeiro pode variar muito entre os fungos liquenícolas. Embora muitos sejam altamente específicos, outros podem colonizar várias espécies de líquens não relacionadas.[3]
Os diferentes níveis de especificidade ao hospedeiro têm implicações evolutivas importantes. Parasitas altamente específicos correm o risco de coextinção com seus hospedeiros, enquanto generalistas podem ter perspectivas de longo prazo mais estáveis. Isso pode explicar por que é incomum que um único gênero de fungos liquenícolas inclua mais de uma espécie que ataca um líquen hospedeiro específico. Quando isso ocorre, os sintomas são frequentemente distintos, possivelmente refletindo diferentes estratégias ecológicas.[3]
Dentro de um único gênero, uma espécie pode ser parasitária em um hospedeiro, enquanto outra é parassimbionte no mesmo hospedeiro. Essa variação nas relações, mesmo entre espécies estreitamente relacionadas, destaca a natureza complexa da ecologia dos fungos liquenícolas.[3]
Estudos moleculares sugerem que alguns fungos liquenícolas podem ter faixas de hospedeiros mais amplas do que se pensava anteriormente com base apenas em observações morfológicas. Algumas espécies foram encontradas em líquens assintomáticos ou até em espécies de líquens não conhecidas anteriormente por abrigar esses fungos.[8]
Hiperparasitismo
Os fungos liquenícolas também podem estar envolvidos em casos complexos de hiperparasitismo, onde ocorrem múltiplos níveis de relações parasitárias. Em alguns casos, fungos não liquenizados podem parasitar líquens liquenícolas. Por exemplo, espécies como Stigmidium arthrorhaphidis, Cercidospora trypetheliza e C. soror foram observadas infectando Arthrorhaphis citrinella, que por sua vez cresce parasiticamente em Baeomyces, escamulas de Cladonia [en] ou líquens em decomposição. Relações ainda mais intricadas existem onde líquens se desenvolvem hiperparasitariamente em líquens liquenícolas. Um exemplo é Rhizocarpon diploschistidina, que parasita Diploschistes muscorum, um líquen liquenícola que inicialmente parasita espécies de Cladonia. Essas relações parasitárias de múltiplos níveis destacam a complexa rede ecológica que pode se desenvolver dentro das comunidades de líquens.[4]
Distribuição
A distribuição dos fungos liquenícolas é influenciada por vários fatores ecológicos e ambientais. Por exemplo, a montanha Koralpe, na Áustria, com suas condições estáveis e variedade de micro-habitats, suporta uma alta diversidade de líquens e fungos liquenícolas. A presença de rochas expostas e falésias fornece numerosos micro-nichos para esses fungos explorarem, desde o córtex externo até a medula interna dos talos dos líquens.[16]
Em regiões alpinas e polares, a estabilidade e longevidade dos talos dos líquens proporcionam micro-habitats consistentes, permitindo que os fungos liquenícolas estabeleçam populações de longo prazo. Essas condições ambientais contribuem para os padrões observados de diversidade beta – a variação na composição de espécies entre diferentes habitats. Pesquisas na área da montanha Koralpe revelaram alta diversidade beta devido a numerosas condições microambientais que suportam várias espécies fúngicas. A diversidade alfa (diversidade dentro de sub-parcelas) foi encontrada como maior que a diversidade beta (diversidade dentro de parcelas), indicando uma diferenciação significativa de habitats mesmo em áreas pequenas.[16]
Fatores ambientais, como a poluição, também podem influenciar a distribuição dos fungos liquenícolas, afetando tanto os líquens quanto seus fungos associados. Isso pode levar a mudanças nas comunidades de líquens e fungos liquenícolas em resposta a alterações ambientais.[3]
Efeitos nos líquens hospedeiros

O impacto dos fungos liquenícolas em seus hospedeiros varia amplamente, desde efeitos menores e localizados até danos extensos ou até mesmo a morte do líquen hospedeiro. Esses efeitos podem se manifestar de várias formas, incluindo descolorações, danos ao talo e malformações semelhantes a galhas.
Descolorações
Os fungos liquenícolas podem causar diferentes tipos de descolorações em seus líquens hospedeiros. Essas podem aparecer como manchas necróticas acastanhadas ou esbranquiçadas, com a extensão e o padrão de descoloração frequentemente dependendo da interação específica fungo-hospedeiro. Por exemplo, Nectriella tincta em Anaptychia fusca e Nesolechia oxyspora em Parmelia saxatilis podem causar branqueamento extenso do talo. Descolorações acastanhadas são características de outras espécies, como aquelas causadas por Lichenoconium echinosporum em Heterodea muelleri.[3]
Alguns fungos podem causar descolorações extensas quando desenvolvidos luxuriantemente. Um exemplo marcante é Xanthoriicola physciae em Xanthoria parietina, que pode conferir ao hospedeiro uma aparência salpicada de fuligem e potencialmente reduzir sua área fotossintética ao ponto de morte local.[3]
Em contrapartida, outros fungos liquenícolas têm efeitos muito localizados. Por exemplo, algumas espécies afetam apenas os apotécios (esporocarpos) de seus hospedeiros, como Vouauxiella lichenicola e V. verrucosa em espécies de Lecanora de esporocarpos vermelhos, o que pode resultar em uma aparência malhada dos discos apoteciais.[3]
Danos ao talo
Alguns fungos liquenícolas podem causar danos significativos aos seus líquens hospedeiros. Por exemplo, o patógeno de amplo espectro Athelia arachnoidea é conhecido por causar danos extensos em comunidades de líquens europeias, particularmente aquelas afetadas pela poluição do ar.[8] Esta espécie, juntamente com outras como Erythricium aurantiacum, Marchandiomyces corallinus e Parmeliicida pandemica, pode danificar gravemente ou matar populações inteiras de líquens.[7] Em um caso documentado, Lecanora conizaeoides se recuperou de uma infecção parasitária por Licheniconium lecanorae. O líquen conseguiu isso por meio de um crescimento vigoroso na margem do apotécio, que efetivamente enterrou tanto o himênio danificado quanto os picnídios do parasita dentro de seu talo.[17]
Malformações semelhantes a galhas

Um grupo significativo de fungos liquenícolas são os táxons cecidogênicos (indutores de galhas). Aproximadamente 40 espécies de ascomicetos e basidiomicetos liquenícolas são conhecidas por induzir formações de galhas em seus talos hospedeiros, muitas vezes de maneira específica para a espécie. Alguns desses fungos estimulam o crescimento tanto do micobionte quanto do fotobionte, embora os mecanismos exatos não sejam completamente compreendidos, enquanto outros parasitam apenas o fotobionte.[3][15]
As malformações semelhantes a galhas podem assumir várias formas, desde inchaços leves até estruturas complexas. Por exemplo, Lichenomyces lichenum forma galhas semelhantes a apotécios estipitados em espécies de Lobaria [en] e Pseudocyphellaria, às vezes até com margens talinas.[3] A formação de galhas por fungos liquenícolas exibe considerável diversidade em estrutura e padrões de desenvolvimento. Essas estruturas induzidas por fungos podem criar micro-habitats complexos, frequentemente iniciando uma sucessão ecológica intricada de vários organismos dentro da galha. Por exemplo, estudos histoquímicos detalhados de infecções por Biatoropsis usnearum em talos de Usnea [en] revelaram que o processo de infecção se inicia na camada cortical do hospedeiro. À medida que a galha se desenvolve, o parasita forma haustórios tremeloides, principalmente na parte central das galhas maduras. Essas galhas totalmente desenvolvidas podem então servir como micro-habitats para outros colonizadores de líquens, como espécies do gênero Cyphobasidium.[4]
As malformações semelhantes a galhas em líquens não são sempre causadas por fungos. Outros organismos, como ácaros (Acari, Eriophyoidea) e nematóides, também podem induzir a formação de galhas em líquens, adicionando complexidade às interações líquen-microrganismo.[3]
Os efeitos dos fungos liquenícolas em seus hospedeiros podem ser influenciados por vários fatores, incluindo as espécies envolvidas, as condições ambientais e a saúde do líquen hospedeiro. Alguns homobasidiomicetos, como Athelia arachnoidea, mostram picos sazonais em seu desenvolvimento e podem sobreviver como pequenos esclerócios ou bulbílios em cascas de árvores ou musgos após matar seus hospedeiros líquens, parecendo ter um estilo de vida facultativamente liquenícola.[7]
Adaptações e transições de estilo de vida
Os fungos liquenícolas demonstram uma notável adaptabilidade em suas estratégias ecológicas. Embora muitos sejam exclusivamente liquenícolas, algumas espécies podem transitar entre diferentes estilos de vida. Por exemplo, Chaenothecopsis consociata (Mycocaliciales) geralmente invade talos de Chaenotheca chrysocephala (Caliciaceae, Lecanorales), mas também pode se associar a Dictyochloropsis symbiontica para formar seu próprio talo crostoso. Da mesma forma, Athelia arachnoidea é necrotrófica em vários táxons de líquens, algas livres e briófitas, mas também foi identificada como o estado sexual de Rhizoctonia carotae, uma doença pós-colheita de cenouras.[15]
Líquens liquenícolas
Os líquens liquenícolas, um subgrupo de fungos liquenícolas, começam como parasitas em outros líquens e eventualmente se tornam liquenizados. Esse processo, chamado cleptossimbiose, envolve o fungo adquirir fotobiontes do seu líquen hospedeiro. Diploschistes muscorum exemplifica esse fenômeno.[18] Os líquens liquenícolas são relativamente comuns; um estudo na Itália descobriu que 189 de 3.005 espécies liquenizadas (cerca de 6%) eram liquenícolas.[19]
Esses líquens apresentam características biológicas e ecológicas distintas. Eles são predominantemente crostosos, possuem principalmente algas verdes não trentepoiloides [en] como fotobiontes e reproduzem-se principalmente sexualmente. Ecologicamente, tendem a ocupar nichos específicos, sendo em sua maioria saxícolas (crescendo em rochas) e preferindo habitats secos e bem iluminados em várias altitudes. Essa preferência pode explicar sua estratégia de "roubar" fotobiontes, possivelmente uma adaptação a ambientes hostis onde formar novas simbioses é desafiador.[19] Os líquens liquenícolas podem ter seu componente algal posicionado de duas maneiras: internamente dentro do líquen hospedeiro ou externamente como talos distintos na superfície do hospedeiro.[20] Um exemplo do primeiro caso é Tetramelas pulverulentus, que cresce em Physconia distorta.[21] Em contrapartida, Erichansenia epithallina foi documentada crescendo na superfície de mais de uma dúzia de espécies de líquens hospedeiros diferentes.[22]
Embora frequentemente chamados de "parasitas", muitos líquens liquenícolas não se encaixam estritamente nessa definição, pois eventualmente desenvolvem seu próprio talo.[19] O verdadeiro parasitismo ocorre frequentemente em líquens liquenícolas dos gêneros Acarospora [en], Diploschistes [en], Rhizocarpon [en] e Verrucaria [en].[20] Pesquisadores sugerem que os líquens liquenícolas conhecidos são apenas uma pequena parte do total, e que essa estratégia pode ser mais difundida do que atualmente reconhecido. Estudos adicionais de sequenciamento de DNA poderiam revelar mais espécies de líquens liquenícolas, variando de formas obrigatórias a facultativas.[19]
|
Distribuição geográfica

Os basidiomicetos liquenícolas estão distribuídos globalmente, habitando diversos ambientes em todos os continentes. Sua presença varia desde os trópicos até regiões polares, demonstrando sua notável adaptabilidade. Descobertas recentes estendem-se até os climas rigorosos da Antártida, demonstrando os amplos nichos ecológicos que esses fungos ocupam. O conhecimento atual de sua distribuição é fortemente influenciado pelos diferentes níveis de exploração e pesquisa em diferentes regiões. Europa, América do Norte e, em menor grau, América do Sul parecem ser as regiões mais bem exploradas. No entanto, isso pode refletir o esforço de pesquisa em vez da diversidade real. Por exemplo, enquanto a Europa tem menos espécies conhecidas do que a América do Norte, ela tem uma proporção menor de espécies recém-descritas, sugerindo que pode estar mais completamente estudada. A América do Sul, apesar de ter um número significativo de espécies conhecidas, é considerada subexplorada. Estudos sistemáticos de fungos liquenícolas nesta região começaram apenas por volta de 2000, e especialistas preveem um aumento substancial na diversidade conhecida nos próximos anos. África e grande parte da Ásia permanecem pouco exploradas para basidiomicetos liquenícolas, e os números atuais de espécies conhecidas provavelmente sub-representam a verdadeira diversidade nessas regiões. Da mesma forma, embora a Oceania tenha um número moderado de espécies conhecidas, a maioria das descobertas foi incidental, e explorações completas na Austrália e Nova Zelândia devem revelar mais muitas espécies.[7]
Estudos mostraram que habitats naturais e não poluídos, como regiões alpinas, suportam uma alta diversidade de fungos liquenícolas. Por exemplo, a área da montanha Koralpe, na Áustria, abriga numerosas espécies devido às suas condições ambientais estáveis e à variedade de micro-habitats. Um estudo conduzido nesta região identificou 63 espécies de líquens e 41 espécies de fungos liquenícolas em uma área relativamente pequena, ilustrando a rica biodiversidade dessas comunidades.[16]
A diversidade de fungos liquenícolas não é uniformemente distribuída em todos os ambientes. Habitats que permaneceram não poluídos e estáveis por longos períodos são particularmente ricos nesses fungos. Em regiões como Hungria, Índia e partes do Holártico, incluindo América do Norte, Rússia e Suécia, listas nacionais documentaram numerosas espécies de fungos liquenícolas. Essas listas, baseadas no reconhecimento morfológico detalhado de amostras ambientais, mostram a diversidade de espécies em diferentes ambientes e em diferentes hospedeiros líquens.[16]
_am_Ausl%C3%A4ufer_der_Koralpe%252C_K%C3%A4rnten.jpg)
Além disso, regiões alpinas e polares, que serviram como refúgios durante eventos climáticos passados, também mostram alta diversidade de fungos liquenícolas. A estabilidade e longevidade dos talos dos líquens nessas regiões criam nichos adequados para comunidades fúngicas diversas. Por exemplo, as comunidades de líquens alpinos da montanha Koralpe, na Áustria, que é uma área de nunatak, suportam uma diversidade excepcionalmente rica de espécies de líquens devido aos variados micro-habitats fornecidos pelos afloramentos de gnaisse e mármore espalhados pela paisagem.[16]
A abordagem de análise entre táxons mostrou que a abundância e diversidade de líquens influenciam significativamente os padrões de diversidade dos fungos liquenícolas. Este método demonstrou que as comunidades de líquens podem servir como indicadores confiáveis para prever a diversidade de fungos liquenícolas, auxiliando na conservação e estudo desses fungos especializados.[16]
Aspectos evolutivos
As relações evolutivas entre líquens e fungos liquenícolas oferecem esclarecimentos sobre o desenvolvimento de simbioses e parasitismo fúngicos. Embora nem todos os aspectos de sua coevolução sejam completamente compreendidos, várias tendências e padrões foram observados que esclarecem os processos evolutivos em jogo.
Coevolução de líquens e fungos liquenícolas
O alto grau de especificidade ao hospedeiro observado em muitos fungos liquenícolas sugere uma longa história de coevolução com seus hospedeiros líquens. Essa relação coevolutiva provavelmente levou ao desenvolvimento de adaptações especializadas tanto nos fungos liquenícolas quanto em seus hospedeiros. No entanto, a trajetória evolutiva nem sempre é direta, como evidenciado pela existência de espécies generalistas que podem colonizar múltiplos hospedeiros líquens não relacionados.[3]
A evolução dos fungos liquenícolas parece favorecer estratégias que garantem a sobrevivência a longo prazo sem eliminar a população hospedeira. Isso é refletido no número relativamente baixo de fungos liquenícolas altamente patogênicos em comparação com aqueles que estabelecem relações mais estáveis e menos destrutivas com seus hospedeiros. Essa estratégia evolutiva faz sentido, pois fungos que matam rapidamente seus hospedeiros correm o risco de sua própria extinção se forem altamente específicos ao hospedeiro.[3]
Tendências no alcance do hospedeiro e desenvolvimento de sintomas
Dentro de gêneros de fungos liquenícolas foram observadas tendências interessantes em termos de alcance do hospedeiro e os sintomas que produzem. É relativamente incomum que um único gênero inclua mais de uma espécie que ataque um líquen hospedeiro específico. Quando isso ocorre, os sintomas produzidos por cada espécie são quase invariavelmente distintos. Essa diferenciação nos sintomas pode representar adaptações evolutivas para explorar diferentes nichos dentro do mesmo hospedeiro, reduzindo a competição direta entre espécies estreitamente relacionadas.[3]
Por exemplo, dentro do gênero Lichenoconium, L. lecanorae faz com que os discos apoteciais de Lecanora conizaeoides fiquem enegrecidos, enquanto o talo mantém sua cor normal. Em contrapartida, L. erodens causa uma leve descoloração dos discos apoteciais do mesmo hospedeiro e extensas lesões esbranquiçadas no talo. Essa diferenciação nos sintomas permite que ambas as espécies coexistam na mesma espécie hospedeira ao explorar diferentes partes do talo do líquen.[3]
Outra tendência evolutiva observada é a tendência de, em um gênero, uma espécie ser parassimbionte e outra ser parasitária em um mesmo hospedeiro. Por exemplo, Corticifraga peltigerae é parasitária em talos de Peltigera, formando manchas circulares clareadas, enquanto Corticifraga fuckelii é aparentemente parassimbionte no mesmo hospedeiro. Isso sugere que, mesmo dentro de um único gênero, diferentes espécies podem desenvolver graus variados de patogenicidade ou mutualismo com seus hospedeiros.[3]
História da pesquisa
O estudo dos fungos liquenícolas remonta ao século XVIII, antes do reconhecimento dos líquens como organismos simbióticos. No entanto, o campo viu um crescimento e desenvolvimento significativos nas últimas décadas.[8]
Observações iniciais

Uma das primeiras observações documentadas de um fungo liquenícola foi Biatoropsis usnearum [en], um heterobasidiomiceto que forma estruturas semelhantes a galhas em talos de Usnea. Johann Jakob Dillenius ilustrou esse fenômeno em sua obra de 1742, Historia Muscorum. Erik Acharius discutiu e ilustrou espécimes de Usnea infectados por B. usnearum em 1795.[24] Em 1810, Acharius publicou ilustrações coloridas detalhadas distinguindo entre apotécios normais em forma de disco e as estruturas nodulares e protuberantes que ele chamou de cefalódios em Usnea.[25] Esses "cefalódios" são agora reconhecidos como os basidiomas de Biatoropsis usnearum.[26]
Séculos XIX e XX
O século XIX viu um aumento na descrição de espécies de fungos liquenícolas. William Lauder Lindsay apresentou a primeira visão geral do grupo em 1869. Friedrich Wilhelm Zopf forneceu uma lista de hospedeiros líquens e seus fungos associados em 1896.[27] Vários pesquisadores fizeram contribuições significativas durante esse período, preparando relatos críticos ilustrados detalhados da taxonomia e biologia de espécies selecionadas. Trabalhos notáveis incluem os de Charles Tulasne (1852), William Lauder Lindsay (1869),[28] e Friedrich Wilhelm Zopf (1897). Henri Olivier forneceu um relato detalhado dos fungos liquenícolas da França (1905–1907), enquanto Léon Vouaux publicou uma flora mundial com chaves e descrições de todas as espécies conhecidas (1912–1914).[29][30][31] Karl von Keissler revisou as espécies da Europa Central em 1930.[3][4][24]
No início do século XX, Werner e seus colaboradores realizaram investigações biológicas e de desenvolvimento em algumas espécies, contribuindo para o conhecimento sobre fungos liquenícolas.[3] Apesar do interesse inicial, os fungos liquenícolas foram frequentemente negligenciados devido à sua natureza discreta e ao conhecimento especializado necessário para estudá-los. Isso levou a um período de relativa negligência em meados do século XX.[3] O estudo desses organismos era desafiador, pois os pesquisadores precisavam de expertise em micologia e liquenologia para identificar e caracterizar com precisão.
Era moderna
Um ressurgimento do interesse em fungos liquenícolas ocorreu no final do século XX. Georges Clauzade e Claude Roux compilaram 457 espécies em 1976,[9] número que aumentou para 686 espécies até 1989.[10] A publicação de David Hawksworth em 1983[32] de chaves para 218 espécies liquenícolas das Ilhas Britânicas estimulou novas pesquisas. Revisões abrangentes de grupos principais seguiram, incluindo Hyphomycetes liquenícolas (Hawksworth 1979[33]), Coelomycetes (Hawksworth 1981),[34] e Heterobasidiomycetes (Diederich 1996).[3][24]
A inclusão de fungos liquenícolas em listas nacionais de líquens, começando com o trabalho de Rolf Santesson em 1993 sobre a Suécia e a Noruega,[35] incentivou ainda mais seu estudo. De 1989 a 2003, o número de espécies conhecidas nesse grupo aproximadamente dobrou.[24] Em seu livro de 2024, The Lives of Lichens, os liquenologistas Robert Lücking e Toby Spribille destacaram a crescente comunidade em torno da pesquisa de fungos liquenícolas: "A caça, coleta e identificação de fungos liquenícolas é uma subcultura da liquenologia por si só, com sua própria literatura, sites e grupos de mídia social".[36]
Desafios históricos nos estudos de conidiomas

As primeiras pesquisas sobre líquens e fungos liquenícolas enfrentaram desafios significativos para distinguir entre os conidiomas do micobionte do líquen e aqueles dos fungos liquenícolas. David L. Hawksworth resumiu a complexidade dessas estruturas e o potencial para má interpretação.[37]
Os conidiomas em líquens podem assumir várias formas, incluindo esféricos ("globosos") ou em forma de frasco ("picnídios"), cupuliformes ("acervulares"), semelhantes a almofadas ("esporodóquios"), em forma de capacete ou peltados ("campilídios") ou eretos ("sinematas", "hifóforos"). O tipo mais comum em fungos formadores de líquens é o conidioma picnidial, que se abre por um único poro. Essas estruturas eram frequentemente chamadas de "espermogônias" na literatura inicial quando se presumia que tinham um papel sexual.[37]
Hawksworth observou que o estudo de conidióforos e células conidiogênicas era desafiador devido ao seu pequeno tamanho. Avanços nas técnicas de microscopia, como o uso de pós de lavagem biologicamente ativos antes da fixação e secagem por ponto crítico para microscopia eletrônica de varredura, permitiram exames mais detalhados dessas estruturas.[37]
Uma questão significativa nos estudos iniciais era a confusão potencial entre conidiomas do micobionte do líquen e aqueles dos fungos liquenícolas. Isso era particularmente problemático quando o fungo invasor causava pouco ou nenhum dano ao líquen hospedeiro. Em alguns casos, novos nomes para fungos conidiais foram erroneamente baseados nos conidiomas normais do líquen hospedeiro. Por exemplo, o gênero Pyrenotrichum foi baseado no que agora se sabe serem os campilídios ("capacetes") de vários líquens foliícolas (que crescem em folhas de plantas). Esses desafios históricos enfatizam como nosso entendimento desses organismos evoluiu ao longo do tempo, com muitas concepções errôneas iniciais sendo corrigidas por pesquisas subsequentes.[37]
Métodos
O estudo de fungos liquenícolas emprega uma gama de metodologias, desde técnicas tradicionais de cultura até abordagens moleculares avançadas. Cada método contribui com conhecimentos únicos sobre a biologia, ecologia e diversidade desses organismos.
Técnicas de isolamento e cultura
Os métodos micológicos tradicionais formam a base para o estudo de fungos liquenícolas. Essas técnicas são cruciais para entender sua biologia e interações com hospedeiros líquens. Os pesquisadores normalmente começam coletando tecidos de líquens infectados no campo. Eles identificam parasitas fúngicos por suas estruturas de frutificação ou pela descoloração que causam nos talos dos líquens. No laboratório, essas estruturas são isoladas e cultivadas em meios sólidos de ágar, como o meio de Sabouraud, ágar de dextrose de batata ou ágar de farinha de milho. Para reduzir a contaminação, a esterilização de superfície com etanol ou hipoclorito de sódio é frequentemente necessária.[38]
Para identificação precisa e estudos genéticos, os pesquisadores preferem culturas de esporo único ou conídio único. Esse processo envolve:
- Maceração de estruturas de frutificação maduras para liberar esporos ou conídios
- Incubação em placas de ágar
- Manutenção de culturas em ambientes controlados
Alguns fungos liquenícolas requerem condições específicas de crescimento, como meios com baixo teor de nitrogênio ou a presença de tecidos de líquen. Esses fungos cultivados são valiosos para vários experimentos, incluindo estudos sobre habilidades degradativas, interações com metabólitos secundários de líquens e análises genéticas. Para garantir disponibilidade futura e verificação de identidade, os pesquisadores frequentemente depositam culturas em coleções reconhecidas de culturas fúngicas.[38]
Métodos de pesquisa modernos
Nos últimos anos, métodos independentes de cultura, particularmente aqueles que empregam técnicas moleculares, revolucionaram o estudo de fungos liquenícolas. Esses incluem:
- Sequenciamento de DNA: Permite identificação precisa e análise filogenética de espécies
- Análise de DNA ambiental (eDNA): Permite a detecção de fungos liquenícolas em amostras ambientais, mesmo quando não visíveis
- Metagenômica: Fornece conhecimentos sobre toda a comunidade microbiana associada aos líquens
Essas técnicas modernas revelaram uma alta diversidade de fungos associados a líquens, muitos dos quais permanecem indetectáveis por métodos tradicionais. Por exemplo, técnicas de impressão genética de DNA mostraram uma alta diversidade de fungos associados a líquens que não necessariamente se correlacionam com a presença de fungos liquenícolas visíveis externamente.[39] Estudos de sequenciamento paralelo em massa de micobiomas de líquens em vários habitats, de ambientes árticos a alpinos, expandiram ainda mais o entendimento da diversidade e distribuição desses fungos.[40][41]
A aplicação dessas métodos avançados sugere que o número real de espécies de fungos liquenícolas pode exceder em muito as estimativas atuais, potencialmente atingindo de 3.000 a 5.000 espécies. Isso indica um potencial substancial para a descoberta de novas espécies e gêneros por meio da aplicação contínua de métodos moleculares.[5][8]
Apesar desses avanços, a microscopia tradicional permanece essencial no estudo de fungos liquenícolas, particularmente para entender suas interações físicas com líquens hospedeiros. No entanto, distinguir hifas estranhas dentro dos talos dos líquens do micobionte propriamente dito permanece um desafio significativo, destacando a necessidade de integrar abordagens de pesquisa tradicionais e modernas.[15]
Análise entre táxons
A análise entre táxons é um método de pesquisa usado para estudar a correlação entre diferentes grupos taxonômicos, analisando seus padrões de diversidade.[42] No contexto dos fungos liquenícolas, esse método ajuda a entender como a diversidade desses fungos se relaciona com seus hospedeiros líquens. Ao coletar dados sobre líquens e fungos liquenícolas dos mesmos habitats, os pesquisadores podem identificar padrões e relações entre os dois grupos. Por exemplo, estudos nas montanhas Koralpe, na Áustria, mostraram que a diversidade de fungos liquenícolas segue de perto a diversidade de seus hospedeiros líquens, sugerindo que os líquens podem ser usados como indicadores para prever a presença e diversidade desses fungos.[16]
Essa abordagem usa técnicas estatísticas, como análise de co-correspondência para criar modelos preditivos, que mostraram que certas espécies de líquens, especialmente aquelas abundantes e amplamente distribuídas, podem indicar de forma confiável a diversidade de fungos liquenícolas. Este método não apenas melhora nosso entendimento das relações ecológicas entre líquens e fungos liquenícolas, mas também fornece uma ferramenta prática para a conservação da biodiversidade. Ao usar líquens como indicadores substitutos, os pesquisadores podem identificar e proteger de maneira mais eficiente áreas com alta biodiversidade, particularmente em regiões pouco exploradas.[16]
Pesquisa
Estudos moleculares revelaram que os fungos liquenícolas podem possuir faixas de hospedeiros mais amplas do que anteriormente inferidas apenas por observações morfológicas. Pesquisadores detectaram algumas espécies em líquens assintomáticos e até em espécies de líquens não conhecidas anteriormente por abrigar esses fungos.[8]
Referências
- ↑ a b c «Lichenicolous fungi : Worldwide Checklist». George Mason University. Consultado em 25 de outubro de 2025
- ↑ Brodo, Irwin; Sharnoff, Sylvia; Sharnoff, Stephen (2001). Lichens of North America. New Haven, Connecticut: Yale University Press. ISBN 978-0300082494
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y Hawksworth, D.L. (1982). «Secondary fungi in lichen symbioses: parasites, saprophytes and parasymbionts». The Journal of the Hattori Botanical Laboratory. 52: 357–366. doi:10.18968/jhbl.52.0_357

- ↑ a b c d e Grube, Martin (2018). «The lichen thallus as a microbial habitat». In: Blanz, Paul. Biodiversity and Ecology of Fungi, Lichens, and Mosses. Col: Biosystematics and Ecology. 34. [S.l.]: Verlag der Österreichischen Akademie der Wissenschaften. pp. 529–546. ISBN 978-3-7001-8219-1
- ↑ a b c d e f g h i j Hafellner, J. (2018). «Focus on lichenicolous fungi: Diversity and taxonomy under the principle "one fungus – one name"». Biosystematics and Ecology. 34: 227–243
- ↑ a b Grimm, Maria; Grube, Martin; Schiefelbein, Ulf; Zühlke, Daniela; Bernhardt, Jörg; Riedel, Katharina (2021). «The lichens' microbiota, still a mystery?». Frontiers in Microbiology. 12: 1–25. PMC 8042158
 . PMID 33859626. doi:10.3389/fmicb.2021.623839
. PMID 33859626. doi:10.3389/fmicb.2021.623839
- ↑ a b c d e f g h i j k Diederich, Paul; Millanes, Ana M.; Wedin, Mats; Lawrey, James D. (20 de agosto de 2022). Flora of Lichenicolous Fungi. Basidiomycota (PDF). 1. Luxembourg: National Museum of Natural History. p. 351. ISBN 978-2-919877-26-3
- ↑ a b c d e f g h i j Diederich, Paul; Lawrey, James D.; Ertz, Damien (2018). «The 2018 classification and checklist of lichenicolous fungi, with 2000 non-lichenized, obligately lichenicolous taxa». The Bryologist. 121 (3): 340–425. doi:10.1639/0007-2745-121.3.340
- ↑ a b Clauzade, G.; Roux, C. (1976). Les champignons lichénicoles non lichénisés [The non-lichenized lichenicolous fungi] (em francês). Montpellier: Université des Sciences et Techniques du Languedoc
- ↑ a b Clauzade, G.; Diederich, P.; Roux, C. (1989). «Nelikenigintaj fungoj likenlogaj–Ilustrita determinlibro» [Non-lichenized lichenicolous fungi – Illustrated identification guide]. Bulletin de la Société Linnéenne de Provence, Numéro spécial (em esperanto). 1: 1–142
- ↑ Freire-Rallo, Sandra; Wedin, Mats; Diederich, Paul; Millanes, Ana M. (2023). «To explore strange new worlds – The diversification in Tremella caloplacae was linked to the adaptive radiation of the Teloschistaceae». Molecular Phylogenetics and Evolution. 180: 107680. Bibcode:2023MolPE.18007680F. PMID 36572164. doi:10.1016/j.ympev.2022.107680

- ↑ Freire-Rallo, Sandra; Diederich, Paul; Millanes, Ana M.; Wedin, Mats (2023). «Five new species in the Tremella caloplacae complex». The Lichenologist. 55 (5): 223–239. Bibcode:2023ThLic..55..223F. doi:10.1017/s0024282923000154

- ↑ Millanes, Ana M.; Diederich, Paul; Westberg, Martin; Wedin, Mats (2021). «Crittendenia gen. nov., a new lichenicolous lineage in the Agaricostilbomycetes (Pucciniomycotina), and a review of the biology, phylogeny and classification of lichenicolous heterobasidiomycetes». The Lichenologist. 53 (1): 103–116. Bibcode:2021ThLic..53..103M. doi:10.1017/S002428292000033X
 . hdl:10115/28130
. hdl:10115/28130
- ↑ Chang, Runlei; Wang, Yichen; Liu, Yanyu; Wang, Yiran; Li, Shiguo; Zhao, Guoyan; Zhang, Susu; Dai, Meixue; Zheng, Xiaoxiao; Bose, Tanay; Si, Hongli (2023). «Nine new species of black lichenicolous fungi from the genus Cladophialophora (Chaetothyriales) from two different climatic zones of China». Frontiers in Microbiology. 14: 1–16. PMC 10312087
 . PMID 37396360. doi:10.3389/fmicb.2023.1191818
. PMID 37396360. doi:10.3389/fmicb.2023.1191818
- ↑ a b c d e Nash III, Thomas H., ed. (2008). Lichen Biology 2nd ed. Cambridge, UK: Cambridge University Press. ISBN 978-0-521-69216-8. Consultado em 25 de outubro de 2025
- ↑ a b c d e f g h De Carolis, Roberto; Muggia, Lucia; Bacaro, Giovanni (2023). «Lichen and lichenicolous fungal communities tested as suitable systems for the application of cross-taxon analysis». Diversity. 15 (2): e285. Bibcode:2023Diver..15..285D. doi:10.3390/d15020285
 . hdl:11368/3039900
. hdl:11368/3039900
- ↑ Christiansen, M. Skytte (1993). «Further observations on the association between the lichen Lecanora conizaeoides and its parasites Lichenoconium erodens and L. lecanorae (Sphaeropsidales)» (PDF). Graphis Scripta. 5: 19–21
- ↑ Moya, Patricia; Molins, Arantzazu; Chiva, Salvador; Bastida, Joaquín; Barreno, Eva (2020). «Symbiotic microalgal diversity within lichenicolous lichens and crustose hosts on Iberian Peninsula gypsum biocrusts». Scientific Reports. 10 (1): 14060. Bibcode:2020NatSR..1014060M. PMC 7441164
 . PMID 32820199. doi:10.1038/s41598-020-71046-2
. PMID 32820199. doi:10.1038/s41598-020-71046-2
- ↑ a b c d Nimis, Pier Luigi; Pittao, Elena; Caramia, Monica; Pitacco, Piero; Martellos, Stefano; Muggia, Lucia (2024). «The ecology of lichenicolous lichens: a case-study in Italy». MycoKeys (105): 253–266. PMC 11161687
 . PMID 38855319. doi:10.3897/mycokeys.105.121001
. PMID 38855319. doi:10.3897/mycokeys.105.121001
- ↑ a b Kirk, Paul M.; Cannon, Paul F.; Minter, David W.; Stalpers, Joost A., eds. (2008). Dictionary of the Fungi 10th ed. Wallingford, UK: CAB Europe. pp. 376–377. ISBN 978-0-85199-826-8
- ↑ Hafellner, Josef; Poelt, Josef (1980). «Der "Flechtenparasit" Buellia pulverulenta — eine bleibend interne parasitische Flechte» [The "lichen parasite" Buellia pulverulenta – a permanently internal parasitic lichen] (PDF). Phyton (Austria) (em alemão). 20 (1–2): 129–133
- ↑ Poelt, Josef (1985). «Caloplaca epithallina: Portrat einer parasitischen Flechte» [Caloplaca epithallina. Portrait of a parasitic lichen]. Botanische Jahrbücher für Systematik, Pflanzengeschichte und Pflanzengeographie (em alemão). 107 (1–3): 457–468
- ↑ Temu, Stella Gilbert; Tibell, Sanja; Tibuhwa, Donatha Damian; Tibell, Leif (2019). «Crustose calicioid lichens and fungi in mountain cloud forests of Tanzania». Microorganisms. 7 (11): e491. PMC 6920850
 . PMID 31717781. doi:10.3390/microorganisms7110491
. PMID 31717781. doi:10.3390/microorganisms7110491
- ↑ a b c d Lawrey, James D.; Diederich, Paul (2003). «Lichenicolous Fungi: Interactions, Evolution, and Biodiversity». The Bryologist. 106 (1): 80–120. doi:10.1639/0007-2745(2003)106[0080:LFIEAB]2.0.CO;2
- ↑ Acharius, Erik; Besemann, Christian Andreas (1810). Lichenographia universalis. In qua Lichenes omnes detectos, adiectis observationibus et figuris horum vegetabilium naturam et organorum carpomorphorum structuram illustrantibus, ad genera, species, varietates differentiis et observationibus sollicite definitas. Tab XIV. Gottingae: Apud Iust. Frid. Danckwerts. Consultado em 26 de outubro de 2025
- ↑ Diederich, Paul; Christianse, M. Skytte (1994). «Biatoropsis usnearum Räsänen, and other heterobasidiomycetes on Usnea». The Lichenologist. 26 (1): 47–66. Bibcode:1994ThLic..26...47D. doi:10.1006/lich.1994.1004
- ↑ Zopf, von W. (1896). «Uebersicht der auf Flechten schmarotzenden Pilze» [Overview of fungi parasitizing lichens]. Hedwigia (em alemão). 35: 312–366
- ↑ Lindsay, W.L. (1869). «Enumeration of micro-lichens parasitic on other lichens». Quarterly Journal of Microscopical Science. New Series. 9: 49–57, 135–146, 342–358
- ↑ Vouaux, L. (1912). «Synopsis des champignons parasites des lichens». Bulletin trimestriel de la Société mycologique de France (em francês). 28: 177–256
- ↑ Vouaux, L. (1913). «Synopsis des champignons parasites des lichens». Bulletin trimestriel de la Société mycologique de France (em francês). 29: 33–128
- ↑ Vouaux, L. (1914). «Synopsis des champignons parasites des lichens». Bulletin trimestriel de la Société mycologique de France (em francês). 30: 135–198; 281–329
- ↑ Hawksworth, D.L. (1983). «A key to the lichen-forming, parasitic, parasymbiotic and saprophytic fungi occurring on lichens in the British Isles». The Lichenologist. 15 (1): 1–44. Bibcode:1983ThLic..15....1H. doi:10.1017/S0024282983000031
- ↑ Hawksworth, D.L. (1979). «The lichenicolous hyphomycetes». Bulletin of the British Museum (Natural History). Botany. 6 (3): 183–300
- ↑ Hawksworth, D.L. (1981). «The lichenicolous coelomycetes». Bulletin of the British Museum (Natural History), Botany Series. 9: 1–98
- ↑ Santesson, Rolf (1993). The Lichens and Lichenicolous Fungi of Sweden and Norway. Lund: SBT-förlaget. ISBN 978-9197125581
- ↑ Lücking, Robert; Spribille, Toby (2024). The Lives of Lichens. Princeton: Princeton University Press. p. 56. ISBN 978-0-691-24727-4
- ↑ a b c d Hawksworth, David Leslie (1988). «Conidiomata, Conidiogenesis, and Conidia». In: Galun, Margalith. CRC Handbook of Lichenology. 1. Boca Raton, Florida: CRC Press. pp. 182–186. ISBN 978-0-429-29178-4
- ↑ a b Lawrey, James D. (2002). «Isolation and culture of lichenicolous fungi». In: Kranner, I.C.; Beckett, R.P.; Varma, A.K. Protocols in Lichenology. Berlin, Heidelberg: Springer Berlin Heidelberg. pp. 75–84. ISBN 978-3-540-41139-0. doi:10.1007/978-3-642-56359-1_6
- ↑ Fleischhacker, Antonia; Grube, Martin; Kopun, Theodora; Hafellner, Josef; Muggia, Lucia (2015). «Community analyses uncover high diversity of lichenicolous fungi in alpine habitats». Microbial Ecology. 70 (2): 348–360. Bibcode:2015MicEc..70..348F. PMID 25792281. doi:10.1007/s00248-015-0579-6
- ↑ Zhang, Tao; Wei, Xin-Li; Zhang, Yu-Qin; Liu, Hong-Yu; Yu, Li-Yan (2015). «Diversity and distribution of lichen-associated fungi in the Ny-Ålesund Region (Svalbard, High Arctic) as revealed by 454 pyrosequencing». Scientific Reports. 5 (1): e14850. Bibcode:2015NatSR...514850Z. PMC 4604449
 . PMID 26463847. doi:10.1038/srep14850
. PMID 26463847. doi:10.1038/srep14850
- ↑ Fernández-Mendoza, Fernando; Fleischhacker, Antonia; Kopun, Theodora; Grube, Martin; Muggia, Lucia (2017). «ITS 1 metabarcoding highlights low specificity of lichen mycobiomes at a local scale». Molecular Ecology. 26 (18): 4811–4830. Bibcode:2017MolEc..26.4811F. PMID 28771869. doi:10.1111/mec.14244
- ↑ de Morais, Gustavo Filete; dos Santos Ribas, Luiz Guilherme; Ortega, Jean Carlo Gonçalves; Heino, Jani; Bini, Luis Mauricio (2018). «Biological surrogates: A word of caution». Ecological Indicators. 88: 214–218. Bibcode:2018EcInd..88..214D. doi:10.1016/j.ecolind.2018.01.027

.jpg)


.jpg)