Tetracloreto de telúrio
Tetracloreto de telúrio é um composto químico inorgânico, um cloreto do elemento telúrio com a fórmula química empírica TeCl
4. Esse composto é um sólido amarelo pálido volátil, sublimando a 200 °C a 0,1 mmHg.[1] TeCl
4 é um composto molecular, embora tetramérico (Te
4Cl
16) no estado sólido, mas no estado líquido após ser fundido, é iônico, dissociando-se em íons TeCl+
3 e Te
2Cl2–
10.[1] No estado de vapor, ele é formado por moléculas discretas TeCl
4.
Tetracloreto de telúrio
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
 | |||||||||||||||||
| Nomes | |||||||||||||||||
| Nome IUPAC | Cloreto de telúrio IV Hexadecacloreto de tetratelúrio | ||||||||||||||||
| Outros nomes | Cloreto de telúrio | ||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
| Página de dados suplementares | |||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||
Estrutura
TeCl
4 é monomérico na fase gasosa, com uma estrutura semelhante à do SF
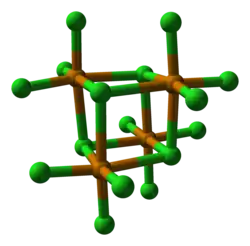
4.[3] No estado sólido, é um aglomerado do tipo cubano tetramérico, consistindo de um núcleo Te
4Cl
4 e três ligantes cloreto terminais para cada Te. Alternativamente, esta estrutura tetramérica pode ser considerada como um tetraedro Te
4 com cloros de cobertura facial e três cloros terminais por átomo de telúrio, dando a cada átomo de telúrio um ambiente octaédrico distorcido.
Síntese
TeCl
4 é preparado pela cloração do pó de telúrio:
Te + 2Cl
2 → TeCl
4
A reação é iniciada com calor. O produto é isolado por destilação.[4] O TeCl
4 bruto pode ser purificado por destilação sob uma atmosfera de cloro.[5]
Alternativamente, TeCl
4 pode ser preparado usando cloreto de sulfurila (SO
2Cl
2) como fonte de cloro.[5] Outro método envolve a reação do telúrio com monocloreto de enxofre (S
2Cl
2) à temperatura ambiente. Esta reação exotérmica forma rapidamente cristais brancos em forma de agulha de TeCl
4.[6]
O tetracloreto de telúrio também pode ser obtido em solução aquosa altamente ácida de telúrio IV, na qual há um grande excesso de íons cloreto (por exemplo, em HCl concentrado). O telúrio IV tem forte afinidade pelo cloro e forma vários complexos de cloreto nessa solução, incluindo o TeCl
4 molecular.[6]
Reações
TeCl
4 sofre hidrólise em água, quando a solução não está fortemente ácida, formando um precipitado branco leitoso de ácido teluroso ou dióxido de telúrio hidratado e uma solução ácida de HCl:[6]
TeCl
4 + 3H
2O → H
2TeO
3 + 4HCl
H
2TeO
3 TeO
2•H
2O
Em uma solução mais concentrada ou com maior acidez (pH 1 ou menor), a hidrólise parcial pode ocorrer:
TeCl
4 + 3H
2O → [Te(OH)
3]+Cl– + 3HCl
Quando dissolvido em HCl concentrado, ele forma uma solução amarela brilhante do complexo hexacoordenado de cloreto:
TeCl
4 + 2HCl → H
2[TeCl
6]
O tetracloreto de telúrio é o composto de entrada para compostos organotelúrio de alta valência. A arilação fornece, dependendo das condições, Te(C
6H
4R)
2Cl
2, [Te(C
6H
4R)
5]–
, [Te(C
6H
4R)
6]2–.[7]
TeCl
4 tem poucas aplicações em síntese orgânica. Seu peso equivalente é alto, e a toxicidade de compostos organotelúrio é problemática. Possíveis aplicações de tetracloreto de telúrio em síntese orgânica foram relatadas.[8] Ele se adiciona a alcenos para dar derivados Cl-C-C-TeCl
3, onde o Te pode ser posteriormente removido com sulfeto de sódio. Arenos ricos em elétrons reagem para dar compostos de Te arílico. Assim, o anisol dá TeCl
2(C
6H
4OCH
3)
2, que pode ser reduzido ao telureto de diarila. TeCl
4 é um precursor de heterociclos contendo telúrio como telurofenos.[5]
O aquecimento de uma mistura de TeCl
4 e telúrio metálico produz dicloreto de telúrio (TeCl
2).[9]
No ar úmido, o TeCl
4 forma oxicloreto de telúrio (TeOCl
2), que se decompõe ainda mais com o excesso de água para formar ácido teluroso (H
2TeO
3). [9]
Segurança
Como é o caso de outros compostos de telúrio, o TeCl
4 é tóxico. A absorção de compostos de telúrio pode causar um odor corporal persistente e extremamente desagradável que lembra alho podre ou rábano, bem como um mau-hálito repulsivo de alho podre, que podem persistir por meses, devido à metabolização do telúrio e sua liberação como telureto de dimetilo ((CH
3)
2Te) volátil.[10] Ele também libera HCl após hidrólise, o qual é altamente corrosivo.[5]
Ver também
Referências
- ↑ a b Greenwood, Norman N. ; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ↑ Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadas:0 - ↑ Cotton, F. Albert ; Wilkinson, Geoffrey ; Murillo, Carlos A.; Bochmann, Manfred (1999), Química Inorgânica Avançada (6ª ed.), Nova York: Wiley-Interscience, ISBN 0-471-19957-5
- ↑ Suttle, JF; Smith, CRF (1950). Audrieth, Ludwig F. (ed.). Sínteses inorgânicas . Vol. 3. pp. 140– 2. doi : 10.1002/9780470132340 . ISBN 978-0-470-13162-6.
- ↑ a b c d Petragnani, Nicola; Mendes, Samuel R.; Silveira, Claudio C. (2008-04-07). "Tetracloreto de telúrio: um método melhorado de preparação" . Tetrahedron Letters . 49 (15): 2371– 2372. doi : 10.1016/j.tetlet.2008.02.085 . ISSN 0040-4039 .
- ↑ a b c Lenher, Victor. "Tetracloreto de telúrio" . Revista da Sociedade Química Americana . 24 . doi : 10.1021/ja02016a007 .
- ↑ Miyasato, Masataka; Sagami, Takao; Minoura, Mao; Yamamoto, Yohsuke; Akiba, Kin-ya (2004). «Syntheses and Reactions of Hexavalent Organotellurium Compounds Bearing Five or Six Tellurium-Carbon Bonds». Chemistry – A European Journal. 10 (10): 2590–2600. PMID 15146530. doi:10.1002/chem.200305260
- ↑ Petragnani, N.; Comasseto, JV (1991). "Reagentes de telúrio em síntese orgânica; avanços recentes. Parte 1". Síntese . 1991 (10): 793– 817. doi : 10.1055/s-1991-26577 . S2CID 260335920 . e Petragnani, N.; Comasseto, JV (1991). "Reagentes de telúrio em síntese orgânica; avanços recentes. Parte 2". Síntese . 1991 (11): 897– 919. doi : 10.1055/s-1991-26605 . S2CID 196716602 .
- ↑ a b Simons, JH (1930-09-01). "As propriedades do tetracloreto de telúrio" . Jornal da Sociedade Química Americana . 52 (9): 3488– 3493. doi : 10.1021/ja01372a003 . ISSN 0002-7863 .
- ↑ tabelaperiodica.org/bafo-de-telurio