Tetraiodeto de telúrio
Tetraiodeto de telúrio
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
| Outros nomes | Iodeto de telúrio IV | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
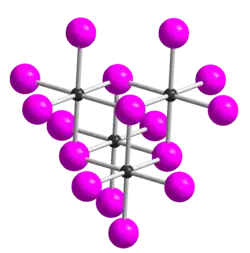
Tetraiodeto de telúrio (TeI
4) é um composto químico inorgânico formado pelos elementos telúrio e iodo. É um sólido cristalino cinza-escuro a preto. Ele tem uma estrutura tetramérica que é diferente das formas sólidas tetraméricas de TeCl
4 e TeBr
4.[1] No TeI
4, os átomos de Te são coordenados octaedricamente e as bordas dos octaedros são compartilhadas.[1]
.
Preparação
O tetraiodeto de telúrio pode ser preparado pela reação química entre Te elementar e iodometano, CH
3I.[1]
Na forma de vapor, TeI
4 dissocia-se:[2]
TeI
4 → TeI
2 + I
2
Também pode ser obtido pela reação do ácido telúrico com iodeto de hidrogênio.[3]
H
6TeO
6 + 6HI → TeI
4 + I
2 + 6H
2O
Também pode ser obtido pela reação dos elementos iodo e telúrio, podendo também produzir diiodeto de telúrio e monoiodeto de telúrio, dependendo das condições de reação:[4]
Te + 2I
2 → TeI
4
TeI
4 → TeI
2 + I
2
Propriedades
O tetraiodeto de telúrio é um sólido cinza-ferro que se decompõe lentamente em água fria e rapidamente em água morna para formar dióxido de telúrio e iodeto de hidrogênio.[5] É estável mesmo em ar úmido e se decompõe quando aquecido, liberando iodo. É solúvel em ácido iodídrico para formar H[TeI
5] e H
2[TeI
6] e é ligeiramente solúvel em acetona.[3]
O tetraiodeto de telúrio é um condutor quando fundido, dissociando-se nos íons TeI+
3 e I–. Em solventes com propriedades doadoras como a acetonitrila, formam-se complexos iônicos de CH
3CN que tornam a solução condutora:[2]
TeI
4 + 2CH
3CN → [(CH
3CN)
2TeI
3]+ + I–
São conhecidas cinco modificações do tetraiodeto de telúrio, todas elas compostas de moléculas tetraméricas.[6] A forma δ é a forma mais estável termodinamicamente. Ela é derivada estruturalmente (assim como as formas α, β e γ) da forma ε.
Na presença de excesso de íons iodeto, o TeI
4 reage para formar o complexo TeI2–
6,[7] que apresenta uma cor vermelha-acastanhada escura. Esta reação é usada em química analítica para detectar a presença de telúrio IV em soluções.
TeI
4 + 2I– → [TeI
6]2–
_e_TeI6(2-).jpg)
Referências
- ↑ a b c Greenwood, Norman N. ; Earnshaw, Alan (1997). Química dos Elementos (2ª ed.). Butterworth-Heinemann . ISBN 978-0-08-037941-8.
- ↑ a b Inorganic Chemistry,Egon Wiberg, Arnold Frederick Holleman Elsevier 2001 ISBN 0-12-352651-5
- ↑ a b Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as "refs" nomeadasbrauer - ↑ Hagen, A. P. (17 de setembro de 2009). Inorganic Reactions and Methods, The Formation of Bonds to Halogens (Part 1) (em inglês). [S.l.]: John Wiley & Sons. ISBN 978-0-470-14538-8
- ↑ Base de dados Tellurium(IV) iodide, 99% (metals basis) por AlfaAesar, consultado em 2013-12-17 .
- ↑ Riedel, Erwin; Janiak, Christoph (2011). Anorganische Chemie: Zusatzmaterial online. Col: Studium 8. Aufl ed. Berlin: de Gruyter. ISBN 978-3-11-022567-9
- ↑ https://pubs.rsc.org/en/content/articlehtml/2023/ra/d3ra00996c