Ácido telúrico
Ácido telúrico
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
 | |||||||||||||||||||
| Nomes | |||||||||||||||||||
| Nome IUPAC | Hexahidroxitelúrio | ||||||||||||||||||
| Outros nomes |
| ||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
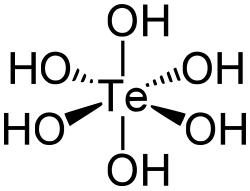
O ácido telúrico, ou mais precisamente ácido ortotélurico, é um composto químico com a fórmula química Te(OH)
6, frequentemente escrito como H
6TeO
6 ou, em alguns casos, H
2TeO
4 • 2H
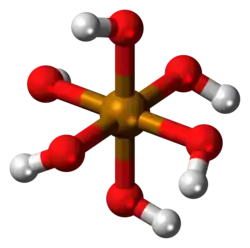
2O. É um sólido cristalino branco composto de moléculas octaédricas de Te(OH)
6 que persistem em solução aquosa.[4] No estado sólido, existem duas formas, romboédrica e monoclínica, e ambas contêm moléculas octaédricas de Te(OH)
6,[5] contendo um átomo de telúrio (Te) hexavalente, no estado de oxidação +6, ligado a seis grupos hidroxila (–OH), portanto, pode ser chamado de hidróxido de telúrio (VI). O ácido telúrico é um ácido fraco que é dibásico, formando sais de telurato com bases fortes e sais de hidrogenotelurato com bases mais fracas ou por hidrólise de teluratos em água.[5][6] É usado como fonte de telúrio na síntese de catalisadores de oxidação.
Preparação
O ácido telúrico é formado pela oxidação do telúrio ou do dióxido de telúrio com um agente oxidante poderoso, como o peróxido de hidrogênio, o trióxido de cromo ou o peróxido de sódio.[5]
- TeO
2 + H
2O
2 + 2H
2O→ Te(OH)
6
A cristalização de soluções de ácido telúrico abaixo de 10°C produz ácido telúrico tetra-hidratado Te(OH)
6·4H2O.[4] É um agente oxidante, como mostrado pelo potencial de eletrodo para a reação abaixo, embora seja cineticamente lento em suas oxidações.
- Te(OH)
6 + 2H+ + 2e–
⇌ TeO
2 + 4H
2O , Eo= +1,02V
O cloro, em comparação, é +1,36V e o ácido selenoso é +0,74 V em condições oxidantes.
Propriedades e reações
O ácido anidro é estável no ar a 100°C, mas acima disso ele desidrata para formar ácido polimetatelúrico, um pó branco higroscópico (composição aproximada (H
2TeO
4)
10), e ácido alotelúrico, um xarope ácido de estrutura desconhecida (composição aproximada: 3H
2TeO
4·4H
2O).[4][7]
Sais típicos do ácido contêm os ânions [TeO(OH)
5]– e [TeO
2(OH)
4]2–. A presença do íon telurato TeO2–
4 foi confirmado na estrutura do estado sólido de Rb
6[TeO
5][TeO
4].[8] O forte aquecimento a mais de 300°C produz a modificação cristalina α do trióxido de telúrio, α-TeO
3.[6] A reação com diazometano (CH
2N
2) fornece o éster hexametílico, Te(OCH
3)
6.[4]
O ácido telúrico e seus sais contêm principalmente telúrio hexacoordenado.[5] Isso é verdade mesmo para sais como o telurato de magnésio, MgTeO
4, que é isoestrutural com molibdato de magnésio e contém octaedros TeO
6.[5]
Outras formas de ácido telúrico
Ácido metatelúrico, H
2TeO
4, o análogo de telúrio do ácido sulfúrico, H
2SO
4, é desconhecido. Ácido alotelúrico de composição aproximada 3H
2TeO
4·4H2O, não é bem caracterizado e pode ser uma mistura de Te(OH)
6 e (H
2TeO
4)n.[4]
Outros ácidos de telúrio
Ácido teluroso, H
2TeO
3, contendo telúrio em seu estado de oxidação +4, é conhecido, mas não bem caracterizado. Telureto de hidrogênio, H
2Te, é um gás instável, tóxico e com odor extremamente desagradável que forma ácido telurídrico após adição à água.
Referências
- ↑ https://www.sciencedirect.com/topics/chemistry/telluric-acid#:~:text=Telluric%20acid%2C%20Te(OH),of%203.07%20g%2Fcm3.
- ↑ https://pubs.rsc.org/en/content/articlehtml/2016/cp/c6cp05892b#:~:text=Measurements%20performed%20for%202%20in,not%20discernible%20at%20this%20scale.
- ↑ Perrin, D. D., ed. (1982) [1969]. Ionisation Constants of Inorganic Acids and Bases in Aqueous Solution. Col: IUPAC Chemical Data, 29 2nd ed. Oxford: Pergamon (publicado em 1984). Entry 219. ISBN 0-08-029214-3. LCCN 82-16524
- ↑ a b c d e Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; Currie, M.; Korneev, A.; Chulkova, G.; Okunev, O.; Kouminov, P.; Smirnov, K.; Voronov, B.; N. Gol'tsman, G.; Sobolewski, Roman (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- ↑ a b c d e Predefinição:Cotton&Wilkinson6th
- ↑ a b Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ↑ Loub, J.; Haase, W.; Mergehenn, R. (1979). «Structure of an adduct of orthotelluric acid and urea». Acta Crystallographica Section B: Structural Crystallography and Crystal Chemistry. 35 (12): 3039–3041. Bibcode:1979AcCrB..35.3039L. doi:10.1107/S0567740879011286
- ↑ Catherine E. Housecroft; Alan G.Sharpe (2008). “Capítulo 16: Os elementos do grupo 16”. Química Inorgânica, 3ª Edição . Pearson. pág. 526. ISBN 978-0-13-175553-6.