Dicloreto de telúrio
Dicloreto de telúrio ou cloreto de telúrio II é o composto químico com a fórmula química TeCl
2. É um cloreto do elemento químico telúrio em seu estado de oxidação +2. É um sólido preto que se funde em um líquido também preto, mas que vaporiza em um gás roxo. Esse composto é instável em relação ao desproporcionamento, decompondo-se para Te elementar e TeCl
4.
Dicloreto de telúrio
| |||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||
 | |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| |||||||||||||||||||
| Página de dados suplementares | |||||||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||||||
Síntese e Reações
O dicloreto de telúrio pode ser produzido pela reação química do telúrio com difluorodiclorometano.[2][3]
Também pode ser produzido pela reação de comproporção de telúrio e tetracloreto de telúrio.[4]
TeCl
4 + Te → 2TeCl
2
Dicloreto de telúrio reage com a água, sofrendo uma reação de hidrólise e dismutação gerando Te, TeO
2 e HCl:
2TeCl
2 + 2H
2O → TeO
2 + Te + 4HCl
TeCl
2 é relativamente instável, mas pode formar alguns complexos estáveis e bem caracterizados com alguns ligantes tais como íons cloreto ou com tioureia. Esses complexos são quadrado-planares.
TeCl
2 + 2Cl– → [TeCl
4]2–
TeCl
2 + 2CS(NH
2)
2 → [TeCl
2(SC(NH
2)
2)
2]
Propriedades
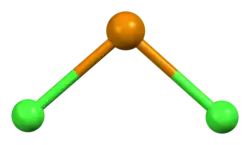
O dicloreto de telúrio é um sólido preto que reage com a água. Ele derrete em um líquido preto e vaporiza em um gás roxo.[1][5] O gás consiste em moléculas monoméricas de TeCl
2 com comprimentos de ligação Te–Cl de 2,329 Å e um ângulo de ligação Cl–Te–Cl de 97,0°.[5]
O dicloreto de telúrio é instável em relação à desproporção.[5] Vários complexos dele são conhecidos e bem caracterizados. Eles são preparados tratando dióxido de telúrio com ácido clorídrico na presença de tioureias. A tioureia serve tanto como um ligante quanto como um redutor, convertendo Te(IV) em Te(II).
TeO
2 + 4HCl + 4CS(NH
2)
2 → [TeCl
2(SC(NH
2)
2)
2] + [(H
2N)
2C—S—S—C(NH
2)
2]Cl
2
Referências
- ↑ a b c d e f g Perry, Dale (2011). Handbook of Inorganic Compounds. Boca Raton, FL: CRC Press. ISBN 978-1-4398-1462-8. OCLC 759865801
- ↑ Gmelin, Leopold (1976). Tellurium (em inglês e alemão). [S.l.]: Springer-Verlag. OCLC 77834357
- ↑ Aynsley, E. E. (1953). «598. The preparation and properties of tellurium dichloride». Royal Society of Chemistry (RSC). Journal of the Chemical Society (Resumed): 3016. ISSN 0368-1769. doi:10.1039/jr9530003016
- ↑ Haaland, Arne (2008). Molecules and models : the molecular structures of main group element compounds. Oxford New York: Oxford University Press. ISBN 978-0-19-152860-6. OCLC 226969121
- ↑ a b c Fernholt, Liv; Haaland, Arne; Volden, Hans V.; Kniep, Rüdiger (1985). «The molecular structure of tellurium dichloride, TeCl2, determined by gas electron diffraction». Elsevier BV. Journal of Molecular Structure. 128 (1–3): 29–31. Bibcode:1985JMoSt.128...29F. ISSN 0022-2860. doi:10.1016/0022-2860(85)85037-7
