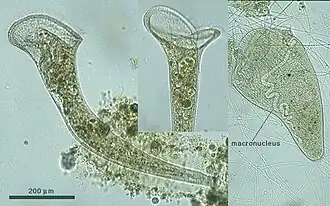
Stentor (ciliado)
Stentor
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Espécies | |||||||||||||||||
| |||||||||||||||||
Stentor é um gênero de protistas ciliados em forma de trombeta, comuns na maior parte do mundo. Esse grupo tem sido estudado detalhadamente por um pequeno conjunto de zoólogos dedicados desde o final do século XIX, com múltiplas revisões ocorrendo entre seus táxons.[1][2]
Todos os membros desse gênero compartilham a mesma morfologia geral: uma extremidade anterior ampla para alimentação e uma extremidade posterior afilada, onde geralmente se fixam ao substrato. São células muito grandes, variando de aproximadamente 0,4 a 2 milímetros (embora isso varie conforme a espécie).[2] Elas também exercem controle fino sobre seus corpos grandes, podendo se contrair em uma bola equivalente a 1/6 de seu tamanho total ou se estender para cima, ampliando a face anterior de alimentação. As espécies podem apresentar pigmentos únicos devido à coloração dos grânulos corticais de seu ectoplasma e organizar configurações distintas de seus grandes macronúcleos.[1]
São heterotróficos e se alimentam usando seus numerosos cílios para criar uma corrente de água, puxando presas para sua grande abertura oral. Muitas espécies desse gênero também possuem algas endossimbióticas, permitindo obter nutrientes tanto de presas quanto da luz solar. São mais comuns em ecossistemas de água doce, mas certas espécies podem ser encontradas em ecossistemas marinhos ou mesmo terrestres.[1][2]
Os membros de Stentor também possuem notáveis capacidades de regeneração. Mesmo uma pequena fração da célula pode se regenerar em um organismo completo. Essa capacidade os torna um ponto interessante de estudo e pode contribuir para a compreensão da cura em larga escala em animais.[3]
Etimologia
O nome Stentor refere-se à forma de trombeta do organismo, especificamente sua "boca" ou aparelho oral alargado. Deriva de um arauto da mitologia grega, que usava sua voz estrondosa para motivar os soldados gregos na Guerra de Troia.[4]
Espécie-tipo
S. muelleri [en] foi a primeira espécie descrita em detalhes como membro do gênero por Christian Gottfried Ehrenberg em 1831.[5] É comumente encontrada em ecossistemas de água doce e ocasionalmente em estuários, dispersa pelo mundo. Caracteriza-se por seu macronúcleo moniliforme (com 10-20 nódulos macronucleares) e grânulos corticais não pigmentados. Apesar de não possuir pigmentos como outras espécies, S. muelleri não é incolor, mas aparece marrom devido à espessura da célula. Geralmente mede de 0,5 a 2 milímetros de comprimento, mas raramente pode se estender até 3 milímetros.[1][2]
Descrição
Stentor pode crescer até dois milímetros de comprimento, tamanho suficiente para que indivíduos sejam vistos a olho nu. Esse tamanho, combinado com sua natureza altamente mótil, confere a Stentor uma fisiologia complexa e interconectada. A superfície da célula é coberta por uma camada protetora. Essa camada é secretada pela célula e pode ser descartada e reformada se o organismo estiver estressado.[2]
Grânulos corticais
Sob essa película, há linhas granulares elevadas alternadas com linhas claras indentadas, ambas correndo longitudinalmente. As linhas granulares aumentam de espessura da esquerda para a direita, de modo que as faixas mais grossas ficam adjacentes às mais finas, onde são divididas pela formação anterior de uma nova faixa clara. Essas linhas granulares contêm os característicos grânulos corticais da célula, que conferem às listras sua pigmentação única.[2] Esses pigmentos endógenos variam muito em aparência, sendo vermelho, verde e azul-esverdeado (estentorina em S. coeruleus) os mais comuns. Em pesquisas, esses pigmentos são frequentemente usados como traço morfológico para agrupar espécies. Para o organismo, os grânulos corticais servem a uma função defensiva e são excretados em grandes volumes quando a célula está sob predação. Os pigmentos liberados pela extrusão desses grânulos corticais possuem propriedades tóxicas que afastam ou até matam protistas atacantes.[2][6]
Cílios e motilidade
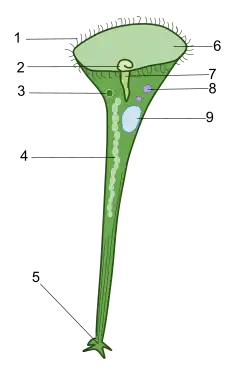
As faixas claras do ectoplasma são onde os cílios estão localizados. Cada faixa clara abriga um cinetídeo, com numerosos cílios adjacentes longitudinalmente ao longo do organismo. Esses cílios somáticos são mais curtos e frequentemente mais rígidos que os cílios da boca, localizados em feixes ao longo do aparelho oral.[2] Essas faixas claras e seus cílios associados são mais numerosos onde as faixas granulares são mais finas e especialmente abundantes nas faixas para garantir a alimentação adequada.
A natureza do controle fino do corpo e das contrações de Stentor está associada a fibras sob as faixas claras. Há dois tipos dessas fibras: fibras km compostas de microtúbulos e faixas M compostas de microfilamentos.[2] As fibras km são longas e se conectam diretamente aos cinetídeos. Provavelmente são responsáveis por manter a estrutura e auxiliar na extensão. As faixas M são feixes de microfilamentos, situados abaixo das fibras km. Essas faixas controlam a contração e encurtam/endireitam dependendo da contorção do ectoplasma. Essas fibras citoesqueléticas são altamente específicas e podem causar contrações e extensões localizadas, permitindo que o organismo se adapte a uma variedade de formas.[2] A célula também possui numerosos alvéolos sob a membrana para suportar sua superfície grande e contorcida. Stentor também tem um vacúolo contrátil e poro associado em seu lado esquerdo anterior para expelir o excesso de água intracelular.
Aparelho de alimentação
A estrutura mais especializada em Stentor é seu aparelho de alimentação. A superfície da cavidade bucal (de alimentação) é chamada campo frontal, que abriga cílios e mionemas.[2] As linhas granulares nessa seção podem ser tão finas quanto uma fileira de grânulos corticais, permitindo o empacotamento denso de cílios de alimentação. Esses cílios se conectam em folhas até o endoplasma, onde são empacotados em um feixe radicular e fixados por uma fibra basal reforçada. O campo frontal espirala e se condensa no esôfago, especializado para forçar o alimento para o citostoma da célula. Na outra extremidade da célula, o órgão de fixação adere ao substrato por meio de muco secretado e contrações de mionemas.[1][2][7][6]
Uma vez que Stentor captura sua presa, ela a conduz para a bolsa oral, que então se fecha parcialmente. É aproximadamente nesse ponto que o Stentor em alimentação decide se consome a presa capturada (embora valha notar que o alimento ainda pode ser rejeitado até o esôfago superior).[2] Se a presa for rejeitada, será ejetada e passada ao longo dos cílios externos do corpo da célula em direção à cauda para evitar ser consumida acidentalmente novamente. Presas mortas há muito tempo e material não orgânico, como toxinas ou vidro, são mais propensos a serem rejeitados, especialmente se Stentor estiver bem alimentado.[2] O alimento é então passado para o esôfago, um aparelho de alimentação invaginado revestido com cílios e mionemas para auxiliar na passagem dos itens alimentares. Os mionemas do esôfago realizam uma espécie de peristaltismo com contrações rítmicas forçando itens alimentares maiores para um vacúolo alimentar ectoplasmático. Vacúolos alimentares também podem ser formados dentro do citoplasma se a presa escapar/romper seu vesícula.[1][2][7]
Nem toda presa pode ser fagocitada integralmente, especialmente presas grandes como outros Stentor. Nesses casos, a cavidade bucal se expandirá para acomodar parte da presa (a extremidade caudal se estiver comendo outro Stentor) e subsequentemente se fechará, cortando parte da presa como se tirasse um pedaço de carne.[2] Esse pedaço menor de alimento será então ingerido conforme descrito acima. Canibalismo foi observado em múltiplas espécies de Stentor, com indivíduos planctônicos sendo atraídos para o vórtice de indivíduos fixos e em alimentação.[2]
Núcleos e divisão celular
Como outros ciliados, os núcleos de Stentor são divididos em um macronúcleo e micronúcleo.[1][2] O macronúcleo é altamente poliploide e qualquer fragmento pode conter muitas cópias de todo o genoma transcripcionalmente ativo. O micronúcleo é muito menor e contém informações necessárias para a formação do macronúcleo e é essencial para o processo de conjugação. A forma do macronúcleo é diversa em Stentor, com muitas espécies tendo macronúcleos moniliformes (em forma de contas), variformes (em forma de tubo) e condensados (semelhantes a um único núcleo enlarguecido). A conjugação é relativamente rara, com a maioria dos organismos se dividindo assexualmente por fissão.[1][2]
-
 Stentor polymorphus com simbiontes algais
Stentor polymorphus com simbiontes algais -
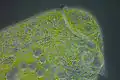 Stentor polymorphus com simbiontes algais
Stentor polymorphus com simbiontes algais -
 Stentor fixado em folhas
Stentor fixado em folhas -
 Stentor coeruleus digerindo Blepharisma sp.
Stentor coeruleus digerindo Blepharisma sp.
Ecologia
Embora certas espécies de Stentor (S. multiformis) tenham sido registradas em ambientes marinhos e terrestres, o gênero vive principalmente em corpos de água doce. No entanto, muitas espécies também são encontradas em ambientes de água doce mais distróficos ou salobros.[1][2] Em um dado lago, a população de Stentor é dividida aproximadamente na proporção 10:1, com a maioria dos indivíduos fixados ao substrato do fundo (como filamentos algais ou detritos) por uma adesão firme do órgão de fixação e uma pequena fração de indivíduos planctônicos, nadando ao longo da corrente com cílios corporais.[2]
Resposta a distúrbios
Quando um ambiente se torna inadequado, seja por aumento de toxinas/predadores prejudiciais ou por diminuição de recursos necessários, os indivíduos se desprendem do substrato e se tornam planctônicos. Esse comportamento de desprendimento é um último recurso, com numerosas etapas de evitação de estresse sendo tomadas pelo indivíduo antes disso.[2] Com um estímulo físico leve, o Stentor ignorará a fonte ou se curvará em sua direção em busca de alimento. Dado estresse adicional por meio de cutucadas ou exposição a toxinas, a célula se curvará para baixo em direções aleatórias até que o estresse cesse. Se o estresse não cessar, o indivíduo pode reverter seus cílios para empurrar a água para longe de si ou se contrair em uma bola.[2] Apenas após essas medidas de evitação serem tentadas o organismo desprenderá seu órgão de fixação e buscará um terreno de alimentação mais adequado, embora tentativas forçada de remoção ocasionalmente causem a célula ser rasgada ao meio em vez de ser removida da superfície.[2] Nesse estado, seu corpo se torna esferoide (até seis vezes mais curto que sua forma estendida) e nada até encontrar um ambiente mais adequado, onde afundará e secretará muco para se fixar novamente.
Alimentação
Os indivíduos realizam sua alimentação quando fixados ao substrato, estendendo seus corpos longitudinalmente por mais de dois milímetros e abrindo suas cavidades bucais.[2] Stentor se alimenta batendo sincronizadamente os cílios firmemente agrupados na faixa que circunda a cavidade bucal. Isso cria um vórtice de água que puxa outros protistas planctônicos para sua cavidade bucal, após o que cílios bucais puxam a presa mais para dentro. Certas espécies são conhecidas por possuir quistos de repouso.[1][2]
Simbiose
Semelhante a outros organismos aquáticos, muitas espécies de Stentor desenvolveram uma associação próxima com algas verdes endossimbióticas (especificamente Chlorella).[2] Quando presentes, as algas Chlorella endossimbióticas estão densamente espalhadas pelo endoplasma. Os endossimbiontes fornecem carboidratos para sustentar seu hospedeiro e se alimentam dos resíduos de Stentor, beneficiando-se da proteção do ciliado. Stentors com simbiontes podem sobreviver sem alimento por muito mais tempo que outros indivíduos, embora nenhuma espécie tenha se tornado totalmente autotrófica.[2] Essa endossimbiose em Stentor não é obrigatória (exceto para S. polymorphus, que provavelmente depende de seu simbionte para uma vitamina específica desconhecida). Se o Stentor hospedeiro morrer e sua estrutura celular se dissolver, a alga Chlorella continuará a persistir como algas de vida livre. Essa associação é naturalmente dissolvida na escuridão completa, onde quase todos os simbiontes Chlorella desaparecerão do Stentor hospedeiro (embora alguns sempre persistam, particularmente na extremidade posterior de Stentor).[2] A dissociação completa foi alcançada em laboratório, quando Stentors foram privados de luz solar com alimento e calor em abundância, dividindo-se rapidamente o suficiente para que alguns não carregassem seus endossimbiontes para a próxima geração. Esse mutualismo é sempre benéfico para Stentor, com indivíduos apoiados por Chlorella superando Stentors sem simbiontes.[1][2][4]
Florações
Muitas espécies de Stentor também são conhecidas por causar eflorescências, onde até 90% de toda a biomassa de ciliados no ecossistema pertence à espécie de Stentor em floração.[2][8] Isso é mais frequente nas espécies menores e comumente planctônicas, que apresentam uma associação mais forte com algas endossimbióticas. O Stentor em floração cobrirá a superfície de um lago ou lagoa, conferindo-lhe a aparência colorida dos grânulos corticais da espécie. O nutriente limitante que causa florações de Stentor não é comumente conhecido, embora certos casos tenham sido estudados e encontrados correlacionados com aumento de chuvas, que podem fornecer bactérias produtoras de vitamina B12 ou aumento de fósforo.[2] Embora florações de Stentor tenham mostrado alguma evidência de dano à vida de peixes e pureza da água, são consideravelmente menos tóxicas que eflorescências algais mais típicas.[1][2][8]
Importância prática
Embora seu grande tamanho e endoplasma robusto tornem Stentor bons sujeitos de estudo, sua dificuldade de cultura e baixa frequência sexual os impediram de serem mais amplamente estudados. A força de Stentor como organismo-modelo para pesquisa reside em suas notáveis capacidades de regeneração.[3] Se contiver um fragmento de macronúcleo e alguma membrana/córtex, qualquer pequeno pedaço de um organismo pode regenerar em um Stentor completamente formado.[1][2][3] Essa regeneração mantém a polaridade e arranjo adequados. Se um indivíduo for cortado em muitos pedaços, ele primeiro alinhará suas faixas ectoplasmáticas. Seções alinhadas e fundidas de ectoplasma são sítios de nucleação onde mais fragmentos se ligam.[2] Uma vez restauradas as características somáticas, o campo frontal se regenerará.[2] Por causa disso, Stentor é frequentemente sujeito a uma ampla gama de experimentos de enxertia. Indivíduos separados podem trocar núcleos, citoplasma e se fundir, mantendo a função. Se dois indivíduos forem enxertados juntos, podem até persistir como um doblete dividindo-se como um.[9] Stentor pode, portanto, fornecer informações sobre especificidade celular em múltiplos níveis. As propriedades regenerativas de Stentor também podem ser aplicadamente úteis a modelos maiores de cura para entender a origem e mecanismos celulares por trás da cura em animais.[2][3][9]
Sistemática
Stentor foi descrito pela primeira vez pelo influente naturalista de Genebra Abraham Trembley em 1744.[10] Trembley inicialmente identificou erroneamente o organismo como um tipo de Hydra de água doce e, em uma carta endereçada à Royal Society, o descreveu como "Polypus", um "animal aquático minúsculo". Essa descrição inicial do organismo focava em sua forma de trombeta (com descrições tanto da cavidade bucal quanto do órgão de fixação), movimento circular de seus cílios orais, comportamento parcialmente planctônico e alimentação por vórtice. O primeiro uso do nome "Stentor" foi pelo naturalista alemão Lorenz Oken em 1815, embora se referisse a um grupo taxonomicamente muito maior e menos específico que o gênero atual.[11]
A primeira grande organização do gênero foi feita por outro naturalista alemão, Christian Gottfried Ehrenberg, em 1831.[5] Ele publicou uma revisão contendo as espécies conhecidas de Stentor e definiu a espécie-tipo do gênero como S. muelleri, um Stentor de água doce com macronúcleo moniliforme e grânulos corticais incolores. Revisões adicionais foram feitas no século seguinte pelos zoólogos Friedrich Stein (1867), William Saville-Kent [en] (1881), Herbert Johnson (1893), Alfred Kahl [en] (1932) e Vance Tartar (1961), todas integradas à revisão de Willhelm Foissner e S. Wölfl de 1994 do gênero.[1] Foissner e Wölfl organizaram o gênero pela presença de endossimbiontes, forma do macronúcleo e pigmentação dos grânulos corticais peliculares, delineando dezenove espécies de Stentor com vinte e sete espécies indeterminadas ou espécies listadas incorretamente como distintas de outros táxons.[1][2]
Desde essa revisão, houve ajustes adicionais ao gênero. Em 2002, Hideo Kumazawa usou suas extensas notas e descrições das espécies de Stentor de água doce ao redor de Hiroshima, Japão, para classificar ulteriormente o gênero e definir uma nova espécie (S. cornutus).[12] Ele focou em caracteres não cobertos na revisão de Foissner e Wölfl, como as características da bolsa oral, orientação dos cílios rígidos (somáticos) e experimentos de enxertia. Finalmente, em 2006, Ying-Chun Gong construiu um clado usando RNA ribossômico de três espécies de Stentor, indicando que são irmãs do gênero Blepharisma [en].[13]
Galeria de vídeos
Ver também
Referências
- ↑ a b c d e f g h i j k l m n o Foissner, W.; Wölfl, S. (1 de janeiro de 1994). «Revision of the genus Stentor Oken (Protozoa, Ciliophora) and description of S.araucanus nov. spec, from South American lakes». Journal of Plankton Research. 16 (3): 255–289. ISSN 0142-7873. doi:10.1093/plankt/16.3.255
- ↑ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab ac ad ae af ag ah ai aj ak al The Biology of Stentor (em inglês). [S.l.: s.n.] ISBN 978-0-08-009343-7. Consultado em 10 de abril de 2025
- ↑ a b c d Marshall, Wallace F. (29 de setembro de 2021). «Regeneration in Stentor coeruleus». Frontiers in Cell and Developmental Biology (em inglês). 9. ISSN 2296-634X. PMC 8511388
 . PMID 34660609. doi:10.3389/fcell.2021.753625
. PMID 34660609. doi:10.3389/fcell.2021.753625
- ↑ a b Slabodnick, Mark M.; Marshall, Wallace F. (8 de setembro de 2014). «Stentor coeruleus». Current Biology (em inglês). 24 (17): R783–R784. Bibcode:2014CBio...24.R783S. ISSN 0960-9822. PMC 5036449
 . PMID 25202864. doi:10.1016/j.cub.2014.06.044
. PMID 25202864. doi:10.1016/j.cub.2014.06.044
- ↑ a b Ehrenberg, Christian Gottfried (1831). «Ober die Entwickelung und Lebensdauer der Infusionsthiere; nebst ferneren Beitragen zu einer Vergleichung ihrer organischen Systeme». Abh. Dt. Akad. Wiss.: 1–154
- ↑ a b Miyake, Akio; Harumoto, Terue; Iio, Hideo (1 de janeiro de 2001). «Defence function of pigment granules in Stentor coeruleus». European Journal of Protistology. 37 (1): 77–88. ISSN 0932-4739. doi:10.1078/0932-4739-00809
- ↑ a b Newman, E. (4 de agosto de 1972). «Contraction in stentor coeruleus: a cinematic analysis». Science. 177 (4047): 447–449. Bibcode:1972Sci...177..447N. ISSN 0036-8075. PMC 2409986
 . PMID 5043148. doi:10.1126/science.177.4047.447
. PMID 5043148. doi:10.1126/science.177.4047.447
- ↑ a b Bai, A. R. Kasturi; Murthy, K. V. Narayana (1975). «Seasonal Blooms of a Red Stentor». Transactions of the American Microscopical Society. 94 (3): 425–427. ISSN 0003-0023. JSTOR 3225510. doi:10.2307/3225510
- ↑ a b Wan, Kirsty Y.; Hürlimann, Sylvia K.; Fenix, Aidan M.; McGillivary, Rebecca M.; Makushok, Tatyana; Burns, Evan; Sheung, Janet Y.; Marshall, Wallace F. (30 de dezembro de 2019). «Reorganization of complex ciliary flows around regenerating Stentor coeruleus». Philosophical Transactions of the Royal Society B: Biological Sciences. 375 (1792). PMC 7017328
 . PMID 31884915. doi:10.1098/rstb.2019.0167
. PMID 31884915. doi:10.1098/rstb.2019.0167
- ↑ Trembley, Abraham (janeiro de 1997). «X. Translation of a letter from Mr. Abraham Trembley, F. R. S. to the President, with observations upon several newly discover'd species of fresh-water Polypi». Philosophical Transactions of the Royal Society of London. 43 (474): 169–183. doi:10.1098/rstl.1744.0040
- ↑ Oken, Lorenz (1813–26). Okens Lehrbuch der naturgeschichte. 1.-[3.] th. Leipzig: C. H. Reclam
- ↑ Kumazawa, Hideo (1 de janeiro de 2002). «Notes on the taxonomy of Stentor Oken (Protozoa, Ciliophora) and a description of a new species». Journal of Plankton Research. 24 (1): 69–75. ISSN 0142-7873. doi:10.1093/plankt/24.1.69
- ↑ Gong, Ying-Chun; Yu, Yu-He; Zhu, Fei-Yun; Feng, Wei-Song (janeiro de 2007). «Molecular Phylogeny of Stentor (Ciliophora: Heterotrichea) Based on Small Subunit Ribosomal RNA Sequences». Journal of Eukaryotic Microbiology (em inglês). 54 (1): 45–48. ISSN 1066-5234. PMID 17300519. doi:10.1111/j.1550-7408.2006.00147.x