Grânulo cortical
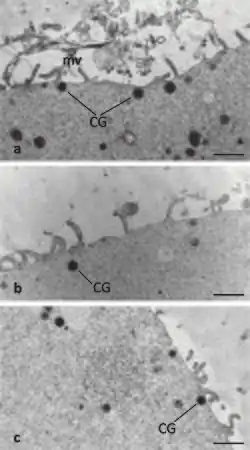
Os grânulos corticais são organelos secretores reguladores (variando entre 0,2 µm e 0,6 µm de diâmetro) encontrados no interior dos ovócitos e estão mais associados à prevenção da polispermia após o evento da fertilização.[1] Os grânulos corticais encontram-se em todos os mamíferos, a maioria vertebrados e alguns invertebrados.[2] No interior do ovócito, os grânulos corticais estão localizados ao longo do córtex, a região mais afastada do centro da célula. Após a fertilização, uma via de sinalização induz os grânulos corticais a fundirem-se com a membrana celular do ovócito e a libertarem o seu conteúdo na matriz extracelular do ovócito. Esta exocitose dos grânulos corticais é conhecida como reação cortical. Nos mamíferos, a matriz extracelular do ovócito inclui uma camada circundante de espaço perivitelino, zona pelúcida e, finalmente, células cumulus. Evidências experimentais demonstraram que o conteúdo libertado dos grânulos corticais modifica a matriz extracelular do ovócito, particularmente a zona pelúcida. Esta alteração dos componentes da zona pelúcida é conhecida por reação de zona. A reação cortical não ocorre em todos os mamíferos, o que sugere a probabilidade de outros propósitos funcionais para os grânulos corticais.[1] Para além de modificar a matriz extracelular do ovócito e estabelecer um bloqueio à poliespermia, a exocitose dos grânulos corticais pode também contribuir para a proteção e suporte do embrião em desenvolvimento durante a pré-implantação.[3] Uma vez que os grânulos corticais completam as suas funções, o ovócito não os repõe.[1]
Formação
A formação de grânulos corticais ocorre durante as fases iniciais do crescimento do ovócito. Mais especificamente, nos humanos, macacos, hamsters e coelhos, os grânulos corticais são estabelecidos quando o folículo ovárico é formado por multicamadas. Em ratos e ratinhos, os grânulos corticais foram observados mais cedo no desenvolvimento do folículo, quando o folículo ovárico tem apenas uma camada. Durante as fases iniciais do crescimento do ovócito, o complexo de Golgi aumenta de tamanho, prolifera e produz pequenas vesículas que migram para a região subcortical da célula. Estas pequenas vesículas fundem-se umas com as outras para formar grânulos corticais maduros, que são então estabelecidos como entidades separadas do Golgi.[1] Em alguns organismos, como nos hamsters, a vesícula secretora do Golgi pode fundir-se com uma vesícula secretora do retículo endoplasmático rugoso para finalmente formar um grânulo cortical.[4] Nos mamíferos, o ovócito produz e transloca continuamente grânulos corticais para o córtex até que ocorra a ovulação. Foi demonstrado em modelos animais mamíferos e não mamíferos que a migração dos grânulos corticais depende de processos do citoesqueleto, particularmente da atividade dos microfilamentos. Para os mamíferos, a migração dos grânulos corticais é considerada um indício da maturidade do ovócito e da organização das organelas.[1]
Distribuição
Como resultado da translocação, os grânulos corticais estão uniformemente distribuídos por todo o córtex do ovócito. No entanto, foi observado em roedores que alguns grânulos corticais estão reorganizados, deixando um espaço entre os restantes grânulos corticais. Este espaço é designado por domínio livre de grânulos corticais (CGFD) e é observado em ambas as regiões do fuso meiótico da célula durante a metáfase I e a metáfase II da meiose. Os CGFDs não foram observados em ovócitos felinos, equinos, bovinos, suínos ou humanos. Estudos com ovócitos de roedores sugerem que certos grânulos corticais sofrem redistribuição e/ou exocitose ao longo do ciclo meiótico, estabelecendo assim os CGFDs. Mais especificamente, as evidências incluem maiores quantidades de grânulos corticais em redor dos CGFDs e uma quantidade generalizada reduzida de grânulos corticais da célula durante o ciclo meiótico. Além disso, alguns eventos exocitóticos de grânulos corticais pré-fertilização ocorrem no sulco de clivagem da célula simultaneamente com a formação do corpo polar.[1]
Existe uma variedade de hipóteses sobre a função biológica dos CGFDs e a exocitose dos grânulos corticais pré-fertilização. Por exemplo, a formação dos CGFDs pode ser o mecanismo do ovócito para reter mais grânulos corticais para uso futuro, em vez de os perder para os corpos polares, à medida que estes são expelidos da célula. Como alguns grânulos corticais libertados provêm de uma região próxima dos fusos meióticos, os investigadores colocaram também a hipótese de que os grânulos corticais libertados podem modificar a matriz extracelular do ovócito, pelo que o esperma não consegue ligar-se a esta região. Se o esperma se ligasse a esta região, o ADN paterno, ao descondensar-se, poderia possivelmente romper a integridade do ADN materno devido à sua proximidade. Este bloqueio do esperma num local específico é denominado bloqueio local. Considerando que os ovócitos de roedores têm cerca de 75% menos área de superfície do que os ovócitos de espécies de mamíferos de maior porte, a ligação do espermatozóide nesta região é mais provável, o que pode exigir o bloqueio local. Os investigadores colocam também a hipótese de que o ovócito liberta alguns grânulos corticais antes da fertilização para fazer pequenas modificações na matriz extracelular do ovócito, de modo a que a ligação seja limitada apenas ao espermatozóide capaz de se ligar, apesar destas pequenas modificações.[1]
Referências
- ↑ a b c d e f g Liu, Min (17 de novembro de 2011). «The biology and dynamics of mammalian cortical granules». Reproductive Biology and Endocrinology. 9 (1). 149 páginas. PMC 3228701
 . PMID 22088197. doi:10.1186/1477-7827-9-149
. PMID 22088197. doi:10.1186/1477-7827-9-149
- ↑ Wessel, Gary M.; Brooks, Jacqueline M.; Green, Emma; Haley, Sheila; Voronina, Ekaterina; Wong, Julian; Zaydfudim, Victor; Conner, Sean (2001). The Biology of Cortical Granules. International Review of Cytology. 209. [S.l.: s.n.] pp. 117–206. ISBN 9780123646132. PMID 11580200. doi:10.1016/s0074-7696(01)09012-x
- ↑ Hoodbhoy, Tanya; Talbot, P. (dezembro de 1994). «Mammalian Cortical Granules: Contents, Fate, and Function» (PDF). Molecular Reproduction and Development. 39 (4): 439–448. PMID 7893493. doi:10.1002/mrd.1080390413. Consultado em 13 de maio de 2015
- ↑ Gulyas, B. J. (1980). Cortical granules of mammalian eggs. International Review of Cytology. 63. [S.l.]: Elsevier. pp. 357–392. ISBN 9780123644633. PMID 395132. doi:10.1016/S0074-7696(08)61762-3