Microtúbulo
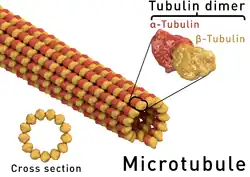
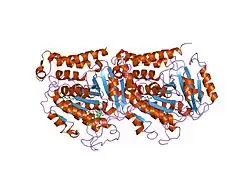
Os microtúbulos são estruturas tubulares presentes nas células, de 25 nm de diâmetro exterior e cerca de 12 nm de diâmetro interior, com comprimentos que variam entre uns poucos nanómetros a micrómetros, que se estendem ao longo de todo o citoplasma. Encontram-se nas células eucarióticas e são formados pela polimerização de um dímero constituído por duas proteínas globulares, a α e a β tubulinas. Os microtúbulos nucleiam-se e organizam-se nos centros organizadores de microtúbulos (COMTs), como o centrossomo ou os corpos basais dos cílios e flagelos. Estes COMTs podem possuir centríolos ou não.
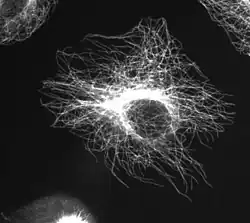
Encontramos microtúbulos no citoplasma formando parte da rede do citoesqueleto (junto com os microfilamentos e os filamentos intermediários), nos cílios e flagelos, nos tripletos dos centríolos e no fuso mitótico.
Os microtúbulos intervêm em diversos processos celulares que implicam movimento de vesículas de secreção, movimento de organelos, transporte intracelular de substâncias (com intervenção das proteínas dineína e quinesina), assim como na divisão celular (mitose e meiose). Além disso, constituem a estrutura interna dos apêndices móveis da célula eucariótica, cílios e flagelos.
Estrutura
Os microtúbulos são heteropolímeros de α- e β-tubulina, as quais formam dímeros, que são a sua unidade estrutural.[1] Os dímeros polimerizam em 13 protofilamentos, que logo se agregam lateralmente para formar estruturas cilíndricas ocas. Para polimerizar requer-se a presença de dímeros com uma concentração mínima determinada denominada concentração crítica, embora o processo se acelere pela adição de núcleos, que são alongados.
Uma importante característica dos microtúbulos é a sua polaridade. A tubulina polimeriza por adição de dímeros num ou em ambos os extremos do microtúbulo. A adição faz-se por união cabeça com cauda durante a formação dos protofilamentos. Assim, vão-se formando fileiras de monómeros de α e β-tubulina na parede do tubo, o que provoca uma polaridade global ao microtúbulo. Devido a que todos os protofilamentos de um microtúbulo têm a mesma orientação, um extremo está composto por um anel de α-tubulina (denominado extremo -) e, o oposto, por um anel de β-tubulina (denominado extremo +).[2]
Funções
Citoesqueleto
Como componentes do citoesqueleto (junto com a actina e os filamentos intermediários), dão à célula um suporte estrutural. Podem crescer e minguar para originar força.
Mobilidade de cílios
Os microtúbulos do axonema dos cílios e flagelos eucarióticos (os procarióticos são diferentes) permitem a mobilidade destes em associação com certas proteínas.
Transporte
Funcionam como autoestradas pelas quais se movem as proteínas motoras que arrastam vesículas, organelos e outros fatores celulares ao longo do microtúbulo. Estas proteínas aproveitam a hidrólise do ATP para gerar energia mecânica e mover-se sobre os microtúbulos. São a dineína, transportador retrógrado, e a quinesina, transportador anterógrado.
A dineína é uma molécula de estrutura similar à quinesina: consta de duas cadeias pesadas idênticas que conformam duas cabeças globulares e de um número variável de cadeias intermediárias e de cadeias leves. Transportam desde o extremo (+) para o (-) do canal intramicrotubular. Pensa-se que a atividade de hidrólise de ATP, fonte de energia da célula, encontra-se nas cabeças globulares. A dineína transporta vesículas e organelos, pelo que deve interagir com as suas membranas, e, para interagir com elas, requer um complexo proteico, cujo elemento mais notável é a dinactina.
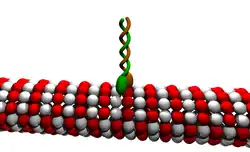
A maioria das quinesinas intervém no transporte anterógrado de vesículas, ou seja, implicam um movimento para a parte mais distal da célula ou da neurite (dendrite, axônio), desde o extremo (-) para o (+) dos microtúbulos, sobre os que se deslocam. Pelo contrário, outra família de proteínas motoras, as dineínas, empregam os mesmos carris mas dirigem as vesículas para a parte mais proximal da célula, pelo que o seu transporte é retrógrado.
Mitose
Uma importante estrutura feita de microtúbulos é o fuso mitótico usado nas células eucarióticas para separar os cromossomos durante a divisão celular. A mitose é facilitada por um subgrupo de microtúbulos denominado microtúbulos astrais, definidos como microtúbulos originados no centrossomo que não se conectam com os cinetocoros dos cromossomos. Os microtúbulos astrais interagem com o córtex celular e ajudam na orientação do fuso. Colocam-se em disposição radial ao redor dos centrossomos. O grau de renovação ou reciclagem desta população de microtúbulos é maior que o de qualquer outra população. Os microtúbulos astrais funcionam concertadamente com as proteínas motoras dineínas, as quais estão orientadas com as suas cadeias leves unidas à membrana celular e a sua porção dinâmica unida ao microtúbulo. Isto permite que a contração da dineína empurre o centrossomo para a membrana, facilitando a citocinese.
Os microtúbulos astrais não são imprescindíveis para que progridam a mitose, mas requerem-se para assegurar a fidelidade do processo, já que intervêm no correto posicionamento e orientação do fuso mitótico. Também estão implicados na determinação do plano de divisão celular baseado na geometria e polaridade das células.
No desenvolvimento
O citoesqueleto de microtúbulos é essencial durante os processos morfoxenéticos do desenvolvimento dos organismos. Por exemplo, durante a embriogénese na mosca da fruta Drosophila melanogaster, requer-se uma rede de microtúbulos intacta e polarizada dentro do ovócito a fim de estabelecer os eixos do ovo; deste modo, os sinais entre as células foliculares e as do ovócito (como os fatores semelhantes ao TGF-alfa) provocam a reorganização dos microtúbulos situando o seu extremo (-) na zona anterior do ovócito, o que polariza a estrutura e comporta o aparecimento de um eixo dorsoanterior.[3] Este envolvimento na arquitetura corporal também se dá em mamíferos.[4]
Outro campo no qual os microtúbulos são essenciais é a formação do sistema nervoso em vertebrados superiores; neles a dinâmica da tubulina e das proteínas associadas aos microtúbulos (MAPs) é controlada com precisão a fim de desenvolver a base neuronal do cérebro.[5]
Regulação da expressão genica
O citoesqueleto celular é um elemento dinâmico que atua a muitos níveis na célula: além de dotá-la de uma forma determinada e de vertebrar o trânsito de vesículas e organelos, pode influir na expressão gênica. Porém, as vias celulares (ou seja, os mecanismos de transdução de sinal) que intervêm nesta comunicação são muito pouco conhecidos. Não obstante, descreveu-se a relação entre a despolimerização de microtúbulos mediada por fármacos e a expressão específica de factores de transcrição e, em consequência, a expressão diferencial dos genes dependentes da presença destes fatores.[6] Esta comunicação entre o citoesqueleto e a regulação da resposta celular está também relacionada com a geração de fatores de crescimento: por exemplo, esta relação existe para o fator de crescimento do tecido conjuntivo.[7]
Na terapia contra o câncer este fato tem vital importância pois o paclitaxel (comercialmente conhecido como taxol, um antitumoral muito empregado) possui como alvo o citoesqueleto de microtúbulos, e é precisamente a interação deste último com elementos que modulam o ciclo celular o que provoca, em presença do antitumoral, uma série de falhas celulares nas células cancerosas que conduzem à sua morte celular programada ou apoptose.[8]
Dinâmica microtubular
A polimerização dos microtúbulos realiza-se num centro organizador de microtúbulos. Nestes centros existe um tipo de tubulina, chamada γ-tubulina, que atua nucleando a adição de novos dímeros, com intervenção de outras proteínas reguladoras. Considera-se que existe um complexo anular de γ-tubulina, sempre situado no extremo - do microtúbulo.[9]
Instabilidade dinâmica
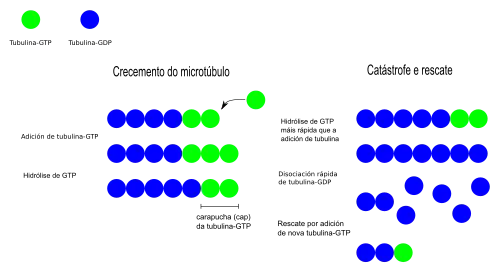
Durante a polimerização, ambas as unidades de tubulina estão unidas a uma molécula de guanosina trifosfato ou GTP.[1] O GTP desempenha uma função estrutural na α-tubulina, mas é hidrolizado a GDP na β-tubulina. Esta hidrólise modula a adição de novos dímeros. Assim, o GTP hidroliza-se após um certo período de tempo, o que permite que, se a adição de dímeros é rápida, se forme no extremo (+) um casquete de β-tubulina unida a GTP, enquanto que, em caso de ser lenta, o que se expõe é tubulina unida a GDP. Esta união a um ou outro nucleótido é a que determina a velocidade de polimerização ou despolimerização do microtúbulo. Deste modo, um casquete no extremo (+) com GTP favorece a elongação, enquanto que um de GDP, a despolimerização.[10]
Agora bem, este processo, de adição ou não de novos monómeros, depende da concentração de dímeros de αβ-tubulina na solução; se a sua concentração é maior que um parâmetro conhecido como concentração crítica (Cc) (que é a constante de equilíbrio de dissociação dos dímeros do extremo do microtúbulo), o microtúbulo cresce, e se é menor, mingua. E segundo a presença de um casquete de GTP ou GDP, a Cc é distinta, o que define que o extremo (+) e (-) tenham valores distintos, o que por sua vez favorece que a atividade dinâmica do extremo (+) seja maior devido a uma menor Cc específica. O microtúbulo, portanto, pode crescer por ambos os extremos ou só por um, dependendo da concentração de dímeros de αβ-tubulina. A interação do extremo (-) com o centro organizador de microtúbulos diminui muito a sua atividade.
Estes fatos estão modulados por proteínas associadas a microtúbulos ou MAPs.
Propriedades da polimerização da tubulina
Resumo global de ditas propriedades:
- Com concentrações de αβ-tubulina superiores à Cc os dímeros polimerizam para formar microtúbulos; por baixo da Cc, os microtúbulos sofrem despolimerização.
- O nucleótido, GTP ou GDP, unido à β-tubulina faz com que a Cc para a montagem nos extremos (+) e (-) de um microtúbulo seja diferente; por analogia com a montagem da actina filamentosa, define-se o extremo (+) como o preferido pela montagem.
- Com concentrações superiores de αβ-tubulina à Cc para a polimerização, os dímeros agregam-se em maior quantidade ao extremo (+).
- Quando a concentração de αβ-tubulina é mais elevada que a Cc do extremo (+) mas menor que a Cc do (-), pode-se dar um crescimento numa só direção agregando subunidades a um extremo e dissociando subunidades do extremo oposto.
Estas características explicam que exista uma inestabilidade dinâmica nos microtúbulos, que consiste em que, numa mesma célula, alguns microtúbulos estão despolimerizando-se (o que se chama catástrofe) e outros alongando-se (o que se chama resgate).
Alteração farmacológica da dinâmica microtubular
Existem uma grande quantidade de drogas capazes de unir-se à tubulina, modular o seu estado de ativação e assim interferir com a dinâmica microtubular a concentrações intracelulares muito mais baixas que a de tubulina. Deste modo, as células detêm o seu ciclo celular, o que pode conduzir à morte celular programada. Os compostos que modulam a atividade da tubulina podem dividir-se de forma geral em dois grandes grupos: em primeiro lugar estão os inibidores da sua polimerização, como a colchicina[11] e a vincristina,[12] que se unem a esta impedindo que forme microtúbulos. Por outro lado, estão os agentes estabilizantes de microtúbulos (MSAs), como o paclitaxel (conhecido comercialmente como taxol)[13] e o docetaxel,[14] os quais se unem preferentemente à tubulina montada, minimizando a dissociação da tubulina-GDP dos extremos dos microtúbulos e induzindo a montagem da tubulina-GDP normalmente inativa.
Os fármacos moduladores da polimerização de microtúbulos foram muito usados na terapia antitumoral. Ao serem indispensáveis para a mitose e ao detê-la, conseguem atuar contra o tumor, mas também se veem afetados aqueles tecidos em rápida proliferação (medula óssea, mucosa intestinal...). O sucesso clínico do paclitaxel e do docetaxel conduziram à procura de novos compostos com o mesmo mecanismo de ação e à descoberta nos últimos anos de uma grande quantidade de agentes estabilizantes de microtúbulos com pelo menos dois sítios de união distintos.
Bibliografia
- Alberts; et al. (2004). Biología molecular de la célula. [S.l.]: Barcelona: Omega. ISBN 84-282-1351-8
- Lodish; et al. (2005). Biología celular y molecular. [S.l.]: Buenos Aires: Médica Panamericana. ISBN 950-06-1374-3
Ver também
Referências
- ↑ a b Weisenberg RC. 1972. Microtubule formation in vitro in solutions containing low calcium concentrations. Science 177:1104–5
- ↑ Walker RA, O’Brien ET, Pryer NK, Soboeiro MF, Voter WA, et al. 1988. Dynamic in- stability of individual microtubules analyzed by video light microscopy: rate constants and transition frequencies. J. Cell Biol. 107:1437–48
- ↑ Van Eeden F. Stjohnston (1999). «The polarisation of the anterior-posterior and dorsal-ventral axes during Drosophila oogenesis» (PDF). Current Opinion in Genetics & Development: 396–404. doi:10.1016/S0959-437X(99)80060-4
- ↑ Beddington R.S.P., Robertson E.J., Hill M. (1999). «Axis Development and Early Asymmetry in Mammals» (PDF). Cell. 96: 195–209. doi:10.1016/S0092-8674(00)80560-7
- ↑ Tucker R.P. (1990). «The roles of microtubule-associated proteins in brain morphogenesis: a review». Brain Res Brain Res Rev. 15 (2): 101–20. doi:10.1016/0165-0173(90)90013-E
- ↑ Rosette C., Karin M. (1995). «Cytoskeletal control of gene expression: depolymerization of microtubules activates NF-kappa B» (PDF). The Journal of Cell Biology. 128 (6): 1111–1119. PMID 7896875. doi:10.1083/jcb.128.6.1111
- ↑ Ott Christian, Iwanciw Dominika, Graness Angela, Giehl Klaudia, Goppelt-struebe Margarete (2003). «Modulation of the Expression of Connective Tissue Growth Factor by Alterations of the Cytoskeleton». Journal of Biological Chemistry. 278 (45): 44305–44311. PMID 12951326. doi:10.1074/jbc.M309140200. Consultado em 15 de maio de 2011
- ↑ Chen J.G., Yang C.P.H., Cammer M., Band Horwitz S. (2003). «Gene Expression and Mitotic Exit Induced by Microtubule-Stabilizing Drugs». Cancer Research. 63 (22): 7891–7899
- ↑ Desai, A., and T. J. Mitchison. 1997. Microtubule polymerization dynamics. Ann. Rev. Cell Dev. Biol. 13:83–117.
- ↑ Weisenberg RC, Deery WJ, Dickinson PJ. 1976. Tubulin-nucleotide interactions during the polymerization and depolymerization of microtubules. Biochemistry 15:4248–54
- ↑ Margolis Robert L., Wilson Leslie (1977). «Addition of colchicine-tubulin complex to microtubule ends: the mechanism of substoichiometric colchicine poisoning» (PDF). Proceedings of the National Academy of Sciences of the United States of America. 74 (8): 3466–3470. PMID 269406. doi:10.1073/pnas.74.8.3466
- ↑ Himes R.H. (1976). «Action of the vinca alkaloids vincristine, vinblastine, and desacetyl vinblastine amide on …» (PDF). Cancer Research. 36 (10): 3798–3802
- ↑ Rowinsky Eric K., Donehower Ross C. (1995). «Paclitaxel (Taxol)». The New England Journal of Medicine. 332 (15): 1004–1014. PMID 7885406. doi:10.1056/NEJM199504133321507. Consultado em 15 de maio de 2011
- ↑ Cortes J.E., Pazdur R. (1995). «Docetaxel» (PDF). Journal of Clinical Oncology. 13 (10). 2643 páginas
