Química organoestânica
A química organoestânica é o estudo da síntese e das propriedades dos compostos organoestânicos ou estananos, que são compostos organometálicos contendo ligações estanho-carbono. O primeiro composto organoestânico descoberto foi o diiodeto de dietilestanho ((CH
3CH
2)
2SnI
2), revelado por Edward Frankland em 1849.[1] A área cresceu rapidamente no começo do século 20, especialmente após a descoberta dos reagentes de Grignard, que são úteis para produzir ligações Sn–C. A área continua prolífica, com muitas aplicações na indústria e atividade contínua de pesquisa acadêmica.[2]
Estrutura
Os compostos organoestânicos são usualmente classificados de acordo com seus estados de oxidação. Os compostos de estanho(IV) são considerados muito mais comuns e mais úteis.
Derivados orgânicos de estanho(IV)
Os derivados tetraorgano são invariavelmente tetraédricos. Compostos do tipo SnRR'R''R''' foram resolvidos em enantiômeros individuais.[3]
Halogenetos organoestânicos
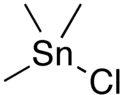
Os cloretos organoestânicos têm a fórmula R
4-nSnCl
n para valores de n até 3. Brometos, iodetos e fluoretos também são conhecidos, mas considerados menos importantes. Esses compostos são conhecidos por apresentarem muitos grupos R, e são sempre tetraédricos. Os tri- e di-haletos formam adutos com bases de Lewis, como a piridina. Os fluoretos tendem a se associar de tal forma que o difluoreto de dimetilestanho forma polímeros em forma de folha. Os haletos di- e especialmente tri-organoestânicos, por exemplo, o cloreto de tributilestanho, apresentam toxicidades que se aproximam daquela do cianeto de hidrogênio.[4]
Hidretos organoestânicos
Os hidretos organoestânicos têm a fórmulaR
4-nSnH
n para valores de n até 3. O membro pai desta série, estanano (SnH
4), é um gás instável e incolor. Sua estabilidade está correlacionada com o número de substituintes orgânicos. O hidreto de tributilestanho é usado como fonte de radical hidreto em algumas reações orgânicas.
Óxidos e hidróxidos organoestânicos
Óxidos e hidróxidos organoestânicos são produtos comuns da hidrólise de haletos organoestânicos. Ao contrário dos derivados correspondentes de silício e germânio, os óxidos e hidróxidos de estanho frequentemente assumem estruturas com centros de estanho penta e até hexacoordenados, especialmente para os derivados diorgano e monoorgano. O grupo SnIV
–O–SnIV
é chamado de estanoxano (que é um análogo de estanho dos éteres), e o grupoSnIV
–O–H também é chamado de estananol (que é um análogo de estanho dos álcoois ).[5] Os derivados triorganoestânicos são os óxidos e hidróxidos estruturalmente mais simples. Um hidróxido de triorganoestanho comercialmente importante é o acaricida cihexaestanho (também chamado de Plictran, hidróxido de triciclohexilestanho e triciclohexilestananol), (C
6H
11)
3SnOH. Os hidróxidos de triorganoestanho existem em equilíbrio com os distanoxanos:
- 2 R
3SnOH ⇌ R
3SnOSnR
3 + H
2O
Com apenas dois substituintes orgânicos em cada centro Sn, os óxidos e hidróxidos diorganoestânicos são estruturalmente mais complexos do que os derivados triorgano.[6] Os dióis geminais simples de estanho (R
2Sn(OH)
2, os análogos de estanho dos dióis geminais R
2C(OH)
2 ) e estananonas monoméricas (R
2Sn=O), e os análogos de estanho das cetonas (R
2C=O) são desconhecidos. Óxidos de diorganoestanho (R
2SnO) são polímeros, exceto quando os substituintes orgânicos são muito volumosos, caso dos trímeros cíclicos ou, no caso em que R é um dímero CH(Si(CH
3)
3)
2, com anéis de Sn
3O
3e Sn
2O
2. Os distanoxanos existem como dímeros com a fórmula [R
2SnX]
2O
2 em que os grupos X (por exemplo, cloreto –Cl, hidróxido –OH, carboxilato RCO
2– ) podem ser terminais ou em ponte (ver Tabela). A hidrólise dos trihaletos de monoorganoestanho tem o potencial de gerar ácidos estananóicos, RSnO
2H. Quanto aos óxidos/hidróxidos diorganoestânicos, as espécies monoorganoestânicas formam estruturas complexas devido à ocorrência de desidratação/hidratação e agregação. A hidrólise do tricloreto de butilestanho resultando em [(CH
3(CH
2)
3Sn)
12O
14(OH)
6]2+ é um exemplo.
-
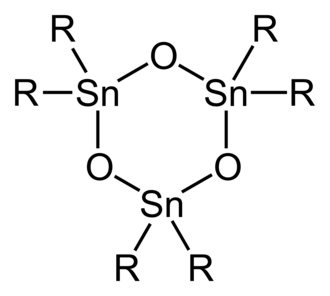 Estrutura idealizada do óxido diorganoestânico trimérico.
Estrutura idealizada do óxido diorganoestânico trimérico. -
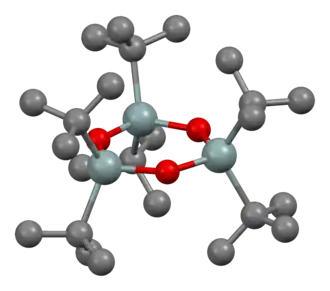 Modelo de bola e bastão para (((CH3)3C)2SnO)3 .
Modelo de bola e bastão para (((CH3)3C)2SnO)3 . -
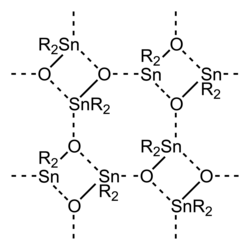 Estrutura do óxido de diorganoestanho, destacando a extensa ligação intermolecular.
Estrutura do óxido de diorganoestanho, destacando a extensa ligação intermolecular.
Estananos hipercoordenados
Diferentemente dos análogos de carbono (IV), mas similar aos compostos de silício, o estanho(IV) também pode ser coordenado em cinco e até seis átomos em vez dos quatro normais. Esses compostos hipercoordenados geralmente têm substituintes eletronegativos. Numerosos exemplos de compostos hipercoordenados são fornecidos pelos óxidos organoestânicos e carboxilatos e derivados associados a pseudohaletos[6] e os haletos organoestânicos para adutos, por exemplo (CH3)2SnCl2(bipiridina).
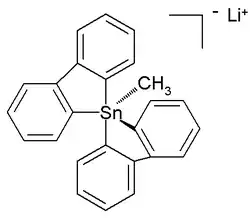
Os penta- e hexaorganoestanatos (IV) totalmente orgânicos foram até mesmo caracterizados,[7] enquanto no ano seguinte um composto tetraorganoestanho de seis coordenadas foi relatado.[8] Uma estrutura cristalina de pentaorganoestanato(IV) de carbono estável à temperatura ambiente (em argônio) foi relatada como o sal de lítio com esta estrutura:[9]
Nesta estrutura bipiramidal trigonal distorcida, os comprimentos de ligação do carbono ao estanho (2,26 Å apical, 2,17 Å equatorial) são mais longas do que as ligações C-Sn regulares (2,14 Å) refletindo sua natureza hipercoordenada.
Cátions triorganoestânicos
Algumas reações de haletos de triorganoestanho implicam um papel para R
3Sn+
intermediários. Esses cátions são análogos aos carbocátions. Eles foram caracterizados cristalograficamente quando os substituintes orgânicos são grandes, como 2,4,6-triisopropilfenil.[10]
Radicais de estanho (derivados orgânicos do estanho(III))
Radicais de estanho, com a fórmula R
3Sn, são chamados radicais estanil.[2] Eles são um tipo de radical tetrel e são invocados como intermediários em certas reações de transferência de átomos. Por exemplo, o hidreto de tributilestanho (tris( n -butil)estanano) serve como uma fonte útil de "átomos de hidrogênio" devido à estabilidade do radical tributilestanho.[11]
Derivados orgânicos de estanho(II)
Os compostos organoestânicos(II) são um tanto raros. Compostos com fórmula empírica SnR
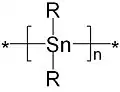
2 são um tanto frágeis e existem como anéis ou polímeros quando R não é volumoso. Os polímeros, chamados poliestananos, têm a fórmula(SnR
2)
n.
Em princípio, espera-se que os compostos de estanho (II) formem análogos de estanho de alcenos com uma ligação dupla formal entre dois átomos de estanho (R
2Sn=SnR
2) ou entre um átomo de estanho e um átomo de grupo carbono (por exemploR
2Sn=CR
2 eR
2Sn=SiR
2). Na verdade, compostos com a fórmula R
2Sn=SnR
2, chamados distanilenos ou distanilenos, que são análogos de estanho dos etilenos R
2C=CR
2, são conhecidos por certos substituintes orgânicos. Os centros Sn nos estanenos são trigonais. Mas, ao contrário dos centros C em alcenos que são trigonais planares, os centros Sn em estanenos tendem a ser altamente piramidais. Compostos monoméricos com a fórmula SnR
2, análogos de estanho de carbenos CR
2 também são conhecidos em alguns casos. Um exemplo é Sn(SiR
3)
2, onde R é o muito volumoso CH(Si(CH
3)
3)
2. Essas espécies dimerizam reversivelmente para o distanileno após a cristalização:[12]
- 2 R
2Sn ⇌ R
2Sn=SnR
2
Os estanenos, compostos com ligações duplas estanho-carbono, são exemplificados por derivados do estanabenzeno. Estanóis, análogos estruturais do ciclopentadieno, exibem pouco caráter de ligação dupla C-Sn.
Derivados orgânicos de estanho(I)
Compostos de Sn(I) são raros e observados apenas com ligantes muito volumosos. Uma família proeminente de gaiolas é acessada pela pirólise do 2,6-dietilfenil-tristanileno substituído [Sn(C6H3-2,6-Et2)2]3, que fornece o cluster do tipo cubano e um prismano. Essas gaiolas contêm Sn(I) e têm a fórmula [Sn(C 6 H 3 -2,6-Et 2 )] n onde n = 8, 10 e Et representa o grupo etila.[13] Um estanho contém um átomo de estanho com um átomo de carbono com ligação tripla (por exemplo R–Sn≡C–R eR–Sn≡Si–R), e uma ligação tripla distante entre dois átomos de estanho (R–Sn≡Sn–R). Distaninos só existem para substituintes extremamente volumosos. Ao contrário dos alcinos, os núcleos C–Sn≡Sn–C dessas distâncias são não-lineares, embora sejam planares. A distância Sn-Sn é 3,066(1) Å, e os ângulos Sn-Sn-C são 99,25(14)°. Esses compostos são preparados pela redução de haletos de arilestanho(II) volumosos.[14]
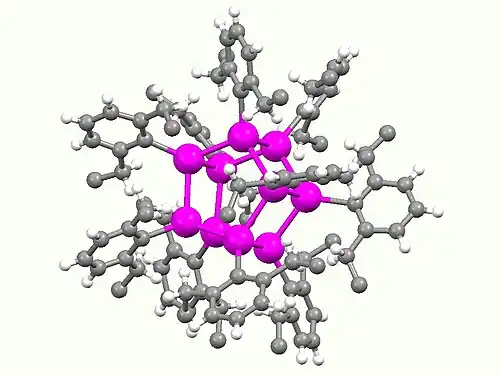
Bolas cinzas: C
Bolas magenta (maiores): Sn
Estrutura de um Ar
10Sn
10 "prismano", um composto contendo Sn(I) (Ar = 2,6-dietilfenil).
Preparação
Os compostos organoestânicos podem ser sintetizados por vários métodos.[15] Clássica é a reação de um reagente de Grignard com haletos de estanho, por exemplo, tetracloreto de estanho. Um exemplo é fornecido pela síntese do tetraetilestanho:[16]
- 4 CH
3CH
2MgBr + SnCl
4 → (CH
3CH
2)
4Sn + 4 MgClBr
Os compostos tetraorganoestânicos simétricos, especialmente os derivados tetraalquilados, podem então ser convertidos em vários cloretos mistos por meio de reações de redistribuição (também conhecidas como "comproporcionamento de Kocheshkov" no caso de compostos organoestânicos):
- 3 R
4Sn + SnCl
4 → 4 R
3SnCl - R
4Sn + SnCl
4 → 2 R
2SnCl
2 - R
4Sn + 3 SnCl
4 → 4 RSnCl
3
Um método relacionado envolve a redistribuição de haletos de estanho com compostos organoalumínio.[2](45-47)
Em princípio, haletos de alquilestanho podem ser formados pela inserção direta do metal na ligação carbono-halogênio. Entretanto, tais reações são temperamentais, normalmente exigindo uma ligação carbono-halogênio muito fraca (por exemplo, um iodeto de alquila ou um haleto de alila) ou um catalisador de sal de metal alcalino complexado em coroa. Ácidos de Lewis ou um solvente iônico também podem promover a reação.[2](51-52)
Os compostos mistos de organo-haloestanho podem ser convertidos em derivados orgânicos mistos, conforme ilustrado pela síntese de dibutildivinilestanho:[17]
- Bu
2SnCl
2 + 2 CH
2=CHMgBr → Bu
2Sn(CH=CH
2)
2 + 2 MgBrCl''";
Os hidretos organoestânicos são gerados pela redução dos cloretos de alquila mistos. Por exemplo, o tratamento do dicloreto de dibutilestanho com hidreto de alumínio e lítio produz o di-hidreto de dibutilestanho, um óleo destilável incolor:
- 2 Bu
2SnCl
2 + Li[AlH
4] → 2 Bu
2SnH
2 + Li[AlCl
4]
O acoplamento tipo Wurtz de compostos de alquil sódio com haletos de estanho produz compostos tetraorganoestânicos.
A hidrostanilação envolve a adição catalisada por metal de hidretos de estanho em substratos insaturados.[18]
Alternativamente, os estanetos atacam eletrófilos orgânicos para produzir organoestananos, por exemplo:[2]:49
- LiSnMe3 + CCl4 → C(SnMe 3 ) 4 + LiCl.
Reações
Reações importantes, discutidas acima, geralmente se concentram em haletos organoestânicos e pseudohaletos com nucleófilos. Os compostos organoestânicos totalmente alquílicos geralmente não se hidrolisam, exceto em ácido concentrado; a principal exceção são os acetiletos de estanho.[19] Uma adição organoestanana é uma adição nucleofílica de um alil-, alenil- ou propargilestanano a aldeídos e iminas, enquanto a hidrostanilação reduz convenientemente apenas ligações múltiplas não polarizadas.[20]
Os hidretos organoestânicos são instáveis às bases fortes, desproporcionais ao gás hidrogênio e aos distananos.[2]:295 Os últimos se equilibram com os radicais correspondentes apenas na presença contínua da base, ou se fortemente impedidos estericamente.[2](299,334-335) Por outro lado, os ácidos minerais clivam os distananos em haletos organoestânicos e mais gás hidrogênio.[2]:300
Na síntese orgânica "pura", a reação de Stille é considerada uma técnica de acoplamento chave. Na reação de Stille, haletos orgânicos hibridizados com sp2 (por exemplo, cloreto de vinilaCH
2=CHCl) catalisado por paládio:
- R1
–X + R2
–Sn(R3
)
3 R1
–R2
+ X–Sn(R3
)
3
Os compostos organoestânicos também são amplamente utilizados na química radicalar (por exemplo, ciclizações radicais, desoxigenação de Barton-McCombie, descarboxilação de Barton, etc.).
Aplicações
Um composto organoestânico é aplicado comercialmente como estabilizante em cloreto de polivinila . Nessa capacidade, eles suprimem a degradação removendo grupos cloreto alílico e absorvendo cloreto de hidrogênio. Esta aplicação consome cerca de 20.000 toneladas de estanho por ano. A principal classe de compostos organoestânicos são os ditiolatos de diorganoestânicos com a fórmula R
2Sn(SR')
2. A ligação Sn-S é o componente reativo. Carboxilatos de diorganoestanho, por exemplo, dilaurato de dibutilestanho, são usados como catalisadores para a formação de poliuretanos, para vulcanização de silicones e transesterificação.[2]
O tricloreto de n -butilestanho é usado na produção de camadas de dióxido de estanho em garrafas de vidro por deposição química de vapor.
Aplicações biológicas
Os "tributilestanhos" são usados como biocidas industriais, por exemplo, como agentes antifúngicos em têxteis e papel, sistemas de fábricas de celulose e papel, cervejarias e sistemas de resfriamento industrial. Derivados de trifenilestanho são usados como componentes ativos de tintas antifúngicas e fungicidas agrícolas. Outros triorganoestânicos são usados como acaricidas e acaricidas. O óxido de tributilestanho tem sido amplamente utilizado como conservante de madeira.[2]
Os compostos de tributilestanho já foram amplamente utilizados como agentes anti- bioincrustantes marinhos para melhorar a eficiência de navios oceânicos. As preocupações com a toxicidade[21] destes compostos (alguns relatórios descrevem efeitos biológicos na vida marinha numa concentração de 1 nanograma por litro) levaram à sua proibição mundial pela Organização Marítima Internacional. Como compostos antiincrustantes, os compostos organoestânicos foram substituídos por diclorooctilisotiazolinona.[22]
- Compostos organoestânicos
-
 Óleo incolor de tetrabutilestanho, precursor de outros compostos de butil-estanho
Óleo incolor de tetrabutilestanho, precursor de outros compostos de butil-estanho -
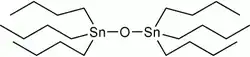 Óxido de tributilestanho, um líquido incolor a amarelo claro usado na preservação de madeira
Óxido de tributilestanho, um líquido incolor a amarelo claro usado na preservação de madeira -
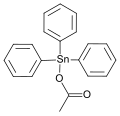 Acetato de trifenilestanho, um sólido cristalino esbranquiçado, usado como inseticida e fungicida
Acetato de trifenilestanho, um sólido cristalino esbranquiçado, usado como inseticida e fungicida -
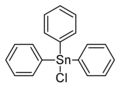 Cloreto de trifenilestanho, um sólido branco altamente tóxico, usado como biocida
Cloreto de trifenilestanho, um sólido branco altamente tóxico, usado como biocida -
 Cloreto de trimetilestanho, um sólido branco tóxico, usado antigamente como biocida
Cloreto de trimetilestanho, um sólido branco tóxico, usado antigamente como biocida -
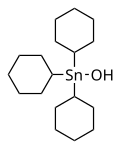
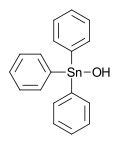 Hidróxido de trifenilestanho, um pó esbranquiçado, usado como fungicida
Hidróxido de trifenilestanho, um pó esbranquiçado, usado como fungicida -
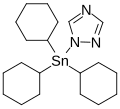 Azocicloestanho, um sólido branco, usado como acaricida de ação prolongada para controle de ácaros em plantas
Azocicloestanho, um sólido branco, usado como acaricida de ação prolongada para controle de ácaros em plantas -
-
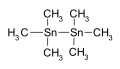 Hexametilditina usada como intermediário em síntese química
Hexametilditina usada como intermediário em síntese química -
![Tetraethyltin, boiling point 63–65° /12 mm [clarification needed] is a catalyst. The "Et" symbol stands for ethyl group.](./_assets_/0c70a452f799bfe840676ee341124611/Tetraethyltin.svg.png) Tetraetilestanho, ponto de ebulição 63–65° /12 milímetros é um catalisador. O símbolo "Et" representa o grupo etila .
Tetraetilestanho, ponto de ebulição 63–65° /12 milímetros é um catalisador. O símbolo "Et" representa o grupo etila .
Toxicidade
As toxicidades dos compostos derivados de tributilestanho e trifenilestanho são comparáveis às do cianeto de hidrogênio. Além disso, os tri -n -alquilestanhos são fitotóxicos e, portanto, não podem ser usados na agricultura. Dependendo dos grupos orgânicos, eles podem ser bactericidas e fungicidas poderosos. Refletindo sua alta bioatividade, os "tributilestanhos" já foram usados em tintas antiincrustantes marinhas.[2] Em contraste com os compostos triorganoestânicos, os compostos monoorganoestânicos, diorganoestânicos e tetraorganoestânicos são muito menos perigosos,[4] embora a DBT possa ser imunotóxica.[23]
Referências
- ↑ Caseri, Walter (2014). «Initial Organotin Chemistry». Journal of Organometallic Chemistry. 751: 20–24. doi:10.1016/j.jorganchem.2013.08.009
- ↑ a b c d e f g h i j k Davies, Alwyn George. (2004) Organotin Chemistry, 2nd Edition Weinheim: Wiley-VCH. ISBN 978-3-527-31023-4
- ↑ Gielen, Marcel (1973). «From kinetics to the synthesis of chiral tetraorganotin compounds». Acc. Chem. Res. 6 (6): 198–202. doi:10.1021/ar50066a004
- ↑ a b Wiley-VCH, ed. (11 de março de 2003). Ullmann's Encyclopedia of Industrial Chemistry (em inglês) 1 ed. [S.l.]: Wiley. Consultado em 23 de maio de 2025
- ↑ «Stannanol | H4OSn | ChemSpider»
- ↑ a b Chandrasekhar, Vadapalli; Nagendran, Selvarajan; Baskar, Viswanathan (2002). «Organotin assemblies containing Sn/O bonds». Coordination Chemistry Reviews. 235: 1–52. doi:10.1016/S0010-8545(02)00178-9
- ↑ Reich, Hans J.; Phillips, Nancy H. (1986). «Lithium-Metalloid Exchange Reactions. Observation of Lithium Pentaalkyl/aryl Tin Ate Complexes». J. Am. Chem. Soc. 108 (8): 2102–2103. doi:10.1021/ja00268a067
- ↑ V. G. Kumar Das; Lo Kong Mun; Chen Wei; Thomas C. W. Mak (1987). «Synthesis, Spectroscopic Study, and X-ray Crystal Structure of Bis[3-(2-pyridyl)-2-thienyl-C,N]diphenyltin(IV): The First Example of a Six-Coordinate Tetraorganotin Compound». Organometallics. 6: 10–14. doi:10.1021/om00144a003
- ↑ Saito, Masaichi; Imaizumi, Sanae; Tajima, Tomoyuki; Ishimura, Kazuya; Nagase, Shigeru (2007). «Synthesis and Structure of Pentaorganostannate Having Five Carbon Substituents». J. Am. Chem. Soc. 129 (36): 10974–10975. PMID 17705378. doi:10.1021/ja072478+
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (em inglês) 2ª ed. [S.l.]: Butterworth-Heinemann. ISBN 978-0-08-037941-8
- ↑ T. V. RajanBabu, P. C. B. Page B. R. Buckley "Tri-n-butylstannane" in e-EROS Encyclopedia of Reagents for Organic Synthesis, 2004. doi:10.1002/047084289X.rt181.pub2
- ↑ Holleman, Arnold Frederik; Wiberg, Egon (2001), Wiberg, Nils (ed.), Inorganic Chemistry, translated by Eagleson, Mary; Brewer, William, San Diego/Berlin: Academic Press/De Gruyter, ISBN 0-12-352651-5.
- ↑ Sita, Lawrence R. (1994). «Heavy-Metal Organic Chemistry: Building with Tin». Acc. Chem. Res. 27 (7): 191–197. doi:10.1021/ar00043a002
- ↑ Power, Philip P. (2007). «Bonding and Reactivity of Heavier Group 14 Element Alkyne Analogues». Organometallics. 26 (18): 4362–4372. doi:10.1021/om700365p
- ↑ Sander H.L. Thoonen; Berth-Jan Deelman; Gerard van Koten (2004). «Synthetic aspects of tetraorganotins and organotin(IV) halides» (PDF). Journal of Organometallic Chemistry (689): 2145–2157
- ↑ Der Kerk, G. J. M. Van; Luijten, J. G. A. (1956). «Tetraethyltin». Org. Synth. 36: 86ff. doi:10.15227/orgsyn.036.0086
- ↑ Seyferth, Dietmar (1959). «Di-n-butyldivinyltin». Org. Synth. 39: 10. doi:10.15227/orgsyn.039.0010
- ↑ Smith, Nicholas D.; Mancuso, John; Lautens, Mark (2000). «Metal-Catalyzed Hydrostannations». Chemical Reviews. 100 (8): 3257–3282. PMID 11749320. doi:10.1021/cr9902695
- ↑ Eisch 1981, pp. 156,169.
- ↑ Elschenbroich, Christoph (2006). Organometallics 3rd ed. [S.l.]: Wiley. p. 310. ISBN 978-3-527-29390-2
- ↑ Gajda, M.; Jancso, A. (2010). «Organotins, Formation, Use, Speciation and Toxicology». Cambridge: RSC publishing. Metal Ions in Life Sciences. 7, Organometallics in environment and toxicology: 111–151. ISBN 9781847551771. doi:10.1039/9781849730822-00111
- ↑ Silva, Vânia; Silva, Cátia; Soares, Pedro; Garrido, E. Manuela; Borges, Fernanda; Garrido, Jorge (2020). «Isothiazolinone Biocides: Chemistry, Biological, and Toxicity Profiles». Molecules. 25 (4): 991. PMC 7070760
 . PMID 32102175. doi:10.3390/molecules25040991
. PMID 32102175. doi:10.3390/molecules25040991
- ↑ C Gumy; et al. (2008). «Dibutyltin Disrupts Glucocorticoid Receptor Function and Impairs Glucocorticoid-Induced Suppression of Cytokine Production». PLOS ONE. 3 (10): e3545. Bibcode:2008PLoSO...3.3545G. PMC 2568824
 . PMID 18958157. doi:10.1371/journal.pone.0003545
. PMID 18958157. doi:10.1371/journal.pone.0003545