Lipogênese
A Lipogênese (português brasileiro) ou Lipogénese (português europeu) é o processo metabólico mediante o qual o corpo converte hidratos de carbono consumidos na dieta em ácidos gordos, que seguidamente são esterificados para formar triacilglicerois e são armazenados em adipócitos. A síntese de ácidos graxos e triglicérides, que serão armazenados subsequentemente no fígado e no tecido adiposo. A Lipogênese é regulada por vários fatores, entre os quais estão os elementos nutricional, hormonal e genético. Geralmente ocorre em dietas hipercalóricas.
A lipogénese começa com acetil-CoA ou malonil-CoA[1] e cresce com a adição de unidades de dois carbonos. A síntese tem lugar no citosol (citoplasma), ao contrário da oxidação β (beta-oxidação), que se produz nas mitocôndrias. Muitas das enzimas que participam na síntese de ácidos gordos estão organizados num complexo multienzimático chamado "ácido gordo sintase".
Nos indivíduos obesos, este processo pode ocorrer fora dos tecidos adiposos. A lipogénese tem uma eficiência baixa, com um custo energético de 20–25% em porcos.[1] A taxa de conversão de hidratos de carbono em triacilglicerois só se torna significativa uma vez que as reservas de energia em forma de glicogénio tenham sido saturadas.[2]
Não há nenhum processo que funcione em sentido contrário, ou seja, que sirva para converter os lípidos em hidratos de carbono no ser humano.[3]
Mecanismo
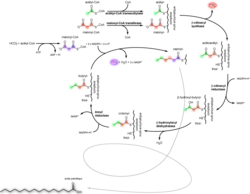
Pelas vias normais de glicólise a glicose é transformada em piruvato que depois é transformado em acetil-CoA, pela ação da piruvato desidrogenase[1]. O acetil-CoA entra no Ciclo de Krebs (CK) unindo-se ao oxaloacetato (OAA(também sintetizado a partir de certos aminoácidos)) formando citrato, onde ocorre a diferença para a lipogênese no CK, mas que em situações normais segue o CK gerando equivalentes de redução para a cadeia respiratória (Cadeia Oxidativa Mitocondrial Transportadora de Elétrons - COMTE, que seria o nome "mais correto") passando para a Fosforilação Oxidativa, onde há a produção de ATP (trifosfato de adenosina).
Neste momento que ocorre a primeira diferenciação para lipogênese, pois ATP sendo produzido em quantidades desnecessárias (em excesso) gera efetores para todas vias metabólicas antecedentes, ou seja, todas as rotas desaceleram, porém o citrato continua a ser produzido, pois ele em excesso acaba não gerando efetores, e sim extravasando para o citosol através da tricarboxilato translocase, uma proteína de membrana da mitocôndria.
O citrato agora no citosol é transformado novamente em acetil-CoA e OAA, através da citrato liase (altamente estimulada por insulina). O OAA é transformado em malato pela malato desidrogenase e é transportado de volta para o interior da mitocôndria, onde mantem uma constante com OAA, e permite que siga contínua a lipogênese, pois é o precursor do citrato, como dito anteriormente.
Já o acetil-CoA gerado entra em uma via metabólica que produzirá ácidos graxos, sendo ela: primeiro passo: Acetil-CoA gera Maloni-CoA, que logo perde sua coenzima A e começa a ser transportada por uma Proteína Carregadora de Acila (ACP) carregando um grupamento 4-fosfopanteteína (cofator - Vitamina B5) formando a Malonil-ACP; segundo passo: ocorre uma reação cíclica onde uma cascata complexa une outro acetil-Coa a esse Malonil-ACP, este ACP retorna ao início do ciclo mais seis vezes, ao final de todas estas vias é formando o palmitato, que é um éster de 16 carbonos que é precursor dos ácidos graxos saturados de cadeia longa do organismo humano que exercem suas devidas diferenciações e funções, mas também armazenados no tecido adiposo na forma de triglicerídeos.
Referências
- ↑ a b c Solinas, G.; Borén, J.; Dulloo, A. G. (2015). «De novo lipogenesis in metabolic homeostasis: More friend than foe?». Molecular Metabolism (em inglês). 4 (5): 367–377. PMC 4443306
 . PMID 26046187. doi:10.1016/j.molmet.2015.03.004
. PMID 26046187. doi:10.1016/j.molmet.2015.03.004
- ↑ Schutz, Y. (2004). «Concept of fat balance in human obesity revisited with particular reference to de novo lipogenesis». International Journal of Obesity (em inglês). 28: S3–S11. PMID 15592534. doi:10.1038/sj.ijo.0802852
- ↑ Hellerstein, M. K. (1999). «De novo lipogenesis in humans: metabolic and regulatory aspects». European Journal of Clinical Nutrition (em inglês). 53 (supplement 1): S53–S65. PMID 10091913. doi:10.1038/sj.ejcn.1600744