Piruvato desidrogenase
| piruvato desidrogenase (lipoamida) alfa 1 | |
|---|---|
| Indicadores | |
| Símbolo | PDHA1 |
| Símbolos alt. | PDHA |
| HUGO | 8806 |
| Entrez | 5160 |
| OMIM | 300502 |
| RefSeq | NM_000284 |
| UniProt | P08559 |
| Outros dados | |
| Número EC | 1.2.4.1 |
| Locus | Cr. X p22.1 |
| piruvato desidrogenase (lipoamida) alfa 2 | |
|---|---|
| Indicadores | |
| Símbolos alt. | PDHAL |
| HUGO | 8807 |
| Entrez | 5161 |
| OMIM | 179061 |
| RefSeq | NM_005390 |
| UniProt | P29803 |
| Outros dados | |
| Número EC | 1.2.4.1 |
| Locus | Cr. 4 q22-q23 |
| piruvato desidrogenase (lipoamida) beta | |
|---|---|
| Indicadores | |
| Símbolo | PDHB |
| HUGO | 8808 |
| Entrez | 5162 |
| OMIM | 179060 |
| RefSeq | NM_000925 |
| UniProt | P11177 |
| Outros dados | |
| Número EC | 1.2.4.1 |
| Locus | Cr. 3 p21.1-14.2 |
A piruvato desidrogenase é o primeiro componente do complexo enzimático piruvato desidrogenase. EC 1.2.4.1.
Função
E1 executa a primeira de duas reacções no complexo. Elas são:
- descarboxilação do substrato 1, o piruvato.
- acetilação redutiva do substrato 2, ácido lipóico. O ácido lipóico está ligado de maneira covalente à dihidrolipoil transacetilase (E2), que é o segundo componente catalítico do complexo.
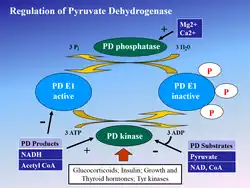
Regulação
Fosforilação de E1 pela piruvato desidrogenase quinase inativa E1 e subsequentemente todo o complexo.
Esta ação é revertida pela alta relação Insulina/Glucagon, que têm como consequência o aumento da transcrição da piruvato desidrogenase fosfatase, e repressão do gene da piruvato desidrogenase quinase. Tal mecanismo resulta em alta produção de Acetil-CoA.
Genes
E1 é uma proteína multimérica:
- As E1 de mamíferos, incluindo a E1 humana, são tetraméricas, compostas de duas subunidades α e duas subunidades β.[1]
- algumas E1 bacterianas, incluindo a E1 de Escherichia coli, são compostas por duas subunidades similares, cada uma delas com uma massa molecular tão grande quanto a soma das subunidades α e β.[2]
Outras formas
Em bactérias, existe uma forma de piruvato desidrogenase, também denominada piruvato oxidase (EC 1.2.2.2). Esta enzima liga a oxidação do piruvato em acetato e dióxido de carbono à redução de ferrocitrocromo. Em E. coli esta enzima é codificada pelo gene pox B e a proteína possui um cofactor flavínico.[3] A enzima aumenta a eficiência do crescimento de E. coli sob condições aeróbica.[4]
Referências
- ↑ Ciszak E, Korotchkina L, Dominiak P, Sidhu S, Patel M (2003). «Structural basis for flip-flop action of thiamin pyrophosphate-dependent enzymes revealed by human pyruvate dehydrogenase». J Biol Chem. 278 (23): 21240-6. PMID 12651851
- ↑ Arjunan P, Nemeria N, Brunskill A, Chandrasekhar K, Sax M, Yan Y, Jordan F, Guest JR, Furey W. (2002). «Structure of the pyruvate dehydrogenase multienzyme complex E1 component from Escherichia coli at 1.85 A resolution». Biochemistry. 41 (16): 5213-21. PMID 11955070
- ↑ Recny MA, Hager LP (1982). «Reconstitution of native Escherichia coli pyruvate oxidase from apoenzyme monomers and FAD». J. Biol. Chem. 257 (21): 12878-86. PMID 6752142
- ↑ Abdel-Hamid AM, Attwood MM, Guest JR (2001). «Pyruvate oxidase contributes to the aerobic growth efficiency of Escherichia coli». Microbiology (Reading, Engl.). 147 (Pt 6): 1483-98. PMID 11390679