Alaranjado de metila
Alaranjado de metila
| |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||
 | |||||||||||||||
 | |||||||||||||||
| Nomes | |||||||||||||||
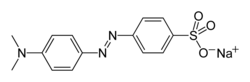
| Nome IUPAC | 4-dimethylaminoazobenzene-4'-sulfonic acid sodium salt | ||||||||||||||
| Outros nomes | ácido p-dimetilamino-azobenzenosulfônico | ||||||||||||||
| |||||||||||||||
| |||||||||||||||
| |||||||||||||||
| Página de dados suplementares | |||||||||||||||
| Estrutura e propriedades | n, εr, etc. | ||||||||||||||
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas | ||||||||||||||
| Dados espectrais | UV, IV, RMN, EM | ||||||||||||||
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão. Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |||||||||||||||
Alaranjado de metila, também chamado de alaranjado de metilo, laranja de metila, laranja de metilo, heliantina ou ainda metilorange (MO) é um indicador de pH frequentemente usado em titulações.É extraido de um inseto
É frequentemente escolhido para ser usado em titulações por causa de sua clara mudança de coloração. Devido a sua mudança de coloração na faixa de pH medianamente ácido, é normalmente usado em titulações de ácidos. Diferentemente de um indicador universal, o alaranjado de metila não tem um largo espectro de mudança de cores, mas tem um bem definido ponto final.
Sua fórmula química é C14H14N3O3SNa quando se apresenta na forma de sal de sódio. O par ácido-base correspondente é C14H14N3O3S-OH / C14H14N3O3S-O-. A pKa do par é 3,39.
Obtenção
É produzido pela reação de copulação entre o sal de diazônio do ácido sulfanílico com a dimetilanilina. Posteriormente, leva-se o corante obtido à sua forma de sal de sódio.[1]
O primeiro passo é chamado diazotação, onde o sulfanilato de sódio é formado e reage com nitrito de sódio em presença de ácido clorídrico (i.e., formação do cátion nitroso), formando o instável sal de diazônio. O segundo passo é a reação de copulação do diazônio. O íon diazônio é usado in situ e reage com a N,N-dimetilanilina para formar o azocorante ácido. Este corante bruto poderá ser isolado, e usado na coloração de nylon, por exemplo, ou reagido com álcali como o hidróxido de sódio ou o carbonato de sódio, de maneira a formar o seu sal de sódio, mais solúvel em água, que é a forma na qual é usado como indicador de pH.[1][2][3]
A síntese do alaranjado de metila é possível a partir de dois líquidos ionizados, o íon 1-hexil-3-metilimidazôlium como cátion e tanto o hexafluorofosfato (PF6−) ou o perclorato (ClO4−) no papel de ânion como solventes para a reação. A vantagem apontada do uso de líquidos iônicos inclui sua reciclagem, a maior estabilidade dos intermediários e rendimentos de reação mais altos. Os derivados de 1-hexil-3-metilimidazôlium podem ser usados para sínteses conduzidas a mais baixas temperaturas e são menos tóxicos que os solventes orgânicos típicos.[4]O
Cores do indicador
| Alaranjado de Metila (indicador de pH)[5] | ||
| pH abaixo de 3.1 | pH acima de 4.4 | |
| vermelho | ⇌ | amarelo |
Em uma solução começando a se tornar menos ácida, o alaranjado de metila tornar-se-á de vermelho para laranja, e caso o processo continue, para amarelo. Processo inverso ocorre para uma solução aumentando em acidez.
Nesta aplicação como indicador, normalmente é utilizado em uma concentração em solução de 0,1 % (1 g / litro) e na titulação a 1 gota para cada 10 ml de líquido a titular.
Outros indicadores
- Alaranjado de metila modificado, comumente citada como solução de alaranjado de metila-xileno cianol, um indicador consistindo de uma solução de alaranjado de metila e xileno cianol, muda de púrpura a verde se a solução torna-se básica.[6][7]
| Alaranjado de Metila em Solução de Xileno Cianol (indicador de pH) | ||
| pH abaixo de 3.2 | pH acima de 4.2 | |
| púrpura | ⇌ | verde |
- Vários outros indicadores normalmente usados são tabelados com seus intervalos de mudança de coloração no verbete sobre indicadores de pH.
Outras aplicações
Também é utilizado em citologia em conjunto com a solução de fucsina. É usado para a identificação de bromo livre em oxidações com bromato de potássio em titulações redox.[8]
Preparo das soluções
Como indicador ácido-base
O indicador é normalmente usado em solução aquosa, dissolvendo-se 0,5 gramas do indicador, seja na forma de ácido livre ou de sal sódico em um litro de água (de onde alaranjado de metila 0,05% aquoso), preferencialmente a quente, e filtrar a solução se houver um precipitado.[8]
Verde de bromocresol-alaranjado de metila
Esta solução muda de laranja para verde azulado a pH 4,2. É produzida pela mistura de uma parte de verde de bromocresol a 0,1% em água (como 0,1 grama em 100 ml) com 1 parte de alaranjado de metila a 0,2 % em água (como 0,2 grama em 100 ml).[8]
Xileno cianol FF-alaranjado de metila
Solução que muda de pH do alcalino para o ácido passando pelas cores verde, cinzento e carmin, com estágio intermediário no cinzento a pH 3,8. É produzida pela dissolução de 1,0 grama de alaranjado de metila e 1,4 grama de xileno cianol FF em etanol a 50% aquoso. É um exemplo de indicador realçado, e no caso, como o indicador é o alaranjado de metila, de um indicador misto de alaranjado de metila realçado.[8]
Referências
- ↑ a b Arthur I. Vogel- Química orgânica qualitativa 3vol- Ao Livro Técnico 1971.
- ↑ Murray Zanger, James McKee; Small Scale Synthesis: A Laboratory Text of Organic Chemistry, Spiralbound, McGraw-Hill, 2002. pp 363. ISBN: 0072846038 ISBN-13: 9780072846034
- ↑ McMurry, J., Organic Chemistry, 7th Ed., Brooks Cole, 2007. pp 500-3 (UV-Vis spectroscopy) and 941-5 (diazonium ions and their coupling reactions) [6th Ed.: pp 483-6, 917-21] ISBN-10: 0495118370 ISBN-13: 978-0495118374
- ↑ Danette L. Astolfi and Francis C. Mayville, Jr.; Synthesis of methyl orange using ionic liquids Arquivado em 24 de janeiro de 2013, no Wayback Machine.; Tetrahedron Letters 44 (2003) 9223–9224.
- ↑ PubChem. «Methyl orange». pubchem.ncbi.nlm.nih.gov (em inglês). Consultado em 22 de abril de 2025
- ↑ Acid Base Indicators Arquivado em 16 de julho de 2011, no Wayback Machine. - ifs.massey.ac.nz (em inglês)
- ↑ Preparation of Acid-Base Indicators - www.csudh.edu
- ↑ a b c d Mendham, J.; Denney, R.C.; Barnes, J.D. & Thomas, M.J.K. - Vogel: Análise Química Quantitativa. 4a. edição (Traduzido por Aïda Espinola, COPPE - UFRJ), Rio de Janeiro, Guanabara Dois (1981), 690pp
Ver também
Compostos estruturalmente similares: