Hydnellum peckii
Hydnellum peckii
| |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||
| Classificação científica | |||||||||||||||||
| |||||||||||||||||
| Nome binomial | |||||||||||||||||
| Hydnellum peckii Banker [en] (1912) | |||||||||||||||||
| Sinónimos[1] | |||||||||||||||||
| |||||||||||||||||
Hydnellum peckii[1] é um fungo do gênero Hydnellum da família Bankeraceae [en]. É uma espécie hidnoide que produz esporos na superfície de espinhos verticais ou projeções semelhantes a dentes que pendem da superfície inferior dos corpos dos corpos frutíferos. É encontrado na América do Norte, na Europa e também foi descoberto no Irã (2008) e na Coreia (2010). Hydnellum peckii é uma espécie micorriza e forma relações mutuamente benéficas com uma variedade de árvores coníferas, crescendo no solo de forma isolada, dispersa ou em massas fundidas.
Os corpos frutíferos normalmente têm um píleo em forma de funil com uma borda branca, embora a forma possa ser muito variável. Os corpos frutíferos jovens e úmidos podem “sangrar” gotículas de gutação vermelha brilhante que contêm um pigmento conhecido por ter propriedades anticoagulantes semelhantes à heparina. Embora os corpos frutíferos do Hydnellum peckii sejam facilmente identificáveis quando jovens, eles se tornam marrons e indescritíveis quando envelhecem.
Taxonomia
A espécie foi descrita cientificamente pela primeira vez pelo micologista americano Howard James Banker [en] em 1913.[2] O italiano Pier Andrea Saccardo colocou a espécie no gênero Hydnum em 1925,[3] enquanto Walter Henry Snell [en] e Esther Amelia Dick a colocaram em Calodon em 1956;[4] Hydnum peckii (Banker) Sacc. e Calodon peckii Snell [en] & E.A.Dick são sinônimos de Hydnellum peckii.[1]
O fungo é classificado no clado Diabolum do gênero Hydnellum, um agrupamento de espécies semelhantes com as seguintes características compartilhadas: carne marcada por linhas concêntricas que formam zonas alternadamente claras e escuras (zonadas); sabor extremamente apimentado; odor adocicado; esporos elipsoides, não amiloides (ou seja, não absorvem iodo quando corados com o reagente de Melzer), acianófilos (não coram com o reagente azul de metila) e cobertos por tubérculos; presença de fíbulas nas hifas.[5]
Etimologia
O epônimo específico homenageia o micologista Charles Horton Peck.[6] O fungo é conhecido no vernáculo por vários nomes, incluindo “strawberries and cream” (morangos e creme), “bleeding Hydnellum” (Hydnellum sangrento),[7] “red-juice tooth” (dente de suco vermelho), “Peck's hydnum” (hydnum de Peck),[8] “bleeding tooth fungus” (fungo do dente sangrento),[9] e “devil's tooth” (dente do diabo).[10]
Descrição
Como em todos os fungos produtores de cogumelos, os corpos frutíferos (esporocarpos) são as estruturas reprodutivas produzidas a partir do micélio fúngico quando as condições ambientais adequadas de temperatura, umidade e disponibilidade de nutrientes são atendidas. O Hydnellum peckii é um fungo hidnoide estipitado, o que significa que ele tem um píleo sobre um estipe (caule) e uma forma semelhante a um Hydnum, caracterizada por um himênio semelhante a um dente, em vez de lamelas ou poros na parte inferior da capa. Os corpos frutíferos que crescem próximos uns dos outros muitas vezes parecem se fundir (isso é chamado de “confluência”). Eles podem atingir uma altura de até 10,5 cm.[5] Os corpos frutíferos frescos exsudam um fluido vermelho espesso e marcante quando estão úmidos,[2] presente até mesmo em espécimes jovens, que têm aparência de grumos.[11]

A superfície do píleo é convexa a achatada, mais ou menos irregular e, às vezes, ligeiramente afundada no centro. Geralmente é densamente coberta por “pelos” que lhe conferem uma textura semelhante à do feltro ou veludo; esses pelos são removidos com a idade, deixando os píleos dos espécimes maduros lisos.[5] Seu formato varia de um pouco redondo a irregular, de 4 a 10 cm, ou até 20 cm de largura como resultado da confluência. O píleo é inicialmente esbranquiçado, mas depois se torna levemente marrom, com manchas irregulares marrom-escuras a quase pretas onde está "machucado". Na maturidade, a superfície é fibrosa e resistente, escamosa e irregular, marrom-acinzentada na parte superior do píleo e um pouco lenhosa. A carne é de um marrom rosado pálido.[12] A esporada é marrom.[13]
Os espinhos são delgados, cilíndricos e afilados, com menos de 5 mm de comprimento, e ficam mais curtos perto da borda do píleo. Eles são aglomerados, com normalmente entre três e cinco dentes por milímetro quadrado.[2] Inicialmente branco-rosado, eles envelhecem para um marrom-acinzentado.[6] O caule é espesso, muito curto e frequentemente deformado. Ele se torna bulboso onde penetra no solo e pode se enraizar no solo por vários centímetros. Embora possa atingir até 5 cm de comprimento total e tenha de 1 a 3 cm de largura, apenas cerca de 0,1 a 1 cm aparecem acima do solo. A parte superior é coberta com os mesmos dentes encontrados na parte inferior do píleo, enquanto a parte inferior é peluda e frequentemente envolve detritos do solo da floresta.[14] O odor do corpo do fruto foi descrito como “suave a desagradável”,[6] ou, como Banker sugeriu em sua descrição original, semelhante ao das nozes de Carya.[2]
Características microscópicas

Na esporada, os esporos parecem marrons. Observá-los com um microscópio de luz revela detalhes mais finos de sua estrutura: eles são aproximadamente esféricos, mas terminam abruptamente em um pequeno ponto, suas superfícies são cobertas por pequenos nódulos semelhantes a verrugas e seu tamanho é entre 5,0-5,3 por 4,0-4,7 μm. Os esporos são inamiloides, o que significa que não absorvem iodo quando corados com o reagente de Melzer.[5]
As células da Hydnellum peckii (as hifas) também apresentam vários caracteres úteis para sua caracterização. As hifas que formam a capa são hialinas (translúcidas), lisas, de paredes finas e com 3-4 μm de espessura. Elas colapsam quando secas, mas podem ser prontamente reavivadas com uma solução fraca (2%) de hidróxido de potássio. Os do píleo formam um emaranhado intrincado com tendência a se estender longitudinalmente. Elas são divididas em compartimentos celulares (septos) e têm fíbulas - ramos curtos que conectam uma célula à célula anterior para permitir a passagem dos produtos da divisão nuclear.[2] Os basídios, as células portadoras de esporos no himênio, são em forma de clube, com quatro esporos e medem 35-40 por 4,7-6 μm.[5]
Espécies similares
O Hydnellum diabolus (o epíteto da espécie recebe o neutro diabolum em algumas publicações)[5][15] tem uma aparência muito semelhante, tanto que alguns a consideram sinônimo do H. peckii; diz-se que o H. diabolus tem um odor adocicado e pungente que não existe no H. peckii.[16] As diferenças entre as duas espécies são ampliadas em espécimes maduros: o H. diabolus tem um caule irregularmente espessado, enquanto o caule do H. peckii é espessado por uma “camada esponjosa definida”. Além disso, os espécimes antigos do H. peckii têm um píleo liso, enquanto o H. diabolus é tomentoso.[5] A espécie relacionada H. pineticola também exala gotículas rosadas de líquido quando jovem e úmida. Comumente encontrada crescendo sob coníferas no nordeste da América do Norte, o H. pineticola tem um sabor “desagradável”, mas não azedo.[7] Os corpos frutíferos tendem a crescer isoladamente, em vez de em grupos fundidos, e, ao contrário do H. peckii, não têm hastes bulbosas.[17]
A análise molecular com base nas sequências do DNA espaçador interno transcrito de várias espécies de Hydnellum colocou o H. peckii como o mais intimamente relacionado ao Hydnellum ferrugineum e ao Hydnellum spongiosipes [en].[18]
O Abortiporus biennis [en] não tem dentes, mas produz gotículas vermelhas a partir de poros expostos.[19]
Ecologia
O Hydnellum peckii é um fungo micorrízico e, como tal, estabelece uma relação mutualística com as raízes de determinadas árvores (chamadas de “hospedeiras”), na qual o fungo troca minerais e aminoácidos extraídos do solo por carbono fixo do hospedeiro. As hifas subterrâneas do fungo formam uma bainha de tecido ao redor das raízes de uma ampla variedade de espécies de árvores, em uma associação íntima que é especialmente benéfica para o hospedeiro (denominada ectomicorrízica), pois o fungo produz enzimas que mineralizam compostos orgânicos e facilitam a transferência de nutrientes para a árvore.[20]
As estruturas ectomicorrízicas do H. peckii estão entre as poucas da família Bankeraceae que foram estudadas em detalhes. Elas são caracterizadas por um manto plectenquimatoso - uma camada de tecido feita de hifas firmemente dispostas em uma orientação paralela, ou paliçada, e que raramente se ramificam ou se sobrepõem umas às outras. Essas hifas, juntamente com as partículas minerais aderentes do solo, são incorporadas em uma matriz gelatinosa. As hifas da ectomicorriza podem se transformar em clamidósporos, uma adaptação que ajuda o fungo a tolerar condições desfavoráveis. Os clamidósporos do H. peckii têm uma estrutura peculiar - marcadamente distinta dos de outras Bankeraceae - com paredes internas grossas e lisas e uma parede externa que é dividida radialmente em "verrugas". A característica mais marcante das ectomicorrizas como um todo é a forma como as camadas externas pretas das seções mais antigas se desprendem, dando uma “aparência carbonizada”.[21] A maior parte da biomassa subterrânea do fungo está concentrada perto da superfície,[22] provavelmente como “tapetes miceliais” - aglomerados densos de ectomicorrizas e micélio.[23] Sabe-se também que o micélio se estende muito além do local dos corpos frutíferos, chegando a 337 centímetros de distância.[23]
Técnicas moleculares foram desenvolvidas para ajudar nos esforços de conservação de fungos hidnoides estipitados, incluindo o H. peckii. Embora a distribuição do fungo tenha sido tradicionalmente determinada pela contagem dos corpos frutíferos, esse método tem uma grande desvantagem, pois os corpos frutíferos não são produzidos de forma consistente todos os anos, e a ausência de corpos frutíferos não é uma indicação da ausência de seu micélio no solo.[24] Técnicas mais modernas que usam a reação em cadeia da polimerase para avaliar a presença do DNA fúngico no solo ajudaram a aliviar os problemas no monitoramento da presença e da distribuição dos micélios do fungo.[25]
Habitat e distribuição

Os corpos frutíferos do Hydnellum peckii são encontrados em crescimento solitário, espalhados ou agrupados no solo sob coníferas, geralmente entre musgos e pinheiros. O H. peckii é um fungo de “estágio tardio” que, em florestas boreais dominadas por pinheiros Pinus banksiana, normalmente começa a se associar a hospedeiros mais maduros depois que o dossel se fecha.[26] Foi observada uma preferência por ecossistemas montanhosos ou subalpinos.[6]
O fungo tem uma ampla distribuição na América do Norte e é particularmente comum no noroeste do Pacífico;[27] sua área de distribuição se estende do norte ao Alasca e do leste à Carolina do Norte.[8] Na área de Puget Sound, no estado americano de Washington, ele é encontrado em associação com Pseudotsuga menziesii, abeto e Tsuga.[5] Ao longo da costa do Oregon, foi coletado sob o pinheiro Pinus contorta.[14] Além da América do Norte, o cogumelo é muito difundido na Europa e sua presença foi documentada na Itália,[28] Alemanha,[29] e Escócia.[30] A espécie é comum neste último local, mas está se tornando cada vez mais rara em vários países europeus, como Noruega,[31] Holanda,[32] e República Tcheca.[33] O aumento da poluição na Europa Central foi sugerido como um possível fator para o declínio do cogumelo na região.[30] Relatórios do Irã em 2008[34] e da Coreia em 2010[35] foram os primeiros fora da Europa e da América do Norte.
Usos
Os corpos frutíferos do H. peckii foram descritos como parecidos com “massa dinamarquesa coberta com geleia de morango”.[7] As espécies de Hydnellum não são conhecidas por serem venenosas,[36] mas não são particularmente comestíveis devido ao seu sabor desagradável.[7] Esse sabor azedo persiste mesmo em espécimes secos.[27]
Os corpos frutíferos dessa e de outras espécies de Hydnellum são muito utilizados para criação de corantes.[37] As cores podem variar de bege, quando não é usado mordente, a vários tons de azul ou verde, dependendo do mordente adicionado.[27]
Química
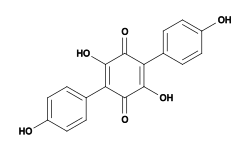
A triagem de um extrato de Hydnellum peckii revelou a presença de um anticoagulante eficaz, denominado atromentina [en] (2,5-dihidroxi-3,6-bis(4-hidroxifenil)-benzoquin-1,4-ona), e semelhante em atividade biológica ao conhecido anticoagulante heparina.[38] A atromentina também possui atividade antibacteriana, inibindo a enzima proteína transportadora de enoil-acil redutase (essencial para a biossíntese de ácidos graxos) na bactéria Streptococcus pneumoniae.[39]
O Hydnellum peckii pode acumular o metal césio. Em um trabalho de campo sueco, até 9% do césio total dos 10 cm superiores do solo foi encontrado no micélio fúngico.[22] Em geral, os fungos ectomicorrízicos, que crescem mais prolificamente nos horizontes orgânicos superiores do solo ou na interface entre as camadas orgânica e mineral, estão envolvidos na retenção e no ciclo do césio-137 em solos florestais ricos em compostos orgânicos.[40]
Referências
- ↑ a b c «Hydnellum peckii Banker 1913». MycoBank. International Mycological Association. Consultado em 4 de outubro de 2010
- ↑ a b c d e Banker HJ. (1913). «Type studies in the Hydnaceae: V. The genus Hydnellum». Mycologia. 5 (4): 194–205. JSTOR 3753385. doi:10.2307/3753385
- ↑ Saccardo PA, Trotter A (1925). «Supplementum Universale, Pars X. Basidiomycetae». Sylloge Fungorum (em latim). 23: 470
- ↑ Snell WA, Dick EA, Jackson HA, Taussig M (1956). «Notes on the pileate hydnums. III». Lloydia. 19 (3): 163–75
- ↑ a b c d e f g h «Pileate Hydnaceae of the Puget Sound area III. Brown-spored genus: Hydnellum». Mycologia. 64 (3): 560–90. 1972. JSTOR 3757873. doi:10.2307/3757873
- ↑ a b c d Evenson VS. (1997). Mushrooms of Colorado and the Southern Rocky Mountains. [S.l.]: Westcliffe Publishers. p. 168. ISBN 978-1-56579-192-3. Consultado em 10 de janeiro de 2010
- ↑ a b c d Arora D. (1986). Mushrooms Demystified: a Comprehensive Guide to the Fleshy Fungi. Berkeley, CA: Ten Speed Press. p. 627. ISBN 978-0-89815-169-5. Consultado em 10 de janeiro de 2010
- ↑ a b Sept JD. (2006). Common Mushrooms of the Northwest: Alaska, Western Canada & the Northwestern United States. Sechelt, BC, Canada: Calypso Publishing. p. 68. ISBN 978-0-9739819-0-2
- ↑ Barron G. (Maio de 2002). «Hydnellum peckii». George Barron's Website on Fungi. University of Guelph. Consultado em 5 de outubro de 2010. Cópia arquivada em 6 de junho de 2011
- ↑ Phillips R. «Hydnellum peckii». Roger's Mushrooms. Consultado em 11 de janeiro de 2010. Cópia arquivada em 31 de dezembro de 2010
- ↑ Trudell, Steve; Ammirati, Joe (2009). Mushrooms of the Pacific Northwest. Col: Timber Press Field Guides (em inglês). Portland, OR: Timber Press. pp. 232–233. ISBN 978-0-88192-935-5
- ↑ Ellis JB, Ellis MB (1990). Fungi without Gills (Hymenomycetes and Gasteromycetes): an Identification Handbook. London: Chapman and Hall. p. 106. ISBN 978-0-412-36970-4. Consultado em 10 de janeiro de 2010
- ↑ «Hydnellum peckii, Devil's Tooth, identification». www.first-nature.com. Consultado em 13 de dezembro de 2019
- ↑ a b Orr DB, Orr RT (1979). Mushrooms of Western North America. Berkeley, CA: University of California Press. p. 56. ISBN 978-0-520-03656-7
- ↑ Tylukti EE. (1987). Mushrooms of Idaho and the Pacific Northwest Vol. 2 Non-gilled hymenomycetes. Moscow, Idaho: The University of Idaho Press. pp. 158–59. ISBN 978-0-89301-097-3
- ↑ Miller HR, Miller OK (2006). North American Mushrooms: a Field Guide to Edible and Inedible Fungi. Guilford, CN: Falcon Guide. p. 405. ISBN 978-0-7627-3109-1. Consultado em 10 de janeiro de 2010
- ↑ Harrison KA, Grund DW (1987). «Preliminary keys to the terrestrial stipitate hydnums of North America». Mycotaxon. 28 (2): 419–26. Consultado em 10 de outubro de 2010. Cópia arquivada em 30 de outubro de 2018
- ↑ Parfitt D, Ainsworth AM, Simpsom D, Rogers HJ, Boddy L (2007). «Molecular and morphological discrimination of stipitate hydnoids in the genera Hydnellum and Phellodon». Mycological Research. 111 (7): 761–77. PMID 17681224. doi:10.1016/j.mycres.2007.05.003
- ↑ Audubon (2023). Mushrooms of North America. [S.l.]: Knopf. 213 páginas. ISBN 978-0-593-31998-7
- ↑ Näsholm T, Ekblad A, Nordin A, Giesler R, Högberg M, Högberg P (1998). «Boreal forest plants take up organic nitrogen». Nature. 392 (6679): 914–16. Bibcode:1998Natur.392..914N. doi:10.1038/31921
- ↑ Agerer R. (1993). «Ectomycorrhizae of Hydnellum peckii on Norway Spruce and their chlamydospores». Mycologia. 85 (1): 74–83. JSTOR 3760481. doi:10.2307/3760481
- ↑ a b Vinichuk MM, Johanson KJ, Taylor AF (2003). «137Cs in the fungal compartment of Swedish forest soils». Science of the Total Environment. 323 (1–3): 243–51. Bibcode:2004ScTEn.323..243V. PMID 15081731. doi:10.1016/j.scitotenv.2003.10.009
- ↑ a b van der Linde S, Alexander IJ, Anderson IC (2009). «Spatial distribution of sporocarps of stipitate hydnoid fungi and their belowground mycelium». FEMS Microbiology Ecology. 69 (3): 344–52. PMID 19558589. doi:10.1111/j.1574-6941.2009.00716.x

- ↑ Cairney JWG. (2005). «Basidiomycete mycelia in forest soils: dimensions, dynamics and roles in nutrient distribution». Mycological Research. 109 (1): 7–20. PMID 15736859. doi:10.1017/S0953756204001753
- ↑ van der Linde S, Alexander I, Anderson IC (2008). «A PCR-based method for detecting the mycelia of stipitate hydnoid fungi in soil». Journal of Microbiological Methods. 75 (1): 40–46. PMID 18586344. doi:10.1016/j.mimet.2008.04.010
- ↑ Visser S. (1995). «Ectomycorrhizal fungal succession in jack pine stands following wildfire». New Phytologist. 129 (3): 389–401. JSTOR 2558393. doi:10.1111/j.1469-8137.1995.tb04309.x

- ↑ a b c Bessette A, Bessette AR (2001). The Rainbow Beneath my Feet: a Mushroom Dyer's Field Guide. Syracuse: Syracuse University Press. p. 118. ISBN 978-0-8156-0680-2. Consultado em 7 de outubro de 2010
- ↑ Papetti C, Chiari M, Restelli V (2006). «Notes on the mycoflora of Brescia». Bollettino del Circolo Micologico G. Carini (em italiano). 52: 3–8. ISSN 1122-5262
- ↑ Doll R. (1979). «Distribution of the stipitate Hydnaceae and the appearance of Hericium creolophus, Cirrhatus spongipellis, Pachyodon and Sistotrema confluens in Mecklenburg, East Germany». Feddes Repertorium (em alemão). 90 (1–2): 103–120. ISSN 0014-8962. doi:10.1002/fedr.19790900107
- ↑ a b Newton AC, Holden E, Davy LM, Ward SD, Fleming LV, Watling R (2002). «Status and distribution of stipitate hydnoid fungi in Scottish coniferous forests». Biological Conservation. 107 (2): 181–92. doi:10.1016/S0006-3207(02)00060-5
- ↑ Gulden G, Hanssen EW (1992). «Distribution and ecology of stipitate hydnaceous fungi in Norway, with special reference to the question of decline» (Abstract). Sommerfeltia. 13: 1–58. ISSN 0800-6865. doi:10.2478/som-1992-0001
 . Consultado em 11 de janeiro de 2010
. Consultado em 11 de janeiro de 2010
- ↑ Arnolds E. (1989). «Former and present distribution of stipitate hydnaceous fungi (Basidiomycetes) in the Netherlands». Nova Hedwigia. 48 (1–2): 107–42
- ↑ Hrouda P. (1999). «Hydnaceous fungi of the Czech Republic and Slovakia». Czech Mycology. 51 (2–3): 99–155. ISSN 0009-0476
- ↑ Asef MR. (2008). «Hydnellum peckii, a new ectomycorrhizea for Iran». Rostaniha. 9 (2): 115. ISSN 1608-4306
- ↑ Han SK, Oh SH, Kim HJ (2010). «Eight unrecorded fungi identified at the Korea National Arboretum». Mycobiology. 38 (2): 81–88. PMC 3741570
 . PMID 23956632. doi:10.4489/MYCO.2010.38.2.081
. PMID 23956632. doi:10.4489/MYCO.2010.38.2.081
- ↑ Ammirati J, Traquair JA, Horgen PA (1985). Poisonous Mushrooms of Canada. Markham, Ontario: Fitzhenry & Whiteside in cooperation with Agriculture Canada. p. 18. ISBN 978-0-88902-977-4
- ↑ Ammirati J, Traquair JA, Horgen PA (1985). Poisonous Mushrooms of Canada. Markham, Ontario: Fitzhenry & Whiteside in cooperation with Agriculture Canada. p. 18. ISBN 978-0-88902-977-4
- ↑ Khanna JM, Malone MH, Euler KL, Brady LR (1965). «Atromentin – anticoagulant from Hydnellum diabolus». Journal of Pharmaceutical Sciences. 54 (7): 1016–20. PMID 5862512. doi:10.1002/jps.2600540714
- ↑ Zheng CJ, Sohn MJ, Kim WG (2006). «Atromentin and leucomelone, the first inhibitors specific to enoyl-ACP reductase (FabK) of Streptococcus pneumoniae». Journal of Antibiotics. 59 (12): 808–12. PMID 17323650. doi:10.1038/ja.2006.108

- ↑ Rühm W, Steiner M, Kammerer L, Hiersche L, Wirth E (1998). «Estimating future radiocaesium contamination of fungi on the basis of behavior patterns derived from past instance of contamination». Journal of Environmental Radioactivity. 39 (2): 129–47. doi:10.1016/S0265-931X(97)00055-6
Ligações externas
 Media relacionados com Hydnellum peckii no Wikimedia Commons
Media relacionados com Hydnellum peckii no Wikimedia Commons
